求氧化镍(NiO)的标准摩尔生成焓并注明出处.
 烟雨红颜bj2022-10-04 11:39:545条回答
烟雨红颜bj2022-10-04 11:39:545条回答
已提交,审核后显示!提交回复
共5条回复
 shiyinzheng 共回答了18个问题
shiyinzheng 共回答了18个问题 |采纳率94.4%- NiO(s) ΔHf (kJ/mol) -244.3
来源:
Masterton,Slowinski,Stanitski,Chemical Principles,CBS College Publishing,1983. - 1年前
 查访 共回答了8个问题
查访 共回答了8个问题 |采纳率- ??我只知道摩尔庄园
- 1年前
 kissyou520 共回答了1个问题
kissyou520 共回答了1个问题 |采纳率- 我也只知道摩尔庄园,是个游戏
- 1年前
 cuiyi1984 共回答了23个问题
cuiyi1984 共回答了23个问题 |采纳率82.6%- 本人的回答是 NiO(s) ΔHf (kJ/mol) -244.3
来源:
Masterton, Slowinski, Stanitski, Chemical Principles, CBS College Publishing, 1983.
http://chemistry.about.com/library/weekly/blheatform.htm - 1年前
 jingzai1211 共回答了5个问题
jingzai1211 共回答了5个问题 |采纳率- NiO(cr) -240.6 KJ/mol
这是从我们化学系的《普通化学》课本里找到的,是华彤文编著的,北京大学出版社 2005出版的第三版,貌似楼上两位的数据有些老了 - 1年前
相关推荐
- 天然或绝大部分人工制备的晶体都存在各种缺陷,例如,在某种氧化镍晶体中就存在这
天然或绝大部分人工制备的晶体都存在各种缺陷,例如,在某种氧化镍晶体中就存在这
天然的和绝大多数人工制备的晶体都存在各种缺陷.例如:在某种氧化镍(NiO)晶体中就存在如图所示的缺陷:一个Ni2+ 空缺,另有两个Ni2+ 被两个Ni3+ 取代.其结果仍显电中性,但化合物中Ni 和O的比值却发生了改变.某种氧化镍样品中Ni和O的个数比为0.97:1(Ni0.97O),该晶体(Ni0.97O)中Ni3+和Ni2+ 的离子个数比为_________. 能多详细就多详细. rbioaz1年前1
rbioaz1年前1 -
 缙云天海 共回答了18个问题
缙云天海 共回答了18个问题 |采纳率94.4%Ni3+个数为x、Ni2+个数为y,则x+y=0.97 ,3x+2y-2=0(此式为化合价代数和为零),可解得
x:y=6:911年前查看全部
- 【求助】氧化镍会与硝酸反应吗?
 gaoqin00111年前1
gaoqin00111年前1 -
 诺诺小七 共回答了20个问题
诺诺小七 共回答了20个问题 |采纳率80%这个结论还需要论证么.:o 我在很多工具书上找NiO+HNO3的反应方程式,但都只找到氧化镍与硫酸,与盐酸的反应.没有找到与硝酸的反应方程式.按理说,这个简单的反应在书上或者网络上有所标出,但遗憾的是我在网上搜寻很多遍,也没有结果.
NiO里如果Ni是最高价态的话就不能被氧化了. Ni 是变价,过渡元素.存在+3价,如Ni2O3zgsdzblg(站内联系TA)你的反应吉布斯自由能变和熵变计算的基础数据有吗?溶液态和纯态的计算是完全不一样的.硝酸镍好像只有溶液态的基础数据,纯态的没有.?馐茄趸?镉胨岱从ι?伤?幕?Ч媛杉蚊?站内联系TA)Originally posted by zgsdzblg at 2011-02-19 12:39:39:1年前查看全部
- 已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近
 已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g•mol-1).
已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g•mol-1).  merylyl1年前0
merylyl1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 天然的和绝大部分人工制备的晶体都存在各种缺陷.例如在某种氧化镍(NiO)晶体中就存在如图所示的缺陷:一个Ni2+空缺,另
天然的和绝大部分人工制备的晶体都存在各种缺陷.例如在某种氧化镍(NiO)晶体中就存在如图所示的缺陷:一个Ni2+空缺,另两个被两个Ni3+所取代.其结果仍呈电中性,但化合物中Ni和O的比值却发生了改变.某种氧化镍的组成为Ni0.970,该晶体中Ni2+和Ni3+的离子个数比为?
请问...我的答案是9:2的
 wybbsx1年前1
wybbsx1年前1 -
 ccuuii0920 共回答了20个问题
ccuuii0920 共回答了20个问题 |采纳率95%设Ni2+个数为X,则Ni3+个数为0.97-X
2X+3(0.97-X)=2
X=0.91,0.97-X=0.06
该晶体中Ni2+和Ni3+的离子个数比为91:61年前查看全部
- 已知镍的相对原子质量为59,其氧化物的相对分子质量为75.若氯化镍中镍的化合价与氧化镍中的相同,则氯化
已知镍的相对原子质量为59,其氧化物的相对分子质量为75.若氯化镍中镍的化合价与氧化镍中的相同,则氯化
镍的化学式为( )
A、 NiCl2 B、 Ni2Cl C、Ci2Cl3 D、NiCl qq1240145371年前1
qq1240145371年前1 -
 说过要爱我 共回答了12个问题
说过要爱我 共回答了12个问题 |采纳率58.3%氧化镍的分子量是75而镍的分子量时59,在氧化镍中氧的分子量总和是75-59=16,故只有一个氧原子,氧是副二价,故镍显正二价,Cl是负一价,故氯化镍的分子式是A:NiCl21年前查看全部
- 已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近
已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g•mol-1).

 桃花岛黄岛主1年前1
桃花岛黄岛主1年前1 -
 Y223548744 共回答了27个问题
Y223548744 共回答了27个问题 |采纳率96.3%解题思路:利用均摊法确定晶胞中原子数,进而确定晶胞的质量,再根据ρ=
计算晶胞的密度.m V 根据均摊法可知,在NiO晶胞中含镍原子数为8×18+6×12=4,氧原子数为1+12×14=4,所以晶胞的质量为4×74.7gNA,由题意可知,晶胞的边长为2a×10-8cm,所以体积为8a3×10-24cm3,所以晶胞的密度ρ=4×74.7NA8a3×10...
点评:
本题考点: 晶胞的计算.
考点点评: 本题主要就考查了晶体密度的计算,难度不大,解题时注意均摊法 运用和基本计算公式的运用.1年前查看全部
- (2014•南京模拟)超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上
(2014•南京模拟)超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上常以Ni(NO3)2•6H2O和尿素[CO(NH2)2]为原料制备.

(1)Ni2+的基态核外电子排布式为______.
(2)与NO3-离子互为等电子体的一种分子的分子式为______.
(3)尿素分子中碳原子的杂化方式为______,1mol尿素分子中含有的σ键数为______.
(4)NiO晶胞结构如图1所示,Ni的配位数为______.天然的和绝大部分人工制备的晶体都存在各种缺陷.某种NiO晶体中就存在如图2所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6:91.若该晶体的化学式为NixO,则x=______. 觅雪_晴韵1年前1
觅雪_晴韵1年前1 -
 litiandi 共回答了20个问题
litiandi 共回答了20个问题 |采纳率85%解题思路:(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,据此答题;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,据此答题;
(3)尿素分子的结构简式为: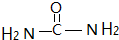 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6,根据化合物化合价代数各为零,可以算出NixO中x的值;(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,故答案为:1s22s22p63s23p63d8;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,故答案为:BF3、SO3、COCl2等;
(3)尿素分子的结构简式为: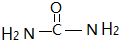 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6;因为氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,所以镍元素的平均价为[6×3+91×2/6+91]=[200/97]根据化合物化合价代数各为零,得[200/97]x=2,则x=0.97,故答案为:6、0.97;点评:
本题考点: 晶胞的计算;配合物的成键情况.
考点点评: 本题主要考查了核外电子的排布、等电子体、原子杂化、化学键、晶胞的计算等知识,中等难度,注重基础知识的考查.1年前查看全部
- 14、天然的和绝大部分人工制备的晶体都存在各种缺陷.例如在某种氧化镍(NiO)晶体中就存在如图所示的缺陷:一个Ni2+空
14、天然的和绝大部分人工制备的晶体都存在各种缺陷.例如在某种氧化镍(NiO)晶体中就存在如图所示的缺陷:一个Ni2+空缺,另两个被两个Ni3+所取代.其结果仍呈电中性,但化合物中Ni和O的比值却发生了改变.某种氧化镍的组成为Ni0.970,该晶体中Ni2+和Ni3+的离子个数比为( )
A、91∶6 B、89∶12 C、97∶3 D、100∶3
说明解题思路 清色茗1年前5
清色茗1年前5 -
 xuwuijie 共回答了17个问题
xuwuijie 共回答了17个问题 |采纳率94.1%Ni3+个数为x、Ni2+个数为y,则x+y=0.97 ,3x+2y-2=0(此式为化合价代数和为零),可解得
x:y=6:911年前查看全部
- 氧化铝15.62氧化硅79.91氧化铁0.25氧化钾3.94氧化镍0.03氧化铜0.02氧化铷0.03氧化锆0.03氧化
氧化铝15.62氧化硅79.91氧化铁0.25氧化钾3.94氧化镍0.03氧化铜0.02氧化铷0.03氧化锆0.03氧化钛0.1 白度83
烧失率4.43 请问这样的矿石能做什么用?有价值吗 天高云淡风轻月暗1年前1
天高云淡风轻月暗1年前1 -
 辽阔无边 共回答了13个问题
辽阔无边 共回答了13个问题 |采纳率100%作为提炼铝来说铝较低,硅及铁都有所偏高,估计价值不大1年前查看全部
- 氧化物溶于盐酸有氯气放出的是那个?A氧化铁 B氧化铜 C氧化钴 D 氧化镍
氧化物溶于盐酸有氯气放出的是那个?A氧化铁 B氧化铜 C氧化钴 D 氧化镍
能写出化学反应式么 啥咪1年前2
啥咪1年前2 -
 MP4手机rrrr 共回答了14个问题
MP4手机rrrr 共回答了14个问题 |采纳率100%不要被人误导了
应该是Co2O3,Ni2O3溶于盐酸放出氯气1年前查看全部
- 氧化镍和氢气反应的化学方程式写它的化学方程式,还有五氧化二磷与氢气加热下的反应方程式
 猎人的眼神1年前3
猎人的眼神1年前3 -
 爱受伤的狼 共回答了13个问题
爱受伤的狼 共回答了13个问题 |采纳率92.3%NiO+H2----->Ni+H2O1年前查看全部
大家在问
- 1分数十五分之a,当a=()时,这个分数的倒数是3
- 2设函数f(x)=[1/3]x3-[1/2]x2+2x,g(x)=[1/2]ax2-(a-2)x,
- 3已知2sinβ=sin(2α+β),求tan(α+β):tanα的值
- 4小明买了3千克梨和3千克苹果共付20.1元,小芳买了1千克梨和3千克苹果共付15.1元.每千克苹果和每千克梨各多少元?
- 5小红对他爸爸说他讲的故事得了第一名.改为直接引语
- 6化学计量数之比等于物质的量之比 这里指的物质的量是反应前的 变化的 还是平衡的
- 7bring/call sb/sth to mind,分下来是bring sth to mind和call sb sth
- 8翻译汤姆每天花一小时踢足球Tom spends...
- 9修改病句。
- 10i can't stand music which is too loud.which表达什么意思.
- 11《统计与可能性》一副扑克,任意抽出一张,是方块的可能性是()?(要填几分之几)是大王的可能性是()?(要填几分之几)
- 12用简洁的文字说明雾是怎样形成的
- 13英语翻译in your diary you must cover in some form,the following
- 14《咏雪》中最能表现谢道韫才气的句子是什么
- 15把成语补全:——如洗 ——如归 ——如流 ——如山 ——如焚 ——如瓶 ——如簧
