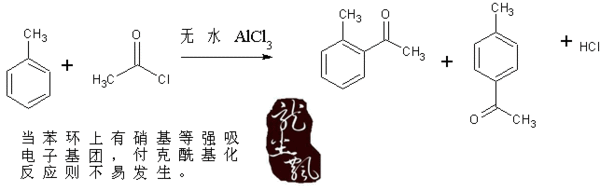
付克酰化反应中为什么无水三氯化铝
 气稚oo睫毛2022-10-04 11:39:542条回答
气稚oo睫毛2022-10-04 11:39:542条回答
付克酰化反应中为什么无水三氯化铝
为什么氯化铝要是无水的?
为什么氯化铝要是无水的?

已提交,审核后显示!提交回复
共2条回复
 lwuele 共回答了18个问题
lwuele 共回答了18个问题 |采纳率83.3%- 水电离出的OH-能进行亲核取代,把酰卤给取代成酸了就不能反应了
- 1年前
 我从哪儿来的 共回答了74个问题
我从哪儿来的 共回答了74个问题 |采纳率- 路易斯酸一般都可以,它们有空轨道,容易夺取酰基化试剂上的CL- 这时酰基化试剂还剩+COR,发生亲电加成,ALCL3的效率最好,
- 1年前
相关推荐
- 付克酰基化反应和酰化反应有什么不同
 三味书城1年前1
三味书城1年前1 -
 雉声何角角 共回答了14个问题
雉声何角角 共回答了14个问题 |采纳率100%1年前查看全部
- 苯的取代问题苯甲酸甲酯如何在脂结构的对位取代上一个碳?可否说的详细些?关于付克反应我知之甚少,只知道烷基化和酰基化 是否
苯的取代问题
苯甲酸甲酯如何在脂结构的对位取代上一个碳?
可否说的详细些?关于付克反应我知之甚少,只知道烷基化和酰基化 是否先做出甲苯,再用AlCl3和所需卤代烃反应就能直接得到对位取代物? 宝_宝_猫1年前3
宝_宝_猫1年前3 -
 ss86280092 共回答了20个问题
ss86280092 共回答了20个问题 |采纳率95%如楼上所说,酯基是间位定位基,所以若想强行在对位取代,须在间位引入两个很强的活化基团以封闭间位并活化酯基的对位,以强迫新的取代基团进入对位.鉴于此有一种合成方案:先在苯甲酸甲酯的间位引入两硝基,再用Sn-HCl将硝基还原成氨基,两氨基的邻对位定位效果使得在酯基对位引入基团成为可能.接着利用付-克烷基化反应,以一溴代烷为原料引入烷基,并在反应后分离副产物:酯基的邻位烷基取代物.再使用NaNO2-HCl生成重氮盐,并用H3PO2-H2O脱氮气处理制得酯基的对位取代物.不过此方法由于涉及到在被钝化的苯环上再引入钝化基团,因而反应条件苛刻,不宜使用.
建议以苯为原料,用付-克烷基化生成烷基苯,再进行付-克酰基化,以甲酰氯为原料,合成对烷基苯甲醛并分离副产物邻烷基苯甲醛(由于位阻效应,邻甲基苯甲醛应是比例较少的产物),再将分离出的对烷基苯甲醛氧化酯化得到对烷基苯甲酸酯.1年前查看全部
- 芳环与乙烯的付克烷基化反应,条件为什么是酸啊?
 renmingbi1年前2
renmingbi1年前2 -
 3435466 共回答了23个问题
3435466 共回答了23个问题 |采纳率100%不涉及双键被破坏的问题,我个人理解,都只是个趋势,lewis酸碱理论认为,凡是能提供空轨道的为酸,其实催化反应用lewis酸也可以,只不过反应后处理难于质子酸,乙烯有π键电子云,这时候是不利于苯环进攻的,加酸之后,乙烯的π电子会进入酸的空轨道,这时乙烯的碳上会缺电子而显正电,有利于苯环的进攻,整个反应过程没有加氢,不涉及到还原过程,1年前查看全部
- 关于付克反应的问题1.付克反应中使用的催化剂有哪些?对溶剂有什么要求?2.付克反应在药物合成中有哪些应用?举例说明.
 chrsitine1年前2
chrsitine1年前2 -
 wave413 共回答了12个问题
wave413 共回答了12个问题 |采纳率91.7%1傅克反应中使用的催化剂有无水三氯化铁、无水三氯化铝等路易斯酸.
傅克反应中溶剂应该是无水溶剂
2 付克反应在药物合成中有哪些应用?
环己烯与乙酰氯在三氯化铝的作用下生成共轭环己烯基酮1年前查看全部
- 苯与1-氟-3-氯丙烷在AlCl3作用下发生付克反应的产物?
苯与1-氟-3-氯丙烷在AlCl3作用下发生付克反应的产物?
RT.
是C-F键断还是C-Cl键断呢? zydlh20031年前1
zydlh20031年前1 -
 翱翔在天空的猪 共回答了15个问题
翱翔在天空的猪 共回答了15个问题 |采纳率93.3%C-F键断.因为傅克反应为亲电取代,攻击苯环氢的应为C正离子.F电负性强于CL,C-F键极性强于C-Cl,更易断裂形成C正离子1年前查看全部
- 大学有机化学中讲到烯丙基碳正离子因为他的ppai共轭和共振而稳定,稳定性极好,反应都发生在该碳上,但付克烷基化反应当中苯
大学有机化学中讲到烯丙基碳正离子因为他的ppai共轭和共振而稳定,稳定性极好,反应都发生在该碳上,但付克烷基化反应当中苯环+CH3CH2CH=CH2 (H2SO4)催化
却得到ph-CH(CH3)CH2CH3,反应历程是R-CH=CH2 + H离子 得到 RCH+CH3(当中那个是碳正离子) 为什么?为什么?为什么?
还有.OH是吸电子基,即使是与苯环共轭,又怎么可能达到“强活化”的程度? aibu放1年前2
aibu放1年前2 -
 衢州柑 共回答了26个问题
衢州柑 共回答了26个问题 |采纳率80.8%1、烯丙基碳正离子因p-π共轭很稳定没错,只是在你说的这个例子中,不会形成烯丙基碳正离子.烯丙基碳正离子主要是由烯丙基氯这类化合物发生SN1反应等时候形成.而在有H3O+情况下,1-丁烯会结合质子生成更稳定的二级碳正离子与苯环发生亲电取代反应,不会脱去一个负氢生成烯丙基正离子.
2、除了吸电子的诱导效应外,羟基还有更重要的给电子共轭效应(通过p-π共轭给电子到苯环上增加了苯环的电子云密度).两者综合下来,还是共轭效应更强,所以是“强活化”基团.1年前查看全部
大家在问
- 1现代语文-用层次分析法分析下列复杂短语
- 2exl函数,如下:=CEILING(FLOOR((F11*F5/100+F5),2.5),5) 具体的意思是什么?
- 3英语句子上面什么是替换主语??有个例题没???
- 4从这文段中你可以得到什么感悟?它是一片不起眼的叶子,但它在春.夏为人们做出了贡献,在秋天,当他飘落在地上时,它发出最后的
- 5甲乙两辆小车运动中的s-t图像如图所示你能否判断出甲乙分别处于什么状态?
- 6请用坐标法 别用向量 写出来.已知三角形ABC.A(x1,y1) B(x2,y2) C(x3,y3) 重心G(x0,y0
- 7已知方程组m+n=6,m-n=2的解满足于 4分之1mn的平方+(2m的平方-1)-(2分之1mn的平方+2分之3m的平
- 8微观经济学的计算体 假设生产函数Q=KL,R和W分别代表资本和劳动力,当Q-100,R=1元,W=4元时,求该厂商应采
- 9我从来没有出过天津.翻译成英文
- 103.物体的重力为200N,放置在水平桌面上,它与地面间的动摩擦因数是0.38,与地面间的最大静摩擦力是80N.
- 11英语翻译翻译句子:我过了一个忙碌但却刺激的周末.I ( )( )( )( )exciting weekend.
- 12某项工程,甲队单独做20天完成,乙队做30天完成.现在甲,乙两队合作六天后,余下的由甲队完成,还要多少天
- 13表示北半球夏至日的图是什么样子的?为什么?其他相关的图又是什么样的?
- 14【初中物理】为什么速度对动能的影响比质量大?
- 15观察这一组分数:6\1 12\1 20\1 30\1 42\1 第20个分数是多少?求大神帮助