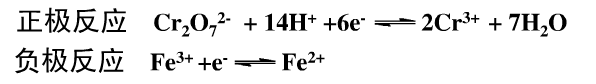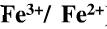氧化型和还原型指什么?在能斯特方程中
 洪洁2022-10-04 11:39:541条回答
洪洁2022-10-04 11:39:541条回答
氧化型和还原型指什么?在能斯特方程中
能斯特方程中的氧化型和还原型
能斯特方程中的氧化型和还原型

已提交,审核后显示!提交回复
共1条回复
 87363333 共回答了19个问题
87363333 共回答了19个问题 |采纳率100%- 氧化型表示发生氧化即失电子的反应,还原型表示发生还原即得电子的反应.电子的得失情况不同,所以方程式也有区别.
- 1年前
相关推荐
- 能斯特方程中的氧化型还原型是什么意思
 爱上牧羊的你1年前4
爱上牧羊的你1年前4 -
 nn狗 共回答了21个问题
nn狗 共回答了21个问题 |采纳率100%氧化型还原型就是一个电极中的氧化还原电对.比如说(Zn,Zn2+)电极,氧化型就是氧化数相对较高的Zn2+,还原型就是氧化数相对较低的Zn.1年前查看全部
- 氧化还原电对中氧化型物质生成沉淀时,电极电势将发生怎样的变化?
 marshalltang1年前1
marshalltang1年前1 -
 陆无双 共回答了17个问题
陆无双 共回答了17个问题 |采纳率94.1%要有相应的降低 一个简单的例子,可以比较氢氧化铁和三价铁离子的氧化性1年前查看全部
- 计算电极电动势时,c(氧化型)/c(还原型),是不是一个完整氧化还原反应中,反应物的浓度/生成物的浓度,还是氧化剂的浓度
计算电极电动势时,c(氧化型)/c(还原型),是不是一个完整氧化还原反应中,反应物的浓度/生成物的浓度,还是氧化剂的浓度/还原剂的浓度,还是怎么搞的????求大神解释
 aids3331年前2
aids3331年前2 -
 luanqisheng 共回答了15个问题
luanqisheng 共回答了15个问题 |采纳率86.7%1年前查看全部
- 大气污染类型按污染物的性质分为还原型和氧化型.
 lorry2191年前1
lorry2191年前1 -
 king5158 共回答了18个问题
king5158 共回答了18个问题 |采纳率88.9%大气污染的分类
1)大气污染按其影响所及范围可分为四类:局部性污染、地区性污染、广域性污染、全球性污染.上述分类方法中所涉及到的范围只能是相对的,没有具体的标准.例如广域污染是大工业城市及其附近地区的污染,但对某些国家来说(面积有限)可能产生国与国之间的广域污染.
(2)根据能源性质和大气污染物组成和反应,一般将大气污染划分为四种类型:煤炭型、石油型、混合型、特殊型.煤炭型污染的一次污染物是烟气、粉尘和二氧化硫.二次污染物是硫酸及其盐类所构成的气溶胶.此污染类型多发生在以燃煤为主要能源的国家与地区,历史上早期的大气污染多属于此种类型.石油型污染又称排气型或联合企业型污染,其一次污染物是烯烃、二氧化氮以及烷、醇、羰基化合物等.二次污染物主要是臭氧、氢氧基、过氧氢基等自由基以及醛、酮和PAN(过氧乙酰硝酸脂).此类污染多发生在油田及石油化工企业和汽车较多的大城市.近代的大气污染,尤其在发达国家和地区一般属于此种类型.混合型污染是指以煤炭为主,还包括以石油为燃料的污染源而排放出的污染物体系.此种污染类型是由煤炭型向石油型过渡的阶段,它取决于一个国家的能源发展结构和经济发展速度.特殊型污染是指某些工矿企业排放的特殊气体所造成的污染,如氯气、金属蒸汽或硫化氢、氟化氢等气体.前三种污染类型造成的污染范围较大,而第四种污染所涉及的范围较小,主要发生在污染源附近的局部地区.
(3)根据污染物的化学性质及其存在的大气环境状况,可将大气污染划分为两种类型:还原型和氧化型.还原型是指以煤、石油等为燃料所产生的大气污染,实质上就是第二种分类方法中的煤炭型和混合型污染.氧化型是指以石油为燃料所产生的大气污染,实质上就是第二种分类方法中的石油型污染.1年前查看全部
- 大一无机化学题目的疑问打三角的地方为什么是lg[1/c(cl-)]不是氧化型除以还原型嘛,……氧化型不是氧化剂嘛,cl的
大一无机化学题目的疑问
打三角的地方为什么是lg[1/c(cl-)]不是氧化型除以还原型嘛,……氧化型不是氧化剂嘛,cl的元素不是化合价没变吗?难道我一直弄错了

 mm敏敏mm1年前1
mm敏敏mm1年前1 -
 saefiuqwefwq 共回答了18个问题
saefiuqwefwq 共回答了18个问题 |采纳率88.9%书上是错的.正确的是银离子浓度c(Ag+),也就是Ksp/c(Cl-).这种错误还是十分严重的,已经不是印刷错误这种级别了.1年前查看全部
- 电极电对中氧化型物质和还原性物质的浓度一样吗
电极电对中氧化型物质和还原性物质的浓度一样吗

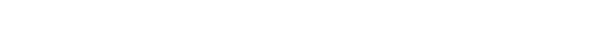

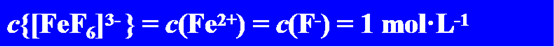
为什么他们三个是相等的?
 冰果茶1年前1
冰果茶1年前1 -
 英子0309 共回答了20个问题
英子0309 共回答了20个问题 |采纳率100%这是定义的时候规定的呀,所有物质必须在标态下测定.1年前查看全部
- 高锰酸根离子得电子生成锰离子的氧化还原半反应中,为什么氢离子和水也是氧化型和还原型.
高锰酸根离子得电子生成锰离子的氧化还原半反应中,为什么氢离子和水也是氧化型和还原型.
氢离子是氧化型,水是还原型. 破马无君1年前1
破马无君1年前1 -
 hebecai 共回答了19个问题
hebecai 共回答了19个问题 |采纳率100%没有,其实这个氧化型还原型不是说的具体物质,而是说方程左右两边的所有物质,发生还原反应要在酸性条件下,那麼H+的浓度是非常重要的,计算的时候必须一起写进去.1年前查看全部
- 常见的漂白类型有哪些举例说明漂白物质?吸附性 化合型 强氧化型
 风渺1年前1
风渺1年前1 -
 iamfly2008 共回答了17个问题
iamfly2008 共回答了17个问题 |采纳率94.1%Na2O2、H2O2、O3、HClO或(Cl2)、浓硫酸、浓硝酸、SO2、活性炭、木炭、和硅胶都有漂白性,但漂白原理及漂白效果是不同的.Na2O2、H2O2、O3、HClO 、浓硫酸、浓硝酸都具有强氧化性,它们的漂白原理:利用Na2O2、H2O2、O3、HClO、浓硫酸、浓硝酸的强氧化性将有机色素氧化成无色物质,褪色后不能恢复原来的颜色.这几种漂白性物质的漂白为永久性漂白.SO2的漂白原理:SO2 与有机色素直接化合,形成不稳定的无色物质,褪色后在一定条件下又恢复原来的颜色.SO2的漂白为暂时性漂白.活性炭、木炭、硅胶的漂白原理:利用的是它们的多孔吸附性漂白,加热后也恢复原来的颜色.活性炭、木炭、硅胶的漂白为物理漂白.活性炭、木炭、硅胶的漂白也是暂时性的.
具有漂白性的物质我们从物理和化学角度可分为两大类:化学漂白和物理漂白.化学漂白又可分为:氧化型漂白和化合型漂白.
其中Cl2、SO2都为气体且都有漂白性,但漂白原理及漂白效果是不同的.Cl2的漂白原理:Cl2 溶于水生成的HClO具有强氧化性,将有色物质氧化成无色物质,褪色后不能恢复原来的颜色.SO2的漂白原理:SO2 与有色物质直接结合,形成不稳定的无色物质,褪色后在一定条件下又恢复原来的颜色.
如果解决问题,在建立团队,1年前查看全部
- 浓硫酸做干燥剂,因为它有吸水性 强酸性 脱水性 强氧化型请说明理由,
 石壁中学同学会1年前6
石壁中学同学会1年前6 -
 go风 共回答了17个问题
go风 共回答了17个问题 |采纳率100%作为干燥剂,那肯定是吸水性!只有吸走空气中的水分,才能显示出它的干燥的作用!
强酸主要显示腐蚀性!
脱水性主要是让物体炭化!
氧化性:举例说:比如说它将二价的铁氧化成三价铁!1年前查看全部
- E值是什么?E值较小的电极其还原型物质愈易失去电子,是愈强的还原剂,对应的氧化型物质则愈难得到电子,是愈弱的氧化剂.E值
E值是什么?
E值较小的电极其还原型物质愈易失去电子,是愈强的还原剂,对应的氧化型物质则愈难得到电子,是愈弱的氧化剂.E值愈大的电极其氧化型物质愈易得到电子,是较强的氧化剂,对应的还原型物质则愈难失去电子,是愈弱的还原剂 E是什么? 乱蝉嘶1年前1
乱蝉嘶1年前1 -
 夜猫Crazy 共回答了6个问题
夜猫Crazy 共回答了6个问题 |采纳率100%基态的气态原子失去一个电子形成气态一价正离子时所需能量称为元素的第一电离能(I1).元素气态一价正离子失去一个电子形成气态二价正离子时所需能量称为元素的第二电离能(I2).第三、四电离能依此类推,并且I1<I2<I3….由于原子失去电子必须消耗能量克服核对外层电子的引力,所以电离能总为正值,SI单位为J mol-1,常用kJmol-1.通常不特别说明,指的都是第一电离能.电离能可以定量的比较气态原子失去电子的难易,电离能越大,原子越难失去电子,其金属性越弱;反之金属性越强.所以它可以比较元素的金属性强弱.影响电离能大小的因素是:有效核电荷、原子半径、和原子的电子构型.(1)同周期主族元素从左到右作用到最外层电子上的有效核电荷逐渐增大,电离能也逐渐增大,到稀有气体由于具有稳定的电子层结构,其电离能最大.故同周期元素从强金属性逐渐变到非金属性,直至强非金属性.(2)同周期副族元素从左至右,由于有效核电荷增加不多,原子半径减小缓慢,有电离能增加不如主族元素明显.由于最外层只有两个电子,过渡元素均表现金属性.(3)同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,电离能由大变小,元素的金属性逐渐增强.(4)同一副族电离能变化不规则.1年前查看全部
- 过氧化钠,次氯酸,臭氧的漂白性都是利用其强氧化型 活性炭利用吸附作用 二氧化硫应能与有色物质结合而漂白]以上的表白那些在
过氧化钠,次氯酸,臭氧的漂白性都是利用其强氧化型 活性炭利用吸附作用 二氧化硫应能与有色物质结合而漂白]以上的表白那些在加热或什么情况下可以是有色物质复原呢呢?还是说他们的漂白都是永久的?还有比如次氯酸他可以表白任何有颜色的物质么?都体现强氧化型么?都可以永久漂白么?加热都不复原的么?3.次氯酸可以漂白含碘使淀粉变蓝的溶液么?
 zz有音乐吗1年前2
zz有音乐吗1年前2 -
 超级无敌宝贝猪 共回答了17个问题
超级无敌宝贝猪 共回答了17个问题 |采纳率76.5%二氧化硫漂白是通过与有色物质结合变为无色,有色物质并未被破坏,所以一但其中的二氧化硫流失就会再显色.
强氧化剂漂白是通过破坏有色物质的分子结构来脱色,并且通常将有色物质分解为小分子,此过程是不可逆的,所以能永久漂白.1年前查看全部
- 如果电解酸性高锰酸钾溶液高锰酸根在酸性中具有强氧化型,那是氢离子得电子还是高锰酸根得电子?
 mm我爱你啊1年前1
mm我爱你啊1年前1 -
 piggy1971 共回答了19个问题
piggy1971 共回答了19个问题 |采纳率94.7%溶液中的离子在通电后可以定向移动的,氢离子会向阴极移动,高锰酸根会向阳极移动,所以在两极都是按离子放电顺序的,阴极是氢离子得电子,阳极是氢氧根失电子.高锰酸根不会到达阴极的,所以锰元素不会还原.1年前查看全部
大家在问
- 1饲养厂鸡的只数比鸭的只数多25%,那么,鸭的只数比鸡的只数少百分之几?
- 2高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用.如图是实验室制备氯气并进行一系列相关实验的装置
- 3上联:品千古文章 下联是什么?急用
- 4下列说法正确的个数有( )①AB=BC,则点B是线段AC的中点;②过两点有且只有一条直线;③过一点有一条而且仅有一条直
- 5已知关于x的二次函数y=ax平方+bx+c的图像经过C(0,1),且与x轴交于不同的两点A,B,点
- 6给你一张长方形的纸片,你怎样通过剪纸得到8个同样大小的小正方形
- 7分类法是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
- 8有关离散数学集合的 请问那个空集是否既属于自身 ,也包含于自身
- 9在273K和1.01×105 Pa下,将1.0 dm3洁净干燥的空气缓慢通过CH3OCH3液体,在此过程中,液体损失0.
- 10有两桶油共重173千克,从第一桶拿走38千克后,第二桶的油是第一桶的2倍还多6千克,问第二桶有多少千克油?
- 11从耳朵可以看出人的一生苦厄,那下面这样的耳朵好不好?请懂的亲们帮我解答一下,细致些的。(不懂者勿进)
- 12Come and buy your clothes at Huaxing's great sale!Do you lik
- 13把下面的词语分类抄写。忐忑不安 和蔼可亲 眉飞色舞
- 14一个《复变函数》里面的问题
- 15英语翻译1.他不努力学习,所以这次英语考试不及格.2.告诉Peter不要看电视了.因为他的作业错误百出.3.蓝色的手提箱