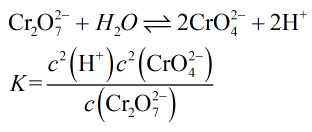Cr2O7(2-)+H2O=2CrO4(2-)+2H(+) ;k=
 枯地和2022-10-04 11:39:542条回答
枯地和2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
相关推荐
- + Cr2O7(2-) + H(+) = CO2 + Cr(3+) + H2O
+ Cr2O7(2-) + H(+) = CO2 + Cr(3+) + H2O
具体的过程,最好有双线桥 abcdef1331年前3
abcdef1331年前3 -
 三猫zz 共回答了22个问题
三猫zz 共回答了22个问题 |采纳率86.4%是氧化还原反应.
C由-2价--->+4价 失去6个e
Cr由+7价--->+3价 得到4个e
____________失去6个e*2_____
| |
C2H5OH +9 H+ +3/2 Cr2O7 = 3Cr3+ +2 CO2 +15/2 H2O
|_________|
得到4个e*3
两边同乘2,就得到配平方程了.
2C2H5OH +18 H+ +3 Cr2O7 =6 Cr3+ +4 CO2 + 15H2O1年前查看全部
- 3.Cr2O7(2-)+6Cl(--)+14H(+)==2Cr(3+)+3Cl2+7H2O
3.Cr2O7(2-)+6Cl(--)+14H(+)==2Cr(3+)+3Cl2+7H2O
当[Cl-]=[H+]=12mol/L,其他离子浓度为1mol/L,p(Cl2)=100Kpa时,E为多少?08V, 老虎灶1年前1
老虎灶1年前1 -
 zhaib007 共回答了14个问题
zhaib007 共回答了14个问题 |采纳率100%将上面的总反应式拆成两个分反应式分别算
(Cr2O7^2-)+(14H^+)+(6e^-)=(2Cr^3+)+(7H2O)
E1=E(标1)-(0.0592/n1)*lg([Cr^3+]^2/[Cr2O7^2-]*[H^+]^14)
(标E1)=1.33V,n1=6,[Cr^3+]=1,[Cr2O7^2-]=1,[H^+]=12
所以E1=1.48V
(2Cl^-)+(2e^-)=Cl2
E2=E(标2)-(0.0591/n2)*lg([p(Cl2)/p(标)]*[Cl^-]^2)
E(标2)=1.36V,p(Cl2)=p(标)=100KPa,[Cl^-]=12
所以,E2=1.42V
E=E1-E2=0.08V1年前查看全部
大家在问
- 1《采薇》一诗中与“断肠人在天涯”有异曲同工之妙的句子是什么?
- 2改成一般疑问句:he is going to see apicture show,You can go by the n
- 3We can read at the library.哪里错了
- 4(2013•黄冈模拟)把0.•7,[7/10]和78%按照从小到大排列是:[7/10]<78%<0.•7______.(
- 5英语选择Did you attend the meeting___yesterday?A.to be held B.ha
- 66 支球队进行足球比赛,每两支队之间都要赛一场,规定胜一场得 3 分,平一场各得 1 分,负一场不得 分.全部
- 7where is mary At_ A mr.brown's B the browns C Mr.Browns DThe
- 8如图,O是矩形ABCD的对角线AC的中点,M是AD的中点,若AB=5,AD=12,则四边形ABOM的面积为_______
- 90.75=( ):12=12c除( )=36分之( )
- 10“我最想对你说的一句话是:”英语怎么讲最好.
- 11高数曲线积分为什么这样做啊 不是对坐标的曲线积分吗 怎么变成对弧长的曲线积分了
- 12(x+y)的平方-(x-y)的平方-[(x+y)加的平方-(x-y)的平方]
- 13这是奥林匹克数学题,我马上要叫了.
- 14The zoo-keeper likes the baby monkey.(改为否定句
- 15八个字成三个成语如:满面(春风得意)门生 我就要7个 ①孤注( )一诺 ②满城( )共济 ③在所( )功高 ④一表( )