石灰乳的主要成分是什么
 茉莉花落1682022-10-04 11:39:541条回答
茉莉花落1682022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 旧瓶装旧酒 共回答了20个问题
旧瓶装旧酒 共回答了20个问题 |采纳率85%- 氢氧化钙Ca(OH)2
- 1年前
相关推荐
- 氯气和石灰乳反应中谁是还原剂谁是氧化剂?
 huayu95871年前1
huayu95871年前1 -
 小生8229 共回答了11个问题
小生8229 共回答了11个问题 |采纳率81.8%2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
可以看出,只有Cl2的化合价发生了改变,其中由0价变为CaCl2中的-1价,得到电子,化合价降低,因此做氧化剂.
由Cl2的0价变为Ca(ClO)2中的+1价,失去电子,化合价升高,因此做还原剂.
故Cl2在反应中既做氧化剂又做还原剂.1年前查看全部
- 石灰乳…………石灰乳在离子方程式里面为什么不拆?他是混合物,成分是什么?
 赵德彪1年前2
赵德彪1年前2 -
 rewty54gh 共回答了15个问题
rewty54gh 共回答了15个问题 |采纳率80%因为氢氧化钙微溶于水,石灰乳中主要是氢氧化钙,少量的电离出来的氢氧根离子和钙离子,所以不拆的1年前查看全部
- 石灰乳的化学式怎么写?
 黎愁别旭1年前1
黎愁别旭1年前1 -
 QQPVP 共回答了16个问题
QQPVP 共回答了16个问题 |采纳率68.8%Ca(OH)21年前查看全部
- 石灰乳的化学式是什么?
 gifyk1年前9
gifyk1年前9 -
 林烬 共回答了17个问题
林烬 共回答了17个问题 |采纳率82.4%石灰乳是Ca(OH)2中加水成乳状体1年前查看全部
- 化学:石灰乳的化学式?详细!
 zhld07691年前5
zhld07691年前5 -
 dongzhihai 共回答了27个问题
dongzhihai 共回答了27个问题 |采纳率85.2%石灰乳:是氢氧化钙的悬浊液,严格意义上没有化学式,其 主要成分为氢氧化钙:Ca(OH)21年前查看全部
- 消石灰、石灰乳、石灰石各是什么?
消石灰、石灰乳、石灰石各是什么?
其中的杂质也写出来用括号表示, angeline0111年前1
angeline0111年前1 -
 yuhegu 共回答了16个问题
yuhegu 共回答了16个问题 |采纳率93.8%消石灰是Ca(OH)2的俗名
石灰乳是Ca(OH)2中加水成乳状体
石灰石是含杂质的CaCO31年前查看全部
- quickly用22.4L(标准状况)氯气通入含86克氢氧化钙的石灰乳,完全反应后除去杂质,得到的漂粉精[含Ca(ClO
quickly
用22.4L(标准状况)氯气通入含86克氢氧化钙的石灰乳,完全反应后除去杂质,得到的漂粉精[含Ca(ClO)2和Ca(OH)2]含次氯酸钙百分之几? wangw_5121年前1
wangw_5121年前1 -
 alienking 共回答了25个问题
alienking 共回答了25个问题 |采纳率96%0.5molCa(ClO)21年前查看全部
- 将2MOL氯气通入足量石灰乳中,理论上可得到次氯化钙多少克
 zhende无话可说1年前1
zhende无话可说1年前1 -
 245841505 共回答了16个问题
245841505 共回答了16个问题 |采纳率93.8%2Ca(OH)2 + 2Cl2===Ca(ClO)2 + CaCl2 + 2H2O
—2————2————1
即1molCa(ClO)2,m[Ca(ClO)2]=1*[40+2*(35.5+16)]=143g1年前查看全部
- 石灰乳和硫酸铜溶液按一定比例混合进行反应,属于哪种反应,置换反应 分解反应 化
 wanfangqiu1年前3
wanfangqiu1年前3 -
 蓝色的雨天 共回答了16个问题
蓝色的雨天 共回答了16个问题 |采纳率75%属于复分解反应
AB+CD===AD+CB
Ca(OH)2+CuSO4===Cu(OH)2↓+CaSO4(微溶)
这个反应是保护性杀菌剂波尔多液的制取方程式1年前查看全部
- 波尔多液是CuSO4与石灰乳的混合溶液,它能防治农作物病虫害的原因是
波尔多液是CuSO4与石灰乳的混合溶液,它能防治农作物病虫害的原因是
A硫酸铜使菌体的蛋白质发生盐析
B石灰乳使菌体的蛋白质水解
C铜离子和碱性条件都能使菌体的蛋白质变性
D蛋白质可以溶解在波尔多液中 lingling_zeng841年前1
lingling_zeng841年前1 -
 fdsaasfkw 共回答了18个问题
fdsaasfkw 共回答了18个问题 |采纳率94.4%正确答案是C1年前查看全部
- 1不用铁桶放波尔多液的原因.2.用石灰乳刷墙坚硬原因.
1不用铁桶放波尔多液的原因.2.用石灰乳刷墙坚硬原因.
3.赤铁矿练铁方程式燃料中高氯酸氨的作用. Wzq83571年前1
Wzq83571年前1 -
 victor_bai2008 共回答了14个问题
victor_bai2008 共回答了14个问题 |采纳率85.7%不用铁桶盛波尔多液的原因是:波尔多液的成分是硫酸铜和氢氧化钙,铁的活动性在铜的前面,二者接触,铁会和硫酸铜反应,生成硫酸亚铁和铜,从而使波尔多液变质,降低药效.故不用铁桶盛波尔多液.石灰乳刷墙变硬使因为石灰乳中的氢氧化钙与空气中的二氧化碳发生反应,生成坚硬的碳酸钙的缘故.1年前查看全部
- 石灰乳跟盐酸反应的化学方程式以及离子方程式
 有来有去M1年前1
有来有去M1年前1 -
 dd128 共回答了16个问题
dd128 共回答了16个问题 |采纳率68.8%Ca(0H)2+2HCl=CaCl2+2H2O
Ca(OH)2+2(H+)=(Ca2+)+2H2O
PS:澄清的石灰水的话离子方程式要改写成OH-
但是由于石灰乳中Ca(OH)2过饱和,并不是澄清全部溶解,我们再这里将它理解为沉淀,所以用Ca(OH)21年前查看全部
- 汽油均匀分散在水中,石灰乳,油溶于汽油中 ,淀粉溶液分别属于悬浊液,乳浊液,胶体,溶液的哪个
汽油均匀分散在水中,石灰乳,油溶于汽油中 ,淀粉溶液分别属于悬浊液,乳浊液,胶体,溶液的哪个
汽油均匀分散在水中,石灰乳,油溶于汽油中
,淀粉溶液分别属于悬浊液,乳浊液,胶体,溶液的哪个 柏施1年前1
柏施1年前1 -
 DAISYKEKE 共回答了24个问题
DAISYKEKE 共回答了24个问题 |采纳率87.5%乳浊液,悬浊液,溶液,胶体1年前查看全部
- 淀粉是胶体还是溶液?石灰乳是悬浊液还是乳浊液?含有金属阳离子的但不是离子晶体的是谁?
 换个地方重新生活1年前1
换个地方重新生活1年前1 -
 夏老二 共回答了15个问题
夏老二 共回答了15个问题 |采纳率93.3%淀粉是胶体
石灰乳是悬浊液
金属晶体~AlCl好像也是~含有金属阳离子的但不是离子晶体的是谁?1年前查看全部
- 什么气体和石灰乳反应后生成氯化钙和另一种物质?
 yubj55221年前2
yubj55221年前2 -
 那里讨烟蓑雨笠 共回答了21个问题
那里讨烟蓑雨笠 共回答了21个问题 |采纳率95.2%氯气Cl2,生成次氯酸钙
2Cl2+2Ca(OH)2=CaCl2+Ca(CLO)2+2H2O1年前查看全部
- 石灰乳和氯气反应方程
 wendy81111年前0
wendy81111年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氯气通入石灰乳中的离子方程式
 yanjingzhao1年前1
yanjingzhao1年前1 -
 鱼水之缘 共回答了19个问题
鱼水之缘 共回答了19个问题 |采纳率84.2%氯气通入石灰乳中的离子方程式
2Cl2 + 2Ca(OH)2 == 2Ca2+ + 2Cl- + 2ClO- + 2H2O
注意石灰乳要写成Ca(OH)2,不能拆开写.1年前查看全部
- 石灰乳和澄清石灰水化学式
 笑神婆1年前1
笑神婆1年前1 -
 25常常 共回答了16个问题
25常常 共回答了16个问题 |采纳率62.5%其实主要成分一样的 化学式都是ca(oh)2 就是在更某些物质反应的时候 这2者有区别的1年前查看全部
- 在苦卤制镁的过程中为什么加入石灰乳不加氢氧化钙水溶液
 希猛特1年前1
希猛特1年前1 -
 木雨馥馥 共回答了19个问题
木雨馥馥 共回答了19个问题 |采纳率89.5%氢氧化钙水溶液中氢氧化钙的浓度太低,在常温下氢氧化钙的溶解度很低,故加入的是石灰乳既氢氧化钙与水的混合物1年前查看全部
- 关于利用苦卤,石灰乳,稀盐酸可制得应用于飞机制造业的金属镁
关于利用苦卤,石灰乳,稀盐酸可制得应用于飞机制造业的金属镁
利用苦卤,石灰乳,稀盐酸可制得应用于飞机制造业的金属镁,其中发生反应的化学方程式是?一共三个化学式 tanggang13141年前1
tanggang13141年前1 -
 jmd007 共回答了18个问题
jmd007 共回答了18个问题 |采纳率94.4%MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl=MgCl2+2H2O
MgCl2(熔融)=电解 Mg+Cl2↑1年前查看全部
- 只用回答这一小问即可.(5)将用F、E、D装置制得的氯气通人含74gCa(OH)2石灰乳中,最多可制得漂白粉 g.这个为
只用回答这一小问即可.
(5)将用F、E、D装置制得的氯气通人含74gCa(OH)2石灰乳中,最多可制得漂白粉 g.
这个为什么不能用正常的思路算呢? 虞雨桂1年前1
虞雨桂1年前1 -
 gabrilpan 共回答了24个问题
gabrilpan 共回答了24个问题 |采纳率83.3%74g的 Ca(OH)2 是1 mol,和氯气反应方程式:
Ca(OH)2+2Cl2==0.5 Ca(ClO)2+0.5 CaCl2 +2HCl
注意,它考察了漂白粉的知识,漂白粉的主要成分是Ca(ClO)2 and CaCl2 其中次氯化钙是有效成分.所以需要把两个 0.5mol 的物质质量加在一起,等于127.
欢迎追问.1年前查看全部
- 石灰乳及漂白粉的化学式
 mei_04521年前2
mei_04521年前2 -
 wxcxq 共回答了14个问题
wxcxq 共回答了14个问题 |采纳率100%石灰乳:Ca(OH)2
漂白粉:Ca(ClO)21年前查看全部
- 高中化学-----卤素氯气通入石灰乳反应得漂白粉,其主要成分为Ca(OH)2*3CaCl(ClO)*nH2O.现有一种漂
高中化学-----卤素
氯气通入石灰乳反应得漂白粉,其主要成分为Ca(OH)2*3CaCl(ClO)*nH2O.现有一种漂白粉的“有效氯”(过量HCl和漂白粉作用生成Cl2的质量和漂白粉质量之比)为35%.若该漂白粉的组成与上述化学式相当,则式中的n的值是( )
A、6.5 B、8 C、8.5 D、10
 988611年前1
988611年前1 -
 长清大侠 共回答了16个问题
长清大侠 共回答了16个问题 |采纳率100%设有1mol漂白粉,然后算出其质量(就是相对分子质量,含有n)
然后分析:过量HCl和漂白粉哪一个部分产生CL2?明显是和ClO-反应.
Cl(-)+ClO(-)+2H(+)====Cl2+H2O
一摩尔漂白粉有3摩尔次氯酸根,会产生3摩尔氯气
然后就是
产生的3摩尔氯气质量/1摩尔漂白粉的质量=0.35
解方程即可
我算到n=8.531,大概是C吧1年前查看全部
- 氯气通入石灰乳中制漂白粉的化学方程式中前面的Ca(OH)2需要标注状态么?(因为是石灰乳的关系所以不太确
氯气通入石灰乳中制漂白粉的化学方程式中前面的Ca(OH)2需要标注状态么?(因为是石灰乳的关系所以不太确
(因为是石灰乳的关系所以不太确定) wait_love99991年前1
wait_love99991年前1 -
 chaidongdong 共回答了14个问题
chaidongdong 共回答了14个问题 |采纳率78.6%是石灰乳氢氧化钙微溶于水不需要标状态
2CA(OH)2+2CL2=CACL2+CA(CLO)2+2H2O1年前查看全部
- 生石灰,石灰乳,冰,干冰,可燃冰,赤铁矿的化学式.急
 眼睛发炎1年前1
眼睛发炎1年前1 -
 纤心素手 共回答了15个问题
纤心素手 共回答了15个问题 |采纳率73.3%化学式分别为
生石灰CaO
石灰乳是一种混合物其溶质化学式为Ca(OH)2
冰H2O
可燃冰CH4
赤铁矿Fe2O31年前查看全部
- 实验室用二氧化锰和浓盐酸共热制氯气时,有14.6g氯化氢被氧化,将所得的气体全部用石灰乳吸收,可得漂白粉
 万俟雪逸1年前1
万俟雪逸1年前1 -
 林中珍宝 共回答了16个问题
林中珍宝 共回答了16个问题 |采纳率93.8%MnO2+4HCl=MnCl2+Cl2+2H2O方程式中有一半的HCl被氧化所以可这样计算
2×36.5 1
14.6 0.2mol
漂白粉为Ca(ClO)2+CaCl2的混合物.其相对质量和254
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
2 254
0.2 25.4g1年前查看全部
- 在牙膏和一些药品中,常用轻质碳酸钙粉末作为填充剂或载体.工业上通常将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要
在牙膏和一些药品中,常用轻质碳酸钙粉末作为填充剂或载体.工业上通常将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要成分是Ca(OH)2],然后将净化后的石灰乳与二氧化碳作用得到纯净的碳酸钙粉末.请用化学方程式表示上述反应的原理.
 ip4w1年前2
ip4w1年前2 -
 cnlilang 共回答了21个问题
cnlilang 共回答了21个问题 |采纳率81%解题思路:根据物质的性质进行分析,石灰石高温能分解生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙.碳酸钙高温能分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙和水,所以本题答案为:CaCO3
高温
.
CaO+CO2↑,
CaO+H2O═Ca(OH)2,CO2+Ca(OH)2═CaCO3↓+H2O.点评:
本题考点: 碳酸钙、生石灰、熟石灰之间的转化;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了常见物质的性质和有关化学方程式的书写,完成此题,可以依据应用的知识进行,要求同学们加强对化学方程式的识记,以便应用.1年前查看全部
- 在牙膏和一些药品中,常用轻质碳酸钙粉末作为填充剂或载体.工业上通常将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要
在牙膏和一些药品中,常用轻质碳酸钙粉末作为填充剂或载体.工业上通常将石灰石煅烧制得氧化钙,再将氧化钙加水制成石灰乳[主要成分是Ca(OH)2],然后将净化后的石灰乳与二氧化碳作用得到纯净的碳酸钙粉末.请用化学方程式表示上述反应的原理.
 会飞的小鼠1年前2
会飞的小鼠1年前2 -
 男人的样子 共回答了17个问题
男人的样子 共回答了17个问题 |采纳率88.2%解题思路:根据物质的性质进行分析,石灰石高温能分解生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙.碳酸钙高温能分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与二氧化碳反应生成碳酸钙和水,所以本题答案为:CaCO3
高温
.
CaO+CO2↑,
CaO+H2O═Ca(OH)2,CO2+Ca(OH)2═CaCO3↓+H2O.点评:
本题考点: 碳酸钙、生石灰、熟石灰之间的转化;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了常见物质的性质和有关化学方程式的书写,完成此题,可以依据应用的知识进行,要求同学们加强对化学方程式的识记,以便应用.1年前查看全部
- 氯气通入石灰乳.其主要成分是Ca(OH)2+3CaCl(OCl)+nH2O设生成的Cl2与漂白粉的质量比为0.35.求n
氯气通入石灰乳.其主要成分是Ca(OH)2+3CaCl(OCl)+nH2O设生成的Cl2与漂白粉的质量比为0.35.求n的值
 MissSammi1年前1
MissSammi1年前1 -
 天黑之后天亮之前 共回答了19个问题
天黑之后天亮之前 共回答了19个问题 |采纳率94.7%氯气通入石灰乳,其主要成分是 Ca(OH)2 .3CaCl(ClO) . nH 2O .为了计算方便,就假设与次氯酸根离子反应的氯离子全部来自3CaCl(ClO)1年前查看全部
- 石灰乳悬浊液是指饱和氢氧化钙吗
 鱼很自由自在吗1年前2
鱼很自由自在吗1年前2 -
 moqinquan 共回答了19个问题
moqinquan 共回答了19个问题 |采纳率84.2%是的!可以这么说.Ca(OH)2饱和溶液1年前查看全部
- 取24g氢氧化钠和碳酸钠的固体混合物,加136g水完全溶解后,再缓慢加入石灰乳(氢氧化钙和水的混合物)至恰好完全反应,过
取24g氢氧化钠和碳酸钠的固体混合物,加136g水完全溶解后,再缓慢加入石灰乳(氢氧化钙和水的混合物)至恰好完全反应,过滤得到4g沉淀和10%的氢氧化钠溶液.试计算反应中应加入石灰乳的质量是多少?
 gld176491年前1
gld176491年前1 -
 jeremy77 共回答了17个问题
jeremy77 共回答了17个问题 |采纳率82.4%解题思路:根据碳酸钠和石灰乳反应产生沉淀碳酸钙的质量4g,可以计算出混合物中的碳酸钠,以及生成的氢氧化钠的质量,根据溶质质量分数的计算公式可以计算出10%的氢氧化钠溶液,根据质量守恒定律进而计算出加入石灰乳的质量.设24g样品中碳酸钠的质量为x,生成的氢氧化钠的质量为y
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
10610080
x4gy
[106/x=
100
4g][100/4g=
80
y]
x=4.24 gy=3.2 g
得到的10%NaOH溶液的质量为(24g-4.24g+3.2g)÷10%=229.6g
加入石灰乳的质量为 229.6 g+4 g-136 g-24 g=73.6g
答:加入石灰乳的质量为73.6g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 该题将溶液和化学方程式结合在一起进行计算,对学生的题目分析理解能力较高;解答该题首先要明确所求溶液的溶质是什么,有几部分组成;然后使溶液的质量要除去沉淀的质量.1年前查看全部
- 氯气与石灰乳(Ca(OH)2)的反应
 wohan151年前1
wohan151年前1 -
 454d54d5dd5d 共回答了15个问题
454d54d5dd5d 共回答了15个问题 |采纳率93.3%2Cl2 + 2 Ca(OH)2====CaCl2 + Ca(ClO)2 + 2H2O1年前查看全部
- 淀粉溶液与石灰乳分散质微粒直径谁大?
 似魔似幻的小妖1年前2
似魔似幻的小妖1年前2 -
 叮当玲儿 共回答了22个问题
叮当玲儿 共回答了22个问题 |采纳率95.5%溶液的直径100nm
所以,肯定是石灰乳直径大1年前查看全部
- 石灰石,石灰水,石灰乳,生石灰,熟石灰这些的化学式
 qq4269891年前2
qq4269891年前2 -
 wang16526 共回答了21个问题
wang16526 共回答了21个问题 |采纳率76.2%生石灰:CaO
熟石灰:Ca(OH)2
石灰水:Ca(OH)2
石灰乳:Ca(OH)2
另外,消石灰也是Ca(OH)2
石灰石(又称白垩石或大理石):CaCO3
碱石灰:CaO与NaOH的混合物1年前查看全部
- 二氧化硫通入石灰乳的方程式Ca(OH)2+SO2=CaSO3+H2O 中的CaSO3要向下箭号吗?
 zlzl1年前1
zlzl1年前1 -
 liutianxy 共回答了18个问题
liutianxy 共回答了18个问题 |采纳率94.4%CaSO3是沉淀,当然要打下箭头
【化学一加一】团队Edogawa_Ai_为您解答,如有疑惑请追问,1年前查看全部
- 用MnO2和浓HCl反应制Cl2,当有0.4molHCl被氧化时,生成的Cl2用石灰乳完全吸收,则生成多少mol Cl2
用MnO2和浓HCl反应制Cl2,当有0.4molHCl被氧化时,生成的Cl2用石灰乳完全吸收,则生成多少mol Cl2?可制得漂白粉多少克?(说明:漂白粉主要成分为氯化钙和次氯酸钙.)
 lxm03711年前1
lxm03711年前1 -
 任玉莹 共回答了19个问题
任玉莹 共回答了19个问题 |采纳率84.2%MnO2 + 4 HCl(浓)==(加热)== MnCl2 + Cl2 + 2 H2O1年前查看全部
- 1.将气体样品溶于水,发现气体A溶于水:2.将A的浓溶液与Mno2,公热产生一种黄绿色气体单质B,B通入石灰乳
1.将气体样品溶于水,发现气体A溶于水:2.将A的浓溶液与Mno2,公热产生一种黄绿色气体单质B,B通入石灰乳
中可以得漂白粉.求A,
写出A的浓溶液与MNO2共热的化学方程式
写出B通入石灰乳中的化学方程式
知道的帮帮忙,关于氯气的,高一必修一的. pisp1年前2
pisp1年前2 -
 mmgzs 共回答了15个问题
mmgzs 共回答了15个问题 |采纳率86.7%代楼上的回答
A是氯化氢气体(HCl)就可以了.1年前查看全部
- 1.CL2通入石灰乳得漂粉精,其主要成分Ca(OH)2·3CaCl(OCl)·nH2O.现有一种漂白粉的“有效氯”(过量
1.CL2通入石灰乳得漂粉精,其主要成分Ca(OH)2·3CaCl(OCl)·nH2O.现有一种漂白粉的“有效氯”(过量HCl和漂白粉作用生成Cl2的量和漂白粉质量之比)为35%,若该漂白粉组成与上述化学式相等,求n值.
2.当NH4HCO3完全分解成氨气、水蒸气、和二氧化碳气体时,所产生的混合气体的密度在S.T.P时为多少?对H2的相对密度为多少?
3.9.4g某金属元素M的氧化物M2O,把它溶于190.6g水中,最后得到质量百分比浓度为5.6%的溶液,若该金属元素原子核中的中子数比质子数多1个,通过计算说明M是什么元素?
4.元素A的最高价氧化物与其气态氢化物相对分子量之和为92,相对分子质量之差为28.已知A原子的质量数是其质子数的2倍,请通过计算说明A是哪种元素. 耒木451年前1
耒木451年前1 -
 海阔天空08981 共回答了11个问题
海阔天空08981 共回答了11个问题 |采纳率90.9%解;设该漂白粉的相对分子质量为X
已知;该漂白粉组成与上述化学式相等且有效氯为35%
则可得;
CL相对分子质量=该漂白粉相对分子质量
又因为根据化学式;
Ca(OH)2·3CaCl(OCl)·nH2O
可知一个该分子含六个CL原子 则有;
6(乘)35.5=35%X
即;213=35%X
解之 得
X(约)=608
再减去其它元素的相对原子质量
水的相对分子质量=
608-40-34-120-213-48=153
再用153(除)18 =8.5
所以; n=8.5
即该漂白粉化学式为;Ca(OH)2·3CaCl(OCl)·8.5H2O
析:碳酸氢铵的化学式为:NH4HCO3,当它完全分解的时候生成三种物质,分别是NH3(氨气),H20(水),CO2(二氧化碳),150摄氏度时,水为气态,因而也要算到混合气体中去,根据化学方程式就可以知道,1mol的NH4HCO3完全分解产生NH3,H20,CO2各1mol,总共得到3mol的混合气体,3mol的该混合气体总质量为79,则1mol的该气体质量约为26.3左右,也既该混合气体的平均密度为26.3,氢气的密度为2,则相对密度为13.15,约等于13.2
溶解后物质=(190.6+9.4)*5.6%=11.2g
即可反应11.2-9.4=1.8g水=0.1mol
M2O+H2o=2MOH
改氧化物的分子量=94
改金属的原子量=(94-16)/2=39
中子数比质子数多1,这原子序数=19
所以M是钾
设化合价为X.质量为M.
16*X/2+4*X+2M=92
16*x/2-4*x=28
16x+2M=120
质子:M/2
x=(M/2-2)/8
得到M/2为14 M=28 为硅1年前查看全部
- 氯气与石灰乳反应制作漂白粉的目的是
氯气与石灰乳反应制作漂白粉的目的是
rt 讨艳1年前4
讨艳1年前4 -
 简单最靠得住 共回答了15个问题
简单最靠得住 共回答了15个问题 |采纳率100%其实真正的是 氯气溶于水后生成的 次氯酸 具有漂白作用,但因为次氯酸不稳定易分解,所以我们多用它的次氯酸盐(较稳定)作为漂白粉原料,即次氯酸盐反应再生成次氯酸用以消毒
而氯气与熟石灰反应会生成次氯酸钙(次氯酸盐较次氯酸稳定些),次氯酸钙再和空气中二氧化碳和水反应生成了次氯酸,即次氯酸钙中有效成分是次氯酸钙,起漂白作用的是次氯酸.
(我们上化学竞赛课讲的.应该没错)1年前查看全部
- 工业上制取漂白粉,为什么用石灰乳而不用石灰水与氯气反应呢?
工业上制取漂白粉,为什么用石灰乳而不用石灰水与氯气反应呢?
工业上生产漂白粉时应采用( )
A、石灰水与氯气反应
B、纯净的熟石灰与氯气反应
C、含适量水分的熟石灰与氯气反应
D、石灰乳与氯气反应 嗷嗷嗷1年前1
嗷嗷嗷1年前1 -
 soiltiger 共回答了20个问题
soiltiger 共回答了20个问题 |采纳率70%石灰水中氢氧化钙的含量太低了,不适用于大量生产
由你问的可知用石灰乳
石灰乳是混合物物所谓纯净,所以答案选D1年前查看全部
- 氯气与石灰乳反应的化学方程式,标出电子转移方向及数目
 yemao52001年前2
yemao52001年前2 -
 robin18 共回答了22个问题
robin18 共回答了22个问题 |采纳率86.4%2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
Cl2 → CaCl2 得到2mol电子
Cl2 → Ca(ClO)2 失去2mol电子1年前查看全部
- 二氧化硫通入石灰乳反应方程式
 独木鱼1年前1
独木鱼1年前1 -
 砸烂汉奸 共回答了17个问题
砸烂汉奸 共回答了17个问题 |采纳率88.2%2SO2+Ca(OH)2===Ca(HSO3)2
希望有所帮助~1年前查看全部
- Cl2通入石灰乳得漂粉精,其主要成分Ca(OH)2·3CaCl(OCl)·nH2O.现在一种漂白粉的“有效氯”(过量HC
Cl2通入石灰乳得漂粉精,其主要成分Ca(OH)2·3CaCl(OCl)·nH2O.现在一种漂白粉的“有效氯”(过量HCl和漂粉精作用生成Cl2的量和漂粉精质量之比)为35%,若该漂白粉组成与上述化学式相等,求n的值.
5 我想问的是为什么35%就是cl在化学式中的质量百分比呢 蓁蓁其华1年前5
蓁蓁其华1年前5 -
 likepp365365365 共回答了17个问题
likepp365365365 共回答了17个问题 |采纳率88.2%其实是很简单的,前面几位说的繁琐了.
漂白精中含有氯的成分是CaCl(OCl)
易得CaCl(OCl)中前面的Cl是-1价,后面的Cl是+1价(后面的Cl相当于HClO中+1价的Cl)
所以HCl和漂粉精作用生成氯气,这氯气全部来自于CaCl(OCl)本身,而不是HCl中的Cl.这是因为+1价的Cl与-1价的Cl发生归中反应生成Cl2,且刚好是1:1.
所以生成Cl2的量和漂粉精质量之比为35%,也就是漂粉精中Cl质量占漂粉精总质量的35%.
6*35.5/(455+18n)=35%
n=8.51年前查看全部
- 氯气与石灰乳的反应实质是什么2Cl2+2Ca(oh)2====ca(clo)2+cacl2+2h2o为什么不是氯气先与水
氯气与石灰乳的反应实质是什么
2Cl2+2Ca(oh)2====ca(clo)2+cacl2+2h2o
为什么不是氯气先与水反应 生成氯化氢与次氯酸 然后这两个物质再与氢氧化钙反应/ 水锈1年前1
水锈1年前1 -
 小人儿45 共回答了21个问题
小人儿45 共回答了21个问题 |采纳率95.2%其实氯气也要和水反应,只是很弱,但是因为石灰乳中水较少并且氢氧化钙电离很少.并且最终方程式加在一起就是这个.
所以2Cl2+2Ca(oh)2====ca(clo)2+cacl2+2h2o
表示了主要反应或者是最终反应.1年前查看全部
- 目前世界上60%的镁是从海水中提取的.海水提镁的主要流程如下: (1)向海水中加入石灰乳的作用是
目前世界上60%的镁是从海水中提取的.海水提镁的主要流程如下: (1)向海水中加入石灰乳的作用是目前世界上60%的镁是从海水中提取的.海水提镁的主要流程如下:
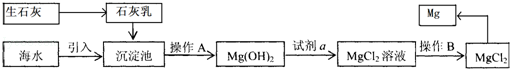
(1)向海水中加入石灰乳的作用是 .
(2)从充分利用海洋化学资源、提高经济效益的角度,生产生石灰的主要原料来源于海洋中的贝壳,生石灰和水反应的化学方程式是 .
(3)操作A是 ,加入的足量试剂a是 (填化学式).
(4)已知MgCl 2 的溶解度随温度的升高而增大.下列各图是某MgCl 2 饱和溶液的浓度随温度升高而变化的图象(不考虑溶剂的质量变化),其中正确的是
(5)海水提镁的过程中,将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁的原因是: .
(6)试剂a具有刺激性气味,我们刚进实验室就能闻到这种气味,说明分子的性质是: .
 eijn31年前1
eijn31年前1 -
 timfu 共回答了22个问题
timfu 共回答了22个问题 |采纳率81.8%(1)使Mg 2+ 形成Mg(OH) 2 沉淀.
(2)CaO+H 2 O═Ca(OH) 2 .
(3)过滤;HCl.
(4)C
(5)海水中氯化镁的含量很大,但镁离子浓度很低,该过程可以使镁离子富集,浓度高,且成本低.
(6)分子在永不停息地做无规律运动.
试题分析:(1)镁离子能与氢氧根离子反应生成氢氧化镁沉淀:Mg 2+ +2OH ﹣ =Mg(OH) 2 ↓,
(2)生石灰和水反应生成熟石灰,反应方程式是CaO+H 2 O═Ca(OH) 2 .
(3)分离不溶于水的固体和液体,可用过滤的方法,从沉淀池中得到氢氧化镁用过滤的方法;
从氢氧化镁到氯化镁,氢氧化镁和盐酸反应得到氯化镁和水,反应的化学方程式为:Mg(OH) 2 +2HCl=MgCl 2 +2H 2 O,加入的足量试剂a是HCl,
(4)将MgCl 2 饱和溶液加热后,虽然溶液由饱和变为不饱和,但溶质的质量与溶剂并未改变,所以溶质质量分数(即浓度)随着温度的升高并未改变.
(5)将海水中的氯化镁含量大,由于未富集,镁离子浓度很低,直接加热浓缩提取须消耗大量的电能,成本高,且提取的氯化镁盐中混有大量的其它氯化钠盐等离子,所以须将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁,
(6)试剂a具有刺激性气味,我们刚进实验室就能闻到这种气味,是因为分子在永不停息地做无规律运动.1年前查看全部
- 氯气和石灰乳反应化学方程式,漂白粉的有效成分,
氯气和石灰乳反应化学方程式,漂白粉的有效成分,
还有漂白粉溶于水后,受空气中CO2作用的离子方程式 wingning1年前1
wingning1年前1 -
 两面赔 共回答了20个问题
两面赔 共回答了20个问题 |采纳率100%Ca(OH)2 + Cl2 = CaCl2 + Ca(ClO)2 + H2O
Ca(ClO)2 + H2O + CO2 = CaCO3↓+ 2HClO
Ca2+ + 2ClO2- + H2O + CO2 = CaCO3↓+ 2HClO1年前查看全部
- 配置波尔多液为什么不用石灰水而用石灰乳与硫酸铜溶液混合?求老师速解答.
 luckcy1年前1
luckcy1年前1 -
 oyayal 共回答了16个问题
oyayal 共回答了16个问题 |采纳率87.5%氢氧化钙溶解度低,石灰水中含量太少,不适合工业生产的需要.所以采用了悬浊液.1年前查看全部
- 在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s)⇌Ca2+(aq)+2OH-(aq),当向此悬
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s)⇌Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是( )
A. n(Ca2+)增大
B. c(Ca2+)不变
C. n(OH-)增大
D. c(OH-)增大 qaz851年前3
qaz851年前3 -
 yanhui_888 共回答了16个问题
yanhui_888 共回答了16个问题 |采纳率81.3%解题思路:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,消耗水,溶液中c(Ca2+)、c(OH-)增大,由于原溶液已达到饱和,则沉淀溶解平衡向逆反应方向移动,故各离子的数目减少,但是饱和溶液的浓度只与温度有关,故浓度保持不变.向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,
A.向悬浊液中加少量生石灰,反应消耗水,会析出氢氧化钙,则n(Ca2+)减小,故A错误;
B.反应后仍为饱和溶液,c(Ca2+),故B正确;
C.反应后仍为饱和溶液,c(OH-)不变,溶液体积减小,所以n(OH-)减小,故C错误;
D.反应后仍为饱和溶液,c(OH-)不变,故D错误;
故选B.点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查难溶电解质的溶解平衡,题目难度一般,要注意向悬浊液中加少量生石灰,发生的反应:CaO+H2O=Ca(OH)2,从平衡移动的角度分析.1年前查看全部
大家在问
- 1英语自传的问题英语自传的结尾一般怎么写呢?能简要说说顺带给一两个例子吗?本人第一次写``
- 21.There is a bowl of rice on the table.(对划线部分提问)
- 3英语时态填空1.What were you doing when he came to see you yesterda
- 4用be good for 句型造句 最少5个
- 5Where is my pen?I
- 6用琐屑.休憩.冥想.萦绕.举止泰然.黯然失色造句 200字左右
- 7I believe that people should not keep pet dogs不是应该否定前置吗
- 8为什么细胞生命活动的调控中心是细胞核而不是核仁?
- 9花店里有若干朵百合花,比菊花少18朵,玫瑰花是菊花的3倍,康乃馨比玫瑰少42朵,康乃馨有84朵,花店里有百合花多少朵?
- 10已知α是第二象限角,且sin(π+α)=(k-1)/(k+1),sin(5π/2+α)=3k-1
- 11生物化学5题选择题1. 蛋白质所形成的胶体颗粒,在下列哪种条件下最不稳定 A.溶液pH大于pI B.溶液pH小于pI C
- 12划分句子成分 日华和月华大多出现在高积云的边缘.
- 13翻译成被动语态 7.Has anybody fed the birds? 8.People wi
- 14在K、H、O、N四种元素中,选择适当的元素组成物质,各写一个符合下列要求的物质的化学式:
- 15读图,完成22、23题.A点的坐标是( )A.(116° E,22°N)B.(116°E,22°S)C.(1
