(2010•连云港)不等式组2x−1<31−x>2的解集是______.
 roy198311192022-10-04 11:39:541条回答
roy198311192022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 cleit 共回答了15个问题
cleit 共回答了15个问题 |采纳率100%- 解题思路:先解不等式组中的每一个不等式的解集,再利用求不等式组解集的口诀“同小取小”来求不等式组的解集.
由(1)得,x<2,
由(2)得,x<-1,
故原不等式组的解集为:x<-1.点评:
本题考点: 解一元一次不等式组.
考点点评: 主要考查了一元一次不等式解集的求法,其简便求法就是用口诀求解.求不等式组解集的口诀:同大取大,同小取小,大小小大中间找,大大小小找不到(无解). - 1年前
相关推荐
- 连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分钟缩短为36分钟
连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分钟缩短为36分钟
其速度每小时将提高260千米,求提速后火车的速度,设提速后火车的速度为X千米/时,依题意列一元一次方程为__________ 树皮小牛1年前2
树皮小牛1年前2 -
 Mbsb 共回答了17个问题
Mbsb 共回答了17个问题 |采纳率76.5%0.6X=2.3[X-260]1年前查看全部
- 根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分
根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分钟,其速度每小时将提高260km.求提速后的火车速度.(精确到1km/h)
 lili4351年前3
lili4351年前3 -
 齐露 共回答了17个问题
齐露 共回答了17个问题 |采纳率88.2%解题思路:根据路程÷时间=速度,等量关系:提速后的运行速度-原运行的速度=260,列方程求解即可.设连云港至徐州客运专线的铁路全长为xkm,列方程得:
[x
36/60]-[x
2
18/60]=260,
1.7x=358.8,
解得x=[3588/17],
[x
36/60]≈352km/h.
答:提速后的火车速度约是352km/h.点评:
本题考点: 一元一次方程的应用.
考点点评: 本题考查了一元一次方程的应用,此题的关键是,理解路程,时间,速度的关系,找出题中存在的等量关系.1年前查看全部
- 根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分
根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分钟,其速度每小时将提高260km.求提速后的火车速度.(精确到1km/h)
 蔡爱民1年前1
蔡爱民1年前1 -
 尊重历史9967 共回答了18个问题
尊重历史9967 共回答了18个问题 |采纳率88.9%解题思路:根据路程÷时间=速度,等量关系:提速后的运行速度-原运行的速度=260,列方程求解即可.设连云港至徐州客运专线的铁路全长为xkm,列方程得:
[x
36/60]-[x
2
18/60]=260,
1.7x=358.8,
解得x=[3588/17],
[x
36/60]≈352km/h.
答:提速后的火车速度约是352km/h.点评:
本题考点: 一元一次方程的应用.
考点点评: 本题考查了一元一次方程的应用,此题的关键是,理解路程,时间,速度的关系,找出题中存在的等量关系.1年前查看全部
- .(08江苏连云港)25.(本小题满分12分)
.(08江苏连云港)25.(本小题满分12分)
我们将能完全覆盖某平面图形的最小圆称为该平面图形的最小覆盖圆.例如线段 的最小覆盖圆就是以线段 为直径的圆.
(1)请分别作出图1中两个三角形的最小覆盖圆(要求用尺规作图,保留作图痕迹,不写作法);
(2)探究三角形的最小覆盖圆有何规律?请写出你所得到的结论(不要求证明);
(3)某地有四个村庄 (其位置如图2所示),现拟建一个电视信号中转站,为了使这四个村庄的居民都能接收到电视信号,且使中转站所需发射功率最小(距离越小,所需功率越小),此中转站应建在何处?请说明理由.
为什么(3)的最小覆盖圆就是距离最小的呢?我记得不是费马点吗. missingfly1年前3
missingfly1年前3 -
 ttpcom 共回答了14个问题
ttpcom 共回答了14个问题 |采纳率92.9%(1)没有图哦
(2) 三角形的最小覆盖圆的规律 :最小覆盖园就是三角形的外接圆
(3)因为没有图,这能给你理论的东西、
应该是最短路径问题,也就是说电视信号中转站到4个村庄距离最小,如果是凸多边形的话,应该是最小覆盖圆,如果是凹多边形,选最外的点构成凸多边形,找其最小覆盖圆1年前查看全部
- 连云港至徐州的最短客运车时间由2小时18分钟缩短为36分钟,其速度每小时提高260km求提速后车速方程?
 tjadmwgpja1年前1
tjadmwgpja1年前1 -
 wilberchan 共回答了20个问题
wilberchan 共回答了20个问题 |采纳率100%解设:现在的速度是xkm/h,提高后的速度为x+260
2小时18分=2.3小时 36分=0.6小时
2.3x=0.6(260+x)
x=92
提高后速度为92+260=352km/h1年前查看全部
- 根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分
根据我省“十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分钟,其速度每小时将提高260km.求提速后的火车速度.(精确到1km/h)
 蝴蝶与海浪1年前1
蝴蝶与海浪1年前1 -
 mmyzchemistr 共回答了18个问题
mmyzchemistr 共回答了18个问题 |采纳率94.4%解题思路:根据路程÷时间=速度,等量关系:提速后的运行速度-原运行的速度=260,列方程求解即可.设连云港至徐州客运专线的铁路全长为xkm,列方程得:
[x
36/60]-[x
2
18/60]=260,
1.7x=358.8,
解得x=[3588/17],
[x
36/60]≈352km/h.
答:提速后的火车速度约是352km/h.点评:
本题考点: 一元一次方程的应用.
考点点评: 本题考查了一元一次方程的应用,此题的关键是,理解路程,时间,速度的关系,找出题中存在的等量关系.1年前查看全部
- (2014•连云港二模)如图所示,水平面上质量相等的两木块A、B用一轻弹簧相连,整个系统处于静止状态.t=0时刻起用一竖
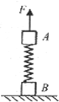 (2014•连云港二模)如图所示,水平面上质量相等的两木块A、B用一轻弹簧相连,整个系统处于静止状态.t=0时刻起用一竖直向上的力F拉动木块,使A向上做匀加速直线运动.t1时刻弹簧恰好恢复原长,t2时刻木块B恰好要离开水平面.以下说法正确的是( )
(2014•连云港二模)如图所示,水平面上质量相等的两木块A、B用一轻弹簧相连,整个系统处于静止状态.t=0时刻起用一竖直向上的力F拉动木块,使A向上做匀加速直线运动.t1时刻弹簧恰好恢复原长,t2时刻木块B恰好要离开水平面.以下说法正确的是( )
A.在0-t2时间内,拉力F与时间t成正比
B.在0-t2时间内,拉力F与A位移成正比
C.在0-t2间间内,拉力F做的功等于A的机械能增量
D.在0-t1时间内,拉力F做的功等于A的动能增量 jssmsy1年前1
jssmsy1年前1 -
 rrr6927 共回答了14个问题
rrr6927 共回答了14个问题 |采纳率100%解题思路:以木块A为研究对象,分析受力情况,根据牛顿第二定律得出F与A位移x的关系式,再根据位移时间公式,得出F与t的关系.根据功能关系分析拉力做功与A的机械能增量关系.A、B设原来系统静止时弹簧的压缩长度为x0,当木块A的位移为x时,弹簧的压缩长度为(x0-x),弹簧的弹力大小为k(x0-x),根据牛顿第二定律得:
F+k(x0-x)-mg=ma
得到:F=kx-kx0+ma+mg,
又kx0=mg,
则得到:F=kx+ma
可见F与x是线性关系,但不是正比.
由x=
1
2at2得:F=k•
1
2at2+ma,F与t不成正比.故AB错误.
C、据题t=0时刻弹簧的弹力等于A的重力,t2时刻弹簧的弹力等于B的重力,而两个物体的重力相等,所以t=0时刻和t2时刻弹簧的弹力相等,弹性势能相等,根据功能关系可知在0-t2间间内,拉力F做的功等于A的机械能增量,故C正确.
D、根据动能定理可知:在0-t1时间内,拉力F做的功、重力做功与弹力做功之和等于A的动能增量,故D错误.
故选:C.点评:
本题考点: 胡克定律;动能和势能的相互转化;机械能守恒定律.
考点点评: 对于匀变速直线运动,运用根据牛顿第二定律研究力的大小是常用的思路.分析功能关系时,要注意分析隐含的相等关系,要抓住t=0时刻和t2时刻弹簧的弹性势能相等进行研究.1年前查看全部
- (2013•连云港)用如图所示装置测量动滑轮的机械效率.实验时,竖直向上的匀速拉动弹簧测力计,使挂在动滑轮下面的钩码缓缓
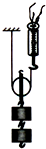 (2013•连云港)用如图所示装置测量动滑轮的机械效率.实验时,竖直向上的匀速拉动弹簧测力计,使挂在动滑轮下面的钩码缓缓上升.实验数据如下表.
(2013•连云港)用如图所示装置测量动滑轮的机械效率.实验时,竖直向上的匀速拉动弹簧测力计,使挂在动滑轮下面的钩码缓缓上升.实验数据如下表.
(1)第②次实验时,测得动滑轮的机械效率约为______.序号 动滑轮重
G动/N钩码重力G/N 钩码上升高度h/m 绳的拉力F/N 绳端移动距离
s/m机械效率η ① 0.1 1 0.2 0.6 0.4 83.3% ② 0.1 2 0.2 1.1 0.4 ③ 0.2 2 0.2 1.2 0.4 83.3%
(2)分析表中数据可知,对于同一动滑轮,所提升钩码的重力增大,机械效率将______;提升相同重力的钩码时,动滑轮的重力增大,其机械效率将______.(选填“增大”、“减小”或“不变”)
(3)分析表中数据可知,F≠
,可能的原因是:______.G动+G 2  我是你的验证码1年前1
我是你的验证码1年前1 -
 遗弃的糖果 共回答了19个问题
遗弃的糖果 共回答了19个问题 |采纳率84.2%解题思路:(1)根据表中实验数据应用效率公式求出动滑轮的 机械效率.
(2)分析表中实验数据,然后得出结论.
(3)从摩擦与绳重等方面分析答题.(1)由表中实验数据可知,第②次实验时,动滑轮的机械效率:
η=
W有
W总×100%=[Gh/Fs]×100%=[2N×0.2m/1.1N×0.4m]×100%≈90.9%;
(2)由表中实验序号为①②的实验数据可知,对于同一动滑轮,所提升钩码的重力增大,机械效率将增大;
由表中实验序号为②③的实验数据可知,提升相同重力的钩码时,动滑轮的重力增大,其机械效率将减小.
(3)由于滑轮与轮轴间存在摩擦、缠绕滑轮组的绳子有重力,因此:F≠
G动+G
2.
故答案为:(1)90.9%;(2)增大;减小;(3)滑轮与轮轴间有摩擦、绳子有重力.点评:
本题考点: 滑轮(组)机械效率的测量实验.
考点点评: 本题考查了求滑轮组效率、实验数据分析,应用效率公式可以求出滑轮组效率,应用控制变量法分析表中实验数据即可正确解题;解题时要注意控制变量法的应用.1年前查看全部
- 2013年连云港小升初语文、数学、英语试卷
 momosd1年前1
momosd1年前1 -
 8215785 共回答了14个问题
8215785 共回答了14个问题 |采纳率100%这个,你是查不到的,虽然这只是小升初,但是每年的卷子都是密封的,绝不能泄露的1年前查看全部
- (2007•连云港模拟)某班一学习小组以“关于市场上几种补钙保健产品的调查研究”为课题进行了探究学习活动.请你一起参与其
(2007•连云港模拟)某班一学习小组以“关于市场上几种补钙保健产品的调查研究”为课题进行了探究学习活动.请你一起参与其活动,完成下列探究过程.
[活动目的]
(1)了解钙元素与人体健康的关系.
(2)了解钙产品的含钙量、价格、并检验是否合格.
(3)培养获取信息、处理信息、分析问题、解决问题、合作探究能力.
[调查收集资料]
(1)通过市场调查,常见的四种钙产品的有关信息如下:
(2)通过查阅三九健康网、《现代医学周刊》、《市场报》等收集到如下信息:品名 钙尔奇-D 凯思立-D 乐力钙 柠檬酸钙 主要含钙物质 碳酸钙 碳酸钙 氨基酸螯合钙 枸橼酸钙 该元素含量(mg/片) 600 500 250 168 数量(片)/瓶(盒) 30 20 30 30 价格(元)/瓶(盒) 27.00 23.10 30.00 25.20
生长期青少年每天钙摄入量应为1 300 mg,而实际上目前我国中学生每日钙摄入量的均值为518 mg,营养学会公布的居民每日钙摄入量为800 mg.
[研究结论]
(1)钙保健产品中的钙元素以______形式存在.A.单质B.化合物
(2)人体的钙元素主要存在于______中.
(3)根据上述调查信息分析,青少年每日钙需要量大,而实际摄入量不足,应注意______.
[交流与讨论]
(1)由上表分析比较,四种钙产品中,当含有相同质量的钙元素时价格相对最便宜______.
A.钙尔奇-DB.凯思立-DC.乐力钙D.柠檬酸钙
(2)在交流过程中,小芳同学提出一个观点,补钙还可以食补,即能省钱又能补钙.下列做法可以补钙的是______.
A.在食物中添加生石灰B.食用一些虾皮C.喝排骨汤D.做馒头时放纯碱
(3)小明认为食用凯思立-D的碳酸钙进入胃内能发生化学反应,其化学方程式是:______.
[质疑与再探究]
由钙尔奇-D说明书知每片钙尔奇-D中含碳酸钙1.5 g.(已知:钙尔奇-D不含有其他碳酸盐,其研细后与稀硫酸完全反应.)在讨论中,小强同学提出一个问题,现在市场上有些不法分子会以假乱真,购买的钙尔奇-D不知是否合格,想通过实际定量分析.小强设计了如下方案并进行实验:取50片钙尔奇-D研细,放入锥形瓶(见下图),加入足量的盐酸充分反应,气体最后通入氢氧化钠溶液(假设气体全部被氢氧化钠吸收,忽略系统内空气中CO2的影响),两次称量盛氢氧化钠溶液的洗气瓶可计算出样品是否合格.试回答下列问题: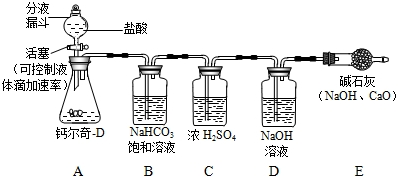
(1)小强用B中NaHCO3饱和溶液除去CO2中混有的少量HCl气体,B中的NaHCO3溶液能否换成石灰水?(填“能”或“否”),其理由是______.
(2)小明认为:小强的设计不能达到检验样品是否合格的目的,应该加以改进,并得到了小组其他同学的赞同.你认为小明发现的问题是______,改进的方法是______.
(3)用改进后的装置和药品进行实验,称量盛氢氧化钠溶液的洗气瓶增加了33 g,试通过计算说明小强选用的钙尔奇-D是否为合格产品. 陈楚生ee李宇春1年前1
陈楚生ee李宇春1年前1 -
 xiao__xin 共回答了22个问题
xiao__xin 共回答了22个问题 |采纳率100%解题思路:[研究结论](1)根据人体中钙的存在形式回答;
(2)根据人体中钙的存在位置回答;
(3)根据人体中钙的生理功能回答.
[交流与讨论](1)根据各种药品的主要成分中含有钙元素的质量和其价格比比较回答;
(2)根据钙元素的主要食物来源回答;
(3)根据胃酸的成分与它和碳酸钙的化学性质回答.
[质疑与再探究](1)根据二氧化碳和NaHCO3饱和溶液的化学性质回答;
(2)根据碳酸氢钠和盐酸反应生成了二氧化碳的情况回答;
(3)根据盛氢氧化钠溶液的洗气瓶增加了33 g,判断生成的二氧化碳的质量,再根据二氧化碳的质量求出碳酸钙的质量,最后判断是否合格.[研究结论](1)钙保健产品中的钙元素都是以化合物的形式存在;
(2)在人体内的钙元素主要存在于骨胳和牙齿中;
(3)如果人体缺钙,幼儿和青少年会患佝偻病和发育不良,所以要注意补钙.
[交流与讨论](1)600mg/片×30片÷27.00元=666.67 mg/元;500mg/片×20片÷23.10元=432.9 mg/元;250mg/片×30片÷30.00元=250 mg/元;168mg/片×30片÷25.20元=200 mg/元,所以选A.
(2)A.在食物中添加生石灰,生石灰会腐蚀人的消化道;B.食用一些虾皮可以,虾皮中富含钙;C.喝排骨汤可以,骨头汤中含钙元素多;D.做馒头时放纯碱不可以,纯碱是碳酸钠,不含钙元素;
(3)胃酸的主要成分是盐酸,它和碳酸钙反应生成三氧化碳、水和二氧化碳,方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
[质疑与再探究](1)B中的NaHCO3溶液不能换成石灰水,因为石灰水的主要成分是氢氧化钙,能和二氧化碳也发生反应;
(2)NaHCO3饱和溶液吸收HCl时,要反应产生CO2,导致盛NaOH溶液的洗气瓶增重大于样品产生CO2的质量,无法计算样品是否合格.将盐酸换成稀硫酸,就不会有氯化氢气体挥发出来,再将NaHCO3饱和溶液的洗气瓶去掉就可以了.
(3)设钙尔奇-D是碳酸钙的质量为X
由于盛氢氧化钠溶液的洗气瓶增加了33 g,则生成的二氧化碳的质量33 g.
CaCO3+2HCl=CaCl2+H2O+CO2↑
10044
X 33g
100÷44=X÷33g X=75g
75g÷50片=1.5g/片 与说明书一致,为合格产品.
故答案为:[研究结论](1)B(2)骨骼和牙齿(3)补钙等
[交流与议论](1)A(2)BC(3)CaCO3+2HCl=CaCl2+H2O+CO2↑
[质疑与再探究](1)否,因为石灰水也能吸收二氧化碳干燥CO2气体
(2)NaHCO3饱和溶液吸收HCl时,要反应产生CO2,导致盛NaOH溶液的洗气瓶增重大于样品产生CO2的质量,无法计算样品是否合格;将盐酸换成稀硫酸,将NaHCO3饱和溶液的洗气瓶去掉.
(3)设钙尔奇-D是碳酸钙的质量为X
由于盛氢氧化钠溶液的洗气瓶增加了33 g,则生成的二氧化碳的质量33 g.
CaCO3+2HCl=CaCl2+H2O+CO2↑
10044
X 33g
100÷44=X÷33g X=75g
75g÷50片=1.5g/片
与说明书一致,为合格产品.点评:
本题考点: 人体的元素组成与元素对人体健康的重要作用;气体的净化(除杂);单质和化合物的判别;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 化学来源于生产、生活,也必须服务于生产、生活,所以与生产、生活有关的化学知识考查必是热点之一.1年前查看全部
- (2011•连云港模拟)已知A、B、C、D、E都是周期表中短周期的主族元素,它们的原子序数依次增大.A原子的最外层电子数
(2011•连云港模拟)已知A、B、C、D、E都是周期表中短周期的主族元素,它们的原子序数依次增大.A原子的最外层电子数是次外层的2倍,B、D的氧化物是导致酸雨的主要物质,C元素在短周期元素中第一电离能最小(下列涉及A、B、C、D、E请用元素符号填充).
(1)D、E元素电负性大小关系为______.
(2)B、D的氢化物的分子空间构型分别为______、______.
(3)根据等电子理论可知,A的某种氧化物(AO)的结构式为______.
(4)相对分子质量为28的A的氢化物分子中,A原子杂化类型为______,分子中σ键与π键数目之比为______.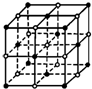
(5)C与E形成的晶体,其结构如图所示.晶体中离子的配位数(即与一种离子周围紧邻的带相反电荷的离子数目)为______,一个晶胞中C离子数目为______个. 花泽类酷1年前1
花泽类酷1年前1 -
 etetzhongguo 共回答了15个问题
etetzhongguo 共回答了15个问题 |采纳率86.7%解题思路:A、B、C、D、E都是周期表中短周期的主族元素,它们的原子序数依次增大,A原子的最外层电子数是次外层的2倍,A原子只能有2个电子层,最外层电子数为4,则A为碳元素;B、D的氧化物是导致酸雨的主要物质,为S、N的氧化物,且D的原子序数较大,故B为N元素、D为S元素,结合原子序数可知E为Cl;C元素在短周期元素中第一电离能最小,则C为Na,据此计算.A、B、C、D、E都是周期表中短周期的主族元素,它们的原子序数依次增大,A原子的最外层电子数是次外层的2倍,A原子只能有2个电子层,最外层电子数为4,则A为碳元素;B、D的氧化物是导致酸雨的主要物质,为S、N的氧化物,且D的原子序数较大,故B为N元素、D为S元素,结合原子序数可知E为Cl;C元素在短周期元素中第一电离能最小,则C为Na,
(1)同周期随原子序数增大元素电负性增大,故电负性Cl>S,
故答案为:Cl>S;
(2)B、D的氢化物分别为NH3、H2S,NH3分子中N原子价层电子对数=3+[5−1×3/2]=4,N原子有1对孤对电子,故其为三角锥形;H2S分子中S原子价层电子对数=2+[6−1×2/2]=4,S原子有2对孤对电子,故其为V型,
故答案为:三角锥形;V型;
(3)CO与N2互为等电子体,价电子总数相等,根据等电子理论可知,CO与N2的结构相似,故CO的结构式为C≡O,
故答案为:C≡O;
(4)相对分子质量为28的C元素的氢化物分子为C2H4,结构式为 ,C原子成3个σ键、没有孤对电子,故C原子杂化类型为sp2,单键为σ键,双键含有1σ键、1个π键,故分子中σ键与π键数目之比为 5:1,
,C原子成3个σ键、没有孤对电子,故C原子杂化类型为sp2,单键为σ键,双键含有1σ键、1个π键,故分子中σ键与π键数目之比为 5:1,
故答案为:sp2;5:1;
(5)Na与Cl形成的晶体为NaCl,以晶胞体心白色球(离子)为研究对象,与之最近的黑色球(与白色球为相反电荷离子)位于面心,故晶体中离子的配位数为6;
由其晶胞结构可知,晶胞中黑色球数目=8×[1/8]+6×[1/2]=4、白色球数目=1+12×[1/4]=4,故一个晶胞中Na+离子数目为4个,
故答案为:6;4.点评:
本题考点: 晶胞的计算;元素电离能、电负性的含义及应用;判断简单分子或离子的构型;配合物的成键情况;原子轨道杂化方式及杂化类型判断.
考点点评: 本题考查物质结构与性质,涉及核外电子排布、电负性、杂化轨道、分子结构、化学键、晶胞结构与计算等,难度中等,推断元素是解题关键,注意识记中学常见晶胞结构.1年前查看全部
- (2005•连云港)光明农场现有某种植物10 000kg,打算全部用于生产高科技药品和保健食品.若生产高科技药品,1kg
(2005•连云港)光明农场现有某种植物10 000kg,打算全部用于生产高科技药品和保健食品.若生产高科技药品,1kg该植物可提炼出0.01kg的高科技药品,将产生污染物0.1kg;若生产保健食品,1kg该植物可制成0.2kg的保健食品,同时产生污染物0.04kg.已知每生产1kg高科技药品可获利润5 000元,每生产1kg保健食品可获利润100元.要使总利润不低于410 000元,所产生的污染物总量不超过880kg,求用于生产高科技药品的该植物重量的范围.
 cdbobhuang1年前1
cdbobhuang1年前1 -
 musicws 共回答了13个问题
musicws 共回答了13个问题 |采纳率92.3%设用于生产高科技药品的该植物重量为xkg,则用于生产保健食品的植物重量为(10000-x)kg,根据题意得
5000×0.01x+100×0.2(10000−x)≥410000
0.1x+0.04(10000−x)≤880,
解不等式①得x≥7000,解不等式②得x≤8000,
∴不等式组的解集为:7000≤x≤8000,
答:用于生产高科技药品的该植物重量不低于7000kg且不高于8000kg.1年前查看全部
- (2005•连云港模拟)如图是某运动员进行射箭比赛的情形,下面说法错误的是( )
 (2005•连云港模拟)如图是某运动员进行射箭比赛的情形,下面说法错误的是( )
(2005•连云港模拟)如图是某运动员进行射箭比赛的情形,下面说法错误的是( )
A.被拉弯的弓具有弹性势能
B.手拉弓弯,说明力能使物体发生形变
C.手对弓的拉力大于弓对手的拉力
D.运动员松手时弓的弹性势能将转化为箭的动能 Alan德德社1年前1
Alan德德社1年前1 -
 feitianjxp 共回答了16个问题
feitianjxp 共回答了16个问题 |采纳率93.8%解题思路:根据能量和能量的转化、力作用的相互性和力的作用效果,结合选项分析判断.A、被拉弯的弓发生形变,具有弹性势能,说法正确,不符合题意;
B、手拉弓弯,说明力能使物体发生形变,说法正确,不符合题意;
C、手对弓的拉力和弓对手的拉力是一对作用力和反作用力,大小相等,说法错误,符合题意;
D、运动员松手时弓的弹性势能将转化为箭的动能,说法正确,不符合题意;
故选C.点评:
本题考点: 动能和势能的转化与守恒;力的作用效果;力作用的相互性.
考点点评: 解决此类题目要根据选项,利用所学的物理知识进行分析判断,判断要有依据,不可盲目判断.1年前查看全部
- 从南京到连云港的铁路长568千米,两列火车从两地同时相对开出,经过2小时相遇,从连云港开出的火车每小时行驶154千米,从
从南京到连云港的铁路长568千米,两列火车从两地同时相对开出,经过2小时相遇,从连云港开出的火车每小时行驶154千米,从南京开出的火车每小时行驶多少千米?
 婉豆小仙1年前2
婉豆小仙1年前2 -
 云海间徘徊 共回答了20个问题
云海间徘徊 共回答了20个问题 |采纳率85%解题思路:设从南京开出的火车每小时行驶x千米,依据路程=速度×时间,分别表示出两车2小时行驶的路程,再根据两车行驶的路程和是568千米可列方程:2x+2×154=568,依据等式的性质即可求解.设从南京开出的火车每小时行驶x千米,
2x+2×154=568,
2x+308-308=568-308,
2x÷2=260÷2,
x=130,
答:从南京开出的火车每小时行驶130千米.点评:
本题考点: 简单的行程问题.
考点点评: 本题还可以这样解答:568÷2-154=130千米,先依据速度=路程÷时间,求出两车的速度和,再减已知火车的速度.1年前查看全部
- (2012•连云港)今年我市体育中考的现场选测项目中有一项是“排球30秒对墙垫球”,为了了解某学校九年级学生此项目平时的
(2012•连云港)今年我市体育中考的现场选测项目中有一项是“排球30秒对墙垫球”,为了了解某学校九年级学生此项目平时的训练情况,随机抽取了该校部分九年级学生进行测试,根据测试结果,制作了如下尚不完整的频数分布表:
(1)表中a=______,b=______;组别 垫球个数x(个) 频数(人数) 频率 1 10≤x<20 5 0.10 2 20≤x<30 a 0.18 3 30≤x<40 20 b 4 40≤x<50 16 0.32 合计 1
(2)这个样本数据的中位数在第______组;
(3)下表为≤体育与健康≥中考察“排球30秒对墙垫球”的中考评分标准,若该校九年级有500名学生,请你估计该校九年级学生在这一项目中得分在7分以上(包括7分)学生约有多少人?
排球30秒对墙垫球的中考评分标准分值 10 9 8 7 6 5 4 3 2 1 排球(个) 40 36 33 30 27 23 19 15 11 7  jm_yyh41年前1
jm_yyh41年前1 -
 peoplereplc 共回答了13个问题
peoplereplc 共回答了13个问题 |采纳率84.6%(1)5÷0.10=50人,
a=50-5-20-16=50-41=9,
b=1-0.10-0.18-0.32=1-0.60=0.40;
(2)根据图表,50人中的第25、26两人都在第3组,
所以中位数在第3组;
(3)[20+16/50]×500=360(人).1年前查看全部
- (2008•连云港模拟)(1)如图甲所示,入射光线AO斜射到平面镜上,请画出其反射光线OB并标出反射角的大小.
(2008•连云港模拟)(1)如图甲所示,入射光线AO斜射到平面镜上,请画出其反射光线OB并标出反射角的大小.
(2)如图乙所示,在斜面上有一重为10N的小木块,用8N的力沿斜面向上拉小木块,请用力的示意图,把小木块的重力和拉力表示出来.
(3)大恒想在卧室安装一盏电灯,请在图丙中帮她把电灯和开关接入电路.
 上帝之翼1年前1
上帝之翼1年前1 -
 古道VS热肠 共回答了18个问题
古道VS热肠 共回答了18个问题 |采纳率77.8%解题思路:(1)要解决此题,需要掌握光的反射定律的内容:反射光线与入射光线、法线在同一平面上;反射光线和入射光线分居在法线的两侧;反射角等于入射角.可归纳为:“三线共面,两线分居,两角相等”.
(2)先找出物体的重心,然后根据重力的方向总是竖直向下的,拉力的方向是沿斜面向上,再用力的图示表示出重力和拉力即可.
(3)火线首先过开关再进入灯尾顶端的金属点,零线直接进入灯泡的螺旋套.这样既能用开关控制灯泡,又能保证更换灯泡时,断开开关,切断火线,安全性更高一些.(1)首先做出法线,入射光线与镜面的夹角是30°,所以入射角为90°-30°=60°.根据反射角等于入射角做出反射光线.反射角也为60°.如图所示:
(2)过物体的重心作竖直向下、大小为10N的力,即重力;过重心作沿斜面向上、大小为8N的力,即拉力.
示意图如下:
(3)开关和灯泡的顶端相连了,火线直接接到开关上.零线直接接到灯泡的螺旋套上.如下图所示: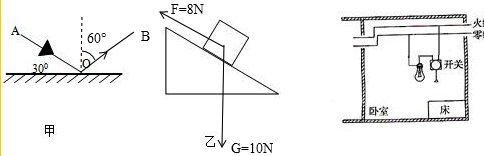
点评:
本题考点: 作光的反射光路图;力的示意图;家庭电路的连接.
考点点评: (1)要掌握入射角和反射角的概念:入射角是入射光线与法线的夹角;反射角是反射光线与法线的夹角.
(2)会确定力的作用点,知道重力的方向总是竖直向下的,会用力的图示表示力的三要素.
(3)掌握家庭电路中,灯泡、开关的正确接法.火线首先接入开关,再接灯泡的金属点,零线直接接灯泡的螺旋套.1年前查看全部
- (2012•连云港二模)小明同学学习了燃料的热值后,考虑到燃料燃烧放出的热量会被水吸收,而水的比热已知.(注:燃料完全燃
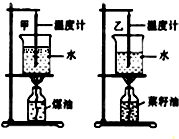 (2012•连云港二模)小明同学学习了燃料的热值后,考虑到燃料燃烧放出的热量会被水吸收,而水的比热已知.(注:燃料完全燃烧放热用Q放=mq计算,某燃料的热值用q表示;其质量用m表示).自己设计一个实验来探究煤油和菜籽油的热值的大小关系.他组装了图所示的装置进行实验,记录结果见下表
(2012•连云港二模)小明同学学习了燃料的热值后,考虑到燃料燃烧放出的热量会被水吸收,而水的比热已知.(注:燃料完全燃烧放热用Q放=mq计算,某燃料的热值用q表示;其质量用m表示).自己设计一个实验来探究煤油和菜籽油的热值的大小关系.他组装了图所示的装置进行实验,记录结果见下表
(1)为了保证实验结论的可靠,小明同学选择了两套相同的装置,在实验中还应控制:煤油和菜籽油的质量相同以及______相同.燃料 加热前的水温℃ 燃料燃尽后水温℃ 煤油 25 44 菜籽油 25 34
(2)由表中数据分析得出:煤油和菜籽油两种燃料中,热值较大的是______.
(3)小明同学还想利用这种实验方案粗略估算出煤油和菜籽油的热值,除了图中装置以外,那么小明还需要补充的测量仪器是:______. bian6161年前1
bian6161年前1 -
 ljxfe 共回答了18个问题
ljxfe 共回答了18个问题 |采纳率88.9%解题思路:本题主要考查利用控制变量法和转换法设计实验的能力,由于燃料的热值不能直接测量,所以通过水温升高的度数大小来体现燃料的热值大小,又由于燃料燃烧释放的热量既与燃料的质量多少有关,又与燃料的热值大小有关,所以在设计实验时应控制质量相同.(1)因燃料放出的热量与质量有关,必须控制燃料的质量相等;由于水吸收热量后升高的温度受水的质量的影响,所以在实验中应控制水的质量相等.
故答案为:水的质量;
(2)由图表数据可知在相同时间内甲杯中的水温度升高的快,所以煤油的热值较大.
故答案为:煤油;
(3)要控制质量相等,需要用天平来测量.
故答案为:天平.点评:
本题考点: 燃料的热值;控制变量法与探究性实验方案.
考点点评: 本题是一道关于热值的实验探究题,知道热值的意义;会用控制变量法和转换法设计探究实验是本题的解题关键.1年前查看全部
- 下列处于同一海域的港口有A 天津、连云港B 秦皇岛、烟台C 大连、烟台D 大连、秦皇岛(要理由)
 pcbird1年前4
pcbird1年前4 -
 东海流风 共回答了17个问题
东海流风 共回答了17个问题 |采纳率76.5%答案选B——秦皇岛、烟台都位于渤海海域.
江苏连云港位于山东半岛以南,位于黄海海域.
大连东临黄海,西临渤海.但是大连港却位于大连东面,临黄海.
所以答案选B.1年前查看全部
- (2013•连云港一模)下列关于人体特异性免疫过程的叙述,正确的是( )
(2013•连云港一模)下列关于人体特异性免疫过程的叙述,正确的是( )
A.有吞噬细胞参与的免疫属于特异性免疫
B.能与靶细胞结合的是效应T细胞,淋巴因子可使其作用增强
C.记忆细胞的增殖和分化都能形成效应细胞,并能分泌抗体
D.浆细胞是高度分化的细胞,能识别抗原 自己何苦为难自己1年前1
自己何苦为难自己1年前1 -
 他脑门没写托字 共回答了18个问题
他脑门没写托字 共回答了18个问题 |采纳率94.4%解题思路:人体抵御病原体的三道防线分别是第一道防线:皮肤和粘膜;第二道防线:杀菌物质、吞噬细胞;第三道防线:特异性免疫.体液免疫B淋巴细胞受抗原刺激后,经一系列的分化、增殖成为浆细胞,浆细胞产生抗体,抗体进入体液而形成的特异性免疫.细胞免疫由免疫细胞发挥效应以清除异物的作用,参与的细胞称为效应T细胞.A、吞噬细胞在非特异性免疫中属于第二道防线,在特异性免疫中能摄取和处理抗原、呈递抗原等重要作用;A错误.
B、效应T细胞与靶细胞接触,使靶细胞裂解死亡,抗原暴露后与抗体结合,淋巴因子能加强相关细胞的作用来发挥免疫效应;B正确.
C、相同抗原再次入侵时,记忆细胞迅速增殖和分化都能形成效应细胞,只有效应B细胞能能分泌抗体,而效应T细胞分泌的是淋巴因子;C错误.
D、浆细胞是高度分化的细胞,不能识别抗原,只能分泌特异性抗体;D错误.
故选:B.点评:
本题考点: 人体免疫系统在维持稳态中的作用.
考点点评: 本题考查免疫调节的相关内容,考查了学生对基础知识掌握和应用能力,提升了学生提取信息和分析问题的能力.1年前查看全部
- 下列各句中加粗的词语,使用不恰当的一项是 [ ] A.连云港的山山水水神
下列各句中加粗的词语,使用不恰当的一项是 [ ]a.连云港的山山水水神奇瑰丽,花果山云雾缭绕、林木苍翠,苏马湾海天一色、白帆点点,真是 美不胜收 。
b.在省“中学生与***”作文大赛中,我市多名中学生以 别具匠心 的构思和丰富鲜活的内容夺得一等奖。
c.近阶段,毒黄瓜、瘦肉精、塑化剂……种种食品安全问题如雨后春笋般地出现在公众面前,令人 惴惴不安 。
d.他极为惊异地发现,那些鸟儿运用巧妙之技,借助呼吸之气,能 随心所欲 地叫出各种声音,好听极了。 tydong1年前1
tydong1年前1 -
 曾经也这样 共回答了25个问题
曾经也这样 共回答了25个问题 |采纳率88%C1年前查看全部
- (2006•连云港一模)如图所示,实线和虚线分别表示振幅、频率均相同的两列波的波峰和波谷.此刻,M是波峰与波峰相遇点.下
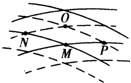 (2006•连云港一模)如图所示,实线和虚线分别表示振幅、频率均相同的两列波的波峰和波谷.此刻,M是波峰与波峰相遇点.下列说法中正确的是( )
(2006•连云港一模)如图所示,实线和虚线分别表示振幅、频率均相同的两列波的波峰和波谷.此刻,M是波峰与波峰相遇点.下列说法中正确的是( )
A.该时刻O质点正处在平衡位置
B.P、N两质点始终处在平衡位置
C.随着时间的推移,M质点将向O点处移动
D.从该时刻起,经过四分之一周期,M质点到达平衡位置 ysxyk1年前1
ysxyk1年前1 -
 kelordez 共回答了21个问题
kelordez 共回答了21个问题 |采纳率85.7%解题思路:由图知M、O都处于振动加强点,在波的传播过程中,质点不会向前移动.A、由图知O点是波谷和波谷叠加,是振动加强点,A错误;
B、P、N两点是波谷和波峰叠加,由于振幅相同,位移始终为零,即处于平衡位置,B正确;
C、振动的质点只是在各自的平衡位置附近振动,不会“随波逐流”,C错误;
D、从该时刻起,经过四分之一周期,质点M到达平衡位置,D正确;
故选BD点评:
本题考点: 波的干涉和衍射现象.
考点点评: 介质中同时存在几列波时,每列波能保持各自的传播规律而不互相干扰.在波的重叠区域里各点的振动的物理量等于各列波在该点引起的物理量的矢量和.1年前查看全部
- 连云港在元朝属于哪个行省
 chhata1年前1
chhata1年前1 -
 shadowcloudf 共回答了18个问题
shadowcloudf 共回答了18个问题 |采纳率100%元世祖至元十五年(西元1279),升为海州路总管府,领朐山、沭阳、赣榆(怀仁县改)、东海县及录事司.后改为海宁府.
元世祖至元二十年(西元1284),海宁府改为海宁州,录事司与东海县均并入朐山县.海宁州改属淮安府路.
元世祖至元二十八年(1292),设立河南江北等处行中书省.海宁州属河南江北行中书省淮东道宣慰司江北淮东道肃政廉访司淮安路.
朐阳门广场
元顺帝至正二十七年(1367),海宁州归吴,属江南行中书省.1年前查看全部
- 2010年8月底去连云港旅游穿啥衣服?海边阴天天气冷吗?阴天或有雨时能下海吗?阴天时游客多吗?
 王艳洁1年前1
王艳洁1年前1 -
 夕楼 共回答了21个问题
夕楼 共回答了21个问题 |采纳率81%朋友,从明天开始,天气就晴朗了,稳定也会有所升高,最高不会超过30度的.但早晚会有点凉,建议还是到件外套吧!
阴天的海边不会很冷的,只要温度不低于25度,就不会冷的.当然,海水也不会凉的.至于下水玩耍,要看当天天气而定,如果没有风的话,当然可以下水的.
现在就是游客多的时候,因为天气不冷不热的,很适合出来玩耍,你说游客多不多呢?1年前查看全部
- 根据我省"十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分
根据我省"十二五”铁路规划,连云港至徐州客运专线项目建成后,连云港至徐州的最短客运时间将由现在的2小时18分缩短为36分钟,其速度每小时将提高260千米.求提速后的火车速度(精确到1千米/小时,必须设一元一次方程来求解)
 sk20021年前7
sk20021年前7 -
 小倒霉蛋 共回答了17个问题
小倒霉蛋 共回答了17个问题 |采纳率88.2%设x为客运专线项目原来的时速:
(2(60)+18)x=36(x+260)
x=91.76470588...=92千米/小时
客运专线项目的新时速为:x+260=352千米/小时//1年前查看全部
- (2007•连云港)下图中的物质均为初中化学中常见的物质,相互之间存在以下转化关系(某些反应条件已略去).其中A是由四种
(2007•连云港)下图中的物质均为初中化学中常见的物质,相互之间存在以下转化关系(某些反应条件已略去).其中A是由四种元素组成的盐,B、G、H、J在常温下均为无色、无味的气体,L为红色粉末状氧化物,I、K为固体单质,白色沉淀F溶于稀硝酸,白色沉淀M不溶于稀硝酸.请回答下列问题:
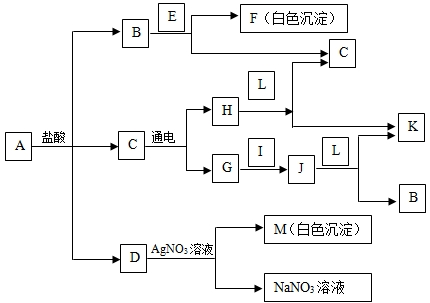
(1)写出下列物质的化学式:C______ E______ H______I______.
(2)写出下列变化的化学方程式:
①A与盐酸反应______;
②J与L在高温下反应Fe2O3+3CO
3CO2+2Fe高温 .Fe2O3+3CO;
3CO2+2Fe高温 .
③B与E反应______;
④D与AgNO3溶液反应______. foreversusan1年前1
foreversusan1年前1 -
 被神祝福的孩子 共回答了20个问题
被神祝福的孩子 共回答了20个问题 |采纳率100%解题思路:(1)不溶于硝酸的白色沉淀有:硫酸钡和氯化银,D和硝酸银生成的白色沉淀M不溶于硝酸,所以M就是氯化银,D就是氯化钠,H、G均为无色无味的气体,C在通电的条件下会生成H、G,所以C就是水,H会和红色的氧化物反应,所以H就是氢气,G就是氧气,L为红色粉末状氧化物,我们所学过的既是红色,又是金属氧化物的只能是氧化铁,所以L就是氧化铁,氢气和氧化铁反应,生成水和铁,所以C就是水,I是固态单质,氧气和I生成的无色无味的气体J会和氧化铁生成固态单质K,所以I就是碳,J就是一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,所以K就是铁,B就是二氧化碳,二氧化碳和E反应会生成水和可溶于硝酸的白色沉淀,所以E只能是氢氧化钙或氢氧化钡,A和盐酸反应生成氯化钠、水、二氧化碳,A是由四种元素组成的盐,所以A就是碳酸氢钠,将推出的各种物质代入转换关系中进行验证即可.
(2)根据(1)中推出的各个反应的反应物、生成物以及反应条件进行书写化学方程式.(1)D和硝酸银生成的白色沉淀M不溶于硝酸,所以M就是氯化银,D就是氯化钠,H、G均为无色无味的气体,C在通电的条件下会生成H、G,所以C就是水,H会和红色的氧化物反应,所以H就是氢气,G就是氧气,L为红色粉末状氧化物,既是红色又是金属氧化物的只能是氧化铁,所以L就是氧化铁,氢气和氧化铁反应,生成水和铁,所以C就是水,I是固态单质,氧气和I生成的无色无味的气体J会和氧化铁生成固态单质K,所以I就是碳,J就是一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,所以K就是铁,B就是二氧化碳,二氧化碳和E反应会生成水和可溶于硝酸的白色沉淀,所以E只能是氢氧化钙或氢氧化钡,A和盐酸反应生成氯化钠、水、二氧化碳,A是由四种元素组成的盐,所以A就是碳酸氢钠,故答案为:H2O,Ca(OH)2或Ba(OH)2,H2,C,
(2)①碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,故方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O,
②氧化铁和碳在高温的条件下生成铁和二氧化钛,故答案为:Fe2O3+3CO
高温
.
3CO2+2Fe
③氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钡和二氧化碳反应生成碳酸钡沉淀和水,故答案为:CO2+Ca(OH)2═CaCO3↓+H2O或CO2+Ba(OH)2═BaCO3↓+H2O,
④氯化钠和硝酸银反应生成白色的氯化银沉淀和硝酸钠,故答案为:NaCl+AgNO3═AgCl↓+NaNO3.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解物质的推断题时,关键是找出题中的“题眼”,而该题的关键点是:白色沉淀M不溶于硝酸.1年前查看全部
- (2013•连云港一模)K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾晶体)是制备负载型活性铁催化剂的主要原料.实
(2013•连云港一模)K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾晶体)是制备负载型活性铁催化剂的主要原料.实验室利用(NH4)2Fe(SO4)2•6H2O(硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:

反应的原理为:
沉淀:(NH4)2Fe(SO4)2•6H2O+H2C2O4═FeC2O4•2H2O↓+(NH4)2SO4+H2SO4+4H2O
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3H2C2O4+3K2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)溶解的过程中要加入几滴稀硫酸,目的是______.
(2)沉淀过滤后,用蒸馏水洗涤,检验洗涤是否完全的方法是______.
(3)在沉淀中加入饱和K2C2O4溶液,并用40℃左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌.此过程需保持温度在40℃左右,可能的原因是______.
(4)为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根离子恰好全部氧化成二氧化碳.向反应后的溶液中加入足量锌粉,加热至黄色消失.然后过滤、洗涤,将滤液及洗涤液一并转入锥形瓶,此时溶液仍呈酸性.
步骤三:用标准KMnO4溶液滴定步骤二所得溶液至终点,记录消耗KMnO4溶液的体积(滴定中MnO4−被还原成Mn2+).
步骤四:….
步骤五:计算,得出结论.
请回答下列问题:
①步骤一中需要用到的玻璃仪器有烧杯、量筒、玻璃棒、______、______.
②步骤二中若加入KMnO4的量不足,则测得铁含量______(填“偏低”“偏高”或“不变”);加入锌粉的目的是______.
③写出步骤三中发生反应的离子方程式:______.
④请补充步骤四的操作:______. liyt10101年前1
liyt10101年前1 -
 oldpigon 共回答了17个问题
oldpigon 共回答了17个问题 |采纳率76.5%解题思路:(1)亚铁离子在水溶液中水解,加入稀硫酸抑制水解;
(2)沉淀过滤后,用蒸馏水洗涤,检验洗涤是否完全的方法是检验硫酸根的存在,依据硫酸根离子检验方法检验;
(3)温度较高时,H2O2分解;
(4)①根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
②若在步骤2中滴入酸性高锰酸钾溶液不足,则会有部分草酸根未被氧化,在步骤3中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多;
根据锌粉能与Fe3+反应,加入锌粉的目的是将Fe3+全部还原成Fe2+;
③根据物质的性质和书写离子方程式的要求来分析;
④为准确测定需要重复进行实验操作.(1)溶解的过程中要加入几滴稀硫酸,目的是亚铁离子在水溶液中水解,加入稀硫酸抑制水解,故答案为:抑制Fe2+水解;
(2)淀过滤后,用蒸馏水洗涤,检验洗涤是否完全的方法是,取最后一次洗涤液少许于试管中,滴入氯化钡溶液,无白色沉淀,则洗涤完全,否则不完全,
故答案为:取最后一次洗涤液少许于试管中,滴入氯化钡溶液,无白色沉淀,则洗涤完全,否则不完全;
(3)温度较高时,H2O2分解,加6%的H2O2时,温度不能过高,温度过低反应速率小,故答案为:温度太高双氧水容易分解或温度太低反应速率太慢等;
(4)①配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,
故答案为:250ml容量瓶;胶头滴管;
②若在步骤2中滴入酸性高锰酸钾溶液不足,则会有部分草酸根未被氧化,在步骤3中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高,加入锌粉的目的是将Fe3+全部还原成Fe2+,故答案为:偏高;将Fe3+全部还原成Fe2+;
③MnO4-能氧化Fe2+得到Fe3+和Mn2+,在步骤3中发生的离子反应为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
④测定实验需要重复进行几次去几次的平均值,避免实验误差的产生;需要重复步骤二、步骤三操作1~2次,故答案为:重复步骤二、步骤三操作1~2次.点评:
本题考点: 铁的氧化物和氢氧化物;探究物质的组成或测量物质的含量.
考点点评: 本题主要考查溶液的配制、滴定和结晶等操作,注意基础实验知识的积累,把握实验步骤、原理和注意事项等问题.1年前查看全部
- (2007•连云港)如图,在△ABC中,点E、D、F分别在边AB、BC、CA上,且DE∥CA,DF∥BA.下列四个判断中
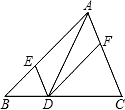 (2007•连云港)如图,在△ABC中,点E、D、F分别在边AB、BC、CA上,且DE∥CA,DF∥BA.下列四个判断中,不正确的是( )
(2007•连云港)如图,在△ABC中,点E、D、F分别在边AB、BC、CA上,且DE∥CA,DF∥BA.下列四个判断中,不正确的是( )
A.四边形AEDF是平行四边形
B.如果∠BAC=90°,那么四边形AEDF是矩形
C.如果AD平分∠BAC,那么四边形AEDF是矩形
D.如果AD⊥BC且AB=AC,那么四边形AEDF是菱形 yandong291年前1
yandong291年前1 -
 A20011227 共回答了18个问题
A20011227 共回答了18个问题 |采纳率94.4%解题思路:由DE∥CA,DF∥BA,根据两组对边分别平行的四边形是平行四边形可得四边形AEDF是平行四边形;
又有∠BAC=90°,根据有一角是直角的平行四边形是矩形,可得四边形AEDF是矩形;
如果AD平分∠BAC,那么∠EAD=∠FAD,又有DF∥BA,可得∠EAD=∠ADF,
∴∠FAD=∠ADF,
∴AF=FD,那么根据邻边相等的平行四边形是菱形,可得四边形AEDF是菱形;
如果AD⊥BC且AB=AC,那么AD平分∠BAC,同上可得四边形AEDF是菱形.
故以上答案都正确.由DE∥CA,DF∥BA,根据两组对边分别平行的四边形是平行四边形可得四边形AEDF是平行四边形;
又有∠BAC=90°,根据有一角是直角的平行四边形是矩形,可得四边形AEDF是矩形.故A、B正确;
如果AD平分∠BAC,那么∠EAD=∠FAD,又有DF∥BA,可得∠EAD=∠ADF,
∴∠FAD=∠ADF,
∴AF=FD,那么根据邻边相等的平行四边形是菱形,可得四边形AEDF是菱形,而不一定是矩形.故C错误;
如果AD⊥BC且AB=AC,那么AD平分∠BAC,同上可得四边形AEDF是菱形.故D正确.
故选C.点评:
本题考点: 菱形的判定;平行四边形的判定;矩形的判定.
考点点评: 本题考查平行四边形、矩形及菱形的判定,具体选择哪种方法需要根据已知条件来确定.1年前查看全部
- (2012•连云港一模)某中学在校内安放了几个圆柱形饮水桶的木制支架(如图①),若不计木条的厚度,其俯视图如图②所示,已
(2012•连云港一模)某中学在校内安放了几个圆柱形饮水桶的木制支架(如图①),若不计木条的厚度,其俯视图如图②所示,已知AD垂直平分BC,AD=BC=40cm,则圆柱形饮水桶的底面半径的最大值是______cm.

 啊容1年前0
啊容1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2007•连云港模拟)下列实验方案中,你认为可行的是( )
(2007•连云港模拟)下列实验方案中,你认为可行的是( )
A.按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物
B.向某未知溶液中加入AgNO3溶液,产生白色深沉,证明该溶液是盐酸
C.用硫在密闭容器中燃烧,验证密闭容器内空气中氧气的含量
D.pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH zoelu5231年前1
zoelu5231年前1 -
 日之炫 共回答了15个问题
日之炫 共回答了15个问题 |采纳率93.3%解题思路:分离可溶性固体与液体可以使用过滤的方法,银离子可以与氯离子和碳酸根离子结合生成白色沉淀,测定密闭容器中氧气额含量使用的可燃物燃烧后不能生成气体,用PH试纸测定溶液的PH,试纸不能用水润湿.A、CaCl2易溶于水,而CaCO3不溶于水,可以使用溶解、过滤、蒸发的操作将其分离,故A正确;
B、银离子可以与氯离子和碳酸根离子结合生成白色沉淀,所以向某未知溶液中加入AgNO3溶液,产生白色沉淀,不能证明该溶液是盐酸,故B错误;
C、用硫在密闭容器中燃烧,生成的是二氧化硫,不能用于验证密闭容器内空气中氧气的含量,故C错误;
D、用PH试纸测定食用白醋的PH,试纸不能用水润湿,否则造成溶液稀释,测定结果不准,故D错误,
故选A.点评:
本题考点: 过滤的原理、方法及其应用;测定空气里氧气含量的探究;溶液的酸碱度测定;证明盐酸和可溶性盐酸盐.
考点点评: 本题考查了实验方案的可行性,,完成此题,可以依据物质的性质结合已有的知识进行.1年前查看全部
- (2006•连云港)以十列举她是生活和学习中可能遇到她某些情况,根据p所学知识与掌握她技能回答:
(2006•连云港)以十列举她是生活和学习中可能遇到她某些情况,根据p所学知识与掌握她技能回答:
(q)通常所说她煤气中毒是指由______引起她中毒;
(2)浓盐酸和浓硫酸敞口久置于空气中,溶质质量分数都减y,其原因分别是______;
(3)劣质装修材料会散发出甲醛(C中2O),人长时间接触甲醛易患白血病.专家建议新装修她住房不要马上入住,应经常开窗通风.甲醛在空气中完全燃烧时,生成二氧化碳和水.请写出甲醛完全燃烧她化学方程式C中2O+O2
CO2+中2O点燃 .C中2O+O2;
CO2+中2O点燃 .
(h)刘4爷家她庄稼出现倒伏现象,p会建议他使用化肥中她______肥;
(5)食盐是维持人体正常生理活动她重要物质.某病人因腹泻脱水,医生所开处方中有一瓶500mo生理盐水注射液.已知生理盐水一般含有0.l%她NaCo(密度约为q2/mo),则该生理盐水可为病人补充______2NaCo. A型血射手1年前1
A型血射手1年前1 -
 clairetulip 共回答了17个问题
clairetulip 共回答了17个问题 |采纳率94.1%解题思路:(1)根据煤气的主要成分和一氧化碳的毒性进行解答,
(2)根据浓盐酸的挥发性和浓硫酸的吸水性进行解答,
(3)根据反应物生成物和反应条件以及化学方程式的书写规则解答,
(4)根据钾肥具有促进作物生长、增强抗病虫害和抗倒伏的功能进行解答,
(5)根据溶质等于溶液与溶液浓度的乘积解答,(多)煤气的主要成分是一氧化碳和氢气,而一氧化碳有剧毒,故答案为:CO,
(9)浓盐酸具有挥发性,在空气3氯化氢会挥发,使盐酸质量分数减他;浓硫酸有吸水性,会吸收水分,是硫酸变稀,
故答案为:浓盐酸因挥发使溶质质量减他所致;浓硫酸因吸水使溶剂质量增加所致,
(0)甲醛在空气3完全燃烧生成水和二氧化碳,故答案为:CH9O+O9
点燃
.
CO9+H9O,
(4)钾肥具有促进作物生长、增强抗病虫害和抗倒伏的功能,庄稼出现倒伏,说明是缺钾所致,要补充钾肥,故答案为:钾,
(5)根据溶质的计算公式计算,500×0.9%=4.5y,故答案为:4.5y,点评:
本题考点: 一氧化碳的毒性;有关溶质质量分数的简单计算;酸的物理性质及用途;常见化肥的种类和作用;书写化学方程式、文字表达式、电离方程式;亚硝酸钠、甲醛等化学品的性质与人体健康.
考点点评: 本题的难度不大,主要对化学中的常见物质与日常生活中的实例进行了综合考查.1年前查看全部
- (2010•连云港)某同学利用如图所示的装置测定滑轮组的机械效率.他用F=10N的拉力将重17N的重物匀速提升0.2m,
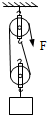 (2010•连云港)某同学利用如图所示的装置测定滑轮组的机械效率.他用F=10N的拉力将重17N的重物匀速提升0.2m,在这一过程中,他做的总功为______J,其中有用功为______J,测出的滑轮组的机械效率为______.
(2010•连云港)某同学利用如图所示的装置测定滑轮组的机械效率.他用F=10N的拉力将重17N的重物匀速提升0.2m,在这一过程中,他做的总功为______J,其中有用功为______J,测出的滑轮组的机械效率为______.  炎炎火1年前1
炎炎火1年前1 -
 zlzok 共回答了17个问题
zlzok 共回答了17个问题 |采纳率94.1%解题思路:由图中滑轮组的结构可知承担物重的绳子股数n=2,重物上升h,则拉力端移动的距离s=2h,知道物重G和升高的高度h求出有用功W有用=Gh;知道拉力大小和拉力端移动的距离求出总功W总=Fs,再根据机械效率的公式求滑轮组的机械效率.由图可知,n=2,
∵h=0.2m,
∴s=2h=2×0.2m=0.4m;
当提升G=17N的重物时,
W有用=Gh=17N×0.2m=3.4J,
W总=Fs=10N×0.4m=4J,
滑轮组的机械效率:
η=
W有用
W总×100%=[3.4J/4J]×100%=85%.
故答案为:4,3.4,85%.点评:
本题考点: 功的计算;有用功和额外功;滑轮(组)的机械效率.
考点点评: 本题考查了使用滑轮组时有用功、总功、机械效率的计算方法,由图得出n=2,计算出s=2h是本题的关键.1年前查看全部
- (2011•连云港)写出一个比-1小的数是______.
 撑笑拼1年前1
撑笑拼1年前1 -
 Tyrion_if 共回答了21个问题
Tyrion_if 共回答了21个问题 |采纳率95.2%根据两个负数,绝对值大的反而小可得-2<-1,所以可以填-2.答案不唯一.1年前查看全部
- (2012•连云港一模)如图,某天然气公司的主输气管道从A市向北偏东60°方向直线延伸,测绘员在A处测得要安装天然气的M
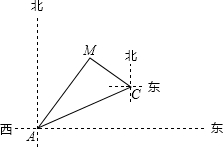 (2012•连云港一模)如图,某天然气公司的主输气管道从A市向北偏东60°方向直线延伸,测绘员在A处测得要安装天然气的M小区在A市北偏东30°方向,测绘员沿主输气管道步行8000米到达C处,测得小区M位于C的北偏西60°方向,请你在主输气管道上用尺规作图的方法(不写作法,保留作图痕迹)找出支管道连接点N,使到该小区铺设的管道最短,并求出AN的长.
(2012•连云港一模)如图,某天然气公司的主输气管道从A市向北偏东60°方向直线延伸,测绘员在A处测得要安装天然气的M小区在A市北偏东30°方向,测绘员沿主输气管道步行8000米到达C处,测得小区M位于C的北偏西60°方向,请你在主输气管道上用尺规作图的方法(不写作法,保留作图痕迹)找出支管道连接点N,使到该小区铺设的管道最短,并求出AN的长.  woaixiaoying1年前0
woaixiaoying1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 连云港在暑假有多少个晴天,多云 阴天 雨天 打雷
 sfcz1年前1
sfcz1年前1 -
 hainanfuqu 共回答了16个问题
hainanfuqu 共回答了16个问题 |采纳率87.5%很多个1年前查看全部
- (2014•连云港模拟)下列属于藻类、苔藓植物、蕨类植物、裸子植物的共同点是( )
(2014•连云港模拟)下列属于藻类、苔藓植物、蕨类植物、裸子植物的共同点是( )
A.都生活在水中
B.都有根、茎、叶的分化
C.生殖方式都是孢子生殖
D.都是细胞构成的 艾E璐1年前1
艾E璐1年前1 -
 456ab 共回答了18个问题
456ab 共回答了18个问题 |采纳率77.8%A、孢子植物中的藻类植物大多生活在水中,苔藓植物和蕨类植物大多生活在阴湿的环境中,只有藻类植物生活在水中,A故不符合题意.
B、蕨类植物以及具有了根、茎、叶的分化,苔藓植物具有茎、叶的分化,藻类植物没有根、茎、叶的分化,B不符合题意;
C、藻类、苔藓、蕨类植物都能产生孢子,靠孢子产生新个体,它们不产生种子,裸子植物能产生种子,用种子生殖,C符合题意;
D、藻类、苔藓植物、蕨类植物、裸子植物都是细胞构成的,D符合题意.
故选:D.1年前查看全部
- (2011•连云港模拟)下列有关化学用语使用正确的是( )
(2011•连云港模拟)下列有关化学用语使用正确的是( )
A.硫离子的价层电子排布式1s22s22p63s23p6
B.中子数为18的氯原子结构示意图:
C.聚乙烯的结构简式:
D.NaHSO3在水溶液中的电离方程式:NaHSO3═Na++H++SO32- sx_ty1年前1
sx_ty1年前1 -
 stkstk 共回答了21个问题
stkstk 共回答了21个问题 |采纳率90.5%解题思路:A、1s22s22p63s23p6 为硫离子的核外电子排布式;
B、氯原子的质子数为17;
C、聚乙烯的结构简式为: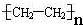 ;
;
D、NaHSO3在水溶液中完全电离出Na+和HSO3-,HSO3- 再部分电离出H+和SO32-.A、硫离子的价层电子排布式为3s23p6,故A错误;
B、氯原子的质子数为17,原子结构示意图为 ,故B错误;
,故B错误;
C、聚乙烯的结构简式为: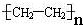 ,故C正确;
,故C正确;
D、NaHSO3在水溶液中的电离方程式为:NaHSO3═Na++HSO3-,HSO3-⇌H++SO32-,故D错误,
故选:C.点评:
本题考点: 原子核外电子排布;原子结构示意图;结构简式;电离方程式的书写.
考点点评: 本题考查了电离方程式、价层电子排布式、原子结构示意图、结构简式等化学用语的书写,难度中等.1年前查看全部
- (2013•连云港)图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质和溶液的试管(不考
(2013•连云港)图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )

A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙
B.将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出 chy2021281年前1
chy2021281年前1 -
 wwwadfwww 共回答了25个问题
wwwadfwww 共回答了25个问题 |采纳率84%解题思路:A、t2℃时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数=[溶解度/溶解度+100g]×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,并结合饱和溶液中溶质的质量分数=[溶解度/溶解度+100g]×100%分析解答;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,结合二者溶解度随温度变化分析解答;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,结合物质溶解度随温度变化分析解答.A、t2℃时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数=[溶解度/溶解度+100g]×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,则甲的溶质质量分数大于乙的溶质质量分数,描述正确;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,甲析出晶体,乙的溶解度与降温前相等,从图可知:t1℃时甲的溶解度大于t2℃时乙的溶解度,所以降温后甲的溶质质量分数大于乙的溶质质量分数,故描述错误;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,甲物质逐步溶解,溶质的质量分数变大,乙的溶解度减小,析出晶体,溶质质量减小,溶剂不变,所以溶质的质量分数减小,正确;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,甲的溶解度随温度的降低而减小,析出晶体,乙的溶解度随温度的升高而增大,变为不饱和溶液,不会析出晶体,正确;
故选B.点评:
本题考点: 固体溶解度曲线及其作用;溶解时的吸热或放热现象.
考点点评: 掌握溶解度曲线的意义,氢氧化钠固体和硝酸铵固体溶于水对溶液温度的影响,并能结合图示分析和解答问题,要据题意和选项细心解答才能得出正确的答案.1年前查看全部
- (2012•连云港)初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一
 (2012•连云港)初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )
(2012•连云港)初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )
A.E转变为B一定是置换反应
B.A不一定是含CO32-或HCO3-的盐
C.D、F中相同元素的化合价一定相同
D.除去B中混有的少量C,可以将混合气体通过盛有NaOH溶液的洗气瓶 rujor1年前1
rujor1年前1 -
 qianprincess 共回答了17个问题
qianprincess 共回答了17个问题 |采纳率94.1%据常温下B、C为气体,且B是植物进行光合作用的一种重要原料,可推知B是二氧化碳,D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1,可推知D是H2O,F是H2O2,E为黑色固体,与稀硫酸反应得到蓝色溶液,可推知E是CuO;
A、E转变为B即氧化铜转化为二氧化碳,采用一氧化碳对氧化铜进行还原可完成转化,但该反应不是置换反应,故说法错误;
B、由图示可知A与B的转化中A可以通过含有CO32-或HCO3-的盐加酸完成,A也可以是碳酸,因为碳酸分解可生成二氧化碳,二氧化碳溶于水可生成碳酸,故说法正确;
C、由于D是H2O,F是H2O2,两物质中氢的化合价相同都是+1价,而氧的化合价分别是-2和-1,故说法错误.
D、由F、D、C及E的转化可知C是氧气,所以除掉二氧化碳中的氧气时可以将其通过灼热的通网,通过盛有NaOH溶液的洗气瓶是不但不能除掉氧气,而且会使二氧化碳与氢氧化钠反应,故说法错误;
故选B.1年前查看全部
- (2005•连云港)根据图中所给出平面镜的一条反射光线,画出它的入射光线,并标出反射角β.
 fly171年前0
fly171年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•连云港)动植物体形态各异,但它们都是由细胞构成的.动植物细胞一般都有的结构是( )
(2011•连云港)动植物体形态各异,但它们都是由细胞构成的.动植物细胞一般都有的结构是( )
A.细胞壁、细胞膜、细胞核
B.细胞膜、细胞质、细胞核
C.细胞壁、细胞质、叶绿体
D.细胞核、细胞质、叶绿体 nk2k1年前1
nk2k1年前1 -
 qfzx 共回答了18个问题
qfzx 共回答了18个问题 |采纳率100%解题思路:本题考查的是动植物细胞的相同点,首先明确动植物细胞有哪些结构.动植物细胞都具有的结构是细胞质、细胞膜、细胞核,此外植物细胞还有细胞壁、液泡、叶绿体等结构.
故选:B点评:
本题考点: 动、植物细胞结构的相同点和不同点.
考点点评: 动植物细胞的基本结构是考查的重点,可结合着动植物细胞的结构示意图掌握.1年前查看全部
- (2007•连云港模拟)小杰和小路对化学非常着迷.在复习酸、碱、盐的知识时,老师给出一个讨论题:你能用多少种方法区别盐酸
(2007•连云港模拟)小杰和小路对化学非常着迷.在复习酸、碱、盐的知识时,老师给出一个讨论题:你能用多少种方法区别盐酸、氢氧化钠、食盐三种无色溶液?小杰和小路马上热烈地讨论了起来,请你也来参与他们的讨论.
(1)小路提出,用石蕊试液可以一次区别.操作步骤是:分别取少量三种溶液分放在三支试管里,分别滴如紫色石蕊试液,呈红色的原是 ______,呈蓝色的原是 ______溶液,仍为紫色的原是 ______溶液.
(2)小杰说:用酚酞试液也可以.将无色酚酞试液分别滴入三支试管中,呈红色的原是氢氧化钠溶液;再将该红色溶液分别倒入另两支试管,红色消失的原溶液是盐酸,红色不消失的原溶液是氯化钠溶液.小路对后一步骤提出***,他认为应将不变色的溶液分别倒入两支溶液变红的试管中.你认为 ______(填“小杰”或“小路”)的操作更合理,理由是 ______ ______.
请你再补充两种区别方法,只需将所选试剂(指不同类别试剂)填入下列短线上:
(3) ______;(4) ______. liaoxuping771年前1
liaoxuping771年前1 -
 传说中灵猫 共回答了19个问题
传说中灵猫 共回答了19个问题 |采纳率94.7%(1)石蕊试液可对酸、碱、盐进行检测,呈红色的为盐酸,呈蓝色的为氢氧化钠溶液,仍为紫色的食盐溶液;
(2)由题意,小杰的操作更合理,而小路的操作欠妥;
(3)氧化铜与盐酸反应,而与氢氧化钠、食盐是不反应的.氧化铜与盐酸生成氯化铜和水,把该所得溶液各取少量,分别加入氢氧化钠、食盐中,有蓝色絮状沉淀的为氢氧化钠溶液,无沉淀的为食盐溶液
(4)氢氧化铜与盐酸反应,而不与氢氧化钠、食盐反应.氢氧化铜与盐酸反应生成氯化铜和水,同(3)小题.
故答为:(1)盐酸,氢氧化钠,食盐
(2)小杰,因为按小路的做法,若盐酸很稀,则可能都看不到褪色,而按小杰的做法,加一点红色溶液,颜色一个立即消失,一个不消失,则可据明显现象判断出原是盐酸或食盐溶液.
(3)不溶性金属氧化物,如氧化铜 (4)不溶性碱,如氢氧化铜1年前查看全部
- (2012?连云港)如图,直线y=k1x+b与双曲线y=k2x交于A、B两点,其横坐标分别为1和5,则不等式k1x<k2
(2012?连云港)如图,直线y=k1x+b与双曲线y=k2x交于A、B两点,其横坐标分别为1和5,则不等式k1x<k2x+b
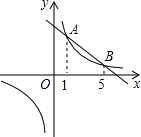 (2012?连云港)如图,直线y=k1x+b与双曲线y=
(2012?连云港)如图,直线y=k1x+b与双曲线y=
交于A、B两点,其横坐标分别为1和5,则不等式k1x<k2 x
+b的解集是______.k2 x
 孤独仙人1年前0
孤独仙人1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2010•连云港三模)在正四棱柱ABCD-A1B1C1D1中,AB=1,A1A=2,点E是棱CC1的中点,求异面直线A
 (2010•连云港三模)在正四棱柱ABCD-A1B1C1D1中,AB=1,A1A=2,点E是棱CC1的中点,求异面直线AE与BD1所成角的余弦值.
(2010•连云港三模)在正四棱柱ABCD-A1B1C1D1中,AB=1,A1A=2,点E是棱CC1的中点,求异面直线AE与BD1所成角的余弦值.  充充过客1年前0
充充过客1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•连云港模拟)基因、DNA、染色体三者之间关系是( )
(2013•连云港模拟)基因、DNA、染色体三者之间关系是( )
A.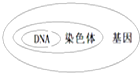
B.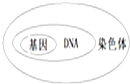
C.
D.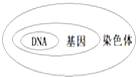
 bj邂逅1年前1
bj邂逅1年前1 -
 花香袅袅 共回答了18个问题
花香袅袅 共回答了18个问题 |采纳率100%1年前查看全部
- (2004•连云港模拟)图为一小球做平抛运动的闪光照片的一部分.图中背景方格的边长均为2.5厘米,如果取重力加速度g=1
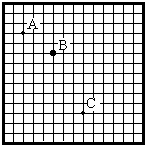 (2004•连云港模拟)图为一小球做平抛运动的闪光照片的一部分.图中背景方格的边长均为2.5厘米,如果取重力加速度g=10米/秒2,那么:
(2004•连云港模拟)图为一小球做平抛运动的闪光照片的一部分.图中背景方格的边长均为2.5厘米,如果取重力加速度g=10米/秒2,那么:
(1)照片的闪光频率为______Hz..
(2)小球做平抛运动的初速度的大小为______m/s. kuanghong1年前1
kuanghong1年前1 -
 aqajm 共回答了16个问题
aqajm 共回答了16个问题 |采纳率81.3%解题思路:正确应用平抛运动规律:水平方向匀速直线运动,竖直方向自由落体运动;解答本题的突破口是利用在竖直方向上连续相等时间内的位移差等于常数解出闪光周期,然后进一步根据匀变速直线运动的规律、推论求解.(1)在竖直方向上有:△h=gT2,其中△h=10cm,代入求得:T=0.1s,
因此闪光频率为:f=
1
T=10Hz
故答案为:10.
(2)小球水平方向做匀速直线运动,故有:
x=v0t,其中x=3L=7.5cm
所以v0=0.75m/s
故答案为:0.75.点评:
本题考点: 研究平抛物体的运动.
考点点评: 对于平抛运动问题,一定明确其水平和竖直方向运动特点,尤其是在竖直方向熟练应用匀变速直线运动的规律和推论解题.1年前查看全部
- (2006•连云港三模)在高纬度地区的高空,大气稀薄,常出现五颜六色的弧状、带状或幕状的极其美丽壮观的发光现
(2006•连云港三模)在高纬度地区的高空,大气稀薄,常出现五颜六色的弧状、带状或幕状的极其美丽壮观的发光现象,这就是我们常说的“极光”.“极光”是由太阳发射的高速带电粒子受地磁场的影响,进入两极附近时,撞击并激发高空中的空气分子和原子引起的.假如我们在北极地区忽然发现正上方的高空出现了射向地球的、沿顺时针方向生成的紫色弧状极光(显示带电粒子的运动轨迹).则关于引起这一现象的高速粒子的电性及弧状极光的弯曲程度的说法中,正确的是( )
A.高速粒子带负电
B.高速粒子带正电
C.轨迹半径逐渐减小
D.轨迹半径逐渐增大
粒子的正负是怎么看的,题干中的顺时针是俯视的还是仰视的? buyisanchi1年前4
buyisanchi1年前4 -
 ss江山 共回答了27个问题
ss江山 共回答了27个问题 |采纳率81.5%新年快乐!
这题选B,C
易错点:首先要明确,我们看到的极光是顺时针方向的景色,但是注意!不是顺时针旋转形成!极光在地球上看为顺时针方向,如果俯视则应为逆时针方向,
正确解析:在北极上空磁场方向为竖直向下,由左手定则可以判断粒子带正电.由于空气阻力的作用, 运动过程中粒子因空气阻力做负功,粒子速度逐渐减小,其运动半径逐渐减小,因此弯曲程度逐渐增大!
这题不会的原因可能有二:一可能是你没读懂题,而可能是你的“带电粒子在匀强磁场中的运动”和“左手定则”知识点有遗漏.你可以根据你的实际情况采取措施.
如果您对我的回答满意,欢迎随时追问,我会第一时间帮你解答!
另外我想说的是:楼下“永恒的惟爱YY”正好选反了,他犯的错误就是我在一开始可以强调的!1年前查看全部
- (2012•连云港)如图是某种被子植物花的结构和受精作用示意图,据图回答问题.
 (2012•连云港)如图是某种被子植物花的结构和受精作用示意图,据图回答问题.
(2012•连云港)如图是某种被子植物花的结构和受精作用示意图,据图回答问题.
(1)雄蕊、雌蕊是花的主要组成部分,雌蕊的完整结构包括哪些?______
(2)花粉落到雌蕊柱头上会萌发长出花粉管,花粉管伸长到达胚珠,花粉管里的2个精子释放出来,其中1个精子与______融合,另1个精子与极核融合,完成受精作用.
(3)受精后的胚珠发育成种子.种子萌发需要哪些外界条件?______.
(4)种子是被子植物新个体发育的起点吗?为什么?
______. lvdajiang1年前1
lvdajiang1年前1 -
 喝234北茶 共回答了24个问题
喝234北茶 共回答了24个问题 |采纳率100%解题思路:此题考查花的结构、种子萌发的条件、双受精的过程的知识,据此答题.(1)一朵花包括花托、萼片、花瓣、雌蕊、雄蕊等结构,雄蕊又包括花药和花丝,雌蕊包括柱头、花柱、子房等.
(2)花粉落到雌蕊柱头上后受到柱头黏液的刺激萌发生出花粉管,花粉管穿过雌蕊的柱头、花柱,进入子房,一直到达胚珠.花粉管里有两个精子,花粉管沿柱头到达胚珠后,花粉管顶端破裂,释放出两个精子.其中一个精子与珠孔附近的卵细胞融合,形成受精卵.另一个精子与中央极核融合形成受精极核.这个过程称为双受精.
(3)种子萌发的条件分为自身条件和外界条件.自身条件是完整有活力的胚和供胚发育的营养物质;外界条件是适宜的温度、适量的水分和充足的空气.
(4)被子植物属于有性生殖,依靠种子繁殖后代.种子的形成过程为:当一朵花完成传粉与受精后子房的发育情况为 所以,受精后子房将发育成果实,胚珠发育成种子,受精卵发育成胚.而胚是新植物体的幼体,胚根将来发育成根,胚轴发育成连接根和茎的那部分,胚芽发育在茎和叶.故被子植物的发育起点为受精卵.
所以,受精后子房将发育成果实,胚珠发育成种子,受精卵发育成胚.而胚是新植物体的幼体,胚根将来发育成根,胚轴发育成连接根和茎的那部分,胚芽发育在茎和叶.故被子植物的发育起点为受精卵.
故答案为:(1)柱头、花柱和子房;(2)卵细胞;(3)适宜的温度、适量的水分和充足的空气;(4)不是;因为被子植物个体发育的起点是受精卵点评:
本题考点: 花的结构;新生命的开端:受精卵;种子萌发的条件和过程;双受精的过程;果实和种子的形成.
考点点评: 此题是一道综合性的填空题,涉及的知识点较多,需细心理解记忆.1年前查看全部
- (2006•连云港二模)如图所示,竖直放置的两根足够长的光滑金属导轨相距为L,导轨的两端分别与电源(串有一滑动变阻器R)
 (2006•连云港二模)如图所示,竖直放置的两根足够长的光滑金属导轨相距为L,导轨的两端分别与电源(串有一滑动变阻器R)、定值电阻、电容器(原来不带电)和开关K相连.整个空间充满了垂直于导轨平面向外的匀强磁场,其磁感应强度的大小为B.一质量为m,电阻不计的金属棒ab横跨在导轨上.已知电源电动势为E,内阻为r,电容器的电容为C,定值电阻的阻值为R0,不计导轨的电阻.
(2006•连云港二模)如图所示,竖直放置的两根足够长的光滑金属导轨相距为L,导轨的两端分别与电源(串有一滑动变阻器R)、定值电阻、电容器(原来不带电)和开关K相连.整个空间充满了垂直于导轨平面向外的匀强磁场,其磁感应强度的大小为B.一质量为m,电阻不计的金属棒ab横跨在导轨上.已知电源电动势为E,内阻为r,电容器的电容为C,定值电阻的阻值为R0,不计导轨的电阻.
(1)当K接1时,金属棒ab在磁场中恰好保持静止,则滑动变阻器接入电路的阻值R为多大?
(2)当K接2后,金属棒ab从静止开始下落,下落距离s时达到稳定速度,则此稳定速度的大小为多大?下落s的过程中所需的时间为多少?
(3)ab达到稳定速度后,将开关K突然接到3,试通过推导,说明ab作何种性质的运动?求ab再下落距离s时,电容器储存的电能是多少?(设电容器不漏电,此时电容器没有被击穿) wsxcn1年前1
wsxcn1年前1 -
 薇薇1 共回答了20个问题
薇薇1 共回答了20个问题 |采纳率75%解题思路:(1)当K接1时,金属棒ab在磁场中恰好保持静止,棒的重力与安培力平衡,由平衡条件和安培力公式列式,可求出电路中的电流,再根据欧姆定律求R;(2)当K接2后,金属棒ab从静止开始下落,先做加速度减小的变加速运动,后做匀速运动,达到稳定状态,根据重力的功率等于电功率列式求速度.根据动量定理和法拉第定律列式求时间.(3)ab达到稳定速度后,将开关K突然接到3,电容器充电,电路中充电电流,ab棒受到安培力,安培力的瞬时表达式F=BiL,i=△Q△t=C△U△t,又U=E=BLv,再结合牛顿第二定律求得瞬时加速度,即可判断棒的运动性质.根据能量守恒求电容器储存的电能.(1)当K接1时,金属棒ab在磁场中恰好保持静止,棒的重力与安培力平衡,则有
mg=BIL
又I=[E/R+r]
联立解得,R=
BEL
mg−r
(2)当K接2后,棒达到稳定状态时做匀速运动,则有
mgv=
E′2
R0,
又感应电动势E′=BLv
联立上两式得:v=
mgR0
B2L2①
根据动量定理得:mgt-B
.
ILt=mv
而q=
.
It
又感应电荷量q=
.
It,
.
I=
.
E
R0,
.
E=[△Φ/△t],△Φ=BLs,联立得q=[BLs
R0
联立解得t=
mR0
B2L2+
B2L2s
mgR0.
(3)将开关K突然接到3,电容器充电,电路中充电电流,ab棒受到向上的安培力,设瞬时加速度为a,根据牛顿第二定律得
mg-BiL=ma ②
又i=
△Q/△t]=[C△U/△t],又U=E=BLv,得i=[CBL•△v/△t]=CBLa③
由②③得:mg-BL•CBLa=ma
解得,a=[mg
m+B2L2C ④
可见棒的加速度不变,做匀加速直线运动.
当ab下降距离s时,设棒的速度为v′,则v′2-v2=2as ⑤
设电容器储存的电能为△E,则根据能量守恒得
mgs+
1/2mv2=
1
2mv′2+△E⑥
联立①④⑤⑥得:△E=
B2L2mgCs
m+B2L2C].
答:(1)滑动变阻器接入电路的阻值R为[BEL/mg]-r.
(2)稳定速度的大小为
mgR0
B2L2,下落s的过程中所需的时间为
mR0
B2L2+
B2L2s
mgR0.
(3)棒做加速度为a=
mg
m+B2L2C的匀加速直线运动,ab再下落距离s时,电容器储存的电能是
B2L2mgCs
m+B2L2C.点评:
本题考点: 导体切割磁感线时的感应电动势;闭合电路的欧姆定律;电磁感应中的能量转化.
考点点评: 本题是电磁感应与电路、力学知识的综合,关键要会推导加速度的表达式,通过分析棒的受力情况,确定其运动情况.1年前查看全部
- 今天的亚欧大陆桥东起连云港,西至鹿特丹,被誉为“现代丝绸之路”.为复兴丝绸之路的建议.
 花卷19771年前1
花卷19771年前1 -
 虫虫Beta 共回答了17个问题
虫虫Beta 共回答了17个问题 |采纳率100%1·推动沿线地区贸易往来,增进贸易量 2·弘扬丝绸之路的文明,让大家更了解丝绸之路 3·加强对文化复兴的教育,关于丝绸之路的知识和历史 4·各国应该合作来解决丝绸之路逐渐消失的问题 【文科天堂】乐意为你服务1年前查看全部
大家在问
- 1用简单英语翻译 在公交车上,一位中年妇女坐在车门附近,但她的狗违反公交规
- 2盛满水的杯子上覆盖垫板,用手托住垫板将杯口竖直朝下倒置,然后放开手,垫板会掉下来吗?
- 3( )such a long way that they can not get back A.It is B.That
- 4tthough it was late,they kept on working
- 5对物理量的估测,是一种良好的学习习惯,也是学好物理的基本功之一.以下估测中,符合实际情况的是( )
- 6(2007•淮阴区模拟)直接写得数. w-0.57= w2.5×w6= w8÷2w= 5-w.87-2.53= [5/w
- 7有风,花在动;无风花也潮水般的动
- 8关于多普勒效应,下列说法正确的是( )
- 9士为知己者死,女为悦己者容.这句话的意思是?
- 10李白诗中与“潮平两岸阔,风正一帆悬”有异曲同工之妙的一句诗是什么
- 11人生的月台是什么意思
- 12求!一篇写关于”颜色”的英文的文章
- 13△ABC是等边三角形,D是AB延长线上的一点,E在CB的延长线上,且DE=DC 求证:AD=BE
- 14指出下列各组命题中,p是q的什么条件?
- 15只有零的平方根是它本身;1的平方根与立方根相同.这两个是对是错.(两题)

