如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性.请根据图示判断下列有关说法不正确的是(
 全民皆猪2022-10-04 11:39:541条回答
全民皆猪2022-10-04 11:39:541条回答 如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性.请根据图示判断下列有关说法不正确的是( )
如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性.请根据图示判断下列有关说法不正确的是( )A.甲池是原电池、乙池是电解池
B.通入乙醇的惰性电极的电极反应式为:C2H5OH+16OH--12e-═2CO32-+11H2O
C.反应一段时间后,两池溶液的pH均未变化
D.假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色

已提交,审核后显示!提交回复
共1条回复
 木为麦浪 共回答了22个问题
木为麦浪 共回答了22个问题 |采纳率95.5%- 解题思路:A、燃料电池是原电池,通入燃料的电极是负极,负极上失电子发生氧化反应,充电电池充电时A接原电池负极,B是正极发生还原反应;
B、C2H5OH在碱性条件下放电生成碳酸盐;
C、甲池放电的总方程式为C2H5OH+4OH-+3O2=2CO32-+5H2O,消耗氢氧根离子溶液的PH值变小;
D、如果乙池中加入NaI溶液,则碘离子在阳极C极放电,生成棕黄色的固体碘,用有机物萃取,有机层在下层.A、燃料电池是原电池,通入燃料的电极是负极,负极上失电子发生氧化反应,充电电池充电时A接原电池负极,B是正极发生还原反应,故A正确;
B、C2H5OH在碱性条件下放电生成碳酸盐,方程式为:C2H5OH+16OH--12e-═2CO32-+11H2O,故B错误;
C、甲池放电的总方程式为C2H5OH+4OH-+3O2=2CO32-+5H2O,消耗氢氧根离子溶液的PH值变小,故C错误;
D、如果乙池中加入NaI溶液,则碘离子在阳极C极放电,生成棕黄色的固体碘,用有机物萃取,有机层在下层,故D错误;故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池、电解池原理、热化学反应方程式的书写,明确燃料电池正负极的判断方法、电解池离子放电顺序即可解答,难点是电极反应式的书写,难度中等. - 1年前
相关推荐
- 如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )

A.两个装置之间没有盐桥,故不能形成电流 B.a电极的电极反应式:C 2 H 5 OH+16OH - -12e - =2CO+11H 2 O C.一段时间后,乙池d电极周围的溶液呈现棕褐色 D.乙池在反应前后溶液的pH不变  td87771年前1
td87771年前1 -
 猫样的女人 共回答了11个问题
猫样的女人 共回答了11个问题 |采纳率100%B
图示是原电池与电解池的联合装置,不需要盐桥就能形成电流,选项A错;乙醇作还原剂,失电子,发生氧化反应,选项B正确;乙池中,阳极反应式:2I - -2e - =I 2 ,c电极为阳极,生成单质碘,故c电极周围的溶液呈棕褐色,选项C错;d电极作阴极,阴极反应式:2H 2 O+2e - =H 2 ↑+2OH - ,故乙池溶液的pH增大,选项D错。1年前查看全部
- 如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )

A.两个装置之间没有盐桥,故不能形成电流
B.a电极的电极反应式:C2H5OH+16OH--12e-═2CO32-+11H2O
C.一段时间后,乙池d电极周围的溶液呈现棕褐色
D.乙池在反应前后溶液的pH不变 自然的暖风1年前1
自然的暖风1年前1 -
 山风一号 共回答了17个问题
山风一号 共回答了17个问题 |采纳率94.1%解题思路:燃料电池中,通入燃料的电极是负极,负极上失电子发生氧化反应,在乙池中,乙池溶液分层,上层溶液为盐溶液,电解时阴极上氢离子放电同时生成氢氧根离子,电极反应中后碘单质生成,阳极上碘离子失电子发生氧化反应,以此解答该题.A.图示是原电池与电解池的联合装置,不需要盐桥就能形成电流,故A错误;
B.乙醇作还原剂,失电子,电极方程式为C2H5OH+16OH--12e-═2CO32-+11H2O,发生氧化反应,故B正确;
C.乙池中,阳极反应式:2I--2e-═I2,c电极为阳极,生成单质碘,故c电极周围的溶液呈棕褐色,故C错误;
D.d电极作阴极,阴极反应式:2H2O+2e-═H2↑+2OH-,故乙池溶液的pH增大,故D错误,
故选B.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题综合考查原电池和电解池知识,侧重于学生的分析能力和应用能力的考查,注意把握电极方程式的书写,为解答该题的关键,难度中等.1年前查看全部
- 如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
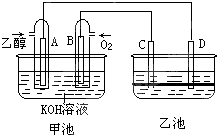 如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
(1)通入乙醇(C2H5OH)的惰性电极的电极反应式为______.若甲池可以充电,充电时A接电源的负极,此时B极发生的电极反应式为______.
(2)在乙池反应过程中,可以观察到______电极周围的溶液呈现棕褐色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色,C极发生的电极反应式______.
(3)若在常温常压下,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为______. 飘摇0071年前1
飘摇0071年前1 -
 colinyou2002 共回答了16个问题
colinyou2002 共回答了16个问题 |采纳率93.8%解题思路:(1)燃料电池中,通入燃料的电极是负极,负极上失电子发生氧化反应,充电电池充电时A接原电池负极,B是阳极,阳极上氢氧根离子失电子发生氧化反应;
(2)在乙池中,乙池溶液分层,上层溶液为盐溶液,电解时阴极上氢离子放电同时生成氢氧根离子,根据题意知,电极反应中后碘单质生成,且上层是盐溶液,为可溶性的碘盐,阳极上碘离子失电子发生氧化反应;
(3)1g乙醇的物质的量=[1/46]mol,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,1mol乙醇完全燃烧生成二氧化碳和液态水放出的热量是1366.7kJ,据此写出其热化学反应方程式.(1)该燃料电池中,负极上乙醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO32-+11H2O,
若甲池可以充电,B电极上应该失电子发生氧化反应,所以应该与电源正极相连,电解氢氧化钾溶液时,B电极上氢氧根离子失电子生成氧气,电极反应式为4OH--4e-=2H2O+O2↑,
故答案为:C2H5OH+16OH--12e-=2CO32-+11H2O;4OH--4e-=2H2O+O2↑;
(2)在乙池中,C是阳极,D是阴极,阳极上碘离子失电子发生氧化反应,电极反应式为 2I--2e‑=I2,碘溶于水溶液呈现棕褐色,所以C电极附近呈现棕褐色,
故答案为:C; 2I--2e‑=I2 ;
(3)1g乙醇的物质的量=[1/46]mol,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,1mol乙醇完全燃烧生成二氧化碳和液态水放出的热量是1366.7kJ,所以其热化学反应方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.7kJ/mol,
故答案为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.7kJ/mol.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池、电解池原理、热化学反应方程式的书写,明确燃料电池正负极的判断方法、电解池离子放电顺序即可解答,难点是电极反应式的书写,难度中等.1年前查看全部
大家在问
- 1如图为一个点电荷的电场中的三条电场线,已知电子在A点的电势能为-8eV(以无穷远处为零电势参考点),则以下判断中正确的是
- 2一根钢材长18米,第一次用全长的2/9,第二次用了全长的1/4,二次一共用了多少?还剩多少米?
- 3小学数学题目计算:7-3/2-5/4-9/8-17/16-33/32-65/64
- 4为什么双曲线y2/b2-x2/a2=1的渐近线是y=+-b/ax?
- 5问个英语问题:where对什么进行提问?how 对什么进行提问?what 对什么进行提问?
- 6竖式计算并验算. 375÷3= 946÷3= 456÷4= 900÷8= 792÷6= 350÷3=
- 7我看得见你的眼泪 作文
- 8有关刑法的小偷甲盗窃某乙的钱包,被某乙发现后追赶,追至以小池塘,小偷慌不择路跳入水中,因水性不好.
- 9英语翻译Moreover,The law efficiency of justice department leads
- 10当我看足球比赛时,我很容易感到兴奋 英文翻译 准确的哦,越准确分越高.
- 11原文:蒲留仙先生《聊斋志异》,用笔精简,寓意处全无迹相,盖脱胎于诸子,非仅抗于左史、龙门也.相传先生居乡里,落拓无偶,性
- 12已知函数f(x)=a x的平方+bx+3a+b 为偶函数,其定义域为[a-1,2a],则a的值是多少.
- 13已知每秒从太阳射到地球的垂直于太阳光的每平方米截面上的辐射能为1.4×10 3 J,其中可见光部分约占45%,假如认为可
- 14句中划线的词语解释不当的一项是 [ ] A、停车 坐 爱枫林晚。
- 15(1²+3²+5²+……+99²)-(2²+4²+6
