氯化铯密度梯度是怎么回事?为什么在同一管溶液中还存在不同的密度区?这个“密度梯度”指的是什么?
 aeiaeidl2022-10-04 11:39:541条回答
aeiaeidl2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 exi_dirx 共回答了18个问题
exi_dirx 共回答了18个问题 |采纳率94.4%- 一般情况下一管溶液在其溶质的溶解过程中或完全溶解之后,其在溶剂中的密度分布是不同的,在溶液尚未达到完全混合的均匀状态之前,单位尺度上存在的密度的差值,即为密度梯度.可以表示为:(密度2-密度1)/(密度2的位置坐标-密度1的位置坐标)
- 1年前
相关推荐
- 已知氯化铯的摩尔质量为168.5g/mol,其分子结构如图所示,氯原子(白点)位于立方体的中心,铯原子(黑点)位于立方体
已知氯化铯的摩尔质量为168.5g/mol,其分子结构如图所示,氯原子(白点)位于立方体的中心,铯原子(黑点)位于立方体八个顶点上,这样的立方体紧密排列成氯化铯晶体。已知两个氯原子的最近距离为4×10 -10 m,则氯化铯的密度为多少? 
 hdbiao1年前1
hdbiao1年前1 -
 hang_liang 共回答了24个问题
hang_liang 共回答了24个问题 |采纳率95.8%1年前查看全部
- 通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如下图所示 下列关于这些晶体结构和性质的叙述不正确的是 [&
通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如下图所示 
下列关于这些晶体结构和性质的叙述不正确的是 [ ]A.同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构
B.一个CO 2 晶体的最小重复结构单元中含有6个CO 2 分子
C.二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键
D.在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 Honey茶香1年前1
Honey茶香1年前1 -
 kdcheng 共回答了20个问题
kdcheng 共回答了20个问题 |采纳率85%B1年前查看全部
- 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M g/m
 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M g/mol,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M g/mol,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
A.[8MNA•a3  4everPac1年前0
4everPac1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氯化钠和氯化铯熔点比较及原因,谢谢
 韵想1年前2
韵想1年前2 -
 camillezh 共回答了19个问题
camillezh 共回答了19个问题 |采纳率89.5%氯化钠由钠离子和氯离子构成.
氯化铯由铯离子和氯离子构成.
钠离子和铯离子都带1 个单位正电荷,但钠离子半径小,和氯离子距离小,根据库仑定律F=kQq/r2,钠离子和氯离子之间引力大,拆开它们更困难,需要吸收更多的能量,所以氯化钠熔沸点均高于氯化铯.1年前查看全部
- 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl - 离子核间距为a cm,氯化铯的摩尔质量为M g/mol
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl - 离子核间距为a cm,氯化铯的摩尔质量为M g/mol,N A 为阿伏加德罗常数,则氯化铯晶体的密度为()

A. 
B. 


C. 
D. 
 lostgirllvye1年前1
lostgirllvye1年前1 -
 5本红楼梦 共回答了17个问题
5本红楼梦 共回答了17个问题 |采纳率88.2%C
1年前查看全部
- 1.已知氯化铯的摩尔质量为168g/mol,其分子结构如图所示,氯原子(白点)位于立方体中心,铯原子(黑点)位于立方体八
1.已知氯化铯的摩尔质量为168g/mol,其分子结构如图所示,氯原子(白点)位于立方体中心,铯原子(黑点)位于立方体八个顶角上,这样的立方体紧密排列成氯化铯晶体.已知两个氯原子的最近距离为4×10-10m,则氯化铯的密度为多大?
2. 精神至上qq1年前1
精神至上qq1年前1 -
 czj_521 共回答了16个问题
czj_521 共回答了16个问题 |采纳率93.8%一个边长为4×10^(-10)m的立方体(晶胞)中正好含有一个CsCl分子,所以1mol这种立方体的体积就是168gCsCl的体积
V=(4×10^(-10))^3×6.02×10^23=3.85×10^(-5)立方米
密度p=16.8kg/3.85立方米=4.36×10^3kg/立方米1年前查看全部
- 氯化钠和氯化铯的化学式可用同一通式(AB型)表示,但晶体结构却不相同,
 宝蓝兔1年前1
宝蓝兔1年前1 -
 NNBBAA 共回答了24个问题
NNBBAA 共回答了24个问题 |采纳率87.5%Cs+的离子半径大,如果采用NaCl型的堆积方式,没有足够的空间给Cs+.
通式只能体现晶体结构中离子数目的比值,并不能体现其具体的空间排布.
NaCl是普通立方格子,CsCl是体心立方格子.
其本质解释是:Na+ 和Cs+的离子半径相差较大,极化能力差别也大,形成的晶体结构不同1年前查看全部
- 在氯化铯晶体中与铯离子距离最近的铯离子有几个?
 ndvb040rj44ae1年前1
ndvb040rj44ae1年前1 -
 wanqingmm 共回答了15个问题
wanqingmm 共回答了15个问题 |采纳率93.3%补充一下是6个嘿嘿1年前查看全部
- 下图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子。已知晶体中2个最近
下图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子。已知晶体中2个最近的铯离子的核间距离为acm,氯化铯的摩尔质量为Mg/mol,则氯化铯晶体的密度为  [ ]A.
[ ]A.
B.
C.
D.
 Bahamut_0031年前1
Bahamut_0031年前1 -
 Junixs 共回答了26个问题
Junixs 共回答了26个问题 |采纳率96.2%C1年前查看全部
- 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs + 离子核间距为a cm,氯化铯的摩尔质量为M,N A 为 阿伏加德罗
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs + 离子核间距为a cm,氯化铯的摩尔质量为M,N A 为 阿伏加德罗常数,则氯化铯晶体的密度为( )

A. 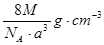
B. 
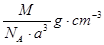
C. 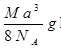
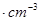
D. 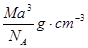
 木每三青1年前1
木每三青1年前1 -
 我不是张韶涵 共回答了11个问题
我不是张韶涵 共回答了11个问题 |采纳率81.8%B
1年前查看全部
- 下列说法中不正确的是( )A.1molSiO2晶体和1molSi晶体中所含的共价键数之比为2:1B.在氯化铯晶体中每一
下列说法中不正确的是( )
A.1molSiO2晶体和1molSi晶体中所含的共价键数之比为2:1
B.在氯化铯晶体中每一个Cs+周围与其等距离且最近的Cl-有8个
C.在氯化钠晶体中每一个Na+距离相等且最近的Cl-所围成的空间几何构型为正八面体
D.水是一种非常稳定的化合物,这是由于水分子间能形成氢键的缘故 话涝1年前1
话涝1年前1 -
 sky_naruto 共回答了17个问题
sky_naruto 共回答了17个问题 |采纳率88.2%解题思路:A.计算1molSiO2晶体和1molSi晶体中所含的共价键数判断;B.根据氯化铯晶胞结构判断;C.根据氯化钠晶胞结构判断;D.水的稳定性与化学键有关,与分子间作用力和氢键无关.A.计算SiO2晶体中Si原子与4个O原子形成共价键,即1molSiO2晶体含有4mol共价键,Si晶体中一个Si与另外4个Si原子形成共价键,每条共价键被两个原子共有,数目为4×[1/2]=2,即1molSi晶体中所含的共价键为2mol,共价键数目之比为2:1,故A正确;
B.氯化铯晶体晶胞结构为体心立方,Cs+位于体心,Cl-位于8个顶点,即每一个Cs+周围与其等距离且最近的Cl-有8个,故B正确;
C.氯化钠晶胞中Na+位于体心,与其距离最近的Cl-位于六个面的面心,构成正八面体,故C正确;
D.水的稳定性与化学键有关,与分子间作用力和氢键无关,故D错误;
故选D.点评:
本题考点: 晶胞的计算;金刚石、二氧化硅等原子晶体的结构与性质的关系.
考点点评: 本题考查晶胞结构和均摊法计算化学键,以及化学键与物质性质的关系,难度不大,对于晶胞结构要有一定的空间想象能力.1年前查看全部
- 为什么氯化铯的熔沸点小于氯化钠?
为什么氯化铯的熔沸点小于氯化钠?
离子晶体 爱情小乖乖1年前1
爱情小乖乖1年前1 -
 niuniubie 共回答了26个问题
niuniubie 共回答了26个问题 |采纳率88.5%距离远,作用力小.1年前查看全部
- 下列叙述正确的是 A.氯化铯晶体中,每一个Cs+与其他8个Cs+等距离紧邻 B.金刚石网状结构中共价键
下列叙述正确的是 A.氯化铯晶体中,每一个Cs+与其他8个Cs+等距离紧邻 B.金刚石网状结构中共价键
下列叙述正确的是
A.氯化铯晶体中,每一个Cs+与其他8个Cs+等距离紧邻
B.金刚石网状结构中共价键构成的碳原子环中,最小的环上有4个碳原子
C.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 vvvv051年前2
vvvv051年前2 -
 85年的牛仔 共回答了20个问题
85年的牛仔 共回答了20个问题 |采纳率100%B和D应该是错的.A和C里面选C吧
金刚石是C-C键,晶体硅是Si-Si键,碳化硅是C-Si键
因为C的原子半径小于Si
所以C-C键键长最短,Si-Si键键长最长,C-Si键键长介于两者之间
所以应该是金刚石>碳化硅>晶体硅1年前查看全部
- 氯化铯晶体中距离钠离子最近的有几个氯原子
 xianshi8881年前1
xianshi8881年前1 -
 艾珊珊 共回答了14个问题
艾珊珊 共回答了14个问题 |采纳率85.7%问错了.氯化铯中距离铯离子最近的氯离子有8个氯离子1年前查看全部
- 氯化铯晶体中每个铯离子吸引多少个氯离子
 dksfo1年前1
dksfo1年前1 -
 flms000 共回答了18个问题
flms000 共回答了18个问题 |采纳率83.3%8个,氯化钠中钠离子吸引6个1年前查看全部
- 为什么氯化铯晶体结构不能说成体心立方(本人看到一本无机化学上这么写,但并未作解释)
 yangshifeng1年前1
yangshifeng1年前1 -
 wanghual 共回答了19个问题
wanghual 共回答了19个问题 |采纳率100%说体心立方应该是正方体的八个顶点与体心原子相同
比如钾 它就属于体心立方
而氯化铯位于正方体八个顶点的是氯离子(或铯离子)处于正方体中心的是铯离子(或氯离子) 因此不能说它的晶体结构是体心立方
它应该是两个简单立方的结合1年前查看全部
- 氯化铯和氯化钠晶体在空间排布上的差异
 人不醉酒1年前1
人不醉酒1年前1 -
 小观众 共回答了19个问题
小观众 共回答了19个问题 |采纳率84.2%氯化铯为体心立方(氯在立方体的八个顶点上,铯在体心);氯化钠为面心立方(氯和钠在立方体的顶点、面心、体心上相间排列).1年前查看全部
- 氯化钠和氯化铯的化学式可用同一通式(AB型)表示,但晶体结构却不相同,
 vi28011年前3
vi28011年前3 -
 gayboy3477 共回答了17个问题
gayboy3477 共回答了17个问题 |采纳率88.2%半径比不同1年前查看全部
大家在问
- 1英语翻译你的手受伤了吗?怎么会这样呢?怎么不好好的照顾自己呢?
- 2go down ,go along ,go straight 有什么区别?
- 3If you don’t know how to use the word, you should _________
- 4已知{an}是等差数列,公差为d,首项a1=3,前n项和为Sn.令cn=(?1)nSn(n∈N*),{cn}的前20项和
- 5数学证明题,会的进.1.在正方形ABCD中,F为DC的中点,E为BC上的一点,且EC=1/4 BC.求证AF⊥EF2.在
- 6带如等有比喻词的成语
- 7(2013•济宁模拟)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2 是新一代饮
- 8解方程怎么做
- 9一块长方形木料长是1.2米宽是1米高是1.1米以某个面为底面把它加工成一个圆柱圆柱的体积最小是多少
- 10英语里i'mma和i'ma的全写是什么
- 11等腰直角三角形的斜边与斜边上的高和为30cm,则这个直角三角形的面积是
- 12Over the river there is ____________ bridge. A.a 110-meter-
- 13怎么用一元一次方程来解这两道运用题(求过程谢谢)题目在问题补充
- 14在某次测试中,小明、小方和小华三人的平均成绩为85分,已知小明和小方的平均成绩为88分,小明和小华的平均成绩为86分.求
- 15使一元一次方程—kx=k的解为x=—1,k要满足的条件 A,k0


