二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪
 心之木2022-10-04 11:39:541条回答
心之木2022-10-04 11:39:541条回答 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.则下列说法不正确的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.则下列说法不正确的是( )A.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl
B.S2Cl2为含有极性键和非极性键的极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2
D.S2Cl2的电子式是


已提交,审核后显示!提交回复
共1条回复
 十字改刀 共回答了19个问题
十字改刀 共回答了19个问题 |采纳率100%- 解题思路:A.S2Cl2中S元素化合价为+1价,遇水易水解,并产生能使品红褪色的气体,则可生成SO2,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S);
B.同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键多为极性键;
C.组成与结构相似,相对分子质量越大,分子间作用力越强;
D.由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对.A.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,故A正确;
B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称,正负电荷重心不重合,为极性分子,故B正确;
C.组成与结构相似,相对分子质量越大,分子间作用力越强,则熔沸点:S2Br2>S2Cl2,故C错误;
D.由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为 ,故D正确.
,故D正确.
故选C.点评:
本题考点: 不同晶体的结构微粒及微粒间作用力的区别;共价键的形成及共价键的主要类型.
考点点评: 本题以S2Cl2的结构为载体,考查分子结构、化学键、电子式、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握,是一道不错的能力考查题目. - 1年前
相关推荐
- (2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与
 (2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
(2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
A.S2Cl2的结构中各原子均达到8电子的稳定结构
B.S2Cl2为含有极性键和非极性键的共价化合物
C.若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl chenxiuying1年前1
chenxiuying1年前1 -
 misskiss520 共回答了21个问题
misskiss520 共回答了21个问题 |采纳率90.5%A.由A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为 ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;
B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,所以S2Cl2为含有极性键和非极性键的共价化合物,故B正确;
C.组成与结构相似,相对分子质量越大,分子间作用力越强,所以S2Cl2<S2Br2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,则S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl,故D正确.
故选C.1年前查看全部
- 二氯化二硫和水反应生成二氧化硫.但是二氧化硫要和二氯化二硫反应.
二氯化二硫和水反应生成二氧化硫.但是二氧化硫要和二氯化二硫反应.
2S2Cl2+2H2O=3S+SO2+4HCl
但是二氧化硫为什么不是中间产物呢. 塞外胡人1年前2
塞外胡人1年前2 -
 zhjian168 共回答了14个问题
zhjian168 共回答了14个问题 |采纳率92.9%SO2和S2Cl2是不会发生反应的.
SO2中的化合价S+4
S2Cl2中的化合价S+1
整个反应Cl的化合价没有变.只有S发生变化,从S+1到S+4,化合升高,S被氧化了,
SO2是氧化产物,就不能再做氧化济.
假如反应是这样的3S2Cl2+3H2O=3S+S2O3+6HCl 而中间的S2O3也会同HCl发生反应
最终生成 SO2
所以SO2不是间产物.1年前查看全部
- (2012•奉贤区一模)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2
(2012•奉贤区一模)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H202相似,熔点为l93K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )
A.S2C12晶体中不存在离子键
B.S2C12分子中各原子均达到8电子稳定结构
C.S2C12在熔融状态下能导电
D.S2C12与水反应后生成的气体难溶于水 舞黛纤纤1年前1
舞黛纤纤1年前1 -
 yonger1010 共回答了19个问题
yonger1010 共回答了19个问题 |采纳率100%解题思路:S2Cl2的分子结构与H2O2相似,熔点为193K,沸点为411K,熔沸点较低,则存在分子,应为共价化合物,对应晶体为分子晶体,S2Cl2的电子式为 ,根据反应物和生成物写出水解方程式,以此解答该题.
,根据反应物和生成物写出水解方程式,以此解答该题.
A.S2Cl2晶体熔沸点较低,应为分子晶体,则一定不存在离子键,故A正确;
B.S2Cl2的电子式为 ,分子中各原子均达到8电子稳定结构,故B正确;
,分子中各原子均达到8电子稳定结构,故B正确;
C.S2Cl2为分子晶体,在液态下不能电离出自由移动的离子,则不能导电,故C错误;
D.S2Cl2溶于水H2O反应产生的气体能使品红褪色,则水解方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl,水解生成的气体易溶于水,故D错误.
故选AB.点评:
本题考点: 不同晶体的结构微粒及微粒间作用力的区别.
考点点评: 本题以S2Cl2的结构为载体,考查分子结构、化学键、水解反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握.1年前查看全部
- 酸碱滴定PH值得变化和二氯化二硫的电子式
酸碱滴定PH值得变化和二氯化二硫的电子式
氢氧化钠溶液滴定盐酸溶液PH值得变化,为什么PH值得曲线涨的那么突然,就是猛地一下.你知道我意思吧.二氯化二硫的电子式是什么,两个氯原子不可以排在中间吗 STUPIDEAF1年前1
STUPIDEAF1年前1 -
 小小0808 共回答了16个问题
小小0808 共回答了16个问题 |采纳率93.8%........
:Cl:S:S:C
........
不可以
在靠近终点时,溶液的酸碱性发生突跃改变.1年前查看全部
- 二氯化二硫与水反应的方程式
 狂风暴雨和老渔翁1年前1
狂风暴雨和老渔翁1年前1 -
 胭脂与骨灰 共回答了25个问题
胭脂与骨灰 共回答了25个问题 |采纳率84%2S2CL2+2H2O=4HCL+3S+SO21年前查看全部
- 用等电子体来解决二氯化二硫的问题
用等电子体来解决二氯化二硫的问题
易得 二氯化二硫和三氯化磷是等电子体 但他们的电子式却不相同 为什么? 猜童1年前1
猜童1年前1 -
 nonolovemin 共回答了18个问题
nonolovemin 共回答了18个问题 |采纳率88.9%等电子体并不意味着电子式相同.
一般来说,解释三氯化磷使用杂化轨道理论就可以了,比较简单(sp3),四面体构型.
可以通过等电子体来推测二氯化二硫也是同样的杂化类型和空间结构.
具体是不是,我就没有考证了.
当然,从分子轨道理论角度来说,也可能拥有相同或类似的sigma、pi键和相应的反键轨道.
这个也没有考证.
如果上升到这个高度,就没有必要纠结于电子式了吧?1年前查看全部
- 二氯化二硫(S 2 Cl 2 )在工业上用于橡胶的硫化.为在实验室合成S 2 Cl 2 ,某化学研究性学习小组查阅了有关
二氯化二硫(S 2 Cl 2 )在工业上用于橡胶的硫化.为在实验室合成S 2 Cl 2 ,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S 2 Cl 2 粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:物质 熔点/℃ 沸点/℃ 化学性质 S 112.8 444.6 略 S 2 Cl 2 -77 137 遇水生成HCl、SO 2 、S;300℃以上完全分解;S 2 Cl 2 +Cl 2
2SCl 2△ . 
(1)上图中尾气处理装置不够完善,请你提出改进意见______.利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式______.
(3)C中的试剂是______.F的作用是______.
(4)如果在加热E时温度过高,对实验结果的影响是______,在F中可能出现的现象是______.
(5)为了提高S 2 Cl 2 的纯度,关键的操作是控制好温度和______. qihaitao1年前1
qihaitao1年前1 -
 浴火白凤凰 共回答了8个问题
浴火白凤凰 共回答了8个问题 |采纳率62.5%(1)①G收集产品,H中氢氧化钠溶液中水蒸气易挥发,进入G中,易使S 2 Cl 2 水解.在G和H之间增加干燥装置.
②若B中气压过大,A中浓盐酸不容易滴下,A与B之间应接一根导管,使A与B内气压相平衡,浓盐酸在重力作用下顺利滴入烧瓶.故答案为:在G和H之间增加干燥装置.
(2)用固液加热的方法制Cl 2 ,常用浓盐酸和二氧化锰反应制取,反应离子方程式为MnO 2 +4H + +2Cl -
△
.
Mn 2+ +Cl 2 ↑+2H 2 O.
故答案为:MnO 2 +4H + +2Cl -
△
.
Mn 2+ +Cl 2 ↑+2H 2 O.
(3)氯气中氯化氢用饱和食盐水吸收,用浓硫酸干燥,先除氯化氢,后干燥.故C中试剂饱和食盐水(或水).F导管较长有两个作用:导出产品和冷凝产品.导气、冷凝.
故答案为:饱和食盐水;导气、冷凝.
(4)产品热稳定性差,温度过高,产品部分生成了二氯化硫,产率偏低.根据硫的熔点和沸点知,温度过高,使部分硫变成蒸汽,而硫的熔点较低,易凝固,导致堵塞F管.
故答案为:产率降低(或S 2 Cl 2 分解);有固体产生.
(5)由信息可知,可能因温度、水蒸气因素引入HCl,S,SO 2 ,SCl 2 杂质.若滴加盐酸过快,部分水蒸气没有被硫酸吸收,导入E管中.故应控制浓盐酸的滴速不要过快.
故答案为:控制浓盐酸的滴速不要过快.1年前查看全部
- (2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与
 (2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
(2014•海南模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
A.S2Cl2的结构中各原子均达到8电子的稳定结构
B.S2Cl2为含有极性键和非极性键的共价化合物
C.若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl 4b491年前1
4b491年前1 -
 6wbpc 共回答了17个问题
6wbpc 共回答了17个问题 |采纳率94.1%解题思路:A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,写出电子式确定每个原子周围的电子数;
B、同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键为极性键;
C、组成与结构相似,相对分子质量越大,分子间作用力越强;
D、S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理.A.由A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为
 ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;
B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,所以S2Cl2为含有极性键和非极性键的共价化合物,故B正确;
C.组成与结构相似,相对分子质量越大,分子间作用力越强,所以S2Cl2<S2Br2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,则S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl,故D正确.
故选C.点评:
本题考点: 不同晶体的结构微粒及微粒间作用力的区别;极性键和非极性键.
考点点评: 本题以S2Cl2的结构为载体,考查分子结构、化学键、电子式、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握.1年前查看全部
- 二氯化二硫的疑问二氯化二硫是否是极性分子,为什么?为什么硫的化合价是+1.还有,二氯化二硫可溶于苯,怎样用相似相溶的原理
二氯化二硫的疑问
二氯化二硫是否是极性分子,为什么?为什么硫的化合价是+1.还有,二氯化二硫可溶于苯,怎样用相似相溶的原理来解释? qingshuijiu1年前1
qingshuijiu1年前1 -
 为什么战旗美如画 共回答了22个问题
为什么战旗美如画 共回答了22个问题 |采纳率95.5%是极性分子,分子结构类似H2O2.硫为sp3杂化,但3d轨道和Cl的3p轨道成共轭,二面角结构,S-S在公共棱上,两个Cl在不同的两个面上.由于正负电荷中心不重合,故为极性分子.其中,Cl电负性大,吸电子能力比S强,故呈负电性-δ,S呈正电性+δ.所以硫的化合价就显+1价.溶于苯、醚、二硫化碳等溶剂.看起来违背相似相容原理,这是可能是由于极性较小,且能发生分子间相互诱导的结果.1年前查看全部
- (2013•马鞍山一模)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2是一种
 (2013•马鞍山一模)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl下列说法中错误的是( )
(2013•马鞍山一模)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl下列说法中错误的是( )
A.S2Cl2的结构式为Cl-S-S-Cl
B.反应中SO2是还原产物,S是氧化产物
C.S2Cl2为含有极性键和非极性键的分子
D.反应中,生成1molSO2,转移电子为3mol mzlsh1年前1
mzlsh1年前1 -
 solike 共回答了19个问题
solike 共回答了19个问题 |采纳率73.7%解题思路:A.由结构可知,含有S-S键、S-Cl键;
B.根据元素的化合价升降来确定氧化产物和还原产物;
C.S-S键为非极性共价键,S-Cl键为极性共价键,该物质结构不对称;
D.根据元素的化合价升降来确定电子转移情况.A.由结构可知,含有S-S键、S-Cl键,则S2Cl2的结构式为Cl-S-S-Cl,故A正确;
B、反应中硫元素的化合价升高为二氧化硫中的+4价,所以SO2是氧化产物,硫元素的化合价降低为0价,所以S是还原产物,故B错误;
C.S-S键为非极性共价键,S-Cl键为极性共价键,该物质结构不对称,则为极性分子,即S2Cl2为含有极性键和非极性键的极性分子,故B正确;
D.在反应中,S元素发生自身氧化还原反应,生成1molSO2,转移电子为3mol,故D正确.
故选B.点评:
本题考点: 含硫物质的性质及综合应用;极性分子和非极性分子.
考点点评: 本题为信息习题,注意利用信息中物质的结构结合所学知识来解答,选项D为解答的难点,注意氧化还原反应的发生,题目难度中等.1年前查看全部
- 二氯化二硫与二溴化二硫哪个熔沸点高
 yang23141年前2
yang23141年前2 -
 zhugehang 共回答了21个问题
zhugehang 共回答了21个问题 |采纳率90.5%二溴化二硫 二者形成的都是分子晶体 熔沸点与分子间作用力有关 分子间作用力与该物质的式量有关 二溴化二硫式量大 故分子间作用力大 溶沸点高 PS:式量 =相对分子质量1年前查看全部
- (2009•肇庆一模)二氯化二硫(S2C12)在工业上用于橡胶的硫化.为了在实验室合成S2C12,某化学研究性学习小组查
(2009•肇庆一模)二氯化二硫(S2C12)在工业上用于橡胶的硫化.为了在实验室合成S2C12,某化学研究性学习小组查阅了有关资料,得到如下信息:
①在110℃~140℃时,将干燥的氯气与硫反应可得到S2C12的粗产品.
②有关物质的部分性质如下表:
设计实验室合成装置如图:物质 熔点/℃ 沸点/℃ 化学性质 S 112.8 444.6 略 S2C12 -77 137 S2C12
遇水生成HCl、SO2、S,300℃以上完全分解;
S2C12+C12
2SCl2△ .SCl2 -121 59.6(分解) 
(1)C中的试剂名称是______;仪器F的作用是______.
(2)上图中气体发生和尾气处理装置不够完善,请你提出改进意见:A装置______;G、H装置______.
利用改进后的正确装置进行实验,请回答下列问题:
(3)E中反应的化学方程式为2S+C12
S2C12△ .2S+C12.
S2C12△ .
(4)如果在加热E时温度过高,对实验结果的影响是______,在F中可能出现的现象是______.
(5)S2C12粗品中可能混有的杂质是______、______、______,为了提高S2C12的纯度,关键的操作是控制好温度和______. kfsse1年前1
kfsse1年前1 -
 头顶上的花匠 共回答了19个问题
头顶上的花匠 共回答了19个问题 |采纳率73.7%解题思路:(1)图中均是中学常见仪器,氯气制取过程中要除杂,先用饱和食盐水除去氯气中的HCl,再用浓硫酸进行干燥即可得纯净干燥的氯气,根据物质的熔沸点确定获得S2C12的方法;
(2)S2Cl2遇水生成HCl、SO2、S,在G中生成的 S2Cl2易与H中扩散过来的水蒸气反应而变质,故应在G和H之间增加干燥装置;
(3)E中反应的化学方程式由信息可得;
(4)由表中信息 S2Cl2在300℃以上完全分解考虑;
(5)根据信息,温度控制不当,则会生成SCl2,还有未反应的氯气以及蒸发出的硫.(1)氯气制取过程中的产生杂质HCl、H2O,因此先用饱和食盐水除去氯气中的HCl,再用浓硫酸进行干燥即可得纯净干燥的氯气,因为S2C12的沸点是137°C,可以采用冷凝的方法获得,故答案为:饱和食盐水;导气、冷凝;
(2)气体发生和尾气处理装置可以改进,用导管将A的上口和B相连(或将A换成恒压滴液漏斗)即可,因S2Cl2遇水生成HCl、SO2、S,在G中生成的 S2Cl2易与H中扩散过来的水蒸气反应而变质,故应在G和H之间增加干燥装置,故答案为:用导管将A的上口和B相连(或将A换成恒压滴液漏斗);在G和H之间增加干燥装置;
(3)E中反应的化学方程式由信息可得:2S+C12
△
.
S2C12,故答案为:2S+C12
△
.
S2C12;
(4)由表中信息 S2Cl2在300℃以上完全分解,所以加热E时温度过高会导致产率降低,在F中可能有硫析出,故答案为:因副反应产率降低;有固体产生;
(5)根据信息,温度控制不当,则会生成SCl2,还有未反应的氯气以及蒸发出的硫.所以关键的操作是控制好温度和氯气的气流速度要恰当,应控制浓盐的滴速不要过快.
故答案为:SCl2;Cl2;S; 控制浓盐酸的滴速不要过快.点评:
本题考点: 氯气的实验室制法;氯气的化学性质;含硫物质的性质及综合应用.
考点点评: 本题主要考查了在实验室中合成S2C12,根据题目信息分析原因,培养了学生运用知识的能力与解决问题的能力,综合性较强,难度大.1年前查看全部
- 固态二氯化二硫是分子晶体吗?
 蓝难澜1年前1
蓝难澜1年前1 -
 huang5662 共回答了27个问题
huang5662 共回答了27个问题 |采纳率81.5%是
分子间以范德华力相互结合形成的晶体.大多数非金属单质及其形成的化合物如干冰(CO2)、I2、大多数有机物,其固态均为分子晶体.分子晶体是由分子组成,可以是极性分子,也可以是非极性分子.分子间的作用力很弱,分子晶体具有较低的熔、沸点,硬度小、易挥发,许多物质在常温下呈气态或液态,例如O2、CO2是气体,乙醇、冰醋酸是液体.同类型分子的晶体,其熔、沸点随分子量的增加而升高,例如卤素单质的熔、沸点按F2、Cl2、Br2、I2顺序递增;非金属元素的氢化物,按周期系同主族由上而下熔沸点升高;有机物的同系物随碳原子数的增加,熔沸点升高.但HF、H2O、NH3、CH3CH2OH等分子间,除存在范德华力外,还有氢键的作用力,它们的熔沸点较高.
分子组成的物质,其溶解性遵守“相似相溶”原理,极性分子易溶于极性溶剂,非极性分子易溶于非极性的有机溶剂,例如NH3、HCl极易溶于水,难溶于CCl4和苯;而Br2、I2难溶于水,易溶于CCl4、苯等有机溶剂.根据此性质,可用CCl4、苯等溶剂将Br2和I2从它们的水溶液中萃取、分离出来.1年前查看全部
- (2010•巢湖模拟)二氯化二硫(S2C12)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅
(2010•巢湖模拟)二氯化二硫(S2C12)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2C12粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:物质 熔点/℃ 沸点/℃ 化学性质 S 112.8 444.6 略 S2Cl2 -77 137 遇H2O生成HCl、SO2、S;
300℃以上完全分解;
S2C12+C12
2SCl2△ .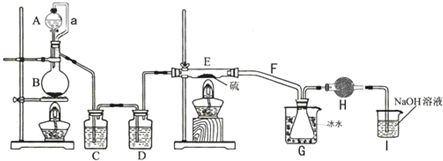
请回答下列问题:
①如何检查装置的气密性______;
②装置中导管a的作用是______;
③C、D中的试剂分别是______、______;
④F导气管管径要大一些是为了防止______;
⑤S2Cl2粗品中可能混有的杂质是(填写两种化学式)______、______;
⑥如果没有H装置产率会大大降低,原因是______;(用化学方程式表示)
⑦I中NaOH的作用是______. 心下无碍1年前1
心下无碍1年前1 -
 xwhh520 共回答了16个问题
xwhh520 共回答了16个问题 |采纳率87.5%解题思路:①气密性主要根据内外气压来检测的,瓶内的气压大于外界气压时,插到水中的导气管应该有气泡冒出;
②平衡压强;
③氯气制取过程中的除杂问题,先用饱和食盐水除去氯气中的HCl,再用浓硫酸进行干燥即可得纯净干燥的氯气;
④F长玻璃管是起到导气冷凝作用;
⑤根据信息,温度控制不当,则会生成SCl2,还有未反应的氯气以及蒸发出的硫;
⑥S2Cl2能与水反应;
⑦吸收未反应的气体.①在烧杯中加入适量的水,将导气管末端插入液面以下,用酒精灯稍稍加热烧瓶,导气管末端产生气泡,移走双手后,导气管中有一段水柱,说明气密性良好,
故答案为:在烧杯中加入适量的水,将导气管末端插入液面以下,用酒精灯稍稍加热烧瓶(或用双手捂住烧瓶),导气管末端产生气泡,移走双手后,导气管中有一段水柱;
②使分液漏斗与烧瓶气压相等,便于液体流下,故答案为:使分液漏斗与烧瓶气压相等便于滴加溶液;
③氯气制取过程中的产生杂质HCl、H2O,因此先用饱和食盐水除去氯气中的HCl,再用浓硫酸进行干燥即可得纯净干燥的氯气.所以C中为饱和食盐水,D中为浓硫酸,故答案为:饱和食盐水(或水);浓硫酸;
④F长玻璃管是起到导气冷凝作用,F导气管管径要大一些,防止S蒸气冷凝成固体S堵塞导管,故答案为:S蒸气冷凝成固体S堵塞导管;
⑤根据信息,温度控制不当,则会生成SCl2,还有未反应的氯气以及蒸发出的硫,故答案为:SCl2;C12;S任写其中两种即可;
⑥S2Cl2能与水反应,产率降低,方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl,故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl;
⑦吸收未反应的气体,防止污染环境,故答案为:吸收尾气,防止污染环境.点评:
本题考点: 制备实验方案的设计.
考点点评: 本题主要考查了在实验室中合成S2C12,根据题目信息分析原因,培养了学生运用知识的能力与解决问题的能力,综合性较强,难度大.1年前查看全部
- 已知二氯化二硫的结构式为CL-S-S-CL,它易与水反应;2S2CL2+2H2O=4HCL+SO2上箭头+3S下箭头.对
已知二氯化二硫的结构式为CL-S-S-CL,它易与水反应;2S2CL2+2H2O=4HCL+SO2上箭头+3S下箭头.对该反应的说法正确的是:AS2CL2即作氧化剂又作还原剂;BH2O作还原剂;C每生成1MOL SO2转移4MOL电子;D氧化产物与还原产物物质的量比为3:1
 mosoft1年前1
mosoft1年前1 -
 匪兵175号 共回答了22个问题
匪兵175号 共回答了22个问题 |采纳率95.5%正确答案a
二氯化二硫中硫为正一价反应后s单质0价SO2正四价,故a对b错 每生成1MOL SO2转移3MOL电子,c错 氧化产物与还原产物物质的量比为1:1d错1年前查看全部
大家在问
- 1人们饮食文化与什么有密切相关
- 2磨难加努力等于成功 作文
- 3she _(stay) in the supermark for 3 hours last sunday
- 4将溶质质量分数为7.3%的稀盐酸滴入盛有100g氢氧化钠溶液的烧杯中,恰好完全反应时消耗此稀盐酸的质量为5g,求此氢氧化
- 5意思在不同句子中的近义词这本书可有意思啦!意思的近义词这句话的意思只有我指导.意思的近义词
- 6一道小学四年级数学奥数题.在图上画一条直线,使图形分成两个三角形.
- 7平方差公式 和 完全平方公式, 是什么了 要字母的 求解 谢谢了
- 8橡胶硬度计的萧氏A和萧氏D有什么区别?
- 9“东边日出西边雨,道舟无情却有情”运用了什么修辞手法?
- 10有一含Na2S,NaSO3和Na2SO4的混合物,经测定含硫25.6∮,则此混合物中含氧质量分数是
- 11词语组词 ‘ 蛟’这个字可以组些什么词?
- 12因式分解(x+2y)2-(x+z)2
- 13一份读书小报的主题叫什么名字呢?
- 14sin61度*cos31度-sin29度*sin31度 的值
- 15There are no winners or losers in the game什么意思
