溴化钾和氯水反应后溶液什么颜色,原因是什么
 润起来2022-10-04 11:39:543条回答
润起来2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 狂舞的流沙 共回答了14个问题
狂舞的流沙 共回答了14个问题 |采纳率92.9%- 溶液呈橙黄色
CL2+2KBr==Br2+2KCL
变为了溴水
溴水呈橙黄色 - 1年前
 nnjjj 共回答了283个问题
nnjjj 共回答了283个问题 |采纳率- 2KBr+Cl2===2KCl+Br2
溴离子被氧化为单质,反应后溶液颜色是溴水的颜色,橙红色。当然也与浓度有关,红色深浅有点差别。 - 1年前
 hawkzh 共回答了92个问题
hawkzh 共回答了92个问题 |采纳率- 下层是棕色,上层无色或浅黄绿色
- 1年前
相关推荐
- 将23.6克氯化钠、溴化钾的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并高温加热,高温加热后残留物的质量为19.1
将23.6克氯化钠、溴化钾的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并高温加热,高温加热后残留物的质量为19.15克.求原混合物中Nacl的质量分数.
 tamadebi1年前1
tamadebi1年前1 -
 庙庙 共回答了16个问题
庙庙 共回答了16个问题 |采纳率93.8%溴化钾里的溴被氯置换了
减少的质量就是溴被氯换了的质量
所以有溴化钾(23.6-19.15)/(80-35.5)=0.1MOL
就是11.9G
所以氯化钠是23.6-11.9=11.7G
质量分数11.7/23.6=49.6%1年前查看全部
- 1.氯化亚铁2.碱式碳酸铜3.锰酸根4.硫酸铵5.碳酸氢铵6.氢氧化亚铁7.溴化铜8.溴化钠 9溴化钾 10.碘化钾 1
1.氯化亚铁
2.碱式碳酸铜
3.锰酸根
4.硫酸铵
5.碳酸氢铵
6.氢氧化亚铁
7.溴化铜
8.溴化钠 9溴化钾 10.碘化钾 11.熟石灰 12.氨气 13.食盐
那个``化合价也标下`三客油啦~ 帘外暮雨1年前1
帘外暮雨1年前1 -
 阿奎 共回答了18个问题
阿奎 共回答了18个问题 |采纳率94.4%FeCl2,Cu2(OH)2CO3,MnO3-,(NH4)2SO4,NH4HCO3,Fe(OH)2,CuBr2,NaBr,KBr,KI,Ca(OH)2,NH3,NaCl1年前查看全部
- 氯水与溴化钾溶液的反应;氯水与碘化钾的反应;溴水与碘化钾溶液的反应
氯水与溴化钾溶液的反应;氯水与碘化钾的反应;溴水与碘化钾溶液的反应
请分别写下实验的现象..化学方程式随便你们写不写
 若无花月美人1年前1
若无花月美人1年前1 -
 人之幸福在于心 共回答了22个问题
人之幸福在于心 共回答了22个问题 |采纳率86.4%氯水与溴化钾反应溶液变橙色(Br2)
氯水与碘化钾反应溶液变淡黄色(I2)
溴水与碘化钾反应溶液变淡黄色1年前查看全部
- 海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等.综合利用海水制备金属镁的流程如下图所示:
海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等.综合利用海水制备金属镁的流程如下图所示: 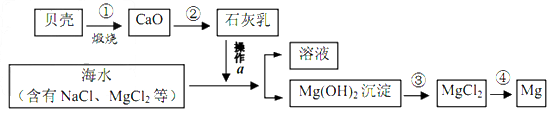
〔1〕贝壳主要成分的化学式是________ ;
〔2〕操作a的名称是_________,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、_________。
〔3〕写出第②步反应的化学方程式____________ 。
〔4〕写出第③步反应的化学方程式 ____________。 bluekate1年前1
bluekate1年前1 -
 syrain 共回答了21个问题
syrain 共回答了21个问题 |采纳率95.2%(1)CaCO 3
(2)过滤 ;漏斗
(3)CaO + H 2 O ==Ca(OH) 2
(4)Mg(OH) 2 + 2HCl==MgCl 2 + 2H 2 O1年前查看全部
- 在250g溴化钾的溶液中通入一定量干燥的氯气,待反应完全后,把溶液蒸干,剩余物经干燥后为40g,经分析知固体中含20%的
在250g溴化钾的溶液中通入一定量干燥的氯气,待反应完全后,把溶液蒸干,剩余物经干燥后为40g,经分析知固体中含20%的化合态溴.
(1)原溴化钾溶液中溶质的物质的量浓度.(溴化钾溶液密度为1.01g/cm3)
(2)在标准状况下,通入多少体积氯气可使原溶液中KBr全部氧化.
固体中含20%的化合态溴 是个什么概念.为什么又要给溴化钾溶液的密度. 181度1年前1
181度1年前1 -
 乙一秋 共回答了22个问题
乙一秋 共回答了22个问题 |采纳率100%化合态溴就是溴化钾.你只要算出蒸干后KCL和KBR物质的量就是原来KBR的物质的量.1年前查看全部
- (10肇庆市21).(8分)海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如
(10肇庆市21).(8分)海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如下图所示:
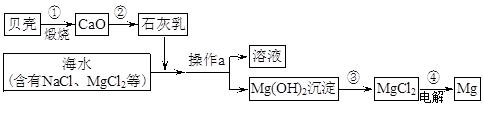
(1)贝壳主要成分的化学式是 。 (2)操作a的名称是 ,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、 。
(2)操作a的名称是 ,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、 。
(3)工业冶炼镁常用电解MgCl 2 的方法,反应为:MgCl 2 Mg+ 。
(4)写出第②、③两步反应的化学方程式:
② ,③ 。 西北望小乔1年前1
西北望小乔1年前1 -
 demontcn 共回答了14个问题
demontcn 共回答了14个问题 |采纳率85.7%(8分)
(1)(1分)CaCO 3 (2)(2分)过滤漏斗
(3)(1分)Cl 2 (4)(4分)②CaO+H 2 O=Ca(OH) 2 ③Mg(OH) 2 +2HCl=MgCl 2 +2H 2 O
本题具体考查了以下几个知识点:物质间的相互转化,过滤的原理、方法及其应用,生石灰的性质与用途,碳酸钙、生石灰、熟石灰之间的转化,正确书写化学方程式。
(1)碳酸钙以多种物质形式在自然界中存在,贝壳、蛋壳、石灰石等主要成分都是碳酸钙;
(2)过滤是分离固液混合物的常用的操作方法,该操作后可得到溶液和固体;再根据操作需要,可判断完成该操作需要的玻璃仪器是漏斗;
(3)根据质量守恒定律及化学方程式书写要求,可知电解氯化镁的生成物并写成反应的化学方程式;
(4)石灰乳主要成分为氢氧化钙,反应②即为氧化钙与水生成氢氧化钙的反应;根据碱类物质的性质及变化规律,可判断反应③为氢氧化镁与盐酸的反应。1年前查看全部
- 测试红外光谱时,样品容器一般常用氯化钠和溴化钾,它们适用的波数范围各为多少?
 一叶障目的人1年前1
一叶障目的人1年前1 -
 蚯蚓78 共回答了22个问题
蚯蚓78 共回答了22个问题 |采纳率81.8%测试红外光谱时使用氯化钠和溴化钾作为基底的原因是因为它们在中红外光谱区域(400 4000 cm^-1)范围内基本不吸收,不影响样品光谱吸收峰的形状和大小.1年前查看全部
- 写出下列物质的化学式:溴化钾______ 氧化镁______氧化铁______
写出下列物质的化学式:
溴化钾______氧化镁______
氧化铁______二氧化硫______
碘化钾______硫化锌______
氯化铵______碳酸钠______
氢氧化钙______ 硝酸银______
硫酸镁______氯酸钾______. zjw98191年前1
zjw98191年前1 -
 爱上你是我的决定 共回答了18个问题
爱上你是我的决定 共回答了18个问题 |采纳率100%解题思路:化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.溴化钾中钾元素显+1价,溴元素显-1价,其化学式为KBr.氧化镁中镁元素显+2价,氧元素显-2价,其化学式为MgO.氧化铁中铁元素显+3价,氧元素显-2价,其化学式为Fe2O3.二氧化硫的化学式为SO2.碘化钾中钾元素显+1价,...
点评:
本题考点: 化学式的书写及意义.
考点点评: 本题难度不大,掌握化合物化学式的书写一般规律(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.1年前查看全部
- 将10.000 g氯化钠、溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并灼烧(高温加热),灼烧后残留
将10.000 g氯化钠、溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并灼烧(高温加热),灼烧后残留物的质量为9.813 g.若将此残留物再溶于水并加入足量的碳酸钠溶液,所得的沉淀经干燥后质量为0.721 g.求原混合物中各化合物质量.
 随风一叶1年前1
随风一叶1年前1 -
 达华2004 共回答了22个问题
达华2004 共回答了22个问题 |采纳率86.4%氯化钠8.700g,溴化钾为:0.500g,氯化钙为:0.800g.
设混合物中各物质的质量:NaCl为 x g,KBr为 y g,CaCl 2 为 z g
x + y + z =10.000 g①
2KBr+Cl 2 ====2KCl+Br 2
混合物中KBr转化为KCl,灼烧后溴全部挥发,因此:
x +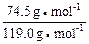 y + z =9.813 g②
y + z =9.813 g②
①式-②式得:(1-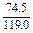 ) y =10.000-9.813
) y =10.000-9.813
解得 y =0.500 g
残留物溶于水后加入足量碳酸钠溶液,发生如下反应:
CaCl 2 +Na 2 CO 3 ====CaCO 3 ↓+2NaCl
从所得CaCO 3 的质量可以算出CaCl 2 的质量:
z =0.721 g× =0.800 g
=0.800 g
氯化钠的质量为: x =10.000-0.500 g-0.800g=8.700g1年前查看全部
- [急.]卤素单质的实验现象.1.氯水和溴化钾的反应.2.氯水和碘化钾的反应.3.溴水和碘化钾的反应.请看清题.
 130310720011年前1
130310720011年前1 -
 mm小虫 共回答了15个问题
mm小虫 共回答了15个问题 |采纳率93.3%这个就是看你平时基础扎不扎实了.氯水什么颜色来着?黄绿色?
第一个现象中,会产生溴单质,溴水是橙色,所以溶液会变橙色.
同理,第二个反应会产生碘单质,碘溶于水中是浅黄色.
第三个反应会发生橙色变为浅黄色的现象.
有一种帮别人做作业的感觉.1年前查看全部
- 将10克的氯化钠,溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后将溶液蒸干并灼烧,灼烧后残留物的质量为9.813
将10克的氯化钠,溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后将溶液蒸干并灼烧,灼烧后残留物的质量为9.813克,若将此残留物再溶于水,并加入足量的碳酸钠溶液,所得沉淀经干燥后质量为0.721克,求原混合物中各化合物的质量分数
 8b6p1年前1
8b6p1年前1 -
 fyyswj74 共回答了29个问题
fyyswj74 共回答了29个问题 |采纳率82.8%氯化钠,溴化钾和氯化钙中,只有KBr与氯气反应.生成的溴被灼烧挥发.固体减少的质量为Br被Cl取代造成的.
2KBr + Cl2 = 2KCl + Br2(l)
KBr ----- Br - Cl
119 80 - 35.5 = 44.5
x 10-9.813 = 0.187
x = 0.500 g
CaCl2 + Na2CO3 = CaCO3(s) + 2NaCl
111.0 100.1
y 0.721
y = 0.800 g
NaCl质量:10 - 0.800 -0.500 = 8.700 g,质量分数:8.700/10 = 87.00%
CaCl2质量分数:0.800/10 = 8.00%
溴化钾质量分数:0.500/10 = 5.00%1年前查看全部
- 1.20摄氏度时溴化钾的溶解度是65.9克,求20摄氏度时120克水中可以溶解多少克溴化钾才能达到饱和?
1.20摄氏度时溴化钾的溶解度是65.9克,求20摄氏度时120克水中可以溶解多少克溴化钾才能达到饱和?
2.计算在20摄氏度时,1000克食盐饱和溶液中含氯化钠多少克?(已知20摄氏度时食盐的溶解度是36克)
3.已知硝酸钾70摄氏度时的溶解度是140克,9摄氏度时为20克,将70摄氏度的硝酸钾饱和溶液200克降低到9摄氏度时,析出硝酸钾晶体多少克? qq30870170201年前1
qq30870170201年前1 -
 清流枫 共回答了14个问题
清流枫 共回答了14个问题 |采纳率92.9%1.100 :65.9=120 :X
X=79.08 克
2.(100+36):36=1000:X
X =264.7 克
3.100:140 =200:x
x = 280 克
100:20 =200:y
y= 40 克
析出硝酸钾晶体:280-40=220 克1年前查看全部
- 溴化钾与氯水的反应方程式
 KAIPEI5211年前1
KAIPEI5211年前1 -
 gch1121 共回答了21个问题
gch1121 共回答了21个问题 |采纳率90.5%左右观之,前面的答案都不很正确…氯水是氯气溶于水的物质…是氯化氢和次氯化氢的混合溶液…氯水和溴化钾反应的实质是次氯化氢和溴化钾反应…剩下的有楼主自己完成1年前查看全部
- 碘化锂,氟化锂,氯化钠,溴化钾中,哪一个阳离子和阴离子半径之比最小,为什么?
 vigi_ou1年前1
vigi_ou1年前1 -
 noeastpig 共回答了17个问题
noeastpig 共回答了17个问题 |采纳率88.2%碘化锂
阳离子中锂离子半斤最小
阴离子中碘离子半径最大1年前查看全部
- 溴化钾 碘量法测定苯酚的浓度了.
 6ds5h46v1年前1
6ds5h46v1年前1 -
 时间的赌徒 共回答了19个问题
时间的赌徒 共回答了19个问题 |采纳率94.7%如果我没记错的话,定量KBr与过量KBrO3反应,先生成过量Br2(相对苯酚来说).然后通过生成的溴单质与苯酚取代,然后,剩余的溴单质氧化KI,生成I2,再用硫代硫酸钠滴定I2,可知剩余的Br2.然后,通过KBr相当量关系,求出生成Br2的量,减去剩余的Br2,就是与苯酚反应的Br2.
现象是,
生成溴,就是水相变红色.
三溴苯酚沉淀,白色
剩余溴水与KI反应,水相紫色
用硫代硫酸钠滴定,至水相无色
然后通过,
5Br(-)—>3Br2—>苯酚
Br2—>I2—>2Na2S2O3
可求解两处分别的Br2,通过此,就可以求出苯酚的浓度1年前查看全部
- 2 ml溴化钾溶液加入1ml 四氯化碳再通入氯气,求实验现象
 辛易达1年前2
辛易达1年前2 -
 zheng571337 共回答了20个问题
zheng571337 共回答了20个问题 |采纳率95%溴化钾溶液加入 四氯化碳后分层,通入氯气后震荡,下层呈橙红色,上层无色!
这是因为氯气与溴化钾反应,置换出溴单质,震荡后,由于溴单质在四氯化碳中的溶解度大于水中溶解度,溴单质进入下层的四氯化碳导致下层呈橙红色.1年前查看全部
- 向溴酸钾中滴加少量的溴化钾的硫酸溶液后,所得产物除水后还有什么?
 74875221年前1
74875221年前1 -
 zouzhi0312 共回答了11个问题
zouzhi0312 共回答了11个问题 |采纳率90.9%BrO3- + 5Br- + 6H+ == 3Br2 + 3H2O
K+和SO4 2-结合生成K2SO4
因为溴化钾少量,所以所得产物除水后还有溴酸钾和溴单质和硫酸钾.1年前查看全部
- 在溴化钾和碘化钾的混合溶液中通入过量氯气,把溶液蒸干后并将剩余物灼烧,最后残余的物质是
在溴化钾和碘化钾的混合溶液中通入过量氯气,把溶液蒸干后并将剩余物灼烧,最后残余的物质是
A.氯化钾B.氯化钾和碘C.氯化钾和溴D.氯化钾和溴化钾 菜刀门下1年前1
菜刀门下1年前1 -
 住在外星球 共回答了14个问题
住在外星球 共回答了14个问题 |采纳率85.7%应该是A吧.
足量氯气把碘和溴都置换出来,生成氯化钾了.1年前查看全部
- 氯化铁与溴化钾反应式怎么写?求高手指导,
氯化铁与溴化钾反应式怎么写?求高手指导,
我们做实验,FeCl3+KBr+CCl4,现象是分层,上层是浅绿,下层无色,咋回事? syg08551年前2
syg08551年前2 -
 gyx071126 共回答了18个问题
gyx071126 共回答了18个问题 |采纳率88.9%他俩不反应吧
单质溴可以氧化二价铁离子 所以不能反应1年前查看全部
- 间接碘量法测定苯酚含量实验中,配制溴酸钾-溴化钾标准溶液,称取溴化钾是否应过量,为什么?
 韻韻_o1年前1
韻韻_o1年前1 -
 julycom 共回答了16个问题
julycom 共回答了16个问题 |采纳率100%应该溴化钾过量.不然苯酚溴代之后产生HBr,又生成Br2.1年前查看全部
- 下列化合物中阳离子与阴离子半径比值最大的是 A 氟化钙 B 碘化镁 C 氯化钙 D 溴化钾
 busybusybee1年前3
busybusybee1年前3 -
 踏弩 共回答了19个问题
踏弩 共回答了19个问题 |采纳率84.2%B,碘离子半径大1年前查看全部
- 检验溴化钾中是否含有碘负离子的实验
 腹黑猫猫1年前1
腹黑猫猫1年前1 -
 一成不变 共回答了22个问题
一成不变 共回答了22个问题 |采纳率77.3%滴加溴水,再加淀粉溶液,变蓝证明有碘负离子.
2I-+Br2=2Br-+I2
I2遇淀粉变蓝.1年前查看全部
- 氯化钾中含有硫酸钾和溴化钾杂质,要去除这2个杂质要什么?
氯化钾中含有硫酸钾和溴化钾杂质,要去除这2个杂质要什么?
硫酸钾是用氯化钡吗? tianmeng10001年前1
tianmeng10001年前1 -
 竹林风雨 共回答了23个问题
竹林风雨 共回答了23个问题 |采纳率87%加氯化钡去除硫酸;通入氯气去除溴化钾;然后过滤.1年前查看全部
- 氯气通入溴化钾方程式
 jcw0012121年前2
jcw0012121年前2 -
 1banren 共回答了18个问题
1banren 共回答了18个问题 |采纳率77.8%2KBr+Cl2=2KCl+Br21年前查看全部
- 将250g的溴化钾溶液中通入一定量干燥氯气,等反应完全后,吧溶液蒸干,剩余物经干燥质量为40g,经分析知,
将250g的溴化钾溶液中通入一定量干燥氯气,等反应完全后,吧溶液蒸干,剩余物经干燥质量为40g,经分析知,
固体中含20%的化合态溴,求:
(1)原溴化钾溶液中溶质的质量分数;
(2)通入多少克氯气可使原溶液中的KBr全部氧化? dubang1年前1
dubang1年前1 -
 jiduo2000 共回答了20个问题
jiduo2000 共回答了20个问题 |采纳率90%(1)依题意可知发生的反应如下:2KBr+Cl2=2KCl+Br2,因为溴易挥发,所以蒸干溶液后剩余物位KBr和KCl的混合物;又因为化合态的溴的质量分数为20%,
所以化合态溴元素的质量为40g×20%=8g;
根据溴元素守恒可得:KBr Br-
119 80
m(KBr) 8g
119/80= m(KBr)/8g ;解得:m(KBr)=11.9g;
所以混合物中氯化钾的质量为m(KCl)=40g- m(KBr)=28.1g;
2KBr + Cl2 = 2KCl + Br2
238 149
m'(KBr) 28.1g
238/149=m'(KBr)/28.1g,所以反应的溴化钾的质量为 m'(KBr)=44.88g;
所以原溶液中溴化钾的质量为m(KBr)+m'(KBr)=56.78g;
所以原溴化钾溶液中溶质的质量分数为56.78g/250g=22.7%;
(2) 2KBr + Cl2 = 2KCl + Br2
238 71
56.78g m(Cl2)
238/71=56.78g/m(Cl2);所以:m(Cl2)=16.94g;
答:原溴化钾溶液中溶质的质量分数22.7%;通入16.94g氯气可使原溶液中的KBr全部氧化.
如果还有什么不明白的地方可以问我,很高兴为你解答.1年前查看全部
- 将一定量的氯气通入100mL溴化钾溶液中,再将所得溶液蒸干,得到16g干燥的固体物质.经测定该固体物质中含有溴离子,其质
将一定量的氯气通入100mL溴化钾溶液中,再将所得溶液蒸干,得到16g干燥的固体物质.经测定该固体物质中含有溴离子,其质量分数为25%.则:
(1)反应中通入氯气的体积(按STP)为多少L?
(2)反应前溴化钾溶液的物质的量浓度. tangmu20031年前1
tangmu20031年前1 -
 白色牛奶树 共回答了13个问题
白色牛奶树 共回答了13个问题 |采纳率100%溴元素质量为:16g×25% = 4g
KBr的质量为:4g/80×119 = 5.95g,物质的量为:0.05mol
KCl的质量为:16g-5.95g = 10.05g,物质的量为:0.135mol
Cl2+2KBr==2KCl+Br2
1 2 2
0.135
所以n(Cl2)=0.135/2=0.0675mol V=0.0675mol*22.4L/mol=1.512L
所以溴化钾总物质的量为:0.05mol+0.135mol = 0.185mol1年前查看全部
- 溴化钾和溴酸钾在酸性溶液中发生归中反应,溴元素全部变为溴单质的反应方程式是什么?
 zzfrent1年前2
zzfrent1年前2 -
 a310054903 共回答了22个问题
a310054903 共回答了22个问题 |采纳率90.9%5KBr+KBrO3+3H2SO4===3Br2+3H2O+3K2SO41年前查看全部
- 溴酸钾和溴化钾在硫酸中反应
 65343171年前1
65343171年前1 -
 22446745 共回答了19个问题
22446745 共回答了19个问题 |采纳率94.7%KBrO3+5KBr+3H2SO4=3Br2+3H2O+3K2SO41年前查看全部
- 在盛有少量氯水的试管中加入过量的溴化钾溶液,再加入少量四氯化碳,振荡静置后可观察到的现象是 a溶...
在盛有少量氯水的试管中加入过量的溴化钾溶液,再加入少量四氯化碳,振荡静置后可观察到的现象是 a溶...
在盛有少量氯水的试管中加入过量的溴化钾溶液,再加入少量四氯化碳,振荡静置后可观察到的现象是
a溶液呈橙色不分层
b溶液分两层,上层呈橙色
c溶液分两层,下层呈橙色
d溶液呈紫色不分层 yiyayiziyao1年前2
yiyayiziyao1年前2 -
 藤我的责任 共回答了19个问题
藤我的责任 共回答了19个问题 |采纳率89.5%c溶液分两层,下层呈橙色
Cl2+2KBr===2KCl+Br2
Br2水和CCl4萃取,Br2易溶于CCl4,CCl4密度大,在下层1年前查看全部
- 溴酸钾和溴化钾在酸性溶液中反应,溴元素完全转化成单质溴,试写出反应的离子方程试_____________________
溴酸钾和溴化钾在酸性溶液中反应,溴元素完全转化成单质溴,试写出反应的离子方程试__________________________________________该反应中的___________mol溴酸钾中含有mg溴元素,它能________(氧化,还原)____mol的_______
 但愿海波平1年前1
但愿海波平1年前1 -
 物权王子 共回答了17个问题
物权王子 共回答了17个问题 |采纳率88.2%BrO3- + 5Br- + 6H+ = 3Br2 + 3H2O;1mol;80000 mg;氧化;5mol;溴化钾1年前查看全部
- 氯气通入溴化钾的CCl4溶液氯气通入碘化钾的CCl4溶液溴气通入碘化钾的CCl4溶液
 爱我你醉了么1年前2
爱我你醉了么1年前2 -
 einsnian 共回答了18个问题
einsnian 共回答了18个问题 |采纳率100%Cl2+2KBr===2KCl+Br2
2KI+Cl2=I2+2KCl
2KI+Br2==2KBr+I21年前查看全部
- 氯气与溴化钾的反应方程式
 五里一徘徊1年前1
五里一徘徊1年前1 -
 superhfzy 共回答了27个问题
superhfzy 共回答了27个问题 |采纳率81.5%CL2+2KBr=2KCL+Br21年前查看全部
- 除去液溴中溶解的少量氯气,为什么不能用溴化钾固体,在过滤呢
 dorothylilac1年前1
dorothylilac1年前1 -
 weiwei_nwpu 共回答了29个问题
weiwei_nwpu 共回答了29个问题 |采纳率96.6%因为氯气与溴化钾的反应是 在水溶液中进行的饿,应该用溴化钾溶液,再萃取.不是过滤.1年前查看全部
- 氯化钾和溴化钾的混合物3.87克,溶于岁水并加入过量的硝酸银溶液后,产生6.63克沉淀,则混合物中含钾______
氯化钾和溴化钾的混合物3.87克,溶于岁水并加入过量的硝酸银溶液后,产生6.63克沉淀,则混合物中含钾______
A.24.1% B.40.3% C.25.9% D.48.7% krose191年前2
krose191年前2 -
 丹尼尔迷 共回答了19个问题
丹尼尔迷 共回答了19个问题 |采纳率84.2%选B啊!
KCl+AgNO3==AgCl(沉淀)+KNO3
KBr+AgNO3==AgBr(沉淀)+KNO3
你设KCL有Xg,把AgCl的质量算一下,得到的是带X的代数式
然后KBr有(3.87-X)g,可以把AgBr的质量算出来.
AgCl的质量+AgBr的质量=6.63!
这样,X就出来了,等于1.49克.
K-KCL
39:74.5=K的质量:1.49
K-KBr
39:119=K的质量:(3.87-1.49)
最后把2个K的质量+在一起,除以混合物的总质量,就得到了答案!
选B!1年前查看全部
- 氯气加入碘化钾和溴化钾,是先和碘化钾反应还是一起反应?
 杨紫1年前3
杨紫1年前3 -
 lins8501 共回答了20个问题
lins8501 共回答了20个问题 |采纳率90%先和碘化钾.因为即使先和溴化钾反应,生成的溴也会跟碘化钾反应.根据吉普斯自由能判断结果也是一样1年前查看全部
- 有四瓶失去标签的无色溶液,它们是氯水、氯化钠、硝酸银和溴化钾溶液.把四种溶液标上A、B、C、D记号,进行实验,观察到的现
有四瓶失去标签的无色溶液,它们是氯水、氯化钠、硝酸银和溴化钾溶液.把四种溶液标上A、B、C、D记号,进行实验,观察到的现象是:
1.把A和B混合,有淡黄色沉淀生成
2.把A和C混合,有白色沉淀生成
3.把B和D混合,溶液变成深黄色
推断A、B、C、D各是什么溶液,写出有关反应的化学方程式 凌凌青-灵灵蓝1年前6
凌凌青-灵灵蓝1年前6 -
 smilejia 共回答了18个问题
smilejia 共回答了18个问题 |采纳率88.9%A、B混合有淡黄色沉淀生成,对这四种溶液而言只可能是AgBr沉淀
A、C混合有白色沉淀生成 ,可能为AgCl
所以A是有银离子的溶液,硝酸银
B是有溴离子的溶液,溴化钾
C是有氯离子的溶液,氯水或氯化钠
看3,B和D混合,溶液变成深黄色 ,说明生成了溴,所以D是氯水
那么C就是氯化钠
A:硝酸银;B:溴化钾;C:氯化钠;D:氯水
1:AgNO3+KBr=AgBr+KNO3
2:AgNO3+NaCl=AgCl+NaNO3
3:2KBr+Cl2=2KCl+Br21年前查看全部
- 必修一化学三个方程式氯水与溴化钾的反应,氯水与碘化钾的反应,溴水和碘化钾的反应3q~
 jamp1年前2
jamp1年前2 -
 ww1217 共回答了12个问题
ww1217 共回答了12个问题 |采纳率91.7%cl2 + 2kbr =br2 + 2kcl
cl2 + 2kI = I2 + 2kcl
br2 + 2kI = I2 + 2k1年前查看全部
- 红外光谱中使用高温台>1000度应注意什么?高温台窗片的选择:因氟化钡、溴化钾
 sisselmm1年前1
sisselmm1年前1 -
 liupenghn 共回答了13个问题
liupenghn 共回答了13个问题 |采纳率92.3%使用耐高温的Al2O3-SiO2-MgO-CaO的玻璃应该是可以的.1年前查看全部
- 下列物质中,有极性共价键的是A、单质碘 B、氯化镁 C、溴化钾 D、水求解释·
 yeerfei5201年前2
yeerfei5201年前2 -
 ganfangbao 共回答了21个问题
ganfangbao 共回答了21个问题 |采纳率90.5%A、单质碘
I-I 非极性共价键
B、氯化镁
MgCl2 离子键
C、溴化钾
KBr 离子键
D、水
H-OH 极性共价键
选D
祝你新春快乐1年前查看全部
- 银离子与钾离子半径相近,但溴化钾易溶于水,溴化银却不能
 3232k1年前1
3232k1年前1 -
 jan_1888 共回答了18个问题
jan_1888 共回答了18个问题 |采纳率100%离子的化学特性主要与元素的最外层电子有关,离子半径不是主要影响因素.比如锂(Li)钠(Na)钾(K)铷(Rb)铯(Cs)钫(Fr),他们都是第一主族元素,原子最外层电子数均为1,化学性质都相似.1年前查看全部
- 溴化钾饱和溴水溶液在做一个实验的过程中,出现这样的现象:300g溴化钾加入到1000g水中,然后再继续加液溴,加到一定量
溴化钾饱和溴水溶液
在做一个实验的过程中,出现这样的现象:
300g溴化钾加入到1000g水中,然后再继续加液溴,加到一定量,会有溴化钾析出.
请问下为什么会出现这样的现象. tianbing951年前2
tianbing951年前2 -
 朔北苍狼 共回答了19个问题
朔北苍狼 共回答了19个问题 |采纳率84.2%液溴溶于水形成溴水,使得溴离子浓度不断增大,当达到饱和之后,溴化钾析出1年前查看全部
- 溴化钾和氯水反应会有什么现象
 jgqww07231年前1
jgqww07231年前1 -
 pierrewu 共回答了17个问题
pierrewu 共回答了17个问题 |采纳率94.1%溴化钾中的溴离子会被氯水中的氯置换出来.现象是溶液由淡黄绿色变黄色(水溶液中)或棕色(四氯化碳中)1年前查看全部
- 求溴化钾和高锰酸钾和硫酸的反应方程式……
求溴化钾和高锰酸钾和硫酸的反应方程式……
还有如果把硫酸换成醋酸该咋写…
谢谢喽
再问个:高锰酸钾在酸性,中性,碱性条件下分别是咋反应了…
真的谢谢,嘿嘿 穿上猪皮1年前4
穿上猪皮1年前4 -
 亚安 共回答了25个问题
亚安 共回答了25个问题 |采纳率96%10KBr + 2KMnO4 + 8H2SO4 = 6K2SO4 + 2MnSO4 + 5Br2 + 8H2O
至于醋酸,我认为醋酸不被高锰酸钾氧化,只提供酸性环境
10KBr + 2KMnO4 + 16CH3COOH = 12CH3COOK + 2(CH3COO)2Mn + 5Br2 + 8H2O
酸性条件下高锰酸钾氧化性最强,中性其次,碱性最弱.在酸性条件下,高锰酸钾被还原为两价的肉色锰离子;中性和弱碱性条件下还原成黑色的二氧化锰沉淀;pH〉13后被还原成六价的绿色锰酸根离子.1年前查看全部
- 溴化钠,溴化钾,溴酸钠,氢溴酸分别属于几级危险品
 josephine02111年前1
josephine02111年前1 -
 魂没 共回答了17个问题
魂没 共回答了17个问题 |采纳率82.4%溴化钠,溴化钾,溴酸钠属于危险品的第六等级,是有毒物质;氢溴酸属于危险品的第八等级,是腐蚀品.1年前查看全部
- 将一定量的氯气同入50mL溴化钾溶液中,然后将所的的溶液蒸干,并将残渣略微灼烧,干燥残渣的质量等于40.0g.分析残渣,
将一定量的氯气同入50mL溴化钾溶液中,然后将所的的溶液蒸干,并将残渣略微灼烧,干燥残渣的质量等于40.0g.分析残渣,其中含有25%的化合态溴,试 计算:
(1)同如的氯气的体积(标准状况)
(2)原溴化钾溶液的物质的量浓度. lovehomeland1年前2
lovehomeland1年前2 -
 boopoo 共回答了18个问题
boopoo 共回答了18个问题 |采纳率100%我就省略设了
br=80 cl=35.5 k=39
首先分析题意,最后残渣中还剩下化合态的溴,说明反应的kBr是没有完全反应,而氯气反应完全
1,根据40g残渣中化合态溴的含量,可以算出没有参加反应的溴
kBr----------------Br
119 80
--------- = -----------(对应项成比例)
为参加反应的(a) 40*25%
a=14.875g
同理可以算出来残渣剩余部分也就是生成的kcl的质量
40-14.875=25.125g
有这两步就非常好算了吧
2kBr + cl2 = 2kcl + br2
2 44.8l/mol 149
y x 14.875
这样就算出来了x=4.47L
y=0.2mol
总共的kBr是参加反应的和剩余的总和 14.875/119+0.2=0.325mol
o.325mol .05L=6.5moll
答:氯气的体积为4.47L,原溶液的物质的量浓度为6.5moll1年前查看全部
- 将氯化钾溶液和溴化钾溶液混合,其中有溶质13.4g,溶液体积为500mL,通入氯气充分反应后,将溶液蒸干,得固体物11.
将氯化钾溶液和溴化钾溶液混合,其中有溶质13.4g,溶液体积为500mL,通入氯气充分反应后,将溶液蒸干,得固体物11.75g.则原溶液中K,Cl,Br,物质的量之比为
 沧海落雪1年前1
沧海落雪1年前1 -
 seeddd 共回答了17个问题
seeddd 共回答了17个问题 |采纳率100%3:2:1
2KBr+Cl2=Br2+2KCl
,蒸干后,Br2跑掉
由差量法,加入71gCl2可以跑掉160gBr2,差量为89g,实际差量为1.65g,可设KBr物质的量为xmol
∴2/x=89/1.65,解出x即原溶液中Br的物质的量,剩下的就很简单了.
这道题主要分析差量与平衡.
高中这一类题的解法:1.找差量及对应量; 2.找守恒; 3.找摩尔关系
本人也是高一的,在绵阳东辰,昨儿老师才讲了这一道题的1年前查看全部
- 在做重氮化分析时,用NaNO2和HCL与氨基进行重氮反应,而分析条件中要求加入溴化钾溶液或溴化钾,且不同的样品要求加入溴
在做重氮化分析时,用NaNO2和HCL与氨基进行重氮反应,而分析条件中要求加入溴化钾溶液或溴化钾,且不同的样品要求加入溴化钾的量也不同,请问溴化钾在重氮化反应中起什么作用?为何用量又大不相同?
 大灰狼东东1年前1
大灰狼东东1年前1 -
 qiuqingxu 共回答了17个问题
qiuqingxu 共回答了17个问题 |采纳率88.2%主要是防止NaNO2(氧化剂,有强氧化性)的过量,一旦NaNO2过量将会对反应产生不利影响,为减少这种副反应根据对合成参数(收率,产量,温度,原料的质量的多少)的要求会加入适量的KBr(有还原性,作还原剂)NO2-+Br-+H+----N2+Br2(BrO3-)+H2O1年前查看全部
- 溴化钾与碘化钾分别与三氯化铁如何反映
 娃哈哈v9we1年前1
娃哈哈v9we1年前1 -
 笨笨的zz基尼 共回答了24个问题
笨笨的zz基尼 共回答了24个问题 |采纳率91.7%溴化钾不和三价铁反应
碘化钾可以,一般认为是:
2KI+2FeCl3=I2+2FeCl2+2KCl1年前查看全部
- 银氨配离子配位数实验中溴化钾可换成氯化钾或碘化钾吗?为什么?
 FBI3216541年前1
FBI3216541年前1 -
 tonny041111 共回答了13个问题
tonny041111 共回答了13个问题 |采纳率76.9%一般来说不行.原因:1、本实验是利用二个平衡:二个平衡同时存在:Ag+ + nNH3 = [Ag(NH3)n]+Ag+ + Br- = AgBr体系中[Ag+]必须同时满足二个平衡,二个平衡同时存在是本实验的前提.2、不能用Cl-代替Br- ,因为AgCl的溶解...1年前查看全部
大家在问
- 1(2011•淮安)七(1)班的大课间活动丰富多彩,小峰与小月进行跳绳比赛.在相同的时间内,小峰跳了100个,小月跳了14
- 2一根电线剪成三段,第一段占全长的25%,正好是4.5米,第二、三段的长度的比是7:8,求第二、三段长度各是多少?
- 3英语问题:根据情景填上恰当的词语使对话完整.
- 43×(2/15+1/12)-2/5,能简算吗
- 5制作黄鳝的配合饲料请问饲料中:蚯蚓(鲜)30%(蚯蚓的蛋白质含量约占53.5%~65.1%) 猪肺20%(100克含蛋白
- 6自相矛盾扩写500字
- 7把一外表不规则的实心小塑料块(该塑料块不溶于酒精和水)先后放入盛有足够水和做够多的酒精的两个容器中.该塑料块所受到的浮力
- 8交通部公路科学研究院和交通运输部科学研究院有区别吗?
- 9(2012•怀化)下列化学符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是( )
- 10帮助老人们做一些力所能及的事 英语
- 11____to reach them on the phone,we sent an email instead. A.F
- 12作文[这就是真实的我]200字以上
- 13一个最简分数,分数单位是四分之一,如果改写成以十二分之一做分数单位,则分数单位的个数比原来增加六个
- 14人教版六年级上册语文第八单元作文(写学小号的)
- 15聪聪要用自己的零花钱买一辆山地自行车,价格是580元,近两年他已经存了450元零花钱以后每个月还想存25元.
