(2014届上海市松江区第一学期期末试题)互为同素异形体的一组物质是 A.氧气和液氧 B.金刚石和石墨 C.一氧化碳和二
 随心的风2022-10-04 11:39:541条回答
随心的风2022-10-04 11:39:541条回答| (2014届上海市松江区第一学期期末试题)互为同素异形体的一组物质是
|

已提交,审核后显示!提交回复
共1条回复
 有有成功 共回答了23个问题
有有成功 共回答了23个问题 |采纳率95.7%- B
- 1年前
相关推荐
- 眉山市高2014届第一学期期末教学质量检测
 风弛人生1年前1
风弛人生1年前1 -
 五彩尽逝迦楼罗 共回答了25个问题
五彩尽逝迦楼罗 共回答了25个问题 |采纳率92%多项选择题(共25小,每小题2分,共50分)
问题1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案DCBBDCDBDBAAB
>问题14 15 16 17 18 19 20 21 22 23 24 25
答案CCBAABBCBDBA
二,非多项选择题(共四个小问题,共50分)
BR /> 26(11分)(1)(1)活跃的地壳运动,断裂构造?发育;②压裂松动;③地形,大坡,陡坡深谷;④夏季降水和暴雨(A 1点1分钟以上回答说,在3:00分)
(2)B地,是一个合理的判断对方的回答共4分内陆,气候干燥,降水稀少(2)
(3)人口迅速增长和经济的集约发展,促进人口分布集中,大规模的人类工程活动和自然环境的严重破坏,使地质灾害和灾害强度的频率不断增加.(2)
(4)只要听到碎屑流和泥石流发出报警的声音,双方快速逃离山区的河流垂直,(2),直到它来到相对安全的高度(1点).(3分)
27(14分)(1)北半球夏季(五月至十月).(1)在这种频繁的飓风和雨季,河流径流量大.(2)
(2)地势低平,河流众多,海岸是钟形,密集的城市,人口众多.(曾任1:00 1 A,共3分)的危险
(3):(1)损坏堤防工程设施(沿海海堤,海岸工程,道路及海堤会造成严重的伤害);造成2点伤害(由水引起的风暴潮将淹没码头,仓库和其他工业和农业生产活动对沿海和近海,导致工厂瘫痪,严重的会导致海上油田关闭,影响水产养殖和海上捕鱼);③海岸侵蚀加速破坏的生态系统(风暴潮,海岸侵蚀,并伴随着大量的海水,淹没农田和湿地,加快沿海生态系统退化);④海水倒灌造成的河水和地下水水质的恶化.(1:00 1 A,3分服务)
(4)类型:台风风暴潮(或热带气旋风暴潮).(1)的空间分布特征:在海南岛的东南沿海.(1)减灾对策:良好的风暴潮预报和监测,良好的组织协调灾害的打击,公众广泛参与减灾活动,建设沿海防护林体系和沿海保护项目(堤).(1:00 1 A,3分服务)
28(13分)(1)锋面雨带的影响,留在该地区很长一段时间(或准静止锋的影响),导致的降水,导致洪水的发生.(2)
(2)非工程措施:加强洪泛区土地管理,实施洪水保险,洪水预报和预警系统,的建议应急疏散预案和对策居民.(2)
工程措施:绿化,防护林体系,保持土壤和水.修水库的上游,中游建设蓄洪,分洪工程下游挖新河入海.(2)(其他答案合理的判断分)
(3)关注汛期天气预测;学习逃生技能,逃生的知识,准备逃跑物资.
(A 1点1点,3点)(4)有利影响:有利于抑制害虫和疾病;(1)有利于缓解旱情.(1)的
不利的影响:农业设施(如大棚温室损失)(1)蔬菜及其他农作物,畜牧业,林业(果树)的破坏,渔业遭受冻害.(1)(其他答案合理酌情给分)
29(12分)(1)草原生态环境,特别适合刺槐的生长和繁殖,特别是在干旱年份,更容易引发的形成蝗灾蝗虫大量繁殖.
(A凌晨1点1分,2分)(2)变化:今年夏天的频率最高,冬季最低.(2)
原因:夏季气温高,适宜蝗虫繁殖,生长,冬季气温低,蝗虫不能生长和繁殖(冬季蝗虫卵的形式存在,没有成年的活动)(1:00 1 2点)
(3)人工诱捕幼虫,成虫;农药病虫害防治;起火和投入的天敌生物措施,加强蝗情监测,掌握反映蝗虫发生动态变化,预防和控制女性蝗虫产卵环境.(曾任1:00 1 A,3其他答案合理酌情给分)
(4)利用地理信息技术和其他手段,加强对大鼠灾害监测,改善生态环境受影响的地区,使用天敌灭鼠,使用药物灭鼠,内置防鼠墙.(曾任1:00 1 A,3其他答案合理酌情给分)1年前查看全部
- (2014届南京市秦淮区第一学期期末试题)(10分)铁矿石冶炼成铁是一个复杂的过程。炼铁的原理是利用一氧化碳与氧化铁的反
(2014届南京市秦淮区第一学期期末试题)(10分)铁矿石冶炼成铁是一个复杂的过程。炼铁的原理是利用一氧化碳与氧化铁的反应,该化学方程式为 。
(1)某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可以日产含铁98%的生铁的质量是多少?(请写出计算过程,结果精确到0.1t)
(2)某化学兴趣小组在实验室中模拟炼铁原理的实验,并对固体产物的成分进行探究。
[设计实验] 用一氧化碳还原纯净的氧化铁粉末,实验装置如右图,酒精灯b的作用是 。
[进行实验]该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)。
②反应后玻璃管和内盛黑色固体的总质量m(冷却到室温称量)。
[分析与讨论]本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁。
③
[进一步实验和得出结论]物质
性质四氧化三铁 氧化亚铁 氧化铁 铁粉 颜色 黑色 黑色 红色 黑色 能否被磁铁吸引 能 不能 不能 能
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 。
②该小组同学将黑色固体粉末投入硫酸铜溶液中,一段时间后无紫红色固体析出,则该黑色固体粉末为 。其实,进行如上图所示实验后,若测得反应后玻璃管和内盛黑色固体的总质量m为 g,也能得出这个结论。
[反思与评价]一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间。上图所示实验装置中,应作的一处修改是 。 benladeng9111年前1
benladeng9111年前1 -
 ln99099 共回答了21个问题
ln99099 共回答了21个问题 |采纳率90.5%3CO+Fe 2 O 3 高温 2Fe+3CO 2 (1)2714.3t (2)【设计实验】尾气处理,防止空气污染
[进一步实验和得出结论]①氧化亚铁 ②四氧化三铁 65.8g
[反思与评价]将酒精灯a换成酒精喷灯
1年前查看全部
- (2014届上海市六校高三第二次联考化学试卷)
(2014届上海市六校高三第二次联考化学试卷)
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.
(一)用铁屑与硫酸反应制备FeSO 4
已知4Fe 2+ +O 2 +4H + = 4Fe 3+ +2H 2 O。FeSO 4 在水中的溶解度见图。
(1)首先,将铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。此步骤中,分离出液体的方法通常不用过滤,使用的操作是____________(填写操作名称)。
(2)向处理过的铁屑中加入适量的硫酸,在一定温度下使其反应到不再产生气体,趁热过滤,得FeSO 4 溶液。此处:硫酸浓度应选择
温度宜控制在______;加热的同时需适当补充水,原因是 。反应中应保持n(Fe)/n(H 2 SO 4 ) 1(填“<”、“>”或“=”)。A.浓硫酸 B.10moL/L硫酸 C.3moL/L硫酸 D.任意浓度硫酸;
(3)亚铁盐在空气中易被氧化,但形成复盐可稳定存在。如“摩尔盐”,即硫酸亚铁铵[(NH 4 ) 2 SO 4 •FeSO 4 •6H 2 O],就是在FeSO 4 溶液中加入少量稀H 2 SO 4 溶液,再加入饱和(NH 4 ) 2 SO 4 溶液,经过蒸发浓缩、冷却结晶、过滤等一系列操作后所得。过程中稀硫酸的作用是 。
(二)用含有少量Al的废铁屑制备Fe 2 (SO 4 ) 3 其操作流程及有关资料如下:
沉淀物 Fe(OH) 3 Fe(OH) 2 Al(OH) 3 开始沉淀 2.3 7.5 3.4 完全沉淀 3.2 9.7 4.4
(4)加NaHCO 3 时,混合液pH值应控制在_______________________。
(5)反应Ⅱ中反应的离子方程式是:___________________。
(6)实际生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是________,气体X与NO配比的比例是_____________。 hnhkmmy1年前1
hnhkmmy1年前1 -
 竹露水波 共回答了23个问题
竹露水波 共回答了23个问题 |采纳率91.3%(1)倾析
(2)C ; 60℃左右;防止硫酸亚铁晶体析出;>
(3)抑制Fe 2+ 、NH 4 + 的水解
(4)4.4~7.5
(5)3Fe 2+ +NO 3 - +4H + =3Fe 3+ +NO↑+2H 2 O
(6)节约Fe(NO 3 ) 3 、防止NO污染(同理即可); 3:4
(1)首先,将铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。此步骤中,由于Fe屑沉在容器的底部,溶液在上部,所以分离出液体的方法通常不用过滤,使用的操作是倾析法。
(2)在室温下,Fe在浓硫酸中会发生钝化现象。在10moL/L硫酸中容易发生氧化还原反应产生硫酸铁和SO 2 和水。不能得到硫酸亚铁。所以要用3moL/L硫酸。选项为C。由于FeSO 4 在60℃左右溶解度最大,所以温度宜控制在60℃左右。为防止硫酸亚铁晶体析出,加热的同时需适当补充水。为了防止在加热的过程中Fe 2+ 被氧化为Fe 3+ ,Fe粉应该稍微过量一些。所以反应中应保持n(Fe)/n(H 2 SO 4 )>1。
(3)在制取摩尔盐如硫酸亚铁铵[(NH 4 ) 2 SO 4 •FeSO 4 •6H 2 O]的过程,就是在FeSO 4 溶液中加入少量稀H 2 SO 4 溶液,再加入饱和(NH 4 ) 2 SO 4 溶液,经过蒸发浓缩、冷却结晶、过滤等一系列操作后所得。过程中稀硫酸的作用是为了抑制Fe 2+ 、NH 4 + 的水解,防止产物不纯。
(4)含有少量Al的废铁屑硫酸溶解得到硫酸铝、硫酸亚铁、硫酸铁。为了除去杂质Al 3+ 、Fe 2+ .要加NaHCO 3 时,来调节混合液pH值。Al(OH) 3 沉淀完全的pH为4.4,而Fe(OH) 2 开始形成沉淀的pH为应控制在7.5。若把混合液pH值控制在4.4~7.5,就可以使Al(OH) 3 沉淀完全但Fe元素都留在溶液中。
(5)当向含有FeSO 4 、Fe 2 (SO 4 ) 3 溶液中加入Fe(NO 3 ) 3 和H 2 SO 4 时也就相当于加入了稀硝酸。发生氧化还原反应。在反应Ⅱ中反应的离子方程式是:3Fe 2+ +NO 3 - +4H + =3Fe 3+ +NO↑+2H 2 O。
(6)由于在室温下会发生反应:2NO+O 2 =2NO 2 ;3NO 2 +H 2 O =2HNO 3 +NO。叠加得到总方程式为4NO+3O 2 +2H 2 O =4HNO 3 。所以实际生产中,将反应Ⅱ产生的NO配比一种气体O 2 ,混合后重新通入反应Ⅱ中,该设计的目的是节约Fe(NO 3 ) 3 、防止NO污染。根据上述总方程式可以看出气体O 2 与NO配比的比例是3:4。1年前查看全部
- (2014届山西省山大附中高三下学期第一次月考化学试卷)
(2014届山西省山大附中高三下学期第一次月考化学试卷)
已知某有机物的分子式为C 3 H a O b (a、b均是不为0的正整数),下列关于C 3 H a O b 的说法中正确的是( )A.当a=8时,该物质可以发生加成反应 B.无论b为多少,a不可能为奇数 C.当a=6、b=2时,该物质不可能含有两种官能团 D.1个C 3 H a O b 可能含有3个醛基  水滴_rr1年前1
水滴_rr1年前1 -
 发贴鲸宝宝 共回答了19个问题
发贴鲸宝宝 共回答了19个问题 |采纳率94.7%B
当a=8时,有机物的饱和度为0,即不会有不饱和键的存在,不能发生加成反应,A选项不正确;C 3 H 6 O 2 的不饱和度为1,可以含有-OH和-CHO;C选项不正确;,C 3 H a O b 只有三个碳原子,不可能含有3个醛基,D选项不正确。1年前查看全部
- 河南省开封市2014届高三下学期冲刺模拟试题 英语
 大连机床rr1年前0
大连机床rr1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 南通市2014届高三第二次调研测试英语试题答案
南通市2014届高三第二次调研测试英语试题答案
谁把南通市2014届高三第二次调研英语试卷答案给我啊 东东鸟东东1年前1
东东鸟东东1年前1 -
 g222c 共回答了10个问题
g222c 共回答了10个问题 |采纳率100%建议你还是去贴吧(像高考吧,地理吧,数学吧,英语吧)问下…大.家在学.校做都是做纸制.的,根.本不是电,.子的,谁也不会给你一题..题..手.打.即使有也要给你找试卷,拍照,上网上传等麻烦的步骤基本没人会去做,所..以别..干等了.
还有就是你可以在百度文库里搜题目,或者把题目打几十个字出来用百度直接搜索下,说不定能找到.或者你可以去出这本书的官网看下,官网上也可能有答案.还有就是大型的考试也不会有答案了,除非是考完成绩出来后,与其在这求答案,你还不如去好好复习,争取考好来.1年前查看全部
- (2014届江西省重点中学盟校高三第二次联考英语试卷)33. -You didn’t invite Mary to th
(2014届江西省重点中学盟校高三第二次联考英语试卷)33. -You didn’t invite Mary to the ball?
-_____ ?A.Must I invite B.Should I have invited? C.must I have invited D.Should I invite  tecdlc1年前1
tecdlc1年前1 -
 板凳小子007 共回答了13个问题
板凳小子007 共回答了13个问题 |采纳率92.3%B
本句考察的情态动词和虚拟语气。Should have done本应该做某事实际上却未做(表示对过去的虚拟);must have done一定做了某事(对过去情况的有把握的肯定推测)。句义:—你没有邀请Mary来参加舞会?—我应该请她吗?根据第一句中的did说明是对过去情况的说明,排除AD项。Must have done通常只用于肯定句中。故B正确。1年前查看全部
- (2014届黑龙江省伊春市伊春区第一学期期末试题)根据下图所示,回答有关问题:
(2014届黑龙江省伊春市伊春区第一学期期末试题)根据下图所示,回答有关问题:

(1)写出图中标有字母的仪器名称:a 。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是 (填字母),实验时该装置试管口应放一团棉花,其目的是 ;反应的化学方程式为 。实验结束,停止加热前要先将导管移出水面,目的是 。(3)实验室制取二氧化碳气体时如果用E装置收集该气体,则气体应从 端进入(填“b”或“c”)。请写出实验室制CO 2 的化学方式 。通常用澄清石灰水来检验二氧化碳,反应的化学方程式为 。
如果发生装置选用C,其优点是 ;
(4)若D装置中盛有紫色石蕊溶液,通入CO 2 气体后,溶液变 ,原因是 。(用化学方程式表示) 黑夜冥妖1年前1
黑夜冥妖1年前1 -
 青黄不接070 共回答了28个问题
青黄不接070 共回答了28个问题 |采纳率96.4%1年前查看全部
- 湖北省部分重点中学2014届高三第一次联考化学选择题答案
湖北省部分重点中学2014届高三第一次联考化学选择题答案
2013年11月8日考的,武钢三中命题的 胖胖叶子1年前2
胖胖叶子1年前2 -
 hzyd 共回答了26个问题
hzyd 共回答了26个问题 |采纳率96.2%没人回答,我还是自己做的,只错了两个,自己动手,丰衣足食!1年前查看全部
- (2014届湖南省益阳市高三下学期模拟考试理综化学试卷)为了防止或减少机动车尾气和燃煤产生的烟气对空气
(2014届湖南省益阳市高三下学期模拟考试理综化学试卷)为了防止或减少机动车尾气和燃煤产生的烟气对空气(2014届湖南省益阳市高三下学期模拟考试理综化学试卷)
为了防止或减少机动车尾气和燃煤产生的烟气对空气的污染,人们采取了很多措施。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO 2 (g)+ N 2 (g) △H<0,
2CO 2 (g)+ N 2 (g) △H<0,
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t 1 时刻达到平衡状态的是 (填代号)。
(下图中υ 正 、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH 4 催化还原NO X 可以消除氮氧化物的污染。已知:
CH 4 (g)+2NO 2 (g)=N 2 (g)+CO 2 (g)+2H 2 O(g) △H=-867 kJ/mol①
2NO 2 (g) N 2 O 4 (g) ΔH=-56.9 kJ/mol②
N 2 O 4 (g) ΔH=-56.9 kJ/mol②
H 2 O(g) = H 2 O(l) ΔH=-44.0 kJ/mol③
写出CH 4 催化还原N 2 O 4 (g)生成N 2 和H 2 O(l)的热化学方程式: 。
(3)用NH 3 催化还原NO X 也可以消除氮氧化物的污染。如图,采用NH 3 作还原剂,烟气以一定的流速通过催化剂,通过测量逸出气体中氮氧化物含量,从而可确定烟气脱氮率,反应原理为:NO(g) +NO 2 (g)+2NH 3 (g) 2N 2 (g) + 3H 2 O(g)。
2N 2 (g) + 3H 2 O(g)。
①该反应的△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(p B )代替物质的量浓度(c B )也可以表示平衡常数(记作K P ),
则上述反应的K P = 。
(4)NO 2 、O 2 和熔融NaNO 3 可制作燃料电池,其原理见图,石墨I为电池的 极。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。
(5)硝酸工业尾气中氮氧化物(NO和NO 2 )可用尿素〔CO(NH 2 ) 2 〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO 2 体积比为1︰1)的质量为 g。
 浅浅滴笑1年前1
浅浅滴笑1年前1 -
 langzi791015 共回答了18个问题
langzi791015 共回答了18个问题 |采纳率94.4%(1)B D(各1分,共2分,选错不得分)
(2)CH 4 (g)+N 2 O 4 (g)=N 2 (g)+2H 2 O(l)+CO 2 (g)△H=" —898.1kJ/mol" (2分)
(3)①<(2分)②P(N 2 ) 2 P(H 2 O) 3 /P(NO)P(NO 2 )P(NH 3 ) 2 (2分)
(4)负 (2分) NO 2 +NO 3 - -e - =N 2 O 5 (2分)
(5)76g(2分)
(1)可逆反应达化学平衡状态时正逆反应速率不再变化,所以A错误;该物质的浓度在化学平衡时保持不变,所以K不再变化,B正确;对于恒容容器而言,各物质的物质的量不再改变,所以C错误;平衡时NO的质量分数不再改变,正确,所以答案选BD;
(2)根据盖斯定律,目标方程式=①-②+③×2,所以CH 4 催化还原N 2 O 4 (g)生成N 2 和H 2 O(l)的热化学方程式为CH 4 (g)+N 2 O 4 (g)=N 2 (g)+2H 2 O(l)+CO 2 (g)△H= —898.1kJ/mol;
(3)据图可知,当反应达平衡后继续升温,脱氮率降低,说明升温,平衡逆向移动,所以正向是放热反应,△H<0;根据平衡常数的表达式,用平衡压强表示的平衡常数为K P =P(N 2 ) 2 P(H 2 O) 3 /P(NO)P(NO 2 )P(NH 3 ) 2
(4)在该反应中,二氧化氮中氮元素化合价升高,发生氧化反应,负极发生氧化反应,所以石墨I为电池的的负极,该电池在使用过程中石墨I电极上生成氧化物Y,则Y是N 2 O 5 ,电极反应式为NO 2 +NO 3 - -e - =N 2 O 5 ;
(5)NO和NO 2 与尿素〔CO(NH 2 ) 2 〕反应生成无污染物质是氮气、二氧化碳、水,化学方程式为
NO+NO 2 +CO(NH 2 ) 2 =2N 2 +2H 2 O+CO 2 ,所以1 mol尿素能吸收NO和NO 2 的物质的量是1mol,其质量为76g。1年前查看全部
- 各位大神好,我是2014届2班的(初中的),请大家为我们班设计一个积极向上的班名,班级口号,班训,班级目标。请有想法的大
各位大神好,我是2014届2班的(初中的),请大家为我们班设计一个积极向上的班名,班级口号,班训,班级目标。请有想法的大神多多告诉我。大家,谢谢哒。
 cffzxs1年前7
cffzxs1年前7 -
 金飘飘 共回答了2个问题
金飘飘 共回答了2个问题 |采纳率可以用英文吗?1年前查看全部
- 2014届初三数学模拟测试卷(2) 第25题
2014届初三数学模拟测试卷(2) 第25题
已知点A(m,n),B(p,q)(m<p)在直线y=kx+b上.
(1)若m+p=2,n+q=2b²+6b+4.试比较n和q的大小,并说明理由;
(2)若k<0,过点A与x轴平行的直线和过点B与y轴平行的直线交于点C(1,1),AB=5,且△ABC的周长为12,求k、b的值. 324530f6691608e61年前1
324530f6691608e61年前1 -
 巴扎利 共回答了16个问题
巴扎利 共回答了16个问题 |采纳率87.5%1)n=km+b,q=kp+b
n+q=k(m+p)+2b=2k+2b=2b²+2b+4,得:k=b²+2
因此y=(b²+2)x+b
故y为单调增函数,因此n1年前查看全部
- 安徽百校联盟,安徽第一卷,2014届高三年级联合统考(二)理综,理科数学,英语答案
安徽百校联盟,安徽第一卷,2014届高三年级联合统考(二)理综,理科数学,英语答案
急用!>3 风风雨雨一起走81年前1
风风雨雨一起走81年前1 -
 chencu 共回答了18个问题
chencu 共回答了18个问题 |采纳率100%第一部分:听力(共20小题;每小题1.5分,满分30分)1-5 BAACB 6-10 CABCA 11-15 BABCA 16-20 BBACB第二部分:英语知识运用第一节 语法和词汇 (共15小题;每小题1分,满分15分)21–25 CBCDB 26–30 BBACA 31–35 BCC...1年前查看全部
- (2014届湖北省天门市高中毕业生四月调研测试理综化学试卷)
(2014届湖北省天门市高中毕业生四月调研测试理综化学试卷)
Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO 2 与太阳能电池电解水产生的H 2 合成甲醇,其过程如下图所示,试回答下列问题:
(1)该合成路线对于环境保护的价值在于 。
(2)15~20%的乙醇胺(HOCH 2 CH 2 NH 2 )水溶液具有弱碱性,上述合成线路中用作CO 2 吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因 。
(3)CH 3 OH、H 2 的燃烧热分别为:△H=-725.5 kJ/mol、△H=-285.8 kJ/mol,写出工业上以CO 2 、H 2 合成CH 3 OH的热化学方程式: 。
Ⅱ.将燃煤废气中的CO 2 转化为甲醚的反应原理为:
2CO 2 (g) + 6H 2 (g) CH 3 OCH 3 (g) + 3H 2 O(g)
CH 3 OCH 3 (g) + 3H 2 O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO 2 的转化率见下表:投料比[n(H 2 ) / n(CO 2 )] 500 K 600 K 700 K 800 K 1.5 45% 33% 20% 12% 2.0 60% 43% 28% 15% 3.0 83% 62% 37% 22%
(4)该反应的焓变△H 0,熵变△S 0(填>、<或=)。
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。
(6)若以1.12 L·min -1 (标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L -1 CuSO 4 溶液,通电0.50 min后,理论上可析出金属铜 g。 623houzi1年前1
623houzi1年前1 -
 街头公主 共回答了11个问题
街头公主 共回答了11个问题 |采纳率81.8%(1)有利于防止温室效应 (2分)
(2)HOCH 2 CH 2 NH 2 +H 2 O HOCH 2 CH 2 NH 3 + +OH - (2分)
HOCH 2 CH 2 NH 3 + +OH - (2分)
(3)CO 2 (g)+3 H 2 (g)= CH 3 OH(l)+ H 2 O(l) △H=-131.9kJ/mol(3分)
(4)< (1分),< (1分)
(5) CH 3 OCH 3 -12e - +16 OH - =2CO 3 2- +11 H 2 O (3分 )
(6)9.6(2分 )
(1)氢气与二氧化碳合成甲醇,减少了二氧化碳的排放,有利于防止温室效应
(2)HOCH 2 CH 2 NH 2 水解使溶液呈碱性,发生的离子方程式为HOCH 2 CH 2 NH 2 +H 2 O HOCH 2 CH 2 NH 3 + +OH -
HOCH 2 CH 2 NH 3 + +OH -
(3)根据盖斯定律,将甲醇与氢气的燃烧热化学方程式作相应调整,得△H=-285.8 kJ/mol×3-(-725.5 kJ/mol)=-131.9kJ/mol,所以合成甲醇的热化学方程式为CO 2 (g)+3 H 2 (g)= CH 3 OH(l)+ H 2 O(l) △H=-131.9kJ/mol
(4)随温度升高,二氧化碳1年前查看全部
- (2014届上海市十三校高三测试化学试卷)
(2014届上海市十三校高三测试化学试卷)
锂被誉为“金属味精”,以LiCoO 2 为正极材料的锂离子电池已被广泛用作便携式电源。工业上常以β锂辉矿(主要成分为LiAlSi 2 O 6 ,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂。其中一种工艺流程如下:
已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
请回答下列问题:氢氧化物 Fe(OH) 3 Al(OH) 3 Mg(OH) 2 开始沉淀pH 2.7 3.7 9.6 完全沉淀pH 3.7 4.7 11
(1)写出反应Ⅰ中有电子转移的化学方程式_________________________;
(2)反应Ⅱ加入碳酸钙的作用是_______________;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由 ____________;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至________出现时,就可停止该操作。
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处。这种相似性称为对角线规则。步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是___________。
(6)请设计一种从水洗后的矿泥中分离出Al 2 O 3 的流程:
(流程常用的表示方式为: )
) wootsren1年前1
wootsren1年前1 -
 yilin99999 共回答了13个问题
yilin99999 共回答了13个问题 |采纳率84.6%(1)2FeO+4H 2 SO 4 (浓) Fe 2 (SO 4 ) 3 +SO 2 ↑+4H 2 O
Fe 2 (SO 4 ) 3 +SO 2 ↑+4H 2 O
(2)除去反应Ⅰ中过量的H 2 SO 4 ;控制pH,使Fe 3 + 、Al 3 + 完全沉淀
(3)不能,镁离子不能完全除去。
(4)晶体膜
(5)加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li 2 O,电解时产生O 2 .
(6)
或
(1)浓硫酸有氧化性,FeO有还原性,二者在加热时会发生氧化还原反应。根据质量守恒定律和电子守恒可得该反应的方程式为:2FeO+4H 2 SO 4 (浓) Fe 2 (SO 4 ) 3 +SO 2 ↑+4H 2 O。
Fe 2 (SO 4 ) 3 +SO 2 ↑+4H 2 O。
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的剩余的H 2 SO 4 ;调节溶液的pH,同时使Fe 3 + 、Al 3 + 完全转化为沉淀而除去。
(3)在反应Ⅲ中只需加入碳酸钠溶液,因为其碱性是盐水解产生的,碱性不如NaOH强,而且MgCO 3 的溶解度比Mg(OH) 2 大,不能很好的把Mg 2+ 沉淀出去。因此不能达成该步骤的目的。
(4)加热蒸发时,只要看到大量固体析出或者仅余少量液体时,停止加热,利用余热把固体蒸干。
(5)步骤③中电解时,阳极产生的氯气中会混有少量氧气,是因为在加热蒸干LiCl溶液时,LiCl有少量发生水解反应产生了LiOH混在LiCl中。LiOH受热分解生成Li 2 O,电解时产生了O 2 。
(6)水洗后的矿泥中含有Fe 2 O 3 、Al 2 O 3 、SiO 2 .可以先加盐酸把Fe 2 O 3 、Al 2 O 3 溶解变为FeCl 3 、AlCl 3 ,除去难溶的SiO 2 .然后向溶液中加入过量的NaOH溶液,发生反应:FeCl 3 +3NaOH=Fe(OH) 3 ↓+3NaCl。AlCl 3 +4NaOH=NaAlO 2 +3NaCl+2H 2 O。把Fe(OH) 3 沉淀过滤除去,然后向滤液中通入过量的CO 2 气体,发生反应NaAlO 2 + CO 2 +2H 2 O= Al(OH) 3 ↓+NaHCO 3 .把Al(OH) 3 沉淀过滤出来洗涤干净,然后灼烧既得Al 2 O 3 。另一种方法是把矿泥用NaOH溶液处理,可以得到NaAlO 2 和Na 2 SiO 3 溶液,而Fe 2 O 3 不溶,过滤除去。然后向滤液中加入过量的盐酸发生反应NaAlO 2 +4HCl= AlCl 3 +NaCl+2H 2 O。Na 2 SiO 3 +2HCl=H 2 SiO 3 ↓+2NaCl。把硅酸沉淀过滤除去,再向滤液中通入过量的氨气,发生反应AlCl 3 +3NH 3 +3H 2 O= Al(OH) 3 ↓+3NH 4 Cl。再把Al(OH) 3 沉淀过滤出来洗涤干净,然后灼烧既得Al 2 O 3 。1年前查看全部
- (2014届江苏省南京市、淮安市高三第二次模拟考试化学试卷)
(2014届江苏省南京市、淮安市高三第二次模拟考试化学试卷)
尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质。其转化过程如下:
下列说法错误的是A.酪氨酸既能与盐酸反应,又能与氢氧化钠反应 B.1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br 2 C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 D.1 mol尿黑酸与足量NaHCO 3 反应,最多消耗3 mol NaHCO 3  gogochencn781年前1
gogochencn781年前1 -
 newwine 共回答了19个问题
newwine 共回答了19个问题 |采纳率94.7%D
A、酪氨酸含有酚羟基与碱反应,含有氨基与酸反应,正确;B、尿黑酸含有2个酚羟基,苯环上3个空位均为羟基的邻位,可被溴取代,故1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br 2 ,正确;C、本结构中含有两个平面,苯环平面共7个碳原子一定共平面,碳氧双键平面一定有3个碳原子共平面,正确;D、尿黑酸中含有酚羟基不与NaHCO 3 反应,含羧基与NaHCO 3 反应,所以只能消耗1mol,错误。1年前查看全部
- 跪求河南开封2014届高三理科综合试题生物选择第二题解析
跪求河南开封2014届高三理科综合试题生物选择第二题解析
2.对下列四幅图所对应的生物活动叙述错误的是

A. 若增温至适宜温度(其他条件不变),则示其生成物量变化的是图a中虚线
B.若要抑制肿瘤细胞增殖,药物作用最好选在图b的S期(DNA复制)
C.若图c表示次级精母细胞,则该生物体细胞中染色体数最多为4个
D.图d中物质①④的基本单位不同,③约有20种
 coolxiong1年前1
coolxiong1年前1 -
 dingyanfa 共回答了17个问题
dingyanfa 共回答了17个问题 |采纳率100%此题选C,C选项要考虑体细胞进行有丝分裂时的情况,如果某一体细胞正处于有丝分裂后期,则染色体数最多为8个.1年前查看全部
- 在昆明市2014届第一次统测中我校的理科数学考试成绩ξ~N(90,σ2)(σ>0),统计结果显示P(60≤ξ≤120)=
在昆明市2014届第一次统测中我校的理科数学考试成绩ξ~N(90,σ2)(σ>0),统计结果显示P(60≤ξ≤120)=0.8,假设我校参加此次考试的人数为420人,那么试估计此次考试中.我校成绩高于120分的有______人.
 nini0121年前1
nini0121年前1 -
 鬼手 共回答了16个问题
鬼手 共回答了16个问题 |采纳率100%解题思路:先根据正态分布曲线的图象特征,结合P(60≤ξ≤120)=0.8,可得成绩在120分以上的人数约为总人数的[1/2](1-0.8)=0.1,从而可求得成绩高于120分的学生数.∵成绩ξ~N(90,σ2),
∴其正态曲线关于直线x=90对称,
又∵P(60≤ξ≤120)=0.8,
由对称性知:成绩在120分以上的人数约为总人数的[1/2](1-0.8)=0.1,
∴成绩高于120分的学生约有:0.1×420=42.
故答案为:42.点评:
本题考点: 正态分布曲线的特点及曲线所表示的意义.
考点点评: 本小题主要考查正态分布曲线的特点及曲线所表示的意义等基础知识,考查运算求解能力,考查数形结合思想、化归与转化思想.属于基础题.正态分布是概率论中最重要的一种分布,也是自然界最常见的一种分布.该分布由两个参数--平均值和方差决定.概率密度函数曲线以均值为对称中线,方差越小,分布越集中在均值附近.1年前查看全部
- 长沙市一中2014届高三月考(七)数学文科,急
 牛奶的味道EG1年前1
牛奶的味道EG1年前1 -
 原木艺术灯工作室 共回答了22个问题
原木艺术灯工作室 共回答了22个问题 |采纳率81.8%DBCAB DCDC.10.2 11.1/2 12.-1 13.(-1/3,0) 14.3分之根号3 15.255 81年前查看全部
- (2014届北京市延庆县高三第一次模拟理综化学试卷)
(2014届北京市延庆县高三第一次模拟理综化学试卷)
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是
装置①装置②装置③A.装置①研究的是电解CuCl 2 溶液,b电极上有红色固体析出 B.装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e - = Fe 2+ C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl - -2e - = Cl 2 ↑ D.三个装置中涉及的主要反应都是氧化还原反应  jlc513691年前1
jlc513691年前1 -
 gg永存 共回答了15个问题
gg永存 共回答了15个问题 |采纳率86.7%C
A、装置①中b极是阴极,阳离子放电,所以有红铜析出,正确;B、装置②中Fe、C、食盐水构成原电池,在中性环境中铁易发生吸氧腐蚀,铁做负极,发生的反应为Fe-2e - = Fe 2+ ,正确;C、装置③中B极为阴极,阳离子放电,则B极有氢气放出,氯气应在A极放出,错误;D、电化学反应均是氧化还原反应,正确,答案选C。1年前查看全部
- (2014届江西省重点中学盟校高三第二次联考英语试卷)32. The new technology, if _____t
(2014届江西省重点中学盟校高三第二次联考英语试卷)32. The new technology, if _____to rice growing, will help increase the grain output.
A.applying B.applied C.to apply D.having applied  温泉老鼠1年前1
温泉老鼠1年前1 -
 白云天_dd 共回答了18个问题
白云天_dd 共回答了18个问题 |采纳率88.9%B
当状语从句的主语和主句主语一致且含有be动词的时候,可以把状语从句的主语和be动词一起省略。本句在if的后面省略了it is;动词apply在本句中表示“运用”,构成固定搭配apply sth to sth把…运用到..之上。句义:如果这项新技术被运用于水稻种植,它将会帮助提高谷物产量。故B正确。1年前查看全部
- (2014届南京市高淳区第一学期期末试题)(7分)在宏观,微观和符号之间建立联系是化学学习的特点。
(2014届南京市高淳区第一学期期末试题)(7分)在宏观,微观和符号之间建立联系是化学学习的特点。
(1)用化学用语填空:
①一个镁离子 ;②-2价的氧元素 ;
③两个铁原子 ;④空气中最多的物质的构成微粒
(2)属素[CO(NH 2 ) 2 ]是一种常用的化肥,工业上生产属素的反应的微观示意图如下:
①尿素由_________种元素组成,相对分子质量为___________。
②生产尿素的反应中,A与B的质量比为___________。 huazizi1年前1
huazizi1年前1 -
 我就是王斌 共回答了14个问题
我就是王斌 共回答了14个问题 |采纳率100%1年前查看全部
- 湖南师大附中2014届地理月考试卷(五)的答案。
 q82oc1年前1
q82oc1年前1 -
 太阳升起la 共回答了9个问题
太阳升起la 共回答了9个问题 |采纳率66.7%上ks5u高考网,有答案1年前查看全部
- (2014届江西省重点中学盟校高三第二次联考英语试卷)34. He wrote a long letter ___he
(2014届江西省重点中学盟校高三第二次联考英语试卷)34. He wrote a long letter ___he explained what had happened in the accident.
A.what B.which C.where D.how  high1231年前1
high1231年前1 -
 Tity_Dou 共回答了16个问题
Tity_Dou 共回答了16个问题 |采纳率100%C
本题是一个定语从句,先行词是a long letter,后面的定语从句he explained what had happened in the accident的句子结构很完整,所以使用关系副词引导这个定语从句,选项里只有where是关系副词。句义:他写了一封很长的信,在信里,他解释了事故里所发生的事情。故C正确。1年前查看全部
- (2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷)
(2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷)
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH 4 (g)+3O 2 (g)=2CO(g)+4H 2 O(l) △H=" —1214" kJ/mol
②2CO(g)+O 2 (g)=2CO 2 (g) △H=" —566" kJ/mol
则表示甲烷燃烧热的热化学方程式 。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH 4 和O 2 ,构成甲烷燃料电池。其负极电极反应式是: 。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH) 2 的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H + + 2e - = H 2 ↑
(4)将不同量的CO(g)和H 2 O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H 2 O(g) CO 2 (g)+H 2 (g),得到如下三组数据:
CO 2 (g)+H 2 (g),得到如下三组数据:实验组 温度/℃ 起始量/mol 平衡量/mol 达到平衡所需时间/min H 2 O CO CO 2 1 650 2 4 1.6 5 2 900 1 2 0.4 3 3 900 1 2 0.4 1
①实验1中,以v (H 2 )表示的平均反应速率为 。
②实验3跟实验2相比,改变可能相似的问题-
(2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷)
1年前1个回答
-
(2014届浙江省温州市十校联合体高三上学期期中联考化学试卷)
1年前1个回答
-
【苏北四市2009届高三第三次调研考试化学】下列化学用语正确的是
1年前1个回答
-
1年前1个回答
-
1年前1个回答
-
1年前1个回答
-
1年前1个回答
-
(2014届江苏省南京市、淮安市高三第二次模拟考试化学试卷)
1年前1个回答
-
1年前1个回答
-
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.056 s. - webmaster@yulucn.com 不晓得啊不晓得1年前1
不晓得啊不晓得1年前1 -
-
 刘水沙沙沙 共回答了18个问题
刘水沙沙沙 共回答了18个问题 |采纳率88.9%1年前查看全部
- (2014届苏州市第一学期期末试题)(5分 )右图为A、B两种固体物质的溶解度曲线。
(2014届苏州市第一学期期末试题)(5分 )右图为A、B两种固体物质的溶解度曲线。

(1)在 ℃时,A、B两种物质的溶解度相等。
(2)t 2 ℃时,100g水中溶解 gA物质恰好饱和,该饱和溶液中溶质的质量分数为 。若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 g。
(3)t 2 ℃时,分别将恰好饱和的A、B两种物质的溶液降温至t 1 ℃,溶质的质量分数保持不变的是 。 bbx20071年前1
bbx20071年前1 -
 肉砣了的 共回答了15个问题
肉砣了的 共回答了15个问题 |采纳率66.7%(1)t1;(2)25;20%;125;(3)B
1年前查看全部
- (2014届北京市海淀区高三第二学期适应性练习理综化学试卷)
(2014届北京市海淀区高三第二学期适应性练习理综化学试卷)
某实验小组同学探究铜与硝酸的反应。
(1)用浓硝酸和水按照不同体积比配成不同浓度的硝酸溶液,各取10 mL硝酸溶液分别与铜片反应,实验记录如下:序号 浓硝酸与水的体积比 实验现象 Ⅰ 1:1 反应速率快,溶液很快变成蓝色,铜丝表面有大量气泡冒出,气体呈红棕色 Ⅱ 1:3 反应速率较快,溶液变成蓝色,铜丝表面有大量气泡冒出,气体无色 Ⅲ 1:5 反应速率慢,微热后速率加快,溶液变成蓝色,铜丝表面有气泡冒出,气体无色
铜与稀硝酸反应的离子方程式为 ;若生成标准状况下0.56 L NO气体,反应中被还原的HNO 3 的质量为 g(小数点后保留两位有效数字)。
依据上表,制备NO气体最适宜的是实验II,理由是 。
(2)为防止有毒气体逸散造成空气污染,该小组同学改进实验装置,如右图所示(夹持仪器略去)。
用该装置进行铜与稀硝酸的反应并验证产生NO气体的性质,实验步骤如下:
Ⅰ.安装好装置后,检查装置气密性。
Ⅱ.打开旋塞C,从B管上端加入所选浓度的硝酸,至铜丝下沿(不接触铜丝)。
Ⅲ.向上移动B管,使A管液面上升至与橡皮塞恰好接触,关闭旋塞C,反应开始。
Ⅳ.当液面重新下降至与铜丝脱离接触时,反应停止。
Ⅴ.打开旋塞C,向下移动B管,使A中迅速进入少量空气,关闭旋塞C,观察现象。
……
①步骤Ⅰ中检查装置气密性的操作是:关闭旋塞C,从B管上端加入水,若观察到 ,说明装置的气密性良好。
②步骤Ⅲ操作的目的是 。
③为使A管内的NO气体完全被溶液吸收,可进一步采取的操作是 ,能确定NO完全被溶液吸收的现象是 。 clara20081年前1
clara20081年前1 -
 躁动不安 共回答了16个问题
躁动不安 共回答了16个问题 |采纳率81.3%(1)①3Cu + 8H + + 2NO 3 - = 3Cu 2+ + 2NO↑+ 4H 2 O 1.58
② 产物是NO , 反应速率较快(不用加热) 。
(2)①A、B间 形成液面差 ,且 保持不变
② 赶走液面上方空气, 防止NO被空气中的O 2 氧化, 以便观察生成气体的颜色。
③ 重复步骤 Ⅴ 的操作 (或答“向下移动B管,使A中迅速进入空气,关闭旋塞C,待气体变为红棕色,反复上述操作”)。
再次重复操作后 气体不再变为红棕色 。
(1)①铜与稀硝酸反应的离子方程式为3Cu + 8H + + 2NO 3 - = 3Cu 2+ + 2NO↑+ 4H 2 O ;
8HNO 3 (全部) ~ 2HNO 3 (被还原) ~ 2NO
2×63g 2×22.4L
1.58 g 0.56 L
②依据上表,制备NO气体最适宜的是实验II,理由是产物是NO,反应速率较快(不用加热)。
(2)①步骤Ⅰ中检查装置气密性的操作是:关闭旋塞C,从B管上端加入水,若观察到A、B间形成液面差,且保持不变 ,说明装置的气密性良好。
② 步骤Ⅲ操作的目的是 赶走液面上方空气,防止NO被空气中的O 2 氧化,以便观察生成气体的颜色。
③为使A管内的NO气体完全被溶液吸收,可进一步采取的操作是重复步骤Ⅴ的操作(或答"向下移动B管,使A中迅速进入空气,关闭旋塞C,待气体变为红棕色,反复上述操作")。能确定NO完全被溶液吸收的现象是再次重复操作后气体不再变为红棕色。1年前查看全部
- 高频考点测试卷 2014届高三物理一轮复习答案谁有?
高频考点测试卷 2014届高三物理一轮复习答案谁有?
需要高频考点1--9的就够了 ^O^ vv淡定宽容1年前1
vv淡定宽容1年前1 -
 alisa919 共回答了12个问题
alisa919 共回答了12个问题 |采纳率91.7%都高三了,好好学习吧1年前查看全部
- 安徽省第一卷2014届九年级第一学期月考(四)人教版数学答案!
 诺秀才1年前3
诺秀才1年前3 -
 幻灯机 共回答了18个问题
幻灯机 共回答了18个问题 |采纳率72.2%请赋予卷图1年前查看全部
- 2014届高三语文单元测试卷 湖南卷 第二单元 正确使用词语
 火魔炼心剑1年前1
火魔炼心剑1年前1 -
 我沈默006 共回答了14个问题
我沈默006 共回答了14个问题 |采纳率92.9%请给出完整具体的问题,这样我们才能准确地回答,生活快乐1年前查看全部
- (2014届上海市崇明县第一学期期末试题)下列四个图像中,能正确表示对应变化关系的是
(2014届上海市崇明县第一学期期末试题)下列四个图像中,能正确表示对应变化关系的是

中加水稀释 硝酸钾溶液中加入硝酸钾钾和二氧化锰固体中加入二氧化锰固体A.向一定量稀盐酸 B.一定温度下,向不饱和 C.加热一定量的氯酸 D.向一定量的双氧水溶液  ll的烟火21年前1
ll的烟火21年前1 -
 侠之小者 共回答了21个问题
侠之小者 共回答了21个问题 |采纳率95.2%B
1年前查看全部
- 2014届镇江市一模英语答案
 cxd797971年前1
cxd797971年前1 -
 yqm820619 共回答了16个问题
yqm820619 共回答了16个问题 |采纳率75%BABCB CCACA BCBAA CBBCB ABDAD CCBDC BBCDA ACBDA BCDDC ABCDA BBCCA DBAA BAD CBAD CDBA1年前查看全部
- (2014届浙江省温州中学高三上学期期末理综化学试卷)
(2014届浙江省温州中学高三上学期期末理综化学试卷)
下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是
A.此装置能将化学能转变为电能 B.石墨电极的反应式:O 2 +2H 2 O+4e — =4OH — C.电子由Cu电极经导线流向石墨电极 D.电池总的反应是:2Cu+O 2 +4HCl=2CuCl 2 +2H 2 O  一辈子顺着你1年前1
一辈子顺着你1年前1 -
 噩梦鬼魅 共回答了25个问题
噩梦鬼魅 共回答了25个问题 |采纳率84%B
A、原电池能将化学能转变为电能,A正确;B、原电池中负极失去电子发生氧化反应,正极得到电子发生还原反应,则铜是负极,氧气在正极通入,由于电解质是盐酸,因此石墨电极的反应式:O 2 +4H + +4e — =2H 2 O,B不正确;C、铜电极是负极,石墨是正极,则电子由Cu电极经导线流向石墨电极,C正确;D、电池总的反应是:2Cu+O 2 +4HCl=2CuCl 2 +2H 2 O,D正确,答案选B。1年前查看全部
- (2014届北京市房山区第一学期期末试题)2013年世界环境日中国主题为“同呼吸,共奋斗”。下列做法不符合这一主题的是
(2014届北京市房山区第一学期期末试题)2013年世界环境日中国主题为“同呼吸,共奋斗”。下列做法不符合这一主题的是
A.植树造林,绿化家园 B.露天焚烧秸秆和垃圾 C.工业“三废”达标后排放 D.推广使用太阳能、风能  风中小草1年前1
风中小草1年前1 -
 你手 共回答了26个问题
你手 共回答了26个问题 |采纳率80.8%B
1年前查看全部
- (2014届江西省重点中学盟校高三第二次联考英语试卷)23. They moved here in 2002. Unti
(2014届江西省重点中学盟校高三第二次联考英语试卷)23. They moved here in 2002. Until then they ______ in the London area.
A.lived B.have lived C.were living D.had lived  丛霖1年前1
丛霖1年前1 -
 tsqj_sun 共回答了12个问题
tsqj_sun 共回答了12个问题 |采纳率100%D
句义:他们是在2002年搬到这里的,到那时他们已经在伦敦地区生活了。根据句义可知他们在那个伦敦生活是在搬到这里之前,而搬来这里已经使用了moved,在这之前要使用过去的过去,也就是过去完成时。故D正确。1年前查看全部
- (2014届上海市长宁区第一学期期末测试)下列除杂质(括号内为杂质)的方法错误的是 A.MnO 2 (NaCl)溶解、过
(2014届上海市长宁区第一学期期末测试)下列除杂质(括号内为杂质)的方法错误的是
A.MnO 2 (NaCl)溶解、过滤、烘干 B.NaCl(KNO 3 )溶解、过滤、蒸发 C.CaO(CaCO 3 )高温煅烧 D.CO 2 (CO) 通过灼热的氧化铜  醒辰1年前1
醒辰1年前1 -
 dty6 共回答了16个问题
dty6 共回答了16个问题 |采纳率93.8%B
1年前查看全部
- (2014届广东省揭阳市高中毕业班高考第一次模拟考试理综化学试卷)
(2014届广东省揭阳市高中毕业班高考第一次模拟考试理综化学试卷)
卤块的主要成分是MgCl 2 ,此外还含 Fe 3+ 、Fe 2+ 和Mn 2+ 等离子。以卤块为原料可制得轻质氧化镁,工艺流程如下图: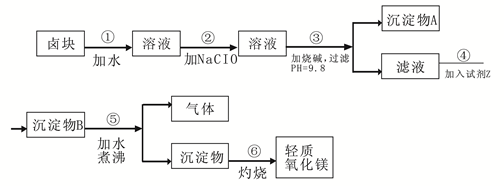
已知:Fe 2+ 氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe 3+ ,生成Fe(OH) 3 沉淀除去。若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH物质 开始沉淀 沉淀完全 Fe(OH) 3 2.7 3.7 Fe(OH) 2 7.6 9.6 Mn(OH) 2 8.3 9.8 Mg(OH) 2 9.6 11.1
表2化学试剂价格表试剂 价格(元/吨) 漂液(含NaClO,25.2%) 450 双氧水(含H 2 O 2 ,30%) 2400 烧碱(含98% NaOH) 2100 纯碱(含99.5% Na 2 CO 3 ) 600
(1)在步骤②中加入漂液而不是双氧水其原因是 。
写出加入NaClO发生反应的离子方程式 。
(2)在步骤③中控制pH=9.8,其目的是 。
(3)沉淀物A的成分为 ,试剂Z应该是 。
(4)在步骤⑤中发生反应的化学方程式是 。
(5)若在实验室中完成步骤⑥,则沉淀物必需在 (填仪器名称)中灼烧。 xiaocharis1年前1
xiaocharis1年前1 -
 人老珠黄999 共回答了19个问题
人老珠黄999 共回答了19个问题 |采纳率84.2%(1)漂液比H 2 O 2 的价格低得多。 (2分)2Fe 2+ +ClO - +2H + =2Fe 3+ +Cl - +H 2 O(3分)
(2)使除Mg 2+ 以外的各种杂质金属离子都生成氢氧化物沉淀,以便过滤除去。(2分)
(3)Fe(OH) 3 、 Mn(OH) 2 、 Mg(OH) 2 (2分,写3个且全对得2分,只写其中2个且写对得1分,其他情况都得0分)纯碱(2分)
(1年前查看全部
- 2014届高中化学学考
 am_nymph1年前1
am_nymph1年前1 -
 lw828316 共回答了12个问题
lw828316 共回答了12个问题 |采纳率91.7%学习化学最基础的同时也最重要的是深度了解课本,特别是书上的定义概念必须熟记和深刻理解,没事多看教科书其他资料什么的没太大必要,至于做题没必要太多做题主要是巩固知识点回归课本,这一科我感觉最大的特点就是知识点和细节的组合,只要用心去看和记每天花上半小时七八十分肯定是不存在什么问题的1年前查看全部
- 求2014届先知月考卷新课标数学二答案
 城里流浪狗1年前1
城里流浪狗1年前1 -
 宇恋莉 共回答了18个问题
宇恋莉 共回答了18个问题 |采纳率83.3%先给你做第22题吧,这个题目很简单,a1a2a3分别等于2,4,6这个很简单我不说了
那么可以推断ak=2k,那么现在归纳法证明这个推断是成立的
首先假设n=k时,有ak=2k,那么前k项和sk=k(k+1)
当n=k+1时有,k+1+ak+1/(2*(k+1))=(sk+ak+1)/(k+1),把sk=k(k+1)
代入上式就可以得到ak+1=2(k+1)
也就是说n=k+1时也是成立的
所以an=2n成立1年前查看全部
- (2014届广东省江门市高三一模理综化学试卷)
(2014届广东省江门市高三一模理综化学试卷)
从明矾[KAl(SO 4 ) 2 ·12H 2 O]制备Al、K 2 SO 4 和H 2 SO 4 的流程如下:
明矾焙烧的化学方程式为:4KAl(SO 4 ) 2 ·12H 2 O+3S=2K 2 SO 4 +2Al 2 O 3 +9SO 2 ↑+48H 2 O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂是 。
(2)步骤②中,为提高浸出率,可采取的措施有 。
(3)从水浸后的滤液中得到K 2 SO 4 晶体的方法是 。A.粉碎固体混合物 B.降低温度 C.不断搅拌 D.缩短浸泡时间
(4)步骤③电解的化学方程式是 ,电解池的电极是用碳素材料做成,电解过程中,阳极材料需要定期更换,原因是: 。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH) 2 ,则该电池的正极电极反应式是 。
(6)焙烧a吨明矾(摩尔质量为b g/mol),若SO 2 的转化率为96%,可生产质量分数为98%的H 2 SO 4 质量为 吨(列出计算表达式)。 4574hty1年前1
4574hty1年前1 -
 jqhcppsu3012 共回答了16个问题
jqhcppsu3012 共回答了16个问题 |采纳率93.8%(1)KAl(SO 4 ) 2 ·12H 2 O(2分)
(2) AC (2分,多选、错选0分)
(3)蒸发结晶(2分,“蒸发浓缩、冷却结晶”给1分)
(4) (2分)
(2分)
阳极中碳被氧化成CO 2 (CO)(2分,用化学方程式表示也可,如:
C+O 2 CO 2 或2C+O 2
CO 2 或2C+O 2  2CO ,条件用加热或970℃也可)
2CO ,条件用加热或970℃也可)
(5)NiO(OH)+H 2 O+e - =Ni(OH) 2 +OH - (2分)http://w ww.xkb1.com
(6)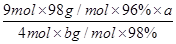 或
或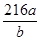 (3分,不带单位不扣分,化简也可以)
(3分,不带单位不扣分,化简也可以)
(1)明矾的焙烧已经给出了方程式,因此本题主要是考查氧化还原反应的特征。该方程式中发生化合价变化的只有S元素,明矾中的S元素一部分发生化合价降低,而S单质的化合价升高,因此反应中的氧化剂是明矾(KAl(SO 4 ) 2 ·12H 2 O),还原剂是单质S。
(2)步骤②是水浸明矾焙烧后的固体混合物,因此要提高浸出率,往往需要增大接触面积、充分溶解;因此粉碎固体混合物、不断搅拌都是可行的。
(3)焙烧后的固体混合物是K 2 SO 4 和Al 2 O 3 ,水浸后的溶液则是易溶于水的K 2 SO 4 溶液,所以要从单一组分的溶液中得到改溶质,可以直接蒸发结晶。
(4)氧化铝电解制备铝单质,该反应方程式为 ;在电解反应中阴极还原得到单质铝,阳极得到O2,由于阳极电极材料是C单质,所以在高温环境下,碳素材料会被氧气氧化为CO或CO2,从而导致阳极碳素电极受损,要定期更换。
;在电解反应中阴极还原得到单质铝,阳极得到O2,由于阳极电极材料是C单质,所以在高温环境下,碳素材料会被氧气氧化为CO或CO2,从而导致阳极碳素电极受损,要定期更换。
(5)以Al和NiO(OH)为电极构成的碱性电池,首先判断出单质Al做负极,NiO(OH)为正极;因此放电时正极得到电子被还原,从Ni的化合价变化可以得出得失电子数目,所以充分运用电荷守恒、原子守恒,再结合反应环境可以的该正极的反应式为NiO(OH)+H 2 O+e - =Ni(OH) 2 +OH - 。
(6)计算思路:计算明矾物质的量,根据方程式计算SO2的总物质的量,根据S原子守恒H2SO4溶质的物质的量等于96%的SO2,把溶质H2SO4的物质的量转化为质量,再用溶质H2SO4的质量除以质量分数求得H2SO4溶液的总质量。计算列式为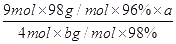 。
1年前查看全部
。
1年前查看全部
- 2014届11月调研考试(SX)答案
2014届11月调研考试(SX)答案
求答案 如题要生物英语 生物卷第3题 3.下列不属于某种固醇具有的生物学功能是() A.构成细胞膜 B.调节生活活动 C.促进肠道吸收 D.主要能源物质 十万火急 7:10前给答案给分
 爱吃甜品的猪1年前1
爱吃甜品的猪1年前1 -
 dgfls 共回答了17个问题
dgfls 共回答了17个问题 |采纳率94.1%a1年前查看全部
- (2014届浙江省宁波市十校高三3月联考理综化学试卷)
(2014届浙江省宁波市十校高三3月联考理综化学试卷)
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na 2 FeO 4 的装置如图所示。下列推断合理的是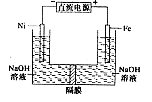
A.铁是阳极,电极反应为Fe-6e 一 +4H 2 O=FeO 4 2 - + 8H + B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 C.若隔膜为阴离子交换膜,则OH - 自右向左移动 D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)  lsgz1年前1
lsgz1年前1 -
 wenjue567 共回答了21个问题
wenjue567 共回答了21个问题 |采纳率81%D
A项中,铁是阳极,但溶液是碱性,不可能生成8H + ,不正确;B项中,电解时电子的流动方向为:负极→Ni电极,溶液中是离子导电,再是Fe电极→正极,故不正确;C项中,因阳极消耗OH - ,故OH - 通过阴离子交换膜自左向右移动,C不正确; D项中,电解时阳极吸引OH - 而使附近的pH降低、阴极区因OH - 向右侧移动而pH升高;因为总反应消耗OH - ,撤去隔膜混合后,与原溶液比较pH降低,说法正确。1年前查看全部
- 宁夏银川一中2014届高三下学期第二次模拟英语试卷语法题66答案为啥不用复数,跟后面的their一致?
宁夏银川一中2014届高三下学期第二次模拟英语试卷语法题66答案为啥不用复数,跟后面的their一致?
Lynn:I see.Anything ______6____would you suggest I should pay attention to?
Kate:Well,second,be sure to do some research on the company for ______65____ you are being interviewed.This will help you know if you have the needed skills or experience to work for that company.You can also ask the ________66____(interview),usually their personnel manager,about three intelligent questions about their business.That will show you are interested in their company.
语篇语法填空(15分) boot2341年前1
boot2341年前1 -
 买49只飘马鞋 共回答了19个问题
买49只飘马鞋 共回答了19个问题 |采纳率100%interviewer 面试官,后面的usually their personnel manager 是其同位语.同位语是单数名词,所以,interviewer用单数形式.1年前查看全部
- (2014届河南省中原名校高三下学期第一次联考化学试卷)
(2014届河南省中原名校高三下学期第一次联考化学试卷)
亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及生成气体产物的成分。已知:
①NO+NO 2 +2OH - =2NO 2 - +2H 2 O
②气体液化的温度:NO 2 21℃、NO -152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→C→_______→_______→_______;组装好仪器后,接下来进行的操作是________________。
(2)关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后, A中产生红棕色气体.
①确认A中产生气体含有NO,依据的现象是_____________________________.
②装置E的作用是_______________________________________________________
(3)如果向D中通入过量O 2 ,则装置B中发生反应的化学方程式为________________.
如果没有装置C,对实验结论造成的影响是______________________________。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是_______________。
(5)工业生产中氮氧化物的排放会造成环境污染,可采用如下方法处理氮氧化物:
CH 4 (g)+2NO 2 (g)=N 2 (g)+CO 2 (g)+2H 2 O(g) △H=-867kJ·mol -1
CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g) △H=-1160kJ·mol -1
则CH 4 将NO 2 还原为NO的热化学方程式为:___________________________. lxakgl1年前1
lxakgl1年前1 -
 知秋一叶123 共回答了16个问题
知秋一叶123 共回答了16个问题 |采纳率100%(1)E D B(2分);检验装置的气密性(1分) (2)①D中出现红棕色气体(2分) ②冷凝,使NO 2 完全液(2分)(3)4NO 2 +O 2 +4NaOH=4NaNO 3 +2H 2 O(2分)水会与NO 2 反应产生NO,影响NO的确定(2 分)
(4)2NaNO 2 +H 2 SO 4 =Na 2 SO 4 +NO 2 ↑+NO↑+H 2 O(2分)
(5) CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H=-574kJ·mol -1 (2分)
本题是实验题。实验题是同学们的难点。也是最难得分的题型。对于实验题,首先需看清楚实验目的是什么。在结合看清实验流程,实验操作,物质检验等知识会穿插其中。这题是一道实验探究题,探究NaNO 2 与H 2 SO 4 的反应。从所给装置中,A显然是发生装置。B是NaOH溶液,可能是除杂装置,C是浓硫酸,显然是干燥装置。D是热水浴,并通入了O 2 ,需要通O 2 检验的是NO气体。E是冷水浴装置。显然是冷却物质。由题中所给2个信息,第一个信息是NO与NO 2 的混合气体与NaOH发生归中反应。第二个信息是NO、NO 2 两种气体的物理性质。从液化的温度来看,显然NO 2 比NO更易液化。A中三颈瓶,采用固液不加热反应,还有一个弹簧夹用来控制通氮气,显然要氮气,目的应是排除氧气。因氧气有氧化性。可能会对实验结果产生干扰。通过上述信息就可以猜测出产生的两种气体可能是NO和NO 2 。
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):
A是发生装置,C是干燥除去水,NO和NO 2 的分离,先分离NO 2 因为更易液化。所以接E,NO 2 分离后再检验NO,需通氧气。接D。观察到气体从无色变成红棕色。所以说明是NO。B是尾气处理。吸收反应后剩余的NO和NO 2 的混合气体。在这里存在几个先后问题,首先NO和NO 2 的检验,根据液化温度判断得到NO 2 更易液化,可以观察到E中有红棕色液体产生。而后NO会和氧气生成NO 2 。对于NO 2 的检验会产生干扰。所以先检验NO 2 。还有一问题就是除水,如果不除去水的话,NO 2 会与H 2 O反应生成NO,所以又会对NO的检验产生干扰,同时也影响NO 2 的检验。还有一问题就是在A中药品反应之前需通氮气将O 2 排出来。否则也会影响NO和NO 2 的检验。装置连接好之后,就是检查装置气密性。
(2)关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后, A中产生红棕色气体。说明生成了NO 2 气体。
①确认A中产生气体含有NO,是在D装置中通O 2 来检验的。观察气体是否变红棕色。
②装置E的作用是冷凝,是使NO 2 完全液化。
(3)如果向D中通入过量O 2 ,不存在NO剩余,但有过量的O 2 会与NO 2 发生氧化还原反应,O 2 降低,NO 2 升高,所以可推断出反应方程式为:4NO 2 +O 2 +4NaOH=4NaNO 3 +2H 2 O。如不干燥,水会与NO 2 反应产生NO,影响NO的确定。
(4)通过上述实验探究过程,可得出装置A中反应应产生两种气体。+3价氮元素发生歧化反应。化学方程式是2NaNO 2 +H 2 SO 4 =Na 2 SO 4 +NO 2 ↑+NO↑+H 2 O。
(5)工业生产中氮氧化物的排放会造成环境污染,可采用如下方法处理氮氧化物:
CH 4 (g)+2NO 2 (g)=N 2 (g)+CO 2 (g)+2H 2 O(g)△H=-867kJ·mol -1
CH 4 (g)+4NO(g)=2N 2 (g)+CO 2 (g)+2H 2 O(g)△H=-1160kJ·mol -1
根据盖斯定律上式×2-下式可得出:CH 4 (g)+4NO 2 (g)=4NO(g)+CO 2 (g)+2H 2 O(g)△H=-574kJ·mol -1 (2分)1年前查看全部
- 2014届苏锡常镇三模语文,英语,
 雨中沉思ing1年前0
雨中沉思ing1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 南昌市2014届九年级第一次大联考数学、英语、.
 光头狗蛋1年前1
光头狗蛋1年前1 -
 MimiM313 共回答了14个问题
MimiM313 共回答了14个问题 |采纳率92.9%额,怎么可能有,你给问题,我帮你看.1年前查看全部
- 2014届虹口区的数学一模是什么时候?
2014届虹口区的数学一模是什么时候?
题目和答案什么时候可以看到? rmccc1年前1
rmccc1年前1 -
 xiaogaangel 共回答了20个问题
xiaogaangel 共回答了20个问题 |采纳率90%考完以后一个星期1年前查看全部
- 非常急有没有谁有2014届广雅、执信、六中高三下学期2月联考文科综合题地理部分的答案解析啊.十万火急,求大神发力.
 love198601年前1
love198601年前1 -
 法语大片 共回答了17个问题
法语大片 共回答了17个问题 |采纳率88.2%解析好像木有 我把试卷答案发给你
假如有地理题搞不懂 直接贴题出来 我来给你说
我教地理的 哈哈哈哈哈1年前查看全部
- (2014届北京市门头沟区第一学期期末试题)下列关于右图所示实验的说法,正确的是
(2014届北京市门头沟区第一学期期末试题)下列关于右图所示实验的说法,正确的是
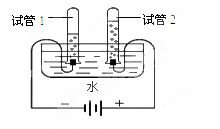
A.试管1和试管2中气体质量比为2:1 B.试管1中的气体是氢气 C.试管1和试管2中气体体积比为1:2 D.该实验证明水是由氢气和氧气组成的  yxqvip1年前1
yxqvip1年前1 -
 shanghaiboom 共回答了18个问题
shanghaiboom 共回答了18个问题 |采纳率100%B
1年前查看全部
大家在问
- 1数学拓展题:我最爱解方程*数=最爱解方程我 每个汉字代表什么数字
- 2两辆汽车同时从AB两地相向而行,甲的速度40千米每时,乙50千米每时,两车在距中点20千米处相遇,
- 3求下列各数的平方根与算术平方根:64分之25,10付六次幂,2又49分支46,根号81²
- 4已知双曲线中心在原点,离心章e=2,实轴在坐标轴上,且焦点到渐近线距离为3,求双曲线标准方程伫和渐近...
- 5只用因为,怎么造句
- 6英语翻译Stainless Steel,Titanium,Nickel,Nickel Alloys and certai
- 7老师说世界上有一种动物由黑白色组成,请问是什么马.
- 8安塞腰鼓的声音,可以用什么来形容
- 9阅读下列材料:材料一 东汉桓帝、灵帝时的童谣说:“举秀才,不知书;举孝廉,父别居。寒素清白浊如泥,高第(门第)良将怯如鸡
- 10化石吟诗歌运用什么手法写的,这样写有什么好处?
- 11在她的帮助下,我们的英语特别是口语进步很快“翻译成英语
- 12化合价与离子符号的关系
- 13若x的m次方乘X的2m次方等于2,求X的9m次方
- 14求一片英语作文!高分!座天使周日,用英语写出你及你的家人这一天的主要活动.要求用一般过去时,字数60以上.本人必重谢!最
- 15英语翻译说出个大致客套话的意思就好了.送别.






