赤热炎炎,在沙漠里即使相距不太远的人也难以听清对方的大声叫喊,则声音传播时向哪里拐弯?
 鸭子612022-10-04 11:39:541条回答
鸭子612022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 huibeauty319 共回答了24个问题
huibeauty319 共回答了24个问题 |采纳率87.5%- 并没有转弯,声音其实是像球面一样向外发散的,沙漠空旷,单位面积剩余的声音能量很少,城市里,建筑反射有加强部分方向上单位能量的作用,所以,在沙漠中不太听的清.而并非转弯.
- 1年前
相关推荐
- 如下变化关系所示,常温下B为液体C为气体D为固体 A加热生成B C D B通电生成E F C通过赤热的碳层生成G G
如下变化关系所示,常温下B为液体C为气体D为固体 A加热生成B C D B通电生成E F C通过赤热的碳层生成G G
如下变化关系所示,常温下B为液体C为气体D为固体 A加热生成B C D B通电生成E F C通过赤热的碳层生成G G+D(加热)生成铜 推断B C D
写出A受热的化学方程式 liutongji801年前2
liutongji801年前2 -
 人在兰州 共回答了29个问题
人在兰州 共回答了29个问题 |采纳率79.3%水,二氧化碳,氧化铜1年前查看全部
- 用天然气和水煤气(主要成分是CO和H 2 )代替蜂窝煤作燃料可明显改善城市空气质量,工业上用水蒸气通过赤热的炭来制取水煤
用天然气和水煤气(主要成分是CO和H 2 )代替蜂窝煤作燃料可明显改善城市空气质量,工业上用水蒸气通过赤热的炭来制取水煤气。
回答下列问题:
(1)写出工业上制取水煤气的化学方程式,并注明反应类型。反应方程式__________________;反应类型___________。
(2)空气质量日报中常列出的主要污染物有:①二氧化硫②二氧化氮③一氧化碳④臭氧⑤可吸入颗粒物
用天然气或水煤气代替蜂窝煤后,上述污染物中明显降低的是__________(填序号)。
(3)送入居民家中的天然气、水煤气中常加入一种有臭味的物质(乙硫醇),其作用是______________。
(4)用天然气、水煤气代替蜂窝煤作燃料,除明显改善空气质量外,还具有的优点是_________、_________ (任答两点)。 一休vv1年前0
一休vv1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2009•常州模拟)在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
(2009•常州模拟)在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
(1)猜想与假设
甲认为有H2、CO生成;
乙认为有H2、CO、CO2生成;
丙认为除有H2、CO、CO2外,可能还有N2生成.
探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是______.
(2)设计与实验
甲乙同学为了证明他们的猜想是正确的,设计了如如图所示的实验装置:
(提示:无水硫酸铜遇到水变蓝色,H2和CuO反应生成Cu和H2O,CO与CuO反应的原理与工业炼铁的反应原理相似.)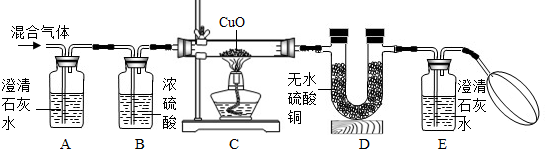
①证明混合气体中含有H2,相应的反应现象是______;
②证明混合气体中含有CO,相应的反应现象是______;
③证明混合气体中含有CO2,相应的反应现象是______.
(3)理论与思考
①写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式C+H2O
H2+CO高温 .C+H2O;
H2+CO高温 .
②丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装______溶液,才能弥补上述设计的不足. 我爱红桃81年前1
我爱红桃81年前1 -
 shenzhou12 共回答了20个问题
shenzhou12 共回答了20个问题 |采纳率95%解题思路:(1)根据质量守恒定律回答.
(2)根据H2、CO和氧化铜反应的产物和无水硫酸铜遇水变蓝色,以及二氧化碳能使澄清的石灰水变浑的性质回答.
(3)①根据甲的猜想,判断反应物、生成物和反应条件,再写出方程式;②根据氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好的情况回答.(1)根据质量守恒定律,化学反应前后元素的种类不变,反应物中没有N元素,根据质量守恒定律不可能生成N2.
(2)①氢气和氧化铜在加热的条件下反应生成铜和水,一氧化碳与氧化铜反应生成铜和二氧化碳,如混合气体中含有H2,则
D中无水硫酸铜变蓝.
②一氧化碳与氧化铜反应生成铜和二氧化碳,如证明混合气体中含有一氧化碳,A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊.
③二氧化碳能使澄清的石灰水变浑,如混合气体中含有CO2,则A中澄清石灰水变浑浊.
(3)①甲认为在高温下炽热的焦炭能与水蒸气发生反应,其反应后的生成物有H2、CO,所以方程式为:C+H2O
高温
.
H2+CO.
②氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好,在A、B装置之间再加一个洗气瓶,内装吸收二氧化碳能力较强的氢氧化钠溶液更好.
故答案为:(1)反应物中没有N元素,根据质量守恒定律不可能生成N2;
(2)①无水硫酸铜变蓝色;②A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊;③A中澄清石灰水变浑浊;
(3)①C+H2O
高温
.
H2+CO;②NaOH.点评:
本题考点: 常见气体的检验与除杂方法;二氧化碳的化学性质;一氧化碳的化学性质;水的性质和应用;书写化学方程式、文字表达式、电离方程式;氢气的化学性质与燃烧实验.
考点点评: 气体的检验和除杂是初中化学实验的重点内容之一,是学生应掌握的基本技能,也是化学实验考查的热点之一,首先要熟悉气体的性质,并能利用其性质对它进行检验、鉴别,能利用气体间性质的差别进行分离和除杂;特别是石灰水、氢氧化钠溶液、浓硫酸、无水硫酸铜在气体制取和检验中的作用.1年前查看全部
- 描写“热”的词语有哪些?除了:火热,灼热,炙热,炽热,酷热,暴热,暑热,燥热,闷热,湿热,溽热,赤热,毒热。还有哪些同类
描写“热”的词语有哪些?
除了:火热,灼热,炙热,炽热,酷热,暴热,暑热,燥热,闷热,湿热,溽热,赤热,毒热。还有哪些同类的?急用 lovelou111年前1
lovelou111年前1 -
 虎皮兔55 共回答了17个问题
虎皮兔55 共回答了17个问题 |采纳率88.2%炎热1年前查看全部
- (2008•宝山区二模)工业上用赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物中含有H2O,H2,CO,CO2等物质.
(2008•宝山区二模)工业上用赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物中含有H2O,H2,CO,CO2等物质.课外兴趣n组的同学设计i下实验装置,用来证明水煤气中含有H2和CO,请根据下图回答有关问题:(装置图中省去了铁架台)
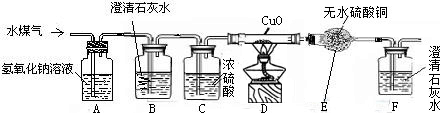
(9)装置A、B、C的作用分别是______、______、______.
(2)证明水煤气中有H2的现象是______.
(3)D装置中发生反应的化学方程式为 H2+CuO
Cu+H2O CO+CuO△ .
Cu+CO2△ .
(0)该装置的设计,有一处明显的不足,应i何改进?
答:______. 20218131年前1
20218131年前1 -
 良班黄瓜 共回答了10个问题
良班黄瓜 共回答了10个问题 |采纳率90%解题思路:根据一氧化碳、氢气还原氧化铜的反应原理及操作注意事项分析;
根据浓硫酸、氢氧化钠溶液、澄清石灰水的用途作答.(2)赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物6含有H2O,H2,CO,CO2等物质,现在做该实验的目的是为5证明水煤气6含有H2和CO,所以在验证水煤气的成分前需要把H2O、CO2除去,氢氧化钠能吸收二氧化碳,浓硫...
点评:
本题考点: 常见气体的检验与除杂方法;二氧化碳的化学性质;一氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 在做实验时需注意:通入高温试管中的气体必须是干燥的,若不干燥,很可能炸裂试管,潮湿的气体在通入高温试管前必须经干燥剂干燥.1年前查看全部
- 将空气与CO2按5:1体积比混合,跟足量的赤热焦炭充分反应.
将空气与CO2按5:1体积比混合,跟足量的赤热焦炭充分反应.
(1)写出有关的化学方程式.
(2)若反应前后的温度相同,求反应后所得气体中CO的体积分数. lj5551年前0
lj5551年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2004•黄冈)在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,甲、乙、丙三位同学作了如下猜想:甲认为有H2
(2004•黄冈)在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,甲、乙、丙三位同学作了如下猜想:甲认为有H2、CO生成;乙认为有H2、CO、CO2生成;丙认为除有H2、CO、CO2外,可能还有其它的含碳化合物生成.
(1)探究小组组长丁认为三位同学的猜想均存在其合理性,请你从原子--分子论的观点解释他们猜想的合理性.______.
(2)乙同学为了证明他的猜想是正确的,设计了如下实验,实验装置图如下: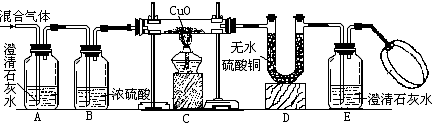
请运用你所学到的化学知识评价乙同学设计的实验原理的合理性:______. a绿蔷薇a1年前1
a绿蔷薇a1年前1 -
 osamama 共回答了23个问题
osamama 共回答了23个问题 |采纳率87%解题思路:根据质量守恒定律可知反应前后元素种类是不变的,再根据反应物的元素组成可推出生成物的可能元素组成,再根据澄清石灰水具有检验二氧化碳的性质,浓硫酸具有吸水性,无水硫酸铜可以吸水来分析它的合理性即可.(1)质量守恒定律的实质是在反应前后原子的数目没有增减,原子的种类没有改变,原子的质量没有变化,所以三位同学的猜想均存在其合理性;
(2)先通过澄清石灰水是检验是否有二氧化碳的,通过浓硫酸是为了除水的,通过氧化铜是看气体是否具有还原性的,再通过无水硫酸铜如果变蓝说明有水生成,就说明有氢气,再通过澄清石灰水如果变浑浊,说明有一氧化碳.所以说乙同学设计的探究实验原理是合理的.
故答案为:(1)化学反应前后元素种类没有改变,原子个数没有增减.但反应后的生成物是否存在,必须用实验进一步探究验证.
(2)①观察A中澄清石灰水的变化情况可检验混合气中是否有CO2; ②观察C中灼热的氧化铜和D中的无水硫酸铜的变化情况可检验混合气中是否有H2;③观察C中灼热的氧化铜和E中澄清的石灰水的变化情况可检验混合气中是否有CO;故乙同学设计的探究实验原理是合理的.点评:
本题考点: 常见气体的检验与除杂方法;猜想与事实验证.
考点点评: 通过回答本题知道了除去水分用浓硫酸,验证水分用无水硫酸铜,验证二氧化碳用澄清石灰水,验证氢气和一氧化碳时将气体通过氧化铜再检验是否有水和二氧化碳生成.1年前查看全部
- 下列反应属于吸热反应的是( ) A.二氧化碳与赤热的碳反应生成一氧化碳 B.葡萄糖在人体内氧化分解 C.Ba(OH)
下列反应属于吸热反应的是( ) A.二氧化碳与赤热的碳反应生成一氧化碳 B.葡萄糖在人体内氧化分解 C.Ba(OH) 2 •8H 2 0与NH 4 Cl反应 D.锌粒与稀H 2 S0 4 反应制取H 2  fbi_8611年前1
fbi_8611年前1 -
 鱼游沙漠 共回答了17个问题
鱼游沙漠 共回答了17个问题 |采纳率82.4%A、二氧化碳与赤热的碳反应生成一氧化碳属于吸热反应,故A正确;
B、葡萄糖在人体内氧化分解的反应是放热反应,故B错误;
C、Ba(OH) 2 •8H 2 0与NH 4 Cl反应是吸热反应,故C正确;
D、锌粒与稀H 2 S0 4 反应是常见放热反应,故D错误;
故选AC.1年前查看全部
- 高温下,向1mol 赤热的硫化亚铜中通入足量的水蒸气,生成2mol 氢气,同时还生成金属铜和一种刺激
高温下,向1mol 赤热的硫化亚铜中通入足量的水蒸气,生成2mol 氢气,同时还生成金属铜和一种刺激性气味的气体.
(1)该反应的化学方程式是Cu2S+2H2O(g)
2Cu+2H2+SO2,高温 .Cu2S+2H2O(g).
2Cu+2H2+SO2,高温 .
(2)该反应中氧化产物是______.
(3)每生成1mol H2,氧化剂与还原剂之间转移的电子是______mol. jack-1231年前1
jack-1231年前1 -
 绛_尜舞 共回答了20个问题
绛_尜舞 共回答了20个问题 |采纳率85%解题思路:(1)根据反应前后元素守恒判断该刺激性气味的气体是二氧化硫,然后根据反应物、生成物和反应条件写出反应方程式;
(2)还原剂对应的产物是氧化产物;
(3)根据氢气与转移电子之间的关系式计算.(1)同一化学反应中,参加反应的各物质的量之比等于计量数之比;根据反应前后各元素的原子守恒知,1mol 赤热的硫化亚铜中通入足量的水蒸气,生成2mol 氢气,需要2mol水蒸气参加反应,生成2mol铜,所以生成的一种刺激性气味的气体是二氧化硫;所以该反应中反应物是硫化亚铜和水蒸气,生成物是铜、氢气和二氧化硫,反应条件是高温,
故答案为:Cu2S+2H2O(g)
高温
.
2Cu+2H2+SO2;
(2)Cu2S+2H2O(g)
高温
.
2Cu+2H2+SO2,该反应中各元素的化合价变化为:Cu2S→SO2,硫元素由-2价变为+4价,所以硫元素被氧化,氧化产物是二氧化硫;Cu2S→Cu,铜元素的化合价由+1价变为0价,所以铜元素被还原,还原产物是铜;H2O→H2,氢元素的化合价由+1价变为0价,所以氢元素被还原,还原产物是氢气,
故答案为:SO2;
(3)设转移电子为xmol,
Cu2S+2H2O
高温
.
2Cu+2H2+SO2 转移电子
2mol 6mol
1mol x
所以x=3
故答案为:3.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应方程式的书写、氧化产物的判断等知识点,难度不大,明确氧化剂对应的产物还原产物,还原剂对应的产物是氧化产物.1年前查看全部
- 在高温下赤热的焦炭能与水蒸气反应,对其反应后的生成物化学小组的同学提出了可能生成氢气,一氧化碳和二氧化碳的猜想,为了验证
在高温下赤热的焦炭能与水蒸气反应,对其反应后的生成物化学小组的同学提出了可能生成氢气,一氧化碳和二氧化碳的猜想,为了验证这种猜想设计了如下装置. 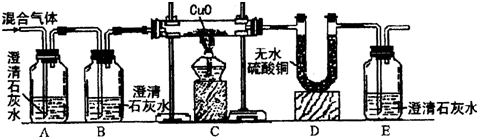
请回答下列问题
(1)A瓶中溶液变浑浊说明______;B瓶中溶液不浑浊说明______.
(2)当C中玻璃管中出现红色后,D中u型管中物质变蓝是因为白色无水硫酸铜遇水变成蓝色硫酸铜晶体,但这一现象不能说明生成物中有氢气,原因是______
(3)E瓶中溶液变浑浊说明______.
(4)尾气排放到空气中会造成朽染,改进的方法是______. blueflyfish1年前1
blueflyfish1年前1 -
 hmlaree 共回答了23个问题
hmlaree 共回答了23个问题 |采纳率100%(1)A瓶中装有氢氧化钙溶液,所给的气体中只有二氧化碳能使其变浑浊,所以可以知道该气体中含有二氧化碳,而B瓶中不变浑浊,则说明二氧化碳已被完全吸收;
(2)虽然氢气还原氧化铜生成的水会使无水硫酸铜变蓝,但是在之前气体接触了溶液,会干扰现象,所以不能确定水是反应中生成的还是从AB中带出的,故不能判断是否含有氢气;
(3)E瓶中溶液变浑浊说明反应中生成了二氧化碳,进而可以判断在混合气体中含有一氧化碳;
(4)为了防止污染空气,应该将尾气进行收集或是利用一氧化碳的可燃性来进行点燃.
故答案为:(1)混合气体中有CO 2 气体;CO 2 已被A瓶全部吸收;
(2)气体通过A、B两瓶后可能带出水蒸气;
(3)还原后生成了CO 2 ,说明原混合气体中有CO;
(4)用酒精灯将尾气中的CO气体燃烧掉(或其他合理方法均可).1年前查看全部
- 工业上用赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物中含有H 2 O、H 2 、CO、CO 2 等物质。课外兴趣小组
工业上用赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物中含有H 2 O、H 2 、CO、CO 2 等物质。课外兴趣小组的同学设计如下实验装置,用来证明水煤气中含有H 2 和CO,请根据下图回答有关问题:(装置图中省去了铁架台) 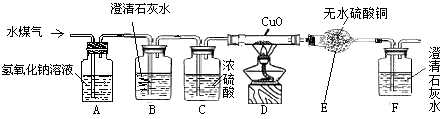
(1)装置A、B、C的作用分别是________________ 、_________________ 、___________________ 。
(2)证明水煤气中有H 2 的现象是________________ 。
(3)D装置中发生反应的化学方程式为 _______________________。
(4)该装置的设计,有一处明显的不足,应如何改进_____________________ 。 erhjngftrj1年前1
erhjngftrj1年前1 -
 唐陵魂 共回答了13个问题
唐陵魂 共回答了13个问题 |采纳率84.6%1年前查看全部
- 在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
(1) 猜想与假设甲认为有H 2 . CO生成;乙认为有H 2 、CO、CO 2 生成;丙认为除有H 2 、CO、CO 2 外,可能还有N 2 生成。探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是____________。
(2) 设计与实验 甲乙同学为了证明他们的猜想是正确的,设计了如下图所示的实验装置: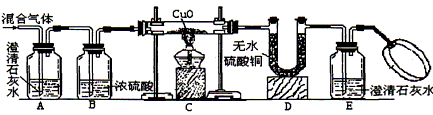
(提示:无水硫酸铜遇到水变蓝色,H 2 和CuO反应生成Cu和H 2 O,CO与CuO反应的原理与工业炼铁的反应原理相似。)
① 证明混合气体中含有H 2 ,相应的反应现象是_________________________;
② 证明混合气体中含有CO,相应的反应现象是_______________________;
③ 证明混合气体中含有CO 2 ,相应的反应现象是_______________________。
(3) 理论与思考
① 写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式__________________;
② 丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装________溶液,才能弥补上述设计的不足。 loveruru2091年前1
loveruru2091年前1 -
 weiwan1314 共回答了20个问题
weiwan1314 共回答了20个问题 |采纳率95%1年前查看全部
- 在高温下赤热的焦炭能与水反应,对其反应后的生成物化学小组的同学提出了“可能生成氢气、一氧化碳和二氧化碳”的猜想,为了验证
在高温下赤热的焦炭能与水反应,对其反应后的生成物化学小组的同学提出了“可能生成氢气、一氧化碳和二氧化碳”的猜想,为了验证这种猜想设计了如下装置.
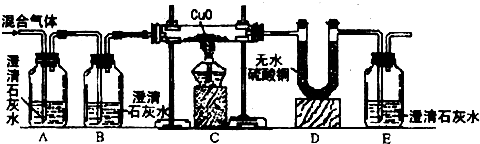
请根据以下实验现象作出合理判断:
(1)A瓶中溶液变浑浊说明______;
(2)B瓶中溶液不变浑浊说明______.
(3)C中玻璃管内出现红色,且D中U形管内物质变蓝,但是这些现象并不能说明生成物中有氢气,原因是______.
(4)E瓶中溶液变浑浊说明______.
(5)根据上述实验现象确定,赤热的焦炭与水反应的生成物中一定存在______,其中一定发生了的某一反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O或CuO+CO
Cu+CO2△ .CO2+Ca(OH)2═CaCO3↓+H2O或CuO+CO.
Cu+CO2△ .
(6)该实验可能对环境有污染,针对性的改进方法是______. bbf171年前1
bbf171年前1 -
 xml_jing 共回答了15个问题
xml_jing 共回答了15个问题 |采纳率93.3%解题思路:(1)根据检验二氧化碳常用澄清石灰水进行解答;
(2)根据B瓶中溶液不变浑浊说明二氧化碳已被完全吸收进行解答;
(3)根据氢气还原氧化铜生成的水会使无水硫酸铜变蓝,但是在之前气体接触了溶液,会干扰现象,可以据此解答;
(4)根据一氧化碳还原氧化铜生成的二氧化碳会使澄清石灰水变浑浊的性质检验完成解答;
(5)根据上述现象可知焦炭与水反应的生成物中一定存在二氧化碳和一氧化碳以及二氧化碳和石灰水反应生成碳酸钙沉淀和水或一氧化碳和氧化铜反应生成铜和二氧化碳进行解答;
(6)对尾气可以进行收集或点燃,可以据此解答.(1)A瓶中装有氢氧化钙溶液,所给的气体中只有二氧化碳能使其变浑浊,所以可以知道该气体中含有二氧化碳;故填:混合气体中有CO2气体;
(2)而B瓶中不变浑浊,则说明二氧化碳已被完全吸收;故填:CO2已被A瓶全部吸收;
(3)虽然氢气还原氧化铜生成的水会使无水硫酸铜变蓝,但是在之前气体接触了溶液,会干扰现象,所以不能确定水是反应中生成的还是从AB中带出的,故不能判断是否含有氢气;故填:气体通过A、B两瓶后可能带出水蒸气;
(4)E瓶中溶液变浑浊说明反应中生成了二氧化碳,进而可以判断在混合气体中含有一氧化碳;故填:生成物中含有CO;
(5)根据上述现象可知焦炭与水反应的生成物中一定存在二氧化碳和一氧化碳;二氧化碳和石灰水反应生成碳酸钙沉淀和水,反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;一氧化碳和氧化铜反应生成铜和二氧化碳,反应的化学方程式为CuO+CO
△
.
Cu+CO2;故填:CO2、CO;CO2+Ca(OH)2═CaCO3↓+H2O或CuO+CO
△
.
Cu+CO2;
(6)为了防止污染空气,应该将尾气进行收集或是利用一氧化碳的可燃性来进行点燃.
故答案为:用酒精灯将尾气中的CO气体燃烧掉.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法.
考点点评: 气体的检验和除杂是初中化学实验的重点内容之一,是学生应掌握的基本技能,也是化学实验考查的热点之一,首先要熟悉气体的性质,并能利用其性质对它进行检验、鉴别,能利用气体间性质的差别进行分离和除杂;特别是石灰水、氢氧化钠溶液、浓硫酸、无水硫酸铜在气体制取和检验中的作用.1年前查看全部
- 将空气与CO2按5∶1体积比混合,跟足量的赤热焦炭充分反应后,若反应前后的温度相同,则在所得气体中,CO的体积分数为(假
将空气与CO2按5∶1体积比混合,跟足量的赤热焦炭充分反应后,若反应前后的温度相同,则在所得气体中,CO的体积分数为(假设空气中氮气、氧气的体积比为4∶1,其他成分可忽略不计) ( )
A、29% B、43% C、50% D、100% TU70091年前1
TU70091年前1 -
 lakexiu 共回答了29个问题
lakexiu 共回答了29个问题 |采纳率82.8%C
其实有足量的热焦炭就代表所有的氧元素全部转化成为CO,由题目可以知道氧元素和氮元素的mol比例为2:1,全部转化后,N2与CO的比例为1:1,那么就是50%1年前查看全部
- 1.某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行):①通过赤热的炭层后,
1.某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行):①通过赤热的炭层后,恢复到原状态,气体体积不变;②通过灼热的CuO时,固体变成红色;③通入澄清石灰水中,石灰水变浑浊;④通过白色CuSO4粉末时,粉末变成蓝色晶体(白色CuSO4粉末遇水变蓝色).下列判断正确的是( )
A.原混合气体中一定含有CO2、CO、H2
B.原混合气体中一定含有CO,可能含有H2,一定没有CO2
C.原混合气体中一定含有H2和CO,一定没有CO2
D.原混合气体中一定含有CO,可能含有H2和CO2
2.1.6g某物质在空气中完全燃烧生成4.4g二氧化碳和3.6g水,则关于这种物质的组成描述不正确的是( )
A.该物质只含有碳元素和氢元素 B.该物质中碳元素与氢元素 的质量比是3:1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质的分子中碳原子与氢原子的个数比是1:4 爱乔米妖1年前2
爱乔米妖1年前2 -
 娃哈哈y238 共回答了17个问题
娃哈哈y238 共回答了17个问题 |采纳率88.2%1.B
①CO2+C→高温2CO,体积变大,无CO2
②说明有还原性气体
③说明有CO2(由CO+CuO→高温Cu+CO2而来)
④不能说明有H2,因为先通入澄清石灰水,带有H2O气体
2.C
4.4g二氧化碳含C元素1.2g,3.6g水含H元素0.4g
该物质为CH4,不含O1年前查看全部
- 利用氨气和赤热的氧化铜反应,生成了氮气、铜和水,化学方程式可表示为什么?
利用氨气和赤热的氧化铜反应,生成了氮气、铜和水,化学方程式可表示为什么?
利用氨气和赤热的氧化铜反应,生成了氮气、铜和水,化学方程式可表示为_____________________,推测反应中发生的现象是____________________反应前后铜元素的化合价由___价变为___价. livilyxu1年前4
livilyxu1年前4 -
 lalahooo 共回答了26个问题
lalahooo 共回答了26个问题 |采纳率84.6%利用氨气和赤热的氧化铜反应,生成了氮气、铜和水,化学方程式可表示为_3CuO+2NH3=(加热)3Cu+N2↑+3H2O _,推测反应中发生的现象是 黑色固体变红 反应前后铜元素的化合价由+2价变为0价.1年前查看全部
- 某无色气体可能含有CO2,CO,H2中的一种或几种,依次进行以下实验:(1)通过赤热的碳层后,恢复到原状态,气体体积不变
某无色气体可能含有CO2,CO,H2中的一种或几种,依次进行以下实验:(1)通过赤热的碳层后,恢复到原状态,气体体积不变;(赤热的碳层是什么意思,化学方程式怎么表达?)
 琼1231年前6
琼1231年前6 -
 e6j1 共回答了19个问题
e6j1 共回答了19个问题 |采纳率94.7%高温加热下与C反应 具体点就是:
CO2+C=2CO;
CO不和C反应;
H2不和C反应;1年前查看全部
- 在下列反应中,氧化产物与还原产物是同一种物质的是 A.二氧化碳通过赤热的碳层
在下列反应中,氧化产物与还原产物是同一种物质的是 A.二氧化碳通过赤热的碳层
B.氧化铜和木炭在高温下反应 C.氢气通过灼热的氧化铜 D.一氧化碳通过高温的赤铁矿 娃哈哈pg1年前3
娃哈哈pg1年前3 -
 wdxysyx 共回答了21个问题
wdxysyx 共回答了21个问题 |采纳率95.2%本题答案选A.生成物只有二氧化碳一种物质,所以二氧化碳既是氧化产物,又是还原产物.
B.氧化铜和木炭在高温下反应
氧化产物是二氧化碳,还原产物是铜.
C.氢气通过灼热的氧化铜
氧化产物是水,还原产物是铜.
D.一氧化碳通过高温的赤铁矿
氧化产物是二氧化碳,还原产物是铁.
理解请及时采纳!祝你进步!1年前查看全部
- 在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
(1)猜想与假设
甲认为只有H2、CO生成;
乙认为有H2、CO、CO2生成;
丙认为除有H2、CO、CO2外,可能还有N2生成.
探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是______.
(2)设计实验
甲乙同学为了证明他们的猜想是正确的,设计了如图所示的实验装置:
(提示:无水硫酸铜遇到水变蓝色.)
①A中澄清石灰水变浑浊,说明混合气体中含有______;
②证明混合气体中含有H2,相应的反应现象是______;
③证明混合气体中含有CO,相应的反应现象是______.
(3)反思与评价
①写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式C+H2O
CO+H2高温 .C+H2O;
CO+H2高温 .
②丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装______溶液,才能弥补上述设计的不足. 高冬1年前1
高冬1年前1 -
 喝闷酒 共回答了23个问题
喝闷酒 共回答了23个问题 |采纳率100%解题思路:(1)根据质量守恒定律的微观解释分析解答,化学反应前后元素的种类不变,
(2)①检验二氧化碳常用澄清石灰水,
②根据氢气还原氧化铜生成的水会使无水硫酸铜变蓝的性质检验,
③根据一氧化碳还原氧化铜生成的二氧化碳会使澄清石灰水变浑浊的性质检验,
(3)①结合反应物、生成物和反应条件书写方程式,
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对一氧化碳的检验产生影响.(1)在化学反应前后,元素的种类是不发生改变的,反应前的物质中没有氮元素,生成物中也不会有氮元素,所以水和碳反应后不会生成氮气;
故答案为:质量守恒定律;
(2)①二氧化碳能使澄清石灰水变浑浊,根据石灰水变浑浊的现象,可以确定混合其中存在二氧化碳,故答案为:CO2;
②水能够使无水硫酸铜变蓝,氢气和氧化铜反应会生成水,只要D中的无水硫酸铜变蓝,就证明水的存在,也证明了混合气中有氢气;
故答案为:D中硫酸铜变成蓝色物质;
③二氧化碳能使澄清石灰水变浑浊,一氧化碳和氧化铜反应会生成二氧化碳,只要澄清石灰水变浑浊,证明了二氧化碳的存在,也证明了混合气中有一氧化碳;
故答案为:E中澄清石灰水变浑浊;
(3)①根据焦炭和水在高温条件下生成氢气和一氧化碳,书写化学方程式,故答案为:C+H2O
高温
.
CO+H2;
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对后面的一氧化碳的检验产生影响,氢氧化钠吸收二氧化碳比较完全,故答案为:NaOH.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了常见气体的检验和除杂方法,以及质量守恒定律在在化学方程式中的应用.1年前查看全部
- 用天然气和水煤气(主要成分是CO和H2)代替蜂窝煤作燃料可明显改善城市空气质量,工业上用水蒸气通过赤热的炭来制取水煤气.
用天然气和水煤气(主要成分是co和h2)代替蜂窝煤作燃料可明显改善城市空气质量,工业上用水蒸气通过赤热的炭来制取水煤气.回答下列问题.
(1)写出工业上制取水煤气的化学方程式,并注明反应类型:反应方程式c+h2o
co+h2高温 .c+h2o,反应类型______.
co+h2高温 .
(2)空气质量日报中常列出的主要污染物有:①二氧化硫 ②二氧化氦 ③一氧化碳 ④臭氧 ⑤可吸人颗粒物.用天然气或水煤气代替蜂窝煤后,上述污染物中明显降低的是______(填***)
(3)送入居民家史的天然气、水煤气中常加入一种有臭味的物质(硫醇),其作用是:______.
(4)用天然气、水煤气代替蜂窝煤作燃料,除明显改善空气质量外,还具有的优点是:______. liona_hu1年前1
liona_hu1年前1 -
 saldek 共回答了14个问题
saldek 共回答了14个问题 |采纳率78.6%解题思路:根据反应物和生成物及其质量守恒定律可以书写化学方程式,可以判断物质的反应类型,根据天然气或水煤气燃烧的生成物方面可以判断污染物的变化情况,天然气、水煤气代替蜂窝煤作燃料有许多优点:改善空气质量,提高燃料利用率,减少空气污染物等.(1)水蒸气通过赤热的炭来制取水煤气的化学方程式为:C+H2O
高温
.
CO+H2.
(2)天然气或水煤气燃烧的生成物中二氧化硫、二氧化氮、可吸入颗粒物的含量明显降低.故填:①②⑤.
(3)因为天然气是无色、无味的气体,泄漏时不容易察觉,加入一种有臭味的物质(硫醇)后,如果天然气泄漏容易及时发觉.故填:发生泄漏时报警.
(4)用天然气、水煤气代替蜂窝煤作燃料,除明显改善空气质量外,还具有的优点是:提高燃料利用率,减少空气污染物等.点评:
本题考点: 常用燃料的使用与其对环境的影响;反应类型的判定;书写化学方程式、文字表达式、电离方程式;资源综合利用和新能源开发;易燃物和易爆物安全知识.
考点点评: 解答本题要掌握化学方程式的书写方法和节能环保的重要性,只有这样才能对问题做出正确的判断.1年前查看全部
- 求作业方程式.现有氮气,氢气,二氧化碳,一氧化碳,水蒸气五种气体,将他门依此通过赤热的焦炭,灼热的氧化铜,饱和石灰水溶液
求作业方程式.
现有氮气,氢气,二氧化碳,一氧化碳,水蒸气五种气体,将他门依此通过赤热的焦炭,灼热的氧化铜,饱和石灰水溶液,浓硫酸(做干燥剂,吸收水分),若每一步都完全反应,则最后剩下的气体是?过程中的化学方程式是什么? 人在他乡001年前2
人在他乡001年前2 -
 冰雹QQ 共回答了16个问题
冰雹QQ 共回答了16个问题 |采纳率87.5%跟在符号后面的数字是下标……
第一步:C+CO = CO2 ,除去CO;
第二步:CuO + H2 = Cu + H2O 除去 H2
第三步:Ca(OH)2 + CO2 = CaCO3 + H2O 除去 CO2
第四步:浓硫酸吸水,除去水蒸气;
剩下的是N2(氮气).1年前查看全部
- 化学问题 工业上将苯的蒸气通过赤热的铁合成一种可做传热载体的化合物.该化合物分子中苯环上的一氯代物有3种,1mol该化合
化学问题 工业上将苯的蒸气通过赤热的铁合成一种可做传热载体的化合物.该化合物分子中苯环上的一氯代物有3种,1mol该化合物催化加氢时最多消耗6mol氢气.这种化合物可能是?
 kokodea1年前1
kokodea1年前1 -
 帅气萧萧 共回答了22个问题
帅气萧萧 共回答了22个问题 |采纳率90.9%应该是联苯
肯定是有苯环构成的
一个苯环催化加氢时最多消耗3mol氢气,所以有两个苯环,那为什么不是萘呢?因为萘的一氯代物只有两种,所以应该是联苯1年前查看全部
- 要除去CO2中少量的CO,A将气体点燃 B将气体通入石灰水 C将气体通过赤热的炭层 D将气体通入灼热的CUO
要除去CO2中少量的CO,A将气体点燃 B将气体通入石灰水 C将气体通过赤热的炭层 D将气体通入灼热的CUO
有助于回答者给出准确的答案 zhqdx1年前3
zhqdx1年前3 -
 拉呀啦 共回答了6个问题
拉呀啦 共回答了6个问题 |采纳率100%D将气体通入灼热的CUO(氧化还原反应,CO变成了CO2)
A将气体点燃 引进了新的杂质 O2
B将气体通入石灰水 除去了CO2而不是CO
C将气体通过赤热的炭层 除去了CO2并且生成了 CO1年前查看全部
大家在问
- 1设曲线y=(ax-1)•ex在点A(x0,y1)处的切线为l1,曲线y=(1-x)•e-x在点A(x0,y2)处的切线为
- 2XX中心小学翻译成英语该怎么写?
- 3(2009•株洲)继“分子足球”C60之后,科学家又发现另一种“分子足球”N60. 一定条件下N60中积累的巨
- 4改写单数第三人称,复数第一人称 ,小学六年级上册PEP教材,人民教育出版社,英语书的第一篇课文.急,谢
- 5原子团是由什么组成的假如是由原子组成的那么为什么会带电离子也是原子的一种?
- 6纸上谈兵〔 〕完壁归赵〔 〕背水一战〔 〕精中报国〔 〕负荆请罪〔 〕闻鸡起舞〔 〕
- 7百度百科说“任何置换反应都属于复分解反应”?这句话是对还是错的
- 8求Y=X^3-6X+2的拐点?这道题先求二阶导数,Y=6X,那他的拐点不是(0,可是选项是(0,4);(0,2);(0,
- 9关于Al的方程式 Al三角的化学方程式和离子方程式还有氯化铝和氨水偏铝酸钠和二氧化碳(少量)(过量)氯化铝和偏铝酸钠明矾
- 10求《新目标英语》Go for it!七至九年级课本同步听力,请发到liu914768984@163.com
- 11四道数学题,是大神级的帮个忙一:早上九点时,旗杆的高度与它的影子的长度比是5:4,小明测得学校旗杆的影长为12米,那么学
- 12过两直线3x+2y-3=0与2x+y-6=0的交点和原点的直线方程是?如何确定斜率?
- 13臭氧阻挡紫外线是不是物理性质为什么?
- 14请达人帮忙翻译成英语,非常感谢哈!谢绝翻译软件~
- 151.Chinese students should pay more attention ---- their pron



