二氧化二钠加二氧化硫反应生成什么方程式怎么写
 卖刀杨志12022-10-04 11:39:543条回答
卖刀杨志12022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 闽乡茶缘 共回答了20个问题
闽乡茶缘 共回答了20个问题 |采纳率95%- Na2O2+SO2=Na2SO4
- 1年前
 senllz 共回答了2个问题
senllz 共回答了2个问题 |采纳率- Na2O2+SO2=Na2SO4
生成硫酸钠 - 1年前
 阿弥陀佛3194 共回答了108个问题
阿弥陀佛3194 共回答了108个问题 |采纳率- Na2O2 + SO2 == Na2SO4
(过氧化钠) - 1年前
相关推荐
- 酸雨是pH小于5.6的降水.我国大部分地区所降酸雨的主要原因是由居民和工厂燃烧含硫的煤及某些化工厂生产过程中排放的二氧化
酸雨是pH小于5.6的降水.我国大部分地区所降酸雨的主要原因是由居民和工厂燃烧含硫的煤及某些化工厂生产过程中排放的二氧化硫气体经过一系列化学反应而形成的.
(1)如果硫粉在氧气中燃烧,观察到的现象是产生______色的火焰,其反应的化学方程式为S+O2
SO2点燃 .S+O2.
SO2点燃 .
(2)要检验某工厂废气中是否含有SO2气体,可用KMnO4溶液(SO2能使KMnO4溶液由紫红色变为绿色),化学方程式为:3SO2+K2Cr2O7+H2SO4=K2SO4+X+H2O,则X的化学式为______,反应前K2Cr2O7中Cr元素的化合价为______.
(3)为测定某雨水是否属于酸雨,应选用______(填序号)
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸
(4)酸雨造成的危害很大,如______(任写一种合理答案),防止的酸雨的措施有______(任写一种合理答案). tt7788991年前1
tt7788991年前1 -
 等号 共回答了17个问题
等号 共回答了17个问题 |采纳率94.1%解题思路:(1)硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成二氧化硫;
(2)此题根据质量守恒定律,反应前后原子种类和个数都不变,分别统计出反应前后原子种类及个数,比较分析就可以求出所的物质的化学式;
(3)石蕊试液和酚酞试液只是酸碱指示剂,并不能准确的测出PH值;
(4)酸雨的危害很多,酸雨能使非金属建筑材料(混凝土、砂浆和灰砂砖)表面硬化水泥溶解,出现空洞和裂缝,导致强度降低,从而建筑物损坏,酸雨可导致土壤酸化;对燃煤进行脱硫处理、使用清洁能源等都能防止酸雨.(1)硫在氧气中燃烧,发出明亮的蓝紫色火焰;燃烧的化学方程式是S+O2
点燃
.
SO2.
(2)由反应的化学方程式3SO2+K2Cr2O7+H2SO4=K2SO4+X+H2O,反应前后各元素原子的个数为
反应前 反应后
K原子2 2
S原子41
O原子17 5
Cr原子 20
H原子 2 2
根据化学变化前后原子的种类、数目不变,可判断物质X中含有12个O原子、3个S原子,2个Cr原子,物质X的化学式可表示为Cr2(SO4)3;
K2Cr2O7中Cr元素的化合价为+6价;
(3)石蕊试液和酚酞试液只是酸碱指示剂,并不能准确的测出PH值,故测定降雨是否为酸雨,要选用PH试纸;
(4)酸雨能使非金属建筑材料(混凝土、砂浆和灰砂砖)表面硬化水泥溶解,出现空洞和裂缝,导致强度降低,从而建筑物损坏,酸雨可导致土壤酸化;对燃煤进行脱硫处理、使用清洁能源等都能防止酸雨.
故答案为:(1)蓝紫;S+O2
点燃
.
SO2;
(2)Cr2(SO4)3;﹢6;
(3)C;
(4)腐蚀金属或大理石的建筑和塑像(合理即可);开发利用新能源,减少化石燃料的使用(合理即可).点评:
本题考点: 酸雨的产生、危害及防治;溶液的酸碱度测定;氧气的化学性质;有关元素化合价的计算;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查化学方程式的书写、质量守恒定律、溶液酸碱度、酸雨的危害等知识,难度不大.1年前查看全部
- 下列实验结论正确的是( )A.碳粉在氧气中燃烧比在空气中剧烈,说明空气中氧气和纯氧气化学性质不同B.双氧水中加入二氧化
下列实验结论正确的是( )
A.碳粉在氧气中燃烧比在空气中剧烈,说明空气中氧气和纯氧气化学性质不同
B.双氧水中加入二氧化锰产生的气泡快,说明催化剂的化学性质在反应前后发生了改变
C.二氧化碳通入紫色石蕊试液中,石蕊变红,说明二氧化碳和水反应后生成了碳酸
D.铜绿粉末受热变黑,说明铜绿加热反应后生成了黑色的碳粉 Lechu6681年前1
Lechu6681年前1 -
 heian2006 共回答了18个问题
heian2006 共回答了18个问题 |采纳率94.4%解题思路:A、根据氧气的浓度不同分析;
B、根据催化剂的作用分析;
C、根据碳酸有酸性分析;
D、根据氧化铜是黑色的分析.A、碳粉在氧气中燃烧比在空气中剧烈,说明空气中氧气和纯氧气浓度不同,浓度越大燃烧的越旺.故A错误;
B、双氧水中加入二氧化锰产生的气泡快,说明二氧化锰能加快了过氧化氢的分解.故B错误;
C、二氧化碳通入紫色石蕊试液中,石蕊变红,说明二氧化碳和水反应后生成了碳酸,碳酸显酸性,能使紫色的石蕊试液变红色.故C正确;
D、铜绿粉末受热变黑,说明铜绿加热反应后生成了黑色的氧化铜,显黑色的物质不是碳粉.故D错误.
故选C.点评:
本题考点: 碳的化学性质;催化剂的特点与催化作用;二氧化碳的化学性质;盐的化学性质.
考点点评: 本题主要考查了常见物质的性质、变化、现象等知识,难度不大.加强常见物质的知识学习是解答本题的关键.1年前查看全部
- 分别取两份相同质量、相同浓度的过氧化氢溶液,其中一份(用a表示)直接加热制取氧气,在另一份(用b表示)中加入少量的二氧化
分别取两份相同质量、相同浓度的过氧化氢溶液,其中一份(用a表示)直接加热制取氧气,在另一份(用b表示)中加入少量的二氧化锰后,再加热.下列关于a、b的图象正确的是( )
A.
B.
C.
D.
 明月心20061年前1
明月心20061年前1 -
 珺譞 共回答了16个问题
珺譞 共回答了16个问题 |采纳率87.5%解题思路:催化剂可以加快或减慢化学反应速率,本身不参加反应所以不影响生成物的产量,据此可以解答.本题中过氧化氢溶液质量和浓度相同,所以最后产生氧气的质量相等,但加入二氧化锰会加快过氧化氢分解速率,起始时间又相同,故答案选C.
点评:
本题考点: 催化剂的特点与催化作用;实验探究物质变化的条件和影响物质变化的因素;根据化学反应方程式的计算.
考点点评: 看图题要求学生把化学原理转化为正确的图象,对学生的思维能力有一定的要求.1年前查看全部
- 下列物质的性质与其用途对应关系不正确的是( ) A.氧气助燃--切割金属 B.氮气化学性质稳定--作保护气 C.二氧化
下列物质的性质与其用途对应关系不正确的是( ) A.氧气助燃--切割金属 B.氮气化学性质稳定--作保护气 C.二氧化碳能与水反应--人工降雨 D.碳具有还原性--冶炼金属  冲动的羔羊1年前1
冲动的羔羊1年前1 -
 wen2flower 共回答了24个问题
wen2flower 共回答了24个问题 |采纳率95.8%物质的用途取决于物质的性质,可根据上述物质的性质来判断用途的正误.
A、氧气有助燃性,可切割金属;故A正确;
B、氮气的化学性质不活泼,一般不与其它物质发生反应,可用作保护气;故B正确.
C、二氧化碳能与水反应生成碳酸,而二氧化碳能灭火是因为二氧化碳不燃烧不支持燃烧,密度比空气大,故C不正确;
D、碳具有还原性,能冶炼金属,故D说法正确.
故选C.1年前查看全部
- 1.碳在氧气中不完全燃烧2.氧化钙与水反应3.氧化钠与水反应4.氧化钾与水反应5.氧化钡与水反应6.氢氧化钠溶液与二氧化
1.碳在氧气中不完全燃烧
2.氧化钙与水反应
3.氧化钠与水反应
4.氧化钾与水反应
5.氧化钡与水反应
6.氢氧化钠溶液与二氧化碳反应
7.氢氧化钠溶液与三氧化硫反应
8.氢氧化钙溶液与碳酸钠溶液反应
9.氯酸钾与二氧化锰共热制氧气
能回答多少算多少~知道多少回答多少谢谢~ 十林1年前1
十林1年前1 -
 aa了 共回答了15个问题
aa了 共回答了15个问题 |采纳率80%2C+O2=2CO
CaO+H2O=Ca(OH)2
Na2O+H2O=2NaOH
K2O+H2O=2KOH
BaO+H2O=Ba(OH)2
NaOH+CO2=NaHCO3
2NaOH+SO3=Na2SO4+H2O
Ca(OH)2+Na2CO3=CaCO3沉淀符号+2NaOH
KClO3+MnO2这个记不清了.1年前查看全部
- 氯酸钾和二氧化锰混合物26g 加热完全反应 最后剩余物质质量16.4g 求氧气多少克 生成氯化钾多少克 原混合物中二氧化
氯酸钾和二氧化锰混合物26g 加热完全反应 最后剩余物质质量16.4g 求氧气多少克 生成氯化钾多少克 原混合物中二氧化锰和氯酸钾各多少克(要详细过程)
 卡迪那鱼1年前1
卡迪那鱼1年前1 -
 我的恨 共回答了18个问题
我的恨 共回答了18个问题 |采纳率77.8%加热完全反应可知剩下的就是催化剂二氧化锰的质量,
氯酸钾的质量 26-16.4=9.6
2KClO3→2KCl+3O2↑
245 149 96
9.6/245= M(O2)/96,M(O2)=3.76g
9.6/245=M(KCl)/149,M(KCl)=5.84g1年前查看全部
- N02+H2O=HN03好像配不平,但老师说什么先从分数什么的化,然后配,好像有一步是乘5这方程就是第七单元所谓的二氧化
N02+H2O=HN03
好像配不平,但老师说什么先从分数什么的化,然后配,好像有一步是乘5
这方程就是第七单元所谓的二氧化氮和水生成硝酸 happyhui6509271年前1
happyhui6509271年前1 -
 leozhang85 共回答了18个问题
leozhang85 共回答了18个问题 |采纳率83.3%3N02+H2O=2HN03+NO1年前查看全部
- (2014•福州模拟)在探究某物质的组成时,某实验小组的同学将3g该物质放在氧气中充分燃烧后,测得生成物有8.8g二氧化
(2014•福州模拟)在探究某物质的组成时,某实验小组的同学将3g该物质放在氧气中充分燃烧后,测得生成物有8.8g二氧化碳和5.4g水,你认为该物质中( )
A.一定含有碳、氢、氧三种元素
B.一定含有碳、氢元素,可能含有氧元素
C.碳元素与氢元素质量比为3:1
D.氢元素的质量分数为20% Rose04511年前1
Rose04511年前1 -
 为细节着迷 共回答了12个问题
为细节着迷 共回答了12个问题 |采纳率83.3%解题思路:根据可燃物完全燃烧时,其中C元素全部转变为二氧化碳、H元素全部转变成水的燃烧规律,由生成的二氧化碳和水中C、H元素质量和与可燃物质量进行对比,对选项中的判断进行评价.A、8.8g二氧化碳中所含C元素的质量=8.8g×[12/44]×100%=2.4g;5.4g水中所含H元素的质量=5.4g×[2/18]×100%=0.6g;生成物8.8g二氧化碳和5.4g水所含C、H元素的质量和=2.4g+0.6g=3g,则3g可燃物中只含C、H两种元素,一定不含氧元素;故A不正确;
B、根据选项A的分析,可知一定不含氧元素,故B不正确;
C、可燃物中碳元素与氢元素质量比=2.4g:0.6g=4:1;故C不正确;
D、可燃物中氢元素质量比=[0.6g/3g]×100%=20%;故D正确.
故选:D.点评:
本题考点: 质量守恒定律及其应用;元素质量比的计算;元素的质量分数计算.
考点点评: 利用化合物的化学式,一定质量的化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数.1年前查看全部
- 氧化铁和二氧化三铁的区别.氧化铁中铁是二价,三氧化二铁铁是三价的.那什么情况下生成氧化铁?或二氧化三铁呢
 金鱼QE1年前3
金鱼QE1年前3 -
 艾姍 共回答了15个问题
艾姍 共回答了15个问题 |采纳率86.7%不完全氧化时生成氧化亚铁
完全氧化是生成三氧化二铁1年前查看全部
- 某县是有30万户人口的中等县市,每户每天烧煤5kg,这种煤中含有FeS2百分之5,燃烧时,设有百分之90的硫转化为二氧化
某县是有30万户人口的中等县市,每户每天烧煤5kg,这种煤中含有FeS2百分之5,燃烧时,设有百分之90的硫转化为二氧化硫.FeS2+11O2=2Fe2O3+8SO2.燃烧1吨煤,可产生多少千克二氧化碳?
 失恋的标签1年前1
失恋的标签1年前1 -
 yangwei0577 共回答了18个问题
yangwei0577 共回答了18个问题 |采纳率94.4%某县是有30万户人口的中等县市,每户每天烧煤5kg,这种煤中含有FeS2百分之5,燃烧时,设有百分之90的硫转化为二氧化硫.FeS2+11O2=2Fe2O3+8SO2.燃烧1吨煤,可产生多少千克二氧化碳?1年前查看全部
- (2013•黑龙江模拟)在我们生活中许多食品的制作都要利用某些细菌和真菌.如制作馒头或面包时,______菌产生的二氧化
(2013•黑龙江模拟)在我们生活中许多食品的制作都要利用某些细菌和真菌.如制作馒头或面包时,______菌产生的二氧化碳气体会在面团中形成许多小孔,使馒头或面包膨大和松软.
 爱杰杰的qq星1年前1
爱杰杰的qq星1年前1 -
 zhengwei0627 共回答了20个问题
zhengwei0627 共回答了20个问题 |采纳率100%解题思路:微生物的发酵在食品的制造中的应用十分广泛,如制馒头和面包要用到酵母菌,据此答题.做馒头或面包时,经常要用到酵母菌,酵母菌经过发酵可以分解面粉中的葡萄糖,产生二氧化碳,二氧化碳是气体,遇热膨胀而形成小孔,使得馒头或面包暄软多孔.可见D符合题意.
故答案为:酵母点评:
本题考点: 发酵技术在食品制作中的作用.
考点点评: 熟练掌握制馒头和面包的原理,同时也要注意其它的发酵产品的知识.1年前查看全部
- (2008•枣庄一模)学习元素周期律后,某研究性学习小组的同学们对第四周期过渡元素的氧化物产生了浓厚的兴趣.在已知二氧化
(2008•枣庄一模)学习元素周期律后,某研究性学习小组的同学们对第四周期过渡元素的氧化物产生了浓厚的兴趣.在已知二氧化锰对氯酸钾催化分解知识的基础上,联想到氧化铁、氧化铜、氧化铬等对氯酸钾的分解是否有催化作用,对此他们进行了实验研究.
请根据要求完成下列部分实验报告:
(1)课题名称:探究氧化铁、氧化铜、氧化铬等对氯酸钾分配是否有催化作用探究氧化铁、氧化铜、氧化铬等对氯酸钾分配是否有催化作用.
(2)实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、试管、酒精灯、秒表试管、酒精灯、秒表等.
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
(3)实验步骤:略
(4)实验数据:
(5)实验讨论:实验
编号KClO3/g 氧化物 产生气体/mL
(已折算到标况)耗时/s 化学式 质量/g 回收 1 0.60 - - - 10 480 2 0.60 MnO2 0.20 90% 67.2 36.5 3 0.60 CuO 0.20 90% 67.2 79.5 4 0.60 Fe2O3 0.20 90% 67.2 34.7 5 0.60 Cr2O3 0.20 90% 67.2 188.3
①在氧化物的回放过程中,要进行的操作是溶解、过滤过滤、洗涤、干燥干燥、称量.
②实验编号3的实验中KClO3的分解率为40.840.8(保留一位小数).
③在和Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气味的气体是C12C12,可用湿润的KI淀粉湿润的KI淀粉试纸检验.上述异常现象产生的原因是Cr2O3与KC1O3发生氧化还原反应Cr2O3与KC1O3发生氧化还原反应.
(6)实验结论Fe2O3、CuO能对KC1O(3分)解起催化作用Fe2O3、CuO能对KC1O(3分)解起催化作用. 装得不像1年前1
装得不像1年前1 -
 0201shuai 共回答了21个问题
0201shuai 共回答了21个问题 |采纳率85.7%(1)本实验的目的是探究CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解有没有催化作用,所以其课题名称为探究CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解反应的催化作用.
故答案为:探究氧化铁、氧化铜、氧化铬等对氯酸钾分配是否有催化作用;
(2)试根据实验要测定时间,所以应有秒表,还有反应容器和加热仪器,故答案为:试管、酒精灯、秒表;
(5)①CuO、Fe2O3、Cr2O3都难溶于水,所以回收是要溶解、洗涤、过滤、干燥、称量,
故答案为:过滤、干燥;
②生成氧气的物质的量为n=
V
Vm=
0.0672L
22.4L/mol=0.003mol,
2KCl3
CuO
.
△2KCl+3O2↑
2mol 3mol
0.002mol 0.003mol
所以反应的氯酸钾的物质的量为 0.002mol,质量为m=nM=0.002mol×122.5g/mol=0.245g,
所以其分解率为
0.245g
0.6g×100%=40.8%,
故答案为:40.8%;
③用Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色,则Cr元素的化合价升高,Cl元素的化合价降低,氯酸钾与氧化铬发生了氧化还原反应,生成氯气,其化学式为Cl2,氯气能使湿润的淀粉碘化钾试纸变蓝,则可以使用湿润的淀粉碘化钾试纸检验氯气,
故答案为:Cl2;湿润的淀粉碘化钾;KClO3与Cr2O3发生了氧化还原反应;
(6)根据图表中回收的氧化物及耗时分析,CuO、Cr2O3 与二氧化锰比较,耗时较长且Cr2O3 的回收物有异常,氯化铁和二氧化锰的催化能力相近.
故答案为:Fe2O3、CuO能对KC1O分解起催化作用.1年前查看全部
- 1、大气中主要吸收太阳紫外线的气体成分为_B_.A二氧化B臭氧C氧气D氮气 把答案放在本题的最后面,
1、大气中主要吸收太阳紫外线的气体成分为_B_.A二氧化B臭氧C氧气D氮气 把答案放在本题的最后面,
就是说答案另起一行放在本题的最后面,大哥大姐们帮帮忙, 行渐远1年前2
行渐远1年前2 -
 celin423 共回答了23个问题
celin423 共回答了23个问题 |采纳率87%A.二氧化碳是温室气体,它具有保温的作用.
B.臭氧主要吸收的是紫外线,吸收小于240μm波长的太阳光中的紫外线,并分解形成氧原子.这些氧原子与氧分子相结合生成臭氧,生成的臭氧可以吸收太阳光而被分解掉,也可与氧原子相结合,再度变成氧分子.它也对红外波长10微米左右很窄的频带范围内的辐射有个很强的吸收峰,可以吸收此波段的长波辐射并加热大气.
C.氧气 普通气体
D.氮气 通常用作生产氮肥
答案:选B1年前查看全部
- 氧化铁是否二氧化三铁
 wllok1年前1
wllok1年前1 -
 chencola 共回答了18个问题
chencola 共回答了18个问题 |采纳率88.9%三氧化二铁1年前查看全部
- 下图为云南路南石林不同植被下,土壤中的二氧化碳浓度示意图(二氧化破浓度越高,溶蚀作用越显著),据此完成下列小题。
下图为云南路南石林不同植被下,土壤中的二氧化碳浓度示意图(二氧化破浓度越高,溶蚀作用越显著),据此完成下列小题。
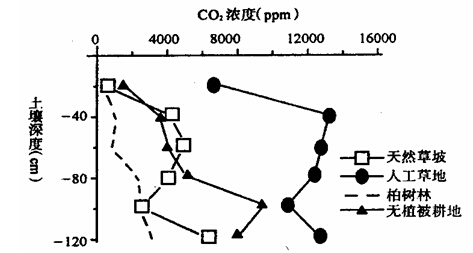
小题1:如果水分条件相同,土壤、岩石最易被溶蚀的是
小题2:如果当地植被破坏严重,最终产生的环境问题是A.无植被耕地 B.人工草地 C.柏树林 D.天然草坡 A.沙化 B.泥石流 C.石漠化 D.滑坡  兰州牛1年前1
兰州牛1年前1 -
 不下残阳 共回答了20个问题
不下残阳 共回答了20个问题 |采纳率95%小题1:B
小题2:C
1年前查看全部
- 葡萄糖是一种有甜味、易溶于水的白色粉末状固体,化学式是C 6 H 12 O 6 。葡萄糖在人体内发生缓慢氧化转化为二氧化
葡萄糖是一种有甜味、易溶于水的白色粉末状固体,化学式是C 6 H 12 O 6 。葡萄糖在人体内发生缓慢氧化转化为二氧化碳和水,并释放出热量。试回答:
(1)每个葡萄糖分子共有 个原子;
(2)葡萄糖分子的相对分子质量 ;
(3)葡萄糖中各元素的质量比C:H:O ;
(4)列式计算葡萄糖中碳元素的质量分数。 周游很多列cc1年前1
周游很多列cc1年前1 -
 mt301 共回答了22个问题
mt301 共回答了22个问题 |采纳率86.4%(1)24 ;(2)180 ;(3)6:1:8 ;(4)40%1年前查看全部
- 阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化
阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化硫和水生成.硫化氢的实验室制法是用块状硫化亚铁和液体状稀硫酸反应,则属硫化氢的化学性质的是( )
A.无色
B.有臭鸡蛋气味
C.比空气重
D.能燃烧 superangry11年前1
superangry11年前1 -
 whant928 共回答了20个问题
whant928 共回答了20个问题 |采纳率100%解题思路:化学性质主要有:可燃性、毒性、氧化性、还原性、稳定性等.物理性质主要有:颜色、状态、气味、密度、硬度、熔点、沸点等.可以根据物质的物理性质和化学性质进行综合解释.解;A、硫化氢是无色气体,颜色属于物理性质;
B、硫化氢气味有臭鸡蛋气味,气味属于物理性质;
C、硫化氢比空气重,密度属于物理性质;
D、硫化氢能燃烧,可燃性属于化学性质;
故选D.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题主要考查了物质的两种性质的区别与联系的内容,可以依据题干提供的信息进行.1年前查看全部
- 如图是某课外学习小组设计的气体制各与性质验证的组合实验,其中装置B的作用是对二氧化碳气体进行干燥,装置C的作用是将二氧化
如图是某课外学习小组设计的气体制各与性质验证的组合实验,其中装置B的作用是对二氧化碳气体进行干燥,装置C的作用是将二氧化碳和炭粉在高温下转化为一氧化碳.请看图回答下列问题:

(1)写出装置A中发生反应的化学方程式______.
(2)写出装置C中发生反应的化学方程式CO2+C
2CO高温 .CO2+C.
2CO高温 .
(3)E中的现象是______.
(4)该套装置中有一个明显的不足之处,应在装置E后放置燃着的酒精灯处理尾气.这样做的原因是______. 你静静挽着1年前1
你静静挽着1年前1 -
 hualin_bai 共回答了24个问题
hualin_bai 共回答了24个问题 |采纳率75%解题思路:(1)装置A是利用石灰石与稀盐酸反应来制取二氧化碳的,根据反应物、反应条件以及生成物来书写方程式;
(2)装置C是利用炭和二氧化碳来制取一氧化碳的,根据反应物、反应条件以及生成物来书写方程式;
(3)装置E中是二氧化碳与氢氧化钙发生反应,生成白色沉淀;
(4)一氧化碳有毒,应该做一下尾气处理.(1)装置A中发生的反应为碳酸钙和稀盐酸的反应,该反应生成了氯化钙、水和二氧化碳,其化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)装置C中,炭粉与二氧化碳在高温的条件下反应生成一氧化碳,其化学方程式为:CO2+C
高温
.
2CO;故填:CO2+C
高温
.
2CO;
(3)二氧化碳与氢氧化钙发生反应,生成白色沉淀碳酸钙和水.其反应方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
故填:澄清石灰水变浑浊;
(4)一氧化碳有毒,会污染空气,所以应该将其燃烧,转化为二氧化碳.
故填:使剩余的CO全部燃烧,防止污染空气(或CO有毒,防止污染空气).点评:
本题考点: 二氧化碳的实验室制法;气体的干燥(除水);二氧化碳的化学性质;一氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题通过实验巧妙的把二氧化碳的制法和性质以及一氧化碳的性质融合在一起,有较强的综合性,要熟记实验室制取二氧化碳的反应原理、实验步骤、装置示意图及其中仪器.1年前查看全部
- 下列物质含原子个数最多?A 0.4摩尔氧气 B 4摄氏度时5.4毫升水 C 10克氖D 6.02乘10的22次方个二氧化
下列物质含原子个数最多?A 0.4摩尔氧气 B 4摄氏度时5.4毫升水 C 10克氖D 6.02乘10的22次方个二氧化碳分子
 夜色阑珊艾子1年前3
夜色阑珊艾子1年前3 -
 勇敢_de心 共回答了18个问题
勇敢_de心 共回答了18个问题 |采纳率88.9%A 0.4mol氧气中含有0.4NA个氧气分子,但一个氧气分子中含有2个氧原子,所以有0.8NA个氧原子
B 4摄氏度时水的密度最大,为1,5.4ml水的质量为5.4g ,是0.3mol,1mol水分子中含有1mol的氧原子和2mol的H原子,所以0.3mol的水中有0.9mol的原子
C 10gNe也就是0.5mol的氖,有0.5mol的氖原子
D 6.02*10^22二氧化碳分子也就是0.1mol二氧化碳,每个二氧化碳分子有1个碳原子和2个氧原子,所以0.1mol二氧化碳中含有0.3mol的氧原子,选B
其实这些题很简单,楼主努力学习一定会学好的1年前查看全部
- 将12.5克的石灰石放入36.5克的稀盐酸中(石灰石中的杂质,不与酸反应,也不溶于水).恰好完全反应,放出4.4克二氧化
将12.5克的石灰石放入36.5克的稀盐酸中(石灰石中的杂质,不与酸反应,也不溶于水).恰好完全反应,放出4.4克二氧化碳.求
石灰石中碳酸钙的质量分数? cv4655z1年前1
cv4655z1年前1 -
 白色野百合 共回答了13个问题
白色野百合 共回答了13个问题 |采纳率76.9%设CaCO3质量为x,HCl质量为y,CaCl2质量为z
CaCO3+2HCl=CaCl2+CO2↑+H20
100 73 111 44
x y z 4.4g
100:44= x:4.4g 73 :44=y :4.4g 111:44= z :4.4g
x=10g,y=7.3g,z=11.1g
(1)石灰石中CaCO3的质量分数为:10g/12.5*100%=80%
(2)稀盐酸中溶质的质量分数为:7.3g/36.5g*100%=20%
(3)所得CaCl2溶液中溶质的质量分数为:11.1g/(10+36.5g-4.4g)*100%=26.4%
答略.1年前查看全部
- 在一倒置于水槽且装满水的容器中,依次通过一定体积的二氧化氮、一氧化氮和氧气,充分反应后,若容器中仍充满水,则通入的二氧化
在一倒置于水槽且装满水的容器中,依次通过一定体积的二氧化氮、一氧化氮和氧气,充分反应后,若容器中仍充满水,则通入的二氧化氮、一氧化氮和氧气的体积比可能是
A.1:1:1
B.4:3:2
C.4:16:13
D4:3:4 ozhma1年前5
ozhma1年前5 -
 liumangtu2006 共回答了19个问题
liumangtu2006 共回答了19个问题 |采纳率89.5%由3NO2+H2O=2HNO3+NO,2NO+O2=2NO2综合推出:
4NO2+O2+2H2O=4HNO3.
先根据2NO+O2=2NO2除去NO.
譬如A选项,消耗掉1的NO,0.5的O2,生成1的NO2.
则还剩余0.5的O2和2的NO2.
根据4NO2+O2+2H2O=4HNO3.恰好NO2:O2=1:4全部反应.
没有气体剩余.容器中仍然充满水.
C选项一样的道理:2NO+O2=2NO2
因为有16份的NO,消耗8份的O2,生成16份的NO2.
还剩13-8=5份的O2, 4+16=20份的NO2.
满足1:4,全部反应.
BD选项都会有气体剩余,不符合条件.
所以答案AC.
很高兴为你解答,希望能够帮助到你.基础教育团队祝你学习进步!
不理解就追问,理解了请采纳!1年前查看全部
- ①甲烷在空气中燃烧生成什么物质?②在空气中加热汞 ③一氧化碳在高温的条件下还原氧化铁生成铁和二氧化
①甲烷在空气中燃烧生成什么物质?②在空气中加热汞 ③一氧化碳在高温的条件下还原氧化铁生成铁和二氧化
④一氧化碳在高温的条件下还原四氧化三铁生成铁和二氧化碳
注:如果需要写 [加热,点燃] 请写在答案后面.
第三问最后面是二氧化碳 8g4q11年前2
8g4q11年前2 -
 ff7ff9 共回答了20个问题
ff7ff9 共回答了20个问题 |采纳率100%①生成二氧化碳和水
CH4+2O2==CO2+2H20 条件点燃
②2HgO==2Hg+O2↑ 条件加热
③3CO+Fe2O3==2Fe+3CO2 条件高温
④4CO+Fe3O4==3Fe+4CO2 条件高温1年前查看全部
- 苏打水和碳酸水的区别?查了一下百科反而糊涂了,先说苏打水是碳酸氢钠的水溶液,又说市面上的苏打水大多是纯化后的水压入二氧化
苏打水和碳酸水的区别?
查了一下百科反而糊涂了,先说苏打水是碳酸氢钠的水溶液,又说市面上的苏打水大多是纯化后的水压入二氧化碳制成?然后我就不明白了,我也许过一些化学,第一:苏打水肯定是弱碱性的!第二:水压入二氧化碳会形成碳酸,是弱酸性的!第三,纯化后的水应该几乎没有钠,即使压入二氧化碳,哪来的碳酸氢钠呢?那不是碳酸么?第四:苏打水和碳酸饮料都是水压入二氧化碳,到底有什么区别呢?仅仅是加入了不同口味么?为什么一个是碱性一个是酸性呢? 柳叶飘飘21年前3
柳叶飘飘21年前3 -
 邱小妞 共回答了18个问题
邱小妞 共回答了18个问题 |采纳率83.3%苏打水在加入二氧化碳之后,一定会再和含钠的盐反应,生成的碳酸氢钠是溶液呈碱性的盐(该溶液加入石蕊变蓝,酚酞变红).
而碳酸饮料只加入二氧化碳,碳酸呈酸性
提醒:如果你看到反应生成物中,含有反应物不存在的元素,一定是有其他反应发生.1年前查看全部
- 下列气体既能用向上排空气法收集,又能用排水法收集的是 [ ] A.二氧化
下列气体既能用向上排空气法收集,又能用排水法收集的是 [ ]A.二氧化碳
B.一氧化碳
C.氧气
D.氢气 娴情物语1年前1
娴情物语1年前1 -
 ywyacjc 共回答了23个问题
ywyacjc 共回答了23个问题 |采纳率78.3%C1年前查看全部
- (2013•日照)在密闭的玻璃容器中放置一株生长状况良好的天竺葵,在适宜条件下进行光照.能正确表示随时间延长容器中二氧化
(2013•日照)在密闭的玻璃容器中放置一株生长状况良好的天竺葵,在适宜条件下进行光照.能正确表示随时间延长容器中二氧化碳浓度变化趋势的曲线是( )
A.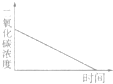
B.
C.
D.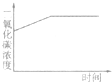
 hsh6001年前1
hsh6001年前1 -
 帕拉帕拉帕拉 共回答了19个问题
帕拉帕拉帕拉 共回答了19个问题 |采纳率89.5%解题思路:在密闭的玻璃容器中放置一株生长状况良好的天竺葵,考虑问题一定要全面周到,植物光合作用的同时一定还要考虑呼吸作用,呼吸作用是不会停止的.据此答题.根据光合作用进行的场所是叶绿体,表达式为:二氧化碳+水
光能
叶绿体有机物(储存能量)+氧气.呼吸作用进行的场所为线粒体,表达式为:有机物+氧→二氧化碳+水+能量.在适宜的条件下培养密闭容器内的植物,密闭容器内的二氧化碳含量有限,随着光合作用的持续进行,二氧化碳逐渐被消耗,浓度降低,进而光合作用强度跟着降低,当二氧化碳浓度降低到一定水平时,植物的光合作用和呼吸作用强度相等,则装置内的二氧化碳浓度就保持相对稳定,故本题选C.
故选:C点评:
本题考点: 探究光合作用的条件、原料和产物.
考点点评: 本题以密闭容器内绿色植物生长为背景,考查环境条件对植物光合作用的影响,有一定的难度.1年前查看全部
- 下列说法错误的是( )A.制取肥皂时,常常加入少量乙醇,目的是加快皂化反应B.海水提镁的主要步骤为:C.工业上将二氧化
下列说法错误的是( )
A.制取肥皂时,常常加入少量乙醇,目的是加快皂化反应
B.海水提镁的主要步骤为: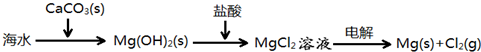
C.工业上将二氧化碳和氨气通入食盐水中制的碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠
D.用蒸馏法便可分离苯和溴苯 Johny_R1年前1
Johny_R1年前1 -
 被遗弃的我 共回答了16个问题
被遗弃的我 共回答了16个问题 |采纳率93.8%解题思路:A.用乙醇溶解NaOH和油脂,使其充分接触;
B.碳酸钙与镁离子不反应;
C.将二氧化碳和氨气通入饱和食盐水中,控制一定温度,制得碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠;
D.苯和溴苯的沸点不同.A.用乙醇溶解NaOH和油脂,使其充分接触,使皂化反应更快,更充分,故A正确;
B.应加入氢氧化钙,Ca(OH)我加入海水溶液中,得到氢氧化镁沉淀,故B错误;
C.工业上制取碳酸钠m方法是:将二氧化碳和氨气通入饱和食盐水中,控制一定温度,制得碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠,故C正确;
D.苯和溴苯m沸点不同,可用蒸馏分离,故D正确.
故选B.点评:
本题考点: 油脂的性质、组成与结构;纯碱工业(侯氏制碱法);海水资源及其综合利用;蒸馏与分馏.
考点点评: 本题考查物质的制取以及分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.1年前查看全部
- 氮气,铁.镁,硫,水,二氧化二铝,碳酸氢铵,氯酸钾分别属于什么
 独孤uu1年前1
独孤uu1年前1 -
 hznetboy 共回答了15个问题
hznetboy 共回答了15个问题 |采纳率86.7%氮气,非金属单质
铁 金属单质.
镁, 金属单质
硫, 非金属单质
水, 化合物(氧化物)
二氧化二铝, 化合物(氧化物)
碳酸氢铵,化合物(盐)
氯酸钾 化合物(盐)1年前查看全部
- 某同学用过氧化氢溶液和二氧化锰制取氧气,化学方程式为2H2O2═2H2O+O2↑,该同学将50g过氧化氢溶液和1g二氧化
某同学用过氧化氢溶液和二氧化锰制取氧气,化学方程式为2H2O2═2H2O+O2↑,该同学将50g过氧化氢溶液和1g二氧化锰混合,完全反应后,称量剩余的混合质量为49.4g.
求:(1) 反应产生氧气的质量是______g.
(2) 该同学所用过氧化氢溶液的溶质质量分数是多少(列式计算)? liwson1年前0
liwson1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 一氧化碳还原氧化铁实验中用澄清石灰水增重的质量测定氧化铁的质量,那么盛有澄清石灰水的洗气瓶的进气管(进反应后生成的二氧化
一氧化碳还原氧化铁实验中用澄清石灰水增重的质量测定氧化铁的质量,那么盛有澄清石灰水的洗气瓶的进气管(进反应后生成的二氧化碳)应伸入底部还是露出橡皮塞一点?为什么?
 不抓老鼠的阿笨猫1年前1
不抓老鼠的阿笨猫1年前1 -
 vickvick 共回答了17个问题
vickvick 共回答了17个问题 |采纳率100%答:应伸入底部,因为只有这样才能使二氧化碳充分与石灰水接触并反应,同时完全吸收掉二氧化碳.1年前查看全部
- 煤是一种化石燃料,燃烧后产生的二氧化硫会造成大气污染.有一种煤每燃烧1t就会释放53.3kg的二氧化硫.若将产生的二氧化
煤是一种化石燃料,燃烧后产生的二氧化硫会造成大气污染.有一种煤每燃烧1t就会释放53.3kg的二氧化硫.若将产生的二氧化硫用熟石灰来吸收,反映的化学方程式为S02+Ca(OH)2===CaSO3沉淀+H2O,那么燃烧5t这种煤产生的二氧化硫在理论上需要多少千克含杂质百分之二十的熟石灰来吸收
 露华沉香1年前3
露华沉香1年前3 -
 Oscar0707 共回答了21个问题
Oscar0707 共回答了21个问题 |采纳率90.5%1 先求5t煤燃烧生成的SO2 5x53.3kg=266.5kg =0.2665吨
根据方程式进行计算
SO2 + Ca(OH)2====CaSO3 + H2o
64 74
0.2665 X=0.308吨 故含杂质百分之二十的熟石灰 为 0.308/80%=0.385吨1年前查看全部
- 蜡烛熄灭时白烟的成分蜡烛刚熄灭时,总会有一缕白烟冒出,它的成分是什么呢?你可能会提出如下假设:A、白烟是燃烧生成的二氧化
蜡烛熄灭时白烟的成分
蜡烛刚熄灭时,总会有一缕白烟冒出,它的成分是什么呢?你可能会提出如下假设:
A、白烟是燃烧生成的二氧化碳 B、白烟是燃烧生成的水蒸气C、白烟是石蜡蒸气凝成的石蜡固体
实验:
(1)吹灭蜡烛,立即用一个沾有澄清石灰水的烧杯罩住白烟,其目的是为了验证假设(填序号,下同).
(2)吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片上没有出现水珠,说明上述中假设是错误的.
(3)吹灭蜡烛,立即用燃着的木条去点白烟,发现蜡烛重新被点燃,说明白烟具有可燃性,这为假设提供了证明,同时排出了假设
,由此可推知二氧化碳气体具有
的化学性质.
 cltf0011年前1
cltf0011年前1 -
 我错了吗123 共回答了15个问题
我错了吗123 共回答了15个问题 |采纳率73.3%选C,它的成分是石蜡蒸气凝成的石蜡固体.
(1),选A,澄清石灰水即Ca(OH)2加CO2能生成白色沉淀CaCO3,即澄清石灰水变浑浊,这个反应常用于检验CO2.
(2),选B,如果白烟是水蒸气,干冷玻璃片放在白烟上,水蒸气遇冷会液化成小水珠.
(3),选C,二氧化碳、水蒸气不具有可燃性.同时排除了假设AB.
二氧化碳具有不燃烧,不助燃的化学性质.与Ca(OH)2反应能生成CaCO3和H2O.1年前查看全部
- 在空气中燃烧既能生成二氧化又能生成水的物质是 蜡烛?为什么?
 chenii161年前2
chenii161年前2 -
 铁乐门 共回答了17个问题
铁乐门 共回答了17个问题 |采纳率94.1%纠正:蜡烛是由碳、氢元素组成的烃类混合物.
其实所有像蜡烛这样的烃类(甲烷、乙炔等),由于内部含C、H两种元素,所有燃烧产物都有CO2和H2O1年前查看全部
- 某工厂欲炼1500t含杂质2%的生铁,需要含二氧化三铁80%的赤铁矿多少吨?
某工厂欲炼1500t含杂质2%的生铁,需要含二氧化三铁80%的赤铁矿多少吨?
很着急,会的请火速回答, 雪晴2201年前1
雪晴2201年前1 -
 noformet 共回答了20个问题
noformet 共回答了20个问题 |采纳率95%设,需要含二氧化三铁80%的赤铁矿x吨
80%*x*112/160*100%=1500*(1-2%)
x=2625
需要含二氧化三铁80%的赤铁矿2625吨1年前查看全部
- 阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化
阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水.在空气中点燃硫化氢气体有二氧化硫和水生成.硫化氢的实验室制法是用块状硫化亚铁和液体状稀硫酸反应,则属硫化氢的化学性质的是 [ ]A.无色
B.有臭鸡蛋气味
C.比空气重
D.能燃烧 tangelo1年前1
tangelo1年前1 -
 zwking_1981 共回答了21个问题
zwking_1981 共回答了21个问题 |采纳率85.7%D1年前查看全部
- 现将四摩尔二氧化硫两摩尔氧气冲入二升密闭容器反应平衡后在加入二摩尔二氧化 硫二摩尔氧气4摩尔三氧
现将四摩尔二氧化硫两摩尔氧气冲入二升密闭容器反应平衡后在加入二摩尔二氧化 硫二摩尔氧气4摩尔三氧
硫问平衡如何移动 sbppscnjlhh1年前2
sbppscnjlhh1年前2 -
 风孤独 共回答了12个问题
风孤独 共回答了12个问题 |采纳率83.3%这个不一定,因为你是恒容反应器,加入物质后浓度增大要向正反应方向移动你;但是你不仅加了反应物,还加了生成物,那么可能又会向逆反应方向移动.所以不一定1年前查看全部
- 科技人员向农民建议:在利用温室生产作物时,向温室里施放适量的二氧化,可获得更好的经济效益,这主要是因为( )
科技人员向农民建议:在利用温室生产作物时,向温室里施放适量的二氧化,可获得更好的经济效益,这主要是因为( )
A.CO2可使害虫窒息而死,从而有效的防止植物病虫害
B.CO2一般不支持燃烧,施用CO2可避免火灾
C.植物的光合作用需要CO2,施用CO2可促进作物生长
D.CO2可产生“温室效应”,能使室内的温度稳中有升 pp_mutong1年前1
pp_mutong1年前1 -
 sanbu777 共回答了15个问题
sanbu777 共回答了15个问题 |采纳率93.3%解题思路:本题考查光合作用原理在生产上的应用,影响绿色植物进行光合作用的因素有:光照、二氧化碳的浓度等,所以光照时间越长,光合作用越强,植物制造的有机物就越多,根据这一原理可以解答此题.A.二氧化碳不供给呼吸,只有当二氧化碳达到一定浓度时才能使害虫死亡,故A错.
B.二氧化碳能灭火,但在温室中施用的二氧化碳参与了植物的光合作用,不能达到用来防止火灾的目的,故B错.
C.植物光合作用需要CO2,增加CO2含量可以提高农作物产量,故C对.
D.二氧化碳含量增多会产生温室效应,是指大气能使太阳短波辐射到达地面,但地表向外放出的长波热辐射线却被大气吸收,使地表与低层大气温度增高,而温室中温度升高是由于塑料薄膜能让太阳的光、热量进入,阻止冷空气进入和热量挥发,故D错.
故选C.点评:
本题考点: 二氧化碳的用途.
考点点评: 本题主要考查二氧化碳的性质与用途,要明确二氧化碳与光合作用、温室效应之间的关系.1年前查看全部
- 手机、笔记本电脑等电子产品中使用的锂电池,具有体积小、充电时间短、放电时间长等优点,放电时的工作原理是锂(Li)跟二氧化
手机、笔记本电脑等电子产品中使用的锂电池,具有体积小、充电时间短、放电时间长等优点,放电时的工作原理是锂(Li)跟二氧化锰作用生成LiMnO 2 .
(1)在LiMnO 2 里,锂元素显+1价,则锰元素的化合价为______;
(2)写出锂电池放电时的化学方程式______;
(3)锂电池充电时,是将电能转化为______能. 沧海一生笑6181年前1
沧海一生笑6181年前1 -
 joewu2005 共回答了23个问题
joewu2005 共回答了23个问题 |采纳率91.3%(1)氧元素为-2价,根据化合物中化合价的代数和为零可以求出锰元素的化合价为+3价.故填:+3.
(2)反应的化学方程式为:Li+MnO 2 =LiMnO 2
(3)充电时电能转化成化学能.故填:化学.1年前查看全部
- 下列对相关化学知识的描述不正确的是( ) A.单质是由同种元素组成的,但同种元素组成的物质不一定是单质 B.可用二氧化
下列对相关化学知识的描述不正确的是( ) A.单质是由同种元素组成的,但同种元素组成的物质不一定是单质 B.可用二氧化锰区分水和过氧化氢溶液 C.向pH=11的溶液中滴加紫色石蕊试液,溶液呈红色 D.配制10%的氯化钠溶液,需要经过计算、称量、溶解、装瓶贴标签等步骤  浅蓝的雪1年前1
浅蓝的雪1年前1 -
 zz的暖窝 共回答了15个问题
zz的暖窝 共回答了15个问题 |采纳率80%A、单质是由同种元素组成的,但同种元素组成的物质不一定是单质,氧气和臭氧组成的物质属于混合物,正确;
B、分别向水和过氧化氢溶液的试管中,加入二氧化锰,有气泡冒出的是过氧化氢,无变化的是水,正确;
C、向pH=11的溶液中滴加紫色石蕊试液,溶液呈蓝色,错误;
D、配制10%的氯化钠溶液,需要经过计算、称量、溶解、装瓶贴标签等步骤,才会步骤齐全,正确;
故选C1年前查看全部
- 写出下列带点数字的意义ca2+ 2mg2+ so2- 意义2个带2个单位正电荷的铜离子带2个单位负电荷的流离子3个二氧化
写出下列带点数字的意义
ca2+ 2mg2+ so2- 意义
2个带2个单位正电荷的铜离子
带2个单位负电荷的流离子
3个二氧化碳分子
4个钠离子
7个五氧化二磷分子
8个氮分子
带1个单位正电荷的银离子 小气的鬼1年前1
小气的鬼1年前1 -
 搬座泰山来砸你 共回答了15个问题
搬座泰山来砸你 共回答了15个问题 |采纳率80%一、
题目打错了吧是,S04(2-)还是SO3(2-),不可能是SO2-
Ca2+:一个钙离子带两个单位正电荷
2Mg2+:【第一个2】两个镁离子,【第二个2】一个镁离子带两个单位正电荷
S04-:一个硫酸根离子带两个单位负电荷
或者SO3(2-):一个【亚硫酸根】离子带两个单位负电荷
二、下面是写出化学式吧.
2个带2个单位正电荷的铜离子:2Cu2+
带2个单位负电荷的硫离子:S2-
3个二氧化碳分子:3CO2
4个钠离子:4Na+
7个五氧化二磷分子:7P205
8个氮分子:8N2
带1个单位正电荷的银离子:Ag+
〖友情提示〗:这里粒子所带电荷数和电性都应该写在右上角.LZ书写的时候一定要注意.1年前查看全部
- 二氧化硅与氢氧化钠反应实质.会不会和二氧化碳一样,先与水反应生成碳酸,再与氢氧化钠反应.但二氧化...
二氧化硅与氢氧化钠反应实质.会不会和二氧化碳一样,先与水反应生成碳酸,再与氢氧化钠反应.但二氧化...
二氧化硅与氢氧化钠反应实质.会不会和二氧化碳一样,先与水反应生成碳酸,再与氢氧化钠反应.但二氧化硅不与水反应的,那是为什么! 豌豆巴果1年前4
豌豆巴果1年前4 -
 selina912 共回答了12个问题
selina912 共回答了12个问题 |采纳率91.7%虽然是同一主族,但随着电子层数的增多,同一主族的元素还是在性质上还是有差别的.二氧化硅与氢氧化钠高温下反应,生成硅酸钠,可以在水中发生电离,形成硅酸,胶状物1年前查看全部
- 谁能教我一下化合价,铁的化合价是2,3.氧的是-2,可我就是不知道四氧化三铁是怎么算出来的.我只算的出三氧化二铁和二氧化
谁能教我一下化合价,铁的化合价是2,3.氧的是-2,可我就是不知道四氧化三铁是怎么算出来的.我只算的出三氧化二铁和二氧化二铁.有这种物质吗?
 112358001年前1
112358001年前1 -
 莱阅经 共回答了17个问题
莱阅经 共回答了17个问题 |采纳率88.2%四个氧是-8价,既然铁有2或3价,那那三个铁的化合价就不可能相同,只有两个3价的铁,一个2价的铁,加起来正好8价!1年前查看全部
- 氯酸钾可以加热分解产生氧气,实验室为什么不用加热的方式,而要借助于催化剂二氧化
 begins1年前2
begins1年前2 -
 asdasdasdsa 共回答了19个问题
asdasdasdsa 共回答了19个问题 |采纳率78.9%氯酸钾可以加热分解产生氧气,但反应速率极慢,加热很长时间也无法收集到大量氧气.
加入催化剂MnO2后,化学反应速率大大加快,能在短时间内收集到大量氧气.
节约时间、节约燃料1年前查看全部
- 蜡烛在空气中燃烧后,会产生水及二氧化碳.若蜡烛在空气中燃烧后质量减轻了a千克,用去b千克氧气,生成x千克水及y千克二氧化
蜡烛在空气中燃烧后,会产生水及二氧化碳.若蜡烛在空气中燃烧后质量减轻了a千克,用去b千克氧气,生成x千克水及y千克二氧化碳,则下列关系式正确的是( )
A、a=b B、x=y C、a+b=x+y D、a=b+x+y neptune4251年前2
neptune4251年前2 -
 hhxdq 共回答了18个问题
hhxdq 共回答了18个问题 |采纳率88.9%C、a+b=x+y1年前查看全部
- 分别取两份相同质量、相同浓度的过氧化氢溶液,其中一份(用A表示)直接加热制取氧气,在另一份(用B表示)中加入少量的二氧化
分别取两份相同质量、相同浓度的过氧化氢溶液,其中一份(用A表示)直接加热制取氧气,在另一份(用B表示)中加入少量的二氧化锰,下列关于A、B的图象正确的是( )
A.
B.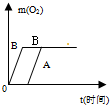
C.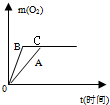
D.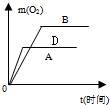
 影舞传说1年前14
影舞传说1年前14 -
 hongfenbufeifei 共回答了16个问题
hongfenbufeifei 共回答了16个问题 |采纳率75%解题思路:催化剂可以加快或减慢化学反应速率,本身不参加反应所以不影响生成物的产量,据此可以解答.本题中过氧化氢溶液质量和浓度相同,所以最后产生氧气的质量相等,但加入二氧化锰会加快过氧化氢分解速率,起始时间又相同,所以C是正确的.
故选C.点评:
本题考点: 催化剂的特点与催化作用.
考点点评: 看图题要求学生把化学原理转化为正确的图象,对学生的思维能力有一定的要求.1年前查看全部
- 8个硫的方程式和离子方程式1.二氧化硫溶液中通入氯气2.向饱和碳酸钠溶液中通入二氧化硫3.向饱和碳酸氢钠溶液中通入二氧化
8个硫的方程式和离子方程式
1.二氧化硫溶液中通入氯气
2.向饱和碳酸钠溶液中通入二氧化硫
3.向饱和碳酸氢钠溶液中通入二氧化硫
4.向氢氧化钠溶液中通入少量的二氧化硫
5.向氢氧化钠溶液中通入多量的二氧化硫
6.亚硫酸氢钠溶液与硫酸氢纳
7.亚硫酸钠电离
8.硫酸氢纳电离 ss19991年前3
ss19991年前3 -
 poison1944 共回答了16个问题
poison1944 共回答了16个问题 |采纳率81.3%SO2+Cl2+2H2O=H2SO4+2HCl
Na2CO3+SO2=Na2SO3+CO2↑
2NaHCO3+SO2=Na2SO3+CO2↑+H2O
2NaOH+SO2=Na2SO3+H2O
NaOH+SO2=NaHSO3
NaHSO3+NaHSO4=Na2SO4+H2O+SO2↑
Na2SO3=2(Na+)+[(SO3)2-]
NaHSO4=(Na+)+[(SO4)2-]+(H+)1年前查看全部
- 在化学知识中有许多规律,下列具体物质的性质符合对应规律的是( ) A.某些非金属氧化物能和碱反应生成盐和水;例如:二氧化
在化学知识中有许多规律,下列具体物质的性质符合对应规律的是( )
A.某些非金属氧化物能和碱反应生成盐和水;例如:二氧化碳和三氧化硫 B.一般固体物质的溶解度随温度的升高而增大;例如:氢氧化钙和氯化钠 C.常温下金属一般为固态;例如:汞和金 D.某些非金属单质可以将金属从其氧化物中还原出来;例如:氢气和一氧化碳  咪渣1年前1
咪渣1年前1 -
 百分百纯咖啡 共回答了22个问题
百分百纯咖啡 共回答了22个问题 |采纳率95.5%A
1年前查看全部
- 强氧化剂都有什么?硝酸HNO3,浓硫酸H2SO4,高锰酸钾K2MnO4,二氧化锰MnO2,重铬酸钾K2Cr2O7,二氧化
强氧化剂都有什么?
硝酸HNO3,浓硫酸H2SO4,高锰酸钾K2MnO4,二氧化锰MnO2,重铬酸钾K2Cr2O7,二氧化铅PbO2,双氧水H2O2,氯气CIO2,除了这些还有什么? 风浅云绻1年前6
风浅云绻1年前6 -
 天堂和地狱之门 共回答了20个问题
天堂和地狱之门 共回答了20个问题 |采纳率80%过二硫酸铵(NH4)2S2O8 铋酸钠 NaBiO3
高铁酸钾K2FeO4 再加上 PbO2 都可在酸性溶液中氧化Mn2+到MnO4- (有的需要Ag+作为催化剂) 都是著名的强氧化剂 ()
F2 XeF2 XeF4 XeF6 XeO3 XeO4 高氙酸盐 (XeO42-)
HBrO4 高溴酸 H5IO6 高碘酸 HClO4(必须热浓)
O3
双氧水H2O2不行
都不行就电解吧.电解是最有力的氧化还原手段.
楼上的那次溴酸:HBrO
次碘酸:HIO 根本就不稳定.
过氧化物只能算作中等强度的氧化剂 .MnO4-可以氧化它们到O2的.1年前查看全部
- 干水如何吸收二氧化碳今年中考考的,我填的是SiO2+2H2O+4CO2=Si[HCO3]4题目说能快速且大量地吸收二氧化
干水如何吸收二氧化碳
今年中考考的,我填的是SiO2+2H2O+4CO2=Si[HCO3]4
题目说能快速且大量地吸收二氧化碳 gulanjin1年前1
gulanjin1年前1 -
 jerry1987212 共回答了21个问题
jerry1987212 共回答了21个问题 |采纳率95.2%这个题应该拿到高中来考!
反应原理:强酸制弱酸,硅酸酸性比碳酸弱,硅酸是胶状沉淀.
反应式:H2O+CO2=H2CO3
H2CO3+SiO2=H2SiO3(胶状沉淀)+CO2
干水是一个粒子包含一滴水,SiO2在每滴水的表面.在第二个式子中可以看出CO2在(水中)生成的同时,硅酸也在每个粒子表面生成,减少其透气性,直到几乎没有气体出入,从而达到吸收CO2的目的.1年前查看全部
- 元素周期表的13原子怎么读?二氧化猛制取氧气的化学方程式
 fei天堆堆猪1年前2
fei天堆堆猪1年前2 -
 娃哈哈ql685 共回答了15个问题
娃哈哈ql685 共回答了15个问题 |采纳率86.7%是铝吗? 读“吕”
二氧化锰可以和氯酸钾加热制氧气
2KCLO3(二氧化锰催化加热)=2KCL+3O2
望采纳~~1年前查看全部
大家在问
- 1甲乙两队修人数的比为7:3,如果从甲队派出30人到乙队,则人数比为3:2,甲乙两个修路队原来个有多少人?
- 2已知函数f(x)=[1/3x3−ax2+(a2−1)x+b(a,b∈R).
- 3设f(x)的导函数是f′(x0),若f′(x0)=1,则lim△x→0f(x0+2△x)−f(x0)△x=______.
- 4下面的计算是否正确?如有错误请改正 求解呀 速度呀 大侠们
- 5已知二叉树有50个叶子节点,则该二叉树的家点数至少为多少?最多为多少
- 6设f(x)是定义在区间负无穷到正无穷上以2为周期的函数,对K属于整数,用I*k表示区间2k-1,2k+1,已知当X属于
- 7《风雨哈佛路》英文观后感高中水平100词
- 8There are some things humans can go without. We can lose a k
- 9缺词填空Why do we like T-shirts?What will you choose to wear if
- 10Just because a camera is old does not mean it is valuable. 这
- 11画一次函数的图像时只需要在直角坐标系中描出几个点?再过这几个点作什么就可以了?
- 12(2014•江西一模)甲、乙两种固体物质的溶解度曲线如图所示.
- 13the baby can't wait () his mother
- 14It's a good way to do some warm-up exercises before _____ ba
- 15(2011•重庆模拟)如图所示,MN是一荧光屏,当带电粒子打到荧光屏上时,荧光屏能够发光.MN的上方有磁感应强度为B的匀
