(2013•琼海一模)如图为北半球示意图,若箭头表示洋流动力方向,则该洋流是( )
 凌蓝忧舞2022-10-04 11:39:541条回答
凌蓝忧舞2022-10-04 11:39:541条回答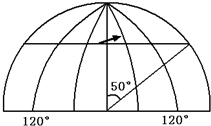 (2013•琼海一模)如图为北半球示意图,若箭头表示洋流动力方向,则该洋流是( )
(2013•琼海一模)如图为北半球示意图,若箭头表示洋流动力方向,则该洋流是( )A.西风漂流
B.日本暖流
C.墨西哥湾暖流
D.北太平洋暖流

已提交,审核后显示!提交回复
共1条回复
 wangzf87 共回答了15个问题
wangzf87 共回答了15个问题 |采纳率73.3%- 解题思路:本题考查世界主要洋流的分布.解答时要根据经纬网确定该洋流所在海域,从而判断该洋流名称.
读图分析:①该洋流在该动力的作用下自西向东运动;
②相邻经线的经度差是30°,图中有两条120°经线.根据经度的变化规律,可推断图中的西侧为120°E,东侧为120°W;
③图中已知角度50°,可判断该纬线是40°N.综合②③,可确定该洋流分布在北太平洋中纬度海域;
结合世界洋流的分布及上述信息,可判断该洋流是北太平洋暖流.
故选:D.点评:
本题考点: 世界洋流分布规律.
考点点评: 本题关键是确定洋流所在的海域. - 1年前
相关推荐
- (2011•琼海一模)如图所示,A、B两物体叠放在水平地面上,A与B之间M、B与地面之间的动摩擦因数均为0.50,A物体
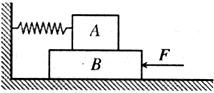 (2011•琼海一模)如图所示,A、B两物体叠放在水平地面上,A与B之间M、B与地面之间的动摩擦因数均为0.50,A物体质量m=30kg,B物体质量为l0kg.处于水平位置的轻弹簧一端固定于墙壁,另一端与A物体相连,弹簧处于自然状态,其劲度系数为250N/m.现有一水平推力F作用于物体B上,使B缓慢地向墙壁移动,当移动到某处时,A、B间开始发生相对滑动,此时水平推力F的大小为______N,在此过程中物体A的位移为______m.(g取l0m/s2)
(2011•琼海一模)如图所示,A、B两物体叠放在水平地面上,A与B之间M、B与地面之间的动摩擦因数均为0.50,A物体质量m=30kg,B物体质量为l0kg.处于水平位置的轻弹簧一端固定于墙壁,另一端与A物体相连,弹簧处于自然状态,其劲度系数为250N/m.现有一水平推力F作用于物体B上,使B缓慢地向墙壁移动,当移动到某处时,A、B间开始发生相对滑动,此时水平推力F的大小为______N,在此过程中物体A的位移为______m.(g取l0m/s2)  arther19821年前1
arther19821年前1 -
 momo1691 共回答了22个问题
momo1691 共回答了22个问题 |采纳率72.7%解题思路:A、B间开始发生相对滑动,对B进行受力分析,根据共点力平衡求出水平推力的大小.对A进行受力分析求出弹簧的弹力,根据胡克定律求出弹簧的形变量,从而求出物体A的位移.A、B间开始发生相对滑动,B在水平方向上受到推力F,地面对B的摩擦力f1,A对B的摩擦力f2,地面的摩擦力f1=μ(mA+mB)g=0.5×400N=200N.A对B的摩擦力大小f2=μmAg=150N.则F=f1+f2=350N.
对A在水平方向上受到摩擦力和弹簧的弹力,有F弹=f2=kx,解得:x=
f2
k=
150
250m=0.6m.所以物体A的位移为0.6m.
故答案为:350,0.6.点评:
本题考点: 胡克定律;共点力平衡的条件及其应用.
考点点评: 解决本题的关键能够正确地进行受力分析,运用共点力平衡进行求解.以及掌握胡克定律.1年前查看全部
- (2013•琼海模拟)某活动小组利用图甲装置验证机械能守恒定律.钢球自由下落过程中,先后通过光电门A、B,计时装置测出钢
 z1ojb1年前1
z1ojb1年前1 -
 5122836 共回答了18个问题
5122836 共回答了18个问题 |采纳率83.3%解题思路:(1)解决本题的关键掌握游标卡尺读数的方法,主尺读数加上游标读数,不需估读.
(2)利用小球通过光电门的平均速度来代替瞬时速度,由此可以求出小铁球通过光电门时的瞬时速度,根据机械能守恒的表达式可以求出所要求的关系式.(1)游标卡尺的主尺读数为:0.9cm,游标尺上第10个刻度和主尺上某一刻度对齐,所以游标读数为0.05×10mm=0.50mm,
所以最终读数为:0.950cm=9.50mm.
(2)利用小球通过光电门的平均速度来代替瞬时速度,故:v=
D/ t],
根据机械能守恒的表达式有:mgh=[1/2]mD2(
1
t2B-
1
t2A );
即只要比较D2(
1
t2B-
1
t2A )与2gh是否相等,
故答案为:(1)9.50;(2)D2(
1
t2B-
1
t2A ).点评:
本题考点: 验证机械能守恒定律.
考点点评: 对于基本测量仪器如游标卡尺、螺旋测微器等要了解其原理,正确使用这些基本仪器进行有关测量.
无论采用什么样的方法来验证机械能守恒,明确其实验原理都是解决问题的关键,同时在处理数据时,要灵活应用所学运动学的基本规律.1年前查看全部
- (2014•琼海二模)下列各式计算正确的是( )
(2014•琼海二模)下列各式计算正确的是( )
A.2a3-a3=2
B.a3•a2=a6
C.a6÷a3=a3
D.(a3)2=a9 理想在1年前1
理想在1年前1 -
 破天2000 共回答了17个问题
破天2000 共回答了17个问题 |采纳率88.2%解题思路:根据合并同类项法则,同底数幂相乘,底数不变指数相加;同底数幂相除,底数不变指数相减;幂的乘方,底数不变指数相乘,对各选项分析判断后利用排除法求解.A、2a3-a3=a3,故本选项错误;
B、a3•a2=a3+2=a5,故本选项错误;
C、a6÷a3=a6-3=a3,故本选项正确;
D、(a3)2=a3×2=a6,故本选项错误.
故选C.点评:
本题考点: 同底数幂的除法;合并同类项;同底数幂的乘法;幂的乘方与积的乘方.
考点点评: 本题考查了同底数幂的乘法,同底数幂的除法,幂的乘方的性质,熟记性质并理清指数的变化情况是解题的关键.1年前查看全部
- (2011•琼海一模)按如图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液.通电一段时间后,c
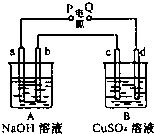 (2011•琼海一模)按如图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液.通电一段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).a、b、c为石墨电极,d为铜电极.
(2011•琼海一模)按如图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液.通电一段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).a、b、c为石墨电极,d为铜电极.
(1)电源P极为______极
(2)a极上所发生的电极反应式为______
(3)标准状况下,b极产生气体的体积为______
(4)c极上析出固体的质量为______. 天之痕迹1年前1
天之痕迹1年前1 -
 6号邮差 共回答了20个问题
6号邮差 共回答了20个问题 |采纳率85%解题思路:c极上有Cu析出,说明c为电解池的阴极,d为阳极,则P为负极,Q为正极,A为电解NaOH溶液,实质上为电极水,B为电解硫酸铜溶液,在阴极析出铜,电极反应:Cu2++2e-=Cu,阳极生成氧气,发生4OH--4e-=2H2O+O2↑,结合电极方程式计算.(1)c极上有Cu析出,说明c为电解池的阴极,d为阳极,则P为负极,故答案为:负;
(2)a极电解池的阴极,发生还原反应,生成氢气,电极方程式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)被电解的水的质量为4.5g,n(H2O)=[4.5g/18g/mol]=0.25mol,A总反应式为2H2O
电解
.
2H2↑+O2↑,由此可知b电极生成氧气0.125mol,标准状况下体积=0.125mol×22.4L/mol=2.8L;
故答案为:2.8L;
(4)b电极为阳极,溶液中氢氧根离子失电子生成氧气,电极反应为4OH--4e-═2H2O+O2↑,依据(3)计算得到氧气为0.125mol,电子转移为0.125mol×4=0.5mol;C电极析出的是铜,由电极反应Cu2++2e-═Cu,计算得到生成铜物质的量为0.25mol,质量=0.25mol×64g/mol=16g;
故答案为:16g.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等.做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.1年前查看全部
- (2011•琼海一模)下列化学用语正确的是( )
(2011•琼海一模)下列化学用语正确的是( )
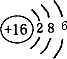
A.硫的原子结构示意图: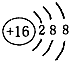
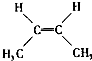
B.顺-2-丁烯的结构简式: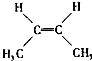
C.乙酸的实验式:C2H4O2
D.原子核内有8个中子的氧原子:188O mimigi1年前1
mimigi1年前1 -
 QQ0721 共回答了20个问题
QQ0721 共回答了20个问题 |采纳率95%1年前查看全部
- (2011•琼海一模)下列溶液中离子浓度的关系一定正确的是( )
(2011•琼海一模)下列溶液中离子浓度的关系一定正确的是( )
A.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(C6H5ONa )>c(NaOH)
B.pH=3的一元酸HX溶液和pH=11的一元碱MOH溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-)
C.NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:2c(H+)+c(HX)═2c(OH-)+c(X-) 成都大河1年前1
成都大河1年前1 -
 愈挫愈用 共回答了19个问题
愈挫愈用 共回答了19个问题 |采纳率89.5%解题思路:A、溶液PH的大小是由溶液中的氢离子浓度大小决定,相同温度下溶液中离子积是常数,题干中的溶液都是显碱性的溶液,有强碱和水解呈碱性的盐,水解程度的大小决定溶液PH的大小,水解程度越大PH越大;
B、若是强酸强碱溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-),若是强酸弱碱溶液,等体积混合溶液显碱性;若是弱酸强碱等体积混合溶液呈酸性;
C、NH4HSO4溶液中滴加NaOH至溶液恰好呈中性,中和氢离子后,和部分铵根反应生成一水合氨;
D、依据溶液中电荷守恒和物料守恒计算得到;A、CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,水解程度Na2CO3溶液>C6H5ONa溶液>CH3COONa溶液,氢氧化钠是强碱,PH相同的溶液中溶质浓度NaOH溶液<Na2CO3溶液<C6H5ONa溶液<CH3COONa溶液;故A错误;
B、若是强酸强碱溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-),若是强酸弱碱溶液,等体积混合溶液显碱性;若是弱酸强碱等体积混合溶液呈酸性;故B错误;
C、溶液中电荷守恒c(Na+)+c(NH4+)+c(H+)=c(OH-)+2c(SO42-)得到:c(Na+)+c(NH4+)=2c(SO42-),依据NH4HSO4溶液中溶质和氢氧根离子反应过程为全部中和氢离子,和铵根离子部分反应,溶液中离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);故C正确;
D、等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:电荷守恒:c(K+)+c(H+)=c(OH-)+c(X-);2c(K+)=c(X-)+c(HX);合并计算得到:2c(H+)+c(HX)═2c(OH-)+c(X-);故D正确;
故选CD.点评:
本题考点: 离子浓度大小的比较;盐类水解的应用;酸碱混合时的定性判断及有关ph的计算.
考点点评: 本题考查了溶液中电荷守恒、物料守恒的计算应用,溶液中离子浓度大小比较的分析判断,酸碱反应后溶液酸碱性的分析判断,题目难度中等.1年前查看全部
- (2011•琼海一模)如图棱柱ABCD-A1B1C1D1的底面是菱形,平面AA1C1C⊥平面ABCD;
(2011•琼海一模)如图棱柱ABCD-A1B1C1D1的底面是菱形,平面AA1C1C⊥平面ABCD;

(Ⅰ)求证:BD⊥AA1;
(Ⅱ)设AB=a,∠BAC=30°,四边形AA1C1C的面积为3a2,求棱柱ABCD-A1B1C1D1的体积、 雪中貂鼠1年前1
雪中貂鼠1年前1 -
 一8878 共回答了22个问题
一8878 共回答了22个问题 |采纳率95.5%解题思路:(I)由已知中棱柱ABCD-A1B1C1D1的底面是菱形,平面AA1C1C⊥平面ABCD,我们根据菱形的性质及面面垂直的性质定理,易得BD⊥平面AA1C1C,再由线面垂直的性质,即可得到BD⊥AA1;
(Ⅱ)由已知中AB=a,∠BAC=30°,四边形AA1C1C的面积为3a2,我们可计算出棱柱底面ABCD的面积及高AA1的长度,然后代入棱柱体积公式,即可得到答案.证明:(Ⅰ)∵棱柱ABCD-A1B1C1D1的底面是菱形,
∴AC⊥BD,
又∵平面AA1C1C⊥平面ABCD
∴BD⊥平面AA1C1C
又由AA1⊂平面AA1C1C
∴BD⊥AA1;
(Ⅱ)∵AB=a,∠BAC=30°,
则AC=
3a,BD=a
∴SABCD=2×[1/2]AB•AD•sin∠A=
3
2a2
又四边形AA1C1C的面积为3a2,
∴AA1=
3a,
∴V=AA1•SABCD=
3
2a2点评:
本题考点: 直线与平面垂直的性质;棱柱、棱锥、棱台的体积.
考点点评: 本题考查的知识点是直线与平面垂直的性质,棱柱的体积,熟练掌握空间直线与直线、直线与平面、平面与平面之间垂直关系的相互转化是解答本题的关键.1年前查看全部
- (2014•琼海一模)不等式2x-6>0的解集为( )
(2014•琼海一模)不等式2x-6>0的解集为( )
A.x>3
B.x<-3
C.x<3
D.x<-3 雾夜飘渺1年前1
雾夜飘渺1年前1 -
 胡说八道008 共回答了27个问题
胡说八道008 共回答了27个问题 |采纳率96.3%解题思路:先移项,再把x的系数化为1即可.移项得,2x>6,
x的系数化为1得,x>3.
故选A.点评:
本题考点: 解一元一次不等式.
考点点评: 本题考查的是解一元一次不等式,熟知不等式的基本步骤是解答此题的关键.1年前查看全部
- (2011•琼海一模)I.科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环
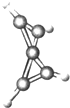 (2011•琼海一模)I.科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是______
(2011•琼海一模)I.科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是______
A.烃X的分子式为C5H4
B.分子中碳原子的化学环境有2种
C.具有2个三元环的X的同分异构体共2种(含本身)
D.X分子中只有碳碳单键,没有碳碳双键
II.分子式为C6H12O的醛应有______
A.5种B.6种C.8种D.9种
III.现有A、B两种有机化合物,已知:
①它们的分子中含有相同数目的碳原子和氧原子,B可以看成A中一个氢原子被氨基取代得到;
②它们的分子中氢元素的质量分数相同,相对分子质量都不超过170,A中碳元素的质量分数为72.00%;
③它们都是一取代苯,分子中都没有甲基,都有一个羧基.
请按要求填空:
(1)A、B的分子中氢元素的质量分数都是______;
(2)A的结构简式是______;
(3)A有一同分异构体C是对位二取代苯,能发生银镜反应也能与金属钠反应,但官能团不直接与苯环相连,C的结构简式是______;
(4)B有一同分异构体D是苯环上的一硝基化合物,其苯环和侧链上的一溴代物各有两种,D的结构简式是______. 爱an心1年前1
爱an心1年前1 -
 fuhaipu 共回答了16个问题
fuhaipu 共回答了16个问题 |采纳率100%解题思路:Ⅰ.A.由球棍模型可知,烃X的分子式为C5H4;
B.分子中存在连接H原子C原子与没有连接H原子的碳原子2种碳原子;
C.具有2个三元环的X的同分异构体,应是2个碳原子为2个三元环共用,则含有1个甲基,还含有1个碳碳双键,甲基与碳碳双键处于不同三元环时,有1种,甲基与碳碳双键处于同一个三元环内时,有2种;
D.X分子中含有2个碳碳双键;
Ⅱ.分子式为C6H12O的醛可以看做-CHO取代戊烷得到,根据戊烷同分异构体,结合等效氢进行判断;
Ⅲ.(1)(2)因B可看成A中1个氢原子被-NH2取代得到,A、B两者碳原子、氧原子分别相等,氢元素百分含量相等,所以设A的摩尔质量为M,A中氢原子个数为a,则 [a/M]×100%=[a+1/M+15]×100%,得到:M=15a,所以A中w(H)=[a/M]×100%=[a/15a]×100%=6.67%,所以A中w(O)=1-72%-6.67%=21.33%,A中C:H:O=[72%/12]:[6.67%/1]:[21.33%/16]=9:10:2,所以A分子式为(C9H10O2)x,因Mr(A)<170,所以x=1,即分子式为C9H10O2,故B的分子式为C9H11NO2.有机物A为一取代苯,分子中不含甲基,含有一个羧基,故A的结构简式为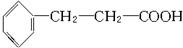 ;
;
(3)C与A互为同分异构体,分子中也没有甲基,但苯环上有两个处于对位的取代基,能发生银镜反应,含有-CHO或-OOCH,能在一定条件下发生消去反应,应含有醇羟基,故C含有的基团为-CHO、-CH2CH2OH;
(4)B有一同分异构体D是苯环上的一硝基化合物,其苯环和侧链上的一溴代物各有两种,则D为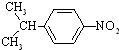 .
.
Ⅰ.A.由球棍模型可知,烃X的分子式为C5H4,故A正确;
B.分子中存在连接H原子C原子与没有连接H原子的碳原子2种碳原子,故B正确;
C.具有2个三元环的X的同分异构体,应是2个碳原子为2个三元环共用,则含有1个甲基,还含有1个碳碳双键,甲基与碳碳双键处于不同三元环时,有1种,甲基与碳碳双键同一个三元环内时,有2种,包含X在内共有4种,故C错误;
D.X分子中含有2个碳碳双键,故D错误,
故选:CD;
Ⅱ.分子式为C6H12O的醛可以看做-CHO取代戊烷得到,戊烷同分异构体有正戊烷、异戊烷、新戊烷,正戊烷有3种H原子,故形成的醛有3种,异戊烷有4种H原子,形成的醛有4种,新戊烷有1种H原子,侧重的醛有一种,故分子式为C6H12O的醛有3+4+1=8种,故选:C;
Ⅲ.(1)因B可看成A中1个氢原子被-NH2取代得到,A、B两者碳原子、氧原子分别相等,氢元素百分含量相等,所以设A的摩尔质量为M,A中氢原子个数为a,则 [a/M]×100%=[a+1/M+15]×100%,得到:M=15a,所以A中w(H)=[a/M]×100%=[a/15a]×100%=6.67%,故答案为:6.67%;
(2)A中w(O)=1-72%-6.67%=21.33%,A分子中N(C):N(H):N(O)=[72%/12]:[6.67%/1]:[21.33%/16]=9:10:2,所以A分子式为(C9H10O2)x,因Mr(A)<170,所以x=1,即分子式为C9H10O2,有机物A为一取代苯,分子中不含甲基,含有一个羧基,故A的结构简式为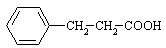 ,故答案为:
,故答案为: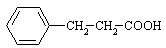 ;
;
(3)C与A互为同分异构体,分子中也没有甲基,但苯环上有两个处于对位的取代基,能发生银镜反应,含有-CHO或-OOCH,能在一定条件下发生消去反应,应含有醇羟基,故C含有的基团为-CHO、-CH2CH2OH,故C的结构简式为 ;
;
(4)B可以看成A中一个氢原子被氨基取代得到,则B的分子式为C9H11NO2,B有一同分异构体D是苯环上的一硝基化合物,其苯环和侧链上的一溴代物各有两种,则D为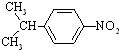 ,故答案为:
,故答案为: .
.点评:
本题考点: 有机物的推断;同分异构现象和同分异构体.
考点点评: 本题考查有机物结构、有机物的推断、官能团的性质、同分异构体的书写等,难度较大,Ⅲ中计算确定A分子氢元素的质量分数是解题的关键.1年前查看全部
- (2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处
(2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处SO42-从右向左移动.下列分析正确的是( )
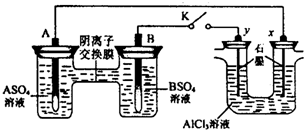
A. 溶液中c(A2+)浓度减小
B. B的电极反应:B-2e-═B2+
C. y电极上有H2产生,发生还原反应
D. 反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 极品红杏1年前1
极品红杏1年前1 -
 wys20066 共回答了14个问题
wys20066 共回答了14个问题 |采纳率78.6%解题思路:该装置中右边装置不能自发的进行氧化还原反应是不能构成原电池只能形成电解池,左边装置中能发生的进行氧化还原反应且符合原电池的构成条件所以是原电池.当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,即A的金属活动性大于B;连接B的y极为Y阳极,连接A的x极为阴极.A、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,原电池中负极A上金属失电子发生氧化反应,生成金属阳离子进入溶液导致溶液中(A2+)浓度增大,故A错误;
B、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,B极上溶液中的金属阳离子得电子生成金属单质,电极反应式为B2++2e-═B,故B错误;
C、右边装置中连接B的y极为阳极,连接A的x极为阴极,电解池工作时,y极上氯离子失电子发生氧化反应,电极反应式为2Cl--2e-═Cl2↑,故C错误;
D、右边装置中y极上发生的电极反应式为2Cl--2e-═Cl2↑,x极上发生的电极反应式为2H++2e-═H2↑,由于氢离子放电而氢氧根离子不放电导致溶液呈碱性,铝离子和氢氧根离子反应生成难溶性的氢氧化铝,氢氧化铝和氢氧化钠反应生成可溶性的偏铝酸钠,故D正确.
故选:D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池和电解池原理,难度较大,明确原电池放电时溶液中阴阳离子的移动方向是解本题的关键.1年前查看全部
- (2011•琼海一模)某市投资甲、乙两个工厂,2008年两工厂的产量均为100万吨,在今后的若干年内,甲工厂的年产量每年
(2011•琼海一模)某市投资甲、乙两个工厂,2008年两工厂的产量均为100万吨,在今后的若干年内,甲工厂的年产量每年比上一年增加10万吨,乙工厂第n年比上一年增加2n-1万吨,记2008年为第一年,甲、乙两工厂第n年的年产量分别为an万吨和bn万吨.
(Ⅰ)求数列{an},{bn}的通项公式;
(Ⅱ)若某工厂年产量超过另一工厂年产量的2倍,则将另一工厂兼并,问到哪一年底,其中哪一个工厂被另一个工厂兼并. ee城商铺1年前1
ee城商铺1年前1 -
 林海别天 共回答了17个问题
林海别天 共回答了17个问题 |采纳率82.4%解题思路:(Ⅰ)由题意知,甲、乙两工厂第n年的年产量分别为an万吨和bn万吨.甲工厂第n年的年产量是一个等差数列的项,其首项为100,公差是10,而乙工厂的第n年的年产量是一个是一个累加和为bn=100+2+22+23+…+2n-1,故数列{an},{bn}的通项公式易得;
(Ⅱ)比较两个通项公式,根据情况求出年份即可(Ⅰ)由题得an=10n+90,bn=100+2+22+23+…+2n-1=100+
2(1−2n−1)
1−2=2n+98
(Ⅱ)由于n,各年的产量如下表
n 1 2 3 4 5 6 7 8
an
100 110 120 130 140 150 160 170
bn 100 102 106 114 130 162 226 354,由表知2015年底甲工厂将被乙工厂兼并.点评:
本题考点: 等差数列与等比数列的综合.
考点点评: 本题考查等差数列与等比数列的综合,考查用数列解决实际问题,其步骤是建立数列模型,进行计算得出结果,再反馈到实际中去解决问题.由于比较两个工厂的产量时两个函数的形式较特殊,不易求解,故采取了列举法,数据列举时作表格比较简捷.1年前查看全部
- (2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
(2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
A. (1,2)
B. (0,0)
C. (
,1)1 2
D. (1,4) freshmanqh1年前1
freshmanqh1年前1 -
 refreshingtea 共回答了15个问题
refreshingtea 共回答了15个问题 |采纳率100%解题思路:根据题意,直线y=4x-5必然与抛物线y=4x2相离,抛物线上的点到直线的最短距离就是与直线y=4x-5平行的抛物线的切线的切点.y'=8x,由8x=4得x=
1
2,
故抛物线的斜率为4的切线的切点坐标是(
1
2,1),
该点到直线y=4x-5的距离是最短.
故选C.点评:
本题考点: 点到直线的距离公式;抛物线的简单性质.
考点点评: 主要考查了导数及其应用,本题以数形结合思想为指导命制,通过形的分析把问题转化为求抛物线的斜率为4的切线的切点坐标.本题也可以直接根据点到直线的距离公式求解,即抛物线上的点到直线y=4x-5的距离是d=|4x−y−5|17=|4x−4x2−5|17=4(x−12)2+417,显然这个函数当x=12时取得最小值,此时y=1.1年前查看全部
- (2011•琼海一模)1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方
 (2011•琼海一模)1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-styletemple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
(2011•琼海一模)1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-styletemple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
A.分子式为C20H20
B.一氯代物的同分异构体只有两种
C.分子中含有二个亚甲基(-CH2-)
D.分子中含有4个五元碳环 hm49t1年前1
hm49t1年前1 -
 lotus2007 共回答了20个问题
lotus2007 共回答了20个问题 |采纳率95%解题思路:A、根据庙宇烷的结构数出分子中的C、H原子数目,交点是C原子,利用H原子饱和碳的四价结构.
B、庙宇烷具有一定的对称性,所以在寻找一氯代物时要将相同的位置合并,在该烷中有三种不同的C可发生一氯取代,即分别位于檐部、肩部和顶部的C原子.
C、由庙宇烷的结构可知,分子中含有4个-CH2-.
D、由庙宇烷的结构可知,分子的每个面均为五元碳环.A、根据庙宇烷的结构可知,分子中含有20个C原子、20个H原子,所以庙宇烷分子式为C20H20,故A正确;
B、庙宇烷具有一定的对称性,分子中又三种不同的H原子,即分别位于檐部、肩部和顶部的C原子,在该烷中有三种不同的C可发生一氯取代,故B错误;
C、由庙宇烷的结构可知,分子中含有4个-CH2-,故C错误;
D、由庙宇烷的结构可知,分子的每个面均为五元碳环,共12个五元环,故D错误.
故选:A.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题考查的是有机物结构、同分异构体等,难度中等,细心观察结构进行解答.1年前查看全部
- (2014•琼海二模)一元二次方程x2+3x=0的解是( )
(2014•琼海二模)一元二次方程x2+3x=0的解是( )
A. x=-3
B. x1=0,x2=3
C. x1=0,x2=-3
D. x=3 sherong1年前2
sherong1年前2 -
 cara4857 共回答了25个问题
cara4857 共回答了25个问题 |采纳率92%解题思路:分解因式得到x(x+3)=0,转化成方程x=0,x+3=0,求出方程的解即可.x2+3x=0,
x(x+3)=0,
x=0,x+3=0,
x1=0,x2=-3,
故选:C.点评:
本题考点: 解一元二次方程-因式分解法;因式分解-十字相乘法等;解一元一次方程.
考点点评: 本题主要考查对解一元二次方程,解一元一次方程,因式分解等知识点的理解和掌握,能把一元二次方程转化成一元一次方程是解此题的关键.1年前查看全部
- (2014•琼海二模)(1)计算:4×(-[1/16])-2cos60°+(2+π)0+2-2;
(2014•琼海二模)(1)计算:4×(-[1/16])-2cos60°+(2+π)0+2-2;
(2)解不等式组:
.x−1<3 2x>−6  李续欢1年前1
李续欢1年前1 -
 lanhuo001 共回答了20个问题
lanhuo001 共回答了20个问题 |采纳率85%解题思路:(1)根据零指数幂、乘方、特殊角的三角函数值、四个考点,针对每个考点分别进行计算,然后根据实数的运算法则求得计算结果;
(2)根据解不等式的步骤,可得不等式解集,根据不等式解集的公共部分,可得不等式组的解集.(1)原式=-[1/4−2×
1
2+1+
1
4]
=0;
(2)由①得:x<4
由②得:x>-3
∴此不等式组的解集为-3<x<4.点评:
本题考点: 实数的运算;零指数幂;负整数指数幂;解一元一次不等式组;特殊角的三角函数值.
考点点评: 本题考查实数的综合运算能力,是各地中考题中常见的计算题型.解决此类题目的关键是熟记特殊角的三角函数值,熟练掌握负整数指数幂、零指数幂、二次根式、绝对值等考点的运算.1年前查看全部
- (e9图e•琼海一模)某学生欲完成eHCl+eAg═eAgCl↓+He↑反应,设计了e列四个实验,你认为可行的实验是(
(e9图e•琼海一模)某学生欲完成eHCl+eAg═eAgCl↓+He↑反应,设计了e列四个实验,你认为可行的实验是( )
A.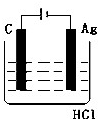
B.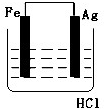
C.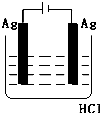
D.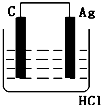
 trend7871年前1
trend7871年前1 -
 zqllz 共回答了15个问题
zqllz 共回答了15个问题 |采纳率86.7%解题思路:盐酸和银不能自发的进行氧化还原反应,所以不能设计成原电池,只能设计成电解池,失电子的物质作电解池阳极,金属或导电的非金属作电解池阴极,失电子的物质作电解质溶液.6H地下+6Ag=6Ag地下↓+H6↑不能自发进行,所以必须设计成电解池,该反应中银失电子,所以银作电解池阳极,金属或导电的非金属作电解池阴极,该反应中氯化氢大电子生成氢气,则选取盐酸作电解质溶液,所以地选项符合条件,
故选地.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查原电池和电解池原理,明确原电池形成条件是解本题的关键,注意原电池必须是自发的进行氧化还原反应,为易错点.1年前查看全部
- (2013•琼海模拟)如图所示,细线的一端固定于O点,另一端系一小球.在水平拉力F作用下,小球以恒定速率在竖直平面内由A
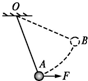 (2013•琼海模拟)如图所示,细线的一端固定于O点,另一端系一小球.在水平拉力F作用下,小球以恒定速率在竖直平面内由A点运动到B点.在此过程中下列说法正确的是( )
(2013•琼海模拟)如图所示,细线的一端固定于O点,另一端系一小球.在水平拉力F作用下,小球以恒定速率在竖直平面内由A点运动到B点.在此过程中下列说法正确的是( )
A.细线对小球的拉力和小球对细线的拉力相互平衡
B.小球所受合外力不为零,但合外力对小球做功为零
C.细线对小球的拉力做正功
D.小球的机械能增加 刀剑君1年前1
刀剑君1年前1 -
 6877410 共回答了16个问题
6877410 共回答了16个问题 |采纳率87.5%解题思路:小球做匀速圆周运动,合外力提供向心力,对其受力分析,受拉力F、重力G、绳子的拉力T,根据功能关系列式求解.A、细线对小球的拉力和小球对细线的拉力是一对作用力和反作用力,不是平衡力,故A错误;
B、小球做匀速圆周运动,合外力提供向心力,合外力不为零,小球匀速率运动,动能不变,根据动能定理,合力做功为零,故B正确;
C、细线对小球的拉力与运动方向始终垂直,不做功,故C错误;
D、小球匀速率运动,重力势能增加,动能不变,故机械能增加,故D正确;
故选:BD.点评:
本题考点: 功的计算.
考点点评: 本题解题的关键点是小球的速率不变,动能不变,细线对小球的拉力与运动方向始终垂直,不做功,难度不大,属于基础题.1年前查看全部
- (2013•琼海一模)如图为经纬网图,设A、B两地和A、D两地之间的距离分别为S1和S2,则( )
(2013•琼海一模)如图为经纬网图,设A、B两地和A、D两地之间的距离分别为S1和S2,则( )
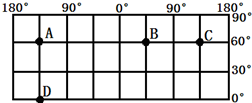
A.S1=0.5S2
B.S1=S2
C.S1=1.5S2
D.S1=2S2 夏天的一把火1年前1
夏天的一把火1年前1 -
 郑副主任 共回答了16个问题
郑副主任 共回答了16个问题 |采纳率100%解题思路:地球自转的线速度由赤道向两极递减,纬线长度赤道最大.根据经纬度的变化可以判断,A、B两地经度差为180°,A、D两地纬度差为60°,60°纬线长度为赤道(经线)处一半,可以判断S1=1.5S2.
故选:C.点评:
本题考点: 地球自转的特征.
考点点评: 主要考查了经纬网相关知识.1年前查看全部
- (2011•琼海一模)欧阳修《卖油翁》中写到:(翁)乃取一葫芦置于地,以钱覆其口,徐以杓酌油沥之,自钱孔入,而钱不湿.可
(2011•琼海一模)欧阳修《卖油翁》中写到:(翁)乃取一葫芦置于地,以钱覆其口,徐以杓酌油沥之,自钱孔入,而钱不湿.可见“行行出状元”,卖油翁的技艺让人叹为观止.若铜钱是直径为3cm的圆,中间有边长为1cm的正方形孔,若你随机向铜钱上滴一滴油,则油(油滴的大小忽略不计)正好落入孔中的概率是( )
A.[9π/4]
B.[9/4π]
C.[4π/9]
D.[4/9π] xmjcook1年前0
xmjcook1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•琼海一模)某烷烃的结构简式为:有甲、乙、丙、丁四个同学将其命名依次为:2,2二甲基4乙基戊烷;3,5,5三甲
(2011•琼海一模)某烷烃的结构简式为:
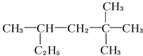 有甲、乙、丙、丁四个同学将其命名依次为:2,2二甲基4乙基戊烷;3,5,5三甲基己烷;4,4二甲基2乙基戊烷;2,2,4三甲基己烷.下列对四位同学的命名判断中正确的是( )
有甲、乙、丙、丁四个同学将其命名依次为:2,2二甲基4乙基戊烷;3,5,5三甲基己烷;4,4二甲基2乙基戊烷;2,2,4三甲基己烷.下列对四位同学的命名判断中正确的是( )
A.甲的命名主链选择是正确的
B.乙的命名编号是错误的
C.丙的命名主链选择是正确的
D.丁的命名是正确的 mroywx1年前1
mroywx1年前1 -
 小--宇--一 共回答了19个问题
小--宇--一 共回答了19个问题 |采纳率94.7%解题思路:烷烃的命名原则:碳链最长称某烷,靠近支链把号编.简单在前同相并,其间应划一短线.
1、碳链最长称某烷:选定分子里最长的碳链做主链,并按主链上碳原子数目称为“某烷“.
2、靠近支链把号编:把主链里离支链较近的一端作为起点,用1、2、3…等数字给主链的各碳原子编号定位以确定支链的位置.
3、简单在前同相并,其间应划一短线:把支链作为取代基,把取代基的名称写在烷烃名称的前面,在取代基的前面用阿拉伯数字注明它在烷烃主链上的位置,而且简单的取代基要写在复杂的取代基前面,如果有相同的取代基,则要合并起来用二、三等数字表示,但是表示相同的取代基位置的阿拉伯数字要用逗号隔开,并在号数后面连一短线,中间用“-“隔开. ,最长碳链含有6个C,主链为己烷;编号从右边开始,在2号C有两个甲基、在4号C有一个甲基,该有机物命名为:2、2、4-三甲基己烷,
,最长碳链含有6个C,主链为己烷;编号从右边开始,在2号C有两个甲基、在4号C有一个甲基,该有机物命名为:2、2、4-三甲基己烷,
A、甲的命名中主链为戊烷,选取的主链是错误的,故A错误;
B、乙选取的主链正确,但是编号是错误的,故B正确;
C、丙选取的主链为戊烷是错误的,正确为己烷,故C错误;
D、该有机物命名为:2、2、4-三甲基己烷,丁的命名正确,故D正确;
故选BD.点评:
本题考点: 烷烃及其命名.
考点点评: 本题考查了考查有机物的命名,题目难度不大,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.1年前查看全部
- (2011•琼海一模)如图,实线表示某电场的电场线,一个带负电的粒子沿虚线所示的路径从a点运动到b点,则( )
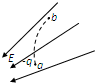 (2011•琼海一模)如图,实线表示某电场的电场线,一个带负电的粒子沿虚线所示的路径从a点运动到b点,则( )
(2011•琼海一模)如图,实线表示某电场的电场线,一个带负电的粒子沿虚线所示的路径从a点运动到b点,则( )
A.带电粒子所受电场力变大
B.带电粒子所受电场力变小
C.带电粒子的电势能变大
D.带电粒子的电势能变小 summerplus1年前1
summerplus1年前1 -
 荣蓉 共回答了15个问题
荣蓉 共回答了15个问题 |采纳率100%解题思路:电场线的疏密表示电场强度的强弱,沿电场方向电势降低.A、电场线的疏密表示电场强度的强弱,从a点运动到b点,电场线变疏,场强变小,所以带电粒子所受电场力变小,故A错误,B正确.
C、沿电场方向电势降低,从a点运动到b点,电势升高,根据电势能表达式Ep=qφ,由于是一个带负电的粒子,所以从a点运动到b点,带电粒子的电势能变小,故C错误、D正确.
故选BD.点评:
本题考点: 电场强度;电势.
考点点评: 电场线的概念是电场中的重要概念,该概念包含物理信息较多,要加强理解和应用.1年前查看全部
- (2014•琼海一模)某班抽6名同学参加体能测试,成绩分别是80,90,75,75,80,80.则这组同学的测试成绩的中
(2014•琼海一模)某班抽6名同学参加体能测试,成绩分别是80,90,75,75,80,80.则这组同学的测试成绩的中位数是( )
A.75
B.80
C.85
D.90 非视1年前1
非视1年前1 -
 丹辰子-1 共回答了15个问题
丹辰子-1 共回答了15个问题 |采纳率86.7%解题思路:中位数是指将一组数据按大小顺序排列后,处在最中间的一个数(或处在最中间的两个数的平均数).将这组数据从小到大的顺序排列为:75,75,80,80,80,90,
中位数是(80+80)÷2=80.
故选:B.点评:
本题考点: 中位数.
考点点评: 考查了确定一组数据的中位数的能力.中位数是将一组数据从小到大(或从大到小)重新排列后,最中间的那个数(最中间两个数的平均数),叫做这组数据的中位数.注意:找中位数的时候一定要先排好顺序,然后再根据奇数和偶数个来确定中位数,如果数据有奇数个,则正中间的数字即为所求.如果是偶数个则找中间两位数的平均数.1年前查看全部
- (2014•琼海二模)海南省2010人口普查数据显示,全省总人口约为8670000,数据8670000用科学记数法表示应
(2014•琼海二模)海南省2010人口普查数据显示,全省总人口约为8670000,数据8670000用科学记数法表示应是( )
A.8.67×106
B.86.7×105
C.8.67×105
D.8.67×107 zyq_txl20041年前1
zyq_txl20041年前1 -
 arken 共回答了13个问题
arken 共回答了13个问题 |采纳率76.9%解题思路:科学记数法的表示形式为a×10n的形式,其中1≤|a|<10,n为整数.确定n的值时,要看把原数变成a时,小数点移动了多少位,n的绝对值与小数点移动的位数相同.当原数绝对值>1时,n是正数;当原数的绝对值<1时,n是负数.8670000=8.67×106.
故选A.点评:
本题考点: 科学记数法—表示较大的数.
考点点评: 此题考查科学记数法的表示方法.科学记数法的表示形式为a×10n的形式,其中1≤|a|<10,n为整数,表示时关键要正确确定a的值以及n的值.1年前查看全部
- (2011•琼海一模)下列物质中,含元素种类由多到少排列正确的是( )
(2011•琼海一模)下列物质中,含元素种类由多到少排列正确的是( )
①液氯;②氨水;③超重水、重水和普通水的混合物;④明矾;⑤水玻璃;⑥天然蛋白质.
A.⑥④⑤②③①
B.④⑥⑤②③①
C.⑥④②⑤③①
D.⑥④⑤②①③ 当当1号1年前1
当当1号1年前1 -
 蓝色的荣耀 共回答了22个问题
蓝色的荣耀 共回答了22个问题 |采纳率86.4%解题思路:①液氯是纯净物,仅含有氯气分子;②氨水是氨气的水溶液;③超重水、重水和普通水是氢元素和氧元素组成的;④明矾是[KAl(SO4)2]•12H2O晶体,属于纯净物;⑤水玻璃是硅酸钠的水溶液;⑥天然蛋白质的组成元素有C、H、N、O,有的还有P、S、Fe、Zn、Cu、B、Mn、I等.①液氯是纯净物,仅含有氯气分子,仅含有氯元素;
②氨水是氨气的水溶液,含有H、O、N元素;
③超重水、重水和普通水都是氢元素和氧元素组成的,含有H元素和氧元素;
④明矾是[KAl(SO4)2]•12H2O晶体,属于纯净物,含有K、Al、S、O、H元素;
⑤水玻璃是硅酸钠的水溶液,含有Na、Si、O、H元素;
⑥天然蛋白质的组成元素有C、H、N、O,有的还有P、S、Fe、Zn、Cu、B、Mn、I等.
故含有元素种类数从多到少依次是⑥④⑤②③①.
故选:A.点评:
本题考点: 物质的组成、结构和性质的关系.
考点点评: 本题考查学生物质的组成元素知识,属于基本知识的考查,难度不大.1年前查看全部
- (2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
(2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
A. (1,2)
B. (0,0)
C. (
,1)1 2
D. (1,4) 鱼露1371年前4
鱼露1371年前4 -
 rising_f 共回答了17个问题
rising_f 共回答了17个问题 |采纳率94.1%解题思路:根据题意,直线y=4x-5必然与抛物线y=4x2相离,抛物线上的点到直线的最短距离就是与直线y=4x-5平行的抛物线的切线的切点.y'=8x,由8x=4得x=
1
2,
故抛物线的斜率为4的切线的切点坐标是(
1
2,1),
该点到直线y=4x-5的距离是最短.
故选C.点评:
本题考点: 点到直线的距离公式;抛物线的简单性质.
考点点评: 主要考查了导数及其应用,本题以数形结合思想为指导命制,通过形的分析把问题转化为求抛物线的斜率为4的切线的切点坐标.本题也可以直接根据点到直线的距离公式求解,即抛物线上的点到直线y=4x-5的距离是d=|4x−y−5|17=|4x−4x2−5|17=4(x−12)2+417,显然这个函数当x=12时取得最小值,此时y=1.1年前查看全部
- (2013•琼海模拟)已知氘核质量为2.0136u,中子质量为1.0087u, 32He核的质量为3.0150
(2013•琼海模拟)已知氘核质量为2.0136u,中子质量为1.0087u,
He核的质量为3.0150u.32
(1)写出两个氘核聚变成
He的核反应方程.32
(2)若两氘核以相等的动能E0=0.35MeV作为对心碰撞即可发生上述核反应,且释放的核能全部转化为机械能,则反应中生成的
He核和中子的动能各是多少?(1u=931.5MeV/c2)32 yuxuelu1年前1
yuxuelu1年前1 -
 陆萧洋 共回答了16个问题
陆萧洋 共回答了16个问题 |采纳率87.5%解题思路:(1)根据电荷数守恒、质量数守恒写出核反应方程.
(2)通过爱因斯坦质能方程求出在核反应中释放的核能.根据动量守恒、能量守恒求出反应中生成的
He核和中子的动能.32(1)根据电荷数守恒、质量数守恒得:12H+12H=23He+01n;
(2)在核反应中质量的亏损为:
△m=2×2.0136u-1.0087u-3.015u=0.0035u
所以释放的核能为:
△E=0.0035×931.5MeV=3.26MeV…①
反应前总动量为0,反应后总动量仍为0,
所以氦核与中子的动量相等.
由EK=
P2
2m得:
EkHe:Ekn=1:3…②
由能量守恒定律得:
EkHe+Ekn=△E+2×0.35…③
由①②③可以算出:EkHe=0.99MeV,Ekn=2.97 MeV.
答:(1)两个氘核聚变成
32He的核反应方程为:12H+12H=23He+01n.
(2)反应中生成的
32He核动能是0.99MeV,中子的动能各是2.97MeV.点评:
本题考点: 爱因斯坦质能方程.
考点点评: 对于核反应书写核反应方程,要抓住微观粒子的碰撞,相当于弹性碰撞,遵守两大守恒:动量守恒和能量守恒.1年前查看全部
- (2012•琼海一模)下列说法正确的是( )
(2012•琼海一模)下列说法正确的是( )
A.pH=2与pH=1的硝酸中c(H+)之比为1:10
B.Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1
C.0.2 mol•L-1醋酸与0.1mol/L醋酸中c (H+)之比为2:1
D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为2:1 幼小心灵1年前1
幼小心灵1年前1 -
 堪破世情堪破胆 共回答了26个问题
堪破世情堪破胆 共回答了26个问题 |采纳率92.3%解题思路:A.强酸溶液中,c(H+)=10-pH;
B.钠离子不水解,碳酸根离子水解,导致n(CO32-)<n(Na2CO3);
C.醋酸是弱酸,在溶液中只有部分电离,且溶液越稀其电离程度越大;
D.根据转移电子数相等确定被氧化的n(NO2)与被还原的n(NO2)之比.A.硝酸是强酸,pH=2的溶液中c(H+)=0.01mol/L,pH=1的硝酸中c(H+)=0.1mol/L,所以两种溶液中氢离子浓度之比为1:10,故A正确;
B.钠离子不水解,碳酸根离子水解,所以碳酸钠溶液中c(Na+):c(CO32-)>2:1,故B错误;
C.醋酸是弱电解质,浓度越大其电离程度越小,所以0.2mol/L醋酸与0.1mol/L醋酸中c (H+)之比小于2:1,故C错误;
D.二氧化氮和水反应方程式为:3NO2+H2O=2HNO3+NO,生成1mol硝酸需要1mol电子,生成1molNO需要2mol电子,要使得失电子数相等,则被氧化的n(NO2)与被还原的n(NO2)之比为2:1,故D正确;
故选AD.点评:
本题考点: pH的简单计算;盐类水解的应用.
考点点评: 本题考查pH的简单计算、氧化还原反应、弱电解质的电离等知识点,注意同一弱电解质的不同溶液,浓度越稀其电离程度越大.1年前查看全部
- (2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处
(2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处SO42-从右向左移动.下列分析正确的是( )

A.溶液中c(A2+)浓度减小
B.B的电极反应:B-2e-═B2+
C.y电极上有H2产生,发生还原反应
D.反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 喜无边1年前1
喜无边1年前1 -
 他说我的游 共回答了17个问题
他说我的游 共回答了17个问题 |采纳率88.2%解题思路:该装置中右边装置不能自发的进行氧化还原反应是不能构成原电池只能形成电解池,左边装置中能发生的进行氧化还原反应且符合原电池的构成条件所以是原电池.当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,即A的金属活动性大于B;连接B的y极为Y阳极,连接A的x极为阴极.A、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,原电池中负极A上金属失电子发生氧化反应,生成金属阳离子进入溶液导致溶液中(A2+)浓度增大,故A错误;
B、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,B极上溶液中的金属阳离子得电子生成金属单质,电极反应式为B2++2e-═B,故B错误;
C、右边装置中连接B的y极为阳极,连接A的x极为阴极,电解池工作时,y极上氯离子失电子发生氧化反应,电极反应式为2Cl--2e-═Cl2↑,故C错误;
D、右边装置中y极上发生的电极反应式为2Cl--2e-═Cl2↑,x极上发生的电极反应式为2H++2e-═H2↑,由于氢离子放电而氢氧根离子不放电导致溶液呈碱性,铝离子和氢氧根离子反应生成难溶性的氢氧化铝,氢氧化铝和氢氧化钠反应生成可溶性的偏铝酸钠,故D正确.
故选:D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池和电解池原理,难度较大,明确原电池放电时溶液中阴阳离子的移动方向是解本题的关键.1年前查看全部
- (2011•琼海一模)某校从参加高三年级第一学期期末考试的学生中抽出50名学生,并统计了他们的数学成绩(成绩均为整数,满
(2011•琼海一模)某校从参加高三年级第一学期期末考试的学生中抽出50名学生,并统计了他们的数学成绩(成绩均为整数,满分为100分),将数学成绩进行分组并根据各组人数制成如下频率分布表:
(Ⅰ)将上面的频率分布表补充完整,并估计本次考试全校85分以上学生的比例;分 组 频 数 频 率 [40,50 ) 2 0.04 [50,60 ) 3 0.06 [60,70 ) 14 0.28 [70,80 ) 15 0.30 [80,90 ) [90,100] 4 0.08 合 计
(Ⅱ)为了帮助成绩差的同学提高数学成绩,学校决定成立“二帮一”小组,即从成绩为[90,100]中任选出两位同学,共同帮助成绩在[40,50)中的某一个同学,试列出所有基本事件;若A1同学成绩为43分,B1同学成绩为95分,求A1、B1两同学恰好被安排在“二帮一”中同一小组的概率. snail111111年前1
snail111111年前1 -
 goniz 共回答了18个问题
goniz 共回答了18个问题 |采纳率94.4%解题思路:(I)利用频率等于频数除以样本容量求出第5行中的值.
(II)列举出所有的二帮一小组的情况,列出A1、B1两同学恰好被安排在“二帮一”中同一小组的情况;利用古典概型的概率公式求出A1、B1两同学恰好被安排在“二帮一”中同一小组的概率.(Ⅰ)第五行的频率=50-(2+3+14+15+4)=12;频率=[12/50]=0.24
因此填入12;0.24
第七行以此填入50;1
估计本次全校85分以上学生比例为[0.24/2+0.08=0.20=20%
(Ⅱ)设数学成绩在[90,100]间的四个同学分别用字母B1,B2,B3,B4表示;被帮助的两个同学为A1,A2
出现的“二帮一”小组有A1B1B2;A1B1B3;A1B1B4;A1B2B3;A1B2B4;A1B3B4
A2B1B2;A2B1B3;A2B1B4;A2B2B3;A2B2B4;A2B3B4
A1、B1两同学恰好被安排在“二帮一”中同一小组的有A1B1B2;A1B1B3;A1B1B4
所以A1、B1两同学恰好被安排在“二帮一”中同一小组的概率为
3
12=
1
4]点评:
本题考点: 频率分布表;等可能事件的概率.
考点点评: 本题考查统计中常用的公式:频率=[频数/样本容量]、解决事件的概率问题,关键是弄清事件属于的概率模型,然后,选择合适的概率模型公式.1年前查看全部
- (2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处
(2011•琼海一模)某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处SO42-从右向左移动.下列分析正确的是( )

A. 溶液中c(A2+)浓度减小
B. B的电极反应:B-2e-═B2+
C. y电极上有H2产生,发生还原反应
D. 反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 xiyuan5211年前1
xiyuan5211年前1 -
 8O前 共回答了12个问题
8O前 共回答了12个问题 |采纳率91.7%解题思路:该装置中右边装置不能自发的进行氧化还原反应是不能构成原电池只能形成电解池,左边装置中能发生的进行氧化还原反应且符合原电池的构成条件所以是原电池.当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,即A的金属活动性大于B;连接B的y极为Y阳极,连接A的x极为阴极.A、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,原电池中负极A上金属失电子发生氧化反应,生成金属阳离子进入溶液导致溶液中(A2+)浓度增大,故A错误;
B、当K闭合时,在交换膜处SO42-从右向左移动,说明A为负极,B为正极,B极上溶液中的金属阳离子得电子生成金属单质,电极反应式为B2++2e-═B,故B错误;
C、右边装置中连接B的y极为阳极,连接A的x极为阴极,电解池工作时,y极上氯离子失电子发生氧化反应,电极反应式为2Cl--2e-═Cl2↑,故C错误;
D、右边装置中y极上发生的电极反应式为2Cl--2e-═Cl2↑,x极上发生的电极反应式为2H++2e-═H2↑,由于氢离子放电而氢氧根离子不放电导致溶液呈碱性,铝离子和氢氧根离子反应生成难溶性的氢氧化铝,氢氧化铝和氢氧化钠反应生成可溶性的偏铝酸钠,故D正确.
故选:D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池和电解池原理,难度较大,明确原电池放电时溶液中阴阳离子的移动方向是解本题的关键.1年前查看全部
- (2012•琼海一模)取三份锌粉,分盛于甲、乙、丙三支试管中,分别加入以下物质后,及时塞上导管塞子,充分反应.甲加入50
(2012•琼海一模)取三份锌粉,分盛于甲、乙、丙三支试管中,分别加入以下物质后,及时塞上导管塞子,充分反应.甲加入50mLpH=2盐酸,乙加入50mL pH=2醋酸,丙加入50mL pH=2醋酸及少量的胆矾粉末.
(1)若反应终了甲和乙中产生氢气的体积一样多,且只有一支试管中金属有剩余,则开始时加入的锌的质量大小关系为______(以上用“甲、乙”和“>、<、=”回答)
(2)若反应终了生成氢气的体积一样多,且没有剩余的锌.回答以下问题.
①三支试管中参加反应的锌的质量大小关系为:______(用“甲、乙、丙”和“>、<、=”回答)
②反应终了,所需时间为:______(同①)
③若以上三组实验,锌粉均过量,产生的氢气体积______(同①) caoweibb7qq181年前1
caoweibb7qq181年前1 -
 fle2o 共回答了17个问题
fle2o 共回答了17个问题 |采纳率94.1%解题思路:(1)pH相等的盐酸和醋酸,醋酸的物质的量浓度大于盐酸,则等体积和等pH的盐酸和醋酸,盐酸的物质的量小于醋酸,生成氢气的体积相同,则消耗酸的物质的量相同,根据剩余的酸确定加入锌的质量;
(2)①根据锌参加的反应确定锌的质量大小;
②构成原电池的反应速率大于没有构成原电池的反应速率,没有构成原电池的反应中,氢离子浓度越大,反应速率越大;
③根据酸的物质的量确定生成氢气的体积大小.(1)pH相等的盐酸和醋酸中,C(CH3COOH)>C(HCl),则等体积和等pH的盐酸和醋酸,n(CH3COOH)>n(HCl),生成氢气的体积相同,则消耗酸的物质的量相同,所以醋酸过量,则醋酸溶液中锌不足,而盐酸溶液中锌有剩余,故甲>乙,
故答案为:甲>乙;
(2)①若反应终了生成氢气的体积一样多,且没有剩余的锌,则甲、乙、丙中与酸反应的锌的质量相同,但丙中锌还和铜离子发生置换反应,所以丙中消耗锌最多,而甲和乙中消耗锌的质量相同,故答案为:丙>甲=乙;
②丙中锌置换出铜,铜、锌和酸构成原电池而加快反应速率,反应过程中,乙中氢离子浓度大于甲,所以乙中反应速率大于甲,反应终了,所需时间为:甲>乙>丙,故答案为:甲>乙>丙;
③乙和丙中醋酸的物质的量相同,甲中酸的物质的量小于丙和乙,且盐酸和醋酸都是一元酸,所以若以上三组实验,锌粉均过量,产生的氢气体积乙=丙>甲,故答案为:乙=丙>甲.点评:
本题考点: 弱电解质在水溶液中的电离平衡;化学反应速率的影响因素.
考点点评: 本题考查弱电解质的电离,注意能构成原电池的金属能加快反应速率,为易错点.1年前查看全部
- (2011•琼海一模)直线x+7y-5=0截圆x2+y2=1所得的两段弧长之差的绝对值是( )
(2011•琼海一模)直线x+7y-5=0截圆x2+y2=1所得的两段弧长之差的绝对值是( )
A. [π/4]
B. [π/2]
C. π
D. [3π/2] sqxxhjw1年前1
sqxxhjw1年前1 -
 文哲Q 共回答了17个问题
文哲Q 共回答了17个问题 |采纳率88.2%解题思路:求出圆心(0,0)到直线x+7y-5=0的距离d,求出弦长,根据弦长和半径的关系求出弦所对的圆心角,即得两段弧长之比.圆x2+y2=1的圆心(0,0)到直线x+7y-5=0的距离为d=
|0+0−5|
1+49=
2
2,
故弦长为 2
r2−d2=
2,故弦所对的圆心角为90°,两段弧长之比为3:1,
两段弧长之差的绝对值是 [3/4]×2π-
1
4×2π=π,
故选C.点评:
本题考点: 直线与圆相交的性质.
考点点评: 本题考查直线和圆的位置关系,点到直线的距离公式,弦长公式的应用,由弦所对的圆心角得到两段弧长之比
是解题的关键.1年前查看全部
- (2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
(2011•琼海一模)抛物线y=4x2上一点到直线y=4x-5的距离最短,则该点的坐标是( )
A. (1,2)
B. (0,0)
C. (
,1)1 2
D. (1,4) cangshanyixiao1年前1
cangshanyixiao1年前1 -
 realsuperzwh 共回答了21个问题
realsuperzwh 共回答了21个问题 |采纳率100%解题思路:根据题意,直线y=4x-5必然与抛物线y=4x2相离,抛物线上的点到直线的最短距离就是与直线y=4x-5平行的抛物线的切线的切点.y'=8x,由8x=4得x=
1
2,
故抛物线的斜率为4的切线的切点坐标是(
1
2,1),
该点到直线y=4x-5的距离是最短.
故选C.点评:
本题考点: 点到直线的距离公式;抛物线的简单性质.
考点点评: 主要考查了导数及其应用,本题以数形结合思想为指导命制,通过形的分析把问题转化为求抛物线的斜率为4的切线的切点坐标.本题也可以直接根据点到直线的距离公式求解,即抛物线上的点到直线y=4x-5的距离是d=|4x−y−5|17=|4x−4x2−5|17=4(x−12)2+417,显然这个函数当x=12时取得最小值,此时y=1.1年前查看全部
- (2011•琼海一模)下列溶液中离子浓度的关系一定正确的是( )
(2011•琼海一模)下列溶液中离子浓度的关系一定正确的是( )
A. pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(C6H5ONa )>c(NaOH)
B. pH=3的一元酸HX溶液和pH=11的一元碱MOH溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-)
C. NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D. 等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:2c(H+)+c(HX)═2c(OH-)+c(X-) 接着呼悠1年前1
接着呼悠1年前1 -
 SwordDancer28 共回答了25个问题
SwordDancer28 共回答了25个问题 |采纳率88%解题思路:A、溶液PH的大小是由溶液中的氢离子浓度大小决定,相同温度下溶液中离子积是常数,题干中的溶液都是显碱性的溶液,有强碱和水解呈碱性的盐,水解程度的大小决定溶液PH的大小,水解程度越大PH越大;
B、若是强酸强碱溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-),若是强酸弱碱溶液,等体积混合溶液显碱性;若是弱酸强碱等体积混合溶液呈酸性;
C、NH4HSO4溶液中滴加NaOH至溶液恰好呈中性,中和氢离子后,和部分铵根反应生成一水合氨;
D、依据溶液中电荷守恒和物料守恒计算得到;A、CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,水解程度Na2CO3溶液>C6H5ONa溶液>CH3COONa溶液,氢氧化钠是强碱,PH相同的溶液中溶质浓度NaOH溶液<Na2CO3溶液<C6H5ONa溶液<CH3COONa溶液;故A错误;
B、若是强酸强碱溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-),若是强酸弱碱溶液,等体积混合溶液显碱性;若是弱酸强碱等体积混合溶液呈酸性;故B错误;
C、溶液中电荷守恒c(Na+)+c(NH4+)+c(H+)=c(OH-)+2c(SO42-)得到:c(Na+)+c(NH4+)=2c(SO42-),依据NH4HSO4溶液中溶质和氢氧根离子反应过程为全部中和氢离子,和铵根离子部分反应,溶液中离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);故C正确;
D、等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:电荷守恒:c(K+)+c(H+)=c(OH-)+c(X-);2c(K+)=c(X-)+c(HX);合并计算得到:2c(H+)+c(HX)═2c(OH-)+c(X-);故D正确;
故选CD.点评:
本题考点: 离子浓度大小的比较;盐类水解的应用;酸碱混合时的定性判断及有关ph的计算.
考点点评: 本题考查了溶液中电荷守恒、物料守恒的计算应用,溶液中离子浓度大小比较的分析判断,酸碱反应后溶液酸碱性的分析判断,题目难度中等.1年前查看全部
- (2012•琼海一模)设NA是阿伏加德罗常数的数值,下列说法正确的是( )
(2012•琼海一模)设NA是阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温下,23 g NO2含有NA个氧原子
B. 1 mol Cl2与足量的铁反应,转移的电子数为3NA
C. 0.1 mol24Mg32S晶体中所含中子总数为2.8 NA
D. 用惰性电极电解硫酸铜溶液,若生成1 mol O2,则转移电子数为2NA 微笑的蒲公英1年前1
微笑的蒲公英1年前1 -
 nonghaha 共回答了18个问题
nonghaha 共回答了18个问题 |采纳率83.3%解题思路:A、质量换算物质的量,结合分子式计算原子数;
B、氯气全部反应,依据氧化还原反应电子守恒计算;
C、依据质量数=中子数+质子数结合化学式计算;
D、依据电极化学方程式的电子守恒计算.A、23 g NO2物质的量=[23g/46g/mol]=0.5mol,含有NA个氧原子,故A正确;
B、1 mol Cl2与足量的铁反应,1mol氯气全部反应转移的电子数为2NA,故B错误;
C、0.1 mol24Mg32S晶体中所含中子总数=0.1mol×(24-12+32-16)×NA=2.8 NA,故C正确;
D、用惰性电极电解硫酸铜溶液,若生成1 mol O2,依据电极反应电子守恒,阳极电极反应4OH--4e-=2H2O+O2↑则转移电子数为4NA,故D错误;
故选AC.点评:
本题考点: 阿伏加德罗常数.
考点点评: 本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,氧化还原反应的电子转移计算,质量数的概念计算应用,电解原理的计算,题目难度中等.1年前查看全部
- (2011•琼海一模)1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃
(2011•琼海一模)1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是( )(气体体积均在相同条件下测定)
A.乙炔
B.丙炔
C.丁炔
D.1,3-丁二烯 bio1234cffbio1年前1
bio1234cffbio1年前1 -
 独与阿独 共回答了19个问题
独与阿独 共回答了19个问题 |采纳率84.2%解题思路:由选项可知,都是链烃,1体积某气态烃和与2体积HCl发生加成反应,说明分子中含2个双键或1个C≡C.生成了1体积该卤代烷能和6体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,以此来解答.1体积某气态烃和与2体积HCl发生加成反应,说明分子中含2个双键或1个C≡C.生成了1体积该卤代烷能和6体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,由选项可知,都是链烃,故该气态烃分子中C原子数目为[4+2/2]=3,故ACD错误,B正确,
故选B.点评:
本题考点: 烯烃;乙炔炔烃.
考点点评: 本题考查有机物分子式的确定,难度不大,理解加成反应与取代反应是解题关键.1年前查看全部
- (2011•琼海一模)设随机变量ξ的概率分布列为P(ξ=k)=c2k,k=1,2,3,…,6,其中c为常数,则P(ξ≤2
(2011•琼海一模)设随机变量ξ的概率分布列为P(ξ=k)=
,k=1,2,3,…,6,其中c为常数,则P(ξ≤2)的值为c 2k [16/21][16/21]. alfaromeo1591年前1
alfaromeo1591年前1 -
 黑家坡 共回答了29个问题
黑家坡 共回答了29个问题 |采纳率86.2%解题思路:根据所给的随机变量的分布列,写出分布列之和是1,得到关于c的方程,解出c的值,写出要求的两个变量对应的概率,得到结果.∵随机变量ξ的概率分布列为P(ξ=k)=
c
2k,k=1,2,3,…,6,
∴c([1/2+
1
4+
1
8+
1
16+
1
32+
1
64])=1,
∴c=[64/63],
∴P(ξ≤2)=P(ξ=1)+P(ξ=2)=([1/2+
1
4])×[64/63]=[16/21],
故答案为:[16/21]点评:
本题考点: 离散型随机变量及其分布列;互斥事件的概率加法公式.
考点点评: 本题考查离散型随机变量的分布列的性质,是一个基础题,题目的运算量不大,只要抓住分布列中各个变量的概率之和等于1的性质就能够做出结果.1年前查看全部
- (2013•琼海模拟)如图所示,质量为m=0.1kg的物体放在升降机底部,一根竖直弹簧上端固定在升降机顶部,下端连接物体
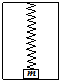 (2013•琼海模拟)如图所示,质量为m=0.1kg的物体放在升降机底部,一根竖直弹簧上端固定在升降机顶部,下端连接物体,当升降机以4m/s2的加速度加速向上运动时,弹簧对物体的拉力为0.4N;当升降机以8m/s2的加速度加速向上运动时,弹簧的拉力为( )
(2013•琼海模拟)如图所示,质量为m=0.1kg的物体放在升降机底部,一根竖直弹簧上端固定在升降机顶部,下端连接物体,当升降机以4m/s2的加速度加速向上运动时,弹簧对物体的拉力为0.4N;当升降机以8m/s2的加速度加速向上运动时,弹簧的拉力为( )
A.0.4N
B.0.8N
C.1.0N
D.1.2N wjkrjzaxwf1txe1年前1
wjkrjzaxwf1txe1年前1 -
 月儿121 共回答了18个问题
月儿121 共回答了18个问题 |采纳率94.4%解题思路:根据牛顿第二定律求出升降机以4m/s2的加速度加速向上运动时,物体与底端的弹力.升降机以8m/s2的加速度加速向上运动时,合力增大,通过物体与底端间是否有弹力,求出弹簧的拉力.当升降机以4m/s2的加速度加速向上运动时,根据牛顿第二定律得,F+N-mg=ma,代入数据解得N=1N.
当升降机以8m/s2的加速度加速向上运动时,合力增大,知支持力增大,由于弹簧的形变量不变,则弹簧的拉力不变,为0.4N.故A正确,B、C、D错误.
故选:A.点评:
本题考点: 牛顿第二定律.
考点点评: 解决本题的关键判断物体与底端是否有弹力,从而确定弹簧形变量是否发生变化,得出弹簧拉力的大小.1年前查看全部
- (四0个个•琼海一模)现有一只标值为“3.0V,xW”小灯泡,其额定功率的标值已模糊不清.某同学想通过测量灯丝伏安曲线的
(四0个个•琼海一模)现有一只标值为“3.0V,xW”小灯泡,其额定功率的标值已模糊不清.某同学想通过测量灯丝伏安曲线的方法,来找出该灯泡正常工作时的功率.
(个)已知该灯泡灯丝电阻较小,请先在图(甲)中补全用伏安法测量灯丝电阻的电路图,再选择合适量程的电流表与电压表,将图(乙)中的实物连成完整的电路.
(四)开关S闭合之前,图(乙)中滑动变阻器的滑片应该置于______(选填“A”端、“q端”、或“Aq正中间”)
(3)该同学通过实验作出了灯丝的伏安曲线如图(丙)所示,根据小灯泡的额定电压的标值为“3.0V”,从图(丙)中可以找出该灯正常工作时的电流I=______A,其额定功率为P=______W.(结果均保留两位有效数字)
 兰孩1年前0
兰孩1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 以下三副对联(1)万里长城山海关,龙头为首.(2)琼海独具大手笔,五指擎天.(3)苗寨黔山黄果树,茅台赤水.(4)川肴蜀
以下三副对联
(1)万里长城山海关,龙头为首.
(2)琼海独具大手笔,五指擎天.
(3)苗寨黔山黄果树,茅台赤水.
(4)川肴蜀绣锦官城,花径草堂.
(5)独门绝技少林寺,天下无双.
(6)石林自有高材生,群峰拔地.
分别代表
a河南 b贵阳 c四川 d云南 e海南 f河北
( )和( )组成一副,分别出自( )( )
( )和( )组成一副,分别出自( )( )
( )和( )组成一副,分别出自( )( ) mark95271年前2
mark95271年前2 -
 redian512 共回答了16个问题
redian512 共回答了16个问题 |采纳率81.3%( 1)和(5 )组成一副,分别出自(F河北 )(A河南 )
(6 )和( 2)组成一副,分别出自( D云南)(B海南 )
( 3)和(4 )组成一副,分别出自(B贵阳 )(D四川 )
左边是上联,右边是下联
从"山海关,琼海,苗寨茅台,川肴蜀绣,少林寺,石林"这些词可以看出来1年前查看全部
- (2013•琼海模拟)在力学理论建立的过程中,有许多伟大的科学家做出了贡献.关于科学家和他们的贡献,下列说法正确的是(
(2013•琼海模拟)在力学理论建立的过程中,有许多伟大的科学家做出了贡献.关于科学家和他们的贡献,下列说法正确的是( )
A.伽利略发现了行星运动的规律,并总结出行星运动的三大定律
B.牛顿总结出万有引力定律,并通过实验测出了引力常量
C.牛顿最早指出力不是维持物体运动的原因
D.笛卡尔对牛顿第一定律的建立做出了贡献 痛失乐园1年前1
痛失乐园1年前1 -
 红裳翠袖 共回答了17个问题
红裳翠袖 共回答了17个问题 |采纳率88.2%解题思路:根据物理学史和常识解答,记住著名物理学家的主要贡献即可.A、开普勒发现了行星运动的规律,并总结出行星运动的三大定律,故A错误
B、牛顿总结出万有引力定律,卡文迪许通过实验测出了引力常量,故B错误
C、伽利略最早指出力不是维持物体运动的原因,故C错误
D、笛卡尔对牛顿第一定律的建立做出了贡献,故D正确
故选:D.点评:
本题考点: 物理学史.
考点点评: 本题考查物理学史,是常识性问题,对于物理学上重大发现、发明、著名理论要加强记忆,这也是考试内容之一.1年前查看全部
- (2011•琼海一模)在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O⇌HCO3-+OH-.下列说法正确的是
(2011•琼海一模)在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O⇌HCO3-+OH-.下列说法正确的是( )
A.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(H+)
B.升高温度,平衡向正反应方向移动
C.稀释溶液,溶液中c(H+)和c(OH-)都减少
D.加入NaOH固体,溶液pH减小 这里的四季是夏天1年前1
这里的四季是夏天1年前1 -
 光光的猪 共回答了19个问题
光光的猪 共回答了19个问题 |采纳率94.7%A、Na2CO3溶液碳酸根离子水解导致溶液显示碱性,其中离子浓度大小顺序是:c(Na+)>c(CO32-)>c(OH-)>c(H+),故A正确;
B、因水解是吸热的,则升温可以促进水解,平衡正向移动,故B正确;
C、稀释溶液,溶液中c(OH-)减少,但是c(H+)增大,故C错误;
D、加入NaOH固体,碱性增强,pH增大,故D错误;
故选:AB.1年前查看全部
- (2014•琼海二模)下列各式计算正确的是( )
(2014•琼海二模)下列各式计算正确的是( )
A. 2a3-a3=2
B. a3•a2=a6
C. a6÷a3=a3
D. (a3)2=a9 小裴0551年前1
小裴0551年前1 -
 屉屉丫头 共回答了7个问题
屉屉丫头 共回答了7个问题 |采纳率100%解题思路:根据合并同类项法则,同底数幂相乘,底数不变指数相加;同底数幂相除,底数不变指数相减;幂的乘方,底数不变指数相乘,对各选项分析判断后利用排除法求解.A、2a3-a3=a3,故本选项错误;
B、a3•a2=a3+2=a5,故本选项错误;
C、a6÷a3=a6-3=a3,故本选项正确;
D、(a3)2=a3×2=a6,故本选项错误.
故选C.点评:
本题考点: 同底数幂的除法;合并同类项;同底数幂的乘法;幂的乘方与积的乘方.
考点点评: 本题考查了同底数幂的乘法,同底数幂的除法,幂的乘方的性质,熟记性质并理清指数的变化情况是解题的关键.1年前查看全部
- (2011•琼海一模)下列离子方程式书写不正确的是( )
(2011•琼海一模)下列离子方程式书写不正确的是( )
A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O
B.用铁做电极电解硫酸铜溶液:2Cu2++2H2O
2Cu↓+O2↑+4H+电解 .
C.碳酸钡溶于醋酸:BaCO3+2H+═Ba2++H2O+CO2↑
D.将氯气通入氯化亚铁溶液:2Fe2++Cl2═2Fe3++2Cl- daldrb1年前1
daldrb1年前1 -
 大鸟类 共回答了15个问题
大鸟类 共回答了15个问题 |采纳率86.7%解题思路:A、AlCl3溶液与烧碱溶液反应,按照1:3反应生成氢氧化铝沉淀,按照1:4反应生成偏铝酸钠,依据反应定量关系分析判断;
B、铁做电极阳极铁失电子发生氧化反应生成亚铁离子,溶液中铜离子得到电子发生还原反应生成铜;
C、醋酸是弱酸存在电离平衡;
D、氯气氧化亚铁离子为铁离子,依据电荷守恒和原子守恒分析;A、AlCl3溶液与烧碱溶液反应,按照1:3反应生成氢氧化铝沉淀,按照1:4反应生成偏铝酸钠,当n(OH-):n(Al3+)=7:2时,反应生成产物为氢化锂和偏铝酸钠,直平得到离子方程式为:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O,故A正确;
B、用铁做电极电解硫酸铜溶液,铁做电极阳极铁失电子发生氧化反应生成亚铁离子,溶液中铜离子得到电子发生还原反应生成铜反应的离子方程式为,Cu2++Fe
电解
.
Cu+Fe2+,故B错误;
C、碳酸钡溶于醋酸,醋酸是弱酸存在电离平衡,反应的离子方程式为:BaCO3+2CH3COOH═Ba2++H2O+CO2↑+2CH3COO-,故C错误;
D、将氯气通入氯化亚铁溶液,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故D正确;
故选:BC.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查了离子方程式的书写方法和正误判断,注意定量关系分析,弱电解质判断,电解原理的分析应用,题目难度中等.1年前查看全部
- (2014•琼海二模)如图,正方形ABCD中,点E从点A出发沿着AD向D运动,(点E不与点A,点D重合)同时点F从点D出
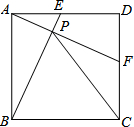 (2014•琼海二模)如图,正方形ABCD中,点E从点A出发沿着AD向D运动,(点E不与点A,点D重合)同时点F从点D出发沿着线段DC向C运动,(点F不与点D,点C重合)点E与F点运动速度相同,当点E停止运动时,另一动点F随之停止运动,设BE与AF相交于点P,连接PC请研究:
(2014•琼海二模)如图,正方形ABCD中,点E从点A出发沿着AD向D运动,(点E不与点A,点D重合)同时点F从点D出发沿着线段DC向C运动,(点F不与点D,点C重合)点E与F点运动速度相同,当点E停止运动时,另一动点F随之停止运动,设BE与AF相交于点P,连接PC请研究:
(1)AF=BE,AF⊥BE;
(2)当点E运动到AD中点位置时:
①PA:PB的值是多少?②PC和BC又怎样的数量关系?并证明你的结论. oijyf1年前1
oijyf1年前1 -
 亲亲1995 共回答了21个问题
亲亲1995 共回答了21个问题 |采纳率76.2%解题思路:(1)根据题意很容易证得△BAE≌△ADF,即可得到AF=BE,利用正方形内角为90°,得出AF⊥DE.
(2)要求两条线段的关系,需要把两者放入一直角三角形中,利用三角函数求解.根据题意可知此时AF⊥BE,又有中点的关系,可以得出tan∠2=[1/2],由∠1=∠2,可以求解.
(3)延长AF交BC的延长线于点G,可以得出△ADF≌△GCF,进而得出CG=AD,通过线段的转换可以得出BC=[1/2]BG,根据题意可以得出PC=[1/2]BG,即可以得出结论.(1)证明:∵E在AD边上(不与A、D重合),点F在DC边上(不与D、C重合).
又∵点E、F分别同时从A、D出发以相同的速度运动,
∴AE=DF,
∵四边形ABCD是正方形,
∴AB=DA,∠BAE=∠D=90°,
在△BAE和△ADF中,
AE=DE
∠BAE=∠ADF=90°
AB=AD,
∴△BAE≌△ADF(SAS),
∴∠1=∠2,
∵∠2+∠3=90°∴∠1+∠3=90°即∠APB=90°
∴AF⊥BE.
(2)由(1)知当点E运动到AD中点时,点F也运动到DC中点,此时就有AF⊥BE.
∵F是CD的中点,
∴DF=[1/2]CD,
∵AD=CD,
∴DF=[1/2]AD,
∵∠1=∠2,
∴tan∠1=tan∠2
在Rt△ADF中,tan∠2=[DF/AD=
1
2],
∴在Rt△APB中,tan∠1=
∴PA:PB的值是1:2.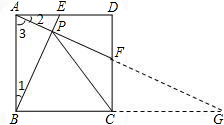
(3)PC=BC.
证明:延长AF交BC的延长线于点G,
在△ADF和△GCF中
∠D=∠DCG=90°
DF=CF
∠AFD=∠GFC,
∴△ADF≌△GCF(ASA),
∴CG=AD,
∵BC=AD,
∴CG=BC=[1/2]BG,
由(1)知AF⊥BE,
∴∠BPG=90°,
∴△BPG为直角三角形
∴PC=[1/2]BG,
∵BC=[1/2]BG,
∴PC=BC.点评:
本题考点: 正方形的性质;全等三角形的判定与性质.
考点点评: 本题考查了正方形的性质以及全等三角形的判定和性质,对学生要求有比较高的读图能力,同时本题也是探求性试题,做这类题前要求大胆的假设,根据假设再去证明.需要在平时做题中培养这种能力.1年前查看全部
- (2011•琼海一模)直线x+7y-5=0截圆x2+y2=1所得的两段弧长之差的绝对值是( )
(2011•琼海一模)直线x+7y-5=0截圆x2+y2=1所得的两段弧长之差的绝对值是( )
A. [π/4]
B. [π/2]
C. π
D. [3π/2] xiaohuafeng_12021年前1
xiaohuafeng_12021年前1 -
 **委员 共回答了20个问题
**委员 共回答了20个问题 |采纳率90%解题思路:求出圆心(0,0)到直线x+7y-5=0的距离d,求出弦长,根据弦长和半径的关系求出弦所对的圆心角,即得两段弧长之比.圆x2+y2=1的圆心(0,0)到直线x+7y-5=0的距离为d=
|0+0−5|
1+49=
2
2,
故弦长为 2
r2−d2=
2,故弦所对的圆心角为90°,两段弧长之比为3:1,
两段弧长之差的绝对值是 [3/4]×2π-
1
4×2π=π,
故选C.点评:
本题考点: 直线与圆相交的性质.
考点点评: 本题考查直线和圆的位置关系,点到直线的距离公式,弦长公式的应用,由弦所对的圆心角得到两段弧长之比
是解题的关键.1年前查看全部
- (2014•琼海二模)如图,梯形ABCD中,AD∥BC,AB=DC=3,AD=5,∠C=60°,则下底BC的长为____
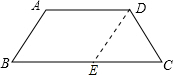
 (2014•琼海二模)如图,梯形ABCD中,AD∥BC,AB=DC=3,AD=5,∠C=60°,则下底BC的长为______.
(2014•琼海二模)如图,梯形ABCD中,AD∥BC,AB=DC=3,AD=5,∠C=60°,则下底BC的长为______.  3638749241年前1
3638749241年前1 -
 苗苗439 共回答了17个问题
苗苗439 共回答了17个问题 |采纳率88.2%1年前查看全部
- (2013•琼海一模)在地球地层大气中,同一地点不同高度上的风并不完全相同.其主要原因是空气做水平运动时所受的摩擦力随高
(2013•琼海一模)在地球地层大气中,同一地点不同高度上的风并不完全相同.其主要原因是空气做水平运动时所受的摩擦力随高度的增加而减少.这样,在气压梯度力作用下不同高度的风向和风速都会发生变化.据此回答2-3题.

2.若某地不同高度的风向、风速投影到同一水平面,则四幅图中能够表示北半球地表到高空大的风向随高度变化而形成的曲线图是( )
3.在图示①中,按地图的一般方向判断,其高空大气高气压可能位于该地的( )
A.东方
B.南方
C.西方
D.北方 激石拉风1年前1
激石拉风1年前1 -
 我要吐了 共回答了22个问题
我要吐了 共回答了22个问题 |采纳率95.5%解题思路:近地面的风受水平气压梯度力、摩擦力和地转偏向力的共同作用,风向与等压线斜交;空气做水平运动时所受的摩擦力随高度的增加而减少,所以高空的风只受水平气压梯度力和地转偏向力的共同作用,风向与等压线平行.近地面的风受水平气压梯度力、摩擦力和地转偏向力的共同作用,风向与等压线斜交;空气做水平运动时所受的摩擦力随高度的增加而减少,所以高空的风只受水平气压梯度力和地转偏向力的共同作用,风向与等压线平行.从而可知,摩擦力越大,风向与等压线夹角越大,摩擦力越小,夹角越小,高空时夹角为零.在图示①中,按地图的一般方向判断,从南到北,夹角越大,即从高空到近地面;图中箭头(风向)右偏,说明该地区是北半球,其箭头所指方向是低压区(北方),所以其高空大气高气压可能位于该地的南方.
故选:B.点评:
本题考点: 气压系统与天气.
考点点评: 本题难度适中,属于知识性试题,解题的关键是掌握大气的受力分析.1年前查看全部
- (2014•琼海一模)2014年海南省中招工作正在进行,预计今年报名参加中考的人数将达到10.5万人,10.5万人用科学
(2014•琼海一模)2014年海南省中招工作正在进行,预计今年报名参加中考的人数将达到10.5万人,10.5万人用科学记数法表示为______人.
 虫子购物狂1年前1
虫子购物狂1年前1 -
 张晗晗 共回答了17个问题
张晗晗 共回答了17个问题 |采纳率94.1%10.5万=105000=1.05×105,
故答案为:1.05×105.1年前查看全部
大家在问
- 1路边画黄线是什么意思啊谢谢了,大神帮忙啊
- 2圆的面积题并有答案
- 3证明直角三角形的难题一个三角形ABC,已知AB=2BC,∠B=2∠A,证明△ABC是直角三角形想了一个中午了,实在是没办
- 4甲乙两地相距2.4千米,某人从甲地步行去乙地,前一半时间平均每分钟行80米,后一半时间平均每分钟行70米
- 5选词填空.虚弱 选词填空.虚弱 软弱 1.他的病刚好,身子还很( ),走几步就气喘吁吁.2.因为你太( )了
- 6学生们搬砖头,每人搬4块,其中有5人要搬两次;如果每人搬5块,就有两人没有砖可搬.搬砖头的学生有多少人?这批砖头共有多少
- 7如图,在Rt三角形ABC中,角ACB=90,分别以AB,BC为一边向外作正方形ABFG,BCED,连接AD,CF,AD与
- 8“Maybe you have been to many countries ,but nowhere else ___
- 9(2007•甘井子区模拟)生物分类的依据是生物在形态结构等方面的特征,在被子植物中,______、果实和种子往往作为分类
- 10中华文明灿烂辉煌,在古代就有许多发明和创造。下列叙述中不涉及到化学变化的是 [
- 11用定义证明(1)函数f(x)=1/x在(0,+∞)上是减函数 (2)函数f(x)=x+1/x在x∈[1,+∞)上是增函数
- 12酸式滴定管是玻璃的,所以不能装碱性溶液,那碱式滴定管里有个玻璃球,难道不会被碱性溶液腐蚀吗?
- 13玲珑什么透 成语
- 14在中学阶段,对许多特定集合(如实数集、复数集以及平面向量集等)的学习常常是以定义运算(如四则运算)
- 15初中的第三课短文两篇一.作者写蝉,先抑后扬.扬在哪里?抑在哪里?一扬一抑表达了作者怎样的思想感情?

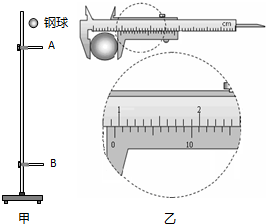 (2013•琼海模拟)某活动小组利用图甲装置验证机械能守恒定律.钢球自由下落过程中,先后通过光电门A、B,计时装置测出钢球通过A、B的时间分别为t1、t2.用钢球通过光电门的平均速度表示钢球球心通过光电门的瞬时速度.测出两光电门间的距离为h,当地的重力加速度为g.
(2013•琼海模拟)某活动小组利用图甲装置验证机械能守恒定律.钢球自由下落过程中,先后通过光电门A、B,计时装置测出钢球通过A、B的时间分别为t1、t2.用钢球通过光电门的平均速度表示钢球球心通过光电门的瞬时速度.测出两光电门间的距离为h,当地的重力加速度为g.