0.18mol/L的醋酸钠溶液的PH怎么求?已知醋酸的电离常数为1.8×10的负五次方
 shaoyi8z2022-10-04 11:39:541条回答
shaoyi8z2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 qishunyong 共回答了17个问题
qishunyong 共回答了17个问题 |采纳率100%- c(OH-)=根号(cKb);
c=0.18mol/L;
Kb=Kw/Ka;
Kw是10^-14;Ka=1.8×10^-5;
算出OH-即可求H+浓度;
有问题请追问~ - 1年前
相关推荐
- 醋酸钠溶液中加入醋酸钠固体,醋酸根水解受抑制还是促进?
 我都会紧1年前2
我都会紧1年前2 -
 清凉男孩 共回答了16个问题
清凉男孩 共回答了16个问题 |采纳率75%稀溶液体系下是促进1年前查看全部
- 浓度均为0.1mol/L的苯酚钠和醋酸钠溶液中:阴离子的总浓度前者小于后者
浓度均为0.1mol/L的苯酚钠和醋酸钠溶液中:阴离子的总浓度前者小于后者
这句话为什么是对的? nnskz1年前1
nnskz1年前1 -
 jykcheung 共回答了15个问题
jykcheung 共回答了15个问题 |采纳率86.7%因为要考虑弱酸离子的和H离子结合生成弱酸,导致电离平衡发生移动,并且他们的影响是相互的,所以导致最后后者的阴离子的数目多于前者.1年前查看全部
- 醋酸钠溶液加热后PH如何变化
 孤性自赏1年前4
孤性自赏1年前4 -
 4ever_echo 共回答了26个问题
4ever_echo 共回答了26个问题 |采纳率88.5%PH应该是逐渐减小,但一直是大于71年前查看全部
- 醋酸钠溶液加热后ph值如何变化?
 luoyandan5201年前2
luoyandan5201年前2 -
 青青苹果酸 共回答了14个问题
青青苹果酸 共回答了14个问题 |采纳率85.7%PH升高.
因为温度升高促进水解.1年前查看全部
- 醋酸钠溶液中为什么钠离子、醋酸离子浓度大于氢氧根、氢离子浓度?
醋酸钠溶液中为什么钠离子、醋酸离子浓度大于氢氧根、氢离子浓度?
c(Na+)>c(CH3COO-)>c(OH-)>(H+)
是不是溶质离子一定大于水的离子? 树鸿先生1年前3
树鸿先生1年前3 -
 金-娃娃 共回答了16个问题
金-娃娃 共回答了16个问题 |采纳率81.3%溶液中的OH-,H+主要来自于水的解离,非常非常少.
CH3COO-与Na+来自醋酸钠解离,但是醋酸根(CH3COO-)是弱酸根,会与H+生成部分醋酸,因此会消耗水中两种离子浓度.
所以c(Na+)>c(CH3COO-)>c(OH-)>(H+)1年前查看全部
- 醋酸溶液的电离平衡常数是1.6×10^-5则1摩尔每升的醋酸钠溶液中氢氧根离子的浓度是多少
 diance57941年前1
diance57941年前1 -
 你情我不愿 共回答了10个问题
你情我不愿 共回答了10个问题 |采纳率100%1.6×10^-5mol1年前查看全部
- PH=12的醋酸钠溶液中有水电离的H离子浓度是多少?
 jxf2291年前1
jxf2291年前1 -
 雅典娜1986 共回答了19个问题
雅典娜1986 共回答了19个问题 |采纳率84.2%10^-2
(1)H2O=H+ + OH-
(2)CH3COO-+H+=CH3COOH
(2)的发生使(1)中电离不断发生,(2)中的H+均为水电离的
所以水电离的H+为10^-2
而溶液中的H+浓度为10~-12,因为大部水电离的H+都用于(2)的反应1年前查看全部
- 氯化铵溶液分别和碳酸钠,醋酸钠溶液混合是否有方程
 duanezhuang1年前2
duanezhuang1年前2 -
 pigmana 共回答了21个问题
pigmana 共回答了21个问题 |采纳率85.7%没有!
它们含有的离子分别有:
NH4+ ,CL-,Na+,CO32-,CH3COO- 均能大量共存
另外,其中的NH4+ 不能和OH-共存
CL-不能和Ag+,Hg2+共存
CO32-,CH3COO-不能和H+共存1年前查看全部
- 如何配置过饱和醋酸钠溶液?还有,加热时用锥形瓶还是烧杯?
 wl0251年前1
wl0251年前1 -
 hunmoon 共回答了16个问题
hunmoon 共回答了16个问题 |采纳率87.5%用品:烧杯、玻棒、酒精灯、滤纸、平底烧瓶、石棉网.醋酸钠晶体、硫代硫酸钠晶体、蒸馏水.
步骤:
①醋酸钠过饱和溶液的制备500 毫升烧杯中加入250 克未潮解的醋酸钠晶体(CH3COONa·3H2O)和150 毫升蒸馏水,用微火加热,不断搅拌,使其完全溶解.趁热将溶液过滤到500 毫升洁净并干燥的平底烧瓶中(注意!不能把溶液滴在烧瓶颈部).静置冷却后,用洁净的橡皮塞将瓶口盖严.
②硫代硫酸钠过饱和溶液的制备250 克硫代硫酸钠晶体(Na2S2O3·5H2O)置于干燥洁净的平底烧瓶中,用水浴加热,使其溶于结晶水中.静置冷却,用洁净橡皮塞将瓶口盖严备用.
操作:
向瓶中投入同种溶质的小晶体,使晶体迅速布满整个烧瓶.
注意事项:
①醋酸钠晶体容易吸潮,药品量可适当增加.
②尘土亦能使过饱和溶液结晶,所以平底烧瓶要洁净,瓶口要盖严.
③晶种要细小,晶形要好,这样晶体生长缓慢,现象清晰.
实验目的:认识过饱和溶液及过饱和溶液不如饱和溶液稳定.1年前查看全部
- 甲醇和醋酸钠溶液怎么样会固化?
 乐乐嗲地1年前1
乐乐嗲地1年前1 -
 蜡笔小新2000 共回答了14个问题
蜡笔小新2000 共回答了14个问题 |采纳率85.7%不是醋酸钠而是醋酸钙.
在醋酸钙饱和溶液中慢慢加入乙醇或甲醇,一定要慢,待溶液冷却后,即可得到固体酒精.1年前查看全部
- 0.15摩尔每升的醋酸钠溶液的PH是多少
 丁三爷1年前1
丁三爷1年前1 -
 玫瑰红茶999 共回答了15个问题
玫瑰红茶999 共回答了15个问题 |采纳率86.7%答:
[OH-]= (cKb)1/2 =( 0.15x10^-9.26)1/2 = (10^-0.82 x 10^-9.26) = (10^-10.08)1/2 = 10^-5.04
POH = 5.04 PH = 14 -POH = 14 - 5.04 = 8.961年前查看全部
- 请问向醋酸钠溶液中加入氯化钠固体,平衡向哪边移动呢?如果加氯化钠溶液呢?
请问向醋酸钠溶液中加入氯化钠固体,平衡向哪边移动呢?如果加氯化钠溶液呢?
特别抱歉,【向醋酸钠溶液】改为【向醋酸溶液】,不好意思~ hewenjiatao1年前4
hewenjiatao1年前4 -
 STENT 共回答了22个问题
STENT 共回答了22个问题 |采纳率100%对于醋酸的电离平衡,加入氯化钠固体,平衡不移动;加氯化钠溶液时,溶液被稀释,平衡右移,但是pH值却是增大.NaCl不起作用.1年前查看全部
- 请问同浓度的氢氧化钠溶液与醋酸钠溶液的导电能力谁强?
 微妮湿的隐泪1年前3
微妮湿的隐泪1年前3 -
 飞向大海的翅膀 共回答了22个问题
飞向大海的翅膀 共回答了22个问题 |采纳率86.4%氢氧化钠强,它属于强碱容易电离;醋酸是弱酸电离度很小1年前查看全部
- 物质的量浓度相同的醋酸和醋酸钠溶液等体积混合 氢离子和醋酸分子浓度关系
 yikoutian1年前2
yikoutian1年前2 -
 婉玉儿 共回答了22个问题
婉玉儿 共回答了22个问题 |采纳率100%醋酸分子浓度远大于氢离子.本来醋酸是弱电解质,电离程度就很小,现在醋酸钠电离出的醋酸根离子还会抑制它的电离,所以分子多.溶液中离子的大小:CH3COO->Na+>H+>OH-1年前查看全部
- 醋酸在醋酸钠溶液中电离的程度小于在纯水中电离的程度 为什么 醋酸钠不是要水解吗 生成消耗H+ 生成醋酸?
 dominikavv1年前4
dominikavv1年前4 -
 为ssss 共回答了19个问题
为ssss 共回答了19个问题 |采纳率100%在醋酸钠溶液中,醋酸根的存在,阻碍了醋酸的电离,所以醋酸在醋酸钠溶液中电离的程度小于在纯水中电离的程度.
在醋酸和醋酸钠的混合溶液中,醋酸的电离是主要的,醋酸钠的水解是次要的,抓住主要反应,忽略次要反应,思路才清晰.1年前查看全部
- 等体积等浓度醋酸与醋酸钠溶液混合为什电离大于水解
 camelchow1年前1
camelchow1年前1 -
 linzong1238 共回答了21个问题
linzong1238 共回答了21个问题 |采纳率85.7%等体积等浓度醋酸与醋酸钠溶液混合时 原有的醋酸和醋酸根离子物质的量和浓度都相通 此时醋酸电离平衡的移动方向取决于醋酸电离平衡常数(该常数度量醋酸电离的倾向) 记得该常数大约是10-5左右 用Kh除以该值 得到一个小于10-9的值 前者(10-5)度量此时醋酸电离的倾向 后者(10-9)度量此时醋酸根水解的倾向 可以看出电离的倾向大 所以电离大于水解
更进一步的 此时溶液酸性
这个问题高考不会考原理吧.最重要是知道此时溶液显酸性
// 楼主还有不明白的请跟进 ~_~1年前查看全部
- 浓度均为0.2摩尔每升的醋酸和醋酸钠溶液等体积混合后溶液显酸性 则醋酸根离子浓度加醋酸浓度等于0.2为什么?
 puupuu1年前2
puupuu1年前2 -
 zero821212 共回答了20个问题
zero821212 共回答了20个问题 |采纳率95%醋酸和醋酸根1:1互相转化,但总量不变1年前查看全部
- 醋酸与醋酸钠溶液混合,PH为7,各离子浓度大小
 lightwhitefish1年前3
lightwhitefish1年前3 -
 亚齐鲁贝 共回答了17个问题
亚齐鲁贝 共回答了17个问题 |采纳率94.1%PH=7,说明c(H+)=c(OH-)=10^-7mol/L
根据电荷守恒c(H+)+c(Na+)=c(OH-)+c(Ac-)
所以,c(Na+)=c(Ac-).
既然醋酸和醋酸钠已经称为溶液了,那么其浓度一定不是痕量的(约定俗成的事情),浓度一定远大于 10^-7mol/L
所以,c(Na+)=c(Ac-)>>c(H+)=c(OH-)1年前查看全部
- 某温度下,0.1 mol/L醋酸溶液的pH=3.将该温度下0.2 mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混
某温度下,0.1 mol/L醋酸溶液的pH=3.将该温度下0.2 mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后
下列说法正确的是
A.该温度下,0.0l mol/L醋酸溶液的pH=4
B.该温度下,用0.1 mol/L醋酸和0.01 mol/L醋酸分别完全中和等体积0.1 mol/L的NaOH溶液,消耗两醋酸的体积比为1∶10
C.该温度下,0.2 mol/L醋酸溶液和0.4 mol/L醋酸钠溶液等体积混合后,混合液的pH<4.7
D.该温度下,0.2 mol/L醋酸溶液和0.4 mol/L醋酸钠溶液等体积混合后,混合液的pH=4.7
答案选B和D。求高手解答 wxs80831年前1
wxs80831年前1 -
 蓝8冰 共回答了22个问题
蓝8冰 共回答了22个问题 |采纳率81.8%C1年前查看全部
- 物质的量浓度相同的醋酸和醋酸钠溶液等体积混合为什么溶液中氢离子浓度大于氢氧根离子浓度?
物质的量浓度相同的醋酸和醋酸钠溶液等体积混合为什么溶液中氢离子浓度大于氢氧根离子浓度?
如何知道醋酸的电离大于水解, 冰雪清凌1年前1
冰雪清凌1年前1 -
 素质不高 共回答了19个问题
素质不高 共回答了19个问题 |采纳率84.2%水解大多数情况比电离要弱1年前查看全部
- 邻二氮菲分光光度法测铁的实验中,盐酸羟胺溶液(新配),邻二氮菲溶液,醋酸钠溶液的作用是什么?
邻二氮菲分光光度法测铁的实验中,盐酸羟胺溶液(新配),邻二氮菲溶液,醋酸钠溶液的作用是什么?
若用NaOH取代NaAc有什么缺点? 心痛的过往1年前2
心痛的过往1年前2 -
 尹晶杰 共回答了14个问题
尹晶杰 共回答了14个问题 |采纳率100%盐酸羟胺(NH2OH•HCl)将Fe3+还原为Fe2+,邻二氮菲与二价铁生成稳定的桔红色配合物((Fe(phen)3)2+),醋酸钠溶液作为缓冲溶液,Nacl是强碱不能做缓冲溶液1年前查看全部
- 向0.1mol/L醋酸钠溶液中分别加入少量硝酸铵、亚硫酸钠、氯化铁固体,则醋酸根的浓度变化依次为?
 carol2czf1年前2
carol2czf1年前2 -
 kkndand 共回答了17个问题
kkndand 共回答了17个问题 |采纳率82.4%醋酸钠是弱酸强碱盐,醋酸钠水溶液呈碱性;
硝酸铵和氯化铁是强酸弱碱盐,硝酸铵和氯化铁的水溶液呈酸性;
亚硫酸钠是弱酸强碱盐,醋酸钠水溶液呈碱性,
所以向0.1mol/L醋酸钠溶液中分别加入少量硝酸铵或氯化铁固体时,硝酸铵和氯化铁能促进醋酸钠的水解,使醋酸根离子浓度降低;
向0.1mol/L醋酸钠溶液中加入少量亚硫酸钠固体,由于两者水溶液都呈碱性抑制了醋酸钠的水解,使醋酸根离子浓度增大.1年前查看全部
- 在醋酸钠溶液中加入少量醋酸钠固体,醋酸根离子与钠离子的比值怎样变化?
 fengqing5131年前2
fengqing5131年前2 -
 回忆无效 共回答了19个问题
回忆无效 共回答了19个问题 |采纳率84.2%变大.
醋酸根存在于醋酸的解离平衡:Ac-+H+=HAc;[Ac-]*[H+]/[HAc]=常数;加入醋酸钠以后,[H+]肯定降低,所以[Ac-]/[HAc]要增加,设[Ac-]=x,[Na+]=y,则[HAc]=y-x(这个是物料平衡);所以x/(y-x)要增大,解得x/y增大,所以醋酸根离子与钠离子的比值增大.1年前查看全部
- 物质的量浓度相等的醋酸和醋酸钠溶液等提及混合,ph=4,则溶液内离子浓度大小为
 兰兰19851年前3
兰兰19851年前3 -
 malong888 共回答了10个问题
malong888 共回答了10个问题 |采纳率90%由溶液中阳离子等于阴离子,则钠离子+氢离子=醋酸根+氢氧根
又因为PH=4,则氢离子>氢氧根,推出钠离子钠离子>氢离子>氢氧根离子1年前查看全部
- 向醋酸钠溶液加盐酸为什么水解程度会增大
 土狼二大爷1年前3
土狼二大爷1年前3 -
 cory_gao 共回答了18个问题
cory_gao 共回答了18个问题 |采纳率100%水解是醋酸根和水中的氢离子其反应,直接加入氢离子;可使生成更多的醋酸;此外加入的氢离子中和了部分水解产生的氢氧根,使水解平衡向右移.1年前查看全部
- 关于醋酸钠溶液中微粒浓度大小醋酸钠溶液中为什么醋酸分子浓度比氢离子浓度大,
 莫莫的小树1年前3
莫莫的小树1年前3 -
 jazzzzz 共回答了20个问题
jazzzzz 共回答了20个问题 |采纳率90%这个可以通过分析得到,水中的氢离子浓度是仅仅通过水的电离得到的,而氢氧根是通过水解得到的,水解的程度要远远大于水的离子积,这你可以查书得到.再者,醋酸钠水解方程是醋酸跟+水=醋酸分子+氢氧根,而正因为水解占主导,那么醋酸分子浓度近似等于氢氧根浓度.因为水解程度大于水的电离,那么氢氧根浓度应该远远大于10的-7次幂,那么氢离子浓度应该远远小于10的-7次幂,而醋酸分子浓度近似等于氢氧根,因此,醋酸浓度大于氢离子浓度.1年前查看全部
- 在醋酸钠溶液中加醋酸钠固体 问 他的电离平衡 怎么移动
 寒情岛1年前3
寒情岛1年前3 -
 myb12003 共回答了16个问题
myb12003 共回答了16个问题 |采纳率87.5%CH3CH2COOH=CH3CH2COO-+H+在这个平衡中加入醋酸钠其实就是加入醋酸根离子,其结果是使反应向醋酸根离子减少的方向移动,也就是说向生成醋酸的方向发展.1年前查看全部
- 醋酸钠溶液中加醋酸纳 平衡怎么移动
 天空中的飞燕1年前2
天空中的飞燕1年前2 -
 隔岸赏景 共回答了24个问题
隔岸赏景 共回答了24个问题 |采纳率87.5%CH3COOH ==可逆== CH3COO- + H+
向逆反应方向移动,H+ 浓度降低 ,pH 增大.1年前查看全部
- 在绝热情况下向两份0.1mol/L的醋酸钠溶液中分别加入少量KNO3固体,为什么 c(Ac-)/c(Na+)会增大!
在绝热情况下向两份0.1mol/L的醋酸钠溶液中分别加入少量KNO3固体,为什么 c(Ac-)/c(Na+)会增大!
RT b4b_11181年前1
b4b_11181年前1 -
 痛打落水狗3377 共回答了17个问题
痛打落水狗3377 共回答了17个问题 |采纳率82.4%加入的少量硝酸钾,电离后发生盐效应使醋酸的表观离解度增大
更多的醋酸分子电离,Ac-浓度增大
故 c(Ac-)/c(Na+)会增大!1年前查看全部
- 2mol/l 的醋酸钠溶液如何配置
 老顽童A1年前1
老顽童A1年前1 -
 灰色黯伤 共回答了24个问题
灰色黯伤 共回答了24个问题 |采纳率91.7%首先应该确定配制溶液的体积,假设是1000毫升,
其次应该知道所用的是无水醋酸钠还是三水醋酸钠,
如果用的是无水醋酸钠,那么需要无水醋酸钠的质量是82×2=162克,加水配制成1000毫升溶液即可.
如果用的是三水醋酸钠,那么需要三水醋酸钠的质量是136×2=272克,加水配制成1000毫升溶液即可.1年前查看全部
- 相同pH的醋酸溶液和氢氰酸中 醋酸钠溶液和氰化钠溶液中 醋酸根和氰酸根浓度谁大
 y6411111年前1
y6411111年前1 -
 shinygh 共回答了22个问题
shinygh 共回答了22个问题 |采纳率81.8%醋酸酸性比氢氰酸强的多 氰酸根比醋酸根水解程度大
电荷守恒 CH3COOH:c(H+)=c(CH3COO-)+c(OH-)
HCN:c(H+)=c(CN-)+c(OH-)
相同pH的醋酸溶液和氢氰酸中 相同pH 氢离子浓度相同 氢氧根浓度相同 醋酸根和氰酸根浓度相同
电荷守恒 醋酸钠溶液 CH3COONa :c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
氰化钠溶液中 NaCN :c(Na+)+c(H+)=c(CN-)+c(OH-)
相同pH 氢离子浓度相同 氢氧根浓度相同
氰酸根比醋酸根水解程度大 氰化钠溶液比 醋酸钠溶液浓度小
醋酸根比氰酸根浓度大1年前查看全部
- 大学无机化学题现有125mL0.1mol/L的醋酸钠溶液配置250mL,PH=5的缓冲溶液,需加入6mol/L的醋酸多少
大学无机化学题
现有125mL0.1mol/L的醋酸钠溶液配置250mL,PH=5的缓冲溶液,需加入6mol/L的醋酸多少毫升. 变卦1年前1
变卦1年前1 -
 xiangnan88 共回答了26个问题
xiangnan88 共回答了26个问题 |采纳率96.2%PH=PKa-lg[HAc]/[Ac-]
5=4.76-lg[HAc]/[Ac-]
lg[HAc]/[Ac-]=-0.24
[HAc]/[Ac-]=0.575
需要6mol/L醋酸的体积1000×0.575×0.125/6=12毫升1年前查看全部
- 醋酸钠溶液与盐酸反应后可生成醋酸和氯化钠 能否证明醋酸是弱酸,为什么
 liang4425339341年前1
liang4425339341年前1 -
 慕容秋水0 共回答了15个问题
慕容秋水0 共回答了15个问题 |采纳率86.7%CH3COONA+HCL=CH3COOH+NACL1年前查看全部
- 现有0.175mol/L醋酸钠溶液500mL(已知醋酸的电离常数Ka=1.75×10-5)
现有0.175mol/L醋酸钠溶液500mL(已知醋酸的电离常数Ka=1.75×10-5)
(1)写出醋酸钠水解反应的化学方程式______.
(2)下列图象能说明醋酸钠的水解反应达到平衡的是______.
(3)在醋酸钠溶液中加入下列少量物质,水解平衡向正反应方向移动的有______.
A.冰醋酸B.纯碱固体C.醋酸钙固体D.氯化铵固体
(4)在醋酸钠溶液中加入少量冰醋酸后,溶液中微粒浓度的关系式能成立的有______.
A.c(CH3COO-)+c(CH3COOH)>c(Na+) B.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)D.c(CH3COO-)>c(H+)>c(OH-)>c(Na+)
(5)欲配制0.175mol/L醋酸钠溶液500mL,可采用以下两种方案:
方案一:用托盘天平称取______g无水醋酸钠,溶于适量水中,配成500mL溶液.
方案二:用体积均为250mL且浓度均为______的醋酸与氢氧化钠两溶液混合而成(设混合后的体积等于混合前两者体积之和).
(6)在室温下,0.175mol/L醋酸钠溶液的PH约为______(已知醋酸根的水解反应的平衡常数K=
).Kw Ka(CH3COOH)  woly_wu1年前1
woly_wu1年前1 -
 小小皇马 共回答了19个问题
小小皇马 共回答了19个问题 |采纳率89.5%解题思路:(1)醋酸钠是强碱弱酸盐,醋酸钠水解生成醋酸和氢氧化钠;
(2)醋酸钠溶液中醋酸根离子水解生成醋酸,所以溶液中醋酸根离子浓度逐渐减小直至达到平衡状态,溶液的PH逐渐增大直至不变,水的离子积常数、钠离子数都不变;
(3)增大反应物的浓度或减小生成物浓度,则水解反应向正反应方向移动;
(4)在醋酸钠溶液中加入少量冰醋酸后,溶液中存在物料守恒、电荷守恒,据此解答;
(5)根据m=CVM计算溶质的质量;
(6)根据水解平衡常数K=
进行计算.KW Ka(CH3COOH) (1)醋酸钠水解生成醋酸和氢氧化钠,化学方程式为CH3COONa+H2O⇌CH3COOH+NaOH,故答案为:CH3COONa+H2O⇌CH3COOH+NaOH;
(2)A.钠离子不水解,所以浓度始终不变,故A错误;
B.醋酸根离子开始时水解速率最大,后逐渐减小,平衡时不再变化,故B正确;
C.随着水解的逐渐进行,pH逐渐增大,平衡时不再变化,故C正确;
D.KW是一温度常数,温度不变,KW不变,故D错误;
故选BC;
(3)A.加入冰醋酸溶液中醋酸浓度增大,平衡左移,故A错误;
B.加入纯碱固体,对平衡体系的离子浓度无影响,平衡不移动,故B错误;
C.加入醋酸钙固体,溶液在醋酸根离子浓度增大,平衡右移,故C正确;
D.加入氯化铵固体,铵根离子与水解生成的氢氧根离子结合成一水合氨,使溶液中氢氧根离子浓度减小,平衡右移,故D正确;
故选CD;
(4)A.加入冰醋酸,使醋酸根离子浓度增大,但钠离子浓度不变,所以存在c(CH3COO-)+c(CH3COOH)>c(Na+),故A正确;
B.加入少量冰醋酸,平衡左移,醋酸根离子浓度增大,大于钠离子浓度,故B错误;
C.加入冰醋酸,当溶液中醋酸浓度较大时,醋酸的电离大于醋酸根离子的水解程度,醋酸根离子浓度增大,溶液呈酸性,故C正确;
D.无论是否电离程度大于水解程度,都不会存在c(OH-)>c(Na+),故D错误;
故选AC.
(5)有m=nM=CVM=0.175mol/L×0.5L×82g/mol=7.175g,所以托盘天平称量的质量为7.2g,
醋酸与氢氧化钠等浓度等体积混合,混合后的溶液浓度减半为0.175mol/L,所以原来的浓度为0.35mol/L,
故答案为:7.2;0.35mol/L;
(6)水解平衡常数K=
KW
Ka(CH3COOH)=
c(H+).c(OH−)
c(H+).c(CH3COO−)
c(CH3COOH)=
c2(OH−)
c(CH3COO−)=
10−14
1.75×10−5,C(OH-)=10-3 mol/L,则溶液的pH=9,故答案为:9.点评:
本题考点: 离子浓度大小的比较;化学平衡状态的判断;弱电解质在水溶液中的电离平衡;溶液的配制.
考点点评: 本题考查较综合,涉及水解平衡常数的计算、盐类水解平衡移动方向的判断等知识点,难点是水解平衡常数公式的灵活变换,注意(5)题托盘天平的感量,为易错点.1年前查看全部
- 在醋酸钠溶液中加入氨水可抑制水解
在醋酸钠溶液中加入氨水可抑制水解
NaAc=Na+和Ac-
Ac- + H2O = HAc+OH-
我知道加入氨水可增加OH-,使反应向逆方向移动从而抑制水解.可氨水不是可以和醋酸反应吗,这样不就使反应向正方向移动,促进水解了吗?
谁能够解答我的疑问? zhtoto0071年前3
zhtoto0071年前3 -
 hnxclhj 共回答了25个问题
hnxclhj 共回答了25个问题 |采纳率96%氨水本身就是碱性的,
所以,抑制作用大于促进作用.1年前查看全部
- ph均为3的NaClO溶液,Na2CO3溶液,醋酸钠溶液,三个溶液的物质的量浓度从大到小排序怎么弄?答案不重要,求思路
 猪是的念着反1年前1
猪是的念着反1年前1 -
 咖啡和咖啡豆 共回答了18个问题
咖啡和咖啡豆 共回答了18个问题 |采纳率94.4%题目有些问题,这些溶液均呈碱性,PH不可能小于7,若改为PH=9,Na2CO3小于NaCIO小于CH3COONa,因为这里它们三个所对应的弱酸强弱顺序为CH3COOH大于HCIO大于HCO3-,所以相同物质的量浓度的三者溶液PH大小Na2CO3大于NaCIO大于CH3COONa,而PH相等则颠倒,1年前查看全部
- 醋酸钠溶液中加入醋酸钠固体,各组分浓度怎么变化
 迷茫人生的龙1年前3
迷茫人生的龙1年前3 -
 冰山衣角 共回答了20个问题
冰山衣角 共回答了20个问题 |采纳率90%分情况勒,如果是饱和溶液则不变,如果不饱和,醋酸钠会电离,醋酸是弱电解质,水解所以钠离子大于醋酸离子,大于氢离子大于醋酸1年前查看全部
- 0.2mol/L醋酸与0.1mol/L醋酸钠溶液等体积混合混合,为什么有2c(CH3COO-)+3c(OH-)=c(CH
0.2mol/L醋酸与0.1mol/L醋酸钠溶液等体积混合混合,为什么有2c(CH3COO-)+3c(OH-)=c(CH3COOH)+3c(H+)
 狮子山一号1年前1
狮子山一号1年前1 -
 奶嘴嘟嘟 共回答了24个问题
奶嘴嘟嘟 共回答了24个问题 |采纳率87.5%电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+)
物料守恒:c(CH3COO-)+c(CH3COOH)=3c(Na+)
一式乘以3,减去二式,得到质子守恒.
质子守恒:2c(CH3COO-)+3c(OH-)=c(CH3COOH)+3c(H+)1年前查看全部
- 下列叙述中,错误的是A向0.1mol/l的醋酸溶液中加入少量的醋酸钠溶液,溶液的ph会增大B向0.1mol/l的醋酸溶液
下列叙述中,错误的是
A向0.1mol/l的醋酸溶液中加入少量的醋酸钠溶液,溶液的ph会增大
B向0.1mol/l的醋酸溶液中加入少量的NAOH固体,溶液中的c(ch3cooh-)会增大
C向0.1mol/l的醋酸溶液中加入大量的水,醋酸的电离度增大,溶液的c(H+)也增大
D向0.1mol/l的醋酸溶液中加入少量的浓盐酸,溶液的导电性增强.
求各个选项详解... fengfeng811年前5
fengfeng811年前5 -
 zle19992002 共回答了18个问题
zle19992002 共回答了18个问题 |采纳率83.3%A对:醋酸是酸性的,醋酸钠是碱性的,从宏观上来说,酸性物质加碱性物质,PH是增大的
B对:醋酸溶液中,存在如下的电离平衡:CH3COOH可逆号CH3COO-+H+,加入NaOH固体,溶解后产生的OH-会中和掉H+,平衡向右移动,n(CH3COO-)增大,溶液体积几乎不变,所以c(CH3COO-)增大
C错:醋酸溶液加水后,醋酸电离程度是增大了,但由于溶液体积增大的更多,溶液中H+浓度还是小 了.从宏观上来说,酸性溶液加水稀释,酸性会下降,所以H+减小.
D对:醋酸溶液加入弄盐酸,会抑制醋酸电离,但是加入的H+要多余因为抑制电离而减少的H+,所以溶液中,总体的H+浓度还是增加了.宏观上来说:酸性溶液加上酸性更强的溶液,酸度会比原来大,也就是H+浓度会增加,H+浓度增大,导电性也就增强了.(溶液中导电性是由离子浓度大小决定的).
若判断不准各离子的浓度的变化,可从宏观上客观存在的事情来推断.1年前查看全部
- 醋酸钠溶液升温,PH怎么变?直接从水解平衡角度考虑吗?可是升温后水的离子积也增大啊?
 c94536fd000e3c7b1年前1
c94536fd000e3c7b1年前1 -
 xinjian007 共回答了21个问题
xinjian007 共回答了21个问题 |采纳率85.7%盐类水解是吸热的,故升温有利水解平衡向右移动,水解程度增大,CO32- +H2O == HCO3-+OH- OH-增多,PH增大
水不考虑 因为水电离的H+和OH- 始终相等1年前查看全部
- ph=7的醋酸和醋酸钠溶液混合液中离子浓度关系是钠离子等于醋酸根大于氢离子等于氢氧根,醋酸浓度排在哪
 booksky0011年前3
booksky0011年前3 -
 尚家gg03 共回答了29个问题
尚家gg03 共回答了29个问题 |采纳率93.1%该混合溶液中,其离子浓度的排序应该是:
[Ac-] > [Na+] > c(HAc) > [H+] = [OH-]1年前查看全部
- 完成下列离子方程式。⑴醋酸钠溶液中加入足量的稀硫酸:___________________________。⑵硫酸铝溶液
完成下列离子方程式。
⑴醋酸钠溶液中加入足量的稀硫酸:___________________________。
⑵硫酸铝溶液中加入过量氨水:____________________________。
⑶电解MgCl 2 溶液:___________________________。
⑷NaHCO 3 溶液加足量石灰水:_____________________________。 66684281年前1
66684281年前1 -
 我输光了 共回答了17个问题
我输光了 共回答了17个问题 |采纳率100%⑴CH 3 COO - +H + = CH 3 COOH;⑵Al 3+ +3NH 3 . H 2 O=Al(OH) 3 ↓+3NH 4 + ;⑶Mg 2 + +2Cl - +2H 2 O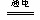 H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
⑴醋酸钠溶液中加入稀硫酸生成弱电解质CH 3 COOH,其离子方程式为:CH 3 COO - +H + = CH 3 COOH;⑵硫酸铝溶液中加入过量氨水,生成的Al(OH) 3 沉淀不会继续溶解到过量的氨水中,其离子方程式为:Al 3+ +3NH 3 . H 2 O=Al(OH) 3 ↓+3NH 4 + ;⑶电解MgCl 2 溶液生成的OH - 会与Mg 2 + 生成Mg(OH) 2 沉淀,其离子方程式为:Mg 2 + +2Cl - +2H 2 O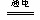 H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷NaHCO 3 溶液加足量石灰水反应,首先是HCO 3 - + OH - = CO 3 2 - + H 2 O,然后生成的CO 3 2 - 与Ca 2+ 反应生成CaCO 3 沉淀,其总离子方程式为:HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
1年前查看全部
H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷NaHCO 3 溶液加足量石灰水反应,首先是HCO 3 - + OH - = CO 3 2 - + H 2 O,然后生成的CO 3 2 - 与Ca 2+ 反应生成CaCO 3 沉淀,其总离子方程式为:HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
1年前查看全部
- 在0.1mol/L的醋酸钠溶液中加适量的水泽离子浓度增大的是氢离子还是氢氧跟离子,为什么
 gordonking20061年前1
gordonking20061年前1 -
 激战102 共回答了26个问题
激战102 共回答了26个问题 |采纳率88.5%25摄氏度时,将1mol/L的醋酸钠溶液用水稀释至0.1mol/L,溶液中增大的是()
A c(OH-)
B c(CH3COOH)
C c(H+)
D c(CH3COOH)/c(CH3COO-)
在0.1mol/L的醋酸钠溶液中加适量的水,醋酸钠的水解程度增大,CH3COOH的物质的量增大了.但溶液的体积增加的更快,所以CH3COOH的物质的量浓度会减小,溶液的碱性变弱,c(OH-)在变小,则c(H+)变大1年前查看全部
- 将盐酸加入到醋酸钠溶液中会使 醋酸根水解向哪个方向移动?资料上说是促进,我想是因为氢离子与醋酸根水解产生的但是OH-结合
将盐酸加入到醋酸钠溶液中
会使 醋酸根水解向哪个方向移动?
资料上说是促进,我想是因为氢离子与醋酸根水解产生的但是OH-结合,使之正向移动。
但是加氢离子会使C(H+)增加,这样由水的离子积不变可知c(OH-)必然减少,使之平衡逆向移动。
我们老师是按第二种方法讲的,到底那一种说法是对的啊? 走过ww冬季1年前1
走过ww冬季1年前1 -
 都市xx别理我 共回答了16个问题
都市xx别理我 共回答了16个问题 |采纳率100%促进水解,正向水解方向.其实应该理解为强酸制弱酸.而对水的解离影响不大,水的解离本来就极微量1年前查看全部
- 盐酸滴加到醋酸钠溶液中能否反映 + 原因
 lisonyang1年前1
lisonyang1年前1 -
 布布狗 共回答了18个问题
布布狗 共回答了18个问题 |采纳率94.4%会的,但是如果盐酸的浓度太低,反应会不是很明显.原因是强酸制弱酸.1年前查看全部
- 浓度相同体积相同醋酸和醋酸钠溶液混合之后 为什么会有 醋酸+醋酸根=2*钠离子 这种物料守恒?
浓度相同体积相同醋酸和醋酸钠溶液混合之后 为什么会有 醋酸+醋酸根=2*钠离子 这种物料守恒?
具体怎么个物料守恒? 寻找印子里的影子1年前1
寻找印子里的影子1年前1 -
 阿可露露 共回答了18个问题
阿可露露 共回答了18个问题 |采纳率94.4%也就是醋酸与醋酸钠的物质的量相同.那么醋酸根的物质的量就是钠的物质的量的二倍了.1年前查看全部
- 盐酸滴加到醋酸钠溶液中的离子方程
 beendy1年前1
beendy1年前1 -
 mengtuolingwo 共回答了24个问题
mengtuolingwo 共回答了24个问题 |采纳率95.8%氢离子+醋酸根离子=醋酸 因为醋酸是弱电解质 而醋酸钠是强电解质1年前查看全部
- 醋酸钠溶液中离子浓度比较醋酸分子和氢离子哪个浓度更大?为什么?总的离子浓度怎样排?我先重申,是醋酸钠,不是醋酸...提问
醋酸钠溶液中离子浓度比较
醋酸分子和氢离子哪个浓度更大?为什么?
总的离子浓度怎样排?
我先重申,是醋酸钠,不是醋酸...
提问一楼:既然是水解,那么醋酸根应该和水中电离的氢离子结合.而氢氧根也是由水电离的,为什么醋酸分子会大于氢氧根离子呢? 手机玩家1年前1
手机玩家1年前1 -
 fitbsky 共回答了28个问题
fitbsky 共回答了28个问题 |采纳率96.4%列出质子守恒就可以了
OH-=CH3COOH+ + H+
醋酸分子和氢离子浓度比较难比较
主要是根据pH来判断
举个例子吧,pH=9的醋酸钠溶液,
氢离子浓度为10的负九次方mol/L
那么氢氧根浓度就是10的负5次方mol/L
用氢氧根的浓度减去氢离子浓度就可以得到醋酸分子浓度...过程比较麻烦
总的离子浓度是Na+>CH3COO->OH->H+
后面的问题比较容易,只要记着电离是百分之一,水解是千分之一就可以了1年前查看全部
- 浓度均为0.1mol/L的醋酸和醋酸钠溶液等体积混合,
浓度均为0.1mol/L的醋酸和醋酸钠溶液等体积混合,
醋酸的浓度+二倍氢离子浓度=醋酸根离子浓度+二倍氢氧根离子浓度
这是对的吗 vfdxgy1年前2
vfdxgy1年前2 -
 小狗饼饼 共回答了14个问题
小狗饼饼 共回答了14个问题 |采纳率85.7%对的
1.醋酸根+氢氧根=氢离子+钠离子 电荷守恒
2.醋酸+醋酸根=2*钠离子 物料守恒
1式*2 再减2式
就.1年前查看全部
大家在问
- 1The last five years have seen many disasters in China.这句话的ha
- 2判断下图中大园的周长和里面两个圆周长之和哪个更长(d1=3厘米,d2=5厘米)
- 3用简便算法计算下面各题102×0.35 (8+0.8)×1.25 7.7×1.7+2.3×7.7 2.98×0.25×4
- 4loading please wait...
- 5DNA才是使R型细菌产生稳定遗传变化的物质为什么没的赞同
- 6这几个序数词怎么写?thirty twenty-six forty-seven one hundred 还有why的反义
- 7四个质点作直线运动,它们的速度图象分别如图所示,下列说法中正确的是( )
- 8近年来,国际上悄然兴起一股温和之风,“伙伴关系”多现报端,冷战时期那种两极对立、剑拔弩张的气氛,正在为二种“碰撞中磨合”
- 9四字成语,成语接龙.大智若愚>>如虎添翼>>逆流而上>>?
- 10求歇后语或成语或俗语 主要意思是 不能在同一个地方犯两次错
- 11你说了那么多,感觉我在你心里一点地位都没有,我真的有那么差吗?这句话翻译英文怎么说?
- 12有一数列:1,5,9,13,17,……,这数列的第300项是几 305是这个数列中的第几项
- 13绝对标高的含义我知道,但真不明白绝对标高有什么作用 呢?意义何在呢?希望朋友们能通俗易懂的解释?
- 14怎么解答这个题:1+一加二分之一再加一加二加三分之一再依次往下加,最后是一加二加三加四一直加到100
- 15小明带了10元钱去书店,先买了一本科技书,用去了总数的 ,接着又买了一本 元的本子,这时小明还剩下(
