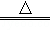侯德榜制碱法,的副产物是什么?书上只说其副产物,可以作化肥或电解液,是不是氯化铵?
 噶发噶2022-10-04 11:39:542条回答
噶发噶2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 笨ben 共回答了21个问题
笨ben 共回答了21个问题 |采纳率71.4%- 原来产生氯化钙,现在产生氯化铵
- 1年前
 爱上被遗忘 共回答了1834个问题
爱上被遗忘 共回答了1834个问题 |采纳率- 是的
- 1年前
相关推荐
- 侯德榜的联合制碱法的原理,
 A200101931年前1
A200101931年前1 -
 nxwzxkt5 共回答了22个问题
nxwzxkt5 共回答了22个问题 |采纳率77.3%(联合制碱法) (1)NH3+H2O+CO2=NH4HCO3(2) NH4HCO3+NaCl=NH4Cl+NaHCO3↓ (3)2NaHCO3=加热=Na2CO3+H2O+CO2↑即:①NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓ ②2NaHCO3=加热=Na2CO3+H2O+CO2↑氨气与水和二氧化碳反...1年前查看全部
- 一道化学计算题 速给我答案、5.侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠.现取仅含氯
一道化学计算题 速给我答案、
5.侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠.现取仅含氯化钠杂质的纯碱样品33.2g,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g.
求:(1)该纯碱样品中Na2CO3的质量; 斗鱼pb1年前1
斗鱼pb1年前1 -
 28years 共回答了23个问题
28years 共回答了23个问题 |采纳率91.3%m=106*13.2/44=31.8g1年前查看全部
- 我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )

A. 沉淀池中的反应物共含有七种元素
B. 过滤得到的“母液”中一定只含有两种溶质
C. 图中X可能是氨气
D. 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 chutzpah11年前0
chutzpah11年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 侯德榜制碱制的是什么碱?纯碱?烧碱?火碱?那它们的化学方程式是什么?
 摆砖1年前3
摆砖1年前3 -
 royalam 共回答了16个问题
royalam 共回答了16个问题 |采纳率93.8%纯碱
1 向已经氨化的饱和食盐水中通入二氧化碳
NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出)
2 加热碳酸氢钠,得到碳酸钠
2NaHCO3=Na2CO3+H2O+CO2
3 利用碳酸钠通入石灰水,制得氢氧化钠
Na2CO3+Ca(OH)2=2NaOH+CaCO3
4 培烧碳酸钙,得到二氧化碳循环
CaCO3=CaO+CO2
CaO+H2O=Ca(OH)2
5 向1步反应的母液中,加入过量食盐,氯化铵结晶析出,制成化肥使用
侯德榜先生经过上千次试验,在1943年研究成功了联合制碱法.这种方法把合成氨和纯碱两种产品联合生产,提高了食盐利用率,缩短了生产流程,减少了对环境的污染,降低了纯碱的成本.1年前查看全部
- 下列物质,在玻璃、洗涤剂等工业上有广泛的应用,著名的化学家侯德榜曾出色地改进了它的生产技术.该物质是( )
下列物质,在玻璃、洗涤剂等工业上有广泛的应用,著名的化学家侯德榜曾出色地改进了它的生产技术.该物质是( )
A.碳酸钠
B.氯化钠
C.氢氧化钠
D.硝酸钾 娃哈哈h1581年前1
娃哈哈h1581年前1 -
 hnjwzq 共回答了19个问题
hnjwzq 共回答了19个问题 |采纳率78.9%解题思路:根据碳酸钠的用途和侯德榜联合制碱法的生产产品判断.著名的化学家侯德榜最突出的贡献是发明了联合制碱法,又称侯氏制碱法,为纯碱和氮肥工业的发展做出了杰出贡献,这里的纯碱就是碳酸钠,而且纯碱广泛用于玻璃、造纸、纺织、洗涤剂的生产等.
故选A.点评:
本题考点: 化学的历史发展过程.
考点点评: 了解化学发展的历史,有利于激发学生学习化学的兴趣,培养社会责任感,符合新课程标准三维目标的要求.1年前查看全部
- 侯德榜制碱法先通co2还NH3侯德榜制碱法向饱和食盐水中依次通入CO2,NH3行不?
 矛筑习1年前4
矛筑习1年前4 -
 月迷津渡su 共回答了13个问题
月迷津渡su 共回答了13个问题 |采纳率92.3%不行;侯德榜制碱法是向氯化钠中通入氨气 再通二氧化碳 利用NaHCO3在水中的溶解度小于
NH4HCO3 使得饱和NaHCO3形成沉淀 其先决条件是:必须使NH4HCO3溶液饱和;CO2在水中的溶解度太小 再通入NH3 无法得到饱和的NH4HCO3 根本不可能得到饱和NH4HCO3,相反 NH3在水中1:700溶解 使溶液呈碱性 大大增大了CO2的溶解度 就可以制取饱和NH4HCO3.1年前查看全部
- (2014•兴化市模拟)我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯
(2014•兴化市模拟)我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要足量的原因:______.实验操作 实验现象 实验结论 取一定量纯碱样品配成溶液后,滴加足量的CaCl2溶液. 产生白色沉淀 反应的化学方程式:
______
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为______.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数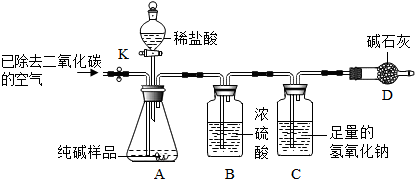
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的______,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应).待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿,目的是______.装置______(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果______(选填“偏大”或“偏小”).
(6)某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品6g,放入20g水中使其完全溶解,再加入稀盐酸26.2g,恰好完全反应,反应后溶液的总质量为50g.试计算:①生成二氧化碳的质量;②样品中Na2CO3的质量分数.(写出计算过程,结果保留一位小数) kiky的笨女人1年前1
kiky的笨女人1年前1 -
 tingyuchun 共回答了19个问题
tingyuchun 共回答了19个问题 |采纳率94.7%解题思路:(1)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
(2)为了使碳酸钠完全转化成碳酸钙沉淀,应该加入足量的氯化钙溶液;
(3)如果不洗涤沉淀物,沉淀物上会附着可溶性物质,从而使沉淀物质量增加;
(4)为了防止A、B装置中的二氧化碳对实验结果的影响,应该先对装置A和B通入已除去CO2的空气一会儿;
(5)为了使反应生成的二氧化碳全部被氢氧化钠溶液吸收,应该待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿;
C装置在反应前后的质量差就是产生CO2的质量;
D中的碱石灰能够吸收空气中的水和二氧化碳,以防二氧化碳进入C装置影响实验结果;
(6)根据反应前后的质量差可以计算生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算碳酸钠的质量分数.(1)碳酸钠和氯化钙反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
故填:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)滴加的CaCl2溶液要足量的原因是使碳酸钠完全反应.
故填:使碳酸钠完全反应.
(3)如果不洗涤沉淀物会造成测定结果大于91%,这是因为如果不洗涤沉淀物,沉淀物上会附着可溶性物质,从而使沉淀物质量增加,通过计算会造成测定结果大于91%.
故填:附着可溶性物质(或杂质)使沉淀物质量增加.
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳.
故填:二氧化碳.
(5)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿,目的是使生成的二氧化碳全部被C装置中的氢氧化钠吸收;
装置C在反应前后的质量差就是产生CO2的质量;
若没有装置D,空气中的二氧化碳会进入氢氧化钠溶液中,将会使测定结果偏大.
故填:使生成的二氧化碳全部被C装置中的氢氧化钠吸收;C;偏大.
(6)①生成二氧化碳的质量为:20g+6g+26.2g-50g=2.2g,
答:生成二氧化碳的质量为2.2g.
②设Na2CO3的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 44
x2.2g
[106/44=
x
2.2g],
x=5.3g,
则样品中Na2CO3的质量分数为:[5.3g/6g]×100%≈88.3%,
答:样品中Na2CO3质量分数为88.3%.点评:
本题考点: 实验探究物质的组成成分以及含量;气体的净化(除杂);盐的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.1年前查看全部
- 下列物质中,有一种盐在玻璃、洗涤剂生产等工业上广泛应用.著名化学家侯德榜在改进它的生产技术方面作出了卓越的贡献.这种盐是
下列物质中,有一种盐在玻璃、洗涤剂生产等工业上广泛应用.著名化学家侯德榜在改进它的生产技术方面作出了卓越的贡献.这种盐是( ) A.碳酸钠 B.氯化钠 C.硝酸钾 D.硫酸铜  1178142861年前1
1178142861年前1 -
 zwlone006 共回答了16个问题
zwlone006 共回答了16个问题 |采纳率87.5%碳酸钠在玻璃、洗涤剂生产等工业上广泛应用,我国著名化学家侯德榜发明了联合制碱法,在改进它的生产技术方面作出了卓越的贡献,所以A正确;氯化钠、硝酸钾、硫酸铜不能用于玻璃、洗涤剂等工业生产.
故选C.1年前查看全部
- 根据侯德榜制碱法原理并参考下表的数据,实验室制备纯碱Na 2 CO 3 的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯
根据侯德榜制碱法原理并参考下表的数据,实验室制备纯碱Na 2 CO 3 的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30~35℃,搅拌下分批加入研细的NH 4 HCO 3 固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO 3 晶体.用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得Na 2 CO 3 固体.四种盐在不同温度下的溶解度(g/100g水)表①>35℃NH 4 HCO 3 会有分解
请回答:温度溶解度盐 0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 100℃ NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 39.8 NH 4 HCO 3 11.9 15.8 21.0 27.0 -① - - - NaHCO 3 6.9 8.1 9.6 11.1 12.7 14.5 16.4 - NH 4 Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.3 77.3
(1)反应温度控制在30~35℃,是因为若高于35℃,则______,若低于30℃,则______;为控制此温度范围,采取的加热方法为______;
(2)加料完毕后,继续保温30分钟,目的是______.静置后只析出NaHCO 3 晶体的原因是______.用蒸馏水洗涤NaHCO 3 晶体的目的是除去______杂质(以化学式表示);
(3)过滤所得的母液中含有______(以化学式表示),需加入______,并作进一步处理,使NaCl溶液循环使用,同时可回收NH 4 Cl;
(4)测试纯碱产品中NaHCO 3 含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色(指示CO 3 2- +H + =HCO 3 - 反应的终点),所用HCl溶液体积为V 1 mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V 2 mL.写出纯碱样品中NaHCO 3 质量分数的计算式:NaHCO 3 (%)=______. 554186901年前1
554186901年前1 -
 zyclq 共回答了18个问题
zyclq 共回答了18个问题 |采纳率83.3%(1)碳酸氢铵10~20℃时,不易分解,30℃时开始大量分解.若温度过低,则反应速率较慢.故反应温度控制在30-35℃之间为宜.水浴加热是把要加热的物质放在水中,通过给水加热达到给物质加热的效果.一般都是把要反应的物质放在试管中,再把试管放在装有水的烧杯中,再在烧杯中插一根温度计,可以控制反应温度.水浴加热的优点是避免了直接加热造成的过度剧烈与温度的不可控性,可以平稳地加热,许多反应需要严格的温度控制,就需要水浴加热.水浴加热的缺点是加热温度最高只能达到100度.
故答案为:NH 4 HCO 3 分解;反应速率降低;水浴加热;
(2)加料完毕后,继续保温30分钟,可以使反应充分进行,使反应完全.碳酸氢铵0℃时溶解度为11.3%;20℃时为21%;40℃时为35%.碳酸氢钠0℃溶解度为6.9 g,5℃为7.45 g,
10℃为8.15 g,15℃为8.85 g,20℃为9.6 g,25℃为10.35 g,30℃为11.1g,35℃为11.9 g,40℃为12.7 g,45℃为13.55 g,50℃为14.45 g,55℃为15.4g,60℃为16.4g.30℃时碳酸氢钠的溶解度更小,故碳酸氢钠先析出.用蒸馏水洗涤NaHCO 3 晶体的目的是为了除去杂质,此反应中杂质为 NaCl、NH 4 Cl、NH 4 HCO 3 .
故答案为:使反应充分进行;NaHCO 3 的溶解度最小;NaCl、NH 4 Cl、NH 4 HCO 3 ;
(3)过滤除去析出的碳酸氢钠,溶液中还有部分碳酸氢钠未析出,还有溶解在溶液中的NaCl、NH 4 Cl、NH 4 HCO 3 ,所得的母液主要成分为NaHCO 3 、NaCl、NH 4 Cl、NH 4 HCO 3 .加入盐酸后,碳酸氢钠转化为氯化钠,碳酸氢铵转化为氯化铵,这时溶液中的NaCl溶液循环使用,同时可回收NH 4 Cl.
故答案为:NaHCO 3 、NaCl、NH 4 Cl、NH 4 HCO 3 ;HCl;
(4)加酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色,指示CO 3 2- +H + =HCO 3 - 反应的终点,所用HCl溶液体积为V 1 mL;再加甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,指示HCO 3 - +H + =CO 2 +H 2 O反应的终点,所用HCl溶液体积为V 2 mL.上述的两个离子方程式为①CO 3 2- +H + =HCO 3 - ②HCO 3 - +H + =CO 2 +H 2 O,故样品中含有的碳酸氢钠反应消耗盐酸体积为(V 2 -V 1 )mL,消耗盐酸的物质的量为c(V 2 -V 1 )÷1000 mol,故碳酸氢钠的物质的量为c(V 2 -V 1 )÷1000 mol,碳酸氢钠的质量为c(V 2 -V 1 )M÷1000 g,碳酸氢钠的质量分数为
c( V 2 - V 1 )M
1000W ×100%,
故答案为:
c( V 2 - V 1 )M
1000W ×100%.1年前查看全部
- 下列物质,在玻璃、洗涤剂等工业上有广泛的应用,著名的化学家侯德榜曾出色地改进了它的生产技术。该物质是 [
下列物质,在玻璃、洗涤剂等工业上有广泛的应用,著名的化学家侯德榜曾出色地改进了它的生产技术。该物质是 [ ]A.碳酸钠
B.氯化钠
C.氢氧化钠
D.硝酸 rainblue06081年前1
rainblue06081年前1 -
 越P越开心 共回答了10个问题
越P越开心 共回答了10个问题 |采纳率80%A1年前查看全部
- 化学中侯德榜制碱的原料 产品 副产物 是什嘛
 i3mu21年前2
i3mu21年前2 -
 落叶2006 共回答了10个问题
落叶2006 共回答了10个问题 |采纳率90%化学原理
侯氏制碱法又名联合制碱法
(1)NH3+H2O+CO2=NH4HCO3
(2)NH4HCO3+NaCl=NH4Cl+NaHCO3↓
(3)2NaHCO3(加热)=Na2CO3+H2O+CO2↑
即:①NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓
②2NaHCO3=加热=Na2CO3+H2O+CO2↑
优点
保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高到 96 %; NH4Cl 可做氮肥;可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2 ,革除了 CaCO3 制 CO2 这一工序.
注:碱就是碳酸钠
原料 NH3 H2O CO2 NaCl
产品 Na2CO3
副产品NH4Cl1年前查看全部
- (2011•南平)侯德榜是中国化学工业先驱者,一生致力于化工事业,1943年他创立了“侯氏制碱法”,其核心原理是:工长里
(2011•南平)侯德榜是中国化学工业先驱者,一生致力于化工事业,1943年他创立了“侯氏制碱法”,其核心原理是:工长里可将二氧化碳温室气体回收用于生产碳酸氢钠(NaHCO3).现有22kg二氧化碳完全参与反应,计算可制得多少千克的碳酸氢钠?
(已知NaHCO3的相对分子质量84) xxz21231年前1
xxz21231年前1 -
 vicewsw 共回答了9个问题
vicewsw 共回答了9个问题 |采纳率100%解题思路:根据二氧化碳的质量为已知量带入化学方程式可求得生成的碳酸氢钠的质量.设生成碳酸氢钠的质量为x
NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl
44 84
22kg x
[44/22Kg=
84
x]
x═42kg
答:生成碳酸氢钠的质量为42kg点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题难度不大主要考查利用化学方程式进行计算,根据已知量带入化学方程式即可求得.1年前查看全部
- 我国著名化学家侯德榜发明的联合制碱法,主要原理是:向浓氨水(NH 3 •H 2 O)中通入足量的CO 2 生成NH 4
我国著名化学家侯德榜发明的联合制碱法,主要原理是:向浓氨水(NH 3 •H 2 O)中通入足量的CO 2 生成NH 4 HCO 3 (碳酸氢铵),然后加入食盐充分搅拌,两者发生复分解反应,由于碳酸氢钠的溶解度很小,便呈晶体析出,将析出的碳酸氢钠加热得碳酸钠,二氧化碳和水.请写出上述原理的三个化学方程式:
①______;
②______;
③______. szwolf1年前1
szwolf1年前1 -
 wvak9 共回答了23个问题
wvak9 共回答了23个问题 |采纳率95.7%①浓氨水和二氧化碳反应生成碳酸氢铵,故答案为:NH 3 •H 2 O+CO 2 =NH 4 HCO 3 ,
②碳酸氢钠的溶解度很小,表现为沉淀,所以可以发生复分解反应,碳酸氢铵和氯化钠反应生成碳酸氢钠和氯化铵,故答案为:NH 4 HCO 3 +NaCl=NH 4 Cl+NaHCO 3 ↓,
③碳酸氢钠在受热的条件下生成碳酸钠、水和二氧化碳,故答案为:2NaHCO 3
△
.
Na 2 CO 3 +H 2 O+CO 2 ↑1年前查看全部
- (2013•上海)与索尔维制碱法相比,侯德榜制碱法最突出的优点是( )
(2013•上海)与索尔维制碱法相比,侯德榜制碱法最突出的优点是( )
A.原料利用率高
B.设备少
C.循环利用的物质多
D.原料易得 打盹的aa猫1年前1
打盹的aa猫1年前1 -
 星冥 共回答了20个问题
星冥 共回答了20个问题 |采纳率85%索尔维法缺点:大量CaCl2用途不大,NaCl利用率只有70%,约有30%的NaCl留在母液中,侯氏制碱法的优点:把合成氨和纯碱两种产品联合生产,提高了食盐利用率,缩短了生产流程,减少了对环境的污染,降低了纯碱的成本.保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高到96%,
故选A.1年前查看全部
- 我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如下:
我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如下:
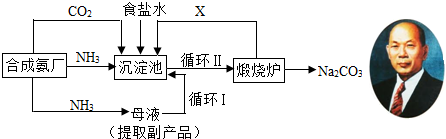
(1)上述生产纯碱的方法称联合制碱法或侯德榜制碱法联合制碱法或侯德榜制碱法,副产品的一种用途为化肥(或电解液、焊药等)化肥(或电解液、焊药等).
(2)沉淀池中发生的化学反应方程式是NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓
或NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NH4Cl+NaHCO3↓NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓
或NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NH4Cl+NaHCO3↓.
(3)写出上述流程中X物质的分子式CO2CO2.
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了II(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是过滤过滤.
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加稀硝酸和硝酸银溶液稀硝酸和硝酸银溶液.
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品.通氨气的作用有ACAC.
A.增大NH4+的浓度,使NH4Cl更多地析出B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度. _wwei1年前1
_wwei1年前1 -
 四级绿化 共回答了25个问题
四级绿化 共回答了25个问题 |采纳率92%解题思路:解答本题关键是清楚侯德榜制碱法的流程和反应原理,清楚每一步的操作和产物便可解答.
对于(5)问可利用检验氯离子的方法进行解答.
(6)问根据氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来分析;
同时通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度.(1)该生产纯碱的方法是侯德榜发现的,所以称侯德榜制碱法,也叫联合制碱法;
最终的副产物是氯化铵,是一种很好的氮肥,也可用作焊药或电解液.
故答案为:联合制碱法或侯德榜制碱法; 化肥(或电解液、焊药等)
(2)从流程图可以看出,沉淀池中加入的反应物有氨气、二氧化碳、氯化钠,根据生成物是碳酸氢钠,可推出反应物有水,同时可知碳酸氢钠为沉淀.
反应原理首先是氨气、二氧化碳和水反应生成碳酸氢氨,然后碳酸氢氨和氯化钠发生复分解反应交换成分生成碳酸氢钠晶体和氯化铵.
故答案为:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓
或NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NH4Cl+NaHCO3↓
(3)煅烧炉中发生的反应是碳酸氢钠受热分解,生成纯碱、二氧化碳气体和水,所以X是二氧化碳.
故答案为:CO2
(4)因为氯化钠最后剩余在母液中,所以循环I是氯化钠的循环;分离沉淀的方法是过滤.
故答案为:I; 过滤
(5)鉴别氯离子可向溶液中加入硝酸酸化的硝酸银溶液,生成白色沉淀证明有氯化钠存在.
故答案为:稀硝酸和硝酸银溶液
(6)氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来,所以选项A正确;
通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度所以选项C正确,选项B错误.
故答案为:AC点评:
本题考点: 纯碱的制取;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题有一定的难度,必须对课本上的制碱法的反应原理和流程十分清楚,同时也考查了化学方程式的书写的技巧、实验过程分析与判断的能力.1年前查看全部
- 我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界制碱技术的发展.下列关于过滤出碳酸氢钠后溶液的说法正确的是( )
我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界制碱技术的发展.下列关于过滤出碳酸氢钠后溶液的说法正确的是( )
A.一定是氯化钠的饱和溶液
B.一定是氯化铵的饱和溶液
C.一定是碳酸氢钠的饱和溶液
D.以上说法都错误 纯真的女生1年前1
纯真的女生1年前1 -
 渝靖 共回答了22个问题
渝靖 共回答了22个问题 |采纳率90.9%解题思路:根据既然有碳酸氢钠晶体析出,所以过滤出碳酸氢钠后溶液一定是碳酸氢钠的饱和溶液进行解答.既然有碳酸氢钠晶体析出,所以过滤出碳酸氢钠后溶液一定是碳酸氢钠的饱和溶液.
故选:C.点评:
本题考点: 饱和溶液和不饱和溶液.
考点点评: 此题是饱和溶液相关知识的考查题,解决的关键是对饱和溶液的理解,属基础性知识考查题.1年前查看全部
- “海水中的食盐用途广泛,例如侯德榜利用食盐为原料制的了纯碱”对吗?为什么?
 cls731年前3
cls731年前3 -
 白ee咪佩 共回答了18个问题
白ee咪佩 共回答了18个问题 |采纳率88.9%对.侯氏制碱法方程式:NaCl+H2O+CO2+NH3=NaHCO3+NH4Cl,2NaHCO3=加热=Na2CO3+H2O+CO2(气体)1年前查看全部
- 我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如下:
我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如下: 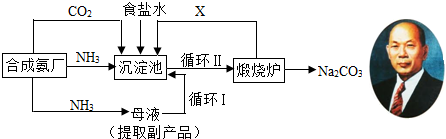
(1)上述生产纯碱的方法称______,副产品的一种用途为______.
(2)沉淀池中发生的化学反应方程式是______.
(3)写出上述流程中X物质的分子式______.
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是______.
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加______.
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品.通氨气的作用有______.
A.增大NH 4 + 的浓度,使NH 4 Cl更多地析出B.使NaHCO 3 更多地析出
C.使NaHCO 3 转化为Na 2 CO 3 ,提高析出的NH 4 Cl纯度. 云扬星汉1年前1
云扬星汉1年前1 -
 gaoshan666 共回答了17个问题
gaoshan666 共回答了17个问题 |采纳率94.1%(1)该生产纯碱的方法是侯德榜发现的,所以称侯德榜制碱法,也叫联合制碱法;
最终的副产物是氯化铵,是一种很好的氮肥,也可用作焊药或电解液.
故答案为:联合制碱法或侯德榜制碱法;化肥(或电解液、焊药等)
(2)从流程图可以看出,沉淀池中加入的反应物有氨气、二氧化碳、氯化钠,根据生成物是碳酸氢钠,可推出反应物有水,同时可知碳酸氢钠为沉淀.
反应原理首先是氨气、二氧化碳和水反应生成碳酸氢氨,然后碳酸氢氨和氯化钠发生复分解反应交换成分生成碳酸氢钠晶体和氯化铵.
故答案为:NH 3 +CO 2 +NaCl+H 2 O=NH 4 Cl+NaHCO 3 ↓
或NH 3 +CO 2 +H 2 O=NH 4 HCO 3 ,NH 4 HCO 3 +NaCl=NH 4 Cl+NaHCO 3 ↓
(3)煅烧炉中发生的反应是碳酸氢钠受热分解,生成纯碱、二氧化碳气体和水,所以X是二氧化碳.
故答案为:CO 2
(4)因为氯化钠最后剩余在母液中,所以循环I是氯化钠的循环;分离沉淀的方法是过滤.
故答案为:I;过滤
(5)鉴别氯离子可向溶液中加入硝酸酸化的硝酸银溶液,生成白色沉淀证明有氯化钠存在.
故答案为:稀硝酸和硝酸银溶液
(6)氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来,所以选项A正确;
通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度所以选项C正确,选项B错误.
故答案为:AC1年前查看全部
- 侯德榜制纯碱的化学方程式1、向浓氨水中通入足量的二氧化碳,生成碳铵;2、再加入食盐细末,并充分搅拌;3、将析出的碳酸氢钠
侯德榜制纯碱的化学方程式
1、向浓氨水中通入足量的二氧化碳,生成碳铵;
2、再加入食盐细末,并充分搅拌;
3、将析出的碳酸氢钠加热便制的纯碱.
请写出3个反应的方程式 eric___hu1年前6
eric___hu1年前6 -
 荣荣55 共回答了22个问题
荣荣55 共回答了22个问题 |采纳率95.5%1.NH3+H2O+CO2=NH4HCO3
2.NH4HCO3+NaCl=NH4Cl+NaHCO3↓
3.2NaHCO3=Na2CO3+CO2+H2O1年前查看全部
- 侯德榜制碱法中的循环物质是什么
 furnival1年前1
furnival1年前1 -
 铅笔盒2005 共回答了21个问题
铅笔盒2005 共回答了21个问题 |采纳率90.5%NACL+CO2+H2O+NH3=NAHCO3+NH4CL
2NAHCO3=NA2CO3+H2O+CO2循环物质是CO21年前查看全部
- 我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:

(1)NH 3 溶于水得到氨水,将无色酚酞溶液滴入氨水中,溶液呈 色.
(2)写出反应I的化学方程式 ;该反应的基本类型为 .
(3)操作a的过程是蒸发浓缩、 、过滤.
(4)上述工艺流程中可循环利用的物质是 . _漏网之灵_1年前1
_漏网之灵_1年前1 -
 helloark 共回答了13个问题
helloark 共回答了13个问题 |采纳率100%1年前查看全部
- 侯德榜的侯氏制碱法中,NaHCO3是因为饱和后析出,变成沉淀.有一个问题如下
侯德榜的侯氏制碱法中,NaHCO3是因为饱和后析出,变成沉淀.有一个问题如下
那么一些反应不可发生的化学反应在其饱和溶液中可否发生?比如NaSO4+MgCl是否可以在饱和的NaCl溶液中生成NaCl沉淀? lanxuese1年前1
lanxuese1年前1 -
 dqpovmg 共回答了13个问题
dqpovmg 共回答了13个问题 |采纳率100%Na2SO4+MgCl2可以在饱和的NaCl溶液中生成NaCl晶体.1年前查看全部
- 钱学森、李四光、竺可桢、侯德榜 谁是著名科学家 谁是地质学家
钱学森、李四光、竺可桢、侯德榜 谁是著名科学家 谁是地质学家
科学家要著名的.认真回答 风没有眼泪1年前1
风没有眼泪1年前1 -
 旋覆子 共回答了29个问题
旋覆子 共回答了29个问题 |采纳率86.2%科学家:钱学森
地质学家:李四光1年前查看全部
- 侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品33.2g
侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品33.2g,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g.
求:(1)该纯碱样品中Na2CO3的质量;
(2)反应后所得溶液中溶质的质量分数. lzqll1年前1
lzqll1年前1 -
 郁闷的大头鱼 共回答了17个问题
郁闷的大头鱼 共回答了17个问题 |采纳率94.1%解题思路:纯碱中碳酸钠与稀盐酸反应放出二氧化碳,根据质量守恒定律,利用反应前后物质总质量差即反应放出二氧化碳的质量;根据反应的化学方程式,计算出纯碱中碳酸钠的质量和反应后溶液中溶质氯化钠的质量,从而计算出反应后所得溶液中溶质的质量分数.反应放出的CO2的质量为:33.2g+130g-150g=13.2g
设参加反应的Na2CO3质量为x,生成的NaCl的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 13.2g
[106/44=
x
13.2g]
解之得 x=31.8g
[117/44=
y
13.2g]
解之得 y=35.1g
纯碱样品中NaCl的质量=33.2g-31.8g=1.4g
反应后溶液中NaCl的质量为=35.1g+1.4g=36.5g
反应后溶液中NaCl的质量分数=[36.5g/150g]×100%=24.3%
故答案为:(1)该纯碱样品中Na2CO3的质量31.8g;
(2)所得溶液中溶质的质量分数为24.3%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 反应后所得溶液中溶质氯化钠由原粉末中所含的氯化钠与反应后生成的氯化钠两部分所组成,解题时要注意到这点.1年前查看全部
- 侯德榜制碱法值得的碱是什么
 做恶的百度1年前1
做恶的百度1年前1 -
 林志龙 共回答了16个问题
林志龙 共回答了16个问题 |采纳率87.5%Na2C031年前查看全部
- 我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl,NaHCO3
Na2CO3+CO2+H2O的反应原理制备纯碱(Na2CO3).下面是在实验室进行模拟实验的生产流程示意图:△ .
饱和食盐溶液
A和食盐的饱和溶液通入足量气体A Ⅱ
悬浊液通入足量的气体B Ⅱ
晶体过滤 Ⅲ
纯碱(Na2CO3),则下列叙述错误的是( )Ⅵ
A.通入的气体B(CO2)可以循环利用
B.第Ⅲ步得到的晶体是NaHCO3,是发酵粉的主要成分
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶 comichunte1年前1
comichunte1年前1 -
 cpafox 共回答了20个问题
cpafox 共回答了20个问题 |采纳率100%解题思路:A.依据侯德榜制碱的原理:向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢钠,加热分解碳酸氢钠来制备碳酸钠;
B.第Ⅲ步得到的晶体是碳酸氢钠,发酵粉的主要成分;
C.通过过滤操作得到碳酸氢钠晶体;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体;A.根据题意“运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl,NaHCO3
△
.
Na2CO3+CO2+H2O的反应原理制备纯碱(Na2CO3)”,则通入的气体B(CO2)可以循环利用,故A正确;
B.发酵粉是一种复合添加剂,主要用作面制品和膨化食品的生产.发酵粉中含有许多物质,主要成分为碳酸氢钠和酒石酸,第Ⅲ步得到的晶体是碳酸氢钠,故B正确;
C.第Ⅲ步操作是过滤操操作,通过过滤得到碳酸氢钠晶体,所以需要的仪器有:烧杯、漏斗、玻璃棒,故C正确;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体,故D错误;
故选:D.点评:
本题考点: 纯碱的制取;过滤的原理、方法及其应用;常用盐的用途.
考点点评: 本题考查了侯德榜制碱的工作原理和流程分析,掌握工艺流程和反应原理是解题关键,题目难度中等.1年前查看全部
- (2011•崇安区二模)侯德榜先生是我国制碱工业的先驱和奠基人.他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的
(2011•崇安区二模)侯德榜先生是我国制碱工业的先驱和奠基人.他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的同时还获得了大量化肥.其主要过程如图所示:
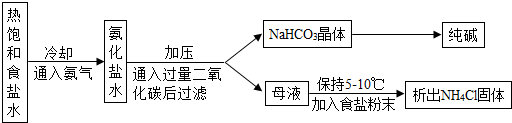
整个过程中涉及的主要反应有:
NH3+H2O+CO2═NH4HCO3
NH4HCO3+NaCl═NaHCO3+NH4Cl(晶体)
2NaHCO3
Na2CO3+H2O+CO2↑△ .
(1)“侯氏制碱法”生产的最终产品中可做化肥的是NH4ClNH4Cl.该化肥能否与熟石灰混合使用?不能不能(填:“能”或“不能”);若不能,为什么?(用化学方程式表示)2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O(若能则此问不做).
(2)实验室中,纯碱也可以和熟石灰用来制取少量的烧碱,用化学方程式表示其过程:Na2CO3+Ca(OH)2═2NaOH+CaCO3↓Na2CO3+Ca(OH)2═2NaOH+CaCO3↓.
(3)根据题目提供的信息,有的原材料可以循环使用,它们是H2O和CO2H2O和CO2.
(4)碳酸钠和碳酸氢钠都是白色固体,从题目信息中可以找到一种鉴别它们的方法:取样,分别加热,若受热能分解(有气泡)为碳酸氢钠,若受热不能分解(无气泡)则为碳酸钠(合题意即可)取样,分别加热,若受热能分解(有气泡)为碳酸氢钠,若受热不能分解(无气泡)则为碳酸钠(合题意即可)_.
(5)工业上制作印制板是利用氯化铁腐蚀Cu的原理:化学反应方程式为2FeCl3+Cu═2FeCl2+CuCl2.工业生产过程中产生的废液对环境有污染,为了节约金属资源并减少对环境的污染,请你设计一个实验流程处理废液回收Cu和FeCl2.
要求:参照上图的流程方式,将设计的实验流程在方框内完成.
查阅资料:Fe+2FeCl3═3FeCl2.
 66度34分1年前1
66度34分1年前1 -
 阿弥陀佛54786 共回答了14个问题
阿弥陀佛54786 共回答了14个问题 |采纳率71.4%(1)“侯氏制碱法”生产的最终产品中氯化铵含有氮元素,可做化肥;氯化铵属于铵态氮肥,与熟石灰反应会产生氨气,降低肥效,故不能与熟石灰混合使用;
(2)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠.
(3)由整个过程中涉及的主要反应可以看出,H2O和CO2可以循环使用;
(4)碳酸钠和碳酸氢钠都是白色固体,从题目信息中2NaHCO3
△
.
Na2CO3+H2O+CO2,故可采用加热观察能否产生气泡的方法进行鉴别;
(5)由题目所给信息,根据金属活动性顺序,过量铁粉与氯化铁,氯化铜发生化学反应;由于过量铁粉参加反应,所以滤渣的成份有多余的铁和化学反应生成的铜;故应加入稀盐酸除去滤渣中的铁;该流程中可以循环、回收利用的物质,了解金属的回收利用.仿照体例设计即可.
故答案为:(1)NH4Cl;不能;2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
(2)Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
(3)H2O和CO2
(4)取样,分别加热,若受热能分解(有气泡)为碳酸氢钠,若受热不能分解(无气泡)则为碳酸钠 (合题意即可)
(5)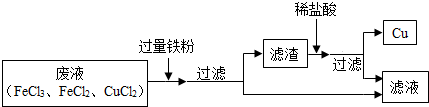 1年前查看全部
1年前查看全部
- (2011•浦东新区一模)(1)Solvay制碱(氨碱)法和侯德榜(联合)制碱法的基本原理均可用反应方程式表示为:
(2011•浦东新区一模)(1)Solvay制碱(氨碱)法和侯德榜(联合)制碱法的基本原理均可用反应方程式表示为:
NaCl+______→NaHCO3↓+______
将NaHCO3沉淀滤出后,母液中残留的离子主要有Cl-、NH4+和______、______.该母液的酸碱性为______(选择填充).
a.强酸性b.强碱性c.接近中性
Solvay对母液的基本处理是:加入______.Solvay法中______是循环使用的.侯德榜对母液的基本处理是:加入______和______,得到重要的副产品______.侯德榜法中______是部分循环使用的.
如果从海水中提取的食盐未经精制(提纯),所得纯碱中含有的难溶性杂质将主要是______和______(用化学式表示).
(2)工业上需要对溶液进行碱化时,常用氨水替代NaOH.好处何在,请说出你对此的看法.
a.______. b.______. susanna7201年前1
susanna7201年前1 -
 zjgdaizi_88 共回答了15个问题
zjgdaizi_88 共回答了15个问题 |采纳率80%解题思路:(1)制碱(氨碱)法的基本原理是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,加热碳酸氢钠即可制备碳酸钠;侯德榜(联合)制碱法第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品;根据盐类的水解来分析;
(2)根据氨碱法对母液的基本处理是含有氯化铵的滤液与石灰乳(生石灰与水反应)混合加热,所放出的氨气可回收循环使用:CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O;同时碳酸氢钠分解放出的二氧化碳气体可回收循环使用;
根据侯德榜对母液的从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用.
根据镁离子用氢氧根离子沉淀,钙离子用碳酸根离子沉淀;
(3)氨水的成本较低,可同时制得氮肥;弱碱容易控制碱度;(1)制碱(氨碱)法的基本原理是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,加热碳酸氢钠即可制备碳酸钠;侯德榜(联合)制碱法第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品,方程式为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3
△
.
Na2CO3+CO2↑+H2O; 将NaHCO3沉淀滤出后,母液中残留物为NaHCO3和NH4Cl,含有的离子为:Cl-、NH4+、Na+、HCO3-,NaHCO3溶液水解呈弱碱性,NH4Cl溶液水解呈弱酸性,最终溶液接近中性,故答案为:H2O+NH3+CO2;NH4Cl;Na+;HCO3-;c;
氨碱法对母液的基本处理是含有氯化铵的滤液与石灰乳(生石灰与水反应)混合加热,所放出的氨气可回收循环使用:CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O;同时碳酸氢钠分解放出的二氧化碳气体可回收循环使用;故答案为:石灰;氨气、二氧化碳;
侯德榜对母液的从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用,故答案为:氨气;食盐;氯化铵;食盐和二氧化碳;
从海水中提取的食盐未经精制(提纯),镁离子用氢氧根离子沉淀,钙离子用碳酸根离子沉淀,所得纯碱中含有的难溶性杂质将主要是:Mg(OH)2和CaCO3,故答案为:Mg(OH)2和CaCO3
(2)氨水的成本较低,可同时制得氮肥;弱碱容易控制碱度;故答案为:成本较低;可同时制得氮肥;容易控制碱度;点评:
本题考点: 纯碱工业(侯氏制碱法).
考点点评: 本题主要考查了氨碱法(索氏)和联合制碱法(侯氏)的原理,掌握原理是解题的关键,难度中等以上.1年前查看全部
- (2013•溧阳市模拟)根据侯德榜制碱法原理,实验室制备纯碱(Na2CO3)的主要步骤是::将配制好的饱和NaCl溶液倒
(2013•溧阳市模拟)根据侯德榜制碱法原理,实验室制备纯碱(Na2CO3)的主要步骤是::将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,经过处理后,转入蒸发皿中,灼烧2小时,得Na2CO3固体.
四种盐在不同温度下的溶解度(g)表
已知:
温度
溶解度
盐0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 100℃ NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 39.8 NH4HCO3 11.9 15.8 21.0 27.0 ① -- -- -- NaHCO3 6.9 8.1 9.6 11.1 12.7 14.5 16.4 -- NH4Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.3 77.3
1、①温度高于35℃NH4HCO3会分解.
2、碳酸氢钠受热分解:2NaHCO3
Na2CO3+H2O+CO2↑△ .
(1)饱和NaCl溶液中加入NH4HCO3固体,发生了复分解反应,生成NaHCO3晶体,写出其中发生反应的化学方程式______.
(2)加料完毕后,继续保温30分钟,目的是______,用蒸馏水洗涤NaHCO3晶体的目的是除去杂质,杂质中一定含有的物质是______(以化学式表示).
(3)过滤掉NaHCO3晶体后的滤液中还有一定量的NaHCO3溶解在水中,此时可向滤液中加入一定量的______,并作进一步处理,使NaCl溶液循环使用.
(4)某小苏打样品中混有少量碳酸钠,取药品2.0g加热到质量不再减少为止,共收集到二氧化碳气体0.22L(二氧化碳的密度为2.0g/L).向加热后的剩余固体中加入一定量质量分数为3.65%的稀盐酸,使其恰好完全反应,求消耗该稀盐酸的质量是多少克? 我等一个人1年前1
我等一个人1年前1 -
 wan10000 共回答了20个问题
wan10000 共回答了20个问题 |采纳率95%解题思路:(1)根据复分解反应的特征书写方程式;
(2)加料完毕后,继续保温一段时间为使反应充分进行,使反应完全;用蒸馏水洗涤NaHCO3晶体中杂质,此反应中杂质一定有反应生成的NH4Cl;
(3)过滤除去析出的碳酸氢钠后所得的母液主要成分为NaHCO3,加入盐酸后产生氯化钠,氯化钠可以重复使用;
(4)根据二氧化碳的体积计算二氧化碳的质量,然后根据化学方程式计算水的质量,固体的质量减去二氧化碳和水的质量就是碳酸钠的质量,然后依据反应的方程式计算盐酸的质量分数.(1)饱和NaCl溶液中加入NH4HCO3固体,发生了复分解反应,生成NaHCO3晶体和氯化铵,反应的方程式为:NaCl+NH4HCO3═NaHCO3+NH4Cl;
(2)加料完毕后,继续保温30分钟,可以使反应充分进行,使反应完全;用蒸馏水洗涤NaHCO3晶体中杂质,此反应中杂质一定有反应生成的NH4Cl;
(3)过滤除去析出的碳酸氢钠,所得的母液主要成分为NaHCO3,加入盐酸后,碳酸氢钠转化为氯化钠,并作进一步处理,使NaCl溶液循环使用;
(4)生成二氧化碳的质量=0.22L×2.0g/L=0.44g
设样品中小苏打分解生成水的质量为X
2NaHCO3
△
.
Na2CO3+H2O+CO2↑
1844
X0.44g
[18/44]=[X/0.44g] X=0.18g
剩余固体全部为碳酸钠,其质量为:2.0g-0.44g-0.18g=1.38g
设消耗盐酸的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
10673
1.38g3.65%×y
[106/73]=[1.38g/3.65%×y]y=26.4g
答:消耗该稀盐酸的质量是26.4g.
故答案为:(1)NaCl+NH4HCO3═NaHCO3+NH4Cl;
(2)使反应充分发生;NH4Cl;
(3)盐酸;
(4)生成二氧化碳的质量=0.22L×2.0g/L=0.44g
设样品中小苏打分解生成水的质量为X
2NaHCO3
△
.
Na2CO3+H2O+CO2↑
1844
X0.44g
[18/44]=[X/0.44g] X=0.18g
剩余固体全部为碳酸钠,其质量为:2.0g-0.44g-0.18g=1.38g
设消耗盐酸的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
10673
1.38g3.65%×y
[106/73]=[1.38g/3.65%×y]y=26.4g
答:消耗该稀盐酸的质量是26.4g.点评:
本题考点: 纯碱的制取;盐的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 本题考查学生根据侯氏制碱法的基本过程进行解题,学生能利用各种物质常见的溶解度结合相关物质的性质和物质的质量分数来计算是解题的关键,难度稍大.1年前查看全部
- 我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
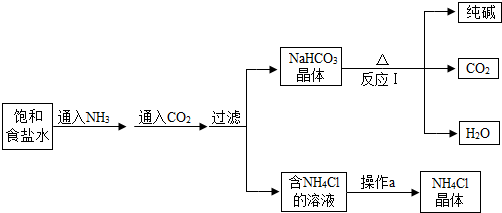
(1)NH3溶于水得到氨水,将无色酚酞溶液滴入氨水中,溶液呈______色.
(2)写出反应I的化学方程式2NaHCO3
Na2CO3+H2O+CO2↑△ .2NaHCO3;该反应的基本类型为______.
Na2CO3+H2O+CO2↑△ .
(3)操作a的过程是蒸发浓缩、______、过滤.
(4)上述工艺流程中可循环利用的物质是______. wuchao75391年前1
wuchao75391年前1 -
 wizardiecb 共回答了16个问题
wizardiecb 共回答了16个问题 |采纳率100%解题思路:(1)根据氨气的水溶液显碱性分析.
(2)根据反应写出反应的方程式,根据反应的特点分析反应的类型.
(3)根据从氯化铵的溶液中得到氯化铵的过程分析.
(4)观察分析工艺流程,找出可循环利用的物质.(1)NH3溶于水得到氨水,氨水显碱性,将无色酚酞溶液滴入氨水中,溶液呈红色.
(2)由工艺流程可知,碳酸氢钠受热分解生成了碳酸钠、二氧化碳和水,反应的方程式是:2NaHCO3
△
.
Na2CO3+H2O+CO2↑.该反应由一种物质生成了三种物质,属于分解反应.
(3)从氯化铵的溶液中得到氯化铵的过程是蒸发浓缩、结晶、过滤.
(4)由工艺流程中可知,向饱和的食盐水中通入了二氧化碳,在加热碳酸氢钠时又生成了二氧化碳,所以,可循环利用的物质是CO2.
故答为:(1)红;(2)2NaHCO3
△
.
Na2CO3+H2O+CO2↑,分解反应;(3)结晶;(4)CO2.点评:
本题考点: 纯碱的制取;酸碱指示剂及其性质;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 化学来源于生产、生活,又服务于生产、生活,本题很好的体现了这一理念;该题涉及化学方程式的书写,反应类型的判断等知识,要根据相关知识细心分析解答.1年前查看全部
- 我国著名的化工专家侯德榜在20世纪20年代所创立的“侯氏制碱法”誉满全球.“侯氏制碱法”中的碱是指下列的( ) A.N
我国著名的化工专家侯德榜在20世纪20年代所创立的“侯氏制碱法”誉满全球.“侯氏制碱法”中的碱是指下列的( ) A.NaOH B.K 2 CO 3 C.Na 2 CO 3 D.NaHCO 3  哎武邮人1年前1
哎武邮人1年前1 -
 apple522157 共回答了23个问题
apple522157 共回答了23个问题 |采纳率91.3%候氏制碱法是向氨化的饱和氯化钠溶液中通入二氧化碳析出晶体,得到晶体受热分解得到碳酸钠;所以“侯氏制碱法”中的碱实质是盐,该盐为碳酸钠(Na 2 CO 3 ),
故选C.1年前查看全部
- 侯德榜是如何制碱的
 xiaotong12191年前3
xiaotong12191年前3 -
 a138666486 共回答了24个问题
a138666486 共回答了24个问题 |采纳率91.7%化学原理
侯氏制碱法又名联合制碱法 (1)NH3+H2O+CO2=NH4HCO3
(2)NH4HCO3+NaCl=NH4Cl+NaHCO3↓
(3)2NaHCO3(加热)=Na2CO3+H2O+CO2↑ 即:①NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓ ②2NaHCO3=加热=Na2CO3+H2O+CO2↑
氨气与水和二氧化碳反应生成一分子的碳酸氢铵,这是第一步.第二步是:碳酸氢铵与氯化钠反应生成一分子的氯化铵和碳酸氢钠沉淀,碳酸氢钠之所以沉淀是因为它的溶解度较小. 根据 NH4Cl 在常温时的溶解度比 NaCl 大,而在低温下却比 NaCl 溶解度小的原理,在 278K ~ 283K(5 ℃~ 10 ℃ ) 时,向母液中加入食盐细粉,而使 NH4Cl 单独结晶析出供做氮肥.1年前查看全部
- 化学实验沉淀剂选择问题某同学在课余时间利用侯德榜制碱法的原理制得了一些纯碱,经检验,样品中含有少量 NaCl.现欲用实验
化学实验沉淀剂选择问题
某同学在课余时间利用侯德榜制碱法的原理制得了一些纯碱,经检验,样品中含有少量 NaCl.现欲用实验测定样品的纯度,该同学设计了多种方法:
方法二:重量法测定样品中CO32-的质量分数:将CO32-沉淀后称量沉淀质量.
方法二中最好选用——————(填“BaCl2” 或“CaCl2”)做沉淀剂. pppp0011年前1
pppp0011年前1 -
 雅舍狂欢 共回答了19个问题
雅舍狂欢 共回答了19个问题 |采纳率94.7%Bacl2,因为用等量的CO3 2-可产生更重的沉淀,减少误差.1年前查看全部
- 我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH 3 +H 2 O+CO 2 +NaCl=NH
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH 3 +H 2 O+CO 2 +NaCl=NH 4 Cl+NaHCO 3 (析出),促进了世界制碱技术的发展.下列说法正确的是
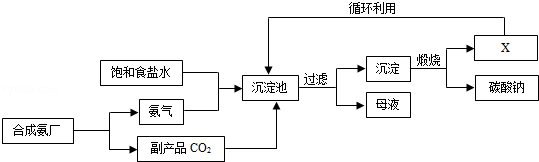
A.沉淀池中的反应物共含有六种元素 B.过滤得到的“母液”中一定只含有两种溶质 C.图中X可能是氨气 D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀  p_ccz1年前1
p_ccz1年前1 -
 伤爱2007 共回答了14个问题
伤爱2007 共回答了14个问题 |采纳率78.6%AD
1年前查看全部
- (2014•槐荫区三模)我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制取纯碱(Na2CO3)
 (2014•槐荫区三模)我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制取纯碱(Na2CO3).其反应原理及部分物质的溶解度曲线如下:
(2014•槐荫区三模)我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制取纯碱(Na2CO3).其反应原理及部分物质的溶解度曲线如下:
①NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
②2NaHCO3
Na2CO3+H2O+CO2↑△ .
试回答下列问题:
(1)60℃时,27.6g NH4Cl完全溶解至少需要______ g水.
(2)上述第②步反应是侯氏制碱法制纯碱的重要反应.
下列叙述中,正确的是______.
A.析出晶体后剩余的溶液中只含有一种溶质
B.饱和氨盐水比食盐水更容易吸收二氧化碳
C.析出晶体后的溶液为NaHCO3的饱和溶液
D.同温度下NaHCO3的溶解度比NH4Cl的大
(3)从图中可以看出温度高于60℃,NaHCO3的溶解度曲线“消失”了,原因是______.
(4)结合上述化学反应方程式和物质溶解度曲线回答,在氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵中,先结晶析出的物质是______(填物质名称),请简述原因______. jingweiyang1年前1
jingweiyang1年前1 -
 artang 共回答了21个问题
artang 共回答了21个问题 |采纳率95.2%解题思路:(1)根据溶解度概念分析;
(2)根据侯氏制碱法制纯碱的流程分析;
(3)根据信息将碳酸氢钠稍加热即分解得到纯碱分析;
(4)根据该温度下碳酸氢钠的溶解度比氯化铵小进行解答.(1)60℃时,NH4Cl的溶解度为55.2g,也就是100g水中最多55.2gNH4Cl达到饱和,所以27.6g NH4Cl完全溶解至少需要50g水;
(2)A、析出碳酸氢钠晶体后剩余的溶液中只含有氯化铵和碳酸氢钠,并且是碳酸氢钠的饱和溶液,故错误;
B、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故正确;
C、析出碳酸氢钠晶体后剩余的溶液是碳酸氢钠的饱和溶液,故正确;
D、NaHCO3的溶解度比NH4Cl小,NaHCO3会在沉淀池中沉淀出来,故错误;
(3)因为将碳酸氢钠稍加热即分解得到纯碱,因此碳酸氢钠溶解度曲线在大于60℃就“消失”了;
(4)工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是在该温度下碳酸氢钠的溶解度比氯化铵小.
故答案为:(1)50;(2)BC(3)碳酸氢钠加热易分解得到纯碱;(4)碳酸氢钠;在该温度下碳酸氢钠的溶解度比氯化铵小.点评:
本题考点: 纯碱的制取;固体溶解度曲线及其作用;晶体和结晶的概念与现象.
考点点评: 本题考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.1年前查看全部
- (2009•韶关一模)我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性
(2009•韶关一模)我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:

则下列叙述错误的是( )
A.A气体是NH3,B气体是CO2
B.把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉
C.纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 晓向1年前1
晓向1年前1 -
 一口气不平 共回答了16个问题
一口气不平 共回答了16个问题 |采纳率87.5%解题思路:A、依据侯德榜制碱的原理是,向氨化的饱和食盐水中通入二氧化碳气体析出碳酸氢钠,加热反应制备;
B、发酵粉是一种复合添加剂,主要用作面制品和膨化食品的生产.发酵粉中含有许多物质,主要成分为碳酸氢钠和酒石酸.通常是碳酸盐和固态酸的化合物;
C、依据纯碱的用途分析判断,碳酸钠是重要的化工原料之一,广泛应用于轻工日化、建材、化学工业、食品工业、冶金、纺织、石油、国防、医药等领域,用作制造其他化学品的原料、清洗剂、洗涤剂,也用于照相术和分析领域.是基本化工原料之一,用途广泛,是玻璃、肥皂、洗涤剂、纺织、制革、香料、染料、药品等的重要原料.
D、第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体.A、依据侯德榜制碱的原理是,向氨化的饱和食盐水中通入二氧化碳气体析出碳酸氢钠,加热反应制备;食盐A为氨气,B为二氧化碳,故A正确;
B、发酵粉是一种复合添加剂,主要用作面制品和膨化食品的生产.发酵粉中含有许多物质,主要成分为碳酸氢钠和酒石酸.通常是碳酸盐和固态酸的化合物;把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉,故B正确;
C、碳酸钠是重要的化工原料之一,用途广泛,是玻璃、肥皂、洗涤剂、纺织、制革、香料、染料、药品等的重要原料.故C正确;
D、第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体,故D错误;
故选D.点评:
本题考点: 纯碱工业(侯氏制碱法).
考点点评: 本题考查了侯德榜制碱的工作原理和流程分析,掌握工艺流程和反应原理是解题关键,题目难度中等.1年前查看全部
- (2013•泉州)我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等
(2013•泉州)我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要过量的原因:______;实验操作 实验现象 实验结论 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. 产生白色沉淀 反应的化学方程式:
______
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为______.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).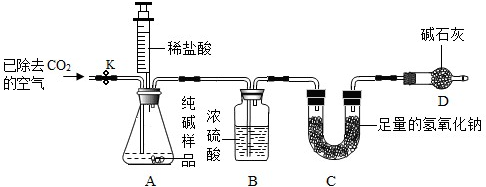
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的______,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为______.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据______ 定律,装置______(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果______(选填“偏大”或“偏小”). xxyy0231年前1
xxyy0231年前1 -
 美望树 共回答了17个问题
美望树 共回答了17个问题 |采纳率88.2%解题思路:(1)根据碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀和氯化钠进行解答;
(2)根据滴加的CaCl2溶液要过量的原因与碳酸钠充分反应进行解答;
(3)根据不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加进行解答;
(4)根据空气中含有二氧化碳进行解答;
(5)根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳进行解答;
(6)根据质量守恒定律可知装置C中反应前后的质量差就是产生CO2的质量进行解答.(1)碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl;故填:Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)滴加的CaCl2溶液要过量的原因与碳酸钠充分反应;故填:与碳酸钠充分反应;
(3)不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大从而导致样品中Na2CO3的质量分数偏大;故填:不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大;
(4)空气中含有二氧化碳,所以打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D;故填:二氧化碳;
(5)盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑;故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(6)由质量守恒定律可知装置C中反应前后的质量差就是产生CO2的质量,装置D的作用是防止空气中的二氧化碳和水蒸气进入装置C,所以若没有装置D,将会使测定结果偏大.故填:质量守恒;C;偏大.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;盐的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题将计算和实验有机地结合起来进行考查,通过认真审题,结合题干中已给出一系列的提示,根据提出的问题,发现有用的信息,充分发挥联想,与已有的知识建立联系,然后进行类比推导,从而达到解决问题的目的.1年前查看全部
- (2014•青岛二模)我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+Na
(2014•青岛二模)我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展.下列说法正确的是( )

A.沉淀池中得到的沉淀是NaHCO3,因为该条件下NaHCO3的溶解度比NH4Cl小
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 1jkhla1年前1
1jkhla1年前1 -
 泪多 共回答了17个问题
泪多 共回答了17个问题 |采纳率94.1%解题思路:A、根据NaHCO3的溶解度比NH4Cl小分析;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的反应物;
C、根据碳酸氢钠受热分解的生成物考虑;
D、根据氨气的水溶液显碱性考虑.A、在该温度下NaHCO3的溶解度比NH4Cl小,NaHCO3会在沉淀池中沉淀出来,故A正确;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故B错;
C、碳酸氢钠分解生成碳酸钠、水、二氧化碳,所以X是二氧化碳,故C错;
D、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故D正确.
答案:AD.点评:
本题考点: 纯碱的制取.
考点点评: 解答本题关键是要知道沉淀池中发生的反应,熟悉碳酸氢钠受热分解的产物,知道考虑反应后溶液中溶质时,还需要考虑反应物是否过量问题.1年前查看全部
- 我国科学家侯德榜创造了一种著名的纯碱生产方法-“联合制碱法”.请你回答:
 我国科学家侯德榜创造了一种著名的纯碱生产方法-“联合制碱法”.请你回答:
我国科学家侯德榜创造了一种著名的纯碱生产方法-“联合制碱法”.请你回答:
(1)纯碱(Na2CO3)属于______类物质(填“酸”、“碱”或“盐”).向纯碱的水溶液中滴入酚酞试液,试液变红色,则其pH______7(填“=”、“<”或“>”).
(2)“联合制碱法”生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O=NH4HCO3
②NH4HCO3+NaCl=NaHCO3↓+NH4Cl
③2NaHCO3
Na2CO3+H2O+CO2↑△ .
该过程中没有涉及到的基本反应类型是(______)
A.化合反应B.分解反应C.置换反应D.复分解反应
(3)第②步中加入的是磨细食盐粉.食盐磨细的目的是:______
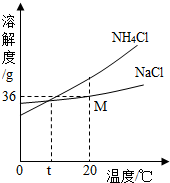
(4)从图中溶解度曲线中,你能获得的信息有:(写出2条)
______
(5)将第②步所得滤液(NH4Cl与剩余NaCl的混合溶液)
降温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中.
结合上图,你认为可能原因是:______.
所得NH4Cl属于化学肥料中的______肥,其中氮元素的质量分数为______.(精确到0.1%) leehom131年前1
leehom131年前1 -
 雨打芭蕉1976 共回答了13个问题
雨打芭蕉1976 共回答了13个问题 |采纳率100%解题思路:(1)根据碳酸钠的组成和结构判断物质种类;根据碳酸钠溶液呈碱性判断其pH大小.
(2)根据四种基本反应类型的定义和特点回答.
(3)根据磨细食盐粉的表面积增大分析回答.
(4)根据溶解度曲线的含义和信息回答.
(5)根据氯化钠和氯化铵的溶解度受温度影响的情况回答前一空;根据氯化铵的组成回答第二空;根据氯化铵的化学式和元素质量分数的公式计算后一空.(1)碳酸钠是由钠离子和碳酸根离子构成的,属于盐类,其水溶液呈碱性,溶液的pH大于7.
(2)①NH3+CO2+H2O=NH4HCO3的特点是“多变一”,符合化合反应的定义和特点,为化合反应,
②NH4HCO3+NaCl=NaHCO3↓+NH4Cl的特点是“两交换,价不变”,符合复分解反应的定义和特点,为复分解反应,③2NaHCO3
△
.
Na2CO3+H2O+CO2↑的特点是“一变多”,符合分解反应的定义和特点,为分解反应,缺少的基本反应类型是置换反应.
(3)磨细食盐粉的表面积增大,加快食盐溶解,增大食盐和碳酸氢铵的接触面积,进而加快反应速率.
(4)由图示的溶解度曲线可得多种信息,如:NH4Cl溶解度随温度升高而明显增大,或NaCl溶解度受温度影响不大,或t℃时,NH4Cl和NaCl的溶解度相同,或20℃时,NaCl的溶解度为36g等.
(5)NH4Cl溶解度受温度影响较大,且随温度降低而明显减小,而NaCl溶解度受温度影响不大,所以降温后NH4Cl晶体大量析出,而NaCl却仍留在了溶液中;氯化铵中含有氮元素,为氮肥;氯化铵的化学式为NH4Cl,其中氮元素的质量分数为[14/14+1×4+35.5]×100%=26.2%.
故答案为:
(1)盐;>;
(2)C;
(3)增大食盐和水的接触面积,加快食盐溶解,进而加快反应速率;
(4)NH4Cl溶解度随温度升高而NaCl溶解度受温度影响不大.(或t℃时,NH4Cl和NaCl的溶解度相同;20℃时,NaCl的溶解度为36g.);
(5)NH4Cl溶解度受温度影响较大,而NaCl溶解度受温度影响不大;氮;26.2%.点评:
本题考点: 纯碱的制取;影响溶解快慢的因素;固体溶解度的影响因素;固体溶解度曲线及其作用;溶液的酸碱性与pH值的关系;常见化肥的种类和作用;常见的氧化物、酸、碱和盐的判别;元素的质量分数计算;反应类型的判定.
考点点评: 学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系等重点内容.1年前查看全部
- 我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )

A.沉淀池中的反应物共含有七种元素
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 ceci81381年前1
ceci81381年前1 -
 teiww 共回答了10个问题
teiww 共回答了10个问题 |采纳率90%解题思路:A、根据沉淀池中发生的反应是氯化钠、氨气、二氧化碳和水,再分析元素种类即可;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的反应物;
C、根据碳酸氢钠受热分解的生成物考虑;
D、根据氨气的水溶液显碱性考虑.A、沉淀池中发生的反应的反应物是氯化钠、氨气、二氧化碳和水,所以含有钠、氯、氮、氢、碳、氧六种元素,故A错误;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故B错误;
C、碳酸氢钠分解生成碳酸钠、水、二氧化碳,所以X是二氧化碳,故C错误;
D、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故D正确.
故选D.点评:
本题考点: 纯碱的制取.
考点点评: 解答本题关键是要知道沉淀池中发生的反应,熟悉碳酸氢钠受热分解的产物,知道考虑反应后溶液中溶质时,还需要考虑反应物是否过量问题.1年前查看全部
- (2002•昆明)某化工厂运用我国著名化学家侯德榜先生的“侯氏制碱法”制得的纯碱(Na2CO3)中含有少量氯化钠.现取某
(2002•昆明)某化工厂运用我国著名化学家侯德榜先生的“侯氏制碱法”制得的纯碱(Na2CO3)中含有少量氯化钠.现取某种仅含有氯化钠杂质的纯碱样品11.1g,全部溶解在120g水中,再加入氯化钡溶液144g,恰好完全反应并生成碳酸钡沉淀:
Na2CO3+BaCl2═BaCO3↓+2NaCl过滤干燥后,称得沉淀质量为19.7g.求:
(1)纯碱样品中Na2CO3的质量.
(2)滤液中溶质的质量分数(计算结果精确到0.1). xdcity1年前1
xdcity1年前1 -
 一只浅水鱼 共回答了20个问题
一只浅水鱼 共回答了20个问题 |采纳率90%解题思路:(1)根据碳酸钠和氯化钡反应的化学方程式,得出各物质之间的质量比,列出比例式,可以计算出纯碱样品中Na2CO3的质量;
(2)根据碳酸钠和氯化钡反应的化学方程式,可以计算出反应后生成NaCl的质量.由此可以计算出反应后溶质的质量=纯碱样品中含氯化钠的质量+反应后生成NaCl的质量;反应后溶液质量=参与反应的物质质量-生成沉淀的质量.然后根据溶质质量分数公式计算即可.(1)设纯碱样品中Na2CO3的质量为x,反应后生成NaCl的质量为y,
Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197 117
x 19.7g y
∴[106/x=
197
19.7g],[197/19.7g=
117
y],
解之得:x=10.6g,y=11.7g,
(2)反应后溶液的质量为:120g+11.1g+144g-19.7g=255.4g,
溶质的质量为:11.1g-10.6g+11.7g=12.2g,
滤液中溶质的质量分数为 [12.2g/255.4g]×100%=4.78%.
答:(1)纯碱样品中Na2CO3的质量为10.6g;
(2)滤液中溶质的质量分数为4.78%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.1年前查看全部
- (2014•毕节市)我国著名的化学家侯德榜发明的“侯氏制碱法”,是向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可
(2014•毕节市)我国著名的化学家侯德榜发明的“侯氏制碱法”,是向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出NaHCO3固体,将其加热得到纯碱.反应的化学方程式为:NaCl+H2O+CO2+NH3═NaHCO3↓+NH4Cl
2NaHCO3
Na2CO3+CO2↑+H2O△ .
由上述信息可知,NaHCO3常温下溶解度较______,受热易______,若Na2CO3中混有NaHCO3杂质,可用______方法将杂质除去. llnec1年前1
llnec1年前1 -
 busuzhike 共回答了21个问题
busuzhike 共回答了21个问题 |采纳率85.7%解题思路:向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出NaHCO3固体,说明NaHCO3常温下的溶解度减小;
碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
碳酸钠的热稳定性强,受热不容易分解.因为向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出NaHCO3固体,说明NaHCO3常温下的溶解度减小;
碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,说明碳酸氢钠受热易分解;
若Na2CO3中混有NaHCO3杂质,可用加热方法将杂质除去.
故填:小;分解;加热.点评:
本题考点: 纯碱的制取;盐的化学性质.
考点点评: 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.1年前查看全部
- (2008•张家界)侯德榜先生潜必研究制碱技术,成功地发明了联合制碱法.其中关键一步的反应原理可表示为:NH3+CO2+
(2008•张家界)侯德榜先生潜必研究制碱技术,成功地发明了联合制碱法.其中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl═NaHCO3+X,则X的化学式为( )
A.NH3
B.NH3C1
C.NH4C1
D.NH5C1 hailuosun1年前1
hailuosun1年前1 -
 li598333861 共回答了22个问题
li598333861 共回答了22个问题 |采纳率81.8%解题思路:根据反应前后原子种类、数目不变,利用反应的化学方程式,判断生成物X的分子构成,确定物质X的化学式.反应的化学方程式NH3+CO2+H2O+NaCl═NaHCO3+X,可知可知反应前各原子个数为:
反应前 反应后
Na原子 1 1
Cl原子 1 0
N原子 1 0
H原子 5 1
C原子 1 1
O原子 3 3
根据反应前后原子种类、数目不变,可判断生成物X的一个分子由4个H原子、1个N原子、1个Cl原子构成,4个H原子与1个N原子可形成NH4+,因此可确定物质X的化学式可表示为NH4Cl.
故选C.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.1年前查看全部
- (2013•上海)与索尔维制碱法相比,侯德榜制碱法最突出的优点是( )
(2013•上海)与索尔维制碱法相比,侯德榜制碱法最突出的优点是( )
A.原料利用率高
B.设备少
C.循环利用的物质多
D.原料易得 yx1053281年前1
yx1053281年前1 -
 摇摇的橘子 共回答了22个问题
摇摇的橘子 共回答了22个问题 |采纳率95.5%索尔维法缺点:大量CaCl2用途不大,NaCl利用率只有70%,约有30%的NaCl留在母液中,侯氏制碱法的优点:把合成氨和纯碱两种产品联合生产,提高了食盐利用率,缩短了生产流程,减少了对环境的污染,降低了纯碱的成本.保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高到96%,
故选A.1年前查看全部
- 侯德榜制碱法为什么要通过量的氨气
 逸飞逸1年前1
逸飞逸1年前1 -
 花卷101 共回答了19个问题
花卷101 共回答了19个问题 |采纳率89.5%为了得到饱和的碳酸氢铵溶液;
然后加入氯化钠,根据碳酸氢钠溶解度小于碳酸氢铵而得到小苏打
小苏打分解得到碳酸钠1年前查看全部
- 我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( ) 
A.沉淀池中的反应物共含有六种元素 B.过滤得到的“母液”中一定只含有两种溶质 C.图中X可能是氨气 D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀  qtxsgong1年前1
qtxsgong1年前1 -
 heiheitiankong 共回答了24个问题
heiheitiankong 共回答了24个问题 |采纳率91.7%A、沉淀池中发生的反应的反应物是氯化钠、氨气、二氧化碳和水,所以含有钠、氯、氮、氢、碳、氧六种元素,故A正确;
B、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故B错;
C、碳酸氢钠分解生成碳酸钠、水、二氧化碳,所以X是二氧化碳,故C错;
D、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故D正确.
故选AD.1年前查看全部
- 道尔顿、卢瑟福、波尔、居里夫人、门捷列夫、凯库勒、侯德榜这些化学家的主要贡献
 scandy51611年前1
scandy51611年前1 -
 aloneship 共回答了17个问题
aloneship 共回答了17个问题 |采纳率88.2%1.道尔顿发现原子
2.卢瑟福提出带核的原子模型,并用α散射实验证明
3.波尔发现原子核外电子有规律运动
4.居里夫人发现镭
5.门捷列夫发现元素周期律,并制元素周期表
6.凯库勒总结出苯环的结构(单双键交替)【其实是错的】
7.侯德榜发明侯氏制碱法
以上皆为中学课本所学,当然还有很多贡献.既然是主要贡献,就点到为止,更不可能与百度百科相比.1年前查看全部
- 侯德榜制的碱是什么?氢氧化钠?碳酸氢钠?碳酸钠?
侯德榜制的碱是什么?氢氧化钠?碳酸氢钠?碳酸钠?
为什么那么麻烦?写了三个方程式!怎么不直接用钠与碳酸置换? wzhps1年前1
wzhps1年前1 -
 chenxz305 共回答了15个问题
chenxz305 共回答了15个问题 |采纳率86.7%碳酸钠
钠与碳酸直接反映成本太高,LS已经写出了反映,利用NaHCO3溶解度较低,将析出的NaHCO3提炼,使得化学平衡的继续向正反应1年前查看全部
- 我国著名化学家侯德榜发明的联合制碱法中的碱是指?
 forestcheng1年前1
forestcheng1年前1 -
 shaoyu6666 共回答了17个问题
shaoyu6666 共回答了17个问题 |采纳率100%侯氏制碱法:向饱和食盐水里通入足量的CO2和氨气,析出NaHCO3晶体
NH3+CO2+H20+NaCl====NaHCO3↓+NH4Cl
再加热NaHCO3固体,制得纯碱 Na2CO3
2NaHCO3=====Na2CO3+CO2↑+H2O
所以碱是Na2co31年前查看全部
大家在问
- 1阅读回答问题Jane is eleven and follows her own ideas.When her pare
- 2这位青年不但热情善良,而且很进取创新.修改病句
- 3(2014•苏州一模)微量元素是指在人体内总量不到万分之一的20多种元素,这些元素对人体正常代谢和健康起着重要作用,下列
- 4【英语】当句子中动词为情态动词或be动词时能不能用do进行强调
- 5高中数学函数的性质那一章如何去归纳总结?
- 6一个长方形宽与长的比是2:3.如果这个长方形的宽是24厘米,长______厘米;如果长是12厘米,宽是______厘米.
- 7什么是老鼠过街人人喊打?
- 8什么的石洞,用什么合适的词语来形容
- 9寻找 作文
- 10一个空瓶子质量是200g,装满水称,瓶和水的总质量是700g.将瓶中的水倒出,先在空瓶内装入一些金属颗粒,称出瓶和金属的
- 11蚊子和狮子出自哪个成语摹仿课文《蚊子与狮子》,给本文加一个结尾,点明文章的寓意15.成语( ) 就出自本文,比喻的是(
- 12因特网的中文简写是什么?英文缩写是什么?那位大虾知道啊?别跟我说一个Internet就把我打发了!
- 13如图为某区域地质剖面示意图,读图完成3~4题.
- 14兰亭集序写了作者怎样的情感以及变化?
- 15某件商品售价为7.2元,利润为成本的20%,如果把利润提高到30%,那么需要提高售价多少元 方程解,