高中化学必修1第三章《金属及其化合物》中所有的化学方程式
 独忆绿草地2022-10-04 11:39:542条回答
独忆绿草地2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 云中漫步d 共回答了25个问题
云中漫步d 共回答了25个问题 |采纳率88%- (必修一)教材中出现的方程式(题号带下划线的教材上有离子反应方程式)
1、Fe(OH)3胶体的制备:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
2、碳还原氧化铜:2CuO+C 2Cu+CO2↑
3、常温下钠与氧气反应:4Na + O2 = 2Na2O (白色)
4、钠在空气中燃烧:2Na + O2 Na2O2 (淡黄色)
5、钠与水反应:2Na + 2H2O = 2NaOH + H2↑
6、过氧化钠与水反应:2Na2O2 + 2H2O = 4NaOH + O2↑
7、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O2
8、铁在氧气中燃烧:3Fe+2O2 Fe3O4
9、铁与水蒸气反应:3Fe + 4H2O(g) Fe3O4 + 4H2↑
10、Al与盐酸反应:2Al+6HCl===2AlCl3+3H2↑
11、Al与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O===2NaAlO2 + 3H2↑
12、Al2O3与盐酸反应:Al2O3 + 6HCl ===2AlCl3 + 3H2O
13、Al2O3与氢氧化钠溶液反应:Al2O3 + 2NaOH === 2NaAlO2 + H2O
14、Al(OH)3 与盐酸反应:Al(OH)3 + 3HCl ===AlCl3 + 3H2O
15、Al(OH)3 与氢氧化钠溶液反应:Al(OH)3 + NaOH === NaAlO2 + 2H2O
16、实验室制取氢氧化铝(铝盐溶液加氨水):Al2(SO4)3 + 6NH3•H2O = 2Al(OH)3↓ + 3(NH4)2SO4
17、氢氧化铝加热分2Al(OH)3 Al2O3 + 3H2O
18、氧化亚铁与盐酸反应:FeO+2HCl=FeCl2+H2O
19、氧化铁与盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O
20、氯化铁与氢氧化钠溶液反应:FeCl3 + 3NaOH = 3NaCl + Fe(OH)3↓(红褐色)
21、硫酸亚铁与氢氧化钠溶液反应:FeSO4 + 2NaOH = Na2SO4 + Fe(OH)2↓(白色)
22、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
23、氢氧化铁加热分2Fe(OH)3 3H2O↑+ Fe2O3 (红棕色粉末,俗称铁红)
24、FeCl3溶液与铁粉反应:2FeCl3 + Fe = 3FeCl2
25、氯化亚铁中通入氯气:2FeCl2 + Cl2 = 2FeCl3
26、FeCl3溶液与铜反应:2FeCl3 + Cu = 2FeCl2 +CuCl2
27、二氧化硅与氢氟酸反应:SiO2 + 4HF = SiF4 ↑+ 2H2O
28、二氧化硅与氧化钙高温反应:SiO2 + CaO CaSiO3
29、二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH = Na2SiO3 + H2O
30、硅酸钠与盐酸反应:Na2SiO3 + 2HCl = 2NaCl + H2SiO3↓
31、氯气的实验室制法:MnO2+4HCl(浓) MnCl2+Cl2↑+H2O
32、氯气与金属反应:2Fe + 3Cl2 2FeCl3 (棕色烟)Cu + Cl2 CuCl2 (棕黄色的烟)
2Na + Cl2 2NaCl (白烟)
33、氯气与非金属反应:H2+Cl2 2HCl (苍白色火焰,有白雾生成)
34、氯气与水反应:Cl2 + H2O = HCl + HClO
35、次氯酸光照分2HClO 2HCl + O2↑
36、氯气与氢氧化钠溶液反应:Cl2 + 2NaOH = NaCl + NaClO + H2O
37、氯气与消石灰反应制漂白粉:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
38、漂白粉长期置露在空气中:Ca(ClO)2 + H2O + CO2 = CaCO3↓ + 2HClO
39、硫的燃烧 S+O2 SO2
40、二氧化硫与水反应:SO2 + H2O H2SO3
41、二氧化硫与氧气反应:2SO2+O2 2SO3
42、三氧化硫与水反应:SO3 + H2O = H2SO4
43、SO3与碱性氧化物反应:SO3+CaO=CaSO4
44、三氧化硫与Ca(OH)2溶液反应:SO3 + Ca(OH)2 = CaSO4 +H2O
45、氮气与氧气在放电下反应:N2 + O2 2NO 46、一氧化氮与氧气反应:2NO + O2 = 2NO2
47、二氧化氮与水反应:3NO2 + H2O = 2HNO3 + NO
48、合成氨反应:N2+3H2 2NH3
49、氨气溶于水:NH3 + H2O =NH3•H2O 氨水受热分NH3•H2O NH3↑ + H2O
50、氨气与氯化氢反应:NH3 + HCl = NH4Cl 氯化铵受热分NH4Cl NH3↑ + HCl↑
51、碳酸氢氨受热分NH4HCO3 NH3↑ + H2O↑ + CO2↑
52、硝酸铵与氢氧化钠反应:NH4NO3 + NaOH NH3↑ + NaNO3 + H2O
53、氨的催化氧化:4NH3+5O2 4NO+6H2O
54、氨气的实验室制取法:2NH4Cl + Ca(OH)2 CaCl2 + 2H2O + 2NH3↑
55、硫酸铵与氢氧化钠反应:(NH4)2SO4 + 2NaOH 2NH3↑ + Na2SO4 + 2H2O
56、浓硫酸与铜反应:Cu + 2H2SO4(浓) CuSO4 + 2H2O + SO2↑
57、浓硫酸与木炭反应:C + 2H2SO4(浓) CO2 ↑+ 2SO2↑ + 2H2O
58、浓硝酸与铜反应:Cu + 4HNO3(浓) ===Cu(NO3)2 + 2H2O + 2NO2↑
59、稀硝酸与铜反应:3Cu + 8HNO3(稀)=== 3Cu(NO3)2 + 4H2O + 2NO↑ - 1年前
 mania2008 共回答了12个问题
mania2008 共回答了12个问题 |采纳率- 自己查书!!!
- 1年前
相关推荐
- 高中化学必修1重要化学方程式
 youwing1年前2
youwing1年前2 -
 蓝色的缘分 共回答了19个问题
蓝色的缘分 共回答了19个问题 |采纳率84.2%过氧化钠与CO2、H2O;
钠与水反应;
铝与氢氧化钠反应;
铝离子转化;
亚铁离子、铁离子转化;
二氧化硅与氢氧化钠、实验室制硅酸;
氯气与水、碱;
二氧化硫与氧气、碱、氯水等反应;
氮元素转化、制氨气、浓硫酸浓硝酸与金属非金属反应等.1年前查看全部
- 苏教版高中化学必修1,必修2,及选修的《化学反应原理》《有机化学基础》《实验化学》中所有的化学方程式
 taws021年前4
taws021年前4 -
 我爱布丁 共回答了16个问题
我爱布丁 共回答了16个问题 |采纳率100%高中化学方程式大全
2Mg+TiCl4(熔融)===Ti+2MgCl2
Mg+2RbCl===MgCl2+2Rb
2Mg+CO2===2MgO+C
2Mg+SiO2===2MgO+Si
Mg+H2S===MgS+H2
Mg+H2SO4===MgSO4+H2
2Al+3Cl2===2AlCl3
4Al+3O2===2Al2O3(钝化)
4Al(Hg)+3O2+2xH2O===2(Al2O3.xH2O)+4Hg
4Al+3MnO2===2Al2O3+3Mn
2Al+Cr2O3===Al2O3+2Cr
2Al+Fe2O3===Al2O3+2Fe
2Al+3FeO===Al2O3+3Fe
2Al+6HCl===2AlCl3+3H2
2Al+3H2SO4===Al2(SO4)3+3H2
2Al+6H2SO4(浓)===Al2(SO4)3+3SO2+6H2O
(Al,Fe在冷,浓的H2SO4,HNO3中钝化)
Al+4HNO(稀)===Al(NO3)3+NO+2H2O
2Al+2NaOH+2H2O===2NaAlO2+3H2
2Fe+3Br2===2FeBr3
Fe+I2===FeI2
Fe+S===FeS
3Fe+4H2O(g)===Fe3O4+4H2
Fe+2HCl===FeCl2+H2
Fe+CuCl2===FeCl2+Cu
Fe+SnCl4===FeCl2+SnCl2
(铁在酸性环境下,不能把四氯化锡完全
还原为单质锡 Fe+SnCl2==FeCl2+Sn)
三, 非金属氢化物(HF,HCl,H2O,H2S,NH3)
1,还原性:
4HCl(浓)+MnO2===MnCl2+Cl2+2H2O
4HCl(g)+O2===2Cl2+2H2O
16HCl+2KMnO4===2KCl+2MnCl2+5Cl2+8H2O
14HCl+K2Cr2O7===2KCl+2CrCl3+3Cl2+7H2O
2H2O+2F2===4HF+O2
2H2S+3O2(足量)===2SO2+2H2O
2H2S+O2(少量)===2S+2H2O
2H2S+SO2===3S+2H2O
H2S+H2SO4(浓)===S+SO2+2H2O
3H2S+2HNO(稀)===3S+2NO+4H2O
5H2S+2KMnO4+3H2SO4===2MnSO4+K2SO4+5S+8H2O
3H2S+K2Cr2O7+4H2SO4===Cr2(SO4)3+K2SO4+3S+7H2O
H2S+4Na2O2+2H2O===Na2SO4+6NaOH
2NH3+3CuO===3Cu+N2+3H2O
2NH3+3Cl2===N2+6HCl
8NH3+3Cl2===N2+6NH4Cl
4NH3+3O2(纯氧)===2N2+6H2O
4NH3+5O2===4NO+6H2O
4NH3+6NO===5N2+6HO(用氨清除NO)
NaH+H2O===NaOH+H2
4NaH+TiCl4===Ti+4NaCl+2H2
CaH2+2H2O===Ca(OH)2+2H2
2,酸性:
4HF+SiO2===SiF4+2H2O
(此反应广泛应用于测定矿样或钢样中SiO2的含量)
2HF+CaCl2===CaF2+2HCl
H2S+Fe===FeS+H2
H2S+CuCl2===CuS+2HCl
H2S+2AgNO3===Ag2S+2HNO3
H2S+HgCl2===HgS+2HCl
H2S+Pb(NO3)2===PbS+2HNO3
H2S+FeCl2===
2NH3+2Na==2NaNH2+H2
(NaNH2+H2O===NaOH+NH3)
3,碱性:
NH3+HCl===NH4Cl
NH3+HNO3===NH4NO3
2NH3+H2SO4===(NH4)2SO4
NH3+NaCl+H2O+CO2===NaHCO3+NH4Cl
(此反应用于工业制备小苏打,苏打)
4,不稳定性:
2HF===H2+F2
2HCl===H2+Cl2
2H2O===2H2+O2
2H2O2===2H2O+O2
H2S===H2+S
2NH3===N2+3H2
四,非金属氧化物
低价态的还原性:
2SO2+O2===2SO3
2SO2+O2+2H2O===2H2SO4
(这是SO2在大气中缓慢发生的环境化学反应)
SO2+Cl2+2H2O===H2SO4+2HCl
SO2+Br2+2H2O===H2SO4+2HBr
SO2+I2+2H2O===H2SO4+2HI
SO2+NO2===SO3+NO
2NO+O2===2NO2
NO+NO2+2NaOH===2NaNO2
(用于制硝酸工业中吸收尾气中的NO和NO2)
2CO+O2===2CO2
CO+CuO===Cu+CO2
3CO+Fe2O3===2Fe+3CO2
CO+H2O===CO2+H2
3 高中化学方程式大全
氧化性:
SO2+2H2S===3S+2H2O
SO3+2KI===K2SO3+I2
NO2+2KI+H2O===NO+I2+2KOH
(不能用淀粉KI溶液鉴别溴蒸气和NO2)
4NO2+H2S===4NO+SO3+H2O
2NO2+Cu===4CuO+N2
CO2+2Mg===2MgO+C
(CO2不能用于扑灭由Mg,Ca,Ba,Na,K等燃烧的火灾)
SiO2+2H2===Si+2H2O
SiO2+2Mg===2MgO+Si
3,与水的作用:
SO2+H2O===H2SO3
SO3+H2O===H2SO4
3NO2+H2O===2HNO3+NO
N2O5+H2O===2HNO3
P2O5+H2O===2HPO3
P2O5+3H2O===2H3PO4
(P2O5极易吸水,可作气体干燥剂
P2O5+3H2SO4(浓)===2H3PO4+3SO3)
CO2+H2O===H2CO3
4,与碱性物质的作用:
SO2+2NH3+H2O===(NH4)2SO3
SO2+(NH4)2SO3+H2O===2NH4HSO3
(这是硫酸厂回收SO2的反应.先用氨水吸收SO2,
再用H2SO4处理: 2NH4HSO3+H2SO4===(NH4)2SO4+2H2O+2SO2
生成的硫酸铵作化肥,SO2循环作原料气)
SO2+Ca(OH)2===CaSO3+H2O
(不能用澄清石灰水鉴别SO2和CO2.可用品红鉴别)
SO3+MgO===MgSO4
SO3+Ca(OH)2===CaSO4+H2O
CO2+2NaOH(过量)===Na2CO3+H2O
CO2(过量)+NaOH===NaHCO3
CO2+Ca(OH)2(过量)===CaCO3+H2O
2CO2(过量)+Ca(OH)2===Ca(HCO3)2
CO2+2NaAlO2+3H2O===2Al(OH)3+Na2CO3
CO2+C6H5ONa+H2O===C6H5OH+NaHCO3
SiO2+CaO===CaSiO3
SiO2+2NaOH===Na2SiO3+H2O
(常温下强碱缓慢腐蚀玻璃)
SiO2+Na2CO3===Na2SiO3+CO2
SiO2+CaCO3===CaSiO3+CO2
五,金属氧化物
1,低价态的还原性:
6FeO+O2===2Fe3O4
FeO+4HNO3===Fe(NO3)3+NO2+2H2O
2,氧化性:
Na2O2+2Na===2Na2O
(此反应用于制备Na2O)
MgO,Al2O3几乎没有氧化性,很难被还原为Mg,Al.
一般通过电解制Mg和Al.
Fe2O3+3H2===2Fe+3H2O (制还原铁粉)
Fe3O4+4H2===3Fe+4H2O
3,与水的作用:
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2
(此反应分两步:Na2O2+2H2O===2NaOH+H2O2 ;
2H2O2===2H2O+O2. H2O2的制备可利用类似的反应:
BaO2+H2SO4(稀)===BaSO4+H2O2)
MgO+H2O===Mg(OH)2 (缓慢反应)
4,与酸性物质的作用:
Na2O+SO3===Na2SO4
Na2O+CO2===Na2CO3
Na2O+2HCl===2NaCl+H2O
2Na2O2+2CO2===2Na2CO3+O2
Na2O2+H2SO4(冷,稀)===Na2SO4+H2O2
MgO+SO3===MgSO4
MgO+H2SO4===MgSO4+H2O
Al2O3+3H2SO4===Al2(SO4)3+3H2O
(Al2O3是两性氧化物:
Al2O3+2NaOH===2NaAlO2+H2O)
FeO+2HCl===FeCl2+3H2O
Fe2O3+6HCl===2FeCl3+3H2O
Fe2O3+3H2S(g)===Fe2S3+3H2O
Fe3O4+8HCl===FeCl2+2FeCl3+4H2O
六,含氧酸
1,氧化性:
4HClO3+3H2S===3H2SO4+4HCl
HClO3+HI===HIO3+HCl
3HClO+HI===HIO3+3HCl
HClO+H2SO3===H2SO4+HCl
HClO+H2O2===HCl+H2O+O2
(氧化性:HClO>HClO2>HClO3>HClO4,
但浓,热的HClO4氧化性很强)
2H2SO4(浓)+C===CO2+2SO2+2H2O
2H2SO4(浓)+S===3SO2+2H2O
H2SO4+Fe(Al) 室温下钝化
6H2SO4(浓)+2Fe===Fe2(SO4)3+3SO2+6H2O
2H2SO4(浓)+Cu===CuSO4+SO2+2H2O
H2SO4(浓)+2HBr===SO2+Br2+2H2O
H2SO4(浓)+2HI===SO2+I2+2H2O
H2SO4(稀)+Fe===FeSO4+H2
2H2SO3+2H2S===3S+2H2O
4HNO3(浓)+C===CO2+4NO2+2H2O
6HNO3(浓)+S===H2SO4+6NO2+2H2O
5HNO3(浓)+P===H3PO4+5NO2+H2O
6HNO3+Fe===Fe(NO3)3+3NO2+3H2O
4HNO3+Fe===Fe(NO3)3+NO+2H2O
30HNO3+8Fe===8Fe(NO3)3+3N2O+15H2O
36HNO3+10Fe===10Fe(NO3)3+3N2+18H2O
30HNO3+8Fe===8Fe(NO3)3+3NH4NO3+9H2O
2,还原性:
H2SO3+X2+H2O===H2SO4+2HX
(X表示Cl2,Br2,I2)
2H2SO3+O2===2H2SO4
H2SO3+H2O2===H2SO4+H2O
5H2SO3+2KMnO4===2MnSO4+K2SO4+2H2SO4+3H2O
H2SO3+2FeCl3+H2O===H2SO4+2FeCl2+2HCl
3,酸性:
H2SO4(浓) +CaF2===CaSO4+2HF
H2SO4(浓)+NaCl===NaHSO4+HCl
H2SO4(浓) +2NaCl===Na2SO4+2HCl
H2SO4(浓)+NaNO3===NaHSO4+HNO3
3H2SO4(浓)+Ca3(PO4)2===3CaSO4+2H3PO4
2H2SO4(浓)+Ca3(PO4)2===2CaSO4+Ca(H2PO4)2
3HNO3+Ag3PO4===H3PO4+3AgNO3
2HNO3+CaCO3===Ca(NO3)2+H2O+CO2
(用HNO3和浓H2SO4不能制备H2S,HI,HBr,(SO2)
等还原性气体)
4H3PO4+Ca3(PO4)2===3Ca(H2PO4)2(重钙)
H3PO4(浓)+NaBr===NaH2PO4+HBr
H3PO4(浓)+NaI===NaH2PO4+HI
4,不稳定性:
2HClO===2HCl+O2
4HNO3===4NO2+O2+2H2O
H2SO3===H2O+SO2
H2CO3===H2O+CO2
H4SiO4===H2SiO3+H2O
七,碱
低价态的还原性:
4Fe(OH)2+O2+2H2O===4Fe(OH)3
与酸性物质的作用:
2NaOH+SO2(少量)===Na2SO3+H2O
NaOH+SO2(足量)===NaHSO3
2NaOH+SiO2===NaSiO3+H2O
2NaOH+Al2O3===2NaAlO2+H2O
2NaOH+Cl2===NaCl+NaClO+H2O
NaOH+HCl===NaCl+H2O
NaOH+H2S(足量)===NaHS+H2O
2NaOH+H2S(少量)===Na2S+2H2O
3NaOH+AlCl3===Al(OH)3+3NaCl
NaOH+Al(OH)3===NaAlO2+2H2O
(AlCl3和Al(OH)3哪个酸性强?)
NaOH+NH4Cl===NaCl+NH3+H2O
Mg(OH)2+2NH4Cl===MgCl2+2NH3.H2O
Al(OH)3+NH4Cl 不溶解
3,不稳定性:
Mg(OH)2===MgO+H2O
2Al(OH)3===Al2O3+3H2O
2Fe(OH)3===Fe2O3+3H2O
Cu(OH)2===CuO+H2O
八,盐
1,氧化性:
2FeCl3+Fe===3FeCl2
2FeCl3+Cu===2FeCl2+CuCl2
(用于雕刻铜线路版)
2FeCl3+Zn===2FeCl2+ZnCl2
FeCl3+Ag===FeCl2+AgC
Fe2(SO4)3+2Ag===FeSO4+Ag2SO4(较难反应)
Fe(NO3)3+Ag 不反应
2FeCl3+H2S===2FeCl2+2HCl+S
2FeCl3+2KI===2FeCl2+2KCl+I2
FeCl2+Mg===Fe+MgCl2
2,还原性:
2FeCl2+Cl2===2FeCl3
3Na2S+8HNO3(稀)===6NaNO3+2NO+3S+4H2O
3Na2SO3+2HNO3(稀)===3Na2SO4+2NO+H2O
2Na2SO3+O2===2Na2SO4
3,与碱性物质的作用:
MgCl2+2NH3.H2O===Mg(OH)2+NH4Cl
AlCl3+3NH3.H2O===Al(OH)3+3NH4Cl
FeCl3+3NH3.H2O===Fe(OH)3+3NH4Cl
4,与酸性物质的作用:
Na3PO4+HCl===Na2HPO4+NaCl
Na2HPO4+HCl===NaH2PO4+NaCl
NaH2PO4+HCl===H3PO4+NaCl
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2
3Na2CO3+2AlCl3+3H2O===2Al(OH)3+3CO2+6NaCl
3Na2CO3+2FeCl3+3H2O===2Fe(OH)3+3CO2+6NaCl
3NaHCO3+AlCl3===Al(OH)3+3CO2
3NaHCO3+FeCl3===Fe(OH)3+3CO2
3Na2S+Al2(SO4)3+6H2O===2Al(OH)3+3H2S
3NaAlO2+AlCl3+6H2O===4Al(OH)3
5,不稳定性:
Na2S2O3+H2SO4===Na2SO4+S+SO2+H2O
NH4Cl===NH3+HCl
NH4HCO3===NH3+H2O+CO2
2KNO3===2KNO2+O2
2Cu(NO3)3===2CuO+4NO2+O2
2KMnO4===K2MnO4+MnO2+O2
2KClO3===2KCl+3O2
2NaHCO3===Na2CO3+H2O+CO2
Ca(HCO3)2===CaCO3+H2O+CO2
CaCO3===CaO+CO2
MgCO3===MgO+CO2
高中化学方程式总结
非金属单质(F2 ,Cl2 , O2 , S, N2 , P , C , Si)
1, 氧化性:
F2 + H2 === 2HF
F2 +Xe(过量)===XeF2
2F2(过量)+Xe===XeF4
nF2 +2M===2MFn (表示大部分金属)
2F2 +2H2O===4HF+O2
2F2 +2NaOH===2NaF+OF2 +H2O
F2 +2NaCl===2NaF+Cl2
F2 +2NaBr===2NaF+Br2
F2+2NaI ===2NaF+I2
F2 +Cl2 (等体积)===2ClF
3F2 (过量)+Cl2===2ClF3
7F2(过量)+I2 ===2IF7
Cl2 +H2 ===2HCl
3Cl2 +2P===2PCl3
Cl2 +PCl3 ===PCl5
Cl2 +2Na===2NaCl
3Cl2 +2Fe===2FeCl3
Cl2 +2FeCl2 ===2FeCl3
Cl2+Cu===CuCl2
2Cl2+2NaBr===2NaCl+Br2
Cl2 +2NaI ===2NaCl+I2
5Cl2+I2+6H2O===2HIO3+10HCl
Cl2 +Na2S===2NaCl+S
Cl2 +H2S===2HCl+S
Cl2+SO2 +2H2O===H2SO4 +2HCl
Cl2 +H2O2 ===2HCl+O2
2O2 +3Fe===Fe3O4
O2+K===KO2
S+H2===H2S
2S+C===CS2
S+Fe===FeS
S+2Cu===Cu2S
3S+2Al===Al2S3
甲烷燃烧
CH4+2O2→CO2+2H2O(条件为点燃)
甲烷隔绝空气高温分解
甲烷分解很复杂,以下是最终分解.CH4→C+2H2(条件为高温高压,催化剂)
甲烷和氯气发生取代反应
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl (条件都为光照. )
实验室制甲烷
CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)
乙烯燃烧
CH2=CH2+3O2→2CO2+2H2O(条件为点燃)
乙烯和溴水
CH2=CH2+Br2→CH2Br-CH2Br
乙烯和水
CH2=CH2+H20→CH3CH2OH (条件为催化剂)
乙烯和氯化氢
CH2=CH2+HCl→CH3-CH2Cl
乙烯和氢气
CH2=CH2+H2→CH3-CH3 (条件为催化剂)
乙烯聚合
nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)
氯乙烯聚合
nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)
实验室制乙烯
CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)
乙炔燃烧
C2H2+3O2→2CO2+H2O (条件为点燃)
乙炔和溴水
C2H2+2Br2→C2H2Br4
乙炔和氯化氢
两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2
乙炔和氢气
两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂)
实验室制乙炔
CaC2+2H2O→Ca(OH)2+C2H2↑
以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式.
CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2
CaC2+2H2O→C2H2+Ca(OH)2
C+H2O===CO+H2-----高温
C2H2+H2→C2H4 ----乙炔加成生成乙烯
C2H4可聚合
苯燃烧
2C6H6+15O2→12CO2+6H2O (条件为点燃)
苯和液溴的取代
C6H6+Br2→C6H5Br+HBr
苯和浓硫酸浓硝酸
C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)
苯和氢气
C6H6+3H2→C6H12 (条件为催化剂)
乙醇完全燃烧的方程式
C2H5OH+3O2→2CO2+3H2O (条件为点燃)
乙醇的催化氧化的方程式
2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)
乙醇发生消去反应的方程式
CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸 170摄氏度)
两分子乙醇发生分子间脱水
2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸 140摄氏度)
乙醇和乙酸发生酯化反应的方程式
CH3COOH+C2H5OH→CH3COOC2H5+H2O
乙酸和镁
Mg+2CH3COOH→(CH3COO)2Mg+H2
乙酸和氧化钙
2CH3COOH+CaO→(CH3CH2)2Ca+H2O
乙酸和氢氧化钠
CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH
乙酸和碳酸钠
Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑
甲醛和新制的氢氧化铜
HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O
乙醛和新制的氢氧化铜
CH3CHO+2Cu→Cu2O(沉淀)+CH3COOH+2H2O
乙醛氧化为乙酸
2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)
烯烃是指含有C=C键的碳氢化合物.属于不饱和烃.烯烃分子通式为CnH2n,非极性分子,不溶或微溶于水.容易发生加成、聚合、氧化反应等.
乙烯的物理性质
通常情况下,无色稍有气味的气体,密度略小比空气,难溶于水,易溶于四氯化碳等有机溶剂.
1) 氧化反应:
①常温下极易被氧化剂氧化.如将乙烯通入酸性KMnO4溶液,溶液的紫色褪去,由此可用鉴别乙烯.
②易燃烧,并放出热量,燃烧时火焰明亮,并产生黑烟.
2) 加成反应:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应.
3) 聚合反应:
2.乙烯的实验室制法
(1)反应原理:CH3CH2OH===CH2=CH2↑+H2O (条件为加热,浓H2SO4)
(2)发生装置:选用“液液加热制气体”的反应装置.
(3)收集方法:排水集气法.
(4)注意事项:
①反应液中乙醇与浓硫酸的体积比为1∶3.
②在圆底烧瓶中加少量碎瓷片,目的是防止反应混合物在受热时暴沸.
③温度计水银球应插在液面下,以准确测定反应液温度.加热时要使温度迅速提高到170℃,以减少乙醚生成的机会.
④在制取乙烯的反应中,浓硫酸不但是催化剂、吸水剂,也是氧化剂,在反应过程中易将乙醇氧化,最后生成CO2、CO、C等(因此试管中液体变黑),而硫酸本身被还原成SO2.SO2能使溴水或KMnO4溶液褪色.因此,在做乙烯的性质实验前,可以将气体通过NaOH溶液以洗涤除去SO2,得到较纯净的乙烯.
乙炔又称电石气.结构简式HC≡CH,是最简单的炔烃.化学式C2H2
分子结构:分子为直线形的非极性分子.
无色、无味、易燃的气体,微溶于水,易溶于乙醇、丙酮等有机溶剂.
化学性质很活泼,能起加成、氧化、聚合及金属取代等反应.
能使高锰酸钾溶液的紫色褪去.
乙炔的实验室制法:CaC2+2H2O→Ca(OH)2+C2H2↑
化学性质:
(1)氧化反应:
a.可燃性:2C2H2+5O2 → 4CO2+2H2O
现象:火焰明亮、带浓烟 .
b.被KMnO4氧化:能使紫色酸性高锰酸钾溶液褪色.
(2)加成反应:可以跟Br2、H2、HX等多种物质发生加成反应.
现象:溴水褪色或Br2的CCl4溶液褪色
与H2的加成
CH≡CH+H2 → CH2=CH2
与H2的加成
两步反应:C2H2+H2→C2H4
C2H2+2H2→C2H6 (条件为催化剂)
氯乙烯用于制聚氯乙烯
C2H2+HCl→C2H3Cl nCH2=CHCl→=-[-CH2-CHCl-]n- (条件为催化剂)
(3)由于乙炔与乙烯都是不饱和烃,所以化学性质基本相似.金属取代反应:将乙炔通入溶有金属钠的液氨里有氢气放出.乙炔与银氨溶液反应,产生白色乙炔银沉淀.
1、 卤化烃:官能团,卤原子
在碱的溶液中发生“水解反应”,生成醇
在碱的醇溶液中发生“消去反应”,得到不饱和烃
2、 醇:官能团,醇羟基
能与钠反应,产生氢气
能发生消去得到不饱和烃(与羟基相连的碳直接相连的碳原子上如果没有氢原子,不能发生消去)
能与羧酸发生酯化反应
能被催化氧化成醛(伯醇氧化成醛,仲醇氧化成酮,叔醇不能被催化氧化)
3、 醛:官能团,醛基
能与银氨溶液发生银镜反应
能与新制的氢氧化铜溶液反应生成红色沉淀
能被氧化成羧酸
能被加氢还原成醇
4、 酚,官能团,酚羟基
具有酸性
能钠反应得到氢气
酚羟基使苯环性质更活泼,苯环上易发生取代,酚羟基在苯环上是邻对位定位基
能与羧酸发生酯化
5、 羧酸,官能团,羧基
具有酸性(一般酸性强于碳酸)
能与钠反应得到氢气
不能被还原成醛(注意是“不能”)
能与醇发生酯化反应
6、 酯,官能团,酯基
能发生水解得到酸和醇
物质的制取:
实验室制甲烷
CH3COONa+NaOH→Na2CO3+CH4 (条件是CaO 加热)
实验室制乙烯
CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)
实验室制乙炔
CaC2+2H2O→Ca(OH)2+C2H2↑
工业制取乙醇:
C2H4+H20→CH3CH2OH (条件为催化剂)
乙醛的制取
乙炔水化法:C2H2+H2O→C2H4O(条件为催化剂,加热加压)
乙烯氧化法:2 CH2=CH2+O2→2CH3CHO(条件为催化剂,加热)
乙醇氧化法:2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂,加热)
乙酸的制取
乙醛氧化为乙酸 :2CH3CHO+O2→2CH3COOH(条件为催化剂和加温)
加聚反应:
乙烯聚合
nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)
氯乙烯聚合
nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)
氧化反应:
甲烷燃烧
CH4+2O2→CO2+2H2O(条件为点燃)
乙烯燃烧
CH2=CH2+3O2→2CO2+2H2O(条件为点燃)
乙炔燃烧
C2H2+3O2→2CO2+H2O (条件为点燃)
苯燃烧
2C6H6+15O2→12CO2+6H2O (条件为点燃)
乙醇完全燃烧的方程式
C2H5OH+3O2→2CO2+3H2O (条件为点燃)
乙醇的催化氧化的方程式
2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)
乙醛的催化氧化:
CH3CHO+O2→2CH3COOH (条件为催化剂加热)
取代反应:有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应.
甲烷和氯气发生取代反应
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
(条件都为光照.)
苯和浓硫酸浓硝酸
C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)
苯与苯的同系物与卤素单质、浓硝酸等的取代.如:
酚与浓溴水的取代.如:
烷烃与卤素单质在光照下的取代.如:
酯化反应.酸和醇在浓硫酸作用下生成酯和水的反应,其实质是羧基与羟基生成酯基和水的反应.如:
水解反应.水分子中的-OH或-H取代有机化合物中的原子或原子团的反应叫水解反应.
①卤代烃水解生成醇.如:
②酯水解生成羧酸(羧酸盐)和醇.如:
乙酸乙酯的水
CH3COOC2H5+H2O→CH3COOH+C2H5OH(条件为无机酸式碱)
加成反应.
不饱和的碳原子跟其他原子或原子团结合生成别的有机物的反应.
乙烯和溴水
CH2=CH2+Br2→CH2Br-CH2Br
乙烯和水
CH2=CH2+H20→CH3CH2OH (条件为催化剂)
乙烯和氯化氢
CH2=H2+HCl→CH3-CH2Cl
乙烯和氢气
CH2=CH2+H2→CH3-CH3 (条件为催化剂)
乙炔和溴水
C2H2+2Br2→C2H2Br4
乙炔和氯化氢
两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2
乙炔和氢气
两步反应:C2H2+H2→C2H4---------C2H2+2H2→C2H6 (条件为催化剂)
苯和氢气
C6H6+3H2→C6H12 (条件为催化剂)
消去反应.有机分子中脱去一个小分子(水、卤化氢等),而生成不饱和(含碳碳双键或碳碳三键)化合物的反应.
乙醇发生消去反应的方程式
CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸 170摄氏度)
两分子乙醇发生分子间脱水
2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸 140摄氏度)
不是很完全,但是基本可以完成1年前查看全部
- 高中化学必修1中的第一课的萃取剂都有那些?分别有什么性质?特点?CCL4是啥?还有碘?BR2?都是什么?
 yichu19991年前3
yichu19991年前3 -
 你是我vv 共回答了16个问题
你是我vv 共回答了16个问题 |采纳率81.3%两种液体互不相溶,需要萃取的物质在两液体中溶解度差别很大的时候可以进行萃取.如四氯化碳加入溴水,溴单质就会从水中溶解入四氯化碳. 选用的萃取剂的原则: ① 和原溶液中的溶剂互不相溶; ② 对溶质的溶解度要远大于原溶剂; ③ 易于挥发; ④ 萃取剂不能与原溶液的溶剂反应.
分液漏斗萃取
常见的萃取剂:苯,四氯化碳,酒精,煤油,直馏汽油,己烷,环己烷…….不要忘记,水是最廉价、最易得的萃取剂.1年前查看全部
- 高中化学必修1第二章第一节习题详细的答案
 sadtgwerhre1年前1
sadtgwerhre1年前1 -
 走过四季都是情 共回答了20个问题
走过四季都是情 共回答了20个问题 |采纳率80%选择题么?1.下列合组混合物中,能用分液漏斗进行分离的是(C) A酒精和水 B碘和四氯化碳 C水和四氯化碳 D汽油和植物油 2.在汽车加油站见到的油罐车上,所贴的危险化学品标志是(B)〔因为油是液体,易燃〕1年前查看全部
- 高中化学必修1知识点总结:第三章金属及其化合物,主要掌握哪几种金属的性质?
 pp2201年前3
pp2201年前3 -
 olivejiajia 共回答了15个问题
olivejiajia 共回答了15个问题 |采纳率93.3%复习提纲可以看这个.
主要是Na、Al、Fe、Cu的性质1年前查看全部
- 高中化学必修1基础题4
 cxvksadfopusadoi1年前1
cxvksadfopusadoi1年前1 -
 TMD小样 共回答了15个问题
TMD小样 共回答了15个问题 |采纳率86.7%8
NaOH=Na+ + OH-
CuCl2=Cu2+ + 2Cl-
Fe2(SO4)3=2Fe3+ +3(SO4)2-
Ba(NO3)2=Ba2+ + 2(NO3)-
9
(1)可以 Na2SO4+BaCl2=BaSO4+2NaCl
(SO4)2- +Ba2+=BaSO4
(2)可以 2Al+3Hg(NO3)2=3Hg+2Al(NO3)3
2Al+3Hg2+=3Hg+2Al3+
(3)可以 HCl+Na2CO3=NaHCO3+NaCl
2HCl+Na2CO3=H2O+CO2+NaCl
H+ +(CO3)2- =HCO3-
2H+ + (CO3)2- = CO2+H2O
(4)不可以 混合不生成气体,沉淀,难溶物或弱电解质
10
1 CuCl2+2NaOH=Cu(OH)2+2NaCl
2 HCl+NaOH=H2O+NaCl
3 2HCl+CaCO3=CaCl2+CO2+H2O
4 2HCl+Na2CO3=2NaCl+H2O+CO2
5 CuCl2+Fe=FeCl2+Cu
11
金属不是电解质
金属导电是靠金属内的自由电子
电解质导电是靠溶液中的正负离子
它们的导电介质不一样1年前查看全部
- 高中化学必修1《第四章非金属》所有的化学方程式
 雪中乐1年前1
雪中乐1年前1 -
 三创 共回答了20个问题
三创 共回答了20个问题 |采纳率75%9、氯气的性质
铜丝在氯气中剧烈燃烧(棕色烟)
Cu + Cl2 CuCl2
之后加水,可由绿色溶液(浓)得到蓝色溶液(稀)
Cl2 +2FeCl2 =2FeCl3
2Cl2+2NaBr=2NaCl+Br2
Cl2 +2NaI =2NaCl+I2
x09Cl2+SO2 +2H2O=H2SO4 +2HCl
2Na + Cl2 2NaCl
氢气在氯气中燃烧(苍白色火焰)
H2 + Cl2 2HCl
氟气与氢气反应(黑暗处即可爆炸)
H2+F2=2HF
12、氯气溶于水(新制氯水中含H+ 、Cl -、ClO -、OH-、Cl2、HClO、H2O)
Cl2 + H2O = HCl + HClO
Cl2 + H2O = H+ + Cl - + HClO
13、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)
2HClO 2HCl + O2↑
14、工业制漂白粉的原理及漂白粉的失效
2Ca(OH)2 + 2Cl2 =Ca(ClO)2 + CaCl2 + 2H2O
2Ca(OH)2 +2Cl2 =2Ca2++2ClO-+2Cl -+2H2O
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
2HClO 2HCl + O2↑
Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
15、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶)
MnO2 +4HCl(浓) MnCl2+Cl2↑+2H2O
MnO2 +4H++2Cl- Mn2++Cl2↑+2H2O
16、新制氯水注入盛溴化钠溶液的试管中
Cl2 + 2NaBr = Br2 + 2NaCl
Cl2 + 2Br- = Br2 + 2Cl-
二氧化硫制三氧化硫(无色固体,熔点16.8℃) 2SO2 + O2 2SO3
吸收塔中(98%的浓硫酸):SO3+H2O=H2SO4
20、铜与浓硫酸反应:
Cu+2H2SO4 (浓) CuSO4 +2H2O+SO2 ↑
21、碳与浓硫酸反应:
C+2H2SO4(浓) 2H2O+CO2↑+2SO2↑
22、工业制单质硅(碳在高温下还原二氧化硅) SiO2 + 2C Si + 2CO↑
23、二氧化硅与氢氧化钠反应
SiO2 + 2NaOH = Na2SiO3 + H2O
SiO2 + 2OH - = SiO32- + H2O
24、氮气和氢气反应(工业合成氨)
N2 + 3H2 2NH3
25、氮气和氧气放电下反应(雷雨发庄稼)
N2 + O2 2NO
2NO + O2 2NO2
二氧化氮溶于水
3NO2 + H2O 2HNO3 + NO
3NO2 + H2O 2H++ 2NO3-+NO
26、HNO3与Fe的反应
Al、Fe遇浓HNO3、浓硫酸钝化(常温)
Fe与浓HNO3加热
Fe+6HNO3 Fe(NO3)3+3NO2↑+3H2O
Fe与稀HNO3反应
Fe+4HNO3=Fe(NO3)3+NO↑+2H2O
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
27、NO2 、O2 的混合气通入水中无剩余气体 4NO2 + O2 + 2H2O = 4 HNO3
28、NO 、O2 的混合气通入水中无剩余气体 4NO + 3O2 + 2H2O = 4 HNO3
29、五氧化二磷与热水反应
P2O5 + 3H2O(热) = 2H3PO4
30.磷在氯气中燃烧 2P + 3Cl2 2PCl3
(白色烟雾) 2P + 5Cl2 2PCl5
31.氨的催化氧化
4NH3 +5O2 4NO + 6H2O
32.碳酸氢铵受热分解
NH4HCO3 NH3 ↑+ H2O↑ + CO2↑
33.用浓盐酸检验氨气(白烟生成)
HCl + NH3 = NH4Cl
34.硫酸铵溶液与氢氧化钠溶液混合加
(NH4)2SO4 +2NaOH 2NH3↑+Na2SO4 +2H2O
NH4+ + OH - NH3 ↑+ H2O
35.硝酸铵溶液与氢氧化钠溶液混合(不加热)
NH4NO3 + NaOH = NH3•H2O + NaNO3 NH4+ + OH- = NH3•H2O1年前查看全部
- 高中化学必修1课本34页答案
 直觉的三次方1年前2
直觉的三次方1年前2 -
 xx旅途谁明了 共回答了20个问题
xx旅途谁明了 共回答了20个问题 |采纳率95%1年前查看全部
- 高中化学必修1所有知识点.
 baobao爱你1年前3
baobao爱你1年前3 -
 哦最稀饭你 共回答了21个问题
哦最稀饭你 共回答了21个问题 |采纳率95.2%物质的量、氧化还原反应、金属及其氧化物、非金属及其氧化物
一、 研究物质性质的方法和程序 1.基本方法:观察法、实验法、分类法、比较法 2.基本程序:3.:用比较的方法对观察到的现象进行分析、综合、推论,概括出结论.
二、 钠及其化合物的性质:1.钠在空气中缓慢氧化:4Na+O2==2Na2O 2.钠在空气中燃烧:2Na+O2点燃====Na2O2 3.钠与水反应:2Na+2H2O=2NaOH+H2↑ 现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色.4.过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑ 5.过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O2 6.碳酸氢钠受热分解:2NaHCO3△==Na2CO3+H2O+CO2↑ 7.氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O 8.在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO3
三、 氯及其化合物的性质
1.氯气与氢氧化钠的反应:Cl2+2NaOH=NaCl+NaClO+H2O
2.铁丝在氯气中燃烧:2Fe+3Cl2点燃===2FeCl3
3.制取漂白粉(氯气能通入石灰浆)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
4.氯气与水的反应:Cl2+H2O=HClO+HCl
5.次氯酸钠在空气中变质:NaClO+CO2+H2O=NaHCO3+HClO
6.次氯酸钙在空气中变质:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
四、 以物质的量为中心的物理量关系 1.物质的量n(mol)= N/N(A)
2.物质的量n(mol)= m/M
3.标准状况下气体物质的量n(mol)= V/V(m)
4.溶液中溶质的物质的量n(mol)=cV
五、 氧化还原反应
1.氧降得还
2.还升失氧
3.氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物
六、 铁及其化合物性质
Fe2+及Fe3+离子的检验:① Fe2+的检验:(浅绿色溶液) a) 加氢氧化钠溶液,产生白色沉淀,继而变灰绿色,最后变红褐色.b) 加KSCN溶液,不显红色,再滴加氯水,溶液显红色.② Fe3+的检验:(黄色溶液) a) 加氢氧化钠溶液,产生红褐色沉淀.b) 加KSCN溶液,溶液显红色.主要反应的化学方程式:① 铁与盐酸的反应:Fe+2HCl=FeCl2+H2↑ ② 铁与硫酸铜反应(湿法炼铜):Fe+CuSO4=FeSO4+Cu ③ 在氯化亚铁溶液中滴加氯水:(除去氯化铁中的氯化亚铁杂质)3FeCl2+Cl2=2FeCl3 ④ 氢氧化亚铁在空气中变质:4Fe(OH)2+O2+2H2O=4Fe(OH)3 ⑤ 在氯化铁溶液中加入铁粉:2FeCl3+Fe=3FeCl2
七、 氮及其化合物的性质 1.“雷雨发庄稼”涉及反应原理:① N2+O2放电===2NO ② 2NO+O2=2NO2 ③ 3NO2+H2O=2HNO3+NO 2.氨的工业制法:N2+3H2 2NH3 3.氨的实验室制法:① 原理:2NH4Cl+Ca(OH)2△==2NH3↑+CaCl2+2H2O ② 收集方法:向下排空气法 4.氨与水的反应:NH3+H2O=NH3钬?2O NH3钬?2O NH4++OH- 5.氨的催化氧化:4NH3+5O2 4NO+6H2O(制取硝酸的第一步) 6.碳酸氢铵受热分解:NH4HCO3 NH3↑+H2O+CO2↑ 7.铜与浓硝酸反应:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O 8.铜与稀硝酸反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 9.碳与浓硝酸反应:C+4HNO3=CO2↑+4NO2↑+2H2O
八、 铝及其化合物的性质 1.铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑ 2.铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ 3.铝在空气中氧化:4Al+3O2==2Al2O3 4.氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O 5.氧化铝与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 6.氢氧化铝与强酸反应:Al(OH)3+3HCl=AlCl3+3H2O 7.氢氧化铝与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]
九、 硅及及其化合物性质 1.硅与氢氧化钠反应:Si+2NaOH+H2O=Na2SiO3+2H2↑ 2.硅与氢氟酸反应:Si+4HF=SiF4+H2↑ 3.二氧化硅与氢氧化钠反应:SiO2+2NaOH=Na2SiO3+H2O 4.二氧化硅与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O
中学化学实验操作中的七原则:1.“从下往上”原则.以Cl2实验室制法为例,装配发生装置顺序是:放好铁架台→摆好酒精灯→根据酒精灯位置固定好铁圈→石棉网→固定好圆底烧瓶.2.“从左到右”原则.装配复杂装置应遵循从左到右顺序.如上装置装配顺序为:发生装置→集气瓶→烧杯.3.先“塞”后“定”原则.带导管的塞子在烧瓶固定前塞好,以免烧瓶固定后因不宜用力而塞不紧或因用力过猛而损坏仪器.4.“固体先放”原则.上例中,烧瓶内试剂MnO2应在烧瓶固定前装入,以免固体放入时损坏烧瓶.总之固体试剂应在固定前加入相应容器中.5.“液体后加”原则.液体药品在烧瓶固定后加入.如上例中浓盐酸应在烧瓶固定后在分液漏斗中缓慢加入.6.先验气密性(装入药口前进行)原则.7.后点酒精灯(所有装置装完后再点酒精灯)原则.1年前查看全部
- 高中化学必修1基础题3
 wanghui60106161年前1
wanghui60106161年前1 -
 野山果 共回答了11个问题
野山果 共回答了11个问题 |采纳率72.7%(3,4,7为半开放试题,答案不确定)
1
混合物:2,8
氧化物:1,4
酸:5
碱:6
盐:7,10
有机物:9
2
一元酸 HCl HNO3 二元酸 H2SO4 H2S 三元酸 H3PO4
强酸 HCl HNO3 H2SO4 中强酸 H3PO4 弱酸 H2S
含氧酸 H2SO4 HNO3 H3PO4 无氧酸 HCl H2S
3
固固混合物 金银混合金属粉末
固液混合物
液液混合物
气气混合物
汽液混合物
4
系统划分,有利于科研的开展
深入的划分,有利于进行深入的研究
5
浊液 >100nm 光照射,由于散射,光无法通过 泥土放入水中
溶液 100nm1年前查看全部
- 人教版高中化学必修1第四章第四节习题第四题,最好ABCD全讲解下
 psrlqg1年前1
psrlqg1年前1 -
 covinle8160 共回答了13个问题
covinle8160 共回答了13个问题 |采纳率92.3%A CaO+H2O=Ca(OH)2 Ca(OH)2+2NH4Cl=CaCl2+2 NH3·H2O NH3·H2O加热生成氨气
B 氯化铵加热生成氨气和氯化氢,不易分离
C 浓氨水加热放出氨气
D 水和生石灰反应生成氢氧化钙,放热,浓氨水受热放出氨气1年前查看全部
- 高中化学必修1,2整理笔记
 胖胖的小蚂蚁1年前2
胖胖的小蚂蚁1年前2 -
 小夹 共回答了17个问题
小夹 共回答了17个问题 |采纳率88.2%...你这是要累死我们?本人下学期高2,高一的,你注意几大反应(离子 氧化还原 。。。)你把这些掌握啦 就行啦!要会根据电子转移配方程式,这样大多反应你都能写出来!1年前查看全部
- 高中化学必修1的重点难点内容是什么?
 wangping1234561年前3
wangping1234561年前3 -
 icfg 共回答了14个问题
icfg 共回答了14个问题 |采纳率78.6%物质的量那一章、氧化还原反应中的有关习题、离子方程式的书写、离子共存问题、元素化合物的有关习题1年前查看全部
- 高中化学必修1人教版实验1-5(P16)
高中化学必修1人教版实验1-5(P16)

图中下面的 “学与问”第1问 坦然邂逅1年前4
坦然邂逅1年前4 -
 lc6238 共回答了10个问题
lc6238 共回答了10个问题 |采纳率90%因为洗涤液中也是含有少量之前的残留液体的,不然的话,配出的溶液物质的量浓度会变低.1年前查看全部
- 高中化学必修1第一章第2节的第9小题怎么做
 2000sheep1年前1
2000sheep1年前1 -
 后qq湖 共回答了15个问题
后qq湖 共回答了15个问题 |采纳率80%你买本教材全解,可以有很大帮助的1年前查看全部
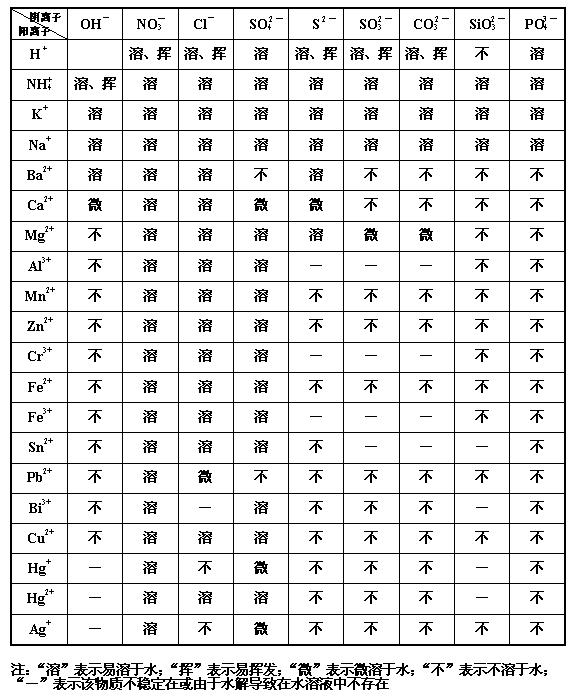
- 跪求,高中化学必修1附录2难溶性那个表
跪求,高中化学必修1附录2难溶性那个表
老师要抽背,急!
 sanmao0371年前1
sanmao0371年前1 -
 yun1314 共回答了17个问题
yun1314 共回答了17个问题 |采纳率100%1年前查看全部
大家在问
- 1费米是美籍意大利物理学家。他从小喜爱书籍,酷爱学习。对数学和物理特别感兴趣,设法去寻求自己想读的书。当时,费米家里生活贫
- 2x1分之x2加x2分之x1如题
- 3英语翻译标题中的英文表述怎么准确地翻译啊,说“一般的75%含量的BPO的密度是”后面的那个“ca.0.ca.是密度单位还
- 4孙吴周郎字公瑾,微风东来把名扬;晚霞把酒与小乔, 安心自得少年狂是什么意思
- 5史密斯先生去年戒烟了.mr smith ___ ___ last year.
- 62、 当质点做匀速直线运动时,其动量是否守恒?角动量是否守恒?
- 7英语存在句是什么?这是一个语言学的问题,
- 8天游峰的扫路人 老人的笑声真的惊动小鸟了吗?
- 9如果麦子没有考验 阅读短文上帝有一天心血来潮,来到他所创造的土地上散步,看到农田里的麦子结实累累,感到非常开心.上帝本来
- 1012个人围成一圈,从中选出两个不相邻的人,共有多少种选法?
- 11关于摘抄的格言有没有描写摘抄有哪些好处的格言?格式可以如"书籍是人类进步的阶梯"其他也行,只要是关于摘抄的!
- 12高一英语选择the boy's pale face suggested_____a.he should be in po
- 13a poor boy was selling goods from door to door to pay his wa
- 14形容春天的伴晚词语想要一个形容春天伴晚时候的词语.最好是三四个字的越经典越好.
- 15Fe3O4,Fe2O3 ,FeO分别与C反应方程式 Fe3O4,Fe2O3 ,FeO分别与CO反应方程式?