氮化碳属于原子晶体吗?
 terminertor2022-10-04 11:39:544条回答
terminertor2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 发芽的祝福 共回答了14个问题
发芽的祝福 共回答了14个问题 |采纳率100%- 正确,它是原子晶体.
- 1年前
 板板951 共回答了1个问题
板板951 共回答了1个问题 |采纳率- 原子晶体
- 1年前
 点点儿0 共回答了16个问题
点点儿0 共回答了16个问题 |采纳率- 是,根据晶体场理论
- 1年前
 shujianzhen 共回答了14319个问题
shujianzhen 共回答了14319个问题 |采纳率- 属于分子晶体
- 1年前
相关推荐
- (2014•上海模拟)根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首届一指的超硬新材料,已
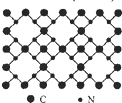 (2014•上海模拟)根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首届一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示.下列有关氮化碳的说法正确的是( )
(2014•上海模拟)根据量子力学计算,氮化碳结构有五种,其中一种氮化碳硬度超过金刚石晶体,成为首届一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示.下列有关氮化碳的说法正确的是( )
A.氮化碳属于分子晶体
B.氮化碳的分了式为C3N4
C.该晶体中的碳、氮原子核外都满足8电子稳定结构
D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 yiniyinii67671年前1
yiniyinii67671年前1 -
 不要迟疑 共回答了24个问题
不要迟疑 共回答了24个问题 |采纳率95.8%解题思路:A.根据原子晶体的性质分析;
B.根据原子晶体不存在分子式判断;
C.根据图中结构可知,每个碳原子周围有四个共价键,每个氮原子周围有三个共价键,据此分析;
D.根据图片判断碳原子和氮原子的连接方式.A.由题给信息,氮化硅是超硬新材料,符合原子晶体的典型物理性质,故A错误;
B.因为氮化碳是原子晶体,不存在分子,故没有分子式,故B错误;
C.根据图中结构可知,每个碳原子周围有四个共价键,每个氮原子周围有三个共价键,碳原子最外层有4个电子,形成四个共价健后成八电子稳定结构,氮原子最外层有5个电子,形成三个共价键后,也是八电子稳定结构,故C正确;
D.根据图知,每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连,故D正确;
故选CD.点评:
本题考点: 晶胞的计算.
考点点评: 本题考查了原子晶体的性质,晶胞的计算,利用均摊法进行分析解答,难度不大.1年前查看全部
- 怎么确定氮化碳的化学式氮有-3,+2,+4,+5价态.碳有+2,+4价态.只知道一种物质由碳氮元素组成,怎么确定这种物质
怎么确定氮化碳的化学式
氮有-3,+2,+4,+5价态.碳有+2,+4价态.只知道一种物质由碳氮元素组成,怎么确定这种物质的化学式? qinwendy1年前3
qinwendy1年前3 -
 尚无为 共回答了17个问题
尚无为 共回答了17个问题 |采纳率100%氮的夺电子能力比碳强.
所以碳是正价态,氮是负价态.
C3N41年前查看全部
- 氮化碳是什么物质?有什么特性?
 不停喝水1年前1
不停喝水1年前1 -
 ghwow116 共回答了18个问题
ghwow116 共回答了18个问题 |采纳率94.4%C是+4价,N是-3价,化学式是C3N4,是一种原子晶体,超硬,比金刚石还硬,耐高温,耐磨,性质稳定,可用做切磨机,钻头,轴承等1年前查看全部
- 人工合成的晶体氮化碳为什么硬度比金刚石大
人工合成的晶体氮化碳为什么硬度比金刚石大
金刚石是每个碳原子都以sp3杂化轨道与另外四个碳原子形成共价键,构成正四面体
而C3N4是C原子sp3杂化,与4个处于4面体顶点的N原子形成共价键,而N原子sp2杂化,与3个C原形成共价键
从这结构上看为什么C3N4的硬度大于金刚石啊? lixuhai8881年前3
lixuhai8881年前3 -
 elf小轩 共回答了23个问题
elf小轩 共回答了23个问题 |采纳率95.7%碳氮键比碳碳键短 键能大 所以硬度大1年前查看全部
- 氮化碳结构如图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料.下列有关氮化碳的说法不正确的是( )
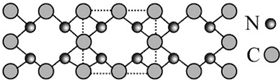 氮化碳结构如图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料.下列有关氮化碳的说法不正确的是( )
氮化碳结构如图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料.下列有关氮化碳的说法不正确的是( )
A.氮化碳属于原子晶体
B.氮化碳中C为-4价,N为+3价
C.氮化碳的化学式为C3N4
D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 啸弘1年前1
啸弘1年前1 -
 尼罗 共回答了20个问题
尼罗 共回答了20个问题 |采纳率95%解题思路:A.根据原子晶体的性质分析;
B.氮元素的电负性大于碳元素,所以在氮化碳中氮元素显负价,碳元素显正价;
C.利用均摊法确定其化学式;
D.根据图片判断碳原子和氮原子的连接方式.A.由题给信息,氮化硅是超硬新材料,符合原子晶体的典型物理性质,故A正确;
B.氮元素的电负性大于碳元素,所以在氮化碳中氮元素显-3价,碳元素显+4价,故B错误;
C.晶体结构模型中虚线部分是晶体的最小结构单元,正方形的顶点的原子占[1/4],边上的原子占[1/2],可得晶体的化学式为C3N4,故C正确;
D.根据图知,每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连,故D正确;
故选B.点评:
本题考点: 原子晶体;晶胞的计算.
考点点评: 本题考查了原子晶体的性质,晶胞的计算,利用均摊法进行分析解答,难度不大.1年前查看全部
- 氮化硅与氮化碳熔沸点高低?
 guangnide1年前2
guangnide1年前2 -
 susanhelen 共回答了22个问题
susanhelen 共回答了22个问题 |采纳率100%解析:.氮化碳熔沸点高于氮化硅
因为氮化硅和氮化碳都是原子晶体,原子晶体的熔沸点高低取决于共价键的键能大小,键能大小取决于原子半径大小,原子半径越小,键能越大,溶沸点越高.
C原子半径小于Si原子半径,即C-N键能>Si-N键能 ,所以氮化碳熔沸点高于氮化硅.1年前查看全部
- 氮化碳结构中一个N与三个C成键,一个C 与四个N成键,为什么化学式就是C3N4.这怎么理解?
 zggxyy1年前1
zggxyy1年前1 -
 质德 共回答了20个问题
质德 共回答了20个问题 |采纳率90%C四价,N三价,化合价代数和为01年前查看全部
- 氮化碳晶体可能还具有的性质或特点有什么 1熔点高2可导电3具有空间网状结构4不存在单个分子
 wangxun19801年前1
wangxun19801年前1 -
 hujiakang 共回答了15个问题
hujiakang 共回答了15个问题 |采纳率86.7%1341年前查看全部
大家在问
- 1Sally is my friend.Amy is my friend,too.合一句 sally and Amy ()
- 2为什么“220V 60W”的节能灯比“220V 60W”的白炽灯更亮?
- 3我不懂英文.Tommy said to me that do what you want and do what you
- 4我的家乡作文800字(湖南凤凰)
- 5帮我做做这些题啊····1.Jack,______borther teaches physics,is an engin
- 61.有一铜块,重量为G,密度为D,电阻率为ρ,把它拉制成截面半径为r的长导线,再用它做成一半径为R的圆形回路(R>>r)
- 7摘抄五段作文开头{写事、景、物 人
- 8英语翻译Dr.Gibbs died several years after I left home.Every now
- 9在《探究物体加速度与合力、质量关系》的实验中:
- 10地面离大气层最少有多少米?
- 11从语言表达的角度上赏析下列句子这是我一生所看到的最为缓慢的笑容,无比脆弱,像一个帝企鹅的蛋在冰天雪地经过长久的孵化,终于
- 12高中的朋友们,这是一道数学题,用二项式定理证明(55的55次方+9)能被8整除.(提示:(55的55次方+9)=(56-
- 13不同生长阶段的细菌有何特征?控制微生物生长阶段在活性污泥法污水处理上有什么意义?
- 14沉字去掉3点旁读什么
- 15如果轴截面为正方形的圆柱侧面积是4派,圆柱的体积是多少 ::>__
