四氯化钛和氨水一起反映呈酸性还是碱性?
 家在大南门2022-10-04 11:39:541条回答
家在大南门2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 pencunjin 共回答了16个问题
pencunjin 共回答了16个问题 |采纳率93.8%- 酸性吧
- 1年前
相关推荐
- 用四氯化钛制备二氧化钛工艺我是在实验室条件下制备的二氧化钛,应该是白色的,可制备出来却是淡黄色和白色的混合物,为什么呢?
用四氯化钛制备二氧化钛工艺
我是在实验室条件下制备的二氧化钛,应该是白色的,可制备出来却是淡黄色和白色的混合物,为什么呢?
其中有些类似的晶体,滴定测量钛含量83%左右, oaoaoaoa1年前2
oaoaoaoa1年前2 -
 Copie 共回答了21个问题
Copie 共回答了21个问题 |采纳率85.7%有可能是分解出的氯粒子与实验室装置上的钢结构件内部的铬结合后形成气体少量进入制备的二氧化钛成品中,铬离子较多时呈绿色,但微量时有可能为淡黄色.
解决方法是避免四氯化钛与钢结构件的接触,特别是在高温下.1年前查看全部
- 写出钛铁矿经氯化法得到四氯化钛的化学方程式?(不用写条件)
 dssdhjdshjsdj1年前1
dssdhjdshjsdj1年前1 -
 105273 共回答了16个问题
105273 共回答了16个问题 |采纳率93.8%FeTiO3+2H2SO4=TiSO4+FeSO4+2H2O
TiOSO4+2H20=H2TiO3+H2SO4
H2TiSO4=TiO2+H2O
TiO2+2Cl2+2C=TiCl4+2CO(加热)1年前查看全部
- 四氯化钛和钛酸四丁酯在使用时有何区别,在何种情况下适宜使用何种药品?
 罗小杰1年前1
罗小杰1年前1 -
 猛犸 共回答了29个问题
猛犸 共回答了29个问题 |采纳率93.1%四氯化钛是无机钛盐,钛酸四丁酯是有机钛盐.
四氯化钛溶于水,不过会冒烟、放热,配置水溶液时要小心,往水中少量对此的加入四氯化钛,并且要强烈搅拌.
钛酸四丁酯,不溶于水,溶于乙醇.但是钛酸四丁酯会和水反应发生水解,得到二氧化钛的溶胶,这个水解反应很缓慢,但是在酸或碱做催化剂的时候,水解过程会加速.1年前查看全部
- 工业上制金属钛采用金属热还原法还原四氯化钛.将钛铁矿和炭粉混合加热进行氯化处理,并使生成的TiCl4在高温下用熔融的镁在
工业上制金属钛采用金属热还原法还原四氯化钛.将钛铁矿和炭粉混合加热进行氯化处理,并使生成的TiCl4在高温下用熔融的镁在氩气中反应可得多孔的海绵钛,这种海绵钛经过粉碎、放入真空电弧炉里熔炼,最后制成各种钛材.下图为某化工厂企业生产流程示意图.
Cl2 H2
↓ CO ↓
FeTiO3、焦炭---------→①氯化------→②合成→甲醇(CH3OH)
↓ ↓TiCl4
FeCl3 ↓-----→ ③冶炼 Ar 800℃→Ti、MgCl2
Mg↗
问:②中为是原料全部转化为甲醛,理论上CO和H2投料的质量比为______.
 爱你哦1年前1
爱你哦1年前1 -
 幽幽紫焰 共回答了16个问题
幽幽紫焰 共回答了16个问题 |采纳率93.8%②中为是原料全部转化为甲醛,理论上CO和H2投料的质量比为__14:1____.1年前查看全部
- 知分析纯的四氯化钛如何配置浓度为0.5mol/l的溶液,最好详细些.
 b0ayrj1年前1
b0ayrj1年前1 -
 欧阳童童 共回答了13个问题
欧阳童童 共回答了13个问题 |采纳率76.9%分析纯的四氯化钛,纯度接近100%.如果配制0.5mol/l的溶液1升,那么需要四氯化钛95克.
即取95克四氯化钛与水混合配制成1升溶液即可.1年前查看全部
- 谁知道四氯化钛的物性数据 粘度 密度 表面张力 等 要不同温度以下的
 1zero1年前2
1zero1年前2 -
 anb1 共回答了19个问题
anb1 共回答了19个问题 |采纳率94.7%四氯化钛的粘度和表面张力数据差了很多资料都没找到
我把找到的数据送给你
四氯化钛
外观与性状:无色或微黄色液体,有刺激性酸味.在空气中发烟.
熔点(℃):-25
密度1.73g/cm³
沸点(℃):136.4
分子式:TiCl4
分子量:189.71
饱和蒸气压(kPa):1.33(21.3℃)
临界温度(℃):358
溶解性:溶于冷水、乙醇、稀盐酸.
折射率:1.61(10.5℃)
比热容:35.7卡/克•℃(液体),22.9卡/克•℃(气体)1年前查看全部
- (2013•北塘区一模)工业上制金属钛采用金属热还原法还原四氯化钛.将钛铁矿和炭粉混合加热进行氯化处理,并使生成的TiC
(2013•北塘区一模)工业上制金属钛采用金属热还原法还原四氯化钛.将钛铁矿和炭粉混合加热进行氯化处理,并使生成的TiCl4在高温下用熔融的镁在氩气中反应可得多孔的海绵钛,这种海绵钛经过粉碎、放入真空电弧炉里熔炼,最后制成各种钛材.下图为某化工企业生产流程示意图:
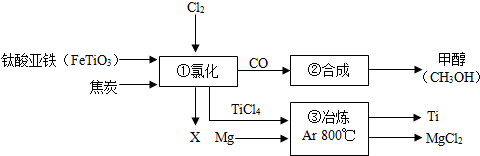
请回答下列问题:
(1)钛酸亚铁(FeTiO3)中钛元素的化合价为______;
(2)①中发生的反应为:2FeTiO3+6C+7Cl2
2X+2TiCl4+6CO,则X为______(填化学式);一定条件 .
(3)③中需要氩气(Ar)作保护气,请写出③中反应的化学方程式TiCl4+2Mg
Ti+2MgCl2800℃ .Ar TiCl4+2Mg,并推测钛的一点化学性质______;
Ti+2MgCl2800℃ .Ar
(4)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为______. lixiaolu691年前1
lixiaolu691年前1 -
 19552662 共回答了17个问题
19552662 共回答了17个问题 |采纳率88.2%解题思路:(1)根据在化合物中正负化合价代数和为零考虑;(2)根据质量守恒定律推断x的化学式;(3)根据化学方程式的书写方法填写化学方程式,根据用氩气作保护气考虑化学性质;(4)根据氢气和一氧化碳反应的方程式考虑质量比.(1)设FeTiO3中P的化合价是x.FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程(+2)+x+(-2)×3=0
解得,x=+4 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价;
(2)根据质量守恒定律,在反应前后各元素原子的个数不变.从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子.铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3;
(3)TiCl4与Mg反应的反应物是TiCl4与Mg,生成物是Ti和MgCl2,用观察法配平即可,因此该反应的化学方程式是TiCl4+2Mg
800℃
.
ArTi+2MgCl2;需要用氩气作保护气说明钛易与氧气反应;
(4)根据从化学方程式2H2+CO═CH3OH
4 28 由此可知一氧化碳和氢气的质量比是:28:4=7:1.
故答案为:(1)+4;(2)FeCl3;(3)TiCl4+2Mg
800℃
.
ArTi+2MgCl2;(4)7:1.点评:
本题考点: 物质的相互转化和制备.
考点点评: 本题主要考查了化合价的计算、化学方程式的书写以及质量守恒定律的应用,同时考查了学生从题目中获取信息并运用的能力.计算元素的化合价时一定要注意,一定不要忘记填上正号.1年前查看全部
- 四氯化钛与氯气在高温条件下生成什么化学物质?
 我在明天等你1年前3
我在明天等你1年前3 -
 月光下的小溪 共回答了28个问题
月光下的小溪 共回答了28个问题 |采纳率85.7%在沸腾通氯气进行氯化生产四氯化钛时,炉内还生成一氧化碳、氯化氢和光气(COCl2)等有毒气体,随每班放渣和氯气一起跑漏出来,它们同氯气一样都会造成急性中毒.1年前查看全部
- 四氯化钛和纳反应的条件
 abeone1年前1
abeone1年前1 -
 ray223 共回答了17个问题
ray223 共回答了17个问题 |采纳率88.2%在惰性气体保护下,TiCl4液体以一定速度注入盛有液体Na的密闭钢制反应器,发生反应
TiCl4 + 4Na = 4NaCl + Ti
反应很快且比较彻底,Na的利用率可接近100%.
缺点是反应温度不能低于NaCl熔点(801度),也不能超过Na的沸点(883度),有很大的控制难度.另外此反应放热很大,须采取有效的排热措施.
反应完成后,过量的Na和产物NaCl通过水洗去除,得到纯的Ti.1年前查看全部
- 请写出金属钠与四氯化钛的反应方程式?
 mikecello1年前3
mikecello1年前3 -
 友谊人生 共回答了28个问题
友谊人生 共回答了28个问题 |采纳率89.3%活泼的金属钠是强还原剂,这个反应是工业制取钛的反应,但是用液体钠才可以
在惰性气体保护下,TiCl4液体以一定速度注入盛有液体Na的密闭钢制反应器,发生反应
TiCl4+4Na=Ti+4NaCl1年前查看全部
- 四氯化钛水溶液怎么测定四氯化钛的含量
四氯化钛水溶液怎么测定四氯化钛的含量
四氯化钛的水溶液中四氯化钛的含量怎么分析? 幻墟1年前1
幻墟1年前1 -
 火欧泊 共回答了15个问题
火欧泊 共回答了15个问题 |采纳率73.3%加入过量氨水,生成钛酸沉淀,再加强热,使之成为TiO2,称重
可计算四氯化钛含量1年前查看全部
- 钛(Ti)和钛合金被认为是21世纪的重要金属材料,生产金属钛常用镁和四氯化钛在高温条件下发生置换反应来制取.计算:要制取
钛(Ti)和钛合金被认为是21世纪的重要金属材料,生产金属钛常用镁和四氯化钛在高温条件下发生置换反应来制取.计算:要制取4.8kg的金属钛,消耗镁的质量是多少?
 taikongchuan1年前1
taikongchuan1年前1 -
 花儿也谢了11 共回答了17个问题
花儿也谢了11 共回答了17个问题 |采纳率82.4%解题思路:根据反应的化学方程式,可得知反应中金属镁与钛的质量关系,由生成金属钛的质量,可计算参加反应镁的质量.设需要镁的质量为x,则TiCl4+2Mg 高温 . Ti+2MgCl2 4848 x ...
点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 金属铁在与酸、盐溶液的置换反应中,只能生成+2价的亚铁盐,而不是+3价的铁盐.1年前查看全部
- 用镁和四氯化钛制取金属钛时用氩气做保护气,是为了防止高温下镁被氧化·还是钛被氧化
 寻梦寻你1年前1
寻梦寻你1年前1 -
 荪恒 共回答了15个问题
荪恒 共回答了15个问题 |采纳率86.7%都保护的.镁钛高温下都会被氧化1年前查看全部
- 四氯化钛加入水中,然后有加氨水的反应方程式怎么写?
四氯化钛加入水中,然后有加氨水的反应方程式怎么写?
四氯化钛加入水中后形成淡白色胶状溶液,然后再加氨水,之后就有白色沉淀,那反应方程式是什么?
我看老师给我的方案上写的是:沉淀是H2TiO3 章鱼烧白1年前2
章鱼烧白1年前2 -
 瓜瓜西 共回答了15个问题
瓜瓜西 共回答了15个问题 |采纳率93.3%我们也是做TiCl4和 TiO2
反应方程式貌似是:TiCl4+3 H2O+4 NH3=H2TiO3+4 NH4Cl
H2TiO3=TiO2+H2O1年前查看全部
- (2011•通州区一模)钛和钛合金被认为是21世纪的重要金属材料,在工业上生产金属钛(Ti)通常是用金属镁和四氯化钛(T
(2011•通州区一模)钛和钛合金被认为是21世纪的重要金属材料,在工业上生产金属钛(Ti)通常是用金属镁和四氯化钛(TiCl4)发生置换反应方式来制取.若某厂预计生产12t金属钛,可同时生产副产品氯化镁多少吨?
 晴天碧涯1年前1
晴天碧涯1年前1 -
 珍惠惠 共回答了22个问题
珍惠惠 共回答了22个问题 |采纳率86.4%解题思路:先根据题意设出未知量,再依据反应原理写出方程式,然后计算相对分子质量、写未知量,列比例式解答,最后总结性的写出答案.生产12吨的钛,可以生成氯化镁的质量为x,
TiCl4+2Mg=2MgCl2+Ti
19048
x12t
[190/x]=[48/12t]
x=47.5t
答:生产12吨的金属钛.可以生成氯化镁47.5吨.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;常见金属的特性及其应用;根据化学反应方程式的计算.
考点点评: 在解此类题时,关键是根据题意列方程式,找等量关系,注意方程式中带入的物质都是纯净物.1年前查看全部
- 四氯化钛(TiCl4)是制取航天航空工业的材料--钛合金的重要原料.由钛铁矿(主要成份是FeTiO3)制备TiCl4等产
四氯化钛(TiCl4)是制取航天航空工业的材料--钛合金的重要原料.由钛铁矿(主要成份是FeTiO3)制备TiCl4等产品的一种工艺流程示意图如下:
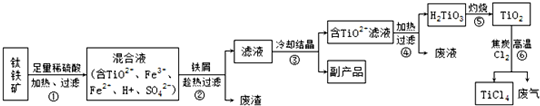
(1)步骤①钛铁矿加硫酸前经过选矿、洗涤、粉碎,其中粉碎的目的是______.
(2)步骤②加入铁屑,发生反应的化学方程式有______和Fe2(SO4)3+Fe═3FeSO4.
(3)步骤③制得的副产品是(填名称)______晶体.
(4)步骤⑤灼烧发生的反应类型是______反应.
(5)步骤⑥TiO2和焦炭、氯气反应生成TiCl4和CO的化学方程式:TiO2+2C+2Cl2
TiCl4+2CO高温 .TiO2+2C+2Cl2.
TiCl4+2CO高温 .
(6)上述工艺具有成本低、可以用低品位的矿物为原料等优点,但依据绿色化学理念,该工艺流程中存在的不足之处是______.
(7)上述流程中多次进行过滤操作,在实验室中,过滤必须用到的玻璃仪器有______. annehechen1年前1
annehechen1年前1 -
 melikexing 共回答了21个问题
melikexing 共回答了21个问题 |采纳率95.2%解题思路:(1)根据加快反应速度的方法考虑;(2)根据混合液中的物质考虑;(3)根据铁与硫酸反应、铁与硫酸铁反应的生成物考虑;(4)根据反应物和生成物的种类考虑;(5)根据方程式的写法考虑;(6)根据排放的物质考虑;(7)根据过滤时用到的仪器考虑.(1)增大可燃物接触面积可以使反应速度加快,反应充分,粉碎的目的是增大接触面积,使反应充分;
(2)由于混合物中含有硫酸,所以加入铁后,铁与硫酸反应生成硫酸亚铁和氢气,氢气后面标上上升符号;
(3)由于在步骤②中铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铁反应生成硫酸亚铁,所以趁热过滤后可得到硫酸亚铁晶体;
(4)步骤⑤灼烧发生的反应的反应物是H2TiO3,生成物是TiO2和H2O,反应物只有一种物质,生成物有两种,属于分解反应;
(5)反应物是TiO2和焦炭、氯气,生成物是四氯化钛和一氧化碳,用观察法配平,反应条件是高温写在等号的上边;
(6)该工艺流程能释放出废液、废气、废渣污染环境;
(7)过滤用到的仪器有:铁架台、烧杯、漏斗、玻璃棒;所以玻璃仪器有:漏斗、烧杯、玻璃棒.
故答案为:(1)增大接触面积,使反应充分;(2)H2SO4+Fe═FeSO4+H2↑;(3)硫酸亚铁;(4)分解;(5)TiO2+2C+2Cl2
高温
.
TiCl4+2CO;(6)产生三废;(7)漏斗、烧杯、玻璃棒.点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;绿色化学;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要熟悉加快反应速度的方法,方程式的书写方法,分解反应的特点,知道过滤操作用到的仪器,尤其是主要的玻璃仪器.1年前查看全部
- 四氯化钛(TiCl 4 )是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO 3 )制备
四氯化钛(TiCl 4 )是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO 3 )制备
TiCl 4 等产品的一种工艺流程示意如下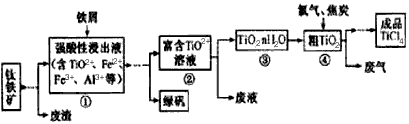
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生。
2Fe 3+ +Fe == 3Fe 2+
2TiO 2+ (无色) +Fe+4H + === 2Ti 3+ (紫色) +Fe 2+ +2H 2 O
Ti 3+ (紫色) +Fe 3+ +H 2 O === TiO 2+ (无色) +Fe 2+ +2H +
加入铁屑的作用是____________。
(2)在②→③工艺中需要控制条件以形成TiO 2 ·nH 2 O溶胶,该分散质颗粒直径大小在_____________范围。
(3)若把③中制得的固体TiO 2 ·nH 2 O用酸清洗除去其中的Fe(OH) 3 杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH) 3 ]=2.79×10 -39 ,该温度下反应Fe(OH) 3 +3H +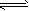 Fe 3+ +H 2 O的平衡常数K=___________。
Fe 3+ +H 2 O的平衡常数K=___________。
(4)已知:TiO 2 (s) +2Cl 2 (g)=== TiCl 4 (l) +O 2 (g) △H=+140KJ·mol -1
2C(s) +O 2 (g)=== 2CO(g) △H=-221KJ·mol -1
写出④中TiO 2 和焦炭、氯气反应生成液态TiCl 4 和CO气体的热化学方程式:_____________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_____________(只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl 4 杂质的TiCl 4 ,可采用_____________方法。
 驴骑士1年前1
驴骑士1年前1 -
 殷玥8125 共回答了20个问题
殷玥8125 共回答了20个问题 |采纳率90%(1)生成Ti 3+ ,保护Fe 2+ 不被氧化
(2)10 -9 ~10 -7 m
(3)2.79×10 3
(4)TiO 2 (s)+2C(s)+2Cl 2 (g)=TiCl 4 (l)+2CO(g) △H=-81kJ·mol -1
(5)产生了废气,废液,废渣等
(6)蒸馏(或分馏)1年前查看全部
- 高纯二氧化钛制备中的四氯化钛精制的目的是什么?
 zhanghuijie11201年前1
zhanghuijie11201年前1 -
 ciscosun 共回答了22个问题
ciscosun 共回答了22个问题 |采纳率90.9%你要制备高纯二氧化钛,当然就要再把四氯化钛提纯了,减少杂质参加反应1年前查看全部
- 镁与四氯化钛在高温条件下生成金属钛上述反应需在氩气环境中进行为什么?
镁与四氯化钛在高温条件下生成金属钛上述反应需在氩气环境中进行为什么?
不是副反应 133512601年前1
133512601年前1 -
 hangle 共回答了24个问题
hangle 共回答了24个问题 |采纳率79.2%惰性气体保护,防止氧气参与反应1年前查看全部
- 用四氯化钛凝胶法制取纳米二氧化钛薄膜的问题
用四氯化钛凝胶法制取纳米二氧化钛薄膜的问题
请问我用10ml的四氯化钛逐滴滴进不停搅拌的100ML含水10%的乙醇溶液中,制成的溶液为淡黄色,静止60个小时后,颜色不变,而且涂布在玻璃上用100度温度烘干,玻璃也呈淡黄色,这是什么原因?谢谢
而且在60度下加热,升温到400度,玻璃出现彩虹现象。 annycfn1年前1
annycfn1年前1 -
 wind779 共回答了18个问题
wind779 共回答了18个问题 |采纳率94.4%钛溶胶一般不会出现淡黄色的,这个原因可能是你在滴加的过程加热过头了,导致四氯化钛水解后氯离子显现本征的黄色,考虑下低温滴加,或者滴加快点,或者冰浴水中滴加,如果还不行,就要考虑水的量了,一般水多的话,水解加速,会有大量氯离子游离.
或者你换个试剂,有时候钛源很容易见空气中的水分水解,时间久了就完蛋了,硅酸盐也有这个缺点,一定保持干燥.
玻璃片基烘干后一般都会有点颜色,只是深浅问题,考虑下升温速度,这个很重要,400度出现彩虹倒没见过,一般有油污才会出现衍射现象,或者薄膜和玻璃基分离了,中间出现空气气泡,出现的密度干涉.
个人之见,仅作参考.
做实验多想,多做,慢慢就知道其中奥妙了.
祝你早日成功.1年前查看全部
- 四氯化钛水解制取粉体二氧化钛
 hvming199991年前1
hvming199991年前1 -
 孤独-云儿 共回答了22个问题
孤独-云儿 共回答了22个问题 |采纳率77.3%TiCl4(aq)+2H2O(l)=(加热)=TiO2(s)+4HCl(g) 需要注意的是 如果要防水解 即在HCl氛围中加热 制取TiO2的话 直接加热水溶液到没水了即可 注意尾气的处理1年前查看全部
- fries 重排正在做一个酯的重排,不知道有人做过没.用溶剂什么好点我是要邻位的产物.用的四氯化钛.能详细点么.
 油炸aa1年前1
油炸aa1年前1 -
 aaa8660357 共回答了24个问题
aaa8660357 共回答了24个问题 |采纳率87.5%用四氯化钛是对的.
还要注意控制反应的温度
较低温度下重排有利于形成对位异构产物,
较高温度下重排有利于形成邻位异构产物.1年前查看全部
- 在稀有气体的保护下,钠与熔融的四氯化钛反应是利用了(),反应的化学方程式是()
 etc121年前4
etc121年前4 -
 whytony 共回答了14个问题
whytony 共回答了14个问题 |采纳率85.7%在稀有气体的保护下,钠与熔融的四氯化钛反应是利用了(钠的活泼性比钛强),反应的化学方程式是(4Na+TiCl4=Ti+4NaCl)1年前查看全部
- 四氯化钛 镁 高温二氯化镁对人身体是否有害?
 为梦想生活1年前1
为梦想生活1年前1 -
 smartkiki 共回答了23个问题
smartkiki 共回答了23个问题 |采纳率87%有害1年前查看全部
- 计算题.“工业上常用金属钠来提炼钛、锆等.已知在700℃~800℃时,钠可从四氯化钛(TiCl4)中还原出钛.请写出有关
计算题.
“工业上常用金属钠来提炼钛、锆等.已知在700℃~800℃时,钠可从四氯化钛(TiCl4)中还原出钛.请写出有关反应的化学方程式,并计算用此法制取95.8g钛时所需钠的理论质量.” oxetjb1年前1
oxetjb1年前1 -
 ygl81711 共回答了24个问题
ygl81711 共回答了24个问题 |采纳率83.3%TiCl4(s) + 4Na(l) = Ti(s) + 4NaCl(l)
4*23 47.9
x 95.8
x=4*23*95.8/47.91年前查看全部
- (2011•福建)四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制
(2011•福建)四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
加入铁屑的作用是______.
(2)在②→③工艺中需要控制条件以形成TiO2•nH2O溶胶,该分散质颗粒直径大小在______范围.
(3)若把③中制得的固体TiO2•nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉.已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+⇌Fe3++H2O的平衡常数K=______.
(4)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1;2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:______.
(5)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流程中存在的不足之处是______(只要求写出一项).
(6)依据如表信息,要精制含少量SiCl4杂质的TiCl4,可采用______方法.
TiCl4 SiCl4 熔点/℃ -25.0 -68.8 沸点/℃ 136.4 57.6  两个小肥肥1年前1
两个小肥肥1年前1 -
 fatexuanwu 共回答了9个问题
fatexuanwu 共回答了9个问题 |采纳率88.9%解题思路:(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm);
(3)依据平衡常数的概念结合反应写出计算式计算平衡浓度得到;
(4)依据热化学方程式和盖斯定律计算分析得到;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,通常采取蒸馏方法分离.(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+,加入铁屑作还原剂,将Fe3+还原为Fe2+,防止Ti3+被Fe3+氧化成TiO2+,
故答案为:防止Ti3+被Fe3+氧化成TiO2+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm),
故答案为:10-9~10-7m(或1nm-100nm);
(3)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=2.79×10-39,反应Fe (OH)3+3H+⇌Fe3++H2O的平衡常数K=
c(Fe3+)
c3(H+)=
c(Fe3+)
(
10−14
c(OH−))3=c(Fe3+)×c3(OH-)×1042=2.79×10-39×1042=2.79×103.
故答案为:2.79×103;
(4)①TiO2 (s)+2Cl2 (g)═TiCl4(l)+O2(g)△H=+140KJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221KJ•mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ•mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ•mol-1
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,要精制含少量SiCl4杂质的TiCl4,可采用蒸馏(或分馏)方法,
故答案为:蒸馏(或分馏);点评:
本题考点: 制备实验方案的设计;热化学方程式;化学平衡常数的含义;难溶电解质的溶解平衡及沉淀转化的本质;常见金属元素的单质及其化合物的综合应用;物质的分离、提纯和除杂.
考点点评: 本题考查学生阅读题目获取信息能力、氧化还原反应、绿色化学、胶体、物质分离提纯,平衡常数计算,溶度积常数的计算应用,盖斯定律的计算应用等,难度不大,注意基础知识的掌握利用.1年前查看全部
- (2014•张家界)钛是一种被广泛应用于航空、航母等领域的重要金属.它可由四氯化钛(化学式TiCl4)金属镁在一定条件下
(2014•张家界)钛是一种被广泛应用于航空、航母等领域的重要金属.它可由四氯化钛(化学式TiCl4)金属镁在一定条件下反应而制得,其化学反应方程式:
TiCl4+2Mg
Ti+2MgCl2.若需要得到720kg钛(化学式为Ti),则理论上需要四氯化钛的质量是多少?一定条件 . sanxing88661年前1
sanxing88661年前1 -
 明思妙语 共回答了14个问题
明思妙语 共回答了14个问题 |采纳率85.7%解题思路:根据四氯化钛和金属镁反应的方程式,由金属钛的质量可求出四氯化钛的质量.设理论上需要四氯化钛的质量是x
TiCl4+2Mg
一定条件
.
Ti+2MgCl2
190 48
x 720kg
[190/48=
x
720kg]
x=2850kg
答案:理论上需要四氯化钛的质量是2850kg.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题属于根据化学方程式的基本计算,掌握根据化学方程式计算的基本方法就可以了.1年前查看全部
- 金属钛(Ti)的氧化物二氧化钛(TiO2)是优良的白色颜料,常用于制作高档油漆,四氯化钛是一种无色液体,非常容易跟空气中
金属钛(Ti)的氧化物二氧化钛(TiO2)是优良的白色颜料,常用于制作高档油漆,四氯化钛是一种无色液体,非常容易跟空气中的水发生反应生成二氧化钛,并有大量酸雾生成,写出四氯化钛跟水反应的化学方程式______.
 3308630011年前1
3308630011年前1 -
 lpjy_dccit4470 共回答了18个问题
lpjy_dccit4470 共回答了18个问题 |采纳率94.4%解题思路:根据题意,四氯化钛容易跟空气中的水发生反应生成二氧化钛,并有大量酸雾(由质量守恒定律,反应前后元素质量不变,该物质是盐酸)生成,写出反应的化学方程式即可.由题意,四氯化钛容易跟空气e的水发生反应生成二氧化钛,并有大量酸雾(由质量守恒定律,反应前后元素质量不变,该物质是盐酸)生成,反应的化学方程式为:三八上l0+3H3O═三八O3+0H上l.
故答案为:三八上l0+3H3O═三八O3+0H上l.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- 钛合金以其优越的性能被誉为第四代金属.工业上在高温和稀有气体的保护下,用镁和四氯化钛发生置换反应来制取钛.该反应的化学方
钛合金以其优越的性能被誉为第四代金属.工业上在高温和稀有气体的保护下,用镁和四氯化钛发生置换反应来制取钛.该反应的化学方程式为2Mg+TiCl4
2MgCl2+Ti高温 .稀有气体 2Mg+TiCl4.
2MgCl2+Ti高温 .稀有气体  超时空毛毛1年前1
超时空毛毛1年前1 -
 oo的涨声 共回答了10个问题
oo的涨声 共回答了10个问题 |采纳率100%解题思路:根据题意,工业上在高温和稀有气体的保护下,用镁和四氯化钛发生置换反应来制取钛,写出该反应的化学方程式即可.工业上在高温和稀有气体的保护下,用镁和四氯化钛发生置换反应来制取钛,同时生成氯化镁,该反应的化学方程式为2Mg+TiCl4高温.稀有气体2MgCl2+Ti.故...
点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- 在氩气的气流中,过量的镁与四氯化钛反应,为什么要在氩气的气流中进行
 qiushengliang1年前1
qiushengliang1年前1 -
 weizyu123456 共回答了13个问题
weizyu123456 共回答了13个问题 |采纳率84.6%在空气中氧气会把镁氧化1年前查看全部
- 四氯化钛与钠反应化学方程式四氯化钛与钠反应生成氯化钠和钛的化学反应方程式!
 yan829011年前4
yan829011年前4 -
 gungun_wc 共回答了19个问题
gungun_wc 共回答了19个问题 |采纳率78.9%就是TiCl4 + 4Na=4NaCl + Ti 条件是熔融
这个是标准的置换反映,Na的金属性比Ti强,所以把Ti置换出来了.1年前查看全部
- 四氯化钛的水解方程式是什么?
 太康公主11年前1
太康公主11年前1 -
 迪克亮仔 共回答了21个问题
迪克亮仔 共回答了21个问题 |采纳率90.5%将TiCl4溶于水配制成TiCl4储备液时,TiCl4部分水解,形成第一个水产物[Ti((OH)nCl6-n]2-.
水解反应式为:
TiCl4 +nH2O—>H2[Ti((OH)nCl6-n]+(n-2)HCl
在强迫水解过程中,加热体系,促进TiCl4水解的进一步进行,[Ti((OH)nCl6-n]2-发生进一步的水解,生成钛羟基络合物,反应过程可以表示为:
H2[Ti((OH)nCl6-n]+ (6-n)H2O—>[Ti((OH)n H2O 6-n] Cl6-n+2HCl
发生的主要水解反应就是这两个,其中有络合物的知识,在高中阶段没有做特别要求,把它当成一个基团即可.1年前查看全部
- 氢化钠和四氯化钛反应的产物是如何判断的,有什么依据?到底是氢气还是氯化氢
 枣胡1年前2
枣胡1年前2 -
 pychenw 共回答了14个问题
pychenw 共回答了14个问题 |采纳率85.7%4NaH +
TiCl4 ===4NaCl + Ti +
H2↑
H- 还原了高价的Ti4+ ,生成了H2 而Cl-与Na+结合变为了NaCl .
要使H-变为H+ 需要能把0价氢转化为H+的物质,没有强氧化剂实现此变化.
NaH +H2O 的反应时,H- 生成了H(0价)1年前查看全部
- 四氯化钛能与钠反应,那么四氟化钛能否与钠反应?四碘化钛能否与钠反应?四溴化钛能否与钠反应?
 ssfzhangpinghua1年前3
ssfzhangpinghua1年前3 -
 drakestone 共回答了24个问题
drakestone 共回答了24个问题 |采纳率95.8%都能,产物是类似的
TiX4 + 4 Na ==高温== Ti + 4 NaX
因为TiCl4最便宜、容易制备,实际生产Ti时,选择了TiCl41年前查看全部
- 四氯化钛非常容易与空气中的水发生反应生成二氧化钛和盐酸,反应的化学方程式为.
 oldtty1年前1
oldtty1年前1 -
 wangziyi19830105 共回答了20个问题
wangziyi19830105 共回答了20个问题 |采纳率95%TiCl4+2H2O==TiO2+4HCl1年前查看全部
- 镁与四氯化钛反应的化学方程式
 太爱厉娜1年前1
太爱厉娜1年前1 -
 huaqiaohao 共回答了14个问题
huaqiaohao 共回答了14个问题 |采纳率85.7%2Mg+TiCl4====2MgCl2+Ti1年前查看全部
- 氢化钠和四氯化钛反应化学方程式
 yukihe911年前2
yukihe911年前2 -
 圣梅西 共回答了20个问题
圣梅西 共回答了20个问题 |采纳率95%2NaH+TiCl4=Ti+2NaCl+2HCl1年前查看全部
- 四氯化钛和镁的化学方程式
 tcccoco1年前3
tcccoco1年前3 -
 至尊红岩 共回答了15个问题
至尊红岩 共回答了15个问题 |采纳率86.7%TiCl4+2Mg=2MgCl2+Ti1年前查看全部
- 求使用四氯化钛水溶液与氨水反应制备二氧化钛溶胶的具体浓度配比和操作细节
 yijianbing1年前2
yijianbing1年前2 -
 何谓 共回答了20个问题
何谓 共回答了20个问题 |采纳率90%偏钛酸是比较不稳定的物质,PH值,浓度,温度都对反应有较大的影响1年前查看全部
- 镁和四氯化钛的反应为什么要需要再氩气的环境中进行
 1acfea11年前1
1acfea11年前1 -
 putaoya 共回答了20个问题
putaoya 共回答了20个问题 |采纳率90%氩气是惰性气体可以防止发生副反应 保证产物是所需产物1年前查看全部
- 镁与四氯化钛反应需在氩气环境中进行的原因是什么
 亲亲的给你一个吻1年前1
亲亲的给你一个吻1年前1 -
 楚梦秦殇 共回答了17个问题
楚梦秦殇 共回答了17个问题 |采纳率94.1%惰性气体作为保护气.防止副反应 比如MG和氧气反应1年前查看全部
- 四氯化钛气体 密度气态时四氯化钛的物理性质是什么?密度、定压比热容等,有人知道吗?
 小小锋儿21年前1
小小锋儿21年前1 -
 我龌龊我存在 共回答了16个问题
我龌龊我存在 共回答了16个问题 |采纳率93.8%常温下纯TiCl4是一种无色透明的液体,在空气中会发出大量白烟,微量时稍带甜味,多量时有强烈的刺激性.TiCl4本身没有可燃性与爆炸性.
常用的TiCl4的物理与热力学数据如下:
分 子 量:189.73
熔 点:-25℃(-24.3℃)
沸 点:136.4℃(135.2℃)(760mmHg)
比 热:35.7卡/克分子•℃(液体),22.9卡/克分子•℃(气体)
蒸汽密度:5.37g/l
先告诉你这么多,基本上全满足你的问题要求了,呵呵!1年前查看全部
- 怎样用 四氯化钛制备二氧化钛溶胶?
 jackiepang1年前1
jackiepang1年前1 -
 801112 共回答了11个问题
801112 共回答了11个问题 |采纳率72.7%四氯化钛在空气里遇水就可以生成浓盐酸,冒白色的烟雾,可以用四氯化钛和去离子水直接反应后静置制得1年前查看全部
- 如何防止四氯化钛水解
 一杯奶酪1年前2
一杯奶酪1年前2 -
 蜜恋璐璐 共回答了11个问题
蜜恋璐璐 共回答了11个问题 |采纳率72.7%TiCl4遇水即水解,想防止水解,操作必须处于无水环境.在制金属钛的过程中要全程保持无水无氧.1年前查看全部
- 试剂四氯化钛上写着98%的,怎么样配制成浓度为0.2mol/L的?
试剂四氯化钛上写着98%的,怎么样配制成浓度为0.2mol/L的?
不知道那试剂上的写着是不是就是质量含量呢?
在配制到这个浓度的时候不都要加水的吗? 光重皇1年前2
光重皇1年前2 -
 啡吗 共回答了19个问题
啡吗 共回答了19个问题 |采纳率94.7%四氯化钛试剂瓶上写的98%是指它的纯度.一个mol的四氯化钛是47.42g,配0.2mol/L的四氯化钛溶液,就是在1升水中添加0.2mol(即9.48g)的100%的TiCl4.因为纯度是98%,故用98%除9.48g,得9.67g.注意:四氯化钛水溶液的配置是很麻烦也很讲究的,最关键的有两个指标,一个是加料速度;二是加料过程的温度,因为四氯化钛很容易水解为二氧化钛(白色沉淀).如果工业上配制,你可以用一台搅拌釜(需要有冷却套),事先把计算好的水量的大部分(如0.8立方米)加进搅拌釜进行搅拌,然后滴加四氯化钛(共加9.67kg),注意滴加过程一定要慢,温度不能高与40度,然后慢慢补加0.2立方水.如果实验用的你可以在烧杯中进行,对烧杯进行强制冷却.加料比例同上.1年前查看全部
- 工厂炼钛的时候为什么用钠区置换四氯化钛,而不是用铝去置换四氯化钛呢?也可以用铝和二氧化钛反应?
 与浍1年前1
与浍1年前1 -
 渴望之星 共回答了19个问题
渴望之星 共回答了19个问题 |采纳率94.7%一个是为了除杂, 另一个是因为高温下钛的化合能力极强,可以与氧、碳、氮以及其他许多元素化合.因此,冶炼或者铸造的时候,都是严格禁止接近这个物质的,甚至连冶金上常用的氧化铝坩埚也禁止使用,因为钛会从氧化铝里夺取氧. 钛的冶炼很复杂,成本也很高,这是必然的.毕竟纯度是最重要的1年前查看全部
- 一般这这种四氯化钛水溶液的用途有那些!看清楚是四氯化钛水溶液而不是四氯化钛的用途!四氯化钛水溶液是50%的水加50%的四
一般这这种四氯化钛水溶液的用途有那些!看清楚是四氯化钛水溶液而不是四氯化钛的用途!四氯化钛水溶液是50%的水加50%的四氯化钛组成的!有知道的麻烦说下!
 穿过琴弦的月光1年前1
穿过琴弦的月光1年前1 -
 瑜鱼儿 共回答了30个问题
瑜鱼儿 共回答了30个问题 |采纳率83.3%主要用途 用于制造钛盐、虹彩剂、人造珍珠、烟幕、颜料、织物媒染剂等1年前查看全部
- 苯的处置苯泄漏应如何处置?苯应该如何保存?我的苯是500ml的瓶子,密封得很好,需要与碱分储吗?可以跟四氯化碳,四氯化钛
苯的处置
苯泄漏应如何处置?苯应该如何保存?我的苯是500ml的瓶子,密封得很好,需要与碱分储吗?可以跟四氯化碳,四氯化钛,氨水,水合肼放在一起吗? linlinchen1年前1
linlinchen1年前1 -
 MARSwht 共回答了18个问题
MARSwht 共回答了18个问题 |采纳率77.8%用抹布等吸取 再用有机溶剂冲洗并清洗 保存在密闭容器 要分开 因为苯和部分碱反映 和四氯化碳 四氯化钛 氨水 水 会分层 但由于溶质的扩散作用 最好不要合并1年前查看全部
- (2010•安徽模拟)四氯化钛是无色液体,沸点为136℃.它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O═
(2010•安徽模拟)四氯化钛是无色液体,沸点为136℃.它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O═TiOCl2+2HCl↑).在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体.下图是实验室制备TiCl4的部分装置.

请回答:
(1)B装置中试剂为______,其作用是______.
(2)C装置中的反应方程式为______.
(3)D装置中冷凝水的方向为______进______出,该装置的作用为______.
(4)评价此装置的缺陷和不妥之处:
编号 装置缺陷和不妥之处 ① ② ③  chaochao09011年前1
chaochao09011年前1 -
 skyflybaby 共回答了16个问题
skyflybaby 共回答了16个问题 |采纳率93.8%解题思路:(1)根据制备的氯气中含有杂质水蒸气;
(2)由于TiO2、C、Cl2混合物在高温条件下制得TiCl4和一种有毒气体,根据化学反应中元素种类不变的规律可知:该有毒气体含有碳、氧两种元素,由碳、氧两种元素组成的有毒气体只有一氧化碳;因此TiO2、C、Cl2混合物在高温条件下反应生成TiCl4和一氧化碳;
(3)根据冷凝管内的水流方向由下向上,因为这样可以提高冷凝效果;四氯化钛沸点低,易挥发,所以要用冷凝管冷凝回收;
(4)①根据TiCl4 遇空气中水蒸气发生水解;
②根据TiCl4 水解产生的氯化氢极易溶于水;
③根据氯气通过二氧化钛和炭粉的混合物得到的CO气体有毒,(1)因制备的氯气中含有杂质水蒸气,可用浓硫酸来除去,故答案为:浓硫酸;干燥氯气;
(2)由于TiO2、C、Cl2混合物在高温条件下制得TiCl4和一种有毒气体,根据化学反应中元素种类不变的规律可知:该有毒气体含有碳、氧两种元素,由碳、氧两种元素组成的有毒气体只有一氧化碳;因此TiO2、C、Cl2混合物在高温条件下反应生成TiCl4和一氧化碳;
该反应的化学方程式为:TiO2+2Cl2+2C TiCl4+2CO,故答案为:TiO2+2Cl2+2C
TiCl4+2CO,故答案为:TiO2+2Cl2+2C  TiCl4+2CO;
TiCl4+2CO;
(3)因根据冷凝管内的水流方向由下向上,即a进b出,因为这样可以提高冷凝效果;四氯化钛是无色液体,沸点为136℃较低,受热易挥发,所以冷凝管冷凝回收,故答案为:a;b;冷凝回流四氯化钛;
(4)①、因TiCl4 遇空气中水蒸气发生水解,缺少阻止水蒸气进入D的装置,所以TiCl4 遇空气中水蒸气发生水解,缺少阻止水蒸气进入D的装置;
②、因TiCl4 水解产生的氯化氢极易溶于水,需要加上防倒吸的装置,所以TiCl4 水解产生的氯化氢极易溶于水,需要加上防倒吸的装置;
③、因氯气通过二氧化钛和炭粉的混合物得到的CO气体有毒,缺少CO的处理装置,所以由于CO气体有毒,缺少CO的处理装置.
故答案为:
编号 装置缺陷和不妥之处
① 不能阻止E装置的水汽进入D装置,而引起四氯化钛水解
② 由于氯化氢和氯气易溶于氢氧化钠溶液,E装置会产生倒吸现象
③ 不能防止CO的逸出点评:
本题考点: 制备实验方案的设计;氯气的化学性质;氯气的实验室制法.
考点点评: 本题是结合物质制备考查了基本实验操作,是一道综合性较强的实验题,考查考生分析实验装置并评价实验方案的能力.1年前查看全部
大家在问
- 1为什么氨水显碱性而叠氮酸显酸性
- 2想知道一些与山有关的诗词,有意境的.
- 3高一的化学(电解质这方面)经常有题目问我们有某某些东西 会导电的是.是电解质的是.非电解质的是.我想知道导电 和 电解质
- 4下列状态的物质,既能导电又属于电解质的是
- 5如图,在△ABC中,AD平分角BAC,AB=AC-BD,则试判断角B与角C的关系,并证明
- 6某人10点10分离家去赶11点的火车.他家离火车站有10km,他离家后先以3km/时的速度走了5min.
- 7用丝绸摩擦过的玻璃棒和用毛皮摩擦过的橡胶棒产生的分别是什么电荷?
- 8参考一道数学题,我明天就要交了,我给高悬赏,要对的
- 9基因组DNA和叶绿体DNA区别
- 10一个分数的分母缩小到原来的四分之一后,化成小数是0.4.若原分数分子扩大到原来的五倍,化成小数是多少
- 11英语翻译如题翻译中文,
- 12判断下列两个集合之间的关系:(1)A={x|x=3k,k∈N},B={x|x=6z,z∈N}(2)A={x|x是4与10
- 13to study better,you should read some( )(magazine) after scho
- 141又5分之3的分数单位是?再添上几个这样的单位就是最小的质数?
- 15小强看一本60页的科技书,上午看了总页数的4分之1 ,下午看了总页数的20%,还余下多少页没有看?
