等电子体具有原子数目相同、电子数目的特征.下列各组物质中属于等电子体的是( ) A.NH 3 和CH 4 B.NO 2
 wanlynn2022-10-04 11:39:541条回答
wanlynn2022-10-04 11:39:541条回答 等电子体具有原子数目相同、电子数目的特征.下列各组物质中属于等电子体的是( )
|

已提交,审核后显示!提交回复
共1条回复
 fengzaifei 共回答了21个问题
fengzaifei 共回答了21个问题 |采纳率76.2%- A、NH 3 和CH 4 ,原子数目不相同;电子数分别为:7+1×3=10,6+1×4=10,故A不符合题意;
B、NO 2 和CO 2 ,原子数目相同都为3个,电子数分别为:7+8×2=23,6+8×2=22,故B不符合题意;
C、NO和O 2 + ,原子数目相同都为2个,电子数分别为:8+7=15,8+8-1=15,故C符合题意;
D、SO 2 和ClO 2 ,原子数目相同都为3个,电子数分别为:16+8×2=32,17+8×2=33,故D不符合题意.
故选C. - 1年前
相关推荐
- 等电子体具有原子数目相同,电子数目相同的特征
等电子体具有原子数目相同,电子数目相同的特征
那为什么NO和O2+ (注:“O2+”中“2”在右下方 “+”在右上方)是等电子体啊?
不是说还要原子数目相同么 可这个一个是15 一个是16啊 PYJ9079071年前3
PYJ9079071年前3 -
 伽枥 共回答了17个问题
伽枥 共回答了17个问题 |采纳率88.2%额...我没听说过“O2+”但是听说过“O2-”不知道是不是打错了...
算一下哈...NO共有7+8=15个电子,O2+有8+8-1=15个电子.
楼上的...一个O有个电子.不是6个.
(⊙o⊙)…
原子数目确实相同啊.都是2个啊.理解清原子的意思没?1年前查看全部
- 写出一种与NO3-互为等电子体的一种非极性分子的化学式 答案是SO3,我想知道C4H8(环状)对不对?
 xzq76210001年前2
xzq76210001年前2 -
 丁子-丁子 共回答了20个问题
丁子-丁子 共回答了20个问题 |采纳率95%写出一种与NO3-互为等电子体的一种非极性分子的化学式 答案是SO3
也可以是BF3
---
C4H8(环状)不对,等电子体要求原子数要相同,最外层电子(价电子)总数要相同1年前查看全部
- 等电子体的找法系统的方法 可以比较准确地找等电子体
 38483621年前1
38483621年前1 -
 jianjun0639 共回答了20个问题
jianjun0639 共回答了20个问题 |采纳率85%首先要熟记基本元素的电子数,再根据题设联想常见的物质.以化合价绝对值较高的元素为主体,向上加氢,氯等常显正负一价的原子,勿忘PCl3,PCl5有时也会考加二价元素的,这种题主要考对元素的熟练程度,找时要有条理,不要眉毛胡子一把抓,也不要怕,1年前查看全部
- Al离子和OH-是等电子体么
 猪头xx1年前3
猪头xx1年前3 -
 barcatiamo 共回答了22个问题
barcatiamo 共回答了22个问题 |采纳率90.9%是的,18电子1年前查看全部
- 1等电子体列举__2.5摩尔每升的硫酸溶液是否为浓硫酸?怎样判断?98%的硫酸为浓硫酸,将它转化为硫酸的物...
1等电子体列举__2.5摩尔每升的硫酸溶液是否为浓硫酸?怎样判断?98%的硫酸为浓硫酸,将它转化为硫酸的物...
1等电子体列举__2.5摩尔每升的硫酸溶液是否为浓硫酸?怎样判断?98%的硫酸为浓硫酸,将它转化为硫酸的物质的量浓度时怎样转化? luofaming1年前1
luofaming1年前1 -
 沙滩上的海鱼 共回答了24个问题
沙滩上的海鱼 共回答了24个问题 |采纳率91.7%1、等电子体列举:N2和CO,NH4+和H3O+等
2、5mol/L的硫酸溶液不是浓硫酸.浓硫酸指浓度大于或等于70%的硫酸溶液.98%的浓硫酸转化为硫酸物质的量浓度时利用的公式是:c=p*w/98,其中p是浓硫酸密度,w是浓硫酸浓度.1年前查看全部
- 1919年,Langmui提出等电子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近
1919年,Langmui提出等电子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。
(1)CNS - 、NO 2 + 具有相同的通式:AX 2 ,它们的价电子总数都是16,因此它们的结构与由第二周期两元素组成的_______分子的结构相同,微粒呈_______形,中心原子取_______杂化轨道。
(2)CO 3 2- 、NO 3 - 等微粒的总价电子数都等于________,呈_______形,中心原子都取_______杂化。 jasonwangbj1年前1
jasonwangbj1年前1 -
 kaseem 共回答了16个问题
kaseem 共回答了16个问题 |采纳率87.5%(1)CO 2 ;直线形;sp
(2)24;平面正三角形;sp 21年前查看全部
- 问:碳酸根与硅酸根为什么不是等电子体?
问:碳酸根与硅酸根为什么不是等电子体?
请给出详细的说明.他们成键的方式有什么不同吗?我先谢谢大家了!
书上说碳酸根与硅酸根的中心原子用于成键的轨道和杂化类型不同而导致离子的结构不同,所以不是等电子体.那么他们又各是什么杂化类型呢?并且为什么会又不同的杂化类型?
并且等电子体的定义是:含有相同重原子和价电子数的分子或离子往往具有相似的几何构型和化学键合情况.所以并不是什么“它们的电子总数不同,所以不是等电子体”. 甜蜜味道1年前3
甜蜜味道1年前3 -
 帅的感动ii 共回答了23个问题
帅的感动ii 共回答了23个问题 |采纳率91.3%因为Si是第三周期的元素,有大量的3d空轨道,和O元素的2p轨道有重叠,形成d-pπ键,而碳酸中C和O只有p-pπ键,所以它们不能称为等电子体.1年前查看全部
- 为什么co 和n2 是等电子体
 kiki12221年前1
kiki12221年前1 -
 fztvxq1213 共回答了19个问题
fztvxq1213 共回答了19个问题 |采纳率89.5%因为它们是核外电子总数及质子总数均相等的粒子:N2、CO、C2H2(14个质子、14个电子)1年前查看全部
- 怎么记八8,14,18等电子体?
 逢鱼必吃1年前1
逢鱼必吃1年前1 -
 df456123 共回答了27个问题
df456123 共回答了27个问题 |采纳率88.9%好比说18电子吧
原子序数是18的是Ar,这是第一个
原子序数比18小1,再加上一个H 得就是HCL
以此类推.H2S PH3 SIH3..
双原子的就是原子序数是9的,就是F2
9=1+8 所以还是过氧化氢 H2O2 还有N2HE (联氨)
还是离子,阳离子:Ar 后面的是K 所以离子有 K离子,Ca离子,
同理,阴离子有P离子,S离子,CL离子 HS离子
关键就是救助中间的那个原子!Ar!
同理8电子 就是中间的O
但是很傻奇偶有用8电子的,一般都是10电子1年前查看全部
- AlO2-与N3-互为等电子体
 fo181年前2
fo181年前2 -
 paciwood66 共回答了19个问题
paciwood66 共回答了19个问题 |采纳率100%价电子数不同,AlO2-17个价电子,N3-18个价电子,等电子体指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团.1年前查看全部
- 钠离子和氯离子为什么不是等电子体!
 Q家小女1年前0
Q家小女1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 由第一第二周期元素组成,与F2互为等电子体的离子有?
 aabad1年前1
aabad1年前1 -
 bluick 共回答了26个问题
bluick 共回答了26个问题 |采纳率92.3%O2(2-)过氧根离子.1年前查看全部
- 等电子体,要求原子数相同,电子数相同,(是总电子数,还是总价电子数?)
等电子体,要求原子数相同,电子数相同,(是总电子数,还是总价电子数?)
做了一道题,与CS2等电子体的阴离子是N3-? sunn19801年前1
sunn19801年前1 -
 Google测试员5114 共回答了14个问题
Google测试员5114 共回答了14个问题 |采纳率92.9%选修三中的等电子体是指原子总数相同 价电子总数相同1年前查看全部
- 价电子总数与原子总数都相同的分子、离子或原子团称为等电子体,等电子体具有相似的结构和性质。下列选项中互称为等电子体的是
价电子总数与原子总数都相同的分子、离子或原子团称为等电子体,等电子体具有相似的结构和性质。下列选项中互称为等电子体的是
A. 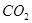 和
和 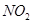
B.  和
和 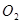
C. 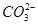 和
和 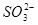
D. 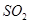 和
和 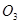
 多所1年前1
多所1年前1 -
 海怪y 共回答了15个问题
海怪y 共回答了15个问题 |采纳率93.3%D
1年前查看全部
- 1)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质.下列各组粒子中属于等电子体的是 ___
1)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质.下列各组粒子中属于等电子体的是 ___ (填字母序号).
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43―和SO42―
2)在HF、F-、NH4+、Mg 2+和OH-五种微粒中相同的是()
A.质子数 B.中子数 C.电子数 D.原子数 dongsohn1年前3
dongsohn1年前3 -
 米兰妖刀 共回答了20个问题
米兰妖刀 共回答了20个问题 |采纳率85%第一题如果题目中信息没错的话BD两项符合.第二题各微粒中电子数都是10个.1年前查看全部
- CO2 ,O3的等电子体请列出CO2,O3的常见等电子体
 znhrpy1年前2
znhrpy1年前2 -
 sxmy43 共回答了24个问题
sxmy43 共回答了24个问题 |采纳率83.3%CO2:N2O C3H4 C2H3N
O3:C3H6 C2H401年前查看全部
- CH3+各原子共面吗?(他和谁是等电子体)
 感觉有点疼1年前1
感觉有点疼1年前1 -
 afei8 共回答了15个问题
afei8 共回答了15个问题 |采纳率100%CH3+各原子共面(他和BH3是等电子体)1年前查看全部
- 二氧化碳的等电子体有什么,电子式分别怎么写?
 lypxcz1年前1
lypxcz1年前1 -
 男人女人谢谢 共回答了21个问题
男人女人谢谢 共回答了21个问题 |采纳率90.5%二硫化碳 S::C::S 周围点满电子就是了~
一氧化二氮 N2O 这个电子式就纠结了 它里面有一个大π键
叠氮酸根~ 这个也有大π键...
如果广义上的等电子体的话 氰酸 H:O:C:::N(其余电子你自己来吧:))1年前查看全部
- 与磷酸根互为等电子体的粒子化学式为
 6pzhuzhu1年前1
6pzhuzhu1年前1 -
 devils-wang 共回答了10个问题
devils-wang 共回答了10个问题 |采纳率80%磷酸氢根,磷酸二氢根1年前查看全部
- 什么叫与O元素形成的某种单质互为等电子体的化合物
 夜叉乙1年前1
夜叉乙1年前1 -
 hill_dj 共回答了18个问题
hill_dj 共回答了18个问题 |采纳率94.4%一种粒子与O2或O3分子的总电子数相同1年前查看全部
- 由1到18号元素组成的微粒中,与NO3-(硝酸根)互为等电子体的微粒有?
 flydh1年前3
flydh1年前3 -
 sahara954 共回答了19个问题
sahara954 共回答了19个问题 |采纳率89.5%CO32-、SO31年前查看全部
- SF4的等电子体有哪些,最好有阴离子
 下雨的池塘1年前1
下雨的池塘1年前1 -
 lxmcql 共回答了20个问题
lxmcql 共回答了20个问题 |采纳率95%PF4^-1年前查看全部
- 等电子体究竟是什么概念?
 zhxil1年前1
zhxil1年前1 -
 xdhpp 共回答了18个问题
xdhpp 共回答了18个问题 |采纳率83.3%langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体.等电子体的结构相似、物理性质相近.
此后,等电子原理又有所发展.倒如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征.1年前查看全部
- 乙炔与一氧化碳算等电子体吗?
 zwj28226201年前4
zwj28226201年前4 -
 wjxm 共回答了20个问题
wjxm 共回答了20个问题 |采纳率100%是的.
等电子体指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团.
乙炔(C2H2)两个原子(不计氢原子),CO两个原子
乙炔10个价电子,CO也是10个1年前查看全部
- 氮气的等电子体我要的是阴离子 不是CO
 zspsbk1年前1
zspsbk1年前1 -
 LansingLuo 共回答了19个问题
LansingLuo 共回答了19个问题 |采纳率94.7%CN-;C22-1年前查看全部
- 一氧化碳的两种等电子体
 avgirl5201年前1
avgirl5201年前1 -
 laomo999 共回答了33个问题
laomo999 共回答了33个问题 |采纳率87.9%N2,CN-,C2^2-,NO^+1年前查看全部
- 下列各物质属于等电子体的是大神们帮帮忙
下列各物质属于等电子体的是大神们帮帮忙
下列各物质属于等电子体的是 A NO和O2 B.CO和N2 C.NO2和CO2 D.SO2和CL2 flychaochao1年前1
flychaochao1年前1 -
 drcd9 共回答了23个问题
drcd9 共回答了23个问题 |采纳率100%选B,原理:等电子体具有原子数目和电子数目相同的特征1年前查看全部
- 空间构型都是正四面体,原子数都为5,且原子最外层电子数之和都为34的几种等电子体,其中分子是 ,阴离子可以是 .它们的中
空间构型都是正四面体,原子数都为5,且原子最外层电子数之和都为34的几种等电子体,其中分子是 ,阴离子可以是 .它们的中心原子都采用的杂化方式是 .
 吸烟的北极熊1年前3
吸烟的北极熊1年前3 -
 ilovewasam 共回答了14个问题
ilovewasam 共回答了14个问题 |采纳率92.9%题绝对错了.最外层电子数应该是32 所以分子可能是SIF4 CCL4 离子可以是SO4-
中心原子杂化方式为sp3杂化1年前查看全部
- 为什么CH4和NH3不是等电子体?
 试着微微笑1年前1
试着微微笑1年前1 -
 nl1764 共回答了20个问题
nl1764 共回答了20个问题 |采纳率95%原子个数不同啊.1年前查看全部
- 与氮3负离子互为等电子体的离子
 cyywjr1年前2
cyywjr1年前2 -
 serqwetwt 共回答了19个问题
serqwetwt 共回答了19个问题 |采纳率68.4%等电子体指原子个数相同、价电子总数也相同的物质.你所说的氮3负有点歧义.
如果是[N]3-,则等电子体有[C]4-、[O]2-、F-、Na+、Mg2+、Al3+等,但这样的等电子体似乎没有意义(只有一个原子,不存在分子问题).
如果是叠氮酸根[N3]-,则等电子体有N2O、CO2等物质.1年前查看全部
- 高中化学常见的6电子体与十电子体?越详细越好.
 宿红尘1年前3
宿红尘1年前3 -
 w0auvkz 共回答了6个问题
w0auvkz 共回答了6个问题 |采纳率100%6电子体:C BeH2
10电子体:He F- O2- N3- OH- NH2- HF H2O NH3 CH4 Na+ Mg2+ Al3+ H3O+ NH4+1年前查看全部
- 高中化学、什么是等电子体?怎么判断?
 yuzhang01年前2
yuzhang01年前2 -
 beastfriend 共回答了24个问题
beastfriend 共回答了24个问题 |采纳率83.3%含有相同电子数的粒子比如NH3和CH41年前查看全部
- 等电子体PCl3和NF3是等电子体么?答案是YES 为什么呢?等电子体到底指核电荷数相同还是最外层电子数相同啊
 泡泡88泡泡1年前3
泡泡88泡泡1年前3 -
 april0922 共回答了18个问题
april0922 共回答了18个问题 |采纳率94.4%等电子体是具有相同的通式——AXm,而且价电子总数相等的分子或离子具有相同的结构特征,这个原理称为等电子体原理1年前查看全部
- 化学10电子等电子体都有哪些?
 seasoll1年前4
seasoll1年前4 -
 taurl 共回答了19个问题
taurl 共回答了19个问题 |采纳率100%化学式为C3H6的丙炔、环丙烯;亚硝酸HNO2;等等吧.C3H6(丙烯或环丙烷),CH3CHO乙醛,HCOOH甲酸,Cr铬原子 ,O3臭氧1年前查看全部
- N2与哪种阴离子互为等电子体
 qwfrwetgwer1年前2
qwfrwetgwer1年前2 -
 mdd796 共回答了24个问题
mdd796 共回答了24个问题 |采纳率91.7%C2^2-
CN-1年前查看全部
- N2与OH-是等电子体吗?
 望远万花筒镜_gg1年前1
望远万花筒镜_gg1年前1 -
 livandint 共回答了17个问题
livandint 共回答了17个问题 |采纳率94.1%不是.氮气14个电子,氢氧根10个.1年前查看全部
- 与二硫化碳互为等电子体的物质 什么叫等电子体
 T独钓寒江T1年前1
T独钓寒江T1年前1 -
 xygtq 共回答了12个问题
xygtq 共回答了12个问题 |采纳率75%原子数和价电子数分别相等的颗粒就是等电子体
CO21年前查看全部
- Na+和Ne是等电子体,为什么他们的第一电离能差别大(I(Ne)=21.6eV I(Na)=47.3eV)
Na+和Ne是等电子体,为什么他们的第一电离能差别大(I(Ne)=21.6eV I(Na)=47.3eV)
错了。I(Na+)=47.3eV写掉了 feaxg1年前2
feaxg1年前2 -
 阿嚏婆 共回答了17个问题
阿嚏婆 共回答了17个问题 |采纳率76.5%由于钠的正电性较强,对核外电子的吸引力比氖更强,想失去电子需要更多的能量,因此钠的第二电离能比氖的高.1年前查看全部
- 与一氧化碳分子互为等电子体的离子是什么?
 xyx33552321年前2
xyx33552321年前2 -
 yiyiyaner 共回答了16个问题
yiyiyaner 共回答了16个问题 |采纳率81.3%离子啊?CN- ,Cu+(亚铜离子),Zn2+1年前查看全部
- 十电子的等电子体有什么?离子,分子,几原的都行
 louisa_cy1年前3
louisa_cy1年前3 -
 谁比谁CJ7 共回答了20个问题
谁比谁CJ7 共回答了20个问题 |采纳率95%分子:甲烷,氨,水,氟化氢,氖
阴离子:氢氧根,氟离子,氨基氟离子,甲基负离子
阳离子:铝离子,镁离子,钠离子,铵根离子,水和氢离子
我给的是考试中常出现的,也是相对来说比较能稳定存在的1年前查看全部
- 在短周期元素组成的物质中,与硝酸根离子互为等电子体的分子有什么
 沈时行1年前3
沈时行1年前3 -
 w345722961 共回答了12个问题
w345722961 共回答了12个问题 |采纳率91.7%HNO3 SO21年前查看全部
- 跪求高二化学所有考到的十电子、14电子、18电子微粒包括分子离子 以及各种等电子体 望诸
跪求高二化学所有考到的十电子、14电子、18电子微粒包括分子离子 以及各种等电子体 望诸
跪求高二化学所有考到的十电子、14电子、18电子微粒包括分子离子 以及各种等电子体 望诸君垂助 不甚感激 waiwai19861年前3
waiwai19861年前3 -
 默默的游 共回答了25个问题
默默的游 共回答了25个问题 |采纳率88%10电子:分子Ne,HF,H2O,NH3,CH4;阳离子Na+,Mg2+,Al3+,H3O+,NH4+阴离子N3-,O2-,F-,OH-,NH2-
18电子:分子Ar,HCl,H2S,PH3,SiH4,F2,H2O2,C2H6,CH3OH,N2H4阳离子Ca2+,K+阴离子P3-,S2-,Cl-,HS-
14电子:N2,CO,C2H2
原子的个数在这里我不会改,你把它写作下标吧、、、、、、1年前查看全部
- 第一、二周期元素组成,与氧化性单质分子互为等电子体有那些
 F13801131年前3
F13801131年前3 -
 名法师甚21 共回答了19个问题
名法师甚21 共回答了19个问题 |采纳率89.5%N2、CO
O3、NO2-
F2、H2O2、C2H6、CH3NH2、N2H41年前查看全部
- 水分子的等电子体微粒有哪些
 畅响天下1年前3
畅响天下1年前3 -
 河边小肥羊 共回答了16个问题
河边小肥羊 共回答了16个问题 |采纳率93.8%电中性:
Ne、HF、NH3、CH4.
阴离子:
F-、O(2-)、N(3-)、C(4-)、OH-、NH2-、CH3-.
阳离子:
Na+、Mg(2+)、Al(3+)、Si(4+)、H3O+、NH4+、CH5+.
----
中学化学范围内常见的有:
Ne、HF、NH3、CH4、F-、OH-、Na+、Mg(2+)、Al(3+)、H3O+、NH4+.
水溶液体系离子中常见的有:
OH-、H3O+、NH4+.
熔盐体系离子中常见的有:
F-、O(2-)、Na+、Mg(2+)、Al(3+).
====
[原创回答团]1年前查看全部
- 环状结构BH(NH)3称为无机苯,它和苯是等电子体,问它的二氯代物有几种
 hds37911年前0
hds37911年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 环状结构(BHNH3)称为无机苯,他和苯都是等电子体
环状结构(BHNH3)称为无机苯,他和苯都是等电子体
无机苯的一氯代物的同分异构体共有几种?
不是只有一条对称轴吗
它的一氯代物是不是有4种 LSER4211年前2
LSER4211年前2 -
 青春何须解风情 共回答了18个问题
青春何须解风情 共回答了18个问题 |采纳率88.9%无机苯的一氯代物的同分异构体共有2种.
只有一条对称轴,但是有2种H,B-H 和 N-H ,所以有两种异构体.1年前查看全部
- CO与HF是等电子体吗
 byad5g71年前1
byad5g71年前1 -
 283637860 共回答了17个问题
283637860 共回答了17个问题 |采纳率94.1%不是,CO的价电子总数为10(C有4个,O有6个),HF的价电子总数为8(H有1个,F有7个),所以不是等电子体1年前查看全部
- 高中化学—关于等电子体做化学竞赛题的时候经常要用到等电子体的概念,可是我发现等电子体的“等”有时候是指电子总数相等,而有
高中化学—关于等电子体
做化学竞赛题的时候经常要用到等电子体的概念,可是我发现等电子体的“等”有时候是指电子总数相等,而有时候却又指价电子总数相等.由于没弄懂,做题时很郁闷,请高手指教. 枫之冥想1年前1
枫之冥想1年前1 -
 怦怦之声 共回答了18个问题
怦怦之声 共回答了18个问题 |采纳率88.9%这个要看题目具体要求,关于等电子体定义很混乱.但是只要你把常见的电子总数相等相同的与价电子总数相等的微粒背住,这种题并不难1年前查看全部
- 与NH3 BF3互为等电子体的分别是
 雪飘开天1年前1
雪飘开天1年前1 -
 zhangxing0610 共回答了24个问题
zhangxing0610 共回答了24个问题 |采纳率83.3%H3O+
CF3+1年前查看全部
大家在问
- 1一列火车通过一座长436米的大桥需要80秒,用同样的速度通过一长399的隧道要77秒.求这列火车的速度和长度
- 2(2011•长沙)墨西哥湾泄漏的原油目前已基本清理干净.在清理过程中,科学家们发现了几种神奇的能“吃油”的细菌,根据所学
- 3铝合金和碳素钢在一起会生锈吗我们定的是铝合金穿线盒和碳素钢管,安装公司说会有反应~真的是这样么~还有铝合金和镀锌钢管也会
- 4阅读下面一首宋词,然后回答后面的问题(8分)
- 5sometimes,l( )for( )after supper.
- 6若分式[1/3−x]的值为整数,则整数x=______或______.
- 7我的好朋友(二) 作文
- 8两个电阻的阻值分别是R1、R2,电路设置如图所示.
- 9已知盐水若干克,第一次加入一定量的水后,盐水浓度变成3%,第二次加入相同的水,盐水浓度变成2%.求第三次加入同样多的水后
- 10(2006•北京)如图所示的四种情景中,人对物体做功的是( )
- 11已知等差数列{a n }的公差d大于0,且a 2 ,a 5 是方程x 2 -12x+27=0的两根,数列{b n }的前
- 12----Rose gave up trying yewterday.----She____to have done th
- 13lim x趋近于正无穷 (1+2/x)^x=
- 14如图所示,过圆C外一点P做一条直线与圆C交于A,B两点,BA=2AP,PT与圆C相切于T点。已知圆C的半径为2,∠CAB
- 15关于x的方程2x^+3x-5m=0有两个小于1的实根,求m取值范围
