过氧化氯的气味如何除掉再详细帮我介绍一下过氧化氯的性质
 123chen1682022-10-04 11:39:543条回答
123chen1682022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 gknds 共回答了19个问题
gknds 共回答了19个问题 |采纳率94.7%- 过氧化氯
分子式:Cl2O2
结构式:Cl-O-O-Cl (由于氧的非金属性强,其中氯为+1价,氧为-1价,和过氧化氢结构很相似.)
过氧化氯一种极不稳定的过氧化物,氧化性极强且易爆,不能在有水或潮湿的情况下存在,常温就会逐渐分解.
Cl2O2+2H2O == 2HClO + H2O2
随后马上会发生氧化还原反应.
2HClO + H2O2 == Cl2↑ + O2↑ + 2H2O - 1年前
 海蛰皮 共回答了58个问题
海蛰皮 共回答了58个问题 |采纳率- 晒晒就行了
- 1年前
 tangfeng783418 共回答了8个问题
tangfeng783418 共回答了8个问题 |采纳率- 冒昧问一句,氧能和氯反应得到过氧化氯吗?没这东西的吧,如果有我真的是有点蛋疼了,是不是打错了呀?
- 1年前
相关推荐
- ClO2的命名为什么不叫过氧化氯而叫二氧化氯?怎么通过化学式区别那些被命名过氧化什么的东西?如CaO2,BaO2
 Sally_yu181年前3
Sally_yu181年前3 -
 y06350 共回答了12个问题
y06350 共回答了12个问题 |采纳率91.7%过氧化物中.过氧根离子的价态是-2 ClO2中,Cl不会是正二价的
一个氧,或多个氧,且氧是负二价的话叫氧化X
两个氧整体是负二价的话是过氧化X
两个氧整体是负一价的话是超氧化X
三个氧整体是负一价的话是臭氧化X1年前查看全部
- 氟利昂(主要成分是过氧化氯)是一种常见的制冷剂.氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如
氟利昂(主要成分是过氧化氯)是一种常见的制冷剂.氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如下: 
下列判断正确的是( )A.臭氧与氧气化学性质相同 B.经过①②③的反应后,氯原子的个数发生改变 C.反应①中的氯原子与反应③中的氯原子化学性质不同 D.少量的氟利昂就能对臭氧层产生巨大的影响  做你hh的uu1年前1
做你hh的uu1年前1 -
 怎么就那么虚伪 共回答了25个问题
怎么就那么虚伪 共回答了25个问题 |采纳率100%A、由两物质的分子模型,氧气分子由2个氧原子构成而臭氧分子由3个氧原子构成,两物质的分子构成不同导致两物质的化学性质不同,故A错误;
B、变化①中一个氯原子与一个氧原子形成一个一氧化氯分子,变化②中每两个一氧化氯分子结合成一个过氧化氯分子,变化③中每个过氧化氯分子又分解出两个氯原子,经过①②③的反应后,氯原子的个数不变,故B错误;
C、在变化前后,氯原子自身不发生改变,因此其个数及化学性质都没有改变,故C错误;
D、由微观图,氯原子与臭氧分子作用变成一氧化氯分子,每两个一氧化氯分子形成一个过氧化氯分子,过氧化氯分子分解出氯原子,在此变化过程中,氯原子在不断循环破坏着臭氧分子,起到了反应中的催化剂的作用,所以,少量的氟利昂就能对臭氧层产生巨大的影响,故D正确.
故选D.1年前查看全部
- 氟利昂主要成分有过氧化氯吗不是氟氯代烷吗,百科里并没有过氧化氯啊,可过氧化氯哪来的
 ken_1985011年前3
ken_1985011年前3 -
 cow198826 共回答了15个问题
cow198826 共回答了15个问题 |采纳率93.3%是的;氟利昂(主要成分是过氧化氯)是一种常见的制冷剂.氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层.【中学题目经常出现】
氟里昂,氟氯烃 英文:freon 几种氟氯代甲烷和氟氯代乙烷的总称 .氟里昂在常温下都是无色气体或易挥发液体,略有香味,低毒,化学性质稳定.其中最重要的是二氯二氟甲烷CCl2F2(F-12).二氯二氟甲烷在常温常压下为无色气体;熔点-158℃ ,沸点-29.8℃,密度1.486克/厘米(-30℃);稍溶于水,易溶于乙醇、乙醚;与酸、碱不反应.二氯二氟甲烷可由四氯化碳与无水氟化氢在催化剂存在下反应制得,反应产物主要是二氯二氟甲烷,还有CCl3F和CClF3,可通过分馏将CCl2F2分离出来.1年前查看全部
- 比如说,氯酸钾生成氧化钾和过氧化氯,即KCLO3——K2O+Cl2O2
比如说,氯酸钾生成氧化钾和过氧化氯,即KCLO3——K2O+Cl2O2
【首先说一下我的思路,
先按最小公倍数法,得出 2 KCLO3——K2O+Cl2O2
接下来就不知道怎么配了
因为氧气的数量总是左右不一致
比如现在左侧为6,右侧为3
如果在右侧增加倍数的话,相应地,在左侧也要增加倍数,而且必须是右侧的2倍(因为K2和Cl2)
这样的话感觉氧原子就永远达不到平衡】
以前也遇到过这样的问题,当时时间比较紧就留了下来,现在又碰到这个问题,
嗯……我只是举一个例子【猛然发现看错题目的某人←
因为以前也有碰到这样的题目,但是那个题目我现在找不到了……
就是如果碰到这种情况该怎么办?总不至于无解啊…… 胡欢洋1年前4
胡欢洋1年前4 -
 Arsen 共回答了22个问题
Arsen 共回答了22个问题 |采纳率77.3%既然是初中化学方程式,那就是用氯酸钾制取氧气了
KClO3→KCl+O2↑
在这个反应式中右边氧原子个数为2,左边是3,则最小公倍数为6,因此KClO3前系数应配2,O2前配3,式子变为:2KClO3→KCl+3O2↑,由于左边钾原子和氯原子数变为2个,则KCl前应配系数2,短线改为等号,标明条件即:
2KClO3==2KCl+3O2↑
氯酸钾加热二氧化锰生成氯化钾加氧气
--------------------------------------------------------------------------1年前查看全部
- 过氧化氯的化学式.
 精神契合1年前3
精神契合1年前3 -
 lvsedeyumao 共回答了24个问题
lvsedeyumao 共回答了24个问题 |采纳率87.5%就是二氧化氯ClO2
【二氧化氯介绍】
【中文名称】二氧化氯;亚氯酸酐;氯酸酐;过氧化氯
【英文名称】chlorine dioxide
【结构或分子式】ClO2
Cl原子以sp3杂化轨道形成σ键,分子为V形分子.[cl 原子以 SP2杂化轨道形成西格玛键 其中一个电子垂直于 o- CL-0 平面,并与 O=O 的4个电子形成 3原子 5电子 大派键(离域派键)]
【化合价】氯元素化合价为+4 氧元素化合价为-2
【相对分子量或原子量】67.46
【密度】3.09(11℃)
【熔点(℃)】-59
【沸点(℃)】111年前查看全部
- 明矾和ClO2 处理水明矾的作用是什么?过氧化氯作用是什么?
 还没睡醒的猫1年前1
还没睡醒的猫1年前1 -
 5201314jiu 共回答了21个问题
5201314jiu 共回答了21个问题 |采纳率81%明矾的作用是其中的铝水解生成氢氧化铝,吸附水中的杂质,净水
过氧化氯作用是+4价的氯有强氧化性,氧化水中的病毒,细菌等,是消毒杀菌的1年前查看全部
- 氟利昂(主要成分是过氧化氯)是一种常见的制冷剂.氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如
氟利昂(主要成分是过氧化氯)是一种常见的制冷剂.氟利昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如下:
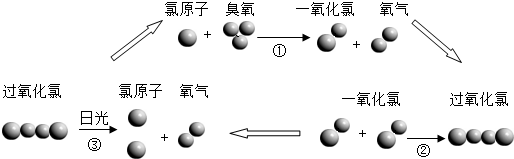
下列判断正确的是( )
A.臭氧与氧气化学性质相同
B.经过①②③的反应后,氯原子的个数发生改变
C.反应①中的氯原子与反应③中的氯原子化学性质不同
D.少量的氟利昂就能对臭氧层产生巨大的影响 fenglinbi1年前1
fenglinbi1年前1 -
 空空汝也 共回答了17个问题
空空汝也 共回答了17个问题 |采纳率94.1%解题思路:A、根据物质的结构与组成决定物质的性质,对比氧气与臭氧的分子构成,得出二者性质;
B、根据过程中氯原子的变化规律,对过程中氯原子的个数进行统计,判断过程中氯原子个数变化情况;
C、根据变化中氯原子的变化规律,判断循环过程中氯原子个数及结构没发生改变;
D、根据变化的微观图,分析循环过程中氯原子的转化关系,判断氯原子在循环过程中的作用.A、由两物质的分子模型,氧气分子由2个氧原子构成而臭氧分子由3个氧原子构成,两物质的分子构成不同导致两物质的化学性质不同,故A错误;
B、变化①中一个氯原子与一个氧原子形成一个一氧化氯分子,变化②中每两个一氧化氯分子结合成一个过氧化氯分子,变化③中每个过氧化氯分子又分解出两个氯原子,经过①②③的反应后,氯原子的个数不变,故B错误;
C、在变化前后,氯原子自身不发生改变,因此其个数及化学性质都没有改变,故C错误;
D、由微观图,氯原子与臭氧分子作用变成一氧化氯分子,每两个一氧化氯分子形成一个过氧化氯分子,过氧化氯分子分解出氯原子,在此变化过程中,氯原子在不断循环破坏着臭氧分子,起到了反应中的催化剂的作用,所以,少量的氟利昂就能对臭氧层产生巨大的影响,故D正确.
故选D.点评:
本题考点: 微粒观点及模型图的应用.
考点点评: 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.1年前查看全部
- 请问:CLO2是过氧化氯还是二氧化氯,如果是,是否代表这两者是同一样东西?如果不是,请问差别在哪里?两者的化学式分别是什
请问:
CLO2是过氧化氯还是二氧化氯,如果是,是否代表这两者是同一样东西?
如果不是,请问差别在哪里?两者的化学式分别是什么,其中氧和氯的化合价又是什么? 躺在海底的鱼1年前11
躺在海底的鱼1年前11 -
 叶子_2008 共回答了12个问题
叶子_2008 共回答了12个问题 |采纳率91.7%是二氧化氯
不是同一样东西
根本就没有过氧化氯这种东西,如果假设存在也不知道过氧化氯中氯的价态,不能推断化学式
氧的化合价是-2价,氯是+4价1年前查看全部
- (2008•松北区一模)实验室有下列仪器和氯酸钾、二氧化锰、稀硫酸、大理石、15%的过氧化氯溶液五种药品及蒸馏水、木块、
(2008•松北区一模)实验室有下列仪器和氯酸钾、二氧化锰、稀硫酸、大理石、15%的过氧化氯溶液五种药品及蒸馏水、木块、火柴等实验用品.

请回答下列问题:
(1)利用上述仪器和药品.可以制取的气体是______,用化学方程式表示制取该气体的化学反应原理2H2O2
2H2O+O2↑MnO2 .2H2O2制取该气体所选择的仪器是(填仪器序号)______,请画出制取该气体的装置图:
2H2O+O2↑MnO2 .
(2)在实验中,若用注射器代替长颈漏斗.其优点是______,换药品后,上述装置还可以制取的气体是______. 雪儿不回家1年前1
雪儿不回家1年前1 -
 zzos 共回答了21个问题
zzos 共回答了21个问题 |采纳率90.5%解题思路:(1)利用上述仪器和药品.可以制取的气体是氧气,如果制氧气只能是用双氧水制氧气,用氯酸钾制氧气需要铁架台,所给仪器中没有,制二氧化碳需用稀盐酸,所以只能制氧气;
(2)若用注射器代替长颈漏斗,可以控制反应的进行,如果换药品后还可以制取二氧化碳.(1)氯酸钾制氧气需要用到铁架台,而所给仪器中没有,制二氧化碳需要用到大理石和稀盐酸,所给药品中也没有,只能是用双氧水制氧气,先检查装置的气密性,再向锥形瓶中加入二氧化锰,从长颈漏斗口加入双氧水,待气泡连续均匀冒出再用向上排空气法收集.所以用到的仪器有:③④⑤⑥⑩.
(2)用注射器,可以控制反应速度,也可以控制反应的发生和停止,节约了药品.
故答案为(1)氧气,2H2O2
MnO2
.
2H2O+O2↑,③④⑤⑥⑩ ;
;
(2)控制反应速度,也可以控制反应的发生和停止,节约了药品;二氧化碳点评:
本题考点: 实验室制取气体的思路;制取气体的反应原理的探究;化学实验方案设计与评价;仪器的装配或连接;书写化学方程式、文字表达式、电离方程式.
考点点评: 利用所给的仪器和药品来制取气体时,首先考虑制取某种气体用到什么药品,所给药品中是否有,如果有了再考虑用到什么仪器,所给的仪器中是否都有,按照这样的思路考虑.1年前查看全部
大家在问
- 1五年级上册语文第六单元作文300字
- 2小学三年级300字的作文
- 3描写景物的四字词语
- 48小时突然停电,小明同时点燃两只同长短相同,但粗细不同的蜡烛.细蜡烛可以燃烧1小时,粗蜡烛可以燃烧2小
- 5形容非常舍不得的成语原题:即将离开母校步入中学的大门,请用上几个成语形容你此刻的心情,( )、( )、( )、( ).
- 6舍什么为什么的成语填入为反义词
- 7数学家的故事50字以内
- 8七年级下册的生物期末复习试卷(带答案)
- 9描写心情高兴的古诗谁的都行,过了明天不给分可不可以多一点?最好5个.追分如下:(除了《闻军官收河南河北》和《游山西村》)
- 10“收获喜悦”造句怎么造
- 11成语故事,描写比赛场面的成语
- 12欢乐怎么造句
- 13电势与电场强度的关系
- 14五年级上册语文第八单元作文:场面描写
- 15快乐怎么造句
