在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行
 6299842022-10-04 11:39:541条回答
6299842022-10-04 11:39:541条回答| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol•L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol•L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
| [NO2]2 |
| [N2O4] |
| [NO2]2 |
| [N2O4] |
c1______c2,c3______c4(填“>”、“<”或“=”).
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为______mol•L-1•s-1.
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是______(填字母序号).
A.扩大容器的容积B.再充入一定量的N2O4C.分离出一定量的NO2D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080mol NO2气体,则达到平衡时NO2气体的转化率为______.

已提交,审核后显示!提交回复
共1条回复
 xuzhh1314 共回答了24个问题
xuzhh1314 共回答了24个问题 |采纳率91.7%- 解题思路:(1)平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,根据方程式计算c2、c1,据此解答;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),依据化学反应速率V=[△c/△t]计算得到;
(3)依据化学平衡原理分析改变条件提高NO2转化率的选项;
(4)依据平衡浓度计算平衡常数,结合化学平衡三段式列式计算,转化率=[消耗量/起始量]×100%;(1)N2O4(g)⇌2NO2(g),反应的平衡常数K=
[NO2]2
[N2O4];
20s时c(NO2)=0.060mol/L
N2O4⇌2 NO2,
浓度变化 0.030mol 0.060mol/L
c1=0.10mol/L-0.03mol/L=0.070mol/L;
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4⇌2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c1;
故答案为:
[NO2]2
[N2O4];<;=;
(2)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
V(N2O4)=[0.060mol/L/60s]=0.001mol/(L•s);
故答案为:0.001;
(3)N2O4=2 NO2 反应是气体体积减小的放热反应,依据化学平衡原理分析选项,增大二氧化氮浓度的条件;
A、增大容器体积,各组分浓度均减小,故A错误;
B、再充入四氧化二氮,平衡正向移动,二氧化氮浓度增大,故B正确;
C、减小NO2的浓度,平衡虽正向进行,但二氧化氮的浓度减小,故C错误;
D、再充入一定量的He,总压增大,气体分压不变,平衡不变,二氧化氮浓度不变,故D错误;
故选B;
(4)依据平衡浓度计算平衡常数,结合化学平衡三段式列式计算;
N2O4⇌2 NO2,
起始量(mol/L) 0.10 0
变化量(mol/L) 0.06 0.12
平衡量(mol/L) 0.04 0.12
K=
0.122
0.04=0.36
若起始时充入N02气体0.080mol,设消耗二氧化氮物质的量浓度为x,2 NO2=N2O4 ,K=[1/0.36]
2 NO2=N2O4
起始量(mol/L) 0.0800 0
变化量(mol/L) x 0.5x
平衡量(mol/L) 0.080-x 0.5x
K=[0.5x
(0.080−x)2=
1/0.36]
x=0.020mol/L
则达到平衡时N02气体的转化率=[0.020/0.080]×100%=25%,
故答案为:25%.点评:
本题考点: 化学平衡的计算;化学平衡的影响因素.
考点点评: 本题考查化学平衡的有关计算、化学平衡的影响因素,题目综合性较大,注意基础知识的积累掌握. - 1年前
相关推荐
- 在约100℃的温度下,NaCl稀溶液中c(H + )=1.0×10 -6 mol·L -1 。下列说法中正确的是 [
在约100℃的温度下,NaCl稀溶液中c(H + )=1.0×10 -6 mol·L -1 。下列说法中正确的是 [ ]A.该溶液呈酸性
B.该溶液呈中性
C.该溶液的K W =1.0×10 -12
D.该溶液的K W =1.0×10 -14 dydydy20041年前1
dydydy20041年前1 -
 vanbao 共回答了15个问题
vanbao 共回答了15个问题 |采纳率93.3%BC1年前查看全部
- 水蒸气加热的温度最高可达( ) A.80℃ B.100℃ C.110℃ D.120℃
 efde1年前3
efde1年前3 -
 tn888 共回答了23个问题
tn888 共回答了23个问题 |采纳率91.3%B1年前查看全部
- 一个大气压下100℃的水蒸气冷凝为100℃的水所放出的热量是多少哦?
一个大气压下100℃的水蒸气冷凝为100℃的水所放出的热量是多少哦?
是不是为水蒸气的焓值减去水的焓值就可以了? sfyzry1年前1
sfyzry1年前1 -
 想恋爱的猫猫 共回答了19个问题
想恋爱的猫猫 共回答了19个问题 |采纳率94.7%如果是100度的水蒸气的焓值减去100度水的焓值就可以了.
水蒸气和水的比热可能不同,如果是常温下的焓值相减,可能不是很准确.1年前查看全部
- -请亲们帮我看看这道物理题.一个铝壶质量是500g,内装2000g20℃的水,要想使水温升高到100℃,则需要吸收多少热
-请亲们帮我看看这道物理题.
一个铝壶质量是500g,内装2000g20℃的水,要想使水温升高到100℃,则需要吸收多少热量? tanym1年前2
tanym1年前2 -
 o0宝宝0o 共回答了17个问题
o0宝宝0o 共回答了17个问题 |采纳率94.1%这种一道比热容的问题.首先要明白,水不但要吸热,而且铝壶也同样要吸收热量,可以将它们吸收的总的热量加起来就行了
得:Q吸=Q铝+Q水=C铝M铝.80℃+C水M水80℃计算出结果就行了,要注意的是质量的单位要化成KG.1年前查看全部
- 求化工原理达人~25.在套管换热器中热流体的温度有150℃降为100℃,冷流体的温度有50℃升为80℃,则逆流操作时对数
求化工原理达人~
25.在套管换热器中热流体的温度有150℃降为100℃,冷流体的温度有50℃升为80℃,则逆流操作时对数平均温差为 ℃,并流操作时对数平均温差为 ℃.
26.以精馏的方式分离液体混合物的基本原理是 .
27.组成为xF的苯-甲苯混合液体,经过部分汽化以后形成的饱和汽相组成为y,饱和液相组成为x.三个组成的大小顺序为 > > .
28.精馏塔进料的为饱和液体时热状况参数q= ,而为饱和汽体的热状况参数q= ,过冷液体的热状况参数q的范围是 ,过热蒸汽的热状况参数q的范围是 ,汽液两相的热状况参数q的范围是 .
29.在精馏塔计算中恒摩尔流假设是指 .
30.某精馏塔的进料流量为F、组成为xF,塔顶产品流量为D,组成为xD,塔顶产品流量为W,组成为xW.则全塔物料衡算方程式为 ,轻组分物料衡算方程式为 . 风雨后的山顶1年前1
风雨后的山顶1年前1 -
 混个屁 共回答了23个问题
混个屁 共回答了23个问题 |采纳率82.6%25逆流 (100-20)/ln(100/20)=49.7 并流(70-50)/ln(70/50)=59.44 约为60
26 挥发度的不同
27 y>xf>x
28 1,0 , q>1, q1年前查看全部
- 物态变化下列几种说法中,正确的是( )A 水的沸点一定是100℃B 水可以在80℃时沸腾C 水在100℃时一定沸腾D利用
物态变化
下列几种说法中,正确的是( )
A 水的沸点一定是100℃
B 水可以在80℃时沸腾
C 水在100℃时一定沸腾
D利用密闭加盖的容器可降低沸点
.把0℃的冰放进0℃的水中,若它们与外界不发生热传递,则( )
A 冰增多,水减少
B 冰多则水就会凝固;水多则冰就会熔化
C 冰和水的多少跟原来相同
D 冰会减少,水会增多 红魔九号1年前3
红魔九号1年前3 -
 crazyboy7 共回答了28个问题
crazyboy7 共回答了28个问题 |采纳率82.1%B对 其余错
首先,熔沸点是压强的一个函数,所以是受压强影响的~
所以AC 错 只要合理加减压强 就可以改变沸点的
D则错在 加盖以后,加热使气体膨胀,使容器内压强上升,导致沸点升高.其实可以类比我们的高压锅~
第二个:嗯嗯我认为是C
因为在0度的时候,冰和水组成的是冰水混合物,这个是可以共存的.
如果没有热交换的话,就可以认为外界没有输入能量,内部也没有给外部能量,那么便不会发生物态的变化.因为物态的变化也是要能量的,具体涉及到氢键的产生与断裂问题,是高中内容就不说了把……1年前查看全部
- 小星用燃气灶将质量为2㎏,温度为25℃的水加热到100℃,则水需要吸收多少热量?该燃气灶的热效率是25%,完全燃烧燃气的
小星用燃气灶将质量为2㎏,温度为25℃的水加热到100℃,则水需要吸收多少热量?该燃气灶的热效率是25%,完全燃烧燃气的质量为20g,则这种燃气的热值是多大
 dashan1101年前2
dashan1101年前2 -
 wlzjfz 共回答了19个问题
wlzjfz 共回答了19个问题 |采纳率94.7%Q=2*4200*75=6.3*10^5J
0.25Q=mq
q=0.25*6.3*10^5/0.02=7.875*10^6J/kg1年前查看全部
- 据说水的临界点是22.05mpa,374.3℃,那为什么烧水时的水100℃就沸腾变成气体了?
 chenrenhe1年前1
chenrenhe1年前1 -
 source975 共回答了27个问题
source975 共回答了27个问题 |采纳率81.5%任何一种物质都存在三种相态----气相、液相、固相.三相呈平衡态共存的点叫三相点.液、气两相呈平衡状态的点叫临界点.在临界点时的温度和压力称为临界温度和临界压力.不同的物质其临界点所要求的压力和温度各不相同.超临界流体(SCF)是指在临界温度和临界压力以上的流体.高于临界温度和临界压力而接近临界点的状态称为超临界状态.处于超临界状态时,气液两相性质非常接近,甚至趋于消失,液态和气态将无法分辨.
因此,水的沸点是T=100度,常压0.1013MPa, 超临界点才是22.05mpa, T=374.3℃, 你可以看到临界点的压力是非常特殊的.1年前查看全部
- 微分方程应用题问题已知物体在空气中冷却的速率与该物体及空气两者温度的差成正比.假设室温为20℃时,一物体由100℃冷却到
微分方程应用题问题
已知物体在空气中冷却的速率与该物体及空气两者温度的差成正比.假设室温为20℃时,一物体由100℃冷却到60℃需经过20分钟,问需经过多长时间才能使此物体的温度从100℃降到30℃?(请用微分方程的方法解答) pentium8881年前1
pentium8881年前1 -
 ly5990 共回答了17个问题
ly5990 共回答了17个问题 |采纳率88.2%设该曲线为y=f(x)
曲线的切线方程是y-f(x.)=f'(x.)(x-x.) 即y=f'(x.)(x-x.) +f(x.)
由题意可得到 x.=-x.f'(x.)+f(x.) 问题转化为求微分方程的解,为了方便我把
该微分方程写成 x=-xdy/dx+y的形式 可写成dy/dx=y/x -1
设z=y/x ,则y=zx ,dy/dx=z+xdz/dx=y/x-1=z-1
xdz/dx=-1 分离变量 dz=-dx/x 两边积分,得 z=-lnx+C=y/x
y=x(C-lnx) 曲线经过点(1,1)代人,得 y=x(1-lnx)1年前查看全部
- 已知在100℃的温度下(本题涉及的溶液其温度均为100℃,水的离子积 K W =1.0×10 - 12 mol 2 ·L
已知在100℃的温度下(本题涉及的溶液其温度均为100℃,水的离子积 K W =1.0×10 - 12 mol 2 ·L - 2 。下列说法中正确的是
A.0.05 mol·L - 1 的H 2 SO 4 溶液,pH=1 B.0.001 mol·L - 1 的NaOH溶液,pH=11 C.0.005 mol·L - 1 的H 2 SO 4 溶液与0.01 mol·L - 1 的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性 D.完全中和pH=3的H 2 SO 4 溶液50 mL,需要pH=11的NaOH溶液50 mL  ifshiba1年前1
ifshiba1年前1 -
 kittyy 共回答了16个问题
kittyy 共回答了16个问题 |采纳率100%A
A:c(H + )=0.1mol/L,pH=—lg c(H + )=1
B:c(OH — )=0.001mol/L,c(H + )=1.0×10 - 9 mol/L,pH=—lg c(H + )=9
C:两者恰好中和,混合溶液的pH=6,溶液呈中性。
D:酸提供的n(H + )=1.0×10 - 3 ×0.05,碱提供的n(OH — )=1.0×10 - 1 ×V,可得V="0.5" mL1年前查看全部
- 100℃时,纯水的离子积等于一乘十的负十二次方,则此时纯水的氢离子为多少?此时纯水是否仍为中性?
 爬上珠峰的蚯蚓1年前2
爬上珠峰的蚯蚓1年前2 -
 CH166 共回答了12个问题
CH166 共回答了12个问题 |采纳率91.7%纯水里只有氢正离子和氢氧根负离子,所以氢离子浓度=氢氧根离子浓度=离子积开根号=10^-6.
水还是中性,因为氢离子浓度=氢氧根离子浓度.
不要被温度欺骗了哟1年前查看全部
- 实验时,水的沸点大都不是100℃的原因有哪些 ?
 唇离1年前1
唇离1年前1 -
 eath 共回答了14个问题
eath 共回答了14个问题 |采纳率71.4%没达到标准大气压1年前查看全部
- 把5kg水从20℃加热到100℃,水需要吸收的热量是多少?小明家以前烧煤气,现在改烧天然气,每立方米天然气的价格接近煤气
把5kg水从20℃加热到100℃,水需要吸收的热量是多少?小明家以前烧煤气,现在改烧天然气,每立方米天然气的价格接近煤气的两倍,但小明发现每月的燃料费用并没有增多.请你帮他简要分析其中原因.
 薛181年前1
薛181年前1 -
 杨斌668 共回答了21个问题
杨斌668 共回答了21个问题 |采纳率81%解题思路:(1)知道水的质量、水的比热容、水温的升高值,利用吸热公式求水吸收的热量;
(2)由Q=vq可知,当需要的热量一定时,天然气的热值大,需要天然气的体积少,但是天然气价格贵,据此分析原因.(1)水吸收的热量:
Q吸=cm△t
=4.2×103J/(kg•℃)×5kg×(100℃-20℃)
=1.68×106J;
答:水需要吸收的热量是1.68×106J;
(2)改烧天然气,因为天然气的热值大,在提供相同的热量(Q=qv)情况下,需要的天然气的体积少,但是天然气的价格高,所以总算起来支出费用并没增多.点评:
本题考点: 热量的计算;燃料的热值.
考点点评: 本题考查了热量的计算,涉及到利用燃料燃烧放热公式Q=vq对两种能源的使用比较,与实际生活相联系,提高了学生利用所学知识解释实际问题的能力.1年前查看全部
- 有一电热水壶,铭牌如表所示。现将质量为1kg、温度为20℃的一壶冷水,加热到100℃。求:
有一电热水壶,铭牌如表所示。现将质量为1kg、温度为20℃的一壶冷水,加热到100℃。求:
(1)水吸收的热量是多少?[水的比热容为4.2×10 3 J/(kg·℃)]
(2)若不计热量损失,电热水壶需正常工作多长时间?
 amei1231年前1
amei1231年前1 -
 xx6606 共回答了16个问题
xx6606 共回答了16个问题 |采纳率100%(1)水吸收的热量Q 吸 = cm(t - t 0 )= 4.2×10 3 J/(kg·℃)×1kg×(100℃-20℃)=3.36×10 5 J;
(2)需消耗的电能W= Q 吸 =3.36×10 5 J,电水壶正常工作所需时间t = W / P = 3.36×10 5 J / 1500W = 224s。1年前查看全部
- 下列试验能构成事件的是( )A. 掷一次硬币B. 射击一次C. 标准大气压下,水烧至100℃D. 摸彩票中头奖
 luwei01101年前1
luwei01101年前1 -
 尊贵假面 共回答了11个问题
尊贵假面 共回答了11个问题 |采纳率81.8%解题思路:由题意知本题要判断哪一个是一个事件,根据事件可以分为必然事件、随机事件和不可能事件,判断A,B,C三个选项不能划分为三种事件中的任意个.由题意知本题要判断哪一个是一个事件,
事件是在一定条件下所出现的某种结果
根据事件可以分为必然事件、随机事件和不可能事件,
A,B,C三个选项不能划分为三种事件中的任意个,
故选D.点评:
本题考点: 随机事件.
考点点评: 本题考查事件,所谓事件,实际上就是在一定条件下所出现的某种结果.在一定条件下必然发生的事件,叫做必然事件.在一定条件下不可能发生的事件,叫做不可能事件.随机事件在一定的条件下可能发生也可能不发生的事件,叫做随机事件.1年前查看全部
- 下列说法正确的是( ) A.100℃时PH=2的盐酸与PH=12的KOH的体积混合,混合后的溶液为中性 B.对于0.
下列说法正确的是()
A.100℃时PH=2的盐酸与PH=12的KOH的体积混合,混合后的溶液为中性 B.对于0.1mol/L的NH 4 Cl溶液,温度不变,则 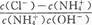 的比值不变
的比值不变C.丙烷分子的比例模型为: 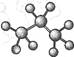
D.碱性氧化物由金属元素和氧元素组成,MgO、K 2 O、Na 2 O 2 、Mn 2 O 7 、Fe 2 O 3 中有四种为碱性氧化物  悠悠草草1年前1
悠悠草草1年前1 -
 stonexinqun 共回答了21个问题
stonexinqun 共回答了21个问题 |采纳率71.4%B
100℃是水的离子积常数是1×10 - 12 ,所以pH=12的氢氧化钾溶液的浓度是1.0mol/L,依次在反应中氢氧化钾是过量的,溶液显碱性,A不正确。C不正确,总是球棍模型。能和酸反应生成盐和水的氧化物是碱性氧化物,过氧化钠和酸反应还有氧气生成,不是碱性氧化物。Mn 2 O 7 是酸性氧化物,D不正确。所以正确的答案是B。1年前查看全部
- 已知100℃时,Kw=1*10-12,在该温度下,将100ml 0.001mol/L的NaOH溶液加水稀释至1L,则该溶
已知100℃时,Kw=1*10-12,在该温度下,将100ml 0.001mol/L的NaOH溶液加水稀释至1L,则该溶液的pH为
 被宠坏的丫头1年前3
被宠坏的丫头1年前3 -
 weixiaodeyuff 共回答了26个问题
weixiaodeyuff 共回答了26个问题 |采纳率88.5%实验室制法
1、利用铜盐如CuSO4与碱(NaOH)反应生成Cu(OH)2 ,再将 Cu(OH)2 加热分解以制得CuO.
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4
Cu(OH)2=△=CuO+H2O
2、加热铜(Cu),使铜与氧气(O2)反应生成氧化铜(CuO).
2Cu+O2==2CuO
3、氧化铜可由金属铜在空气中加热,或者加热分解氢氧化铜、硝酸铜、碱式碳酸铜 等而制得:1年前查看全部
- 在质量是0.5kg的铝壶里装有2kg水,把这壶水从10℃加热到100℃,需要完全燃烧多少千克无烟煤?
在质量是0.5kg的铝壶里装有2kg水,把这壶水从10℃加热到100℃,需要完全燃烧多少千克无烟煤?
铝的比热容为0.88×10^3J/(kg.℃)
水的比热容为4.2*10^3J/(kg.C)
无烟煤的热值为3.4*10^73 J.kg apple_sky1年前5
apple_sky1年前5 -
 狮子不笨 共回答了10个问题
狮子不笨 共回答了10个问题 |采纳率80%铝吸热=0.88*10^3*0.5*(100-10)=3.96*10^4
水吸热=2*4.2*10^3*(100-10)=7.56*10^5
设烧x千克煤
煤燃烧放热=水吸热+铝吸热
3.4*10^7*x=3.96*10^4+7.56*10^5
3.4x=0.00396+0.0756
x=0.0234kg1年前查看全部
- (2011•河北区二模)在温度不变时,从100℃KNO3饱和溶液中去除10g溶液,剩余溶液与原溶液相比,没有变化的是(
(2011•河北区二模)在温度不变时,从100℃KNO3饱和溶液中去除10g溶液,剩余溶液与原溶液相比,没有变化的是( )
A.溶质的质量
B.溶剂的质量
C.溶解度
D.溶液的体积 活出自己的精彩1年前1
活出自己的精彩1年前1 -
 cookingoo 共回答了21个问题
cookingoo 共回答了21个问题 |采纳率81%解题思路:影响固体物质溶解度大小的因素有外因和内因,内因是指溶质的性质和溶剂的性质,外因是温度;所以温度是影响溶解度大小的重要因素.由题意,在温度不变时,从100℃KNO3饱和溶液中去除10g溶液,剩余溶液与原溶液相比,溶解度没有变化.
A、溶质的质量减少,故不符合题意;
B、溶剂的质量减少,故不符合题意;
C、溶解度没有变化,故符合题意;
D、溶液的体积减少,故不符合题意.
故选:C.点评:
本题考点: 固体溶解度的概念.
考点点评: 本题难度不大,是对溶解度影响因素的考查,注意固体物质的溶解度受温度、溶剂和溶质性质的影响,与当前溶液是否处于饱和、溶剂的多少无关.1年前查看全部
- 下列说法正确的是( )A.水沸腾时,温度一定是100℃B.物体温度升高,它一定吸收了热量C.走进鲜花店就可以闻到花香,
下列说法正确的是( )
A.水沸腾时,温度一定是100℃
B.物体温度升高,它一定吸收了热量
C.走进鲜花店就可以闻到花香,这是气体的扩散现象
D.将暂时不吃的蔬菜放入冰箱冷藏,是为了加快蒸发 bailangduo11年前1
bailangduo11年前1 -
 traciehua2006 共回答了20个问题
traciehua2006 共回答了20个问题 |采纳率90%解题思路:A、在一大气压下,水的沸点是100℃,水的沸点随气压的增大而增大;
B、物体温度升高,内能增加,做功与热传递是改变物体内能的两种方式;
C、组成物质是分子不停地做无规则运动;
D、在低温条件下蔬菜的呼吸作用减弱.A、在一大气压下,水的沸点是100℃,水的沸点随气压的增大而增大,水的沸腾温度不一定都是100℃,故A错误;
B、物体温度升高,可能是吸收了热量,也可能是外界对物体做了功,故B错误;
C、走进鲜花店就可以闻到花香,这是气体的扩散现象,故C正确;
D、将暂时不吃的蔬菜放入冰箱冷藏,是为了减弱其呼吸作用,故D错误;
故选C.点评:
本题考点: 沸腾及沸腾条件;影响蒸发快慢的因素;温度、热量与内能的关系;扩散现象.
考点点评: 本题是一道基础题,掌握基础知识即可正确解题.1年前查看全部
- 将标准大气压下正在沸腾的水拿到标准大气压100℃的房间中水是否会继续沸腾?为什么?
 幽蓝若冰1年前1
幽蓝若冰1年前1 -
 烟波至爽 共回答了18个问题
烟波至爽 共回答了18个问题 |采纳率100%解题思路:液体沸腾的条件:温度达到沸点,并且不断吸热,二者缺一不可.答:水不会继续沸腾.标准气压下水的沸点是100℃,但到房间中,应为与房间温度相同不能继续吸热,所以不会再沸腾.
点评:
本题考点: 沸点及沸点与气压的关系;沸腾及沸腾条件.
考点点评: 本题考查了沸腾的条件以及沸点与气压的关系,知道沸腾的两个必要因素是解题的关键.1年前查看全部
- 在一个大气压下,1kg 100℃的水变为1kg 100℃的水蒸气的过程,下列说法中正确的是( )
在一个大气压下,1kg 100℃的水变为1kg 100℃的水蒸气的过程,下列说法中正确的是( )
A.内能不变,对外界做功,一定是吸热过程
B.内能增加,吸收的热量等于内能的增加
C.内能不变,吸收的热量等于对外界做的功
D.内能增加,从外界吸热,吸收的热量等于对外界做的功和增加的内能 猫米鱼1年前1
猫米鱼1年前1 -
 phhgg 共回答了15个问题
phhgg 共回答了15个问题 |采纳率86.7%解题思路:温度是分子平均动能的标志,温度不变平均动能不变,水变成同温度的水蒸气的过程要吸收热量,平均动能不变,分子势能增加,水变成同温度的水蒸气的过程要对外做功.根据热力学第一定律分析.温度是分子平均动能的标志,温度不变平均动能不变.100℃的水变成同温度的水蒸气的过程要吸收热量,平均动能不变,内能增加.
由于要对外做功,所以根据热力学第一定律可知所吸收的热量等于对外界做的功和物体内能的增加量,故ABC错误,D正确.
故选:D点评:
本题考点: 热力学第一定律.
考点点评: 本题考查了温度是分子平均动能的标志,热力学第一定律的公式应用.也可以根据能量守恒定律理解.1年前查看全部
- 高中化学:100℃下,PH=8的氢氧化钡与PH=5的盐酸混合后恰好中和,两者体积比是?
高中化学:100℃下,PH=8的氢氧化钡与PH=5的盐酸混合后恰好中和,两者体积比是?
可不可以用中和那么算,就是H离子等于OH离子浓度?而不用Kw 忆苦的薄荷1年前1
忆苦的薄荷1年前1 -
 szgood9 共回答了17个问题
szgood9 共回答了17个问题 |采纳率82.4%100℃时,水的离子积为1×10^-12,PH=6时为中性
PH=8的氢氧化钡溶液C(OH-)=1×10^-4
PH=5的稀盐酸C(H+)=1×10^-5
混合后PH=7,即呈碱性,
设二者体积分别为V1、V2,则
V1×1×10^-4 - V2×1×10^-5=1×10^-5×(V1+V2)
v1:v2=2:91年前查看全部
- 在100℃时,将0.100mol的四氧化二氮气体充入1L抽空的密闭容器中.隔一定时间对该容器内的物质浓度进行分析得到如下
在100℃时,将0.100mol的四氧化二氮气体充入1L抽空的密闭容器中.隔一定时间对该容器内的物质浓度进行分析得到如下表数据:
时间(S) 0 20 40 60 80
c(N2O4)/mol/L 0.100 a 0.050 c d
c(NO2)/mol/L 0.000 0.06 b 0.120 0.120
(1).20s时N2o4浓度a=( ) ;在0-20s内N2O4的平均反应速率为( );
表中b()c()d (填>.<.= )
(2.)该反应到达平衡时N2O4的转化率为( ) 平衡时容器内压强与开始时压强之比是() 衔杯袒腹1年前2
衔杯袒腹1年前2 -
 ay2137 共回答了23个问题
ay2137 共回答了23个问题 |采纳率82.6%一个N2O4可逆变成两个NO2,20S时产生NO2 0.06mol/l,
因此消耗N2O4 0.03mol/l.还剩0.07mol/l.即a=0.07,同理b=0.1,c=d=0.04.
然后根据各个问的定义进行计算即可.1年前查看全部
- 科学家最近在-100℃的低温下合成一种烃X,此分子的模型如图(图中的连线表示化学键),下列说法正确的是
科学家最近在-100℃的低温下合成一种烃X,此分子的模型如图(图中的连线表示化学键),下列说法正确的是

A.X分子中在同一平面上的碳原子最多有5个 B.X是一种在常温下能稳定存在的液态烃 C.X能使溴的四氯化碳溶液褪色 D.充分燃烧等质量的X和甲烷,X消耗氧气多  charliezhu011年前1
charliezhu011年前1 -
 情人节不哭 共回答了15个问题
情人节不哭 共回答了15个问题 |采纳率93.3%1年前查看全部
- 理想气体内能决定因素?0℃冰和水的内能哪个大?100℃水和水蒸气内能哪个大?
 云游儿1年前1
云游儿1年前1 -
 还珠丫环 共回答了20个问题
还珠丫环 共回答了20个问题 |采纳率90%小家伙,学热学呢吧.理想气体的内能由分子总动能和分子势能共同决定.理想气体分子势能不考虑(因为分子间距大于10r0),所以内能由分子总动能决定.分子总动能决定于分子个数和分子的平均动能,宏观表现为由气体温度决定...1年前查看全部
- 在研究水的升温特性过程中,小明在烧杯中注入200g的水,用酒精灯给烧杯加热,在水温由20℃上升至100℃的过程中,水的内
在研究水的升温特性过程中,小明在烧杯中注入200g的水,用酒精灯给烧杯加热,在水温由20℃上升至100℃的过程中,水的内能增加了 J,水吸收的热量 (选填“大于”、“小于”或“等于”)酒精燃烧所放出的热量。[ c 水 = 4.2×10 3 J/(kg·℃)]
 光光荣1年前1
光光荣1年前1 -
 渔有财1 共回答了16个问题
渔有财1 共回答了16个问题 |采纳率93.8%解题思路:在研究水的升温特性过程中,小明在烧杯中注入
200g 的水,用酒精灯给烧杯加热,在水温由20 ℃上升至100 ℃的过程中,水增加的内能是Q=cmt=4.2×103J/(kg⋅℃)×0.2kg×(100℃−20℃)=6.72×104J, 酒精放出的热量没有都被水吸收,所以水吸收的热量小于酒精燃烧所放出的热量。
6.72×10 4 小于
1年前查看全部
- 质量为200g的水,温度由100℃降低到40℃,放出的热量是多少焦?【c 水 =4.2×10 3 J/(kg•℃)】.
 贱客也是客1年前1
贱客也是客1年前1 -
 会飞的星期一 共回答了21个问题
会飞的星期一 共回答了21个问题 |采纳率85.7%Q 放 =cm△t=cm(t 0 -t)
=4.2×10 3 J/(kg•℃)×0.2kg×(100℃-40℃)
=5.04×10 4 J.
答:水放出的热量是5.04×10 4 J.1年前查看全部
- 一滴100℃的开水比一大杯100℃的开水内能
 egriasword1年前1
egriasword1年前1 -
 jkbl127 共回答了22个问题
jkbl127 共回答了22个问题 |采纳率72.7%答案:小 温度相同时,质量越大,内能越大1年前查看全部
- 求解一道英语完成句子题.If______(加热)100℃,water will change into steam.(h
求解一道英语完成句子题.
If______(加热)100℃,water will change into steam.(heat)
(it is) heated to
而我写的是:being heated to 像这样写问题出在哪呢? USHls1年前1
USHls1年前1 -
 askpan 共回答了16个问题
askpan 共回答了16个问题 |采纳率81.3%if引导条件状语从句,这个句子其实是省略句.前面的从句的主语是water,答案给出(it is) heated to是正确的,括号里的内容是可以省略的.这里不能用being.1年前查看全部
- 下列事件中,必然发生的是 A.某射击运动射击一次,命中靶心 B.通常情况下,水加热到100℃时沸腾 C.掷一次骰子,向上
下列事件中,必然发生的是
A.某射击运动射击一次,命中靶心 B.通常情况下,水加热到100℃时沸腾 C.掷一次骰子,向上的一面是6点 D.抛一枚硬币,落地后正面朝上  马尔代夫啊1年前1
马尔代夫啊1年前1 -
 心純如水 共回答了17个问题
心純如水 共回答了17个问题 |采纳率94.1%B
A、某射击运动射击一次,命中靶心,随机事件;B、通常加热到100℃时,水沸腾,是必然事件.C、掷一次骰子,向上的一面是6点,随机事件;D抛一枚硬币,落地后正面朝上,随机事件;故选B.1年前查看全部
- (2013•南通模拟)小明为了测量天然气炉具烧水的效率,他用天然气炉将5kg的20℃水加热至100℃时,用时24min,
(2013•南通模拟)小明为了测量天然气炉具烧水的效率,他用天然气炉将5kg的20℃水加热至100℃时,用时24min,消耗了0.14m3的天然气.(天然气的热值为4.0×107J/m3,设天然气能完全燃烧)求:
(1)水吸收的热量;[c水=4.2×103J/(kg•℃)]
(2)天然气完全燃烧放出的热量;
(3)天然气炉具烧水的效率. 龙龙5岁1年前1
龙龙5岁1年前1 -
 zy800006 共回答了21个问题
zy800006 共回答了21个问题 |采纳率85.7%解题思路:(1)知道水的质量、水的初温和末温、水的比热容,利用吸热公式求水吸收的热量(有用能量);
(2)知道使用天然气的体积和天然气的热值,利用燃料完全燃烧放热公式求天然气完全燃烧放出的热量(总能量);
(3)利用效率公式求天然气炉具烧水的效率.(1)水吸收的热量:
Q吸=cm(t-t0)
=4.2×103J/(kg•℃)×5kg×(100℃-20℃)
=1.68×106J;
(2)天然气完全燃烧时放出的热量:
Q放=qV
=4.0×107J/m3×0.14m3
=5.6×106J;
(3)天然气炉具的效率:
η=
Q吸
Q放=
1.68×106J
5.6×106J=30%.
答:(1)水吸收的热量为1.68×106J;
(2)天然气完全燃烧放出的热量为5.6×106J;
(3)天然气炉具烧水的效率为30%.点评:
本题考点: 热量的计算;能量利用效率;燃料的热值.
考点点评: 本题考查了学生对吸热公式、燃料完全燃烧放热公式、效率公式的掌握和运用,注意:固体和液体的热值单位为J/kg,气体燃料的热值单位为J/m3.1年前查看全部
- 小星用燃气灶将质量为2㎏,温度为25℃的水加热到100℃,则水需要吸收多少热量?该燃气灶的热效率是25%,则加热这些水需
小星用燃气灶将质量为2㎏,温度为25℃的水加热到100℃,则水需要吸收多少热量?该燃气灶的热效率是25%,则加热这些水需要燃气多少千克?______.(燃气的热值是4.5×10 7 J/㎏)  uvstopme1年前1
uvstopme1年前1 -
 vonkuechler 共回答了14个问题
vonkuechler 共回答了14个问题 |采纳率78.6%(1)水吸收的热量Q 吸 =cm 1 (t-t 0 )
=4.2×10 3 J/(Kg•℃)×2Kg×(100℃-25℃)
=6.3×10 5 J.
(2)燃气完全燃烧时放出的热量 Q 放 =
Q 吸
25% =
6.3× 10 5 J
0.25 =2.52×1 0 6 J ;
燃气的质量 m 2 =
Q 放
q =
2.52× 10 6 J
4.5× 10 7 J/Kg =0.056Kg .
答:水吸收的热量是6.3×10 5 J,需要燃气0.056㎏.1年前查看全部
- (801九•孝感)下列事件:①随意翻到一本书的某页,这页的页码是奇数;②测得某天的最高气温是100℃;③掷一次骰子,向上
(801九•孝感)下列事件:
①随意翻到一本书的某页,这页的页码是奇数;
②测得某天的最高气温是100℃;
③掷一次骰子,向上一面的数字是8;
④度量四边形的内角和,结果是at0°.
其中是随机事件的是______.(填序号) applworm1年前1
applworm1年前1 -
 为什么没有爱 共回答了16个问题
为什么没有爱 共回答了16个问题 |采纳率75%解题思路:随机事件就是可能发生也可能不发生的事件,依据定义即可判断.①是随机事件;
②是不可能事件;
③是随机事件;
④是必然事件.
故答案是:①③.点评:
本题考点: 随机事件.
考点点评: 本题考查了必然事件的定义,解决本题需要正确理解必然事件、不可能事件、随机事件的概念.必然事件指在一定条件下一定发生的事件.不可能事件是指在一定条件下,一定不发生的事件.不确定事件即随机事件是指在一定条件下,可能发生也可能不发生的事件.1年前查看全部
- 在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如表格:
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如表格:
试填空:时间/s
浓度mol•L-10 20 40 60 80 100 c(N2O4)mol•L-1 0.100 c1 0.050 c3 a b c(NO2)/mol•L-1 0.000 0.060 c2 0.120 0.120 0.120
(1)达到平衡时N2O4的转化率为______%,表中c2______c3,a______b (选填“>”“<”“=”).
(2)20s的四氧化二氮的浓度c1=______mol•L-1,在0s~20s内四氧化二氮的平均反应速率为______mol•(L•s)-1.
(3)若在相同情况下最初向该容器充入的是二氧化氮气体要达到上述同样的平衡状态,二氧化氮的起始浓度是______mol•L-1. yueliang5201年前1
yueliang5201年前1 -
 杨念 共回答了22个问题
杨念 共回答了22个问题 |采纳率90.9%解题思路:(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;
根据方程式计算,计算c2、c3,据此解答;
60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);
根据v=[△c/△t]计算v(N2O4).
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为[0.06mol/L/0.1mol/L]×100%=60%;
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4⇌2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c3;
60s后反应达平衡,反应混合物各组分的浓度不变,所以a=b.
故答案为:60;>;=
(2)由表可知,20s时,c(NO2)=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=[0.03mol/L/20s]=0.0015mol•(L•s)-1.
故答案为:0.07mol/L;0.0015mol•(L•s)-1.
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.
所以 N2O4⇌2 NO2,
0.1mol/L 0.20mol/L
故答案为:0.20mol/L点评:
本题考点: 化学平衡的计算.
考点点评: 考查化学平衡的有关计算、等效平衡等,难度中等,注意基础知识的积累掌握.1年前查看全部
- 液压油做抗老化实验,高温和低温分别做多少度合适呢?高温:100℃,低温-8℃,这个可以吗?
 天天向上的我1年前1
天天向上的我1年前1 -
 hh小猪的翅膀 共回答了17个问题
hh小猪的翅膀 共回答了17个问题 |采纳率76.5%只需要做一个高温,高温都不老化,低温当然也没老化的可能了.
液压油的低温性能应该主要是黏度了,高温下才是考验氧化性能的.
建议参考 GB/T12581-1990加抑制剂矿物油的氧化特性测定法,里面对试验方法有详细介绍.1年前查看全部
- 关于物理比热容质量为0.2kg的金属壶中盛有1.5kg的水,把它们从10℃加热到100℃,共需580000J的热量,则该
关于物理比热容
质量为0.2kg的金属壶中盛有1.5kg的水,把它们从10℃加热到100℃,共需580000J的热量,则该金属的比热容多大? 3464736seg1年前2
3464736seg1年前2 -
 63504513yu 共回答了27个问题
63504513yu 共回答了27个问题 |采纳率100%水吸收的热量Q水=c1m1Δt=4.2*10^3*1.5*(100-10)=567000J
金属壶吸收的热量Q壶=Q总-Q水=580000-567000=13000J
由Q=cmΔt可知该金属的比热容为
c2=Q壶/(m2Δt)=13000/0.2*90≈0.72*10^3J/kg.℃1年前查看全部
- 有H2和O2的混合气体aL,经点火反应后,其体积减小为bL,(反应前后气体体积是在同温,同压下测定,且在100℃以下).
有H2和O2的混合气体aL,经点火反应后,其体积减小为bL,(反应前后气体体积是在同温,同压下测定,且在100℃以下).计算混合气体中H2和O2各多少升?
 曾凡新dd1年前3
曾凡新dd1年前3 -
 cxf66766 共回答了19个问题
cxf66766 共回答了19个问题 |采纳率89.5%两种情况
1:氧气过量,则剩余为氧气
参加反应的气体体积比为2:1
所以H2体积为2(a-b)/3,氧气体积为b+(a-b)/3=(a+2b)/3
2:H2过量,则剩余为H2
因为参加反应的气体体积比为2:1
所以O2体积为(a-b)/3,H2体积为b+2(a-b)/3=(2a+b)/31年前查看全部
- 将一壶质量为2kg,初温为25℃的水加热到100℃,需要吸收多少J的热量?[水的比热容为4.2×10 3 J/(kg℃)
将一壶质量为2kg,初温为25℃的水加热到100℃,需要吸收多少J的热量?[水的比热容为4.2×10 3 J/(kg℃)].  茸茸1121年前1
茸茸1121年前1 -
 asdgkljawgkjrsth 共回答了23个问题
asdgkljawgkjrsth 共回答了23个问题 |采纳率95.7%水吸收的热量:Q 吸 =cm(t-t 0 )=4.2×10 3 J/(kg℃)×2kg×(100℃-25℃)
=6.3×10 5 J.
答:水吸收的热量是6.3×10 5 J.1年前查看全部
- 质量为2Kg的水,温度从100℃降低到20℃时,放出的热量是多少?这些热量可以使多少Kg的-10℃的冰温度升高到0℃?(
质量为2Kg的水,温度从100℃降低到20℃时,放出的热量是多少?这些热量可以使多少Kg的-10℃的冰温度升高到0℃?(冰不熔化,C冰=2.1×103J/kg•℃)
 黑棋板凳1年前1
黑棋板凳1年前1 -
 johorlyy1 共回答了17个问题
johorlyy1 共回答了17个问题 |采纳率94.1%解题思路:先利用热量计算公式求出水放出的热量,然后再求冰的质量,二者之间满足:Q吸=Q放.水放出的热量:Q放=Cm(t0-t)=4.2×103J/(kg.℃)×2kg×(100℃-20℃)=6.72×105J;
∵Q吸=Q放=6.72×105J;
∴m2=
Q吸
C冰×10℃ =
6.72×105J
2.1×103J/(kg.℃)×10℃=32kg.
答:水放出的热量是6.72×105J、可以使32kg的冰温度升高到0℃.点评:
本题考点: 热量的计算.
考点点评: 热学计算题的解题方法是:先由题意判断物体是吸热的还是放热的.并明确有哪些是已知量,哪些是未知量,然后选择需要的公式.按解题的书写格式和要求完成题目.1年前查看全部
- 某中学为学生供应开水,用锅炉将200Kg的水从25℃加热到100℃燃烧了6kg的无 烟煤水的比热容 某中学为学生供应开水
某中学为学生供应开水,用锅炉将200Kg的水从25℃加热到100℃燃烧了6kg的无 烟煤水的比热容 某中学为学生供应开水,用锅炉将200Kg的水从25℃加热到100℃燃烧了6kg的无
烟煤水的比热容是4.2乘10的3次焦/(㎏℃)无烟煤热值是3.4乘10的7次方 zhusr1年前1
zhusr1年前1 -
 vegen 共回答了20个问题
vegen 共回答了20个问题 |采纳率70%Q吸=c水m水△t=4200×200×(100-25)=63000000J
Q放=mq=6×3.4×10^7=2.04×10^8J
锅炉的效率为:Q吸/Q放=6.3×10^7J/2.04×10^8J=30.88%1年前查看全部
- 茗茗在家烧水时,将2kg的水从25℃加热到100℃,燃烧了0.1kg的无烟煤.[c水=4.2×103J/(kg•℃),无
茗茗在家烧水时,将2kg的水从25℃加热到100℃,燃烧了0.1kg的无烟煤.[c水=4.2×103J/(kg•℃),无烟煤的热值取3.4×107J/kg]求:
(1)0.1kg无烟煤完全燃烧放出的热量.
(2)水吸收的热量. qr19731年前1
qr19731年前1 -
 色摄之友 共回答了18个问题
色摄之友 共回答了18个问题 |采纳率88.9%解题思路:(1)已知无烟煤的质量与热值,由热值公式可以求出它完全燃烧释放的热量;
(2)已知水的质量与初末温度,由热量公式可以求出水吸收的热量.(1)无烟煤释放的热量:
Q放=qm煤=3.4×107J/kg×0.1kg=3.4×106J;
(2)水吸收的热量:
Q吸=cm△t=4.2×103J/(kg•℃)×2kg×(100℃-25℃)=6.3×105J;
答:(1)0.1kg无烟煤完全燃烧放出的热量为3.4×106J.
(2)水吸收的热量为6.3×105J.点评:
本题考点: 燃料的热值;热量的计算.
考点点评: 本题考查了求每燃烧释放的热量、水吸收的热量,应用热值公式与热量公式即可正确解题.1年前查看全部
- 苯的正常沸点80℃,甲苯于100℃时饱和蒸汽压为74.5kPa,苯,甲苯构成理想溶液,今将含苯为0.325(摩尔分数)的
苯的正常沸点80℃,甲苯于100℃时饱和蒸汽压为74.5kpa,苯,甲苯构成理想溶液,今将含苯为0.325(摩尔分数)的苯,甲苯混合气体鱼100℃下加压,求(1)压力多大时,气相摩尔数和液相摩尔数相等?(2)在***压力下,在1mol的该体系中加入多少摩尔的甲苯可以使整个体系刚好全部液化?
 爱如空气121年前1
爱如空气121年前1 -
 fsdgcxx 共回答了16个问题
fsdgcxx 共回答了16个问题 |采纳率87.5%1.dlnp/dt=H/RT2 求出苯在100摄氏度的蒸汽压(80摄氏度是一个标准大气压),拉乌尔定律计算就行了
2.结合相图,杠杆定律1年前查看全部
- (2012•大连二模)用酒精灯给烧杯里的水加热,把150g的水从20℃加热到100℃,燃烧了10g的酒精,设酒精完全燃烧
(2012•大连二模)用酒精灯给烧杯里的水加热,把150g的水从20℃加热到100℃,燃烧了10g的酒精,设酒精完全燃烧.已知酒精的热值为3×107J/kg,水的比热容为4.2×103J/(kg•℃).试求:
(1)水吸收的热量是多少?
(2)用酒精灯烧水时的效率是多少? jose234671年前1
jose234671年前1 -
 深圳高贵qq 共回答了19个问题
深圳高贵qq 共回答了19个问题 |采纳率84.2%解题思路:(1)水吸收的热量可用公式Q=cm△t来计算.
(2)酒精完全燃烧放出的热量可用Q放=qm来计算.对酒精灯来说,有用功为被水吸引的热量,总功为酒精完全燃烧放出的热量,酒精灯的效率可用公式η=
×100%来计算.W有用 W总 m水=150g=0.15kg,
(1)Q=cm(t末-t初)=4.2×103J/(kg•℃)×0.15kg×(100℃-20℃)=5.04×104J;
(2)Q放=qm=3.0×107J/kg×(10×10-3kg)=3×105J,
η=
W有用
W总×100%=
5.04×104J
3×105J×100%=16.8%
答:(1)水吸收的热量为5.04×104J;
(2)用酒精灯烧水时的效率是为16.8%.点评:
本题考点: 热平衡方程的应用.
考点点评: 考查了学生对吸热公式、燃料完全燃烧放热公式、效率公式的掌握和运用,知道酒精完全燃烧放出的热量不能完全被水吸收是本题的关键.1年前查看全部
- 下列几种说法中错误的是( )A. 纯水的沸点是100℃B. 气温为0℃时,水不会蒸发C. 若物体大于平面镜,则在镜中不
下列几种说法中错误的是( )
A. 纯水的沸点是100℃
B. 气温为0℃时,水不会蒸发
C. 若物体大于平面镜,则在镜中不能成完整的像
D. 物体受热膨胀时,其密度会发生改变 specter00001年前1
specter00001年前1 -
 寻求真爱 共回答了25个问题
寻求真爱 共回答了25个问题 |采纳率84%解题思路:这是一道多项选择题.
(1)水的沸点与气压有关,气压越大沸点越高,气压越小沸点越低;
(2)蒸发是在任何温度下都能发生的,只在液体表面发生的,缓慢的汽化现象;
(3)像的大小取决于物体而不是平面镜的大小,不论多么小的平面镜,所成的像都是完整的;
(4)物体膨胀时,体积变化,所以其密度也会随之变化.(1)纯水在1标准大气压下沸点是100℃,由于题中没说在什么气压下,故A不正确;
(2)由于蒸发在任何温度下都能进行,所以0℃的水也会蒸发,故B不正确;
(3)小的平面镜也可以成大的像,成像是完整的,人看不完整不代表成像不完整,故C不正确;
(4)根据ρ=[m/V]可知,体积变化时,密度会变化,故D正确.
本题选择错误答案,故选A、B、C.点评:
本题考点: 平面镜成像的特点、原理、现象及其实验方案;沸腾及沸腾条件;蒸发及其现象;密度的大小比较.
考点点评: 小平面镜也可以成大物体的完整的像,这是易错点.1年前查看全部
- 在学校组织的游山活动中,队员们带着高压锅准备野炊.因为在高山上用普通锅烧水时,水沸腾后温度()100℃,这是因为水的沸点
在学校组织的游山活动中,队员们带着高压锅准备野炊.因为在高山上用普通锅烧水时,水沸腾后温度()100℃,这是因为水的沸点()
 e2886060301年前1
e2886060301年前1 -
 xiaiwei 共回答了19个问题
xiaiwei 共回答了19个问题 |采纳率94.7%在学校组织的游山活动中,队员们带着高压锅准备野炊.因为在高山上用普通锅烧水时,水沸腾后温度(1年前查看全部
- 已知白磷的着火点是40℃,把白磷放入100℃的沸水中,白磷不会燃烧,原因是什么
 83164721年前3
83164721年前3 -
 zengvv123456 共回答了14个问题
zengvv123456 共回答了14个问题 |采纳率92.9%白磷不会燃烧,因为水中没有氧气(或其他助燃物)1年前查看全部
- 急求:水在100℃时的蒸气压为多少mmHg?再问下25℃下室温蒸气压是不是760mmHg?
 独孤公子1年前1
独孤公子1年前1 -
 云南不孝子 共回答了19个问题
云南不孝子 共回答了19个问题 |采纳率94.7%水蒸气压和相对湿度的计算公式
要求水蒸气压和相对湿度时,虽然最好用通风乾湿计,但也可采用不通风乾湿计.由乾湿计计算水蒸气压和相对湿度的公式为:
1. 从通风乾湿计的度数计算水蒸气压:
(1)湿球不结冰时
e =E’w–0.5(t-t’)P/755
(2)湿球结冰时
e =E’i –0.44(t-t’)P/755
式中,
t:乾球读数(ºC)
t’:湿球读数(ºC)
E’w:t’(ºC)的水饱和蒸气压
E’i:t’(ºC)的冰饱和蒸气压
e:所求水蒸气压
P:大气压力
2. 从不通风乾湿计的度数计算水蒸气压:
(1)湿球不结冰时
e=E’ w-0.0008P(t-t’)
(2)湿球结冰时
e=E’ i-0.0007P(t-t’)
此处所用符号的意义同上.压力单位都统一用mmHg或mb.1年前查看全部
- 100℃的水蒸气遇到人体液化成水时,水的温度为什么还是100℃
 mmm000200021年前4
mmm000200021年前4 -
 1313往往 共回答了10个问题
1313往往 共回答了10个问题 |采纳率100%因为水是晶体,晶体在从一种形态转化成另外一种形态的过程中,其温度是不变化的,这是晶体的一个特性.所以水蒸气在液化成水的过程中温度始终是100℃.只不过在液化过程中,水蒸气要大量放热,所以水蒸气遇到人体后很容易把人烫伤.1年前查看全部
大家在问
- 1We have great bags for only ¥12.为什么句中要用for
- 2求下列各式的有理化因式根号7-根号3+2a-根号2+根号(a的平方-4)
- 3如图,△ABC为等腰三角形,AB=AC,O是底边BC的中点,⊙O与腰AB相切于点D,求证:AC与⊙O相切.
- 4这两句话中,第一句用了拟人的修辞手法;使人感觉到雾既有什么,又富有什么
- 5Of course I'm handsome
- 6在等式y=ax的平方-bx+cz中,当x=1时,y=0.当x=-1时,y=-2.当x=2时,y=8.求abc的值
- 7初一《初中英语课课练》第53业 技能提升 短文缺词填空(填写完整的单词) Mother,
- 8把下列各数表示到数轴上,并将它们从小到大用“<”连接。
- 9计算直径的公式知道圆柱长54.5厘米宽12厘米 怎么算出直径?
- 10i'm applying facial mask now.
- 11英语翻译 四川华运科技发展有限公司 急急急
- 12数学的配方公式怎么做,不会配方,哪位好心人教教我呗
- 13古典概型与现代概型的区别如题,用自己的话概括下,不要定义.要有助于理解的
- 14分子晶体中共价键键能越大,熔点越高?
- 15一个圆柱底面周长是12.56高比底面直径多50%求体积?圆柱若与一个底面半径为3厘米的圆锥

