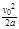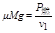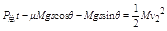氮氧化合物都易溶于水吗?如题
 saekoxu2022-10-04 11:39:541条回答
saekoxu2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 duanming2020 共回答了19个问题
duanming2020 共回答了19个问题 |采纳率89.5%- 不,有些氮氧化合物如NO,NO2都会直接和水发生反应,一般的稳定氮氧化合物都是溶于水的,有机无机都是,氧是亲水基
- 1年前
相关推荐
- 氮氧化合物,以及氟里昂破坏臭氧层的反应方程式!
 耳环妹妹1年前1
耳环妹妹1年前1 -
 ynkf58 共回答了15个问题
ynkf58 共回答了15个问题 |采纳率86.7%氟氯代烷(即氟利昂)的化学性质很稳定,在底层大气中基本不分解,上升到平流层以后,在紫外线的照射下分解出氯原子,参与破坏臭氧的反应:
Cl+O3->ClO+O2
ClO+O->Cl+O2
总反应:
O3+O->2O21年前查看全部
- (2005•普陀区二模)某氮氧化合物中N:O的质量比为7:20,该化合物的化学式______.
 runli1年前1
runli1年前1 -
 秤砣教nikita 共回答了13个问题
秤砣教nikita 共回答了13个问题 |采纳率92.3%解题思路:可先设出N的氧化物的化学式,利用N与O元素的质量比来求出N与O的原子个数比,最后写出化学式.设N的氧化物的化学式为NxOy,
由N:O的质量比为7:20,则
14×x:16×y=7:20,
解得x:y=2:5,
即化学式为N2O5,
故答案为:N2O5.点评:
本题考点: 有关化学式的计算和推断;元素质量比的计算.
考点点评: 本题考查化学式的推断,较简单,学生可直接设出化学式进行化学式的有关计算即可推出化学式.1年前查看全部
- (2009•成都)CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
(2009•成都)CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
A.在某些工业生产过程中,将欲排放的CO2用化学溶剂吸收
B.禁止制备和使用CH4、N2O等温室气体
C.开发无污染的太阳能、风能、地热能
D.变革能源消耗模式 eudidwss1年前1
eudidwss1年前1 -
 蓝色夜未央 共回答了12个问题
蓝色夜未央 共回答了12个问题 |采纳率100%A、将欲排放的CO2用化学溶剂吸收,可以减缓全球气候变暖,故不可选;
B、目前还没有真正能替代CH4等的新型燃料,故不可禁止制备和使用,故可选;
C、开发无污染的太阳能、风能、地热能,可以减少二氧化碳等温室气体的排放,减缓全球气候变暖,故不可选;
D、变革能源消耗模式,通过技术创新、制度创新、新能源开发等多种手段,尽量减少化学燃料的使用,可以减缓全球气候变暖.故不可选.
故选B.1年前查看全部
- 将22.4L某气态氮氧化合物与足量灼热的铜粉完全反应后,气体体积11.2L,体积均在相同条件下测定,则该氮氧化合物的化学
将22.4L某气态氮氧化合物与足量灼热的铜粉完全反应后,气体体积11.2L,体积均在相同条件下测定,则该氮氧化合物的化学式为?
我算了下,好像NO和NO2都可以是,可不可以把两个答案的过程写出来,我只用了一种笨方法,通过体积的物质之比2:1,配平方程式,在看方程式的系数之比,两个的比都是2:1,我用了假设化合物,然后根据方程解,但是好像解糊涂了,所以我希望可以详细写出通过假设得出结果的过程, lisa1231年前1
lisa1231年前1 -
 gncam_boy 共回答了20个问题
gncam_boy 共回答了20个问题 |采纳率95%你的分析是正确.
氮氧化合物被金属还原后的产物应为稳定的氮气,金属变为氧化物.
22.4L某气态氮氧化合物完全反应后气体体积变为11.2L(体积均在相同条件下测定),由此可知反应的气体和生成的气体的物质的量比=22.4L:11.2L=2:1
不过不用写出所有化学方程式:
你只需设氮的氧化物的化学式为NxOy,写出一个化学方程式即可:
2NxOy + 2yCu =△= xN2 + 2yCuO
由上面的化学方程式可知:只要x=1即符合条件,所以NO、NO2都可以.
希望我的回答能对你有帮助!1年前查看全部
- CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
A. 在某些工业生产过程中,将欲排放的CO2用化学溶剂吸收
B. 禁止制备和使用CH4、N2O等温室气体
C. 开发无污染的太阳能、风能、地热能
D. 变革能源消耗模式 睡觉好安逸1年前1
睡觉好安逸1年前1 -
 阳光下的vv人 共回答了26个问题
阳光下的vv人 共回答了26个问题 |采纳率100%解题思路:CO2、CH4和氮氧化合物都是形成温室效应的气体.要想减缓全球气候变暖,就要减少CO2、CH4和氮氧化合物的排放,开发新能源等.A、将欲排放的CO2用化学溶剂吸收,可以减缓全球气候变暖,故不可选;
B、目前还没有真正能替代CH4等的新型燃料,故不可禁止制备和使用,故可选;
C、开发无污染的太阳能、风能、地热能,可以减少二氧化碳等温室气体的排放,减缓全球气候变暖,故不可选;
D、变革能源消耗模式,通过技术创新、制度创新、新能源开发等多种手段,尽量减少化学燃料的使用,可以减缓全球气候变暖.故不可选.
故选B.点评:
本题考点: 二氧化碳对环境的影响;自然界中的碳循环.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,知识面涉及较广,思维跨度大,强调了学生整合知识的能力.1年前查看全部
- 液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排
 液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排放减少35%以上,是目前较为实用的低排放汽车.如图所示为一辆燃气车,现把该车改装为双动力系统,在平路行驶时,只采用燃气动力驱动,发动机的额定功率为15kw,能获得的最大速度为v1=15m/s.当车驶上路面情况相同(动摩擦因数相同)倾角为37°足够长的斜坡时,采用电力与燃气双动力系统发动机的总功率为34kw,由静止开始保持该功率不变,经过20s达到最大速度,求t=45s时车沿斜面运动的路程.已知车与驾驶员总质量为M=1000kg,g=10m/s2.(sin37°=0.6,cos37°=0.8)(车所受阻力近似等于滑动摩擦力)
液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排放减少35%以上,是目前较为实用的低排放汽车.如图所示为一辆燃气车,现把该车改装为双动力系统,在平路行驶时,只采用燃气动力驱动,发动机的额定功率为15kw,能获得的最大速度为v1=15m/s.当车驶上路面情况相同(动摩擦因数相同)倾角为37°足够长的斜坡时,采用电力与燃气双动力系统发动机的总功率为34kw,由静止开始保持该功率不变,经过20s达到最大速度,求t=45s时车沿斜面运动的路程.已知车与驾驶员总质量为M=1000kg,g=10m/s2.(sin37°=0.6,cos37°=0.8)(车所受阻力近似等于滑动摩擦力)  支颐空想1年前1
支颐空想1年前1 -
 王者天地 共回答了24个问题
王者天地 共回答了24个问题 |采纳率79.2%解题思路:汽车获得的最大速度时,阻力等于汽车的牵引力,从而求出汽车受到的阻力;对倾角为37°的斜面上的汽车进行受力分析,求出汽车达到最大速度时的牵引力,然后根据瞬时功率的表达式求出最大速度,最后使用动能定律求得该过程中车沿斜面运动的路程.在平路行驶时获得的最大速度时,汽车匀速运动由:μMg=
P燃
v1
当汽车保持总功率不变,在斜坡上运动,达到最大速度时由:(μMgcosθ+Mgsinθ)v2=P总
代入数据得:v2=5m/s
由动能定理可得:P总t−μMgscosθ−Mgssinθ=
1
2Mv22
代入数据解得:s=370.2m
答:t=45s时车沿斜面运动的路程为370.2m点评:
本题考点: 动能定理的应用;功率、平均功率和瞬时功率.
考点点评: 此题主要考查的是学生对速度计算公式的理解和掌握,弄清楚汽车行驶的路程是解决此题的关键.1年前查看全部
- 下列含氮化合物中,氮元素与氧元素质量比为7:16,则该氮氧化合物的分子式(化学式)是( ) A.NO B.N 2 O
下列含氮化合物中,氮元素与氧元素质量比为7:16,则该氮氧化合物的分子式(化学式)是( ) A.NO B.N 2 O C.N 2 O 3 D.NO 2  攸蓝海水1年前1
攸蓝海水1年前1 -
 wendyhua2007 共回答了18个问题
wendyhua2007 共回答了18个问题 |采纳率77.8%设氮氧化合物的化学式为N x O y ,
根据氮元素与氧元素质量比为7:16,
则N、O元素的质量比为14×x:16×y=7:16,
解得x:y=1:2,
即该氧化物的化学式为NO 2 ,
故选D.1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A. NO2
B. N2O2
C. N2O
D. N2O4 人头马一米一1年前2
人头马一米一1年前2 -
 bqirtss 共回答了19个问题
bqirtss 共回答了19个问题 |采纳率94.7%解题思路:根据该氮氧化合物与足量的灼热铜粉完全反应的原理以及气体体积差量法来计算.假设反应为:2NxOy+2yCu
加热
.
2yCuO+xN2,根据题中数据,反应后气体体积为反应前气体体积的一半,即可以得到x=1,
因为4Cu+2NO2=4CuO+N2,方程式的系数之比等于物质的量之比,所以反应前有NO222.4L即1mol,所以反应后有N20.5mol,所以是NO2 ,
故选A.点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质化学式确定的题目,注意差量法在解题中的灵活运用,难度不大.1年前查看全部
- CO 2 、CH 4 和氮氧化合物都是形成温室效应的气体。下列减缓全球气候变暖的对策中,不恰当的是 [
CO 2 、CH 4 和氮氧化合物都是形成温室效应的气体。下列减缓全球气候变暖的对策中,不恰当的是 [ ]A.在某些工业生产过程中,将欲排放的CO 2 用化学溶剂吸收
B.禁止制备和使用CH 4 、N 2 O等温室气体
C.开发无污染的太阳能、风能、地热能等
D.变革能源消耗模式 lj7063001年前1
lj7063001年前1 -
 东西33 共回答了16个问题
东西33 共回答了16个问题 |采纳率93.8%B1年前查看全部
- 氮氧化物与铜反应22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积变为11.2L(相同条件下测定),则该氮氧
氮氧化物与铜反应
22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积变为11.2L(相同条件下测定),则该氮氧化合物的化学式为 一条深飘的鱼1年前4
一条深飘的鱼1年前4 -
 破烂的梦 共回答了15个问题
破烂的梦 共回答了15个问题 |采纳率100%推测,该氮氧化合物中的氧都用来生成了氧化铜,最后生成氮气和氧化铜,而气体体积变为原来的一半,可知该氮氧化合物每个分子含一个氮原子,所以,可能是NO2,NO1年前查看全部
- 一氧化碳和氮氧化合物反应的化学式
一氧化碳和氮氧化合物反应的化学式
为了降低汽车尾气对空气的污染,可用纳米级的某种氧化物作催化剂,是尾气中的CO与氮氧化合物(NO2)反应,转化为空气中含有的两种气体(其中一种为单质),该反应的化学方程式为? 令狐水中1年前3
令狐水中1年前3 -
 重名的人好多 共回答了19个问题
重名的人好多 共回答了19个问题 |采纳率94.7%这肯定是为了将CO转化为CO2无污染气体
4CO+2NO2=4CO2+N21年前查看全部
- 光化学烟雾的具体形成过程汽车尾气中的碳氢化合物和氮氧化合物在阳光作用下发生化学反应,生成臭氧,它和大气中的其它成份结合就
光化学烟雾的具体形成过程
汽车尾气中的碳氢化合物和氮氧化合物在阳光作用下发生化学反应,生成臭氧,它和大气中的其它成份结合就形成光化学烟雾
各类反应及反应方程式 无情的狼lyouloev1年前1
无情的狼lyouloev1年前1 -
 方丈的初恋 共回答了21个问题
方丈的初恋 共回答了21个问题 |采纳率85.7%1、污染空气中NO2的光解是光化学烟雾形成的起始反应.
(
化学式:
NO2==NO+O(条件为光照)
O+O2==O3
2NO+O2==2NO2
分析:
2NO2(排放的)==2NO[(3)式中有用)]+2O[(2)式中有用)](条件为光照)
2O[(1)式中的O]+2O2(空气中的)==2O3(刺激性气体)
2NO[(1)式中的NO]+O2==2NO2(生成NO2,开始继续反应)
综合一下:
3O2==2O3(光照,NO2)
)
2、碳氢化合物被HO、O等自由基和臭氧氧化,导致醛、酮、醇、酸等产物以及重要的中间产物RO2、HO2、RCO等自由基的生成.
3、过氧自由基引起NO向NO2的转化,并导致O3和PAN等的生成.
光化学反应中生成的臭氧、醛、酮、醇、PAN等统称为光化学氧化剂,以臭氧为代表,所以光化学烟雾污染的标志是臭氧浓度的升高.1年前查看全部
- 下列说法不正确的是( ) A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关 B.根据分散质微粒直径大小可以将分
下列说法不正确的是( ) A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关 B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液 C.SiO 2 可用于制造光导纤维,其性质稳定,不溶于强酸、强碱 D.焰火的五彩缤纷是某些金属元素的性质的展现  witchzz1年前1
witchzz1年前1 -
 mm的熊猫 共回答了23个问题
mm的熊猫 共回答了23个问题 |采纳率100%A.以一氧化氮和二氧化氮为主的氮氧化物是形成“光化学烟雾”“硝酸型酸雨”的形成的一个重要原因,故A正确;
B.分散质微粒直径大小可以将分散系分为溶液、胶体和浊液,故B正确;
C.SiO 2 可用于制造光导纤维,其性质稳定,能和强碱反应生成盐和水,故C错误;
D.焰火的五彩缤纷是某些金属元素的焰色反应,故D正确;
故选C.1年前查看全部
- 与氮氧化合物有关的全球或区域性大气环境问题主要有( ) A.酸雨、温室效应、光化学烟雾 B.酸雨、臭氧层空洞、光化学烟
与氮氧化合物有关的全球或区域性大气环境问题主要有( ) A.酸雨、温室效应、光化学烟雾 B.酸雨、臭氧层空洞、光化学烟雾 C.水华、臭氧层空洞、光化学烟雾 D.酸雨、臭氧层空洞、白色污染  手握手的归宿1年前1
手握手的归宿1年前1 -
 张小花猫 共回答了19个问题
张小花猫 共回答了19个问题 |采纳率89.5%酸雨主要是工业排放的废气二氧化硫和氮氧化合物,二氧化硫在灰尘催化下与氧气反应生成三氧化硫,与水生成硫酸,氮氧化合物与水生成硝酸.使雨水pH<5.6;
光化学烟雾主要是汽车尾气中的氮氧化合物与碳氢化合物在紫外线作用下发生一系列反应生成类似蓝色的烟雾,危害健康;
臭氧空洞指的是因空气污染物质,特别是氮氧化物和卤化代烃等气溶胶污染物的扩散、侵蚀而造成大气臭氧层被破坏和减少的现象;
通过以上分析知,与氮氧化物有关的环境污染是酸雨、光化学烟雾、臭氧空洞,
故选B.1年前查看全部
- 与氮氧化合物有关的全球或区域性大气环境问题主要有( )
与氮氧化合物有关的全球或区域性大气环境问题主要有( )
A.酸雨、温室效应、光化学烟雾
B.酸雨、臭氧层空洞、光化学烟雾
C.水华、臭氧层空洞、光化学烟雾
D.酸雨、臭氧层空洞、白色污染 优海伶1年前1
优海伶1年前1 -
 枫落叶 共回答了22个问题
枫落叶 共回答了22个问题 |采纳率81.8%解题思路:酸雨:主要是工业排放的废气二氧化硫和氮氧化合物,二氧化硫在灰尘催化下与氧气反应生成三氧化硫,与水生成硫酸;氮氧化合物与水生成硝酸.使雨水PH<5.6;
光化学烟雾:主要是汽车尾气中的氮氧化合物与碳氢化合物在紫外线作用下发生一系列反应生成类似蓝色的烟雾,危害健康;
温室效应:主要是化石燃料过多燃烧包括工厂和汽车尾气产生的二氧化碳,反射长波幅射,使地球的热量散失减慢,另外甲烷是温室作用更强的气体;
臭氧空洞:指的是因空气污染物质,特别是氮氧化物和卤化代烃等气溶胶污染物的扩散、侵蚀而造成大气臭氧层被破坏和减少的现象;
水华:淡水水体中藻类大量繁殖的一种自然生态现象,主要由于生活及工农业生产中含有大量氮、磷的废污水进入水体后,蓝藻、绿藻、硅藻等藻类成为水体中的优势种群,大量繁殖后使水体呈现蓝色或绿色的一种现象;
白色污染是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的一种形象称谓.酸雨主要是工业排放的废气二氧化硫和氮氧化合物,二氧化硫在灰尘催化下与氧气反应生成三氧化硫,与水生成硫酸,氮氧化合物与水生成硝酸.使雨水pH<5.6;
光化学烟雾主要是汽车尾气中的氮氧化合物与碳氢化合物在紫外线作用下发生一系列反应生成类似蓝色的烟雾,危害健康;
臭氧空洞指的是因空气污染物质,特别是氮氧化物和卤化代烃等气溶胶污染物的扩散、侵蚀而造成大气臭氧层被破坏和减少的现象;
通过以上分析知,与氮氧化物有关的环境污染是酸雨、光化学烟雾、臭氧空洞,
故选B.点评:
本题考点: 氮的氧化物的性质及其对环境的影响.
考点点评: 本题考查了环境污染,明确环境污染的成因及原理是解本题关键,保护环境是保护我们人类自己,难度不大.1年前查看全部
- 为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用“乙醇汽油”.其具体做法是将乙醇按一定比例和汽油混合.而乙醇在燃烧过
为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用“乙醇汽油”.其具体做法是将乙醇按一定比例和汽油混合.而乙醇在燃烧过程中产生了二氧化碳和水.
(1)乙醇燃烧的化学反应方程式是______;
(2)写出使用车用乙醇汽油的两点好处.______. ajzhangbin1年前1
ajzhangbin1年前1 -
 弹琴 共回答了14个问题
弹琴 共回答了14个问题 |采纳率100%(1)乙醇燃烧时生成二氧化碳和水,反应的化学方程式为:C 2 H 5 OH+3O 2
点燃
.
2CO 2 +3H 2 O;
(2)使用乙醇汽油可以减少空气污染,也可以节约石油资源.1年前查看全部
- 化学氮氧化合物将一试管NO2倒扣在水槽中,经过一段时间水大约上升到试管容积的多少
 痕从1年前1
痕从1年前1 -
 yanzhao2002 共回答了16个问题
yanzhao2002 共回答了16个问题 |采纳率93.8%反应式:3NO2+H2O=2HNO3+NO
每溶解3体积的NO2,就会放出1体积的NO
所以等NO2溶解完毕后,试管内还剩1/3体积的NO
即,水面会上升到试管溶剂的2/3处~1年前查看全部
- 2013年12月以来,杭州备受雾霾天气折磨,空气质量指数一度飙升500+,二氧化硫、氮氧化合物和可吸入颗粒物这三项是雾霾
2013年12月以来,杭州备受雾霾天气折磨,空气质量指数一度飙升500+,二氧化硫、氮氧化合物和可吸入颗粒物这三项是雾霾的主要组成,下列说法不正确的是( )

A.雾是由大量悬浮在近地面空气中的微小水滴或冰晶组成的气溶胶系统,是近地面层空气中水汽凝结(或凝华的产物)。 B.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子组成的。人们将这种非水分组成的气溶胶系统造成的视程障碍称为霾或灰霾 C.大气浑浊视野模糊导致的能见度恶化的原因:一般相对湿度小于80%时是霾造成的,相对湿度大于90%是雾造成的,相对湿度介于80%~90%之间是霾和雾的混合物共同造成的,但其主要成分是霾。 D.颗粒物的英文缩写为PM,颗粒物在空气中只形成气溶胶,其本身既是一种污染物,又是重金属、多环芳烃等有毒物质的载体。  davis_yang1年前1
davis_yang1年前1 -
 可爱卡卡 共回答了13个问题
可爱卡卡 共回答了13个问题 |采纳率84.6%D
1年前查看全部
- 汽车排放的尾气中的氮氧化合物会导致什么?求答案
 tsubaki09171年前1
tsubaki09171年前1 -
 hzl0102 共回答了20个问题
hzl0102 共回答了20个问题 |采纳率85%形成光化学烟雾和酸雨的一个重要原因.汽车尾气中的氮氧化物与氮氢化合物经紫外线照射发生反应形成的有毒烟雾,称为光化学烟雾.1年前查看全部
- 汽车安装的排气净化器的技术核心是使用高效催化剂,使废气中的CO和NO2在催化剂表面进行氧化还原反应.写出氮氧化合物(用N
汽车安装的排气净化器的技术核心是使用高效催化剂,使废气中的CO和NO2在催化剂表面进行氧化还原反应.写出氮氧化合物(用NOx表示)跟CO反应转化为无毒物质的化学方程式______.
 hh了好hh了清净1年前1
hh了好hh了清净1年前1 -
 minl99 共回答了16个问题
minl99 共回答了16个问题 |采纳率87.5%解题思路:根据化学方程式的书写规则书写方程式,反应物为NOX和CO,生成物为N2和CO2,根据生成物和反应物正确书写化学方程式.氮的氧化物(用NOX表示)与CO相互反应,生成N2和CO2.其化学方程式为:2NOx+2xCO═2xCO2+N2.
故答案为:2NOx+2xCO=2xCO2+N2.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查化学方程式的书写,书写时一定要遵循质量守恒定律.1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A. NO2
B. N2O2
C. N2O
D. N2O4 ambroselx1年前2
ambroselx1年前2 -
 lxm850106 共回答了15个问题
lxm850106 共回答了15个问题 |采纳率86.7%解题思路:根据该氮氧化合物与足量的灼热铜粉完全反应的原理以及气体体积差量法来计算.假设反应为:2NxOy+2yCu
加热
.
2yCuO+xN2,根据题中数据,反应后气体体积为反应前气体体积的一半,即可以得到x=1,
因为4Cu+2NO2=4CuO+N2,方程式的系数之比等于物质的量之比,所以反应前有NO222.4L即1mol,所以反应后有N20.5mol,所以是NO2 ,
故选A.点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质化学式确定的题目,注意差量法在解题中的灵活运用,难度不大.1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A. NO2
B. N2O2
C. N2O
D. N2O4 wuyanjin001年前4
wuyanjin001年前4 -
 jiliziyoujian 共回答了20个问题
jiliziyoujian 共回答了20个问题 |采纳率95%解题思路:根据该氮氧化合物与足量的灼热铜粉完全反应的原理以及气体体积差量法来计算.假设反应为:2NxOy+2yCu
加热
.
2yCuO+xN2,根据题中数据,反应后气体体积为反应前气体体积的一半,即可以得到x=1,
因为4Cu+2NO2=4CuO+N2,方程式的系数之比等于物质的量之比,所以反应前有NO222.4L即1mol,所以反应后有N20.5mol,所以是NO2 ,
故选A.点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质化学式确定的题目,注意差量法在解题中的灵活运用,难度不大.1年前查看全部
- 科学化学计算题4某氮氧化合物中氮、氧两种元素质量比为7:12,求氮元素的化合价注:
 学会哭泣1年前1
学会哭泣1年前1 -
 hhw23 共回答了17个问题
hhw23 共回答了17个问题 |采纳率94.1%某氮氧化合物中氮、氧两种元素质量比为7:12.
所以变成14:24,14是1个N,24是1.5个O,配成NO1.5,再变N2O3.
氮元素的化合价是+3.1年前查看全部
- 二氧化硫、悬浮颗粒物、氮氧化合物是主要的大气污染物.20世纪70年代的一项研究表明,对燃煤设备采用高烟囱排除烟和废气,可
二氧化硫、悬浮颗粒物、氮氧化合物是主要的大气污染物.20世纪70年代的一项研究表明,对燃煤设备采用高烟囱排除烟和废气,可有效降低地表空气中粉尘和二氧化硫浓度,这种措施可不可取?为什么?
 yanleiaiwenjie1年前3
yanleiaiwenjie1年前3 -
 木木橙子 共回答了17个问题
木木橙子 共回答了17个问题 |采纳率94.1%不可取.因为采用高烟囱只是将烟和废气排在了高空大气层中,同样是排在了大气层中,对大气层的污染也是同样的,不能从根本上解决这一问题,所以此方法不可取.1年前查看全部
- 汽车尾气转化器中反应的化学方程式(只写氮氧化合物和二氧化碳的)
 jiushijie1年前1
jiushijie1年前1 -
 DINGYINGFANG 共回答了24个问题
DINGYINGFANG 共回答了24个问题 |采纳率100%2CO + 2NO = 2CO2 + N2
或者,2x CO + 2 NOx = 2x CO2 + N2
尾气中的是CO和氮氧化物,反应生成无害并参与循环的CO2和N21年前查看全部
- 液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排
液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排放减少35%以上,是目前较为实用的低排放汽车.如下图所示为一辆燃气车,为检验刹车功能,进行了如下实验:在路旁可以竖起一标志杆,车以v0=72km/h的速度匀速行驶,当车头距标志杆s=20m时,实验室工作人员向司机下达停车的指令,司机经时间t0=0.8s(即反应时间)后开始刹车,若车在标志杆前停止运动则符合安全要求,已知车与驾驶员总质量为M=1000kg,g=10m/s2.求:
(1)刹车过程中的制动力至少多大?
(2)现把该车改装为双动力系统,在平路行驶时,只采用燃气动力驱动,发动机的额定功率为15kw,能获得的最大速度为v1=15m/s.当车驶上路面情况相同倾角为37°足够长的斜坡时,采用电力与燃气双动力系统发动机的总功率为34kw,保持该功率不变,经过20s达到最大速度,求t=45s时车沿斜面运动的路程.(sin37°=0.6,cos37°=0.8) bvmxv1年前1
bvmxv1年前1 -
 cool_yao 共回答了23个问题
cool_yao 共回答了23个问题 |采纳率95.7%解题思路:(1)从发现情况到完全停止所用的时间包括反应时间和刹车时间;根据公式s=vt,求出反应时间内行驶的路程,汽车在这段时间内行驶的总路程等于反应距离加上刹车距离,根据公式2as=v2
再求出加速度,根据牛顿第二定律求得制动力.也可以使用动能定律来求.−v 20
(2)汽车获得的最大速度时,阻力等于汽车的牵引力,从而求出汽车受到的阻力;对倾角为37°的斜面上的汽车进行受力分析,求出汽车达到最大速度时的牵引力,然后根据瞬时功率的表达式求出最大速度,最后使用动能定律求得该过程中车沿斜面运动的路程(1)v0=72km/s=20m/s,故在反应时间内驾驶员匀速运动的距离为:s0=v0t0=20×0.8m=16m
若车在标志杆前停止运动,由运动学公式可得:
v02
2a≤s-s0
可求得:a≥50m/s2
由牛顿第二运动定律可得:F制=ma≥5×104N
(2)在平路行驶时获得的最大速度时,汽车匀速运动由:μMg=
P燃
v1
当汽车保持总功率不变,在斜坡上运动,达到最大速度时由:(μMgcosθ+Mgsinθ)v2=P总
代入数据得:v2=5m/s
对于在斜面上运动的全过程,由动能定理可得:P总t−μMgscosθ−Mgssinθ=
1
2Mv22
代入数据得:s=370.2m
答;(1)刹车过程中的制动力至少5×104N;
(2)t=45s时车沿斜面运动的路程370.2m点评:
本题考点: 动能定理;匀变速直线运动的速度与时间的关系;匀变速直线运动的位移与时间的关系.
考点点评: 此题主要考查的是学生对速度计算公式的理解和掌握,弄清楚汽车行驶的路程是解决此题的关键.1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积变为11.2L则该氮氧化合物的化学式是
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积变为11.2L则该氮氧化合物的化学式是
体积均在相同的条件下 82503211年前1
82503211年前1 -
 fqno1 共回答了23个问题
fqno1 共回答了23个问题 |采纳率87%氮氧化合物被金属还原后的产物一般为稳定的氮气,金属变为氧化物.
22.4L某气态氮氧化合物完全反应后气体体积变为11.2L(体积均在相同条件下测定),则反应气体和生成气体的物质的量比为2:1
所以是2NO2 + 4Cu = N2 + 4CuO1年前查看全部
- “氮的氧化物”和“氮氧化合物”这两种说法有什么区别吗?
 lhp09191年前4
lhp09191年前4 -
 jiangjixing 共回答了24个问题
jiangjixing 共回答了24个问题 |采纳率91.7%就我的感觉,前者的范围小,后者是范围更大一些
氮的氧化物很明确,就是指NO、NO2等只含氮和氧两种元素的化合物
狭义的氮氧化合物和氮的氧化物的意义相同,广义的可指含有这两种元素的化合物,不过一般都是用狭义的,那么二者的意思就基本相同了1年前查看全部
- 如何计算燃烧天燃气的二氧化碳和氮氧化合物的排放量
如何计算燃烧天燃气的二氧化碳和氮氧化合物的排放量
天然气中或者其他可燃气体会含有N,我是想知道这气体燃烧后产生的二氧化碳,氮氧化合物的排放量。假设知道每种份子所占百分数,知道总的气体燃烧量。 true-colors1年前2
true-colors1年前2 -
 D04550223 共回答了21个问题
D04550223 共回答了21个问题 |采纳率81%燃烧一定体积的天然气 分别测二氧化碳和氮氧化物的含量不就得了 氮氧化物可以测定比较复杂下面摘自网络:
在测定氮氧化物浓度时,应先用三氧化铬将一氧化氮氧化成二氧化氮.
二氧化氮被吸收液吸收后,生成亚硝酸和硝酸,其中,亚硝酸与对氨基苯磺酸发生重氮化反应,再与盐酸萘乙二胺偶合,生成玫瑰红色偶氮染料,据其颜色深浅,用分光光度法定量.因为NO2(气)转变为NO2—(液)的转换系数为0.76,故在计算结果时应除以0.76.
还有你的最后一句话有点难以理解 假设知道每种份子所占百分数,知道总的气体燃烧量.能具体点么?1年前查看全部
- 为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用“乙醇汽油”.其具体做法是将乙醇按一定比例和汽油混合.而乙醇在燃烧过
为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用“乙醇汽油”.其具体做法是将乙醇按一定比例和汽油混合.而乙醇在燃烧过程中产生了二氧化碳和水.
(1)乙醇燃烧的化学反应方程式是C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2;
2CO2+3H2O点燃 .
(2)写出使用车用乙醇汽油的两点好处.______. 火1681年前1
火1681年前1 -
 齐鲁才俊 共回答了16个问题
齐鲁才俊 共回答了16个问题 |采纳率81.3%解题思路:根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式;乙醇燃烧时生成二氧化碳和水,对空气无污染.(1)乙醇燃烧时生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O;
(2)使用乙醇汽油可以减少空气污染,也可以节约石油资源.点评:
本题考点: 常用燃料的使用与其对环境的影响.
考点点评: 解答本题时要注意质量守恒定律的应用,同时要充分理解节能环保的重要性,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用"乙醇汽油"。其具体做法是将乙醇按一定比例和汽油混合。而乙醇在燃烧过
为减轻氮氧化合物对空气的污染,现在车用燃油已逐步使用"乙醇汽油"。其具体做法是将乙醇按一定比例和汽油混合。而乙醇在燃烧过程中产生了二氧化碳和水。
(1)乙醇燃烧的化学反应方程式是__________________ ,
(2)写出使用车用乙醇汽油的两点好处。
 yangzhouguo1年前1
yangzhouguo1年前1 -
 zgwhhswq 共回答了19个问题
zgwhhswq 共回答了19个问题 |采纳率84.2%1年前查看全部
- (2009•成都)CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
(2009•成都)CO2、CH4和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
A.在某些工业生产过程中,将欲排放的CO2用化学溶剂吸收
B.禁止制备和使用CH4、N2O等温室气体
C.开发无污染的太阳能、风能、地热能
D.变革能源消耗模式 最新绿茶1年前1
最新绿茶1年前1 -
 深蓝未来的梦 共回答了17个问题
深蓝未来的梦 共回答了17个问题 |采纳率94.1%解题思路:CO2、CH4和氮氧化合物都是形成温室效应的气体.要想减缓全球气候变暖,就要减少CO2、CH4和氮氧化合物的排放,开发新能源等.A、将欲排放的CO2用化学溶剂吸收,可以减缓全球气候变暖,故不可选;
B、目前还没有真正能替代CH4等的新型燃料,故不可禁止制备和使用,故可选;
C、开发无污染的太阳能、风能、地热能,可以减少二氧化碳等温室气体的排放,减缓全球气候变暖,故不可选;
D、变革能源消耗模式,通过技术创新、制度创新、新能源开发等多种手段,尽量减少化学燃料的使用,可以减缓全球气候变暖.故不可选.
故选B.点评:
本题考点: 二氧化碳对环境的影响;自然界中的碳循环.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,知识面涉及较广,思维跨度大,强调了学生整合知识的能力.1年前查看全部
- 光化学烟雾是排入大气的氮氧化合物和碳氢化合物等受太阳紫外线作用产生的一种具有刺激性的浅蓝色的烟雾。你认为美国洛杉矶一年中
光化学烟雾是排入大气的氮氧化合物和碳氢化合物等受太阳紫外线作用产生的一种具有刺激性的浅蓝色的烟雾。你认为美国洛杉矶一年中最易发生光化学污染的月份是 []A、1月
B、4月
C、7月
D、11月 carmentang1年前1
carmentang1年前1 -
 debanggongsi 共回答了21个问题
debanggongsi 共回答了21个问题 |采纳率90.5%C1年前查看全部
- 液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排
液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放减少70%以上,氮氧化合物排放减少35%以上,是目前较为实用的低排放汽车。如下图所示为一辆燃气车,为检验刹车功能,进行了如下实验:在路旁可以竖起一标志杆,车以v 0 =72km/h的速度匀速行驶,当车头距标志杆s=20m时,实验室工作人员向司机下达停车的指令,司机经时间t 0 =0.8s(即反应时间)后开始刹车,若车在标志杆前停止运动则符合安全要求,已知车与驾驶员总质量为M=1000kg,g=10m/s 2 。求:
小题1:刹车过程中的制动力至少多大?
小题2:现把该车改装为双动力系统,在平路行驶时,只采用燃气动力驱动,发动机的额定功率为15kw,能获得的最大速度为v 1 =15m/s。当车驶上路面情况相同倾角为37°足够长的斜坡时,采用电力与燃气双动力系统发动机的总功率为34kw,保持该功率不变,经过20s达到最大速度,求t=45s时车沿斜面运动的路程。(sin37°=0.6,cos37°=0.8)
 ruru妞1年前1
ruru妞1年前1 -
 武汉寒江雪 共回答了17个问题
武汉寒江雪 共回答了17个问题 |采纳率100%1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A. NO2
B. N2O2
C. N2O
D. N2O4 amyxiu1年前5
amyxiu1年前5 -
 小卡西啊 共回答了15个问题
小卡西啊 共回答了15个问题 |采纳率80%解题思路:根据该氮氧化合物与足量的灼热铜粉完全反应的原理以及气体体积差量法来计算.假设反应为:2NxOy+2yCu
加热
.
2yCuO+xN2,根据题中数据,反应后气体体积为反应前气体体积的一半,即可以得到x=1,
因为4Cu+2NO2=4CuO+N2,方程式的系数之比等于物质的量之比,所以反应前有NO222.4L即1mol,所以反应后有N20.5mol,所以是NO2 ,
故选A.点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质化学式确定的题目,注意差量法在解题中的灵活运用,难度不大.1年前查看全部
- 关于氮氧化合物的 某单质与浓硝酸反应时,每有0.25mol单质反应就消耗1molHNO3,则该单质氧化后所显示的化合价为
关于氮氧化合物的
某单质与浓硝酸反应时,每有0.25mol单质反应就消耗1molHNO3,则该单质氧化后所显示的化合价为( )
A +1 B +2 C +3 D +4
麻烦把解题过程说的清楚一点 autoeye1年前1
autoeye1年前1 -
 玄鬼 共回答了22个问题
玄鬼 共回答了22个问题 |采纳率95.5%答案选BD
由于硝酸转变为二氧化氮,1mol被还原硝酸得到1mol电子
若单质M是金属单质,设显x价,那么生成M(NO3)x、NO2、H2O,硝酸物质的量为0.25x+0.25x=0.5x,所以0.5x=1,x=2,显2价
若单质M是非金属单质,设显2y价,生成MOy、NO2、H2O,硝酸物质的量为2y*0.25=1解得y=2,显4价
例如铜、碳与浓硝酸反应1年前查看全部
- 化学高手们请进来!难题难解!22.4升氮氧化合物与铜充分反应.最后剩下11.2升空气.此氮氧化合物化学式是 求过程打错
化学高手们请进来!难题难解!
22.4升氮氧化合物与铜充分反应.最后剩下11.2升空气.此氮氧化合物化学式是 求过程
打错 是剩下11.2升气体 潇潇风雨3581年前3
潇潇风雨3581年前3 -
 facingjoy_sj 共回答了24个问题
facingjoy_sj 共回答了24个问题 |采纳率100%您好,
也许这道题您遗漏了什么条件!
根据气体的摩尔体积提出的条件可知:在同温同压下,摩尔数与气体体积成正比.所以得出下面这个方程式:
NxOy+yCu=0.5xN2+yCuO
反应前后的气体分别为NxOy和N2,只要使x=1的氮氧化合物都符合条件
即:NO、NO2都符合条件.
希望能对您有所帮助,谢谢1年前查看全部
- 形成酸雨的原因是空气受到--和氮氧化合物的污染.请举一例说明酸雨对人类的破坏是什么
 qw03121年前3
qw03121年前3 -
 鬼鬼21 共回答了23个问题
鬼鬼21 共回答了23个问题 |采纳率100%二氧化硫和氮氧化合物,
分为“湿沉降”与“干沉降”两大类,前者指的是所有气状污染物或粒状污染物,随着雨、雪、雾或雹等降水型态而落到地面者,后者则是指在不下雨的日子,从空中降下来的落尘所带的酸性物质.
1.城市大气污染严重程度的改变了季节变化和昼夜变化的规律,大体可分为煤炭型和石油型两类.煤炭型是燃煤引起,因此污染强度以对流最强的夏季和白天为最轻,而以逆温最强、对流最弱的冬季和夜间为最重.伦敦烟雾事件就属于这种类型.石油型是石油和石油化学产品和汽车尾气所产生,由于氮氧化物和碳氢化物等生成光化学烟雾时需要较高气温和强烈阳光,因此污染强度变化规律和煤炭型刚刚相反,即以夏季午后发生频率最高,冬季和夜间少或不发生.洛杉矶光化学烟雾就属于这个类型.
2.此外,城市云量增多的结果,使城区日照时数和太阳辐射量均有减少.城市中烟尘粒子增多的结果,使大气透明度变差,所以有人称城市为“烟霾岛”或“混浊岛”.烟尘大量削弱太阳光中的紫外线部分(在太阳高度较低时甚至可减少30%一50%),这对城市居民的身体健康也是不利的.
3.酸雨可导致土壤酸化.我国南方土壤本来多呈酸性,再经酸雨冲刷,加速了酸化过程;我国北方土壤呈碱性,对酸雨有较强缓冲能力,一时半时酸化不了.土壤中含有大量铝的氢氧化物,土壤酸化后,可加速土壤中含铝的原生和次生矿物风化而释放大量铝离子,形成植物可吸收的形态铝化合物.植物长期和过量的吸收铝,会中毒,甚至死亡.酸雨尚能加速土壤矿物质营养元素的流失;改变土壤结构,导致土壤贫脊化,影响植物正常发育;酸雨还能诱发植物病虫害,使作物减产.
4.酸雨能使非金属建筑材料(混凝土、砂浆和灰砂砖)表面硬化水泥溶解,出现空洞和裂缝,导致强度降低,从而建筑物损坏.建筑材料变脏,变黑,影响城市市容质量和城市景观,被人们称之为 “黑壳"”效应.1年前查看全部
- 氨和氮氧化合物NOx反应通式
 happy小不点1年前1
happy小不点1年前1 -
 龙龙公主 共回答了15个问题
龙龙公主 共回答了15个问题 |采纳率86.7%4xNH3+6NOx=(2x+3)N2+6xH2O1年前查看全部
- 下列说法不正确的是( )A. 豆科植物通过根瘤菌吸收空气中的氮是化学变化B. 汽车尾气中排放的氮氧化合物是由游离态氮转
下列说法不正确的是( )
A. 豆科植物通过根瘤菌吸收空气中的氮是化学变化
B. 汽车尾气中排放的氮氧化合物是由游离态氮转化来的
C. 化石燃料燃烧通常不释放出氮氧化合物
D. 植物秸秆燃烧时放出氮氧化合物,参与了氮的循环 胖胖的小蚂蚁1年前2
胖胖的小蚂蚁1年前2 -
 开心小八 共回答了21个问题
开心小八 共回答了21个问题 |采纳率81%解题思路:A.化学变化一定有新物质的生成;
B.汽油燃烧时,空气中的氮气与氧气反应生成氮的氧化物;
C.化石燃料中含有氮元素,燃烧产生氮的氧化物;
D.植物秸秆含有氮元素,燃烧时反应生成氮的氧化物.A.豆科植物通过根瘤菌吸收空气中的氮,该过程氮元素由游离态转化为化合态,有新物质生成,是化学变化,故A正确;
B.汽油燃烧时,空气中的氮气与氧气反应生成氮的氧化物,故B正确;
C.化石燃料中含有氮元素,燃烧产生氮的氧化物,所以化石燃料燃烧能够释放出氮氧化合物,故C错误;
D.植物秸秆含有氮元素,燃烧时反应生成氮的氧化物,参与了氮的循环,故D正确;
故选:C.点评:
本题考点: 氮的固定;氮的氧化物的性质及其对环境的影响;常见的生活环境的污染及治理.
考点点评: 本题考查了氮的循环,题目难度不大,熟悉含氮物质和氮的固定的概念是解题关键,注意相关知识的积累.1年前查看全部
- (2004•普陀区二模)某氮氧化合物中N:O的质量比为7:4,该化合物的化学式______.
 lile22221年前1
lile22221年前1 -
 spincity 共回答了19个问题
spincity 共回答了19个问题 |采纳率94.7%解题思路:根据氮氧化合物,设出氧化物的化学式,利用元素的质量比确定原子个数比而得到化学式.设氮氧化合物的化学式为NxOy,
由N:O的质量比为7:4,则
14×x:16×y=7:4,
解得x:y=2:1,
即化学式为N2O,故答案为:N2O.点评:
本题考点: 有关化学式的计算和推断;元素质量比的计算.
考点点评: 本题考查化学式的确定,学生应学会利用正向思维先设出化学式,然后进行化学式的简单计算来确定化学式.1年前查看全部
- 造成温室效应的气体有(),还有氯氟烃、甲烷、氮氧化合物、臭氧等气体
造成温室效应的气体有(),还有氯氟烃、甲烷、氮氧化合物、臭氧等气体
A、二氧化碳 B、二氧化碳 C、氧气 D、氮气 huduan1年前1
huduan1年前1 -
 fcpop 共回答了21个问题
fcpop 共回答了21个问题 |采纳率95.2%A B1年前查看全部
- 请问氮氧化合物可以溶于水吗,溶于水后人饮用有什么危害,怎么样可以分解呢?
 ICECF1年前1
ICECF1年前1 -
 紫雨晴_uu 共回答了23个问题
紫雨晴_uu 共回答了23个问题 |采纳率95.7%一般不会,只是有一些用于肉类防腐添加剂的亚硝酸盐有化学致癌作用,长期摄入对身体有害1年前查看全部
- 空气质量报告中一般不涉及的有.A、二氧化硫B、二氧化碳C、氮氧化合物D、可吸入微粒说明原因、谢谢.
 爱玩手枪的小男孩1年前1
爱玩手枪的小男孩1年前1 -
 笑uu亿狼 共回答了17个问题
笑uu亿狼 共回答了17个问题 |采纳率88.2%二氧化碳1年前查看全部
- 氮氧化合物在破坏臭氧层的过程中起到了什么作用
 SkyIsland1年前1
SkyIsland1年前1 -
 xuanze110 共回答了10个问题
xuanze110 共回答了10个问题 |采纳率90%催化剂1年前查看全部
- 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
A. NO2
B. N2O2
C. N2O
D. N2O4 playero1年前1
playero1年前1 -
 午后二点 共回答了17个问题
午后二点 共回答了17个问题 |采纳率100%解题思路:根据该氮氧化合物与足量的灼热铜粉完全反应的原理以及气体体积差量法来计算.假设反应为:2NxOy+2yCu
加热
.
2yCuO+xN2,根据题中数据,反应后气体体积为反应前气体体积的一半,即可以得到x=1,
因为4Cu+2NO2=4CuO+N2,方程式的系数之比等于物质的量之比,所以反应前有NO222.4L即1mol,所以反应后有N20.5mol,所以是NO2 ,
故选A.点评:
本题考点: 复杂化学式的确定.
考点点评: 本题是一道有关物质化学式确定的题目,注意差量法在解题中的灵活运用,难度不大.1年前查看全部
- 物质中能否提取氧气?一氧化碳、碳氢化合物、氮氧化合物、二氧化硫、某些重金属化合物、铅化合物、黑烟及油雾、甲醛等中.能否提
物质中能否提取氧气?
一氧化碳、碳氢化合物、氮氧化合物、二氧化硫、某些重金属化合物、铅化合物、黑烟及油雾、甲醛等中.能否提取氧气呢? 麻辣米粒1年前1
麻辣米粒1年前1 -
 翁田帅哥 共回答了25个问题
翁田帅哥 共回答了25个问题 |采纳率88%能,理论上它有O元素就可以,只不过得到氧气貌似需要巨大的能量1年前查看全部
- 液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放量减少70%以上,氮氧化合物
液化石油燃气汽车简称LPG汽车,该燃气汽车的CO排放量比汽油车减少90%以上,碳氢化合物排放量减少70%以上,氮氧化合物排放量减少35%以上,是目前较为实用的低排放汽车.为检验一辆燃气汽车的刹车功能,进行了如下实验:在路旁竖起一标志杆,车以v0=72km/h的速度匀速行驶,当车头距标志杆s=20m时,实验室工作人员向司机下达停车的指令,司机经时间t0=0.8s(即反应时间)后开始刹车,若车在标志杆前停止运动,则符合安全要求,已知车与驾驶员总质量M=l 000kg,g=10m/s2.求:
(1)刹车过程中的制动力至少多大?
(2)现把该车改装为双动力系统,在平路行驶时,只采用燃气动力驱动,发动机的额定功率为15kW,能获得的最大速度v1=15m/s.当车在路面情况相同、倾角为370足够长的斜坡上行驶时,采用电力与燃气双动力系统,发动机的总功率为34kW,在该功率下经过20s由静止达到最大速度,求该过程中车沿斜面运动的路程. Peony_Pavilion1年前1
Peony_Pavilion1年前1 -
 杨柳岸晚风残月 共回答了25个问题
杨柳岸晚风残月 共回答了25个问题 |采纳率84%解题思路:(1)从发现情况到完全停止所用的时间包括反应时间和刹车时间;根据公式s=vt,求出反应时间内行驶的路程,汽车在这段时间内行驶的总路程等于反应距离加上刹车距离,根据公式2as=v2-
再求出加速度,根据牛顿第二定律求得制动力.也可以使用动能定律来求.v 20
(2)汽车获得的最大速度时,阻力等于汽车的牵引力,从而求出汽车受到的阻力;对倾角为37°的斜面上的汽车进行受力分析,求出汽车达到最大速度时的牵引力,然后根据瞬时功率的表达式求出最大速度,最后使用动能定律求得该过程中车沿斜面运动的路程.(1)在反应时间0.8s内行驶的路程s1=v0t1=20m/s×0.8s=16m,剩下的路程为;s2=s-s1=20m-16m=4m由动能定律得:-Fs2=0-12Mv20代入数据得:F=5×104N(2)汽车获得的最大速度时,阻力等于汽车的牵引力,所以:P=F1v1=f...
点评:
本题考点: 动能定理的应用;功率、平均功率和瞬时功率.
考点点评: 此题主要考查的是学生对速度计算公式的理解和掌握,弄清楚汽车行驶的路程是解决此题的关键.1年前查看全部
- 光化学烟雾是排入大气的氮氧化合物和碳氢化合物等受太阳紫外线作用产生的一种具有刺激性的浅蓝色的烟雾.你认为美国洛杉矶一年中
光化学烟雾是排入大气的氮氧化合物和碳氢化合物等受太阳紫外线作用产生的一种具有刺激性的浅蓝色的烟雾.你认为美国洛杉矶一年中最易发生光化学污染的月份是
A. 1月
B. 4月
C. 7月
D. 11月
 haikuo5551年前1
haikuo5551年前1 -
 娃哈哈on0 共回答了24个问题
娃哈哈on0 共回答了24个问题 |采纳率83.3%答案C
本题考查大气污染.洛杉矶受地中海气候影响,夏季高温少雨,最容易发生光化学烟雾事件,故选C项.1年前查看全部
大家在问
- 1易形成离子化合物元素的特征
- 2有一列有规律地数1/2,4/7,13/24,44/81等,在这组数中,从左往右第6个数是多少
- 3体积是矢量还是标量?这个问题可能有些弱智,我还没读高中,可是两个体积相加又不一定遵循标量的相加规律,比如酒精和水混合,这
- 40,1,3,6,10,15,21·········它们的规律是什么?
- 5华罗庚数学竞赛题 决赛题讲解不用太复杂、尽量简单一点、把各种题型的公式告诉我就可以的、最好加上讲解、没有讲解也行.全班就
- 6什么化合物极易溶于水
- 7不行力,但学文,长浮华,成何人?但力行,不学文;任己见,昧真理.中的重要词的意思
- 8姓 倪 的倪字粤语怎么读
- 9quick and easy cooking
- 101 1 2 4 7 13 24 44 81 求第n项的表达式
- 11在三角形ABC中,角A=角C=15度,AB=2a,则三角形ABC的高AE=?
- 121 2 4 7 13 24 44 81 149 274 504 927 找规律
- 13如何计算倾斜放置的卧式储油罐的液体体积
- 14_____,we missed our train the day when we were back to Paris
- 15温暖的英文怎么写