某毛纺厂女职工占全厂人数的五分之三,女职工比男职工多百分之几?男职工比女职工少百分之几?
 zhuyaol8410262022-10-04 11:39:541条回答
zhuyaol8410262022-10-04 11:39:541条回答求 又算是过程要清楚昂

已提交,审核后显示!提交回复
共1条回复
 tclls1 共回答了13个问题
tclls1 共回答了13个问题 |采纳率84.6%- 女比男多(3/5-2/5)/(2/5)=50%
男比女少(3/5-2/5)/(3/5)约=33.3% - 1年前
相关推荐
- 线性规划问题一个毛纺厂用羊毛和兔毛生产A,B,C三种混纺毛料,生产1单位产品需要的原料(万单位)数如下表所示: A B
线性规划问题
一个毛纺厂用羊毛和兔毛生产A,B,C三种混纺毛料,生产1单位产品需要的原料(万单位)数如下表所示:
A B C
羊毛 3 1 4
兔毛 2 3 4
已知A产品的产品数应为B的2倍,三种产品的单位利润分别为4,1,5元,每月可购进羊毛8万单位,兔毛3万单位。问如何安排生产才能使利润最大?(建立问题的线性规划模型,不需要求解)
 昆虫90131年前1
昆虫90131年前1 -
 落九天 共回答了14个问题
落九天 共回答了14个问题 |采纳率92.9%max=4x+y+5z
s.t.
3x+y+4z1年前查看全部
- 2009年某毛巾厂生产棉纺毛巾100万条,每条毛巾的价值量为24元。如果2010年该毛纺部门生产这种毛巾的劳动生产率提高
2009年某毛巾厂生产棉纺毛巾100万条,每条毛巾的价值量为24元。如果2010年该毛纺部门生产这种毛巾的劳动生产率提高20%,受金融危机的影响该毛巾厂减产10%,其他条件不变,则该毛巾厂毛巾的价值总量和单位商品的价值量分别为 [ ]A、1800万元 24元
B、1800万元 20元
C、2400万元 24元
D、2400万元 20元 xinjianxiaoyu1年前1
xinjianxiaoyu1年前1 -
 ebony123 共回答了20个问题
ebony123 共回答了20个问题 |采纳率85%B1年前查看全部
- 2010年某毛巾厂生产棉纺毛巾100万条,每条毛巾的价值量为24元.如果2011年该毛纺部门生产这种毛巾的劳动生产率提高
2010年某毛巾厂生产棉纺毛巾100万条,每条毛巾的价值量为24元.如果2011年该毛纺部门生产这种毛巾的劳动生产率提高20%,受金融危机的影响该毛巾厂减产10%,其他条件不变,则该毛巾厂毛巾的价值总量和单位商品的价值量分别为 ( )
A.1800万元.24元 B.1800万元.20元
C.2400万元.24元 D.2400万元.20元 lililjf1年前1
lililjf1年前1 -
 liu1in 共回答了19个问题
liu1in 共回答了19个问题 |采纳率84.2%.
楼上的,
商品价值量才是由社会必要劳动时间决定的
答案是B.2011年“该毛纺部门”是指社会劳动生产率,商品的社会劳动生产率与价值量成反比,故2011年每条毛巾的价值量为24/(1+20%)=20.而该毛巾厂减产10%,该毛巾厂的个别劳动生产率并未提高,则2011年该毛巾厂生产了100X(1—10%)=90万条毛巾,故价值总量为20X90万=1800万元.1年前查看全部
- 某毛纺厂某年上半年生产情况如下:
某毛纺厂某年上半年生产情况如下:
毛线产量(千克)
毛线等级
一季度
二季度
出厂价格(元)
一级品
600
500
28
二级品
350
100
20
三级品
50
100
15
要求:(1)计算平均等级说明产品质量变化情况.
(2)由于质量变化对该厂总产值的影响. 姜立羽1年前1
姜立羽1年前1 -
 blue_starts 共回答了16个问题
blue_starts 共回答了16个问题 |采纳率93.8%北京信息科技大学 《统计学》课程期末考试试卷(A卷)
2007 ~2008学年第一学期
课程所在学院:经济管理学院
一、单项选择题(本大题共15小题,每小题1分,共15分)
在每小题列出的四个备选项中只有一个是符合题目要求的,请将其代码填写在题后的括号内.错选、多选或未选均无分.
1.下列哪个不属于一元回归中的基本假定( D ).
A.对于所有的X,误差项的方差都相同
B.误差项 服从正态分布
C.误差项 相互独立
D.
2.某组数据分布的偏度系数为负时,该数据的众数、中位数、均值的大小关系是( A ).
A.众数>中位数>均值
B.均值>中位数>众数
C.中位数>众数>均值
D.中位数>均值>众数
3.一元回归方程为y=11.64一0.25x,则下列说法中正确的是( C ).
A.自变量平均增长一个单位,因变量减少0.25个单位
B.自变量和因变量之间成正相关关系
C.
D.
4.有甲乙两组数列,则( A )数列平均数的代表性高.
A. 1< 2 1> 2,则乙数列平均数的代表性高
B. 1< 2 1> 2,则乙数列平均数的代表性低
C. 1= 2 1> 2,则甲数列平均数的代表性高
D. 1= 2 1< 2,则甲数列平均数的代表性低
5.某连续变量数列,其末组为开口组,下限为500,相邻组的组中值为480,则末组的组中值为( A ).
A.520 B.510 C.500 D.540
6.不受极端变量值影响的平均数是( D ).
A.算术平均数 B.调和平均数
C.几何平均数 D.众数
7.有20个工人看管机器台数资料如下:2,5,4,4,3,4,3,4,4,2,2,4,3,4,6,3,4,5,2,4,如按以上资料编制频数分布数列应采用( A ).
A.单项式分组 B.等距分组 C.不等距分组 D.以上几种分组均可以
8.若无季节变动,则季节比率应为( B ).
A.0 B. 1 C. 大于1 D. 小于1
9.如果一个定性的变量有m类,则要引进( C )个虚拟变量.
A.m B.m+1
C.m-1 D.无法判断
10.第一组工人的平均工龄为5年,第二组为7年,第三组为10年,第一组工人数占总数的20%,第二组占60%,则三组工人的平均工龄为( B )
A.8年 B.7.2年 C.5年 D.7.8年
11.某企业2007年各种产品的产量比2006年增长了8%,总生产费用增长了12%,则该厂2007年单位成本( D )
A.减少了0.62% B.增加了0.62%
C.减少了3.7% D.增加了3.7%
12.相关系数r与斜率b2的符号( A ).
A.相同 B.不同
C.无法判断
13.已知小姜买的两种股票的综合价格指数上涨了24点,本日股票的平均收盘价格为14元,前日股票的平均收盘价格为( C )
A.10.64 B.10.5
C.11.29 D.无法计算
14.若今年比去年的环比发展速度为112%,去年比前年的环比增长率为3%,那么今年比前年的平均增长率为( D ).
A.9.0% B.7.4%
C.7.5% D.15.4%
15.已知今年增长1%的绝对值为0.54,去年比前年增长的绝对值为5,则去年比前年的增长率为( C ).
A.9.3% B.8.7%
C.10.2% D.无法计算
二、多项选择题(每小题2分,共16分)
在每小题列出的若干选项中有多个选项是符合题目要求的,请将正确选项前的字母填在题后的括号内.多选、少选、错选均无分.
1.下列变量,属于离散变量的有( A D E F ).
A.库存产品数量 B.流动资产1年前查看全部
- 一道六年级的应用题某毛纺厂女职工占全厂总人数的五分之四,女职工比男职工多百分之几?男职工比女职工少百分之几?
 grass_gq1年前3
grass_gq1年前3 -
 西北土狼 共回答了19个问题
西北土狼 共回答了19个问题 |采纳率89.5%男职工占全厂总人数的 1-4/5=1/5
女职工比男职工多(4/5-1/5)÷1/5×100%=300%
男职工比女职工少(4/5-1/5)÷4/5×100%=75%1年前查看全部
- (2012•泰州一模)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还
(2012•泰州一模)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下:
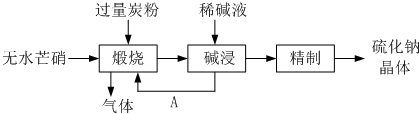
(1)上述流程中“碱浸”后,物质A必须经过______(填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为3Na2SO4+8C
3Na2S+4CO2↑+4CO↑△ .3Na2SO4+8C.
3Na2S+4CO2↑+4CO↑△ .
(2)上述流程中采用稀碱液比用热水更好,理由是______.
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,则此时溶液中c(S2-)=______.(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)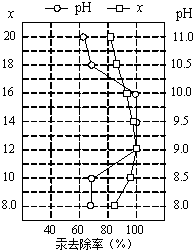 (4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示).为使除汞效果最佳,应控制的条件是______、______.
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示).为使除汞效果最佳,应控制的条件是______、______.
②某毛纺厂废水中含0.001mol•L-1的硫化钠,与纸张漂白后的废水(含0.002mol•L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有______. 地球211年前1
地球211年前1 -
 blinrong 共回答了11个问题
blinrong 共回答了11个问题 |采纳率100%解题思路:(1)从获得固体A的原混合物状态分析操作方法,由于煅烧时加入过量的炭粉,且固体A可以分离并进行煅烧的应用分析A是什么物质;依据题干信息可知生成物中除含有硫化钠外还含有一氧化碳和二氧化碳,以及两种碳的氧化物分子个数比是1:1进行分析判断即可;
(2)依据硫化钠溶液中硫离子水解显碱性的水解平衡影响因素分析判断;
(3)常温时CuS、Cu(OH)2的Ksp,依据溶度积常数计算得到,依据溶液PH计算溶液中铜离子浓度,依据CuS的Ksp计算得到硫离子的浓度;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值;
②依据硫化钠和次氯酸钠在溶液中发生的氧化还原反应电子守恒计算分析判断.(1)由于固体A是从液体中获得,所以得到A的操作是过滤,由于煅烧时加入过量的炭粉,且固体A可以分离并进行煅烧的应用可知A是炭粉,化学式为C;从题干信息可知生成物中除含有硫化钠外还含有一氧化碳和二氧化碳,而反应物是硫酸钠和碳,根据煅烧时一氧化碳和二氧化碳的分子个数比是1:1,所以可设两种气体的化学计量数分别是1和1,可得该反应的方程式为:[3/4]Na2SO4+2C
高温
.
[3/4]Na2S+1CO2↑+1CO↑,该反应两边同乘以4所得的反应方程式为:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑,
故答案为:过滤;3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑;
(2)上述流程中采用稀碱液比用热水更好,硫化钠溶液中硫离子水解显碱性,水解过程是吸热反应,加热促进水解进行,稀碱溶液能起到抑制水解的作用,
故答案为:热水会促进Na2S水解,而稀碱液能抑制Na2S水解;
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20,
Ksp=c(Cu2+)×c2(OH-)=2.2×10-20,pH=4,c(OH-)=10-10mol/L,c(Cu2+)=2.2mol/L,硫化铜中的Ksp=c(Cu2+)c(S2-)=8.8×10-36、计算得到c(S2-)=4×10-36mol/L;
故答案为:4×10-36;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值是x=12 pH介于9~10之间时汞的去除率最大,接近100%;
故答案为:x=12pH介于9~10之间
②某毛纺厂废水中含0.001mol•L-1的硫化钠,与纸张漂白后的废水(含0.002mol•L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,次氯酸钠和硫化钠发生氧化还原反应,n(Na2S):n(NaClO)=0.001mol/L×1:0.002mol•L-1×2=1:4,依据电子守恒分析可知,Na2S+4NaClO=Na2SO4+4NaCl,处理后的废水中所含的主要阴离子有
SO42-、Cl-;
故答案为:SO42-、Cl-.点评:
本题考点: 含硫物质的性质及综合应用;盐类水解的应用.
考点点评: 本题是物质制备的考查题,主要是化学方程式书写方法,溶度积常数的计算分析,氧化还原反应电子守恒的计算应用,掌握基础是关键,题目难度中等.1年前查看全部
- 这个字不知道怎么读左边是绞丝旁,右边是邮寄的寄的字读什么,这个是一个毛纺原料,叫“*麓丝”* 代表的就是这个子,还有叫它
这个字不知道怎么读
左边是绞丝旁,右边是邮寄的寄的字读什么,这个是一个毛纺原料,叫“*麓丝”* 代表的就是这个子,还有叫它莱赛尔的 最爱是xx1年前1
最爱是xx1年前1 -
 爱在轻度台风 共回答了15个问题
爱在轻度台风 共回答了15个问题 |采纳率93.3%左绞丝旁,右边为13笔的只有缰 缱缲缳缴.1年前查看全部
- 【化学--选修2:化学与技术】Ⅰ.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO
【化学--选修2:化学与技术】
Ⅰ.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如图1所示: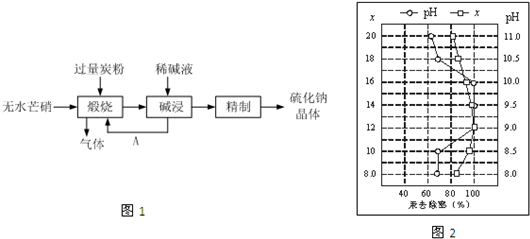
(1)上述流程中若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为3Na2SO4+8C
3Na2S+4CO2↑+4CO↑高温 .3Na2SO4+8C.
3Na2S+4CO2↑+4CO↑高温 .
(2)上述流程中采用稀碱液比用热水更好,理由是______.
(3)皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x 代表硫化钠的实际用量与理论用量的比值)有关(如图2所示).为使除汞效果最佳,应控制的条件是______、______.
(4)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,则此时溶液中c( S2-)=______.(保留两位有效数字)(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
Ⅱ.纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,常用的制备方法有电化学法、湿化学法等.
其中电化学法可用铜棒和石墨作电极,电解Cu(NO3)2稀溶液制备.
(5)电化学法制备Cu2O时,铜棒做______极,阴极生成Cu2O的电极反应式为______. qlust1年前1
qlust1年前1 -
 九月九的久 共回答了23个问题
九月九的久 共回答了23个问题 |采纳率95.7%解题思路:根据图1可知,制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C
3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡抑制硫离子水解,通过精制获得硫化钠晶体,高温 .
(1)根据通过信息确定反应物、生成物,然后根据“产生等物质的量的CO和CO2”及化合价变化相等写出反应的化学方程式;
(2)依据硫化钠溶液中硫离子水解显碱性的水解平衡影响因素分析判断;
(3)依据图象中曲线分析汞去除率最佳PH和x的取值;
(4)常温时CuS、Cu(OH)2的Ksp,依据溶度积常数计算得到,依据溶液PH计算溶液中铜离子浓度,依据CuS的Ksp计算得到硫离子的浓度;
(5)电化学法制备Cu2O时,阴极生成Cu2O,铜离子被还原,铜应为阳极,阳极生成铜离子,以补充铜离子.制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡煅烧产物得硫化钠溶液,通过精制获得硫化钠晶体,
(1)根据题干信息,硫酸钠与碳反应生成等物质的量的CO和CO2,C元素化合价从0价被氧化成+4、+2价,化合价升高至少为:(4-0)+(2-0)=6,硫酸钠中+6价S元素被还原为-2价,化合价降低了8价,则化合价变化的最小公倍数为24,则硫酸钠的系数为3,一氧化碳、二氧化碳的系数为4,然后根据质量守恒定律配平,配平后的化学方程式为:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑,
故答案为:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑;
(2)上述流程中采用稀碱液比用热水更好,硫化钠溶液中硫离子水解显碱性,水解过程是吸热反应,加热促进水解进行,稀碱溶液能起到抑制水解的作用,
故答案为:热水会促进Na2S水解,而稀碱液能抑制Na2S水解;
(3)依据图象中曲线分析,汞去除率最佳PH和x的取值是x=12 pH介于9~10之间时汞的去除率最大,接近100%,
故答案为:x=12; pH介于9~10之间;
(4)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌,若反应后测得溶液的pH=4,c(OH-)=10-10mol/L,
常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20,
根据氢氧化铜的溶度积可得:Ksp=c(Cu2+)×c2(OH-)=2.2×10-20,解得:c(Cu2+)=
2.2×10−20
(10−10)2mol/L=2.2mol/L,
根据硫化铜的溶度积可得:Ksp=c(Cu2+)c(S2-)=8.8×10-36,
则此时溶液中c( S2-)=
8.8×10−36
2.2mol/L=4.0×10-36mol/L,
故答案为:4.0×10-36mol/L;
(5)电解Cu(NO3)2稀溶液制备Cu2O时,阴极生成Cu2O,铜离子化合价降低被还原,电极方程式为:2Cu2++2e-+H2O═Cu2O+2H+,溶液中铜离子浓度减小,则阳极应该为铜,以补充消耗的铜离子,
故答案为:阳;2Cu2++2e-+H2O═Cu2O+2H+.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;化学电源新型电池;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查了物质制备、电解原理及其应用等知识,题目难度中等,试题涉及物质制备原理、化学方程式书写方法、电解原理及电极反应式的书写、溶度积常数的计算等,试题侧重考查学生的分析、理解能力及灵活应用所学知识的能力,是一道质量较好的题目.1年前查看全部
- 毛纺厂去年前七个月完成了全年生产计划的75%,再生产2700米,就可以比原计划多生产1100米,去年生产多少米
 jhl12341年前1
jhl12341年前1 -
 iammsan 共回答了21个问题
iammsan 共回答了21个问题 |采纳率90.5%(2700-1100)/(1-75%)=64001年前查看全部
- 【化学--选修2:化学与技术】Ⅰ.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用
【化学--选修2:化学与技术】Ⅰ.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用
【化学--选修2:化学与技术】
Ⅰ.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如图1所示: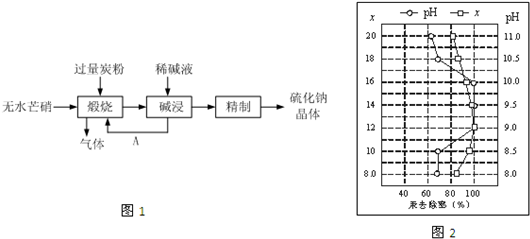
(1)上述流程中若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为3Na2SO4+8C
3Na2S+4CO2↑+4CO↑高温 .3Na2SO4+8C.
3Na2S+4CO2↑+4CO↑高温 .
(2)上述流程中采用稀碱液比用热水更好,理由是______.
(3)皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x 代表硫化钠的实际用量与理论用量的比值)有关(如图2所示).为使除汞效果最佳,应控制的条件是______、______.
(4)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,则此时溶液中c( S2-)=______.(保留两位有效数字)(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
Ⅱ.纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,常用的制备方法有电化学法、湿化学法等.
其中电化学法可用铜棒和石墨作电极,电解Cu(NO3)2稀溶液制备.
(5)电化学法制备Cu2O时,铜棒做______极,阴极生成Cu2O的电极反应式为______.
 青青果香1年前1
青青果香1年前1 -
 shalerbi1 共回答了22个问题
shalerbi1 共回答了22个问题 |采纳率95.5%制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡煅烧产物得硫化钠溶液,通过精制获得硫化钠晶体,
(1)根据题干信息,硫酸钠与碳反应生成等物质的量的CO和CO2,C元素化合价从0价被氧化成+4、+2价,化合价升高至少为:(4-0)+(2-0)=6,硫酸钠中+6价S元素被还原为-2价,化合价降低了8价,则化合价变化的最小公倍数为24,则硫酸钠的系数为3,一氧化碳、二氧化碳的系数为4,然后根据质量守恒定律配平,配平后的化学方程式为:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑,
故答案为:3Na2SO4+8C
高温
.
3Na2S+4CO2↑+4CO↑;
(2)上述流程中采用稀碱液比用热水更好,硫化钠溶液中硫离子水解显碱性,水解过程是吸热反应,加热促进水解进行,稀碱溶液能起到抑制水解的作用,
故答案为:热水会促进Na2S水解,而稀碱液能抑制Na2S水解;
(3)依据图象中曲线分析,汞去除率最佳PH和x的取值是x=12 pH介于9~10之间时汞的去除率最大,接近100%,
故答案为:x=12; pH介于9~10之间;
(4)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌,若反应后测得溶液的pH=4,c(OH-)=10-10mol/L,
常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20,
根据氢氧化铜的溶度积可得:Ksp=c(Cu2+)×c2(OH-)=2.2×10-20,解得:c(Cu2+)=
2.2×10?20
(10?10)2mol/L=2.2mol/L,
根据硫化铜的溶度积可得:Ksp=c(Cu2+)c(S2-)=8.8×10-36,
则此时溶液中c( S2-)=
8.8×10?36
2.2mol/L=4.0×10-36mol/L,
故答案为:4.0×10-36mol/L;
(5)电解Cu(NO3)2稀溶液制备Cu2O时,阴极生成Cu2O,铜离子化合价降低被还原,电极方程式为:2Cu2++2e-+H2O═Cu2O+2H+,溶液中铜离子浓度减小,则阳极应该为铜,以补充消耗的铜离子,
故答案为:阳;2Cu2++2e-+H2O═Cu2O+2H+.1年前查看全部
大家在问
- 1中秋节赏月的作文.500字左右,当时天气不太好,有很多云,月亮忽隐忽现的.不要复制的啊,都说了不要复制的了!
- 2同时掷两个质地均匀的骰子,计算下列事件的概率:
- 3辩论会 有关 课外活动时间少 的 论据
- 4形容朋友不够意思
- 5用英语对话在聚会上招待客人怎么说
- 6两直线平行,且一对同旁内角的差为90°,则这两个角的度数分别是?
- 7小明参加数学竞赛,共10道题,答对一题得10分,答错一题倒扣3分,小明共得72分,它答对了多少题?
- 8下列各组中,元素化学性质相似的是?
- 9英语翻译It's the fastest train in the world.It goes from Shangha
- 10当用右手定则和左手定则判断通电导线时,运动方向与受力方向相反,那通电导线还怎么运动?
- 11给妈妈写一封英文信,水平稍低一点.一百个英文单词左右.
- 12已知圆x²+y²–6y+m=0与直线x+2y–3=0相交于PQ两点,O为原点,且OP垂直OQ,求实数m的值。
- 13计算:(-2×11分之3)的200次方×(0.5×3又3分之2)的199次方
- 14Do you know the to the question?
- 15在通常情况下,水有哪些状态?它们形状、体积有什么特点谢谢了,大神帮忙啊
