蒸发溶液,溶质的质量分数变大吗?请举几个相反的例子,
 _心如止水_2022-10-04 11:39:541条回答
_心如止水_2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 sixi653166 共回答了14个问题
sixi653166 共回答了14个问题 |采纳率100%- 蒸发已经饱和的溶液(恒温),不管蒸走多少溶剂,溶液仍是饱和的.所以溶质的质量分数不变.
盐酸溶液,蒸发溶剂时,其中的溶质氯化氢也会蒸发,并且还快些,溶质质量分数变小. - 1年前
相关推荐
- 相同情况下,将水和酒精同时擦在手上,酒精更容易干,猜想液体蒸发快慢可能与什么有关
 susuge20051年前3
susuge20051年前3 -
 罗卡诺 共回答了26个问题
罗卡诺 共回答了26个问题 |采纳率88.5%与沸点高低和蒸发热有关.1年前查看全部
- 现有含糖10%的糖水200.想要得到20%的糖水该蒸发多少克水
 butterjm11年前3
butterjm11年前3 -
 我TMD疯了 共回答了22个问题
我TMD疯了 共回答了22个问题 |采纳率100%糖:200x10%=20(克)
需要留下的:20÷20%=100(克)
需要减去的:200-100=100(克)(蒸发的)哈哈哈1年前查看全部
- 有一瓶14%的氢氧化钾溶液,加热蒸发掉100g水后,得到28%的氢氧化钾溶液80mL,所得溶液的浓度为( )
有一瓶14%的氢氧化钾溶液,加热蒸发掉100g水后,得到28%的氢氧化钾溶液80mL,所得溶液的浓度为( )
A. 5mol/L
B. 6mol/L
C. 6.25mol/L
D. 6.5mol/L 无声无痕1年前1
无声无痕1年前1 -
 yugang82720000 共回答了14个问题
yugang82720000 共回答了14个问题 |采纳率78.6%解题思路:根据蒸发前后溶质的质量不变,计算出溶液的质量,根据质量分数计算溶质的物质的量,进而计算溶液的物质的量浓度.设14%氢氧化钾溶液的质量为x,蒸发前后溶质的质量不变,则有x×14%=(x-100g)×28%,x=200g,
28%的氢氧化钾溶液中含有氢氧化钾的物质的量为[100g×28%/56g/mol]=0.5mol,
所得溶液的物质的量浓度为[0.5mol/0.08L]=6.25mol/L,
故选C.点评:
本题考点: 物质的量浓度的相关计算;溶液中溶质的质量分数及相关计算.
考点点评: 本题考查物质的量浓度的计算,题目难度不大,本题注意计算蒸发后溶液的质量为解答该题的关键.1年前查看全部
- 下列各组混合物按溶解、过滤、蒸发的操作顺序进行分离的是( )
下列各组混合物按溶解、过滤、蒸发的操作顺序进行分离的是( )
A. 水和花生油
B. 蔗糖和泥沙
C. 面粉和泥沙
D. 蔗糖和食盐 XIaobing1111年前1
XIaobing1111年前1 -
 ee19成仁 共回答了20个问题
ee19成仁 共回答了20个问题 |采纳率90%解题思路:按照“溶解、过滤、蒸发”的步骤进行分离的物质,必须需要满足两种固体物质的溶解性不同,必须具备:一种不能溶于水,另一种物质能溶于水.A、水和花生油均是液体,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
B、蔗糖易溶于水,而泥沙不溶于水,能按溶解、过滤、蒸发的操作顺序分离,故选项正确.
C、面粉和泥沙均难溶于水,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
D、蔗糖和食盐均易溶于水,不能按溶解、过滤、蒸发的操作顺序分离,故选项错误.
故选:B.点评:
本题考点: 混合物的分离方法.
考点点评: 本题考查了混合物的分离,理解过滤的原理(是将不溶于液体的固体分离的方法)、掌握常见物质的溶解性是正确解答此类题的关键.1年前查看全部
- 20℃时有a物质的溶液300,恒温蒸发掉10克水,折出2克a物质,再蒸发
20℃时有a物质的溶液300,恒温蒸发掉10克水,折出2克a物质,再蒸发
(恒温)10克水,又折出4克a物质,则在蒸发20克水,又_____克a物质折
出,20℃a物质的溶解度是多少? 大致1年前3
大致1年前3 -
 liuvivi520 共回答了18个问题
liuvivi520 共回答了18个问题 |采纳率88.9%析出8克a物质,溶解度是40g
经过第一次恒温蒸发后,由于已经有a物质析出,故此时的溶液已经饱和;则由第二次蒸发可知,此物质的饱和溶液中,10g溶剂中能够溶解4g此物质,蒸发20g水则析出4*(20/10)=8;而溶解度即为4*(100/10)=40g1年前查看全部
- 蒸发和沸腾到底是不是物态变化?如果不是,那它们是什么?
蒸发和沸腾到底是不是物态变化?如果不是,那它们是什么?
有人说是,有人说不是,请给我一个正确答案! zwq6351年前2
zwq6351年前2 -
 幸福就像猫 共回答了25个问题
幸福就像猫 共回答了25个问题 |采纳率76%是物态变化.因为蒸发和沸腾产生的水蒸气,几乎与气态性质相同.即水的气态形式有两种,一种是无数水分子产生的水蒸气颗粒,一种是单个水分子产生的水的气态颗粒.这就像物质的最小物理颗粒是分子,但金属的最小物理颗粒是原子一样,所以蒸发和沸腾是物态变化.1年前查看全部
- 0度的水在0度的环境温度下是否蒸发?蒸发是否一定吸热?
0度的水在0度的环境温度下是否蒸发?蒸发是否一定吸热?
0度的水在0度的环境下怎么吸热? 译林1年前1
译林1年前1 -
 monkey8118 共回答了27个问题
monkey8118 共回答了27个问题 |采纳率88.9%蒸发一定吸热,吸热过程中,一部分水会变成含热量更低的冰,然后会维持一个动态平衡,水蒸发,水结冰,冰融化三者同时进行.当然,这是假定水完全不从外界进行热量交换的条件下才能实现的.1年前查看全部
- t℃时,将某硝酸钾溶液第一次蒸发掉l 0g水,冷却至原温度析出晶体1g;第二次蒸发掉10g水,冷却至原温度析出
t℃时,将某硝酸钾溶液第一次蒸发掉l 0g水,冷却至原温度析出晶体1g;第二次蒸发掉10g水,冷却至原温度析出晶体3g;第三次再蒸发掉10g水,冷却至原温度析出晶体应为( )
A.等于3g
B.大于3g
C.等于lg
D.小于或等于lg 一绝阿伟1年前1
一绝阿伟1年前1 -
 besd 共回答了18个问题
besd 共回答了18个问题 |采纳率88.9%在一定温度下,将某硝酸钾溶液蒸发掉10g水,析出晶体1g,说明这时候的溶液是饱和溶液;再蒸发掉10g水,析出3g硝酸钾,则可得出此温度下硝酸钾的溶解度就等于30g,再蒸发10g水,会析出3g晶体.
故选A.1年前查看全部
- 一道科学题加热蒸发食盐水提取盐时要用玻璃棒不断搅拌溶液的目的是___________
 william-19771年前2
william-19771年前2 -
 hu18zheng 共回答了12个问题
hu18zheng 共回答了12个问题 |采纳率91.7%是为了加快蒸发的速度1年前查看全部
- 在水中加入na2so4和kcl在水中会成离子形式存在,蒸发结晶后,会生成na2so4和kcl而不是nacl和k2so4
 酒醒无歌1年前2
酒醒无歌1年前2 -
 很拽的花生 共回答了14个问题
很拽的花生 共回答了14个问题 |采纳率78.6%四种物质都有,是混合物.不比纠结于此,认为发生了复分解反应.1年前查看全部
- 质量分数为30%的某溶液蒸发掉10g水后,溶液的质量分数变为40%,则原溶液的质量是( )
质量分数为30%的某溶液蒸发掉10g水后,溶液的质量分数变为40%,则原溶液的质量是( )
A. 30g
B. 40g
C. 50g
D. 60g amycao121年前1
amycao121年前1 -
 似雪梨花 共回答了20个问题
似雪梨花 共回答了20个问题 |采纳率95%解题思路:根据题意要求“原溶液的质量”那么设原溶液的质量为xg;认真审题后又知,蒸发水的前后溶质的质量是不变的,则可以表示成30%x,溶液的质量变为x-10;那么根据溶质的质量分数=[溶质的质量/溶液的质量]×100%,可以表示出新溶液的质量分数,从而解得x.设原溶液的质量是x,那么溶质的质量为30%x;由蒸发溶剂前后溶质的质量不变,则:蒸发溶剂水后溶质的质量分数=[30%x/x−10g]×100%=40%,解得:x=40g
故选:B点评:
本题考点: 有关溶质质量分数的简单计算.
考点点评: 本题是一道关于溶液变化前后的有关简单的计算,属于基础性内容;解答此题是要抓住蒸发溶剂前后溶质的质量不变,只是溶液的质量发生改变,根据这个等量关系可以列出数学方程进行解答.1年前查看全部
- 将质量分数为a%的NaOH溶液蒸发掉m g水后,变成V mL 2a%NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是
 3843851年前1
3843851年前1 -
 心宽不悔 共回答了18个问题
心宽不悔 共回答了18个问题 |采纳率88.9%(蒸发后仍为不饱和溶液,说明蒸发前也是不饱和溶液.因此没有NaOH晶体析出)
蒸发前后溶液中的NaOH的质量是不变的.
设原溶液总质量为Xg ,则溶液中NaOH质量为 (X*a%)g
蒸发mg水后 溶液总质量为 (X-m)g
(根据题目条件)蒸发后的 NaOH质量为 [(X-m)*2a%]g
由于前后NaOH质量不变
所以 (X*a%)g=[(X-m)*2a%]g
求出X的值 就可以求出NaOH的质量
然后除以NaOH的分子量 就是NaOH的物质的量了 再除以Vml 就是量溶度1年前查看全部
- 下列有关热现象的解释,正确的是( ) A.暮春,小草挂上露珠,是液化形成的 B.盛夏,人在电风扇下吹风感到清凉,是蒸发
下列有关热现象的解释,正确的是()
A.暮春,小草挂上露珠,是液化形成的 B.盛夏,人在电风扇下吹风感到清凉,是蒸发放热的原因 C.深秋,时有白霜生成,是凝固所致 D.隆冬,冰冻的衣物晾干,为汽化现象  周游世界1小时1年前1
周游世界1小时1年前1 -
 张惠cy 共回答了14个问题
张惠cy 共回答了14个问题 |采纳率85.7%解题思路:A. 露珠是空气中的水蒸气遇冷凝结成的小水滴,属于液化现象,该选项说法正确;
B. 人在电风扇下吹风,汗液蒸发,蒸发吸热,人感到凉快,该选项说法不正确;
C. 霜是空气中的水蒸气遇冷凝结成的小冰晶,属于凝华现象,该选项说法不正确;
D. 冰冻的衣服变干,冰直接变成水蒸气,属于升华现象,该选项说法不正确。
故选A.
A
1年前查看全部
- (2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴
(2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴趣小组要分析该化工厂仓库里的固体烧碱样品.
(1)小组成员猜测该样品中含有碳酸钠,支持这种猜测的依据是(用化学方方程式表示)______.小组成员选用了三种不同类别的试剂,进行实验,验证猜想,并得出结论,碳酸钠确实存在.请你将实验过程中涉及的化学方程式填在下表中.
(2)现已知样品中含有氯化钠、氢氧化钠、碳酸钠,设计一个实验方案,来证实一定含有氯化钠存在.化学方程式 试剂1 试剂2 试剂3 
请写出试剂X的化学式______
请写出①反应的化学方程式______
请写出②反应的化学方程式______. 烟雨楼家族之烟灰1年前1
烟雨楼家族之烟灰1年前1 -
 钱之光 共回答了20个问题
钱之光 共回答了20个问题 |采纳率85%解题思路:(1)烧碱易潮解,潮解之后容易和空气中的二氧化碳反应,检验烧碱变质的方法就是根据碳酸钠的化学性质来选择合适的试剂来鉴别
(2)加入试剂A后生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,可以据此答题(1)烧碱露置于空气中时易于空气中的二氧化碳反应而变质,在验证烧碱是否变质实际上就是验证碳酸钠的存在,故可以据其性质来区分,要注意的是当用盐酸时要向把氢氧化钠反应掉,然后才会有气体产生,故本题的答案为:CO2+2NaOH=Na2CO3+H2O
化学方程式
试剂1 Na2CO3 +CaCl2═2NaCl+CaCO3↓
试剂2 Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
试剂3
NaOH+HCl=NaCl+H2O
Na2CO3+2HCl=2NaCl+CO2↑+H2O (2)加入X生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,当加入稀硝酸时除了和碳酸钠反应,还要和氢氧化钠发生中和反应,在混合物中能和硝酸银生成白色沉淀的是氯化钠,
故本题答案为:HNO3 NaOH+HNO3=NaNO3+H2O; Na2CO3+2HNO3=2NaNO3+CO2↑+H2ONaCl+AgNO3=AgCl↓+NaNO3点评:
本题考点: 酸、碱、盐的鉴别;电解水实验.
考点点评: 解答本题要求学生熟练掌握酸、碱、盐的化学性质,并能根据物质之间能否反应及其反应的实验现象来得出结论,熟记化学方程式:CO2+2NaOH=Na2CO3+H2O;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓; NaOH+HCl=NaCl+H2O.1年前查看全部
- R22氟利昂的蒸发温度与压力的关系数值表
 伯昏有人1年前2
伯昏有人1年前2 -
 sotao 共回答了16个问题
sotao 共回答了16个问题 |采纳率93.8%Temperature (℃) → Pressure (MPa)-50 → 0.06453-49 → 0.067919-48 → 0.071448
-47 → 0.075121-46 → 0.078943-45 → 0.082917-44 → 0.087049-43 → 0.091341
-42 → 0.0958-41 → 0.10043-40 → 0.10523-39 → 0.11021-38 → 0.11538-37 → 0.12073
-36 → 0.12628-35 → 0.13203-34 → 0.13797-33 → 0.14413-32 → 0.1505-31 → 0.15708
-30 → 0.16389-29 → 0.17092-28 → 0.17819-27 → 0.18569-26 → 0.19344-25 → 0.20143
-24 → 0.20968-23 → 0.21819-22 → 0.22696-21 → 0.236-20 → 0.24531-19 → 0.25491
-18 → 0.26479-17 → 0.27496-16 → 0.28543-15 → 0.2962-14 → 0.30728-13 → 0.31867
-12 → 0.33038-11 → 0.34242-10 → 0.35479-9 → 0.36749-8 → 0.38054-7 → 0.39394
-6 → 0.40769-5 → 0.4218-4 → 0.43628-3 → 0.45113-2 → 0.46636-1 → 0.48198
0 → 0.497991 → 0.514392 → 0.53123 → 0.548424 → 0.566055 → 0.584116 → 0.60259
7 → 0.621518 → 0.640889 → 0.6606810 → 0.6809511 → 0.7016712 → 0.72286
13 → 0.7445314 → 0.7666815 → 0.7893116 → 0.8124417 → 0.8360718 → 0.8602
19 → 0.8848520 → 0.9100221 → 0.9357222 → 0.9619523 → 0.9887224 → 1.016
25 → 1.043926 → 1.072427 → 1.101428 → 1.130929 → 1.161130 → 1.1919
注意:此处用的压力是绝对压力.如果换算为表压,减去大约0.1MPa.1年前查看全部
- 1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
2 20度时,200克溶液浓度为15%,若保持在T度,再溶解4克该溶质或蒸发25克水后都可以使其饱和,求该物质在T度的溶解度
3 把5.9克氯酸钾和二氧化锰的混合物加热,直到不再产生气体为止,得到残余固体3.98克,求氧气得到多少升,残余固体的祖成
4 现有10克含杂质5%的大理石跟100克盐酸恰好完全反映,求盐酸的浓度,生成物溶液的浓度
- - dzhdhz1年前2
dzhdhz1年前2 -
 心若无底洞 共回答了23个问题
心若无底洞 共回答了23个问题 |采纳率91.3%1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
解析:设T度其溶解度为x有:120*x/100/(120-20)=(120*x/100+5)/(120+5) 解得x=16.7g
注意:其中120*x/100表示溶液120g中含有该物质的质量;120*x/100/(120-20)表示该物质蒸发掉20g水后饱和时的质量分数;(120*x/100+5)表示溶液120g再溶解5克溶质后溶质的总质量;(120*x/100+5)/(120+5)表示加5g溶质后溶液达饱和时的浓度.
2 20度时,200克溶液浓度为15%,若保持在T度,再溶解4克该溶质或蒸发25克水后都可以使其饱和,求该物质在T度的溶解度
解析:此题和上题类似,但不需要列方程,主要考查学生对溶解度和浓度的概念有没有弄清楚.
200克溶液浓度为15%则溶液中含有溶质的质量为:200*15%=30g,溶剂水的质量为200-30=170g,加4g溶质溶液饱和,则其溶解度为:(30+4)g/170g * 100=20g.
没弄懂以上两个概念不访再看看书.
3 把5.9克氯酸钾和二氧化锰的混合物加热,直到不再产生气体为止,得到残余固体3.98克,求氧气得到多少升,残余固体的祖成
解析:要知道发生的反应是:KClO3(加热和二氧化锰催化)=KCl+O2↑
有反应可知,反应物减少的质量是生成的氧气的质量5.9-3.98=1.92g锰催化,不参与反应,所以剩余固体应该为二氧化锰和氯化钾.知道了生成的氧气质量1.92查氧气的密度,就可以知道生成的氧气的体积了,我没有资料查,通过其他方法算的是1.344L
4 现有10克含杂质5%的大理石跟100克盐酸恰好完全反映,求盐酸的浓度,生成物溶液的浓度
大理石的主要成分是碳酸钙,其含杂质5%则10克大理石中碳酸钙的含量为10*95%=9.5g.
反应方程式:CaCO3+2HCL=CaCl2+H2O+CO2
100 73 111 44
知道了CaCO3的质量则反应中消耗的盐酸的质量为:9.5*73/100=6.94g,生成物氯化钙的质量为10.54g,生成的二氧化碳的质量为4.18g(以上数据的取舍原则采取分析化学中的四舍六入五成双的原则)所以盐酸的浓度为:6.94/100*%=6.94% 生成物氯化钙的浓度为:10.54/(100+9.5-4.18)*%=10%1年前查看全部
- 一吨质量的50度水进入负压环境开始蒸发,全部变为水蒸汽,需要吸收多少热量啊 ,考虑下汽化潜热?
 chow45341年前1
chow45341年前1 -
 494533671 共回答了11个问题
494533671 共回答了11个问题 |采纳率100%你知道这个热量有多大吗,你要干什?
1kg水蒸发冷在常压下考虑2450KJ的热量.
1吨水蒸发:带走的热量2450000KJ的热量,你知道热量由多大吗?
如果是流量是1t/h的流量,那么每秒带走的热量是680KW,这个才有实质的意义1年前查看全部
- 某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g晶体,再恒温蒸发掉10g水,又析出了3g晶体,则下列
某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g晶体,再恒温蒸发掉10g水,又析出了3g晶体,则下列说法正确的是( )
A. 原溶液在t℃时一定是不饱和溶液
B. 原溶液一定是稀溶液
C. 最后剩余的溶液一定比原溶液稀
D. 最后剩余溶液的溶质质量分数比原溶液的溶质质量分数小 北方的一条狼1年前1
北方的一条狼1年前1 -
 木鱼糖 共回答了19个问题
木鱼糖 共回答了19个问题 |采纳率94.7%解题思路:根据饱和溶液与不饱和溶液的概念分析;利用溶质质量分数的计算公式分析,溶质质量分数=溶质质量溶液质量×100%A、因为该溶液饱和后恒温蒸发掉10g水,要析出3g晶体,而刚开始恒温蒸发掉10g水,只析出了2g晶体,所以原溶液一定不是饱和溶液,故A正确;
B、溶液的浓稀只是相对来说的,所以不能讨论原溶液的浓稀;故B错误;
C、原溶液为不饱和溶液,而最后的溶液是该温度下的饱和溶液,所以最后的溶液一定比原溶液浓,故C错;
D、原溶液为不饱和溶液,而最后的溶液是该温度下的饱和溶液,所以最后的溶液溶质质量分数比原溶液的溶质质量分数大,故D错;
故选A点评:
本题考点: 晶体和结晶的概念与现象;饱和溶液和不饱和溶液;浓溶液、稀溶液跟饱和溶液、不饱和溶液的关系.
考点点评: 本题考查了饱和溶液和不饱和溶液的相关知识,饱和溶液:一定温度下,一定量的溶剂里不能继续溶解某物质的溶液;不饱和溶液:一定温度下,一定量溶剂里还能继续溶解某物质的溶液.1年前查看全部
- 根据图1和图2回答下列问题. (1)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母)______;A.水分子不
根据图1和图2回答下列问题. 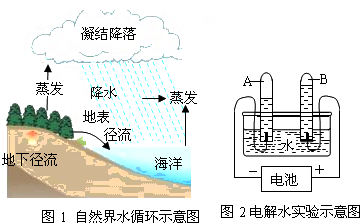
(1)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母)______;
A.水分子不断运动B.水分子之间间隔不变
C.氢、氧原子不发生改变D.水分子大小改变
(2)分析图2可知,试管A中的气体为______;B中的气体为______;正极和负极产生的气体体积之比为______.
(3)在电解水的过程中,下列说法不正确的是(填字母)______;
A.水分子发生了改变B.氢原子和氧原子没有发生变化
C.水分子可以保持水的化学性质 D.水分子是由氢分子和氧分子构成的
(4)面临淡水资源的短缺,小袁倡议“一水多用”.请你举出生活中的一项具体措施______. 碳妹1年前1
碳妹1年前1 -
 卖电视 共回答了20个问题
卖电视 共回答了20个问题 |采纳率95%(1)A、水分子不断运动,该观点符合分子是不断运动的特点,故A正确;
B、水分子之间间隔不变,水蒸发后体积变大,水分子本身没有改变,改变的是分子间的间隔,变大了,故B不正确;
C、氢、氧原子不发生改变,水蒸发是物理变化,水分子不变,其中的氢原子和氧原子也不变,故C正确;
D、水分子可以保持水的物理性质,分子是保持物质化学性质的最小粒子,当物质被分割小到分子时,只能保持物质的化学性质,而不能再保持物质的物理性质,故D不正确;
故选A、C.
(2)试管A中的气体体积大,故是氢气,化学式是 H 2 ,试管B中气体是氧气,电解水生成氧气和氢气的体积比是1:2;
(3)A.水分子发生了改变,在电解水反应中,水分子被分割成氢原子和氧原子,它们又重新组合成氢分子和氧分子,所以水分子改变了;故A不正确;
B.氢原子和氧原子没有发生变化,在化学变化中原子的种类和数目都没有改变,所以在电解水中,氢原子和氧原子没有发生变化;故B不正确;
C.水分子可以保持水的化学性质,水是由水分子构成的,分子是保持物质化学性质的最小粒子,所以水分子能保持水的化学性质;故C不正确;
D.水分子是由氢分子和氧分子构成的,水由水分子构成,只含有一种分子,属于纯净物,氢分子和氧分子是两种分子,它们合在在一起时属于化合物;故D正确.
故选D.
(4)“一水多用”的实例很多,如 用洗衣服的水冲马桶.
故答案为:(1)AC;
(2)H 2 ,O 2 ;1:2;
(3)D;
(4)用洗衣服的水冲马桶(合理即可).1年前查看全部
- 水在蒸发时会不会带走热量?(具体应是:热水、温水蒸发后水蒸气是热的,还是和凉水一样凉的?)
水在蒸发时会不会带走热量?(具体应是:热水、温水蒸发后水蒸气是热的,还是和凉水一样凉的?)
把手放在一杯热水上会感到发热。
另外把问题改为:热水在蒸发时,蒸发变成的水蒸气是( )。(以人体感觉为准)
A.热的 B.凉的 C.___(其他)
并请给出理由,拜托了。^_^ 卡卡蜜拉1年前4
卡卡蜜拉1年前4 -
 天唐 共回答了20个问题
天唐 共回答了20个问题 |采纳率100%答案是肯定的,不管它是热还是凉的.1年前查看全部
- 下列几种说法中错误的是( )A. 纯水的沸点是100℃B. 气温为0℃时,水不会蒸发C. 若物体大于平面镜,则在镜中不
下列几种说法中错误的是( )
A. 纯水的沸点是100℃
B. 气温为0℃时,水不会蒸发
C. 若物体大于平面镜,则在镜中不能成完整的像
D. 物体受热膨胀时,其密度会发生改变 specter00001年前1
specter00001年前1 -
 寻求真爱 共回答了25个问题
寻求真爱 共回答了25个问题 |采纳率84%解题思路:这是一道多项选择题.
(1)水的沸点与气压有关,气压越大沸点越高,气压越小沸点越低;
(2)蒸发是在任何温度下都能发生的,只在液体表面发生的,缓慢的汽化现象;
(3)像的大小取决于物体而不是平面镜的大小,不论多么小的平面镜,所成的像都是完整的;
(4)物体膨胀时,体积变化,所以其密度也会随之变化.(1)纯水在1标准大气压下沸点是100℃,由于题中没说在什么气压下,故A不正确;
(2)由于蒸发在任何温度下都能进行,所以0℃的水也会蒸发,故B不正确;
(3)小的平面镜也可以成大的像,成像是完整的,人看不完整不代表成像不完整,故C不正确;
(4)根据ρ=[m/V]可知,体积变化时,密度会变化,故D正确.
本题选择错误答案,故选A、B、C.点评:
本题考点: 平面镜成像的特点、原理、现象及其实验方案;沸腾及沸腾条件;蒸发及其现象;密度的大小比较.
考点点评: 小平面镜也可以成大物体的完整的像,这是易错点.1年前查看全部
- 固体混合物特点:各组分溶解度随温度变化差异不大方法:物理蒸发结晶 化学使用化学剂将其转变气体或沉淀
 xiao尧1年前1
xiao尧1年前1 -
 sadgkhagkjeg 共回答了24个问题
sadgkhagkjeg 共回答了24个问题 |采纳率83.3%各组分溶解度随温度变化差异不大,所以不能用蒸发结晶的方法,这样不能分离.
所以要用化学方法.1年前查看全部
- 为什么冬天干燥,夏天潮湿? 我觉得反过来才对,冬天的太阳没夏天的热,水蒸气蒸发也就很慢
 singerp1年前1
singerp1年前1 -
 burningls 共回答了16个问题
burningls 共回答了16个问题 |采纳率93.8%冬天降水少气温低,不利于水分的蒸发,自然就形不成水蒸气,湿度就低.夏季刚好相反.1年前查看全部
- 一杯水有450克,混合50克盐.等水蒸发完了里面的盐是不是还是50
 天意诚11年前2
天意诚11年前2 -
 gb212121 共回答了20个问题
gb212121 共回答了20个问题 |采纳率85%还是50g,水蒸发不会导致盐的质量的变化.1年前查看全部
- 水和酒精哪一种先蒸发完呢?
 jelfson1年前1
jelfson1年前1 -
 guyx06 共回答了13个问题
guyx06 共回答了13个问题 |采纳率100%对于初中物理“热现象”一章中“蒸发”的教学,我采用了用实验贯穿整个教学过程的方法,取得了很好的教学效果.今将教学过程介绍如下,以供同仁们参考.
1 用实验引入课题
1.1上课一开始首先做两个实验:
① 将少量的酒精倒在一个金属盘内,把盘子放到酒精灯上加热,很快盘子里的酒精就没有了.
② 又将少量的酒精倒一块小玻璃板上,并把玻璃板放在电风扇前面吹,若两分钟后,玻璃板上的酒精也不见了.
1.2 提出问题引入课题
学生:变成汽体跑到空气中去了.
学生:变成汽体跑到空气中去了.
2 用实验得出影响蒸发快慢的因素
实验1:拿两个相同的盘子,分别倒入同样多的酒精,将其中一个放到酒精灯上稍微加热,另一个不加热.两分钟后发现,加热的盘子内酒精蒸发完了,而没有加热的盘子内的酒精只蒸发了一点点.
引导学生分析得出:蒸发的快慢与温度有关,温度越高,蒸发就越快.
实验2:拿一个相同的盘子和一支试管,分别倒入同样多的酒精,将它们都放到电风扇前面吹风.两分钟后发现,盘子内酒精蒸发完了,而试管内的酒精只蒸发了一点点.
引导学生分析得出:蒸发的快慢与液体的表面积有关,液体的表面积越大,蒸发就越快.
实验3:拿两个相同的盘子,分别倒入同样多的酒精,将其中一个放到电风扇前面吹,另一个放到没有风的地方.过一会儿再看,发现有风吹的酒精减少快,没有风吹的酒精减少慢.有风吹和没有风吹,说明空气是否流动.
引导学生分析得出:蒸发的快慢与空气的流动有关,空气流动越快,蒸发就越快.
学生:与液体的温度、液体的表面积和液体表面的空气流动有关.
学生:将稻谷晾干时,晾在太阳下晒是为了提高温度;把稻谷展开的为了增大表面积;晾在有风的地方是因为那里的空气流动快.这样稻谷就干得快些.……小结:要加快蒸发,可以提高液体的温度,增大液体的表面积,加快液体表面上的空气流动;而要减慢蒸发,应该采取相反的措施.
3 用实验得出蒸发吸热
实验4:拿两支相同的温度计温度相同,将其中一支擦上酒精,另一支不擦酒精.过一会儿看,发现两支温度计的读数不同了.擦了酒精的那支读数减小了,没有擦酒精的温度计温度没变化.
实验5:在一个盘子里装大半盘酒精,用温度计测量酒精的温度,并且将温度计放在酒精内不拿出来;再将盘子放在电风扇前面吹,发现酒精不断减少的同时,温度计的读数也不断降低.
引导学生分析得出:液体蒸发要吸收热量.
老师:请同学们举例说说蒸发吸热的问题.1年前查看全部
- A杯盖上冒 B杯不盖帽 2小时哪个水温低 为什么是B杯 水蒸发会吸热 一吸热不就是B杯热
A杯盖上冒 B杯不盖帽 2小时哪个水温低 为什么是B杯 水蒸发会吸热 一吸热不就是B杯热
常识我知道 求专家解释道理 非非4171年前2
非非4171年前2 -
 6625398 共回答了19个问题
6625398 共回答了19个问题 |采纳率89.5%开盖子的蒸发快,蒸发吸热是被蒸发走的水蒸气吸收的,不是杯子里的水吸热,正相反,是杯子里的水被吸热了,所以B杯子凉的快.1年前查看全部
- 1::将200克10%的食盐水蒸发掉40克水,求溶液的溶质质量分数
1::将200克10%的食盐水蒸发掉40克水,求溶液的溶质质量分数
2:将200克10%的食盐水蒸发掉40克,有5克晶体析出.求溶液的溶质质量分数
3:将40克硝酸钾完全溶解在360克水中,要使溶质质量分数增大一倍,应蒸发多少克水 甜蜜妞儿1年前1
甜蜜妞儿1年前1 -
 我夫 共回答了18个问题
我夫 共回答了18个问题 |采纳率83.3%200×10%=20 20÷(200-40)=12.5%
200×10%=20 (20-5)÷(200-40-5)=9、67%
应该蒸发:(40+360)÷2=200克1年前查看全部
- 蒸发一定要吸收热量吗?求权威回答
蒸发一定要吸收热量吗?求权威回答
请大家回答时详细一点。最好能够举出有说服力的例证来,因为网上其他答案说吸热和不吸热的都有,没有例子,很难服众。
从微观上讲,蒸发就是物质分子自由扩散的过程。扩散不需要吸热,任何温度下都能发生,这怎么解释??
六七年都没解决的问题了,请求权威大侠给解释一下吧!!!!
谢谢“不会打字的黑客”的回答。但是,汽化有两种方式:蒸发和沸腾。
蒸发和沸腾是两个不一样的概念!~!
还是不明白,还是觉得蒸发在任何温度下都能发生,所以可以吸热但不必须吸热。也就是说不吸热也能发生蒸发。 可可天竹1年前3
可可天竹1年前3 -
 521rose 共回答了13个问题
521rose 共回答了13个问题 |采纳率76.9%补充:由于气态的分子势能一定比液态时的大,而蒸发前后的温度是一样的,所以从微观角度来讲,蒸发是一定吸热的.
蒸发是一个相变的过程,不该用分子的自由扩散来解释吧?在蒸发的过程中,分子是发生了变化的(分子势能变大).蒸发是由于物体的相失去了平衡而造成的,例如:一杯水,如果它不蒸发,那么它的液相和气相达到平衡,也就是气体分子转化成液体分子的速度与液体分子转化成气体分子的速度相等,前者放的热量会等于后者吸收 的热量.如果后者的速度快了的话,就发生了蒸发现象,前者放的热量会小于后者吸收的热量 ,所以整体要吸热.1年前查看全部
- 为什么水在阳光下比在室内蒸发得快800字作文的搜索结果
 xwijj1年前1
xwijj1年前1 -
 闪闪红星123 共回答了11个问题
闪闪红星123 共回答了11个问题 |采纳率100%室内的人堆,连同空气和音乐,杂乱地沸腾着.他们像一条泡在开水里的鱼,忍受不住灼热而挣扎叫嚣.即使筋疲力尽.身体与身体的摩擦,夹着...额上的汗珠在金色的阳光中蒸发1年前查看全部
- 将不饱和溶液蒸发,至开始有晶体析出时停止加热,这时得到的溶液是
将不饱和溶液蒸发,至开始有晶体析出时停止加热,这时得到的溶液是
如上.是 饱和溶液 还是 不饱和溶液?
为什么 小鱼瞎溜达1年前7
小鱼瞎溜达1年前7 -
 oO年 共回答了19个问题
oO年 共回答了19个问题 |采纳率84.2%饱和溶液.
从有晶体开始析出时就是饱和溶液了.因为溶液中已经不能溶解更多的溶质了.1年前查看全部
- 英语翻译“制冷剂在蒸发器内,在蒸发压力p0、蒸发温度t0下汽化,从被冷却对象中吸取热量Q0,实现制冷.汽化后的低温低压的
英语翻译
“制冷剂在蒸发器内,在蒸发压力p0、蒸发温度t0下汽化,从被冷却对象中吸取热量Q0,实现制冷.汽化后的低温低压的制冷剂蒸气被压缩机及时抽出,并压缩至冷凝压力pk,送入冷凝器.高温高压制冷剂蒸气在冷凝器内把热量Qk传递给环境冷却介质,首先被冷却然后冷凝为高压常温的制冷剂液体.该液体通过节流装置,降压降温为湿蒸气进入蒸发器,准备再次吸热汽化,这就是一次单级蒸气压缩式制冷循环.”
麻烦大神不要用各类翻译软件翻译整句话,那样翻译出来的东西有问题.另附上一些专业词汇:蒸发器evaporator压缩机compressor冷凝器condenser节流装置throttling device单级蒸气压缩式制冷single-stage
compression-type refrigeration cycle制冷剂refragerant汽化vaporize冷凝condense 投井下石651年前1
投井下石651年前1 -
 jonsh_8411669 共回答了16个问题
jonsh_8411669 共回答了16个问题 |采纳率81.3%LZ你好,我也很讨厌用翻译机的人,下面的人确实都是用翻译机的,我现在帮你改了一下,仅做参考,希望可以帮你一点忙
During the freezer is in the evaporator, it gasified when the pressure of evaporating is p0 and temperature of evaporating is t0.Then the freezer would absorb Q0 heat from the object and complete the process of refrigerating. Low temperature and low pressure refrigerant vapor vaporized timely drawn out by compressor, and compression to the condensing pressure PK, into the condenser. High temperature and high pressure refrigerant vapor in the condenser in the heat transfer to the environment Qk cooling medium. It would first be cooled and condensed into liquid refrigerant pressure at room temperature. The liquid through a throttling device, the pressure and temperature of wet steam into the evaporator, to prepare the next vaporize.This is a single stage vapor compression refrigeration cycle."1年前查看全部
- 卤素灯和氙气灯有啥区别据介绍,卤素灯,是在灯泡内渗入少量的的惰性气碘,从灯丝蒸发出来的钨原子与碘原子相遇反应,生成碘化钨
卤素灯和氙气灯有啥区别
据介绍,卤素灯,是在灯泡内渗入少量的的惰性气碘,从灯丝蒸发出来的钨原子与碘原子相遇反应,生成碘化钨化合物,当碘化钨化合物一接触白热化的灯丝(温度超过1450℃),又会分解还原为钨和碘,钨又重新归队回到灯丝中去,碘则重新进入气体中.如此循环不已,灯丝几乎不会烧断,灯泡也不会发黑,所以它要比传统的白炽前照灯寿命更长,亮度更大.现在的汽车普遍采用的都是这种前照灯.氙气灯,英文简称是hid.它所发出的光照亮度是普通卤素灯的两倍,而能耗仅为其三分之二,使用寿命可达普通卤素灯的十倍.氙气灯极大地增加了驾驶的安全性与舒适性,还有助于缓解人们夜间行驶的紧张与疲劳.驾车者可在第一时间内发现危险,从而获得足够的反应时间,很大程度减少了夜间事故发生率.目前***推出的全新奥迪、帕萨特、别克君威、马自达等豪华款均配备了氙气前照灯.从市场上看,氙气前照灯将会成为市场的主流.[groupid=1185]fjzznjwmc群组[/groupid] elba1年前1
elba1年前1 -
 adslgg 共回答了21个问题
adslgg 共回答了21个问题 |采纳率100%氙气灯,英文简称是HID.它所发出的光照亮度是普通卤素灯的两倍,而能耗仅为其三分之二,使用寿命可达普通卤素灯的十倍.查看原帖1年前查看全部
- 下列各组物质中,可依次通过溶解、过滤、蒸发等操作进行分离的是( )
下列各组物质中,可依次通过溶解、过滤、蒸发等操作进行分离的是( )
A. 氯化钾、氯化银
B. 碳酸钠、硝酸钡
C. 水、酒精
D. 木炭、二氧化锰 caiqingbo81821年前1
caiqingbo81821年前1 -
 d05lgavro0smrwd 共回答了18个问题
d05lgavro0smrwd 共回答了18个问题 |采纳率88.9%解题思路:能够通过用水溶解、过滤、蒸发等操作分离的物质要具有以下特点:一种物质溶于水,一种物质不溶于水,两种物质都溶于水或都不溶于水是不能分离的.A、氯化钾与氯化银一种溶于水一种不溶于水,符合题干要求的分离特点,故正确.
B、两者均溶于水不能利用溶解过滤蒸发的操作分离,故错误.
C、酒精易溶于水,不能与水通过溶解过滤蒸发分离,故错误.
D、两者均不溶于水,故不能通过溶解过滤蒸发操作,故错误.
故选A点评:
本题考点: 混合物的分离方法;过滤的原理、方法及其应用;蒸发与蒸馏操作.
考点点评: 通过回答本题知道了一种物质溶于水,一种物质不溶于水的分离方法是用水溶解、过滤、蒸发.1年前查看全部
- 关于蒸发和沸腾,下列说法错误的是哪一个[ ]
关于蒸发和沸腾,下列说法错误的是哪一个[ ]
1 蒸发和沸腾相比较,沸腾是剧烈汽化现象
2 蒸发是液体表面进行的汽化现象
3 在一标准大气压下,水的温度达到100℃就一定会沸腾
4 液体在任何温度下都会沸腾 dk761年前8
dk761年前8 -
 beaty9696 共回答了18个问题
beaty9696 共回答了18个问题 |采纳率77.8%3是错的.只有继续吸热才能沸腾.
4正确,可以通过改变气压使之沸腾1年前查看全部
- 将质量分数为百分之a,物质的量浓度为c1 mol/L 的稀硫酸蒸发掉一定量的水,使其质量分数为百分之2a 此时若物质的量
将质量分数为百分之a,物质的量浓度为c1 mol/L 的稀硫酸蒸发掉一定量的水,使其质量分数为百分之2a 此时若物质的量浓度为c2 mol/L,则 C1 和 C2 关系为:A C2=2C1 B C1>2C2 C C2>2C1 D C1=2C2 .
还有一道:标准状况下 ,1体积水可溶解500体积HCl 气体,现用一只充满干燥 HCl 气体的烧瓶倒置在足量的水中,请回答下列问题:
若烧瓶中溶液没有扩散,其物质的量浓度为 :.
要有过程阿,我都想半天了,就是不会做.
还有就是顺便问一下 ,用量筒量取液体时 仰视和俯视 读数 会使测量结果 偏大或偏小的问题? 洞天杯蓝丝带1年前1
洞天杯蓝丝带1年前1 -
 fan樊 共回答了18个问题
fan樊 共回答了18个问题 |采纳率83.3%1、c
2、设烧瓶体积为V,物质的量浓度为:V/22.4/V=1/22.41年前查看全部
- 500克与200克质量分数相同的氯化钾溶液在某一温度时恒温蒸发80克水,两者析出晶体质量比较
 我的故事无人能懂1年前1
我的故事无人能懂1年前1 -
 qw008 共回答了15个问题
qw008 共回答了15个问题 |采纳率80%200克的析出晶体质量比较大,(200克的氯化钾溶液在某一温度时恒温蒸发相对含值较小)1年前查看全部
- 取60g的氯化钾饱和溶液,将其恒温蒸发10g水,剩余溶液的质量为45g,则剩余溶液中所含
 令狐倾倾01年前1
令狐倾倾01年前1 -
 iori2000 共回答了22个问题
iori2000 共回答了22个问题 |采纳率86.4%剩余溶液中所含氯化钾质量为 45g*[(60g-45g-10g)/(60g-45g)]=15g1年前查看全部
- cuso4在30度时溶解度为25克,40度时为39克,把40度时18%的cuso4溶液100克,先蒸发50克再冷却到30
cuso4在30度时溶解度为25克,40度时为39克,把40度时18%的cuso4溶液100克,先蒸发50克再冷却到30度,析出胆矾多少克?
大哥,好像40度蒸发50克水也要析出胆矾的额 林筱下1年前1
林筱下1年前1 -
 诸葛默默 共回答了17个问题
诸葛默默 共回答了17个问题 |采纳率82.4%设析出xg,其中含CuSO4有16x/25 g
蒸发50gH2O以后溶液剩下50g,析出xg晶体后,剩余的溶液质量为50-x g,其中含有的CuSO4为(100*18%-16x/25)g,是饱和溶液
根据质量分数得方程:
25:(100+25)=(100*18%-16x/25):(50-x)
解得x=18.2g
40度蒸发水即使有析出不用管(或者就认为它是过饱和溶液),反正在最后一起考虑到了.1年前查看全部
- 1O%NaOH加热蒸发掉100g水后得到80ml20%溶液则其物质的量浓度为?
 爱新觉罗北北1年前1
爱新觉罗北北1年前1 -
 谁越走越远 共回答了12个问题
谁越走越远 共回答了12个问题 |采纳率100%设原10%溶液总质量为 m克
蒸发前后,溶液的质量不变
10%m = 20%(m-100)
m=200
NaOH的质量=200×10% = 20g
NaOH的物质的量=200=0.5mol
20%NaOH物质的量浓度= 0.5/ 0.08 = 6.25mol/L1年前查看全部
- 水循环中的陆地内循环有“地表径流蒸发”吗,如果有,起不起主要作用?
 yhnjiolp1年前0
yhnjiolp1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 下列自然现象与水的三态变化有什么关系,用线连起来.云 雾 霜 露 蒸发 请选择
下列自然现象与水的三态变化有什么关系,用线连起来.云 雾 霜 露 蒸发 请选择
A、水由气态变为液态
B、水由气态变为固态
C、水由液态变成气态 第四纪海水1年前2
第四纪海水1年前2 -
 巨蟹脚下的猪 共回答了17个问题
巨蟹脚下的猪 共回答了17个问题 |采纳率88.2%A、水由气态变为液态 霜 露
B、水由气态变为固态 雾 云
C、水由液态变成气态 蒸发1年前查看全部
- 加热蒸发自来水或天然水,发现蒸发皿中都留下些物质,这说明什么
 swdh1年前2
swdh1年前2 -
 海水鱼 共回答了19个问题
海水鱼 共回答了19个问题 |采纳率89.5%加热蒸发自来水或天然水,发现蒸发皿中都留下些物质,这说明——自来水或天然水中含有可溶性的杂质
如帮到了你,
【你的10分满意,我们团队的无限动力】1年前查看全部
- 某10% NaOH溶液,加热蒸发掉100g水后得到80mL20%的溶液,则该20% NaOH溶液的物
某10% NaOH溶液,加热蒸发掉100g水后得到80mL20%的溶液,则该20% NaOH溶液的物质的量浓度为( )
A. 6.25mol/L
B. 12.5mol/L
C. 7mol/L
D. 7.5mol/L alily9221年前1
alily9221年前1 -
 青花瓷11 共回答了17个问题
青花瓷11 共回答了17个问题 |采纳率82.4%解题思路:根据蒸发前后溶质的质量不变,计算出溶液的质量,根据质量分数计算溶质的物质的量,进而计算溶液的物质的量浓度.设10%氢氧化钠溶液的质量为x,蒸发前后溶质的质量不变,
则有x×10%=(x-100g)×20%,
解得x=200g,
20%的氢氧化钠溶液中含有氢氧化钠的物质的量为[100g×20%/40g/mol]=0.5mol,
所得20%氢氧化钠溶液的物质的量浓度为[0.5mol/0.08L]=6.25mol/L,
故选:A.点评:
本题考点: 物质的量浓度的相关计算.
考点点评: 本题考查物质的量浓度的计算,题目难度不大,本题注意计算蒸发后溶液的质量为解答该题的关键.1年前查看全部
- 30℃时,甲杯中盛有80克食盐饱和溶液,乙杯中盛有40克食盐饱和溶液.若各自蒸发掉20克水后再冷却到30℃时,甲杯中析出
30℃时,甲杯中盛有80克食盐饱和溶液,乙杯中盛有40克食盐饱和溶液.若各自蒸发掉20克水后再冷却到30℃时,甲杯中析出m1克食盐晶体,乙杯中析出m2克食盐晶体,则m1与m2的大小关系是(填大于、小于、相等)__________________.30℃时食盐的溶解度是_____________________(用含有m1或m2的式子表示).
是5m1,我要解题的思路和过程 kjwdszy1年前1
kjwdszy1年前1 -
 鱼翅 共回答了17个问题
鱼翅 共回答了17个问题 |采纳率88.2%1因为都是饱和溶液,质量分数相等,蒸发同样多的水,析出的晶体相同.所以相等.
2.因为20克水溶解m1克盐饱和,而都是饱和溶液,质量分数相等,所以设溶解度为x,
m2/(m2+20)=x/(x+100),解得x=5m1
(问一句,你也是初二的吗)1年前查看全部
- 一定温度下将a%的硝酸钾水溶液分成两等份,一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无
一定温度下将a%的硝酸钾水溶液分成两等份,一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无水晶体,则该温度下硝酸钾的溶解度为()
选项
A、10m克
B、20m克
C、30m克
D、(1000a/100-a)克 晃悠懒猫1年前1
晃悠懒猫1年前1 -
 萧岚 共回答了18个问题
萧岚 共回答了18个问题 |采纳率88.9%一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无水晶体,相当于在饱和溶液中蒸发10克水,析出晶体2m克
2m/10=S/100 S=20m g
选B1年前查看全部
- 在30℃时,把氯酸钾不饱和溶液等分成两份,恒温蒸发,一份蒸发去10克水析出晶体0.5克,另一份蒸发去20克水
在30℃时,把氯酸钾不饱和溶液等分成两份,恒温蒸发,一份蒸发去10克水析出晶体0.5克,另一份蒸发去20克水
析出晶体1.5克,则30℃时氯酸钾的溶解度是? henryxiang19801年前1
henryxiang19801年前1 -
 llhecf 共回答了17个问题
llhecf 共回答了17个问题 |采纳率94.1%蒸发10克水后溶液析出固体,说明蒸发10克水,溶液已经饱和
这样饱和溶液再蒸发10克水析出1.5-0.5=1克固体.(相当与原溶液直接蒸发20克水)
说明10克水溶解1克氯酸钾达到饱和
1/10=10/100 氯酸钾溶解度为10克/100克水1年前查看全部
- 33度时,有250克硝酸钾溶液,若向该溶液加入30克硝酸钾,恰好成为饱和溶液,若原溶液恒温蒸发掉60克水也恰好成为饱和溶
33度时,有250克硝酸钾溶液,若向该溶液加入30克硝酸钾,恰好成为饱和溶液,若原溶液恒温蒸发掉60克水也恰好成为饱和溶液,求33度时硝酸钾的溶解度
 muxi06231年前1
muxi06231年前1 -
 Metadata 共回答了20个问题
Metadata 共回答了20个问题 |采纳率95%说明30克硝酸钾加入60克水可以配成饱和溶液
所以溶解度是50克1年前查看全部
- 干湿泡温度计是用两个相同的温度计并列制成的,在使用时,其中一个温度计下端的玻璃泡包着湿布,因为水在蒸发时要______,
干湿泡温度计是用两个相同的温度计并列制成的,在使用时,其中一个温度计下端的玻璃泡包着湿布,因为水在蒸发时要______,所以这个温度计的读数要比另一个温度计的读数______.在相同室温下,两个温度计读数的差值越大,就表明空气中的水蒸气含量______.
 幼稚的小鬼1年前2
幼稚的小鬼1年前2 -
 5ishe 共回答了23个问题
5ishe 共回答了23个问题 |采纳率95.7%解题思路:要解答本题需掌握:蒸发是一种汽化现象,蒸发吸热,以及干湿温度计原理.干湿泡温度计测空气中水蒸气含量的大致原理:
干泡温度计放置在空气中,显示的是空气的正常温度;
湿泡温度计下端包着湿布,打开湿布后,湿泡上的水分蒸发吸热,因此湿泡温度计的示数比干泡温度计的示数低;
当空气中的水蒸气含量较高时,湿泡温度计上的水分蒸发较慢,温度下降的较少,干、湿温度计的示数差较小;
反之,当空气中的水蒸气含量较低时,湿泡温度计上的水分蒸发较快,温度下降的较多,两个温度计的示数差较大;
故答案为:吸热,低(小),低.点评:
本题考点: 蒸发及其现象.
考点点评: 本题主要考查学生对:蒸发吸热在生活中的应用的了解和掌握,是一道基础题.1年前查看全部
- 海水晒盐的过程中留下少量海水就停止蒸发,为什么
海水晒盐的过程中留下少量海水就停止蒸发,为什么
海水又苦又咸,我们从海水中得到的食盐却只咸不苦,是因为盐工们利用了化学原理的缘故.就是在晒盐的过程中故意留下少量海水就停止蒸发.为什么? jinerlilee1年前1
jinerlilee1年前1 -
 打肿鸟充ii 共回答了13个问题
打肿鸟充ii 共回答了13个问题 |采纳率100%为了防止其他物质蒸发结晶.成为杂质.
海水中有很多溶质,溶解度各不相同.我们要的是氯化钠,所以需要使氯化钠最大限度的结晶,同时还不能析出其他物质.所以留下少量的海水.1年前查看全部
大家在问
- 1父字的甲骨文怎么写可以解释一下这个甲骨文的含义吗?
- 21、We are eating honey.(变一般疑问句)
- 3已知函数y=1/2cos²x+√3/2sinxcosx+1,x∈R(1)求它的振幅周期和初相.(2)用五点法做
- 4英语大师们 帮帮忙翻译这个好吗?
- 5威尼斯之夜 威尼斯蓝天的妩媚和夜空的可爱无法用语言来描绘.在那明净的夜晚,河面水平如镜,连星星的倒影也不会有丝毫的颤动.
- 6计算题:机械方面有一机械系统如图所示,重物G=10000N,上升速度V=0.6m\s,卷筒直径D=0.9m\s;每对齿轮
- 7判断题:不可逆矩阵,奇异矩阵,降秩矩阵指的是同一概念.
- 8小明考试不及格,回家路上他的心情真是(),紧张极了.(填歇后语)
- 9甲、乙两数的和为100,甲是乙的一半多4,求甲、乙两数各是多少?
- 10植物的根不仅具有向地垂直生长的感应性现象,并且还有向较潮湿的地方生长的感应性现象,即植物具向水性.请你对植物的向水性提出
- 11不等式以a为底x的对数大于x-1的平方,恰有三个整数值,求a的范围
- 12英语翻译Cigarette,that is,ths length of our youth
- 13英语翻译1.我们在中学读书时共一张桌子 we share the same table when we study at
- 14海南有七个国家级自然保护区,请说出它们的名称和保护对象?
- 15反义疑问句在什么情况下后句是看从句的
