有两盘鸡蛋共173个,从第一盘取走38个后,第二盘的个数比第一盘的2倍还多6个,第二盘有多少个鸡蛋?
 feifan01072022-10-04 11:39:541条回答
feifan01072022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 待字闺中06 共回答了1个问题
待字闺中06 共回答了1个问题 |采纳率100%- 276
- 1年前
相关推荐
- 已平衡的托盘天平两盘的烧杯里,各盛有等质量且溶质质量分数相同的盐酸,现分别向其中投入等质量的金属镁和锌,充分反应.1.若
已平衡的托盘天平两盘的烧杯里,各盛有等质量且溶质质量分数相同的盐酸,现分别向其中投入等质量的金属镁和锌,充分反应.1.若天平仍保持平衡,那么一定有剩余的金属是 2.若天平失去,那么天平的指针一定会偏向加有金属 的一方
 yishui1983831年前1
yishui1983831年前1 -
 隆哼哼 共回答了14个问题
隆哼哼 共回答了14个问题 |采纳率71.4%1、镁 2、锌(两题都是考虑相对原子质量)1年前查看全部
- 把一些水果糖分别装在四个盘子里,其中20%放入甲盘,[1/4]放入乙盘,放入丙盘的水果糖是甲、乙两盘水果糖总数的[2/3
把一些水果糖分别装在四个盘子里,其中20%放入甲盘,[1/4]放入乙盘,放入丙盘的水果糖是甲、乙两盘水果糖总数的[2/3],丁盘放入10块水果糖,这些水果糖共有多少块?
 new3861年前1
new3861年前1 -
 ghy_007 共回答了19个问题
ghy_007 共回答了19个问题 |采纳率94.7%解题思路:把水果糖总块数看作单位“1”,先求出甲盘和乙盘装进水果块数占总块数的分率,并把此看作单位“1”,依据分数乘法意义,求出丙盘装进水果糖块数占总块数的分率,再求出甲,乙,丙三盘装进水果糖块数占总块数的和,进而求出丁盘水果糖块数占总块数的分率,也就是10块占总块数的分率,最后依据分数除法意义即可解答.10÷[1-(20%+[1/4])×[2/3]-20%-[1/4]]
=10÷[1-45%×[2/3]-20%-[1/4]]
=10÷[1-[3/10]-20%-[1/4]]
=10÷[1-75%]
=10÷25%
=40(块)
答:这些水果糖共有40块.点评:
本题考点: 分数四则复合应用题.
考点点评: 分数除法意义是解答本题的依据,关键是求出10块占总块数的分率.1年前查看全部
- 用天平称取10克氢氧化钠做法是先在托盘天平的两盘上各放______,再在右盘放入10克砝码
 qiaopz1年前1
qiaopz1年前1 -
 liaochuyu 共回答了23个问题
liaochuyu 共回答了23个问题 |采纳率91.3%相同质量的烧杯或称量瓶,不能放称量纸,氢氧化钠会吸潮.1年前查看全部
- 在已调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相等、质量分数相等的稀硫酸,然后在左右两盘的烧杯中分别放入
在已调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相等、质量分数相等的稀硫酸,然后在左右两盘的烧杯中分别放入等质量的铁粉和锌粒.下列现象不可能观察到的是( )
A. 只有锌粒有剩余
B. 天平指针最终偏向放锌粒的烧杯一边
C. 只有铁粉有剩余
D. 天平指针开始时偏向放铁粉的烧杯一边 单眼皮的边缘人1年前1
单眼皮的边缘人1年前1 -
 qd9981 共回答了22个问题
qd9981 共回答了22个问题 |采纳率77.3%解题思路:A、根据酸都被反应完,消耗的铁粉和锌粉的质量大小考虑;B、根据酸是足量的反应完后,比较铁粉与锌粉两种物质反应生成氢气的多少考虑;C、根据锌粉恰好与硫酸反应完,铁把硫酸反应完消耗质量的大小考虑;D、根据金属铁与锌的金属活动性考虑.A、等质量的铁和锌与足量酸反应时,铁生成的氢气多,锌生成的氢气少,如果铁与锌把酸都反应完了时,由于质量相等、质量分数相等的稀硫酸中含有的氢元素质量也相等,所以产生氢气质量相等,产生等质量的氢气时消耗的铁质量少,消耗的锌质量多,所以不可能出现只有锌粒有剩余的情况;故A不可能观察到;
B、如果酸是足量的,由于等质量的铁和锌与足量酸反应时,铁生成的氢气多,锌生成的氢气少,所以放铁的一边轻,天平指针最终偏向放锌粒的烧杯一边,故B现象能观察到;
C、等质量的铁和锌与足量酸反应时,铁生成的氢气多,锌生成的氢气少,如果铁与锌把酸都反应完了时,由于质量相等、质量分数相等的稀硫酸中含有的氢元素质量也相等,所以产生氢气质量相等,产生等质量的氢气时消耗的铁质量少,消耗的锌质量多,如果铁与锌都把硫酸反应完,锌与硫酸恰好完全反应时,这种情况时,只有铁粉有剩余,故C现象能观察到;
D、由于锌比铁活泼,开始反应速度快,产生的氢气多,开始放锌的一边产生的氢气多,放铁的一边质量大,天平指针开始时偏向放铁粉的烧杯一边,故D现象能看到.
故选A.点评:
本题考点: 金属的化学性质.
考点点评: 解答本题关键是要知道等质量的铁和锌与足量酸反应时,铁生成的氢气多,锌生成的氢气少,所以产生等质量的氢气时消耗的铁质量少,消耗的锌质量多.1年前查看全部
- 说明原因,thank you在天平两盘中各放一只大小和质量相同的烧杯,两烧杯中都盛有1mol/L的稀硫酸100ml,然后
说明原因,thank you
在天平两盘中各放一只大小和质量相同的烧杯,两烧杯中都盛有1mol/L的稀硫酸100ml,然后分别向两烧杯中加入一定质量的镁和锌,充分反应后天平仍保持平衡,则镁铝的质量分别是
A.0.1molMg 0.1Zn
B.5gMg 5gZn
C.6.5g 10g
D.6.5g 0.1mol Eve19851年前2
Eve19851年前2 -
 米饭XP 共回答了15个问题
米饭XP 共回答了15个问题 |采纳率86.7%Mg的相对原子质量为24,Zn的相对原子质量为65,要使两边平衡,只能镁的质量大于锌的质量或镁过量而锌不足量.此题中没有镁大于锌的选项,所以只能考虑镁过量而锌不足量的情况.
根据方程式得,
Mg+H2SO4=MgSO4+H2↑ △(增重质量)
24 2 22
Zn △
65 63
锌比镁增重41,所以当锌为1mol时镁应为65/24mol,以此类推,故答案为D1年前查看全部
- 6、大山里面邮喜信——猜四字成语7、生的整两盘 熟的开两盘;不吃还两盘 吃剩还两盘——猜一水产品8、吹落
6、大山里面邮喜信——猜四字成语7、生的整两盘 熟的开两盘;不吃还两盘 吃剩还两盘——猜一水产品8、吹落
谁知道啊 可以给悬赏 帮帮我i 谢谢
 lljheb21年前1
lljheb21年前1 -
 老蔓 共回答了16个问题
老蔓 共回答了16个问题 |采纳率93.8%6喜上眉梢(喜出望外)
7 田螺1年前查看全部
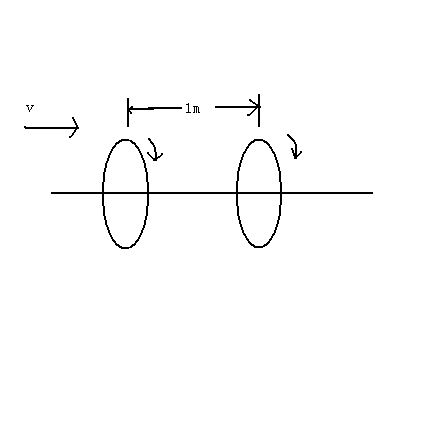
- 如图所示为测定子弹速度的装置,两个纸板圆盘分别装在一个匀速转动的轴上,两盘平行,若它们以3600rad/min的速度旋转
如图所示为测定子弹速度的装置,两个纸板圆盘分别装在一个匀速转动的轴上,两盘平行,若它们以3600rad/min的速度旋转,子弹从垂直于盘面的水平方向射来,先打穿第一个圆盘,再打穿第二个圆盘,测得两盘相距1m,两盘上子弹穿孔的半径夹角为30°,则子弹的速度最大值是多少?
解题的思路我知道,只不过答案解析里面用了这样一步:pi/6=60t,这里的pi竟然是用3.14来求,但是这里的pi不应该是角度的么,怎么能用3.14来求?(pi指圆周率)
 sdatgqert1年前3
sdatgqert1年前3 -
 沙尘暴121 共回答了20个问题
沙尘暴121 共回答了20个问题 |采纳率90%你看一下题目中给出的已知量3600rad/min的单位,它是弧度每分,所以角度的单位用弧度,所以pi用3.14.1年前查看全部
- 【简单】小学数学题 答对加粉丝有一个固定圆盘,一个活动圆盘,他们的半径相等,活动绕固定边缘做无滑动运动(两盘边缘密切相接
【简单】小学数学题 答对加粉丝
有一个固定圆盘,一个活动圆盘,他们的半径相等,活动绕固定边缘做无滑动运动(两盘边缘密切相接)活动绕固定一圈后,它本身转几圈?
要有过程……谢谢 Xiao毛儿5031年前6
Xiao毛儿5031年前6 -
 liping011900 共回答了21个问题
liping011900 共回答了21个问题 |采纳率90.5%肯定是两圈!1年前查看全部
- 甲、乙两盘水里都有冰块,甲盘里的冰块多些,乙盘里的冰块少些,甲盘放在阳光下,乙盘放在背阴处,两盘里的
甲、乙两盘水里都有冰块,甲盘里的冰块多些,乙盘里的冰块少些,甲盘放在阳光下,乙盘放在背阴处,两盘里的
A.甲盘中水的温度比乙盘的高 B.乙盘水的温度可能比乙盘的高 C.两盘水的温度相同 D.不能判定,必须用温度计测量后才能知道.请每一个选项详细说明 pp0o6181年前4
pp0o6181年前4 -
 qqalyf 共回答了16个问题
qqalyf 共回答了16个问题 |采纳率87.5%C,因为是冰水混合物,温度相同都是零度1年前查看全部
- 在托盘天平两盘上,放上A、B两个烧杯,烧杯内均盛有质量不同但都含有硫酸9.8克的稀硫酸,已知A烧杯比B烧杯重,现在A、B
在托盘天平两盘上,放上A、B两个烧杯,烧杯内均盛有质量不同但都含有硫酸9.8克的稀硫酸,已知A烧杯比B烧杯重,现在A、B两烧杯中分别投入等质量的铁和锌反应结束后,天平保持平衡,则反应前A、B烧杯最大质量差为______或______.
 dcgdogb1年前0
dcgdogb1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 确定断层两盘相对运动的主要标志是什么?
 wangypl1年前1
wangypl1年前1 -
 夜泊秋江 共回答了19个问题
夜泊秋江 共回答了19个问题 |采纳率94.7%确定断层的运动主要根据根据两盘中地层的新老关系、牵引构造、擦痕和阶步、羽状节理、断层两侧的小褶皱及断层角砾岩 .
1、 两盘中地层的新老关系:主要根据走向断层效应判别,注意区分断层引起的地层重复与褶皱引起的地层重复,注意断层引起地层缺失与不整合引起地层缺失.
2、牵引构造:牵引褶皱弧形突出的方向代表本盘运动方向.
3、擦痕和阶步
4、 羽状节理
5、断层两侧的小褶皱
6、断层角砾岩1年前查看全部
- 有一个化学题目,求教!在托盘天平的两盘上各放一个盛有足量的稀盐酸的烧杯,调节天平至平衡.在左盘烧杯中加Al和MgCO3的
有一个化学题目,求教!
在托盘天平的两盘上各放一个盛有足量的稀盐酸的烧杯,调节天平至平衡.在左盘烧杯中加Al和MgCO3的混合物,右盘烧杯中加入Mg和MgO的混合物,且MgCO3与MgO的质量比为21:10,充分反应后,若天平最终仍保持平衡,则加入的Al与Mg两种物质的质量比为_______. 尘于1年前2
尘于1年前2 -
 cecily118 共回答了17个问题
cecily118 共回答了17个问题 |采纳率88.2%由题意知盐酸足量,左、右两烧杯中所加物质全部消耗掉.左烧杯中AI、MgCO3与盐酸反应分别放出H2、CO2,右烧杯中Mg、MgO与盐酸反应只有Mg与盐酸反应放出H2.两烧杯中的物质反应后,虽然质量都减轻,但天平最终仍保持平衡,说明左、右烧杯中物质增重的质量相等.即:△m(MgCO3-CO2)+△m
(AI-H2)=△m(MgO)+△m(Mg-H2).设加入的AI的质量为a,Mg的质量为b,有:
MgCO3~CO2 △m
84 44 40
21 10
2AI~3H2↑ △m
54 6 48
a 48a/54
Mg~H2↑ △m
24 2 22
b 22b/24
10+48a/54=10+22b/24,解得a/b=33/32,故AI与Mg质量比为33:32.
小结:
对于此类题,先假设出加入物质的质量,然后用“差量法”计算出左、右两边溶液增加的质量,最后据溶液增加的质量相等来求解.1年前查看全部
- 一道关于二力平衡的实验`木块放在光滑的水平桌面上,首先,向挂在木块两端的小盘中加砝码,当两盘砝码质量相等时,木块保持静止
一道关于二力平衡的实验`
木块放在光滑的水平桌面上,首先,向挂在木块两端的小盘中加砝码,当两盘砝码质量相等时,木块保持静止,现在先把木筷扭转一个角度,过一会儿,松开手,发现木块自动恢复到原来的位置,这是因为____________ yaya_娅娅1年前1
yaya_娅娅1年前1 -
 applexiapingappl 共回答了12个问题
applexiapingappl 共回答了12个问题 |采纳率91.7%二力平衡1年前查看全部
- 1,有两盘苹果,如果从第一盘中拿2个放到第二盘中,那么两盘的苹果数相同;如果从第二盘中拿2个放到第一盘里,那么第一盘的苹
1,有两盘苹果,如果从第一盘中拿2个放到第二盘中,那么两盘的苹果数相同;如果从第二盘中拿2个放到第一盘里,那么第一盘的苹果数是第二盘的2倍.第一盘有苹果多少个?(请详细列式计算,能不设X吗?)
 sjr184841年前4
sjr184841年前4 -
 高个男孩 共回答了19个问题
高个男孩 共回答了19个问题 |采纳率100%第一盘-2=第二盘+2,所以第一盘=第二盘+4
第二盘如果不拿2个给第一盘,那么第一盘需要多加2+2*2才是第二盘的2倍,因此:
第二盘=2+2*2+4=10个
第一盘=10+4=14个1年前查看全部
- 在天平左右两盘分别放上体积相等的铜球和铁球,天平刚好平衡,则
在天平左右两盘分别放上体积相等的铜球和铁球,天平刚好平衡,则
( )球一定是空心的 wsxzzw1年前1
wsxzzw1年前1 -
 hlysky 共回答了14个问题
hlysky 共回答了14个问题 |采纳率85.7%一样重1年前查看全部
- 在调节好的天平两盘内分别放有3个相同的铁球和6个相同的铝球,天平刚好平衡,则铁球和铝球的体积之比是多少?质量之比是多少?
在调节好的天平两盘内分别放有3个相同的铁球和6个相同的铝球,天平刚好平衡,则铁球和铝球的体积之比是多少?质量之比是多少?
已知铝的密度和铁的密度 掌声1年前1
掌声1年前1 -
 Actel 共回答了22个问题
Actel 共回答了22个问题 |采纳率95.5%楼主确定题目?
体积比1:2
质量比1:11年前查看全部
- 小明数豆子,一盘145颗,一盘89颗,每次从多的一盘取出4颗到少的一盘,要使两盘豆子一样多,需拿几次?
 tboychen1年前1
tboychen1年前1 -
 chycloud 共回答了19个问题
chycloud 共回答了19个问题 |采纳率100%两盘豆子相差145-89=56颗,要使两盘豆子一样多,就要将多的一盘中取56÷2=28颗到少的一盘,每次取出4颗,需拿28÷4=7次.1年前查看全部
- 在天平左右两盘各放一杯盛有相同且足量的盐酸溶液,此时天平,在左右两盘的烧杯里各放入质量相等的Zn和大理石,反应停止后,此
在天平左右两盘各放一杯盛有相同且足量的盐酸溶液,此时天平,在左右两盘的烧杯里各放入质量相等的Zn和大理石,反应停止后,此时天平
A左盘比右盘高
B右盘比左盘高
C平衡
D无法确定 蓉儿19811年前3
蓉儿19811年前3 -
 zhonghe200 共回答了18个问题
zhonghe200 共回答了18个问题 |采纳率88.9%可以通过计算说明
1.列出方程式,比较
锌的相对原子质量是65 碳酸钙是100
氢气是2 二氧化碳是44
如果质量相同那么假设都有100g则碳酸钙产二氧化碳44(也就是跑了44质量减少了)再把100的锌代进去列化学方程式计算算出100锌产多少氢气,假设是a
如果a大于44则左盘轻 小于则右盘轻
具体计算过程你就自己算把.方法先教给你
只要自己做出来的东西才真正属于自己
祝你学业进步1年前查看全部
- 没有腐蚀性的化学药品可在天平两盘各放同样的______,然后称量.(需告诉参考答案,不凭空捏造,
 峰峰的海1年前1
峰峰的海1年前1 -
 s317832432 共回答了20个问题
s317832432 共回答了20个问题 |采纳率90%质量大小的纸片1年前查看全部
- 天平A,B两盘分别盛有51g和45g的盐,问应该从A盘拿出多少盐放到B盘内,才能使B盘所澄的盐的质量是A盘的2倍
天平A,B两盘分别盛有51g和45g的盐,问应该从A盘拿出多少盐放到B盘内,才能使B盘所澄的盐的质量是A盘的2倍
列方程, imgift1231年前1
imgift1231年前1 -
 AIallensu 共回答了8个问题
AIallensu 共回答了8个问题 |采纳率100%191年前查看全部
- 如图所示,A,B两个圆盘,半径相等.转动轴处在同一条直线上,两盘相距20cm,都顺时针匀速旋转,转速分别为n1=100r
如图所示,A,B两个圆盘,半径相等.转动轴处在同一条直线上,两盘相距20cm,都顺时针匀速旋转,转速分别为n1=100r/s,n2=200r/s.两个圆盘上都有一条沿半径的裂缝,某时刻两条夹缝恰好在竖直线上对齐,在轴线的正上方有一束粒子流.由A向B沿着平行于轴线的方向以恒定速率做匀速直线运动(不考虑空气阻力),则能够先后通过两条裂缝的粒子的速率是( ).A.10m/s B.20m/s C.30m/s D.40m/s
当粒子流通过A时,经过t到达B,v=20cm/t=0.02/t,而在此期间,B盘转动整数圈,所以t=n×TB,由于TB=0.005s,所以可求出V=40/n(n=1,2,3...)所以可以选A,B,D
提问:为什么可以设t=n×TB? 7hqjrah1年前1
7hqjrah1年前1 -
 hai-sen 共回答了14个问题
hai-sen 共回答了14个问题 |采纳率100%在粒子从裂缝A运动到B的过程中,圆盘B 可能转过了n周,所以时间t=nTB1年前查看全部
- 天平两盘内各放入一只质量相等的小烧杯,
天平两盘内各放入一只质量相等的小烧杯,
天平两盘内各放入一只质量相等的小烧杯,杯内各盛有足量的溶质质量分数相等的盐酸,若向左边加入2.8g铁屑,则想要是天平仍保持平衡,应向右盘加碳酸钙的质量是( ) iamsoil1年前1
iamsoil1年前1 -
 myknos 共回答了9个问题
myknos 共回答了9个问题 |采纳率100%设:加入2.8g铁反应后增加的质量为X
Fe+2HCl=FeCl2+H2↑ 增加
56 2 65-2=54
2.8g X
56:54=2.8g:X
X=2.7g
右盘质量增加2.7g需要加入碳酸钙的质量为Y
CaCO3+2HCl=CaCl2+H2O+CO2 ↑ 增加
100 44 100-44=56
Y 2.7g
100:56= Y:2.7g
Y=4.82g
应向右盘加碳酸钙的质量是4.82g.1年前查看全部
- 天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量且质量分数相等的盐酸,向左边烧杯中加入2.8g铁屑,则若要使天平仍保持
天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量且质量分数相等的盐酸,向左边烧杯中加入2.8g铁屑,则若要使天平仍保持平衡,向右边烧杯中加入碳酸钙的质量为()
A 5.63g B7.8g C 2.8g D 4.82g shannlei1年前1
shannlei1年前1 -
 ysy_s 共回答了23个问题
ysy_s 共回答了23个问题 |采纳率73.9%质量守恒 2Fe+2Hcl=Fecl2+H2
2*56 56+71 1*2
2.8g y x 得x=0.05g 是氢气 y=3.175g
因为盐酸是足量的二价的铁离子会被盐酸继续氧化成铁离子:
2Fecl2+2Hcl=2Fecl3+H2
2*127 2
3.175g z 得z=0.025g 所以产生氢气的质量一共是0.075g,左边小烧杯中实际增加了2.725g的重量
右边加碳酸钙的质量减去生成二氧化碳的质量也应该等于2.725g所以
CaCO3+2Hcl=Cacl2+H2O+CO2
100 44
a a-2.725 a约等于4.86g
我觉得步骤没错呀 可能还有人会吧 只能帮你到这了 大家共同学习 楼主在研究研究吧 选项D是最接近的 最好问问老师吧 嘿嘿~1年前查看全部
- 天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量的溶质质量分数相同的盐酸,若向左边加入2.8g铁屑
天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量的溶质质量分数相同的盐酸,若向左边加入2.8g铁屑
则要使天平保持平衡,应向右盘加碳酸钙的质量是( )
A 7.8g
B 5.63g
C 4.82g
D 2.8g
别复制别人的过程我看过了看不懂 hellium1年前1
hellium1年前1 -
 晓晓0510 共回答了20个问题
晓晓0510 共回答了20个问题 |采纳率90%铁与盐酸反应:
Fe+2HCl=FeCl2+H2(气体符号)
56 2
2.8 X
据:56/2.8=2/x
解出:X=0.1g
即,加入2.8g铁,生成0.1g氢气,氢气跑掉后,总质量增加:
2.8-0.1=2.7g
另一侧的反应方程如下,设CaCO3的质量是X,则:
CaCO3+2HCl=CaCl2+H2O+CO2(气体符号)
100 44
X Y
即:100/x=44/y,且有Y=11x/25
据题意知:X-y=2.7
即:X-11X/25=2.7
化简:14X/25=2.7
解得:X≈4.82g1年前查看全部
- 天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量的溶质质量分数相同的盐酸,若向左边加入2.8g铁屑,
天平两盘内各放一只质量相等的小烧杯,杯内各盛有足量的溶质质量分数相同的盐酸,若向左边加入2.8g铁屑,
则要使天平保持平衡,应向右盘加碳酸钙的质量是( )
A 7.8g
B 5.63g
C 4.82g
D 2.8g hbczljx1年前1
hbczljx1年前1 -
 scsnyb 共回答了24个问题
scsnyb 共回答了24个问题 |采纳率91.7%C 4.82g
向左边加入2.8克的铁屑要产生0.1g氢气,溶液质量增加2.8g-0.1g=2.7g
要使天平平衡,右边也要增加2.7g
CaCO3+2HCl=CaCl2+H2O+CO2 溶液质量增加
100 44 100-44=56
x 2.7g
100/x=56/2.7g
x=4.82g1年前查看全部
- 天平左、右两盘分别放A、B两个体积相同的实心球,在右盘加一个砝码,天平才能平衡,由此可以判知A球的密度
天平左、右两盘分别放A、B两个体积相同的实心球,在右盘加一个砝码,天平才能平衡,由此可以判知A球的密度
比B球的密度_____(选填“大”或“小”.)
分析过程(带公式)(详写): 我晕我醉我糊涂1年前1
我晕我醉我糊涂1年前1 -
 皓月冷风 共回答了15个问题
皓月冷风 共回答了15个问题 |采纳率100%大 右盘为B,右盘加一个砝码,天平才能平衡,说明B轻 ,体积一样,所以A球的密度 大于B1年前查看全部
- 在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入50g溶质质量分数为14.6%的稀盐酸,将天平调节至平衡;
在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入50g溶质质量分数为14.6%的稀盐酸,将天平调节至平衡;然后向左盘烧杯中投入一定质量的碳酸钠固体,向右盘烧杯中投入一定质量的镁,均恰好完全反应,天平指针发生偏转.则下列各项操作中,能使天平重新达到平衡的是( )
A. 将游码向右移动4.2g
B. 向右盘烧杯中再加入4g稀盐酸
C. 在右盘上放4.8g镁
D. 在左盘上放7.2g碳酸钠固体 登徒子oO1年前1
登徒子oO1年前1 -
 ken_lyg 共回答了22个问题
ken_lyg 共回答了22个问题 |采纳率100%解题思路:根据化学方程式计算可知,投入一定质量的碳酸钠固体的左盘恰好完全反应后增重6.2g,而投入一定质量的镁的右盘恰好完全反应后增重2.2g 所以重新平衡需要使右盘增加4g质量,而烧杯内能反应的物质已完全反应,因此所加入的物质不会再发生反应,所加入的量即增加的质量.根据碳酸钠与盐酸反应的化学方程式,可得知:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
10.6g 50g×14.6%=7.3g 4.4g
所以投入碳酸钠的左盘实际增重=10.6g-4.4g=6.2g
根据金属镁与盐酸反应的化学方程式,可得知:
2HCl+Mg═MgCl2+H2↑
73 24 2
7.3g 2.4g 0.2g
所以投入金属镁的右盘实际增重=2.4g-0.2g=2.2g
则均恰好完全反应后,天平左盘增加质量比右盘增加质量多出6.2g-2.2g=4g
所以,要使天平仍然保持平衡,需要使天平右侧质量增加4g;由于烧杯内可以发生反应的物质已完全反应,因此所加入的物质不再发生反应,加入的质量即增加的质量;
故选B.点评:
本题考点: 根据化学反应方程式的计算;称量器-托盘天平;酸的化学性质.
考点点评: 由于反应放出气体,所加固体的质量并非烧杯内物质总质量实际增加的质量,实际增加质量为加入固体质量与放出气体质量的差.1年前查看全部
- 如何根据地质图判断断层两盘的相对运动方向
如何根据地质图判断断层两盘的相对运动方向
如图:

 大碑said1年前5
大碑said1年前5 -
 xzknet 共回答了19个问题
xzknet 共回答了19个问题 |采纳率89.5%地壳岩层因受力达到一定强度而发生破裂,并沿破裂面有明显相对移动的构造称断层.
断层两盘相对移动开的距离叫断距.分为总断距、走向断距、倾向断距、水平断距和铅直断距等.
(1)在垂直于被错断岩层走向的剖面上可测得的断距有:
地层断距 断层两盘上对应层之间的垂直距离;
铅直地层断距 断层两盘上对应层之间的铅直距离;
水平地层断距 断层两盘上对应层之间的水平距离;
以上三终端据构成直角三角形关系,如已知岩层倾角和上述三种断距中任一种断距,即可求出其他两种断距.
(2)在垂直于断层走向的剖面上,也可测得与垂直于岩层走向剖面上相当的各种断距,当岩层走向与断层走向不一致时,除铅直地层断距在两个剖面上相等外,在垂直于岩层走向的剖面上测得的地层断距和水平地层断距都小于垂直断层走向的剖面上测得的数值.
——断层概念
地质图上,你就要看断层性质,断层两边地层的接触关系,然后你根据地层两边谁升谁降,再联系正逆断层,结果就出来了.1年前查看全部
- 在调节好的天平两盘各方一铝块和铁块,天平恰能平衡,则铝块与铁块的质量之比m铝:m铁=————,体积之比V铝:V铁=———
在调节好的天平两盘各方一铝块和铁块,天平恰能平衡,则铝块与铁块的质量之比m铝:m铁=————,体积之比V铝:V铁=—————.(铝的密度=2.7g/立方厘米,铁的密度=7.97g/立方厘米)
 sixundaduiwangju1年前1
sixundaduiwangju1年前1 -
 dieluft 共回答了32个问题
dieluft 共回答了32个问题 |采纳率87.5%(1).铝块与铁块的质量比
因为天平恰能平衡,所以铝块质量等于
铁块质量,它们的质量比是:
m铝:m铁=1:1 .
(2).铝块与铁块的体积比
因为质量等于体积乘密度,所以有下式:
铝块体积v*铝的密度d=铁块体积v*铁的密度d
即:v铝*d铝=v铁*d铁
v铝*2.7g/cm³=v铁*7.97g/cm³
v铝/v铁=7.97/2.7=2.95
所以:v铝:v铁=2.95:1.00 .1年前查看全部
- 如果所有饭桌上各一盘鱼.会剩下一盘鱼,每个饭桌上各两盘鱼,会有一个饭桌没有鱼,该厨师共准备了几盘鱼
如果所有饭桌上各一盘鱼.会剩下一盘鱼,每个饭桌上各两盘鱼,会有一个饭桌没有鱼,该厨师共准备了几盘鱼
设未知数,列出方程 asongsong1年前5
asongsong1年前5 -
 zhuqingyi0123 共回答了13个问题
zhuqingyi0123 共回答了13个问题 |采纳率92.3%x,等式两边都是桌子数目 x-1=1+x/2 x=41年前查看全部
- 趣味题(小学6年级)今有客不知其数,两人共盘少两盘,三人共盘多三盘,问客人和盘共几何?
 王环境1年前1
王环境1年前1 -
 philipskel 共回答了19个问题
philipskel 共回答了19个问题 |采纳率89.5%客人:30人, 盘:13
做法如下:
设x人,y盘 .
列出方程组:
x/2=y+2
x/3=y-3
解出:x=30 y=13
如果还有疑问,请追问~
望采纳1年前查看全部
- {高二数学}三局两胜的概率题,如果连赢两盘还用考虑第三盘是否赢吗
{高二数学}三局两胜的概率题,如果连赢两盘还用考虑第三盘是否赢吗
如题
原题:
甲乙两个选手比赛假设甲胜概率0.乙胜0.那么采用三局两胜还是五局三胜对甲更有利
若甲连赢了两局,第三局还用考虑他是否输赢的概率吗 罪恶的种子1年前4
罪恶的种子1年前4 -
 yuangaojie 共回答了28个问题
yuangaojie 共回答了28个问题 |采纳率92.9%当然不用
这类问题先分类,后分步.
三局两胜,乙胜前两局,或前2局一胜一负且第3局胜
那么乙胜概率:P=0.4^2+C(1,2)0.4*0.6*0.4=0.352
五局三胜,乙胜前3局,或前3局2胜1负且第4局胜,或前4局2胜2负且第5局胜
那么乙胜的概率:P=0.31744
所以三局两胜对乙有利,五局三胜对甲有利
甲的你类似推下1年前查看全部
- 怎么选,为什么一天平的两盘总各放一只烧杯,杯子中盛有适量的水,使天平保持平衡.如果将质量相等的实心铅块和铝块各用一根轻而
怎么选,为什么
一天平的两盘总各放一只烧杯,杯子中盛有适量的水,使天平保持平衡.如果将质量相等的实心铅块和铝块各用一根轻而细的线拴住,然后分别使它们全部浸入水中,水不溢出.下列情况中天平的平衡被破坏的是
A.使它们都沉入杯底
B.把细线挂在天平的钩上,使铅块和铝块都不触底
C.两手分别捏住两根线上,两物块都不触底
D.铝块沉底,把栓铅块的线挂在天平的挂钩上 socong1年前1
socong1年前1 -
 julia_zhu 共回答了20个问题
julia_zhu 共回答了20个问题 |采纳率100%B
B:作为一个整体考虑就可以,在天平左右两边考虑,A:G水+G铜=G水+G铅
C:G水+G铜=G水+G铅
D:G水+G铜=G水+G铅
但是B不同,对于每一个球,G=F手(此项不等)+F浮(此项不等),由于铅铜密度不同,所以在质量相同时,体积不同,浮力不同,球对水的作用力大小等于浮力大小,由于浮力不等,所以天平左右受力不平衡选B.
☆请及时点击【采纳为满意回答】按钮☆1年前查看全部
- 1、在天平左、右两盘中各放一个等质量的烧杯,烧杯中分别加入等质量的足量10%的稀盐酸,天平平衡.向左盘烧杯中加入5.8g
1、在天平左、右两盘中各放一个等质量的烧杯,烧杯中分别加入等质量的足量10%的稀盐酸,天平平衡.向左盘烧杯中加入5.8g的镁和铜的混合物,右盘加入5.6g铁,天平再次平衡,则原镁和铜的混合物中铜的质量为?
2、在天平左、右两盘中各放一个等质量的烧杯,烧杯中分别加入等质量的足量10%的稀盐酸,天平平衡.向左盘烧杯中加入16g的Fe和Cu的混合物,右盘烧杯中加入15.8gCaO,天平平衡,那么两边所加入的盐酸的质量至少为? mm里乱飞的猪猪1年前4
mm里乱飞的猪猪1年前4 -
 帅克88 共回答了22个问题
帅克88 共回答了22个问题 |采纳率63.6%1.第一题中天平再次平衡,则说明两盘中加入金属后增重相同,设镁的质量为x铜的质量为y
左盘:Mg+2HCL==MgCl2+H2 增重
24 2 22
x 22x/24
右盘:Fe+2HCl==FeCl2+H2 增重
56 2 54
5.6 5.4
两盘中增重相同:5.4==22x/24 +y x+y==5.8 解得y==1
所以:铜的质量为 1 克
2.右盘的增重为15.8克,设铁的质量为x,加入盐酸的质量为y
左盘:Fe+2HCl==FeCl2+H2 增重
56 73 2 54
x y *10% 54x/56
则左盘的增重为54x/56+(16—x)
两盘增重相同:54x/56+(16—x)===15.8 解得x==5.6
铁的质量为5.6克,所消耗的盐酸为y*10% ==73x/56==73*5.6/56
解得:y==73
所以至少要加入盐酸73克1年前查看全部
- 初三化学将盛有相同质量相同质量分数稀盐酸的两只烧杯 放在托盘天平左右两盘上向两烧杯中加入质量相等的
初三化学将盛有相同质量相同质量分数稀盐酸的两只烧杯 放在托盘天平左右两盘上向两烧杯中加入质量相等的
镁 和铝 反应停止后根据天平平衡状态判断
1 若天平仍保持平衡 则反应中一定无剩余的是______,一定有剩余的是_____,可能有剩余的是____
2若天平失去平衡 则加入_______(Mg或Al)的一边托盘下沉 蓝梦潇雪1年前1
蓝梦潇雪1年前1 -
 清幽的风 共回答了20个问题
清幽的风 共回答了20个问题 |采纳率95%天平平衡说明生成氢气一样多,应该是盐酸不够,一定有剩余的是铝,可能有剩余的是镁
天平失去平衡,说明,两种金属完全反应,应该是加镁的一边下沉.产生氢气是2/24<3/271年前查看全部
- (2002•普陀区二模)一组学生向放置在天平左右两盘已调节平衡的烧杯中各加入质量相等、溶质质量分数相同的稀硫酸,再向两烧
(2002•普陀区二模)一组学生向放置在天平左右两盘已调节平衡的烧杯中各加入质量相等、溶质质量分数相同的稀硫酸,再向两烧杯中分别加入质量相等的镁和铝(左杯放镁、右杯放铝),待反应完全后,几位学生观察到了不同的现象,你认为可能的是( )
A.左边的托盘往下沉
B.右边的托盘往下沉
C.右盘的溶液浓度大
D.左盘、右盘保持平衡 青未了1年前1
青未了1年前1 -
 nickye1998 共回答了16个问题
nickye1998 共回答了16个问题 |采纳率100%解题思路:此题一定分为两种情况,①酸足量②酸不足量,当酸足量时镁与铝生成的氢气不一样多则铝生成的氢气多,放铝盘质量较小,当酸不足量时两盘生成的氢气质量相等,天平仍然平衡.①假设两盘中的酸都足量,铝与镁生成的氢气质量不等,天平不平衡,铝生成的氢气较多,此盘轻镁盘下沉,即左边的托盘往下沉.
②酸不足量时,酸完全反应生成的氢气量相等,天平仍然平衡.
C不是现象无法看出.
故选AD点评:
本题考点: 金属的化学性质;称量器-托盘天平;反应现象和本质的联系;根据化学反应方程式的计算.
考点点评: 此题是一道天平问题考查题,解题的关键是对酸的量的分析,分不同情况进行探讨,是一道难度较大的讨论题.1年前查看全部
- 在天平两盘的烧杯中,各放入质量相同的稀盐酸,调节天平至平衡,分别向两边烧杯中各加入5g镁和5g铁,镁和铁全部反应而消失后
在天平两盘的烧杯中,各放入质量相同的稀盐酸,调节天平至平衡,分别向两边烧杯中各加入5g镁和5g铁,镁和铁全部反应而消失后,天平的指针( )
A. 偏向加铁的一边
B. 偏向加镁的一边
C. 先偏向加镁的一边,后偏向加铁的一边
D. 最终仍停留在原来的位置 现代楼1年前7
现代楼1年前7 -
 心态真好 共回答了13个问题
心态真好 共回答了13个问题 |采纳率76.9%解题思路:据已有的知识进行分析,金属与酸反应天平要平衡,则加入的金属与产生的氢气的差值相等,天平若不平衡,则会指向质量增加多的一端.1.镁与酸反应物质增加的量为x
Mg+2HCl═MgCl2+H2↑△m
24 2 22
5g x
[24/22]=[5g/x]
x=4.58g
设5g铁与酸反应物质增加的量为y
Fe+2HCl═FeCl2+H2↑△m
56 2 54
5g y
[56/54]=[5g/y]
y=4.82g
所以加铁的一边质量增加多,指针偏向加铁的一边,观察选项,故A对.
2.根据金属活动性顺序镁>铁,金属镁与盐酸反应放出氢气速率大于金属铁,而等质量金属镁完全反应放出氢气质量大于金属铁. 一直向铁偏转.
答案:A.点评:
本题考点: 金属的化学性质.
考点点评: 本题考查了金属与酸反应天平平衡的问题,完成此题,可以依据金属与酸反应的化学方程式求得质量增加量,然后判断天平指针的指向1年前查看全部
- 桌上摆了两盘奶糖,共50块,如果从甲盘子里面拿走5块放到乙盘子里,那么两个盘子的奶糖一样多,原来两个盘子里各有多少奶糖.
 我S如如1年前1
我S如如1年前1 -
 liu476167868 共回答了21个问题
liu476167868 共回答了21个问题 |采纳率100%现在两盘一样多,就是现在各25
甲少了5个,说明拿走之前是30
乙多了5个,说明得到之前是201年前查看全部
- 在天平左右两盘中各放一张白纸后,即可将NAOH固体放在白纸上称量
在天平左右两盘中各放一张白纸后,即可将NAOH固体放在白纸上称量
这样做哪里错了? 春天没有发芽1年前3
春天没有发芽1年前3 -
 琵琶芒果 共回答了17个问题
琵琶芒果 共回答了17个问题 |采纳率88.2%NaOH易潮解,不能直接放在纸上称量,应在玻璃器皿中称量1年前查看全部
- 在天平两盘的烧杯中,各放入质量相同的稀盐酸,调节天平至平衡,分别向两边烧杯中各加入5g镁和5g铁,镁和铁全部反应而消失后
在天平两盘的烧杯中,各放入质量相同的稀盐酸,调节天平至平衡,分别向两边烧杯中各加入5g镁和5g铁,镁和铁全部反应而消失后,天平的指针( )
A. 偏向加铁的一边
B. 偏向加镁的一边
C. 先偏向加镁的一边,后偏向加铁的一边
D. 最终仍停留在原来的位置 做人别太李旭丹1年前0
做人别太李旭丹1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 在托盘天平的两盘上各放一个烧杯,分别盛有等质量足量的稀盐酸,调节天平平衡.向左边烧杯中加入n g镁粉,向右边烧杯中加入n
在托盘天平的两盘上各放一个烧杯,分别盛有等质量足量的稀盐酸,调节天平平衡.向左边烧杯中加入n g镁粉,向右边烧杯中加入n g铝和氧化铝的混合物,充分反应后,若天平仍然平衡,则混合物中铝元素和氧元素的质量比为______.
 clt04151年前2
clt04151年前2 -
 毛毛1021 共回答了16个问题
毛毛1021 共回答了16个问题 |采纳率93.8%解题思路:因天平仍然平衡,说明反应后生成的氢气一样多,据此可以计算出混合物中铝的质量和氧化铝的质量,进而计算出氧化铝中铝元素和氧元素的质量,最后得出本题答案.设混合物中铝的质量为x.由Mg+2HCl=MgCl2+H2↑和2Al+6HCl=2AlCl3+3H2↑根据氢气质量相等,可得3Mg→2Al72 54ngx7254=ngx,x=3n4g氧化铝的质量为ng-3n4g=n4g氧化铝中铝元素的质量为n4g...
点评:
本题考点: 根据化学反应方程式的计算;化合物中某元素的质量计算;有关化学式的计算和推断.
考点点评: 本题主要考查有关化学方程式的计算和化学式的计算,难度较大.1年前查看全部
- 在调好的天平的两个盘中各放一个盛有相同质量的同种洁厕灵的烧杯,在左右两盘的烧杯中放相同质量的纯碱粉末和铁粉,10分钟后观
在调好的天平的两个盘中各放一个盛有相同质量的同种洁厕灵的烧杯,在左右两盘的烧杯中放相同质量的纯碱粉末和铁粉,10分钟后观察现象,
 cnlhb20001年前1
cnlhb20001年前1 -
 ip002 共回答了22个问题
ip002 共回答了22个问题 |采纳率95.5%左边变重了,纯碱有吸水性1年前查看全部
- 有3个盘子 第一个盘4个梨 第二个盘3个梨 第三个个盘5个梨 如果一次只能端两盘,那么一次最多能端几个梨
 冬冬冬冬冬冬1年前1
冬冬冬冬冬冬1年前1 -
 syxb1120 共回答了10个问题
syxb1120 共回答了10个问题 |采纳率90%3+4=7
3+5=8
4+5=9
一次最多能端9个梨1年前查看全部
- 在托盘天平两盘上各放一个烧杯,两烧杯盛有等质量的等质量分数的足量盐酸,天平保持平衡.此时向左盘烧杯中加入10gMgO,若
在托盘天平两盘上各放一个烧杯,两烧杯盛有等质量的等质量分数的足量盐酸,天平保持平衡.此时向左盘烧杯中加入10gMgO,若要使天平再次平衡,应向天平右边的烧杯中加入( )
A. 10gCu
B. 10.9g镁条
C. 10gNa2CO3
D. 12g铝片 信鸟你的邪勒1年前1
信鸟你的邪勒1年前1 -
 maizecai 共回答了30个问题
maizecai 共回答了30个问题 |采纳率83.3%解题思路:10g氧化镁与酸反应时没有气体放出,所以左盘中增加的质量是10g,要使天平再次平衡则要求右端烧杯加入的物质与气体的质量差也应是10g(即右盘增重也应为10g),利用这一原则进行判断即可.A、铜不能与盐酸反应,所以会使右盘增重10g,天平能平衡.
B、设生成气体的质量为x.
Mg+2HCl═MgCl2+H2↑
24 2
10.9g x
[24/2=
10.9g
x]
x≈0.91g 10g-0.91g<10g
故右盘增重小于10g,天平不会平衡;
C、10gNa2CO3与盐酸反应会生成二氧化碳,所以增重一定小于10g,故天平不会平衡;
D、设生成气体的质量为y.
2Al+6HCl═2AlCl3+3H2↑
54 6
12g y
[54/6=
12g
y]
y≈1.33g
12g-1.33g>10g
故右盘增重大于10g,天平不会平衡;
故选A点评:
本题考点: 酸的化学性质.
考点点评: 此题是一道天平问题考查题,解题的关键是找出天平两端质量的增加值相等这一关系,是利用化学方程式计算的综合训练题.1年前查看全部
- 今有客不知其数,两人公盘少两盘,三人共盘多三盘,问客人和盘各几和?
 xl1215321年前1
xl1215321年前1 -
 xiaotonychan 共回答了10个问题
xiaotonychan 共回答了10个问题 |采纳率90%设客x人
x/2-2=x/3+3
x=30 盘x/2-2=131年前查看全部
- 1.在托盘天平两盘各放置盛有50mL浓度为1mol/LH2SO4溶液的烧杯,调节平衡后,根据以下操作回答下列问题:
1.在托盘天平两盘各放置盛有50mL浓度为1mol/LH2SO4溶液的烧杯,调节平衡后,根据以下操作回答下列问题:
(1)若向左盘烧杯中加入0.1molNa,右盘烧杯中加入0.1molMg,充分反应后,天平是否仍处于平衡状态_________(填"是"或"否"),若不平衡,指针的指向是_________(填"左"或"右",若平衡,此空可不填);
(2)若向左盘烧杯中加入2.3gNa,右盘烧杯中加入2.3gMg,充分反应后,天平是否仍处于平衡状态_________(填"是"或"否"),若不平衡,指针的指向是_________(填"左"或"右",若平衡,此空可不填);
(3)若向左盘烧杯中加入m gMg,右盘烧杯中加入w gAl,充分反应后,天平仍处于平衡状态,则m和w的关系可能为_________或__________(用数学式子表示,答到两种情况即可)
请您说明理由和步骤,麻烦你,再见. 香烟_爱上火柴1年前2
香烟_爱上火柴1年前2 -
 巴勒 共回答了18个问题
巴勒 共回答了18个问题 |采纳率100%首先,一共有H+0.1mol
(1)加Na比Mg质量少,但是生成的氢气的量一样,因为Na适量Mg过量,所以,右边比左边重一些.
(2)平衡,因为这次也是氢全部被反应掉,并且加入的一样多.
(3)都过量的时候,m=w,都不过量,那么m-(2/24)m=w-(3/27)w[就是加入的减生成的氢气,剩下的相等]自己化简吧……1年前查看全部
- 在已平衡的托盘天平的左右两盘上各放一只盛有等质量同浓度的过量的盐酸,
在已平衡的托盘天平的左右两盘上各放一只盛有等质量同浓度的过量的盐酸,
向左盘中加入11.2g碳粉,则右盘应该加多少克CaCO3,才能使天平平衡 亚也1年前1
亚也1年前1 -
 Deepliu 共回答了22个问题
Deepliu 共回答了22个问题 |采纳率90.9%20g1年前查看全部
- 桌上有一个固定圆盘与一个活动圆盘,这两个圆盘的半径相等.将活动圆盘绕着固定圆盘的边缘作无滑动的滚动(滚动时始终保持两盘边
桌上有一个固定圆盘与一个活动圆盘,这两个圆盘的半径相等.将活动圆盘绕着固定圆盘的边缘作无滑动的滚动(滚动时始终保持两盘边缘密切相接).当活动圆盘绕着固定圆盘转动一周后,活动圆盘本身旋转了( )圈.
祈求真理! 小小花和尚1年前2
小小花和尚1年前2 -
 明月有情 共回答了18个问题
明月有情 共回答了18个问题 |采纳率94.4%2
可以在圆盘的某个位置做标记,例如一开始的接触点(活动盘在右侧),这个点在活动圆盘左端,当圆盘绕半周时,这个点又回到活动圆盘左端,再过半周,这个点又回到活动圆盘左端.1年前查看全部
- 如图,用定滑轮吊着轻质小盘,当左、右两盘中的钩码的重力分别为5n或3n时,物体保持静止.
如图,用定滑轮吊着轻质小盘,当左、右两盘中的钩码的重力分别为5n或3n时,物体保持静止.
如图,用定滑轮吊着轻质小盘,当左、右两盘中的钩码的重力分别为5n或3n时,物体保持静止.则物体受水平桌面的摩擦力为 n,方向 .若向左盘加2n的钩码,物体恰好向左匀速滑动,那么要使物体向右匀速滑动,需要向右盘加入 n的钩码. liuz19811年前2
liuz19811年前2 -
 影法师504 共回答了10个问题
影法师504 共回答了10个问题 |采纳率90%(1)2N,水平向右 (因为物体保持静止,受力平衡,水平向左的所有力的合力等于水平向右的所有力的合力,即5N=f+3N);
(2)8N (向左盘加2N的钩码后匀速运动,受力平衡,这时摩擦力变为滑动摩擦力,水平向右,同样根据受力平衡原理:2N+5N=3N+f滑,得 f滑=4N;若要使物体向右匀速运动,则滑动摩擦力方向变为水平向左,再次列出平衡方程:7N+4N=3N+G,解得G=8N)1年前查看全部
大家在问
- 1已知浓硫酸具有强氧化性,可与炭粉反应。
- 2He is writing to his friend.对friend提问?
- 3环保和节约能源有什么相同和不同之处?求详细的解答
- 4英语翻译请纠正或者换一种说法,
- 5西语单词问题perder el miedo 为什么用perdertomar la palabra是什么意思 为什么要用t
- 6同一段绳子的拉力一定相等吗一根长为L的易断的均匀细绳,两端固定在天花板上的A、B两点.若在细绳的C处悬一重物,已知AC&
- 7同义句:1:I like then very much.=I like them ____ ____.
- 8观察下列实验,回答问题。 1.该实验可以模拟的地理现象是 [ ] A.温
- 9已知二元一次方程y=kx+b(k·b为常数,且k≠0)当-2<x≤6,-4≤y<3,请写出这个二元一次方程.
- 10某人外出7天,日期数的和再加月份数是84.那么,他是几月几号回家的?
- 11在等腰三角形ABC中,若顶角A的余弦值为-3/5,则其底角B的正弦值
- 12下列常用词语中字音有错误的一组是 A.逾期作废yú鹬yù蚌相争bàng 殒yǔn身不恤xù B.运筹帷wéi幄wò责无旁
- 13求速解已知ABCDE是短周期得五个非金属元素,它们得原子预数依次增大,A元素原子形成得离子核外电子数为零,BCD在元素周
- 1432.5度等于50`24'X332.5_____.
- 15上下结构 左右结构 独体字结构 上中下结构 左中右结构 半包围结构的子哪些
