(2013•芜湖县)数学课上,王老师要求同学们用数学语言描述生活中的事.请你从数学的角度进行分析,在错误的地方画上横线.
 色不异空2022-10-04 11:39:541条回答
色不异空2022-10-04 11:39:541条回答张红说:“真倒霉,我生于1992年2月29日下午14时,一般每四年只过一次生日”.苏伟说:“比赛时常看见3:0这样的比分,所以说比的后项可以是0”.林巧说:“前天,我和四个同学轮换背两个脚扭伤的同学到200米远的医院就诊,平均每人背40米路程”.小玉说:“某种奖券的中奖率是10%,每买100张奖券,肯定中奖10张”.小花说:“上次爸爸想做一个直径为0.3米,长为3米的圆柱形通风管,我建议,如果不计接头耗材,至少要买一块面积为2.8平方米的长方形铁皮”.

已提交,审核后显示!提交回复
共1条回复
 roger2943 共回答了15个问题
roger2943 共回答了15个问题 |采纳率60%- 解题思路:(1)先分析张红说的话,1992年是闰年,因为一般4年一闰,每四年只过一次生日是正确的,但不能说是因为生于1992年2月29日下午14时,才每四年只过一次生日.错在“下午14时”,应删去“下午”;
(2)再看苏伟的说法,要知道比分和比是两个不同的概念,错误的原因在于苏伟没有正确区分这两个概念,不能说“比的后项可以是0”;
(3)再来看林巧的说法,“平均每人背40米路程”说法不妥,应删去“路程”二字;
(4)小玉的说法错在“肯定中奖10张”上,错误的原因在于没有很好理解百分数的意义;
(5)最后我们来分析小花的说法,此题应算出圆柱形通风管的侧面积,S侧=3.14×0.3×3=2.826(平方米)>2.8平方米.因此不正确.错误的地方有以下5处:
①下午14时;②比的后项可以是0;③40米的路程;④肯定中奖10张;⑤2.8平方米
张红说:“真倒霉,我生于1992年2月29日下午14时,一般每四年只过一次生日”.苏伟说:“比赛时常看见3:0这样的比分,所以说比的后项可以是0”.林巧说:“前天,我和四个同学轮换背两个脚扭伤的同学到200米远的医院就诊,平均每人背40米路程”.小玉说:“某种奖券的中奖率是10%,每买100张奖券,肯定中奖10张”.小花说:“上次爸爸想做一个直径为0.3米,长为3米的圆柱形通风管,我建议,如果不计接头耗材,至少要买一块面积为2.8平方米的长方形铁皮”.点评:
本题考点: 平年、闰年的判断方法;比的意义;圆柱的侧面积、表面积和体积;平均数的含义及求平均数的方法;概率的认识.
考点点评: 此题集中体现了数学在生活中的应用,体现了数学的严谨性.考查的知识点较多,同时也考查了学生阅读理解和解决实际问题的能力. - 1年前
相关推荐
- (2013•芜湖县模拟)关于微粒在指定溶液中能否大量共存的评价正确的是( ) 选项溶液微粒评价A8% H2O2水溶液F
(2013•芜湖县模拟)关于微粒在指定溶液中能否大量共存的评价正确的是( )
选项 溶液 微粒 评价 A 8% H2O2水溶液 Fe3+、Mg2+、SO42-、Na+ 可以大量共存 B 室温下pH=12的水溶液 NO3-、Na+、SO32-、K+ NO3-能将SO32-氧化而不能大量共存 C 1 mol/L的NH4Cl溶液 Ba2+、OH-、NH3•H2O、Na+ NH4Cl溶液显酸性,NH3•H2O不能在其中大量共存 D NaHSO4水溶液 I-、K+、CH3COO-、Br- CH3COO-能与NaHSO4溶液反应,不能在其中大量共存
A.A
B.B
C.C
D.D taotao17071年前1
taotao17071年前1 -
 liaashi 共回答了17个问题
liaashi 共回答了17个问题 |采纳率82.4%解题思路:A.铁离子能够促进双氧水的分解,在溶液中不能大量共存;
B.室温下pH=12的水溶液为碱性溶液,NO3-、Na+、SO32-、K+之间不反应,也不与氢氧根离子反应;
C.氢氧根离子与氯化铵溶液反应生成一水合氨;
D.硫酸氢钠在溶液中电离出氢离子,醋酸根离子与氢离子反应生成弱电解质醋酸A.Fe3+为双氧水分解的催化剂,促进了双氧水的分解,在溶液中不可以大量共存,该评价不合理,故A错误;
B.室温下pH=12的水溶液中存在大量氢氧根离子,NO3-、Na+、SO32-、K+离子之间不发生反应,且都不与氢氧根离子反应,在溶液中可以大量共存,该评价错误,故B错误;
C.OH-与NH4Cl发生反应生成一水合氨,在溶液中不能大量共存,评价错误,故C错误;
D.NaHSO4水溶液中存在大量氢离子,CH3COO-能与NaHSO4溶液反应,在溶液中不能大量共存,该评价合理,故D正确;
故选D点评:
本题考点: 离子共存问题.
考点点评: 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色;选项A为易错点,注意铁离子能够促进双氧水的分解.1年前查看全部
- (2013•芜湖县模拟)根据下列现象说明空气中含有哪些成分或用到了哪些成分:
(2013•芜湖县模拟)根据下列现象说明空气中含有哪些成分或用到了哪些成分:
(1)一杯饮料从冰箱中取出来,一会儿杯子的外壁凝结有小水滴,说明空气中含有______.
(2)空气是生产化肥的一种原料,说明了空气中含有______.
(3)澄清石灰水长期放置在空气中,表面出现了一层白色的膜,说明空气中含有______.
(4)夜晚街道两旁亮起了五彩缤纷的霓虹灯,霓虹灯中充了空气中______. 殇鱼1年前1
殇鱼1年前1 -
 susan_1202 共回答了14个问题
susan_1202 共回答了14个问题 |采纳率92.9%解题思路:根据空气的成分及其各种成分的性质方面进行分析、判断、解答.(1)爆米花放在空气中变软了,说明空气中含有水蒸气,故答案为:水蒸气.
(2)空气中的氮气是生产氮肥的一种原料,故答案为:氮气.
(3)澄清石灰水长期放置在空气中,表面出现一层白膜,是因为二氧化碳能使石灰水变浑浊,因此此现象说明空气中含有二氧化碳.故答案为:二氧化碳.
(4)稀有气体化学性质稳定,充入灯泡中能发出不同颜色的光.故答案为:稀有气体.点评:
本题考点: 空气的成分及各成分的体积分数.
考点点评: 本题难度不大,掌握空气中各种成分的性质是解答本题的关键.1年前查看全部
- (2013•芜湖县模拟)X、Y、Z、W是元素周期表前四周期中的常见元素.其相关信息如表:
(2013•芜湖县模拟)X、Y、Z、W是元素周期表前四周期中的常见元素.其相关信息如表:
(1)W位于元素周期表第______周期第______族;Z的基态原子核外有______个原子轨道填充了电子.元素 相关信息 X X的基态原子价电子排布式为:nsnnpn+1 Y Y原子的最外层电子数是次外层的三倍 Z Z存在质量数为27,中子数为14的核素 W W元素最高价氧化物对应的水化物是一种不溶于水的蓝色固体
(2)X的第一电离能比 Y 的______(填“大”或“小”); Y所在族各种元素的气态氢化物中沸点最低的是______(写化学式).
(3)X与Y形成原子个数比为1:2的两种化合物间存在化学平衡,请写出该反应的化学方程式及其平衡常数表达式2NO2⇌N2O4,K=C(N2O4) C2(NO2) 2NO2⇌N2O4,K=.C(N2O4) C2(NO2)
(4)X的原子与氢原子形成的一种分子中同时存在极性键、非极性键,写出该分子的电子式:______.氢元素、X、Y 的原子可共同形成多种分子,写出其中一种分子和Z的简单离子反应的离子方程式:______. pping061年前1
pping061年前1 -
 gdhrqgf 共回答了16个问题
gdhrqgf 共回答了16个问题 |采纳率87.5%解题思路:X、Y、Z、W是元素周期表前四周期中的常见元素,X的基态原子价电子排布式为:nsnnpn+1,s能级上最多排2个电子,且p能级上还有电子,所以n为2,则x的基态原子最外层电子排布式为:2s22p3,所以X基态原子核外有7个电子,则X是N元素;
Y的基态原子Y原子的最外层电子数是次外层的三倍,所以y基态原子核外有8个电子,则Y是O元素;
Z存在质量数为27,中子数为14的核素,则其质子数是13,所以Z是Al元素;
W元素最高价氧化物对应的水化物是一种不溶于水的蓝色固体,则蓝色固体是氢氧化铜,所以W是Cu.X、Y、Z、W是元素周期表前四周期中的常见元素,X的基态原子价电子排布式为:nsnnpn+1,s能级上最多排2个电子,且p能级上还有电子,所以n为2,则x的基态原子最外层电子排布式为:2s22p3,所以X基态原子核外有7个电子,则X是N元素;
Y的基态原子Y原子的最外层电子数是次外层的三倍,所以y基态原子核外有8个电子,则Y是O元素;
Z存在质量数为27,中子数为14的核素,则其质子数是13,所以Z是Al元素;
W元素最高价氧化物对应的水化物是一种不溶于水的蓝色固体,则蓝色固体是氢氧化铜,所以W是Cu.
(1)通过以上分析知,W是铜元素,铜元素位于第四周期第IB族,Z是Al元素,基态原子的核外电子排布式为1s22s22p63s23p1,又因为S只有一个轨道而p有三个轨道,故答案为:四;IB;7;
(2)X是N元素,Y是O元素,由于N元素2p轨道为半充满状态,较稳定,则N的第一电离能大于O,则有N>O;
Y所在族即O、S、Se、Te、Po各种元素的气态氢化物中,由于水分子间含氢键,故沸点最高,其余根据相对分子质量越大沸点越高,所以最低的为H2S
故答案为:大;H2S;
(3)X与Y形成原子个数比为1:2的两种化合物为NO2和N2O4存在化学平衡为2NO2⇌N2O4,再根据平衡常数的表达式得出K=
C(N2O 4)
C 2(NO 2),
故答案:2NO2⇌N2O4,K=
C(N2O 4)
C 2(NO 2);
(4)X的原子与氢原子形成的一种分子中同时存在极性键、非极性键,即N2H4,电子式为 ,
,
氢元素、X、Y 的原子可共同形成多种分子,即H、N、O原子形成的分子要和Al3+反应,则H、N、O原子形成的分子要有碱性即氨水,所以反应的离子方程式为:
Al3++3NH3.H2O=Al(OH)3+3NH4+,故答案为: ;Al3++3NH3.H2O=Al(OH)3+3NH4+.
;Al3++3NH3.H2O=Al(OH)3+3NH4+.点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题考查元素的推断,涉及元素位置的判断、氢化物沸点的判断、电子式的书写、化学平衡常数的书写、离子方程式的书写等知识点,难点是元素的推断,应抓住元素体现的性质来解答.1年前查看全部
- (2013•芜湖县模拟)比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理
(2013•芜湖县模拟)比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理的是( )
序号 化学反映事实 影响化学反应的因素 A 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 反应物浓度 B 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 反应温度 C 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 催化剂 D 粉末状的大理石比块状大理石与盐酸反应快 反应物的种类
A.铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧(影响化学反应的因素:反应物浓度)
B.碳在常温下不与氧气反应,而在点燃时能与氧气反应(影响化学反应的因素:反应温度)
C.双氧水在常温下较难分解,而在加入二氧化锰后迅速分解(影响化学反应的因素:催化剂)
D.粉末状的大理石比石块状大理石与盐酸反应快(影响化学反应的因素:反应物的种类) hueer1年前1
hueer1年前1 -
 weiwei2916188 共回答了20个问题
weiwei2916188 共回答了20个问题 |采纳率95%解题思路:A、铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧,是因为反应物氧气的浓度不同;
B、常温和点燃是不同的温度,所以影响因素是反应的温度;
C、二氧化锰是双氧水分解的催化剂;
D、粉末状的大理石比块状大理石与盐酸反应快,主要是和盐酸的接触面积的不同.A、铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧,是因为反应物氧气的浓度不同,故A正确;
B、常温和点燃是不同的温度,碳在常温下不与氧气发生反应,而在点燃时能与氧气反应所以影响因素是反应的温度,故B正确;
C、二氧化锰是双氧水分解的催化剂,所以双氧水在常温下较难分解,而在加入二氧化锰后迅速分解,影响化学反应的因素催化剂,故C正确;
D、粉末状的大理石比块状大理石与盐酸反应快,主要是和盐酸的接触面积的不同,影响化学反应的因素而不是反应物的种类,故D错误.
故选:D.点评:
本题考点: 影响化学反应速率的因素探究.
考点点评: 影响反应速度的因素主要有:温度、反应物的浓度、催化剂等,在判断影响因素时要注意控制变量来进行判断.1年前查看全部
- (2013•芜湖县)芜湖钢铁厂要生产一批钢材,计划每天生产600吨,20天完成.实际每天生产800吨,实际比计划少用多少
(2013•芜湖县)芜湖钢铁厂要生产一批钢材,计划每天生产600吨,20天完成.实际每天生产800吨,实际比计划少用多少天完成?
 这是马夹不1年前1
这是马夹不1年前1 -
 天蓝天岚 共回答了23个问题
天蓝天岚 共回答了23个问题 |采纳率91.3%解题思路:要求实际比计划少用多少天完成,必须先求出实际用的天数,要求实际用的天,又需要求出这批钢材的生产任务是多少吨,根据工作量、工作效率、工作时间之间的关系解答即可.20-600×20÷800,
=20-12000÷800,
=20-15,
=5(天),
答:实际比计划少用5天完成.点评:
本题考点: 有关计划与实际比较的三步应用题.
考点点评: 解答这类问题一般从问题出发,一步步找到要求的问题与所需的条件,再由条件回到问题即可列式解决.1年前查看全部
- (2010•芜湖县)据调查所知,2008年北京奥运会开幕式的收视人数将高于3976850000人.这个数读作______
(2010•芜湖县)据调查所知,2008年北京奥运会开幕式的收视人数将高于3976850000人.这个数读作______,省略亿后面的尾数是______.
 enternetli1年前1
enternetli1年前1 -
 火花开满枝头 共回答了13个问题
火花开满枝头 共回答了13个问题 |采纳率69.2%解题思路:这是一个十位数,最高位十亿位上是3,亿位上是9,千万位上是7,百万位上是6,十万位上是8,万位上是5,其余各位上都是0,读这个数时,从高位到低位,一级一级地读,每一级末尾的0都不读出来,其余数位连续几个0都只读一个零;省略“亿”后面的尾数就是四舍五入到亿位,把亿位后的千万位上的数进行四舍五入,再在数的后面写上“亿”字.3976850000读作:三十九亿七千六百八十五万;
3976850000≈40亿;
故答案为:三十九亿七千六百八十五万,40亿.点评:
本题考点: 整数的读法和写法;整数的改写和近似数.
考点点评: 本题主要考查整数的读法、改写和求近似数,注意改写和求近似数时要带计数单位.1年前查看全部
- (2013•芜湖县)国务院抗震救灾总指挥部发布:截止2010年5月20日13时,民政部、军队和各地民政部门共向甘肃玉树地
(2013•芜湖县)国务院抗震救灾总指挥部发布:截止2010年5月20日13时,民政部、军队和各地民政部门共向甘肃玉树地震灾区调运救灾帐篷三十七万八千四百六十二顶.三十七万八千四百六十二写作______,四舍五入到万位约是______万.
 haoyanglhy1年前1
haoyanglhy1年前1 -
 feaket 共回答了12个问题
feaket 共回答了12个问题 |采纳率91.7%解题思路:这是一个六位数,最高位十万位上是3,万位上是7,千位上是8,百位上是4十位上是6,个位上是2,写这个数时,从高位到低位,一级一级地写,哪一个数位上一个单位也没有,就在那个数位上写0;省略“万”后面的尾数求它的近似数,要把万位的下一位千位上的数进行四舍五入,再在数的后面写上“万”字.三十七万八千四百六十二 写作:378462;
37 8462≈38万;
故答案为:378462,38万.点评:
本题考点: 整数的读法和写法;整数的改写和近似数.
考点点评: 本题主要考查整数的读法、改写和求近似数,注意改写和求近似数时要带计数单位.1年前查看全部
- (2013•芜湖县)根据下图中提供的信息,完成下列问题.
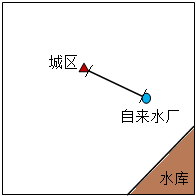 (2013•芜湖县)根据下图中提供的信息,完成下列问题.
(2013•芜湖县)根据下图中提供的信息,完成下列问题.
①自来水厂要从水库取水,取水管道怎样铺最短,请在图中画出来.
②自来水厂到城区的送水管道经测算最短是2000米,请你测算:自来水厂到水库的取水管道最短需多少米? wphwph20071年前1
wphwph20071年前1 -
 猪小者 共回答了23个问题
猪小者 共回答了23个问题 |采纳率82.6%解题思路:(1)因为点到直线的距离垂线段最短,所以只要从自来水厂向水库做一条垂线段即可,即取水管道向水库垂直铺设;
(2)用直尺量出从城区到自来水送管道的图上距离,根据比例尺的含义,先求出比例尺,然后根据“图上距离÷比例尺=实际距离”,代入数字,解答即可.(1)

(2)2000米=200000厘米,
2.5:200000=1:80000,
1.2÷[1/80000]=96000(厘米),
96000厘米=960米,
答:自来水厂到水库的取水管道最短需960米.点评:
本题考点: 图上距离与实际距离的换算(比例尺的应用);过直线上或直线外一点作直线的垂线.
考点点评: 此题做题的关键是先算出这幅图的比例尺,然后根据图上距离、比例尺和实际距离三者之间的关系列式解答即可.1年前查看全部
- (2013•芜湖县)文字题.(1)一个数的3倍比16少0.1,这个数是多少?(用方程解)(2)5除4的商,加上1.2与0
(2013•芜湖县)文字题.
(1)一个数的3倍比16少0.1,这个数是多少?(用方程解)
(2)5除4的商,加上1.2与0.5的积,和是多少? sindy05951年前1
sindy05951年前1 -
 春秋三水 共回答了21个问题
春秋三水 共回答了21个问题 |采纳率90.5%解题思路:(1)设这个数是x它的3倍就是3x,3x加上0.1就是16,由此列出方程求解;
(2)先用4除以5求出商,再用1.2×0.5求出积,然后把求出的商和积相加即可.(1)设这个数为x由题意得:
3x+0.1=16,
3x+0.1-0.1=16-0.1,
3x=15.9,
3x÷3=15.9÷3,
x=5.3;
答:这个数是5.3.
(2)4÷5+1.2×0.5,
=0.8+0.6,
=1.4;
答:和是1.4.点评:
本题考点: 整数、分数、小数、百分数四则混合运算.
考点点评: 这类型的题目要分清楚数量之间的关系,先求什么再求什么,找清列式的顺序,或等量关系,列出算式或方程计算.1年前查看全部
- (2010•芜湖县)甲、乙两辆汽车同时从相距180千米的两地同时相对开出,2.5小时相遇.已知甲乙两车的速度比是5:4,
(2010•芜湖县)甲、乙两辆汽车同时从相距180千米的两地同时相对开出,2.5小时相遇.已知甲乙两车的速度比是5:4,甲与乙速度各多少千米?
 深呼吸0001年前1
深呼吸0001年前1 -
 巨蟒朱蛤 共回答了11个问题
巨蟒朱蛤 共回答了11个问题 |采纳率90.9%解题思路:根据题意,应先求出甲乙两车的速度和,再根据按比例分配的方法,分别求出两车的速度.甲车的速度:
180÷2.5×[5/5+4],
=72×[5/9],
=40(千米);
乙车的速度:
180÷2.5×[4/5+4],
=72×[4/9],
=32(千米);
答:甲车的速度是每小时40千米,乙车的速度是32千米.点评:
本题考点: 简单的行程问题;按比例分配应用题.
考点点评: 此题考查了关系式“路程÷相遇时间=速度和”以及按比例分配的方法.1年前查看全部
- (2013•芜湖县)解方程或解比例.(温馨提醒:注意书写格式哦!) [4/5x−14=34] x:27=14:25.
 aaaa网络收费1年前1
aaaa网络收费1年前1 -
 异欣001 共回答了21个问题
异欣001 共回答了21个问题 |采纳率76.2%解题思路:(1)根据等式的性质,在方程两边同时加上[1/4],再乘[5/4]求解,
(2)先根据比例的基本性质,把原式转化为 [2/5]x=[2/7]×14,再根据等式的性质,在方程两边同时乘[5/2]求解.(1)[4/5]x-[1/4]=[3/4],
[4/5]x-[1/4]+[1/4]=[3/4]+[1/4],
[4/5]x=1,
[4/5]x×[5/4]=1×[5/4],
x=[5/4];
(2)x:
2
7=14:
2
5,
[2/5]x=[2/7]×14,
[2/5]x×[5/2]=4×[5/2],
x=10.点评:
本题考点: 方程的解和解方程;解比例.
考点点评: 本题考查了学生根据等式的性质和比例的基本性质解方程的能力,注意等号对齐.1年前查看全部
- (w050•芜湖县)个.个,y.4,5.n,6.0,4.4,y.4,5.4,y.6,y.4这组数据的众数是______,
(w050•芜湖县)个.个,y.4,5.n,6.0,4.4,y.4,5.4,y.6,y.4这组数据的众数是______,m位数是______,平均数是______.
 林燕1年前1
林燕1年前1 -
 chunwei 共回答了14个问题
chunwei 共回答了14个问题 |采纳率100%解题思路:将一组数据按照从小到大的顺序进行排列,排在中间位置上的数叫作这组数据的中位数,若这组数据的个数为偶数个,那么中间两个数的平均数就是这组数据的中位数,用这组数据的和除以数据的个数就可计算出这组数据的平均数,在这组数据中出现次数最多的数据叫作这组数据的众数.从小到大排列为:4.4,5.2,5.4,6.4,c.c,9.4,9.4,9.4,9.6,
众数为:9.4,
中位数为:c.c,
平均数为:(c.c+9.4+5.2+6.4+4.4+9.4+5.4+9.6+9.4)÷9
=62.6÷9,
≈c.4,
答:这组数据的众数是9.4,中位数是c.c,平均数是c.4.
故答案为:9.4,c.c,c.4.点评:
本题考点: 中位数的意义及求解方法;平均数的含义及求平均数的方法;众数的意义及求解方法.
考点点评: 此题主要考查的是众数、中位数、平均数的含义及其计算方法.1年前查看全部
- (2010•芜湖县)把一个圆柱的侧面展开,得到一个正方形,边长为12.56分米,那么该圆柱体的底面半径是______分米
(2010•芜湖县)把一个圆柱的侧面展开,得到一个正方形,边长为12.56分米,那么该圆柱体的底面半径是______分米,体积是______立方分米.
 hfn5061年前1
hfn5061年前1 -
 春晓雷明 共回答了15个问题
春晓雷明 共回答了15个问题 |采纳率100%解题思路:根据题意可知圆柱的底面周长等于圆柱的高,可利用圆的周长公式C=2πr计算出圆柱的底面半径,然后再利用圆柱的体积=底面积×高进行计算即可得到答案.圆柱的底面半径为:12.56÷3.14÷2
=4÷2,
=2(分米),
圆柱的体积为:3.14×22×12.56
=12.56×12.56,
=157.7536(立方分米),
答:圆柱的底面半径为2分米,体积是157.7536立方分米.
故答案为:2,157.7536.点评:
本题考点: 圆柱的侧面积、表面积和体积.
考点点评: 解答此题的关键是确定圆柱的高,然后再利用圆的周长公式和圆柱的体积公式进行计算即可.1年前查看全部
- (2013•芜湖县)一根绳子长2米,把它平均分成9段,每段长是全长的[1/9][1/9];每段长[2/9][2/9]米.
 风中狂人1年前1
风中狂人1年前1 -
 rewretret1 共回答了23个问题
rewretret1 共回答了23个问题 |采纳率100%解题思路:(1)求每段长是全长的几分之几,平均分的是单位“1”,表示把单位“1”平均分成9份,求的是每一段占的分率;
(2)求每段长的米数,平均分的是具体的数量2米,表示把2米平均分成9份,求的是每一段的具体的数量;都用除法计算.(1)1÷9=
1
9;
(2)2÷9=
2
9(米).
答:每段长是全长的[1/9];每段长[2/9]米.
故答案为:[1/9],[2/9].点评:
本题考点: 分数的意义、读写及分类;分数除法.
考点点评: 解决此题关键是弄清求得是分率还是具体的数量,求分率平均分的是单位“1”;求具体的数量平均分的是具体的数量,要注意:分率不能带单位名称,而具体的数量要带单位名称.1年前查看全部
- (2013•芜湖县)在地图上量得甲、乙两地的距离是5厘米,甲、乙两地之间的实际距离是150千米,这幅地图的数值比例尺是_
(2013•芜湖县)在地图上量得甲、乙两地的距离是5厘米,甲、乙两地之间的实际距离是150千米,这幅地图的数值比例尺是______.
 sunny_hata1年前1
sunny_hata1年前1 -
 1314xiaozhang 共回答了17个问题
1314xiaozhang 共回答了17个问题 |采纳率100%解题思路:比例尺=图上距离:实际距离,根据题意代入数据可直接得出这张地图的比例尺.150千米=15000000厘米,
5:15000000=1:3000000,
答:这幅地图的数值比例尺是1:3000000.
故答案为:1:3000000.点评:
本题考点: 比例尺应用题.
考点点评: 考查了比例尺的概念,掌握比例尺的计算方法,注意在求比的过程中,单位要统一.1年前查看全部
- (2013•芜湖县模拟)电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体
 (2013•芜湖县模拟)电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,下列有关说法正确的是( )(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
(2013•芜湖县模拟)电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,下列有关说法正确的是( )(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
A.a电极反应式为:2H++2e-═H2↑
B.产物丙为硫酸溶液
C.离子交换膜d为阴离子交换膜
D.每转移0.1 mol电子,产生1.12 L的气体乙 shionsky1年前1
shionsky1年前1 -
 hensxhensx 共回答了19个问题
hensxhensx 共回答了19个问题 |采纳率78.9%解题思路:电解硫酸钠溶液时,阳极上生成氧气,电极反应式为2H2O-4e-=O2↑+4H+,阴极反应式为 2H2O+2e-=H2↑+2OH-,测得同温同压下,气体甲与气体乙的体积比约为1:2,则甲是氧气、乙是氢气,则a是阳极、b是阴极,阳极区域生成硫酸、阴极区域生成NaOH,据此分析解答.电解硫酸钠溶液时,阳极上生成氧气,电极反应式为2H2O-4e-=O2↑+4H+,阴极反应式为 2H2O+2e-=H2↑+2OH-,测得同温同压下,气体甲与气体乙的体积比约为1:2,则甲是氧气、乙是氢气,则a是阳极、b是阴极,阳极区域生成硫酸、阴极区域生成NaOH,
A.a为阳极,电极反应式为2H2O-4e-=O2↑+4H+,故A错误;
B.通过以上分析知,a为阳极,同时生成硫酸,所以产物丙是硫酸,故B正确;
C.产物丁是NaOH,则离子交换膜d是阳离子交换膜,故C错误;
D.生成乙的电极反应式为2H2O+2e-=H2↑+2OH-,每转移0.1 mol电子,产生氢气的物质的量为0.05mol氢气,但温度和压强未知,无法确定气体摩尔体积,则无法计算氢气体积,故D错误;
故选B.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查电解原理,判断甲、乙气体成分是解本题关键,再结合电极反应式分析解答,易错选项是D,注意气体摩尔体积的适用范围及适用条件,为易错点.1年前查看全部
- (2010•芜湖县)A、B、C、D四种不同规格的钉子240枚混合在一起,其中A和B的个数之和占总个数的[2/3],且A和
(2010•芜湖县)A、B、C、D四种不同规格的钉子240枚混合在一起,其中A和B的个数之和占总个数的[2/3],且A和B的个数和与A和C的个数和之比为8:9,A和D的个数和占总个数的[3/5],A、B、C、D四种钉子各有多少枚?
 yangzi28161年前1
yangzi28161年前1 -
 叹息暗香 共回答了25个问题
叹息暗香 共回答了25个问题 |采纳率88%解题思路:根据题意,可以求出A和B、A和C、A和D的个数,然后把这三个和相加再减去240枚,就是A的2倍,求出A的个数.进一步求出B、C、D四种钉子的个数,解决问题.A和B的个数之和:
240×[2/3]=160(枚);
A和C的个数和:
160×[9/8]=180(枚);
A和D的个数和:
240×[3/5]=144(枚);
A的个数:
(160+180+144-240)÷2,
=244÷2,
=122(枚);
B的个数:
160-122=38(枚);
C的个数:
180-122=58(枚);
D的个数:
144-122=22(枚);
答:A、B、C、D四种钉子各有122、38、58、22枚.点评:
本题考点: 分数四则复合应用题.
考点点评: 此题解答的关键是分别求出A和B、A和C、A和D的个数.1年前查看全部
- (2010•芜湖县)某公司的出勤率为90%,缺勤人数与出勤人数之比为( )
(2010•芜湖县)某公司的出勤率为90%,缺勤人数与出勤人数之比为( )
A.1:10
B.9:10
C.1:9
D.10:1 月影纱秋1年前1
月影纱秋1年前1 -
 youfeng0313 共回答了10个问题
youfeng0313 共回答了10个问题 |采纳率80%解题思路:根据出勤率的意义与题意知道出勤的人数与公司的总人数的比[90/100],由此把出勤的人数看作90份,总人数是100份,则缺勤的人数为(100-90)份,用缺勤人数的份数比出勤人数的份数,再化简即可.(100-90):90,
=10:90,
=1:9,
答:缺勤人数与出勤人数为1:9;
故选:C.点评:
本题考点: 比的意义;百分率应用题.
考点点评: 解答本题的关键是根据出勤率的意义,找出缺勤人数的份数,写出对应的比化简即可.1年前查看全部
- (2013•芜湖县)把一个棱长为a米的正方体,任意截成两个长方体,这两个长方体的表面积是( )平方米.
(2013•芜湖县)把一个棱长为a米的正方体,任意截成两个长方体,这两个长方体的表面积是( )平方米.
A.6a2
B.8a2
C.10a2
D.12a2 emasaya1年前1
emasaya1年前1 -
 无心插柳了啊08 共回答了16个问题
无心插柳了啊08 共回答了16个问题 |采纳率93.8%解题思路:由题意可知:把一个棱长为a米的正方体,任意截成两个长方体后,表面积增加了两个面的面积,即增加了2a2平方米,于是可以求出两个长方体的表面积.a×a×6+a×a×2,
=6a2+2a2,
=8a2;
答:这两个长方体的表面积是8a2平方米.
故选:B.点评:
本题考点: 长方体和正方体的表面积;用字母表示数.
考点点评: 解答此题的关键是明白:把一个正方体任意截成两个长方体后,表面积增加了两个面的面积.1年前查看全部
- (2013•芜湖县模拟)在恒容的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3
(2013•芜湖县模拟)在恒容的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内气体密度逐渐减小
B.平衡时,若断裂π键0.4 mol,则放出的热量为18.48 kJ
C.平衡后,再向容器中通入1 mol氦气,H2的转化率增大
D.平衡后,缩小容器体积,N2的浓度减小 specterdragon1年前1
specterdragon1年前1 -
 andhe 共回答了19个问题
andhe 共回答了19个问题 |采纳率89.5%解题思路:A、ρ=[m/V],反应前后都是气体,气体质量不变,恒容容器,V不变;
B、1mol氮气中有2molπ键,据热化学放出计算;
C、容器体积不变,充入氦气,平衡不移动;
D、平衡后,缩小容器体积导致每种气体的浓度都增大,平衡正向移动,但每种气体的浓度都比原平衡大.A、ρ=[m/V],反应前后都是气体,气体质量不变,恒容容器,V不变,所以容器内气体密度始终不变,故A错误;
B、1mol氮气中有2molπ键,断裂2molπ键放热92.4J,所以断裂π键0.4 mol,则放出的热量为18.48 kJ,故B正确;
C、容器体积不变,充入氦气,平衡不移动,故C错误;
D、平衡后,缩小容器体积导致每种气体的浓度都增大,平衡向气体体积减小的正向移动,据勒夏特列原理,氮气和氢气的浓度都比原平衡大,故D错误;
故选B.点评:
本题考点: 化学平衡的影响因素;化学平衡建立的过程.
考点点评: 本题考查了π键的相关知识、平衡移动的相关知识、反应容器中气体密度变化,题目难度中等.1年前查看全部
- (2011•芜湖县模拟)学习了热学知识后,小宇通过实验得知,用电热壶将20℃、15kg的水加热到100℃,需要1.05元
(2011•芜湖县模拟)学习了热学知识后,小宇通过实验得知,用电热壶将20℃、15kg的水加热到100℃,需要1.05元电费;用液化气灶做同样的实验,则需要消耗0.42元的液化气.已知水的比热C水=4.2×103J/kg•℃.
(1)如果使用煤炉做同样的实验,已知煤炉燃烧所用无烟煤的热值为3.4×107J/kg,假设煤炉的热能利用率为20%,无烟煤的价格是0.34元/kg,则需花费多少钱?
(2)煤炉的热能利用率仅为20%,请分析无烟煤炉效率低的原因是什么?
(3)如果某地区可以同时提供电、液化气和煤,从经济和环保等角度综合分析,你会建议使用哪种燃料?请阐明理由. 阿财十六1年前1
阿财十六1年前1 -
 果儿罗 共回答了19个问题
果儿罗 共回答了19个问题 |采纳率100%解题思路:(1)知道水的质量、比热容和水升高的温度值,利用吸热公式求实验中水吸收的热量,又知道无烟煤的热值和煤炉的热能利用率,利用Q吸=Q放×η=mqη计算需要的无烟煤,又知道无烟煤的价格,可以算出用无烟煤加热的花费;
(2)用煤燃烧加热时,煤不能完全燃烧、热量散失严重,燃料燃烧放出的热量不能全部被水吸收;
(3)通过分析烧开同一壶水的花费以及污染大小,选择使用哪种燃料.(1)把水加热需吸收的热量:
Q吸=cm(t-t0)=4.2×103J/(kg•℃)×15kg×(100℃-20℃)=5.04×106J
∵煤炉的热能利用率为20%,
∴燃烧煤需放热Q放=
Q吸
20%=
5.04×107J
20%=2.52×107J,
根据Q放=mq可得:
燃烧煤的质量m=
Q放
q=
2.52×107J
3.4×107J/kg≈0.74kg,
燃烧煤需花钱:
0.34元/kg×0.74kg=0.252元;
(2)煤炉的热能利用率仅为20%,无烟煤炉效率低的原因是:煤不能完全燃烧;热量散失严重;
(3)用电热壶将20℃的15㎏的水加热到100℃,需要1.05元电费、需要消耗0.42元的煤气、0.25元的无烟煤.虽然无烟煤花费少,但燃烧时产生废气,污染大;用电,无污染,但花费高;用煤气污染小、价格适中,所以建议使用煤气.
答:(1)如果使用煤炉做同样的实验,则需花费0.252元;
(2)煤不能完全燃烧;热量散失严重;
(3)建议选择液化气,因为液化气价格适中,且污染较小.点评:
本题考点: 电功与热量的综合计算.
考点点评: 本题是一道电学与热学的综合应用题,与生活相连,使学生觉得学了物理有用,且加强了学生的节能环保的意识.1年前查看全部
- (2013•芜湖县)甲2小时做14个零件,乙做一个零件[1/6]小时,丙每小时做8个零件,这三个人中工作效率最高的是__
(2013•芜湖县)甲2小时做14个零件,乙做一个零件[1/6]小时,丙每小时做8个零件,这三个人中工作效率最高的是______.
 jackculb1年前1
jackculb1年前1 -
 gg笔记本 共回答了22个问题
gg笔记本 共回答了22个问题 |采纳率90.9%解题思路:甲:工作效率=工作量÷工作时间,那么甲的工作效率就是14÷2=7(个);乙:乙做一个零件要[1/6]小时,我们看1小时做多少个零件,就是1小时里有多少个[1/6]小时,用除法1÷[1/6]=6(个);丙:每小时做8个零件.比较这三个数的大小.甲:14÷2=7(个),甲每小时做7个;乙:1÷[1/6]=6(个),乙每小时做6个;丙:每小时做8个零件.
6<7<8,故填丙.点评:
本题考点: 简单的工程问题.
考点点评: 甲的工效可用工作效率=工作量÷工作时间求解,而乙的工效是求1小时里包含几个[1/6],用除法,1÷[1/6]=6(个).1年前查看全部
- (2010•芜湖县)列式计算(1)1.5除9的商与3.6的25%的差是多少?(2)比一个数的[5/6]多12的数是17,
(2010•芜湖县)列式计算
(1)1.5除9的商与3.6的25%的差是多少?
(2)比一个数的[5/6]多12的数是17,这个数是多少?
(3)一个数的一半是1[3/4],这个数的80%是多少? grace161年前1
grace161年前1 -
 爱尚希凡 共回答了23个问题
爱尚希凡 共回答了23个问题 |采纳率95.7%解题思路:(1)1.5除9的商为9÷1.5,3.6的25%为3.6×25%,所以1.5除9的商与3.6的25%的差是9÷1.5-3.6×25%;
(2)比一个数的[5/6]多12的数是17,即17减去12是这个数的[5/6],根据分数除法的意义可知,这个数为(17-12)÷[5/6];
(3))一个数的一半是1[3/4],则这个数为1[3/4]×2,它的80%为1[3/4]×2×80%.(1)9÷1.5-3.6×25%
=6-0.9,
=5.1.
答:差是5.1.
(2)(17-12)÷[5/6]
=5÷
5
6,
=6.
答:这个数是6.
(3)1[3/4]×2×80%
=3.5×80%,
=2.8.
答:这个数的80%为2.8.点评:
本题考点: 整数、分数、小数、百分数四则混合运算;分数的四则混合运算.
考点点评: 完成此类题目要认真分析各小题中数据之间的关系,然后列出正确算式.1年前查看全部
- (2013•芜湖县模拟)硫酸亚铁铵晶体[(NH4)2Fe(5O4)2•6H2O]俗称“摩尔盐”,是分析化学中的重要试剂.
(2013•芜湖县模拟)硫酸亚铁铵晶体[(NH4)2Fe(5O4)2•6H2O]俗称“摩尔盐”,是分析化学中的重要试剂.
(1)查阅文献:硫酸亚铁铵晶体在500℃时隔绝空气加热完全分解,固体产物可能有FeO和Fe2O3,则气体产物可能有NH3、5O3、H2O、N2和______.
(2)为检验分解产物的成分,设计如图实验装置.隔绝空气加热十中的硫酸亚铁铵至分解完全.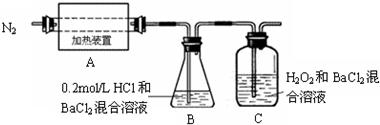
①十中固体充分加热较长时间后,再通入氮气,目的是______.
②装置B的作用是为了检验分解产物中是否有______气体生成;实验中,观察到C中有白色沉淀生成,则C中发生反应的离子方程式为______.
③甲同学设计实验验证十中残留物是否含有FeO,请帮他完成表中内容.
限选试剂:65CN溶液、浓盐酸、稀硫酸、6MnO4溶液、稀硝酸、蒸馏水.仪器和用品自选.
④乙同学认为只需精确称量加热前后固体的质量即可确定残留固体的成分,你是否同意乙同学的看法,并简述理由:______.实验步骤 预期现象和结论 ______ ______  nana12081年前1
nana12081年前1 -
 saullw 共回答了25个问题
saullw 共回答了25个问题 |采纳率84%解题思路:(1)根据硫酸亚铁铵晶体[(NH4)2Fe(SO4)2•6H2O]的化学式组成及质量守恒定律判断;
(2)①依据实验测定过程分析,通入氮气可以使分解生成的气体全部赶到装置BC中完全吸收;
②三氧化硫和氯化钡溶液反应生成硫酸钡沉淀;装置C中通入二氧化硫和过氧化氢发生氧化还原反应,生成硫酸和氯化钡反应生成硫酸钡沉淀;
③氧化亚铁具有还原性,能够被酸性高锰酸钾溶液氧化从而使高锰酸钾溶液褪色,据此可以判断A中残留物否是否有氧化亚铁;
④氧化亚铁和氧化铁的摩尔质量不同,主要(NH4)2Fe(SO4)2•6H2O的质量固定,则生成的氧化亚铁和氧化铁的质量会不同,据此进行判断.(1)硫酸亚铁铵晶体的化学式为:(N她t)2Fe(Syt)2•d她2y,在500℃时隔绝空气加热完全分解,固体产物可能有Fey和Fe2y1,则气体产物可能有N她1、Sy1、她2y、N2,还可能含有Sy2,
故答案为:Sy2;
(2)①A中固体充分加热较长时间后,通入氮气目的是使分解生成的 气体在她C装置中完全吸收,
故答案为:将分解生成的气体在她C装置中完全吸收;
②装置她中她aC12溶液的作用是为了检验分解产物中是否有Sy1气体生成,若含有该气体,会生成硫酸钡白色沉淀,观察到的观象为溶液变浑浊;
装置C中通入二氧化硫和过氧化氢发生氧化还原反应,生成硫酸和氯化钡反应生成硫酸钡沉淀,反应的离子方程式为:Sy2+她2y2+她a2+=她aSyt↓+2她+,
故答案为:Sy1;Sy2+她2y2+她a2+=她aSyt↓+2她+;
③根据亚铁离子的还原性,可以用高锰酸钾溶液检验,方法为:取少量A中残留物与试管中,加入适量稀硫酸,充分振荡使其完全溶解,在所九溶液中滴加高锰酸钾溶液,并振荡,若高锰酸钾溶液褪色,则残留物中含有Fey;若高锰酸钾溶液不褪色,则残留物中不含Fey,
故答案为:
实验步骤预期现象和结论
取少量A中残留物与试管中,加入适量稀硫酸,充分振荡使其完全溶解;
在所九溶液中滴加高锰酸钾溶液,并振荡.若高锰酸钾溶液褪色,则残留物中含有Fey;
若高锰酸钾溶液不褪色,则残留物中不含Fey.④将一定量的(N她t)2Fe(Syt)2•d她2y完全分解后生成Fey或Fe2y1的量是确定的,且二者的质量不相同,所以只需精确称量加热前后固体的质量即可确定残留固体的成分,
故答案为:同意,一定量的(N她t)2Fe(Syt)2•d她2y完全分解后生成Fey或Fe2y1的量是确定的,且各不相同.点评:
本题考点: 性质实验方案的设计.
考点点评: 本题通过探究硫酸亚铁铵晶体的组成成分及检验,考查了性质实验方案的设计方法,题目难度中等,注意掌握常见物质的性质及检验方法,明确性质实验方案的设计与评价原则,试题有利于培养学生的分析、理解能力及化学实验能力.1年前查看全部
- (2011•芜湖县模拟)某校自制一个太阳能热水器,它的反射面的有效面积是2.5m2,太阳光对此镜面辐射的能量平均每小时为
(2011•芜湖县模拟)某校自制一个太阳能热水器,它的反射面的有效面积是2.5m2,太阳光对此镜面辐射的能量平均每小时为2.5×106J/m2,如果整个装置的效率是52%,那么这个热水器每小时可把多少千克15℃的水加热到60℃?
 言随心行1年前1
言随心行1年前1 -
 xxxx29zndb 共回答了21个问题
xxxx29zndb 共回答了21个问题 |采纳率95.2%反射面吸收的能量是:E=2.5×106J/m2×2.5m2=6.25×106J
水吸收的热量为:Q=52%×6.25×106J=3.25×106J
根据公式Q=cm(t-t0)得,
m=
Q
c(t−t0)=
3.25×106J
4.2×103J/(kg•℃)×(60℃−15℃)=17.2kg
答:这个热水器每小时可以把17.2kg15℃的水加热到60℃.1年前查看全部
- (2013•芜湖县模拟)小明为了测定空气的成分,按下图所示装置做实验:
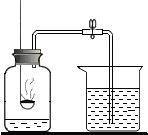 (2013•芜湖县模拟)小明为了测定空气的成分,按下图所示装置做实验:
(2013•芜湖县模拟)小明为了测定空气的成分,按下图所示装置做实验:
(1)将燃烧匙中过量的红磷点燃放入集气瓶中,观察到的现象是______.
(2)反应停止,等集气瓶冷却后,打开弹簧夹,烧杯中的水会______,大约达到集气瓶体积的[1/5][1/5]为止.
(3)剩余气体具有的性质______、______.
(4)小伟也做了上述实验,但结果他所测得的氧气含量偏小,试分析导致小伟实验失败的原因是什么______、______(至少写出两点).
(5)小莉想使用镁条来代替红磷做实验,老师告诉她这种方法不是较好的方法,因为镁条在空气中燃烧非常剧烈,镁既可以和氧气反应,也可以和氮气反应生成氮化镁.写出镁和氮气反应生成氮化镁的化学反应的文字表达式:镁+氮气
氮化镁点燃 镁+氮气.
氮化镁点燃
(6)实验课上,某同学用足量的木炭代替红磷做测定空气中氧气含量的实验,结果实验失败了,请你帮助他分析原因______. 黎樱诺1年前1
黎樱诺1年前1 -
 持有华联控股 共回答了17个问题
持有华联控股 共回答了17个问题 |采纳率94.1%解题思路:(1)根据红磷燃烧的现象分析回答;
(2)根据瓶内压强的变化及空气中氧气的体积分数分析回答;
(3)瓶内剩余的气体主要是氮气,根据上述实验分析氮气的性质;
(4)根据测定空气中氧气含量实验的注意事项分析回答;
(5)根据镁与氮气的反应写出反应的方程式;
(6)根据碳燃烧的产物是二氧化碳气体分析回答.(1)红磷在集气瓶内燃烧的现象是:红磷燃烧、产生大量白烟.(2)由于红磷燃烧消耗了瓶内的氧气,瓶内的压强减小.反应停止,等集气瓶冷却后,打开弹簧夹,烧杯中的水会沿导管进入集气瓶,由于空气中氧气的体积分数...
点评:
本题考点: 空气组成的测定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查的是空气中氧气含量的探究实验,是中考的主要考点之一.本题根据实验操作图,回忆实验中现象,由实验中的注意事项,对实验结果进行评价,从而理解该实验的探究目的.对实验结果进行评价,是近几年中考的重点之一,要好好把握.1年前查看全部
- (2011•芜湖县模拟)如图1所示,用温度计测量液体的温度,下列哪种操作是正确的______,测出的读数如图2所示,则液
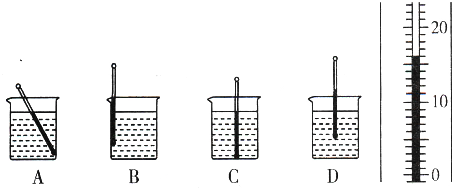
(2011•芜湖县模拟)如图1所示,用温度计测量液体的温度,下列哪种操作是正确的______,测出的读数如图2所示,则液体温度为______℃.
 卡露娜1年前1
卡露娜1年前1 -
 陈毅仁 共回答了19个问题
陈毅仁 共回答了19个问题 |采纳率84.2%解题思路:(1)测量液体温度时,必须使温度计的玻璃泡全部浸在被测液体中,不能碰到容器底和容器壁.
(2)温度计的示数在量程的范围内,且分度值为1℃,可根据这两点读出此温度计的示数.(1)A图中显示温度计的玻璃泡碰到容器底,温度计的使用方法不正确.
B图中显示温度计的玻璃泡碰到容器壁,温度计的使用方法不正确.
C图中显示温度计的玻璃泡碰到容器底,温度计的使用方法不正确.
D图中显示温度计的玻璃泡全部浸在被测液体中,没有碰到容器底和容器壁碰到容器底;使用方法正确.
综上所述,D选项操作正确.
(2)由图2知:温度计的最小刻度值是1℃,因此该温度计的示数是10℃+6℃=16℃.
故答案为:D;16.点评:
本题考点: 温度计的使用及其读数.
考点点评: 实验室温度计的使用中一定要注意如何做才能让玻璃泡全部浸在被测液体中,并不能碰到容器底和容器壁.同时考查了温度计的读数问题,要首先观察温度计的量程和分度值,并且视线要与温度计的液柱上表面持平.1年前查看全部
- (2013•芜湖县模拟)2008年北京奥运会祥云火炬如图所示,其燃料为丙烷(C3H8).下列关于丙烷性质的描述,属于化学
 (2013•芜湖县模拟)2008年北京奥运会祥云火炬如图所示,其燃料为丙烷(C3H8).下列关于丙烷性质的描述,属于化学性质的是( )
(2013•芜湖县模拟)2008年北京奥运会祥云火炬如图所示,其燃料为丙烷(C3H8).下列关于丙烷性质的描述,属于化学性质的是( )
A.无色气体
B.着火点为450℃,易燃
C.沸点为-42.1℃,易液化
D.微溶于水,可溶于酒精 ElainPage1年前1
ElainPage1年前1 -
 hmin888 共回答了17个问题
hmin888 共回答了17个问题 |采纳率94.1%解题思路:物理性质是指物质不需要发生化学变化就表现出来的性质.化学性质是指物质在化学变化中表现出来的性质.而化学变化的本质特征是变化中有新物质生成,因此,判断物理性质还是化学性质的关键就是看表现物质的性质时是否有新物质产生.物质的颜色、状态、气味、熔点、沸点、硬度、密度、溶解性、挥发性等性质,不需要发生化学变化就表现出来,因此,都属于物理性质.
A、无色气体属于物质的颜色、状态不需要通过化学变化表现出来,属于物理性质,故A错;
B、丙烷的易燃性是通过丙烷燃烧表现出来的,丙烷燃烧生成二氧化碳和水,所以易燃性属于化学性质,故B正确;
C、丙烷液化是由气体变为液体,属于物理变化,所以易液化属于物理性质,故C错;
D、微溶于水,可溶于酒精,属于物质的溶解性,不需要通过化学变化表现出来,属于物理性质,故D错.
故选B.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变化、化学变化来理解物理性质和化学性质,则掌握起来并不困难.1年前查看全部
- (2010•芜湖县)求未知数x.
(2010•芜湖县)求未知数x.
(1)32-40%x=8;
(2)0.8:1[1/8]=[24/x];
(3)5x-2.6x=0.64. erik_901年前1
erik_901年前1 -
 63479469 共回答了22个问题
63479469 共回答了22个问题 |采纳率90.9%解题思路:(1)根据等式的性质,在方程两边同时加上40%x,再在方程的两边同时减去8,再同时除以40%得解;
(2)根据比例的性质,先把比例式转化成等式0.8x=1[1/8]×24,再根据等式的性质,在方程两边同时除以0.8得解;
(3)利用乘法分配律的逆运算,先求出5x-2.6x=2.4x,再根据等式的性质,在方程两边同时除以2.4得解.(1)32-40%x=8,
32-40%x+40%x=8+40%x,
40%x+8-8=32-8,
40%x÷40%=24÷40%,
x=60;
(2)0.8:1[1/8]=[24/x],
0.8x=1[1/8]×24,
0.8x÷0.8=27÷0.8,
x=33.75;
(3)5x-2.6x=0.64,
2.4x=0.64,
2.4x÷2.4=0.64÷2.4,
x=[4/15].点评:
本题考点: 方程的解和解方程;解比例.
考点点评: 此题主要考查学生根据比例的性质解比例和根据等式的性质解方程的能力,注意等号对齐.1年前查看全部
- (2013•芜湖县模拟)下列溶液中离子浓度的关系一定正确的是( )
(2013•芜湖县模拟)下列溶液中离子浓度的关系一定正确的是( )
A.等物质的量的弱酸HA与其钾盐KA的混合溶液中:2c(K+)=c(HA)+c(A-)
B.pH相同的CH3COONa溶液、Ba(OH)2溶液、KHCO3溶液:c(K+)>c(Na+)>c(Ba2+)
C.氨水中逐滴加入盐酸得到的酸性溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.pH=3的一元酸HA溶液和pH=11的一元碱MOH溶液等体积混合:c(M+)=c(A-)>c(H+)=c(OH-) chenguang19811年前1
chenguang19811年前1 -
 曾经沧海就是水 共回答了24个问题
曾经沧海就是水 共回答了24个问题 |采纳率79.2%解题思路:A.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
B.pH相等的这三种溶液,氢氧化钡是强碱,其浓度最小,弱酸根离子水解程度越大其溶液浓度越小;
C.混合溶液呈酸性,则c(H+)>c(OH-),如果溶液中盐酸的物质的量大于氯化铵,则存在c(NH4+)<c(H+);
D.混合溶液可能呈中性、酸性或碱性.A.任何电解质溶液中都存在物料守恒,根据物料守恒得2c(K+)=c(HA)+c(A-),故A正确;
B.pH相等的这三种溶液,氢氧化钡是强碱,其浓度最小,弱酸根离子水解程度越大其溶液浓度越小,酸根离子水解程度HCO3->CH3COO-,则这三种溶液浓度大小顺序是CH3COONa>KHCO3>Ba(OH)2,故B错误;
C.混合溶液呈酸性,则c(H+)>c(OH-),如果溶液中盐酸的物质的量大于氯化铵,则存在c(NH4+)<c(H+),故C错误;
D.如果酸是强酸、碱是弱碱,二者等体积混合后溶液呈碱性,如果酸和碱都是强电解质,则二者等体积混合后溶液呈中性,如果酸是弱酸、碱是强碱,二者混合后溶液呈酸性,所以混合溶液可能呈中性、酸性或碱性,故D错误;
故选A.点评:
本题考点: 离子浓度大小的比较.
考点点评: 本题考查离子浓度大小比较,明确物质的性质及混合溶液酸碱性是解本题关键,再结合守恒思想分析解答,易错选项是CD,注意正确判断C选项中是否含有盐酸,为易错点.1年前查看全部
- (2011•芜湖县模拟)小明同学在做“观察水的沸腾”的实验时,
(2011•芜湖县模拟)小明同学在做“观察水的沸腾”的实验时,
(1)下列温度计中应选择______
A.体温计B.水银温度计(量程为-10℃~110℃)
C.家用寒暑表(量程为-20℃~60℃)D.酒精温度计(量程为-80℃~50℃)
(2)温度计的工作原理是______.
(3)测得温度随时间变化的实验数据如下表:
a、该实验的数据纪录中明显错误的是第______min时刻.试分析引起这个明显错误的可能原因是______.时间/min 0 1 2 3 4 5 6 7 8 9 10 温度/℃ 90 92 94 96 97 98 98 96 98 98 …
b、分析表中数据,可知水沸腾时的沸点是______;水沸腾过程中继续对它加热,水的温度将会______.(升高/不变/下降 ) 977551年前1
977551年前1 -
 wulang4004 共回答了22个问题
wulang4004 共回答了22个问题 |采纳率95.5%解题思路:(1)要正确地选择温度计,需要了解各温度计的量程.体温计、家用寒暑表、酒精温度计的最大测量值都不会达到100℃.
(2)常用的温度计(酒精温度计、水银温度计)都是根据液体的热胀冷缩性质制成的.
(3)a、水达到沸点后继续加热,但温度不升高,由此我们可以判断出错误的数据;从温度计的正确度数去分析这个明显错误的原因.
b、根据水沸腾时候的特点:温度不变,继续吸热来解答此题.(1)体温计的量程在35℃~42℃,家用寒暑表的量程是-30℃~50℃,水银温度计的量程为-10℃~110℃,酒精温度计的量程为-80℃~50℃.而标准大气压下水的沸点是100℃,所以应选择水银温度计.(2)温度计是利用液体...
点评:
本题考点: 探究水的沸腾实验.
考点点评: 此题主要考查了对各种温度计的选用、使用,此题是观察水的沸腾,要用温度计测量水的温度,所以要会进行温度计的读数.同时考查了水沸腾的条件及特点,知道水在沸腾过程中温度保持不变,但要不断吸热.1年前查看全部
- (2010•芜湖县)小红有四件裙子,红色、黄色、蓝色、白色.今天她从中任选一件来穿,穿黄色裙子的可能性为[1/4][1/
(2010•芜湖县)小红有四件裙子,红色、黄色、蓝色、白色.今天她从中任选一件来穿,穿黄色裙子的可能性为[1/4][1/4].
 躺在海中央1年前1
躺在海中央1年前1 -
 安田美沙子 共回答了9个问题
安田美沙子 共回答了9个问题 |采纳率77.8%1÷4=[1/4],
答:穿黄色裙子的可能性为[1/4].
故答案为:[1/4].1年前查看全部
- (2013•芜湖县模拟)用下列装置进行实验能达到相应实验目的是( )
(2013•芜湖县模拟)用下列装置进行实验能达到相应实验目的是( )
A.
收集SO2气体
B.
检验产生的C2H4
C.
除去Fe2O3中的Fe(OH)3
D.
配制银氨溶液 CZM2001ren1年前1
CZM2001ren1年前1 -
 色非是空 共回答了20个问题
色非是空 共回答了20个问题 |采纳率95%解题思路:A.根据二氧化硫的密度判断;
B.检验乙烯,应排除乙醇的影响;
C.加热固体,在坩埚中进行;
D.配制银氨溶液,应在硝酸银中滴加氨水.A.二氧化硫的密度比空气大,应用向上排空法收集,故A错误;
B.乙醇易挥发,可与酸性高锰酸钾发生氧化还原反应,检验乙烯,应排除乙醇的影响,故B错误;
C.加热固体,在坩埚中进行,故C正确;
D.配制银氨溶液,应在硝酸银中滴加氨水,注意氨水不能加入过多,至沉淀恰好完全溶解为止,故D错误.
故选C.点评:
本题考点: 化学实验方案的评价.
考点点评: 本题考查较为综合,涉及气体的收集、检验、固体分解以及溶液的配制等知识,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.1年前查看全部
- (2013•芜湖县模拟)下列有关催化剂的说法正确的是( )
(2013•芜湖县模拟)下列有关催化剂的说法正确的是( )
A.没有二氧化锰的催化,过氧化氢也能分解放出氧气
B.二氧化锰是催化剂
C.催化剂就是用来加快化学反应速率的
D.催化剂在化学反应前后的性质不变 kinglijer1年前1
kinglijer1年前1 -
 感谢朋友 共回答了14个问题
感谢朋友 共回答了14个问题 |采纳率78.6%解题思路:在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.A、没有二氧化锰的催化,过氧化氢也能分解放出氧气,但速度太慢,故A正确;
B、二氧化锰在双氧水、氯酸钾分解反应中是催化剂,而在高锰酸钾分解反应中则是生成物催化剂.B法错误;
C、由催化剂的定义可知,催化剂能改变化学反应速率,有的是为了可加快有的是为了减慢,C说法正确;
D、催化剂在化学反应前后化学性质不改变,物理性质有可能改变,故D说法错误.
故选:A.点评:
本题考点: 催化剂的特点与催化作用.
考点点评: 本题考查了对催化剂特点的理解,解题时只要把握催化剂的特点是只改变反应的速度,而本身的质量和化学性质都不变的特性即可.1年前查看全部
- (2013•芜湖县模拟)下列有关规范实验操作的叙述不正确的是( )
(2013•芜湖县模拟)下列有关规范实验操作的叙述不正确的是( )
A.严禁未经清洗的滴管再吸取其它试剂
B.禁止向正燃着的酒精灯里添加酒精
C.不得用手接触药品,更不得品尝任何药品的味道
D.实验用剩余的药品要放回原瓶 uiuuyy22g21年前1
uiuuyy22g21年前1 -
 hanlalala 共回答了14个问题
hanlalala 共回答了14个问题 |采纳率92.9%解题思路:A、严禁未经清洗的滴管再吸取其它试剂,防止污染其他药品;
B、禁止向正燃着的酒精灯里添加酒精,会引起酒精失火,造成危险;
C、不得用手接触药品,更不得品尝任何药品的味道,防止中毒或受腐蚀;
D、实验用剩余的药品不能放回原瓶,防止污染药品.A、严禁未经清洗的滴管再吸取其它试剂,说法正确,故A正确;
B、禁止向正燃着的酒精灯里添加酒精,说法正确,故B正确;
C、不得用手接触药品,更不得品尝任何药品的味道,说法正确,故C正确;
D、实验用剩余的药品要放回原瓶,说法错误,因为实验用剩余的药品不能放回原瓶,防止污染药品,故D错误.
故选D.点评:
本题考点: 实验操作注意事项的探究.
考点点评: 了解具备基本的化学实验技能是学习化学和进行化学探究活动的基础和保证.只有掌握化学实验的基本技能,才能安全、准确地进行化学实验.1年前查看全部
- (2013•芜湖县)看图回答问题
(2013•芜湖县)看图回答问题
2010年初前,我国西南地区发生重大旱灾,某小学学生利用零用钱向遭受旱灾的学校捐资.
(1)______年级的捐资金额最多,这个学校平均每个年级捐款是______元.
(2)二年级捐资金额是四年级捐资金额的______%.
(3)四年级捐资金额比五年级少______%. X娃娃1年前1
X娃娃1年前1 -
 cdwbeckham 共回答了19个问题
cdwbeckham 共回答了19个问题 |采纳率94.7%解题思路:(1)比较直条高矮就可找出捐款的多少;求出六个年级捐款的总数,然除以6就是平均每个年级捐款的钱数;
(2)用二年级捐款的钱数除以四年级捐款的钱数即可;
(3)先求出四年级比五年级少捐多少钱,然用少捐的钱数除以五年级捐款的钱数即可.(1)六年级的捐资金额最多;
(370+350+420+400+500+540)÷6,
=2580÷6,
=430(元).
答:这个学校平均每个年级捐款是 430元.
(2)350÷400=87.5%;
答:二年级捐资金额是四年级捐资金额的 87.5%.
(3)(500-400)÷500,
=100÷500,
=20%;
答:四年级捐资金额比五年级少 20%.
故答案为:六,430,87.5,20.点评:
本题考点: 以一当五(或以上)的条形统计图;百分数的实际应用;从统计图表中获取信息.
考点点评: 先根据统计图读出数据,再结合问题找出数量关系列式求解.1年前查看全部
大家在问
- 1下列各句中,加点的成语(或熟语)使用不恰当的一句是 A.身处高三的我们踌躇满志,意气昂扬,为了自己的理想,为了父母亲人的
- 2资本主义国家和社会主义国家在发展的过程中有怎样的特点
- 3数学问题,求解答著名数学家高斯计日的方法与众不同,在他的“日历”里,只有“日”,没有“年”和“月”,几日的起点是他自己的
- 4描写春天的文章 200字,只要和春天有关的就可以。
- 5H2O2中加入Mno2,当产生0.1mol的O2时,转移的电子数是0.4NA,这句话对吗?为什么?
- 6cute意思是?
- 7直线x=m,y=x将圆面x 2 +y 2 ≤4分成若干块.现在用5种不同的颜色给这若干块涂色,每块只涂一种颜色,且任意两
- 8沃利斯圆周率计算公式!如题.PS:德尼·盖之的[[鹦鹉的定理]]一书里沃利斯圆周率计算公式公式(P387)是否有错误?感
- 9执行力 读后感大伙帮帮忙咯,执行力读后感该如何去写啊,应急
- 10《小石潭记》《醉翁亭记》《鱼我所欲也》《湖心亭看雪》中的难题
- 11动能 势能 机械能 之间的关系?当.时,机械能不变 当.时,机械能增大 当.时,机械能减小
- 12Hello! _______ my parents.
- 13关于能源和能量,下列说法错误的是( ) A.地球上煤、石油、天然气等能源都来自太阳能 B.自然界的能量是守恒的,地球上
- 14两地相距3000米,甲乙两人同时从两地出发,相向而行,甲每分钟行80米,乙每分钟行70米,有一只狗与甲同行,狗每分钟跑1
- 15近义词 浑然不觉- 敬畏- 诧异-
