(2014•夏津县模拟)阅读材料,回答问题.
 cgf132022-10-04 11:39:541条回答
cgf132022-10-04 11:39:541条回答材料一今年2月我市一家歌厅发生火灾,事故的原因是电线起火,引燃了聚氨酯泡沫塑料天花板,造成了一定的财产损失.
材料二氢氧化铝Al(OH)3是一种白色粉末、无臭无味,不溶于水和乙醇.是一种一种无机阻燃剂.当温度达到250℃时,氢氧化铝开始分解出水蒸气和耐高温的氧化铝固体颗粒.利用氢氧化铝的这一性质,将它添加在塑料等易燃材料中起到阻燃作用.
(1)请列举出氢氧化铝的物理性质______.
(2)起火的电线在火灾中起到的作用是______ (填字母).
A.提供可燃物B.使可燃物达到着火点 C.提供氧气
(3)根据灭火原理分析氢氧化铝作阻燃剂的原因______ (答一点);氢氧化铝分解的化学方程式为
| ||
| ||

已提交,审核后显示!提交回复
共1条回复
 luckzh 共回答了19个问题
luckzh 共回答了19个问题 |采纳率78.9%- 解题思路:不需要通过化学变化表现出来的性质属于物质的物理性质;
物质燃烧必需的条件之一是温度要达到可燃物的着火点;
灭火的方法有:(1)与空气(或氧气)隔绝.(2)降温到可燃物的着火点以下.(3)撤走可燃物.(1)氢氧化铝的颜色、状态、气味、溶解性等性质不需要通过化学变化表现出来,属于氢氧化铝的物理性质.
故填:白色粉末,无臭无味,不溶于水和乙醇.
(2)电线燃烧时放出热量,使温度升高,从而达到了聚氨酯泡沫塑料的着火点,聚氨酯泡沫塑料燃烧起来,酿成火灾.起火的电线在火灾中起到的作用是使可燃物达到着火点.
故填:B.
(3)氢氧化铝分解时吸收热量,可以降低温度;氢氧化铝分解出的固体颗粒氧化铝,能够附着在可燃物的表面,从而使可燃物与氧气隔绝.
故填:隔绝氧气.
氢氧化铝分解生成水和氧化铝,反应的化学方程式为:2Al(OH)3
△
.
3H2O↑+Al2O3.
故填:2Al(OH)3
△
.
3H2O↑+Al2O3.点评:
本题考点: 燃烧与燃烧的条件;灭火的原理和方法.
考点点评: 本题主要考查物质的性质、燃烧的条件和灭火的方法、化学方程式的书写等方面的知识,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”. - 1年前
相关推荐
- (2014•夏津县模拟)下列对于化学实验操作的叙述中,正确的是( )
(2014•夏津县模拟)下列对于化学实验操作的叙述中,正确的是( )
A.用胶头滴管滴加液体时,滴管下端紧贴试管内
B.将pH试纸浸入溶液中,测定溶液的pH
C.稀释浓硫酸时,把水慢慢注入盛浓硫酸的烧杯中并不断搅拌
D.点燃可燃性气体前,要检验气体的纯度 agoodmajia1年前1
agoodmajia1年前1 -
 飞翔亚洲之鹰 共回答了15个问题
飞翔亚洲之鹰 共回答了15个问题 |采纳率73.3%解题思路:A、根据胶头滴管的使用方法进行分析判断.
B、根据用pH试纸测定溶液pH的正确操作进行分析判断.
C、根据稀释浓硫酸的方法进行分析判断.
D、点燃可燃性气体时,应先验纯后点燃,防止气体不纯,引起爆炸.A、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故选项说法错误.
B、测定pH最简单的方法是使用pH试纸,测定时,用玻璃棒蘸取待测溶液,滴在试纸上,然后再与标准比色卡对照,便可测出溶液的pH;将pH试纸直接浸入待测液,会污染试剂,故选项说法错误.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;故选项说法错误.
D、为防止气体不纯,引起爆炸,点燃可燃性气体前,要先检验气体的纯度;故选项说法正确.
故选D.点评:
本题考点: 液体药品的取用;浓硫酸的性质及浓硫酸的稀释;溶液的酸碱度测定;氢气、一氧化碳、甲烷等可燃气体的验纯.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2014•夏津县模拟)请从H、Cl、O、Ca、C中选择适当元素,用化学符号和数字表示(各写一例):
(2014•夏津县模拟)请从H、Cl、O、Ca、C中选择适当元素,用化学符号和数字表示(各写一例):
(1)一种常用的溶剂______; (2)一种酸______;
(3)一种微溶于水的碱______; (4)一种盐______. lindcsy1年前1
lindcsy1年前1 -
 黄金桂 共回答了20个问题
黄金桂 共回答了20个问题 |采纳率75%解题思路:根据题中限定元素,利用物质的性质或组成特点,判断物质并写出物质的化学式.(1)一种常用的溶剂是水,化学式为:H2O;(2)一种酸盐酸,化学式为:HCl;
(3)一种微溶于水的碱是氢氧化钙,化学式为:Ca(OH)2;(4)一种盐是氯化钙,化学式为:CaCl2.
故答案为:(1)H2O;(2)HCl;
(3)Ca(OH)2;(4)CaCl2.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题主要考查化学式的表示方法以及酸碱盐的分类,难度较小.1年前查看全部
- (2014•夏津县模拟)碳是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.
(2014•夏津县模拟)碳是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.
①根据表中提供的信息,填写有关含碳物质的对应特性
②CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为______,若要检验1%甲酸水溶液是否显酸性,能选用的有______(填字母序号)物质用途 金刚石切割玻璃 石墨作电极 活性炭净水 对应特性 硬度大
a.无色酚酞溶液b.紫色石蕊溶液c.pH试纸
③化石燃料有煤、石油和天然气,它们都属于______(填“可再生”或“不可再生”)能源.天然气最主要成分是甲烷,完全燃烧生成二氧化碳和水,该燃烧反应的化学方程式为______.从下表数据分析,与煤相比,用天然气作燃料的优点是______.
1g物质完全燃烧 甲烷 碳 产生二氧化碳的质量/g 2.75 3.67 放出的热量/kJ 56 32  toardat1年前1
toardat1年前1 -
 658974 共回答了21个问题
658974 共回答了21个问题 |采纳率90.5%解题思路:①根据物质的性质和用途分析;
②根据方程式的书写及反应前后原子的个数不变分析;根据酸性物质与指示剂的关系选择;
③根据化石燃料形成的特点、甲烷和煤燃烧的特点、数据分析回答.①由于石墨具有导电性,可用作电极;由于活性炭有吸附性,可用于净水.
②CO2和H2在一定条件下可合成甲酸(HCOOH),反应的方程式是:CO2+H2
一定条件下
.
HCOOH,此反应中CO2与H2的分子个数比为1:1,若要检验1%甲酸水溶液是否显酸性,可选用紫色石蕊溶液、pH试纸检验.
③化石燃料有煤、石油和天然气,它们都属于不可再生;甲烷燃烧生成了二氧化碳和水,反应的方程式是:CH4+2O2
点燃
.
CO2+2H2O;由表中的数据可知,等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量小于煤,放出的热量高于煤.
答案:①导电性吸附性
②1:1bc
③不可再生CH4+2O2
点燃
.
CO2+2H2O
等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量小于煤,放出的热量高于煤.点评:
本题考点: 碳单质的物理性质及用途;酸的化学性质;书写化学方程式、文字表达式、电离方程式;常用燃料的使用与其对环境的影响;常见能源的种类、能源的分类.
考点点评: 本题属于信息题,考查了有关二氧化碳、碳酸钙等的性质和用途,难度不大,依据已有的知识结合题目的信息分析即可.1年前查看全部
- (2014•夏津县模拟)下列五种物质中均含有氮元素,它们按下列顺序排列:①NH3 ②N2 ③NO&
(2014•夏津县模拟)下列五种物质中均含有氮元素,它们按下列顺序排列:①NH3②N2 ③NO ④X⑤HNO3根据这种排列规律,X可能是( )
A.N2O
B.NO2或NaNO2
C.N2O5
D.NaNO3 xx江1年前1
xx江1年前1 -
 有多少爱可已乱来 共回答了16个问题
有多少爱可已乱来 共回答了16个问题 |采纳率87.5%解题思路:根据在化合物中正负化合价代数和为零,分别计算各物质中氮元素的化合价,得出化合价的排列规律,进行分析解答即可.根据化合价的原则(在化合物中正、负化合价的代数和为零),已知氢元素的化合价为+1价,氧元素的化合价为-2价,则:①NH3中氮元素的化合价为-3价;②N2单质中氮元素的化合价为0;③NO中氮元素的化合价为+2价;⑤HNO3中氮元素的化合价为+5价.则氮元素的化合价是按照从低到高的顺序排列的,X中氮元素的化合价为在+2到+5之间.
A、N2O中氮元素的化合价为:+1价,不符合要求.
B、NO2中氮元素的化合价为:+4价,符合要求;NaNO2中氮元素的化合价为:+3价,符合要求.
C、N2O5中氮元素的化合价为:+5价,不符合要求.
D、NaNO3中氮元素的化合价为:+5价,不符合要求.
故选:B.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,考查学生灵活应用元素化合价的规律进行分析解题的能力.1年前查看全部
- (2014•夏津县模拟)某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
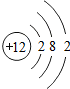 (2014•夏津县模拟)某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
(2014•夏津县模拟)某粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
A.在化学反应中易得2个电子
B.该粒子是镁原子
C.原子核内有12个质子
D.该粒子属于金属元素 musicws1年前1
musicws1年前1 -
 zla2787 共回答了13个问题
zla2787 共回答了13个问题 |采纳率100%解题思路:因为粒子种类与粒子结构间的关系是:阳离子的核内质子数>核外电子数;阴离子的核内质子数<核外电子数;原子的核内质子数=核外电子数.所以可知该粒子为镁原子.A、该元素的原子最外层上有2个电子,易失去2个电子达到稳定结构,说法错误.
B、该粒子核内质子数等于核外电子数,都为12,为镁原子,B说法正确;
C、该元素核内质子数为12,正确;
D、该元素的原子最外层上有2个电子,为金属元素,故D正确;
故选A.点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 本题主要考查原子结构示意图的意义、掌握核内质子数和核外电子数的关系,学会区别阳离子、阴离子、原子的微粒的电子层排布特点.1年前查看全部
- (2014•夏津县模拟)如图是甲、乙、丙三种固体物质的溶解度曲线,请你结合所给曲线,判断下列说法正确的是( )
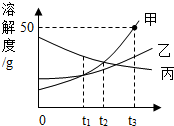 (2014•夏津县模拟)如图是甲、乙、丙三种固体物质的溶解度曲线,请你结合所给曲线,判断下列说法正确的是( )
(2014•夏津县模拟)如图是甲、乙、丙三种固体物质的溶解度曲线,请你结合所给曲线,判断下列说法正确的是( )
A.在t3℃时,甲与丙的溶解度相等
B.t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为1:2:3
C.t1℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是丙>甲>乙
D.温度降低到t2℃时,甲、乙的溶解度相等,得到甲的饱和溶液 gy4291年前1
gy4291年前1 -
 yuhao5 共回答了19个问题
yuhao5 共回答了19个问题 |采纳率78.9%解题思路:A、根据曲线中交点的含义考虑;B、根据t3℃时,甲物质的溶解度考虑;C、根据饱和溶液溶质质量分数=[溶解度/100g+溶解度]×100%;D、根据温度降低到t2℃时溶解度的变化考虑.A、曲线中交点表示该温度时两种物质的溶解度相等,t3℃时甲的溶解度大于乙的溶解度,故A错;
B、根据t3℃时,甲物质的溶解度是50g,即该温度下100g水中最多溶解50g甲物质,所以溶质是50g,溶剂是100g,溶液质量为150g,溶质、溶剂、溶液的质量之比为1:2:3,故B正确;
C、根据饱和溶液溶质质量分数=[溶解度/100g+溶解度]×100%,t1℃时,甲、乙、丙的溶解度大小是:丙>甲=乙,所以溶质质量分数的大小关系是:丙>甲=乙,故C错;
D、温度降低到t2℃时甲的溶解度大于乙的溶解度,故D错.
故选B.点评:
本题考点: 固体溶解度曲线及其作用;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 解答本题关键是要知道溶解度曲线中交点表示的意义,知道溶解度的四要素,饱和溶液溶质质量分数的计算方法.1年前查看全部
- (2014•夏津县模拟)实验室部分仪器或装置如图所示,请回答下列问题.
(2014•夏津县模拟)实验室部分仪器或装置如图所示,请回答下列问题.
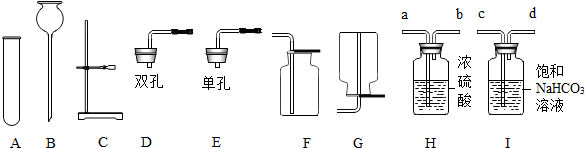
(1)实验室常用石灰石和稀盐酸制取二氧化碳气体,发生装置可选择图中的______(填仪器字母)进行组装,反应的化学方程式为______.
(2)在制取过程中,小雨同学选用F装置收集二氧化碳,并用燃着的小木条放在瓶口验证二氧化碳是否收集满,结果发现小木条始终不灭,说明该瓶______.出现上述情况的原因可能是:①______,②______.
(3)采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气.为获得纯净、干燥的二氧化碳气体,可选用如图所示的H装置和I装置进行除杂和干燥,导管口连接的正确顺序是:气体→______→F. 小木的海洋1年前1
小木的海洋1年前1 -
 阿吱猫 共回答了22个问题
阿吱猫 共回答了22个问题 |采纳率86.4%解题思路:(1)实验室制二氧化碳属于固液常温型,据此选择仪器;要根据反应物、产物以及反应条件来书写化学方程式,且书写要规范;
(2)根据实验注意事项进行解答;
(3)利用该装置净化气体时,导气管要长进短出,除水干燥放在最后一步.(1)实验室制二氧化碳属于固液常温型,所以发生装置所用仪器有锥形瓶、长颈漏斗、双孔胶塞;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳.
(2)在制取过程中,选用F装置收集二氧化碳,因为二氧化碳不燃烧也不支持燃烧,所以并用燃着的小木条放在瓶口验证二氧化碳是否收集满,结果发现小木条始终不灭,说明该瓶气体没有集满.出现上述情况的原因可能是装置漏气、药品量不足(稀盐酸或石灰石不足)、长颈漏斗下端管口未伸入液面下等;
(3)稀盐酸具有挥发性,因此制得的二氧化碳气体中会含有氯化氢气体和水蒸气,利用饱和的碳酸氢钠溶液可除去氯化氢气体,浓硫酸具有吸水性,可吸收水蒸气,对气体进行干燥.利用该装置净化气体时,导气管要长进短出,除水干燥放在最后一步.
故答案为:(1)ABCD;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)没有收集满;装置漏气;药品量不足(稀盐酸或石灰石不足);(3)cdab.点评:
本题考点: 二氧化碳的实验室制法;气体的净化(除杂);书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查的知识点较多,包括气体的制取、气体的净化、实验装置的气密性检查以及化学方程式的书写,要求学生要将这部分知识熟练掌握.1年前查看全部
大家在问
- 1一根长3.4米的绳子,分成4段;前3段每段长度相等,第4段比前3段中的每一段都长0.2米,第4段长多少米
- 2酚酞的化学本质是什么?可不可以常期暴露在空气中?
- 3对括号部分提问 My aunt invites me (to play tennis with her son) .__
- 4(5005•潍坊模拟)中图所示,真空中A、B两点固定两个等量正电荷,一个具有初速度的带负电的粒子仅在这两个电荷的作用下,
- 5若向量a与b不共线,向量a乘以b不等于0,且向量c=a-((a*a)/(a*b))*b,则向量a与c夹角为?
- 6《哨卡》在第2、3自然段分别用横线和波浪线画出具体描写"路太险""天太坏"的句子.
- 7角的定义是什么
- 8关于“木炭在氧气中燃烧是什么变化”提出问题
- 9写出下面各词的近义词、反义词 近义词:得意( ) 反义词:得意( ) 果然( ) 称赞( )
- 10A 化学反应所吸收或放出的热量与参加反应的物质的量成正比 B 热化学方程式未注明温度和压强时《的儿特》H表示标准状况下的
- 11高中物理选择题 关于机械能的长为l的均匀链条平放在光滑水平桌面上,使其长度的1∕4垂在桌边,松手后链条由静止开始由桌边下
- 12方程就是含有未知数的式子.______.
- 13物理题某人从A地到达B地,前1/3的路程中速度为5m/s,后2/3的路程中速度为4m/s求此人在这段路程的平均速度.
- 14怎样写我最爱的城市 英语作文6 句以上
- 15楚人有习操舟者的习和操是什么意思
