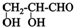1.在用丙炔合成 阿尔法-甲基丙烯酸甲酯:
 sagly19832022-10-04 11:39:541条回答
sagly19832022-10-04 11:39:541条回答H2C=C-COOCH3
|
CH3
欲使原子利用率达到最高,在催化剂下还需要的反应物是
A CO和CH3OH B CO2和H2O C H2和CO
请问,为什么不能选C
2.为什么加活泼金属能促进水的电离
3."电离程度大于水解程度,溶液一定呈酸性",这个说法对吗?
4.A B两元素的原子分别达到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量 若ABCD间分别形成化合物时,属于离子化合物可能性最大的是
A D2A B.C2B C.C2A D.D2B
5.氯化钠溶液中可能混有早知氢氧化钠 碳酸氢钠 碳酸钠中的一种或两种,为测定溶液中混有的杂质成分 可进行如下实验操作:分别取两分等体积混合液,用盐酸的标准液(0.10mol/L)滴定,以酚酞或甲基橙为指示剂,达到重点时消耗的盐酸的体积分别为V1 V2,且V2大于2V1大于0,则氯化钠溶液中混有的杂质可能为
A 氢氧化钠 B 碳酸钠 C 碳酸钠和碳酸氢钠 D 氢氧化钠和碳酸钠
6.某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物 当参加反应的单质与被还原的硝酸的物质的量之比为2:1时,还原产物是
A NO2 B NO C N2O D N2
7.用缩聚反应制取高分子化合物 …CH2-苯环-CH2-N-CH2-苯环-CH2-N…
| |
苯环 苯环
所用的单体中不需要的是
A 苯环-NH2 B CH3OH C 苯酚 D HCHO
8.制备氢氧化铁胶体,向盛有沸水的烧杯中滴加三氯化铁饱和溶液并长时间煮沸.
请问,为什么要长时间煮沸?
9.38.4mg铜与适量的农硝酸反应 铜完全反应后 共收集到0.1mol气体 那么反应消耗的HNO3的物质的量可能是
2×10^(-3)mol,请问怎样算
10.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60mL B.45mL C.30mL D.15mL
第一题的甲基连在第二个C上 第7题的苯环连在N上

已提交,审核后显示!提交回复
共1条回复
 Gubiy 共回答了18个问题
Gubiy 共回答了18个问题 |采纳率100%- 1、CH3-C≡CH+CO+H2O→H2C=C(CH3)COOH
...H2C=C(CH3)COOH+CH3OH→H2C=C(CH3)-COOCH3 +H2O
总方程式:CH3-C≡CH+CO+H2O+CH3OH→H2C=C(CH3)-COOCH3 使原子利用率达到最高
2.为什么加活泼金属能促进水的电离
向水中加入活泼金属,由于与水电离出的H+ 直接作用,因而同样能促进水的电离.
3."电离程度大于水解程度,溶液一定呈酸性",这个说法对吗?
弱酸的酸式盐当其电离程度大于水解程度时,呈酸性,当电离程度小于水解程度时,则成碱性,即比较它电离出H+的能力和阴离子水解的程度了.如果阴离子的水解程度较大(如NaHCO3,NaHS,Na2HPO4),则溶液呈碱性;反过来,如果阴离子电离出H+的能力较强(如NaH2PO4,NaHSO3),则溶液呈酸性.
4.A B两元素的原子分别达到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量 若ABCD间分别形成化合物时,属于离子化合物可能性最大的是 C. C2A
A B两元素的原子分别达到2个电子形成稳定结构→A,B是非金属元素.A放出的能量大于B放出的能量→A比B活泼(活泼的非金属处于高能量状态,形成稳定状态放出的能量多)C D两元素的原子分别失去一个电子形成稳定结构→C,D是金属元素.D吸收的能量大于C吸收的能量→C比D活泼(活泼的金属处于高能量状态,形成稳定状态吸收的能量少)
所以ABCD间分别形成化合物时,属于离子化合物可能性最大的是C2A
5.氯化钠溶液中可能混有早知氢氧化钠 碳酸氢钠 碳酸钠中的一种或两种,为测定溶液中混有的杂质成分 可进行如下实验操作:分别取两分等体积混合液,用盐酸的标准液(0.10mol/L)滴定,且V2大于2V1大于0,则氯化钠溶液中混有的杂质可能为
A 氢氧化钠 B 碳酸钠 C 碳酸钠和碳酸氢钠 D 氢氧化钠和碳酸钠
用盐酸滴定碳酸钠,酚酞的变色范围为8.2~10.2,在这个范围内碳酸钠只被滴定到碳酸氢钠,再往下就无法判断是否滴定到氯化钠了,因为这两个阶段酚酞都是无色的,所以如果只要求停留在碳酸氢钠则滴定用酚酞,要求滴定至氯化钠则选择甲基橙作指示剂,甲基橙变色范围为3.1~4.4
1,如果含只含NaOH杂质,H++OH-=H2O,以酚酞或甲基橙为指示剂,达到重点时消耗的盐酸的体积分别为V1 V2,V1= V2
如果含只含Na2CO3杂质,以酚酞为指示剂,CO32-+H=HCO3-达到重点时消耗的盐酸的体积分别为V1,以甲基橙为指示剂,CO32-+2H+=H2O+CO2达到重点时消耗的盐酸的体积分别为 V2,2V1= V2
现在是V2大于2V1大于0,所以选择D 氢氧化钠和碳酸钠
6.某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物 当参加反应的单质与被还原的硝酸的物质的量之比为2:1时,还原产物是
A NO2 B NO C N2O D N2
首先明确:参加反应的单质与被还原硝酸的物质得量之比为2:1
,意味着2mol金属失去的电子都由1mol硝酸接受,N的化合价降低相应数量.
当金属离子是+1价时,2mol金属失去的电子是2mol,1mol硝酸接受的电子是2mol,1mol N 由+5价降低到+3价,产物为+3价N,可是题中没有.
当金属离子是+2价时,2mol金属失去的电子是4mol,1mol硝酸接受的电子是4mol,1mol N 由+5价降低到+1价,产物为+1价N,C符合题意.
当金属离子是+3价时,2mol金属失去的电子是6mol,1mol硝酸接受的电子是6mol,1mol N 由+5价降低到-1价,产物为-1价N,可是题中没有.
金属离子的化合价再高,N就是负价,不符合题意.
所以选C
7.用缩聚反应制取高分子化合物 …CH2-苯环-CH2-N-CH2-苯环-CH2-N…
| |
苯环 苯环
所用的单体中不需要的是
A 苯环-NH2 B CH3OH C 苯酚 D HCHO
这一题的高分子物质的结构式看不出来,况且缩聚反应高考考纲中已删除了 ,不要做了吧.
8.制备氢氧化铁胶体,向盛有沸水的烧杯中滴加三氯化铁饱和溶液并长时间煮沸.
不能长时间煮沸
氯化铁的水解反应本身是一个吸热反应,加热可以促使平衡向右移动,但是作为胶体的氢氧化铁是有一定的浓度限制的,如果浓度过大就会形成氢氧化铁沉淀,而且温度比较高的话胶体粒子之间碰撞的机会会增多,也不利于胶体的稳定性,所以煮沸的时间不能过长
9. 38.4mg铜与适量的农硝酸反应 铜完全反应后 共收集到0.1mol气体 那么反应消耗的HNO3的物质的量可能是
不考虑二氧化氮与四氧化氮的可逆反应,所以所得到的气体不是NO,就是NO2,因此,每mol被还原的HNO3都会产生1mol的气体.现在有22.4ml气体(STP下),所以被还原的HNO3的物质的量就是22.4/22.4/1000=0.001mol=1×10^(-3)mol.
Cu2+必然要结合NO3-以CU(NO3)2存在,消耗HNO3的物质的量为:2×(38.4mg/64/1000)=1.2×10^(-3)mol.反应消耗的HNO3的物质的量可能是2.2×10^(-3)mol
10.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60mL B.45mL C.30mL D.15mL
NO2、N2O4、NO 的混合气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸
{4NO2+O2+2H2O=4HNO3
{4NO+3O2+2H2O=4HNO3
{2N2O4+O2+2H2O=4HNO3
NO2、N2O4、NO的混合气体重新变回 硝酸
全部 O2--O2- 化合价升降守恒
既, Cu--Cu2+所升化合价= O2--O2- 所降化合价
如果你明白了这个.别的就好办了.
O2物质的量为0.075mol
所以 所得硝酸铜溶液中Cu2+ 为0.15mol Cu2+ + 2OH- = Cu(OH)2
消耗OH-为0.3mol 消耗NaOH溶液的体积是0.3mol除5mol/L=0.06L
既60ml - 1年前
相关推荐
- 1mol某气态烃能和2molHCl加成,其加成产物又可以被6molCL2完全取代,该烃可能为?为什么是丙炔,
 真龙行天下1年前1
真龙行天下1年前1 -
 eagle513 共回答了19个问题
eagle513 共回答了19个问题 |采纳率78.9%该烃能和2molHCl反应说明有两个不饱和度,可能有两个碳碳双键或者一个碳碳三键.能被6molCl2取代说明加成后该烃中有六个氢原子.丙炔和2molHCl加成的产物是CH3CCl2CH3,刚好有六个氢原子可以被6molCl2取代.1年前查看全部
- 按等物质的量混合的下列气体,碳元素的质量分数最大的是A甲烷和乙烯B乙炔和丙烯C乙烷和乙烯D丙炔和乙烯
按等物质的量混合的下列气体,碳元素的质量分数最大的是A甲烷和乙烯B乙炔和丙烯C乙烷和乙烯D丙炔和乙烯
请说明的详细一点,我个人认为B,D都对啊,因为如果是等物质的量的话碳,氢的物质的量都相等啊.为什么选B不选D呢 沈败衣1年前1
沈败衣1年前1 -
 彝族阿惹妞 共回答了13个问题
彝族阿惹妞 共回答了13个问题 |采纳率76.9%A一共CH4+C2H4=C3H8
B 一共C2H2+C3H6=C4H8
C 一共C2H6+C2H4=C4H10
D 一共C3H6+C2H4=C5H10
B=48/56=0.857
D=60/70=0.857
应该是BD吧1年前查看全部
- 由丙炔及必要的原料制备2-庚炔
 咖啡甜甜1年前1
咖啡甜甜1年前1 -
 漂亮女校花 共回答了14个问题
漂亮女校花 共回答了14个问题 |采纳率78.6%先在液氨中与钠反应生成炔钠,然后再与1-溴丁烷反应脱去溴化钠,即得到目标产物1年前查看全部
- 丙炔是C3H4,我们背的儿歌是“二三铁二四碳”,这里一个分子的三个碳原子怎么弄出来-4价?
 nichtsundleer1年前2
nichtsundleer1年前2 -
 xnjdfz 共回答了21个问题
xnjdfz 共回答了21个问题 |采纳率90.5%丙炔是有机物,而二个是描述的无机物中的价态.无机物与有机物是不同的结构,不能混为一谈.1年前查看全部
- 5-炔丙基-1,3-环己二烯 可以叫做 B-(1,4-环己二烯)丙炔
 wangcy981年前1
wangcy981年前1 -
 140516 共回答了21个问题
140516 共回答了21个问题 |采纳率95.2%理论上可以,但是实际上一般在取代基过大的情况下会把官能团作为取代基1年前查看全部
- 有8种物质:①甲烷 ②乙烯 ③苯 ④聚乙烯 ⑤丙炔 ⑥环己烷 ⑦邻二甲苯 ⑧环己烯(),其中既能使酸性KMnO4溶液褪色
有8种物质:①甲烷 ②乙烯 ③苯 ④聚乙烯 ⑤丙炔 ⑥环己烷 ⑦邻二甲苯 ⑧环己烯(
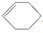 ),其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
),其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
A.②④⑤⑧
B.②⑤⑧
C.②④⑤⑦
D.②④⑤⑦⑧ 11_yao1年前1
11_yao1年前1 -
 残云之剑 共回答了16个问题
残云之剑 共回答了16个问题 |采纳率81.3%解题思路:题给物质中,能与溴水反应的应含有碳碳双键官能团;与酸性高锰酸钾发生反应,应具有还原性,含有碳碳双键,碳碳三键或为苯的同系物等,以此解答.既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的物质应含有不饱和键,可发生加成、氧化反应,题中②⑤⑧符合,
而①③④⑥与溴水、酸性高锰酸钾都不反应;
⑦只与酸性高锰酸钾发生反应,
故选B.点评:
本题考点: 有机化学反应的综合应用.
考点点评: 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物官能团的性质以及反应类型的判断,难度不大.1年前查看全部
- 为什么丙炔和HCl加成生成的是2-氯丙烷而不是1-氯丙烷
 猫眼女王1年前1
猫眼女王1年前1 -
 gxnn113 共回答了21个问题
gxnn113 共回答了21个问题 |采纳率95.2%是丙烯和HCl加成生成的是2-氯丙烷,这是主要产物,也有1-氯丙烷生成,不是主要产物不写在反应方程式中,丙炔和HCl加成生成的是2,2-二氯丙烷.反应符合马氏规则,不对称的烯烃和炔烃与不对称的试剂发生加成反应时,试剂中的负性基团加到双键或三键中不含氢或含氢较少的碳原子上,或者说试剂中的氢原子加到双键或三键中含氢多的碳原子上.也可以从反应机理上解释,或者从烷基是斥电子基团解释.1年前查看全部
- 怎么鉴别丙炔,丙烯,环丙烷,丙烷,丙醇,苯酚?
 蓝狐_bluefox1年前1
蓝狐_bluefox1年前1 -
 seajiro 共回答了16个问题
seajiro 共回答了16个问题 |采纳率93.8%首先用硝酸二氨合银鉴别出丙炔.
然后用三氯化铁溶液鉴别出苯酚.
再用金属钠鉴别出丙醇.
剩余三者,丙烯既可使溴/四氯化碳褪色也可使酸性高锰酸钾褪色,环丙烷只能与溴/四氯化碳发生褪色反应,丙烷则二者均不能褪色.1年前查看全部
- 由丙炔合成反—2己烯
 云慕烟1年前1
云慕烟1年前1 -
 月明265 共回答了17个问题
月明265 共回答了17个问题 |采纳率94.1%加入钠,变成炔钠,再与1-氯丙烷反应,最后用钠和液氨反式加氢.1年前查看全部
- 鉴别丙炔,丙稀,环丙烷,溴丙烷,丙醇
 zflsy1年前1
zflsy1年前1 -
 bh0729ghj 共回答了12个问题
bh0729ghj 共回答了12个问题 |采纳率83.3%编号ABCDE的话 AB 前两者均可使溴的四氯化碳褪色 后者更难 且后者燃烧时黑烟更浓 CDE可直接用水 CD均不溶 C在上层 D在下层 E应该溶解1年前查看全部
- 下列说法正确的是( )A.丙炔中所有原子一定位于一条直线上B.甘油醛分子()中一定存在对映异构现象C.某烯烃的衍生物(
下列说法正确的是( )
A.丙炔中所有原子一定位于一条直线上
B.甘油醛分子(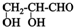 )中一定存在对映异构现象
)中一定存在对映异构现象
C.某烯烃的衍生物(分子式为C2H2Cl2)中一定存在顺反异构现象
D.1-丁烯中所有碳原子一定位于同一平面上 yinong45931年前1
yinong45931年前1 -
 超强力的胶水 共回答了20个问题
超强力的胶水 共回答了20个问题 |采纳率85%1年前查看全部
- 下列各组物质互为同素异形体的是( ) A.乙炔和丙炔 B. 3 7 Li和 3 6 Li C.金刚石和石墨 D.正丁烷
下列各组物质互为同素异形体的是( ) A.乙炔和丙炔 B. 3 7 Li和 3 6 Li C.金刚石和石墨 D.正丁烷和2-甲基丙烷  lbaichil1年前1
lbaichil1年前1 -
 只爱塞北 共回答了14个问题
只爱塞北 共回答了14个问题 |采纳率92.9%A.乙炔和丙炔都是化合物,不属于同素异形体,是同系物,故A错误;
B. 3 7 Li和 3 6 Li都是原子,不属于同素异形体,是同位素,故B错误;
C.金刚石和石墨都是由碳元素组成的不同单质,属于同素异形体,故C正确;
D.正丁烷和2-甲基丙烷都是化合物,不属于同素异形体,是同分异构体,故D错误;
故选:C.1年前查看全部
- 如何鉴别下列有机物?1、甲酸 乙酸 苯甲酸 2、丙烯 丙炔 环丙烷 3、丙酮 丙醇 丙醛4、乙醛 丙醛 丙烯醛
 宝猪宝猪1年前1
宝猪宝猪1年前1 -
 撕烤的驴 共回答了17个问题
撕烤的驴 共回答了17个问题 |采纳率94.1%1.加水(苯甲酸微溶,其余易溶,可鉴定出苯甲酸);加高锰酸钾,甲酸被氧化生成气体(CO2),溶液颜色有变化,乙酸无现象不反应.
2.加高锰酸钾,环丙烷中无现象,可鉴定出,其余二者颜色褪去;再加二氨合银溶液,丙炔中生成白色沉淀(炔化银),乙烯不反应.
3.加高锰酸钾,丙酮中无现象,可鉴定出,其余二者颜色褪去;加入银氨溶液,发生银镜反应的为丙醛;剩下的是丙醇.
4.使溴水褪色的是丙烯醛;加碘单质和氢氧化钾,发生碘仿反应的是乙醛,剩下的是丙醛.1年前查看全部
- 丙酸,丙烯,丙炔,溴乙烷
 ff453ad4730803fa1年前3
ff453ad4730803fa1年前3 -
 狮子骢 共回答了14个问题
狮子骢 共回答了14个问题 |采纳率100%丙酸CH3CH2COOH,丙烯CH3CH=CH2,丙炔CH3C≡CH,溴乙烷CH3CH2B1年前查看全部
- 丙炔与一分子溴化氢反应制2-溴丙烯
丙炔与一分子溴化氢反应制2-溴丙烯
为什么用HgBr2
作催化剂 路过de人1年前1
路过de人1年前1 -
 zcylyl 共回答了19个问题
zcylyl 共回答了19个问题 |采纳率73.7%CHC-CH3+HBR=BRCH=CH-CH31年前查看全部
- 丙炔钠在液氨条件下与二溴乙烷反应
 jie_jiang1年前1
jie_jiang1年前1 -
 rrkl 共回答了20个问题
rrkl 共回答了20个问题 |采纳率85%丙炔钠和1,2-二氯乙烷的物质的量为一比一,主要是5-氯-戊-2-炔.
丙炔钠和1,2-二氯乙烷的物质的量为一比二,主要是辛-2,6-二炔.1年前查看全部
- 某气态烷烃与丙炔混合气体升标况,完全燃烧后生成121克二氧化碳和40.5克水,则原混合气体中烷烃为:
某气态烷烃与丙炔混合气体升标况,完全燃烧后生成121克二氧化碳和40.5克水,则原混合气体中烷烃为:
A:甲烷B:乙烷C:丙烷D:丁烷 pbaddh1年前1
pbaddh1年前1 -
 刚则 共回答了19个问题
刚则 共回答了19个问题 |采纳率94.7%以现有条件判断结果是B乙烷:
根据生成的CO2和H2O,求出对应的C、H原子的物质的量分别是2.75mol、4.5mol
由此可确定一个该混合气体的分子式:C2.75H4.5
其含义是1个分子平均含碳2.75个,含氢4.5个
已知丙炔C3H4,根据平均值是处在组成成分的中间的,所以考虑C、H两方面,只有乙烷合理:C2H6
另外问楼主,“升标况”是什么意思,还有条件没给出吗?1年前查看全部
- 1mol某气态烃能和2molHCl加成,其加成产物又可以被6molCL2完全取代,该烃可能为?为什么是丙炔,
1mol某气态烃能和2molHCl加成,其加成产物又可以被6molCL2完全取代,该烃可能为?为什么是丙炔,
1mol某气态烃能和2molHCl加成,其加成产物分子上的氢原子又可以被6molCL2完全取代,该烃可能为?为什么是丙炔?
加成产物是C3H8CL2啊 为什么 8个H =12个CL?
错了。加成物是c3h6cl2 sdtgqergwerg1年前1
sdtgqergwerg1年前1 -
 拓拔_玉儿 共回答了15个问题
拓拔_玉儿 共回答了15个问题 |采纳率93.3%烃的反应可以用两个2molHCl来描述和不饱和度可以具有两个碳 - 碳双键或碳 - 碳三键.碳氢化合物可以是6molCl2氢原子具有六奖金替换指令后.此外丙炔和2molHCl产物是CH3CCl2CH3,还有只是6个氢原子可被取代6molCl2.1年前查看全部
- 用C3H4(丙炔)合成C5H8O2(2一甲基丙烯酸甲酯)过程中,.在催化剂作用下还需要其他的反应物是 ( )
用c3h4(丙炔)合成c5h8o2(2一甲基丙烯酸甲酯)过程中,.在催化剂作用下还需要其他的反应物是 ( )
“绿色化学”是当今***提出的——个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用c3h4(丙炔)合成c5h8o2(2一甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是 ( )
a.co和ch3oh b.co2和h2o h2和co d.ch3oh和h2 人生如梦0071年前2
人生如梦0071年前2 -
 石川01 共回答了22个问题
石川01 共回答了22个问题 |采纳率90.9%反应中原子全部转化为欲制得的产物,即原子的利用率为100%.
那我们就用
C5H8O2-C3H4=C2H4O2
选项中只有A C2H4O2=CO+CH3OH
所以选A1年前查看全部
- 25℃和101kPa时,甲烷、丙炔(C3H4)和丙烯组成的混合烃10mL与50mL氧气混合,完全燃烧后,除去水蒸气,恢复
25℃和101kPa时,甲烷、丙炔(C3H4)和丙烯组成的混合烃10mL与50mL氧气混合,完全燃烧后,除去水蒸气,恢复到原来的温度和压强,气体总体积为37.5mL,原混合烃中丙烯的体积分数为( )
A.50%
B.25%
C.75%
D.12.5% 黑金战甲1年前1
黑金战甲1年前1 -
 raining1981123 共回答了13个问题
raining1981123 共回答了13个问题 |采纳率84.6%解题思路:发生反应有:CH4+2O2=CO2+2H2O,C3H4+4O2=3CO2+2H2O,C3H6+[9/2]O2=3CO2+3H2O,除去水蒸气,恢复到原来的温度和压强,根据反应方程式可知,CH4和丙炔(C3H4)反应后体积缩小的量是相同的,故可将两者看成是一种物质,设丙炔(C3H4)一共为xmL,C3H6为ymL,利用气体体积缩小了(10+50-37.5)mL=22.5mL及混合气体的体积来列等式计算出丙烯的体积,进而计算丙烯的体积分数.除去水蒸气,恢复到原来的温度和压强,则:
CH4+2O2=CO2+2H2O△V
121 2
C3H4+4O2=3CO2+2H2O△V
1432
C3H6+[9/2]O2=3CO2+3H2O△V
14.53 2.5
CH4和C3H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,
设CH4和C3H4一共为xmL,C3H6为ymL,
则:总体积为:①x+y=10,气体体积减小为:②2x+2.5y=(10+50-37.5)mL=22.5mL
根据①②解得:x=5,y=5,
则原混合烃中丙烯的体积分数为:[5mL/10mL]×100%=50%,
故选A.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题考查混合物计算、化学方程式有关计算,题目难度中等,解答关键是根据方程式判断体积变化,把甲烷与丙炔看作一个组分,从而转化为两组分混合,注意差量法的应用.1年前查看全部
- 丙炔同分异构简式和名称
 yy1年前2
yy1年前2 -
 都说给自己听 共回答了15个问题
都说给自己听 共回答了15个问题 |采纳率80%CH2=C=CH2丙二烯1年前查看全部
- 在“绿色化学工艺”中,最好是反应物中原子全部转化为欲制得的产物,即原子的利用率为100%.在用C3H4(丙炔)合成C5H
在“绿色化学工艺”中,最好是反应物中原子全部转化为欲制得的产物,即原子的利用率为100%.在用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
A. CO和CH3OH
B. CO2和H2O
C. H2和CO
D. CH3OH和H2 卢部尚书1年前1
卢部尚书1年前1 -
 yulin9916 共回答了20个问题
yulin9916 共回答了20个问题 |采纳率85%解题思路:根据“绿色化学工艺”的特征:反应物中原子全部转化为欲制得的产物,即原子的利用率为100%;即生成物质只有一种,由原子守恒推测反应物的种类.用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯),要把一个C3H4分子变成一个C5H8O2分子,还必须增加2个C原子、4个H原子、2个O原子,即原料中另外的物质中C、H、O的原子个数比为1:2:1.
A、CO和CH3OH,两种物质如果按照分子个数比1:1组合,则C、H、O的原子个数比为1:2:1,故选项正确.
B、CO2和H2O,两种物质分子里三种原子不论怎样组合也都不能使C、H、O的原子个数比为1:2:1,故选项错误.
C、H2和CO,两种物质如果按照分子个数比1:1组合,则C、H、O的原子个数为1:2:1,故选项正确.
D、CH3OH和H2,两种物质分子里三种原子不论怎样组合都不能使C、H、O的原子个数比为1:2:1,故选项错误.
故选AC.点评:
本题考点: 绿色化学.
考点点评: 本题难度较大,考查同学们新信息获取、处理及结合所学知识灵活运用所学知识进行解题的能力,抓住一个主要信息(“绿色化学工艺”中反应物中原子全部转化为欲制得的产物,即原子的利用率为100%)是解答本题的关键.1年前查看全部
- 丙醇制丙炔的反应过程?
 qycxc1年前4
qycxc1年前4 -
 或许有一天 共回答了29个问题
或许有一天 共回答了29个问题 |采纳率96.6%CH3-CH2-CH2OH =(热分解) CH3-CH=CH2 + H2O
CH3-CH=CH2 =(热分解) CH3-C = CH + H21年前查看全部
- 请问丙炔和丙烯的电子式怎么写?RT
 stef_ren1年前4
stef_ren1年前4 -
 aok8834 共回答了17个问题
aok8834 共回答了17个问题 |采纳率88.2%我把电子式做成图片形式,这两种物质的电子结构式表示如下图:http://photo.baixun.com/image.php?album=12384&owner=jsflyang&imgname=1209776178.jpg1年前查看全部
- 实验室如何制丙炔
 17017411年前1
17017411年前1 -
 重临人间 共回答了25个问题
重临人间 共回答了25个问题 |采纳率92%借鉴乙烯的制法来制丙醇,乙烯是用乙醇和浓硫酸加热170°C来制的,那丙烯就用丙醇和浓硫酸加热170°C来制.1年前查看全部
- 丙炔与丙炔发生复分解的方程试
 zhuyulk1年前1
zhuyulk1年前1 -
 J小爱 共回答了17个问题
J小爱 共回答了17个问题 |采纳率88.2%2CH3C三CH---->CH3C三CCH3+CH三CH1年前查看全部
- 丙炔双阴离子共振结构丙炔双阴离子[CCCH2]2-,有两种共振结构,哪种贡献更大?为什么?在线等,谢谢!
 岚昕1年前1
岚昕1年前1 -
 秋之希冀 共回答了15个问题
秋之希冀 共回答了15个问题 |采纳率100%丙炔双阴离子[CCCH2]2-,
-C≡C—C- H2 ① ↔HC-=C=C-H ②
我觉得应该是①贡献大.
①可以看做1个烯与一个原子的孤对电子形成p-π共轭,炔的那一端的负电荷比较稳定(电负性强),共轭也比较稳定,应该比②要稳定性好.②的两个负电荷形成的孤对电子不能参与共轭.稳定性差.1年前查看全部
- 由丙炔制丙醇的反应式,可以选用必要的无机试剂.
由丙炔制丙醇的反应式,可以选用必要的无机试剂.
请速速回答,能不能把有关的方程式写上. 王二ii1年前2
王二ii1年前2 -
 万雪蝶儿 共回答了24个问题
万雪蝶儿 共回答了24个问题 |采纳率87.5%氢卤酸,碱的水溶液,氢气1年前查看全部
- 求3-叠氮-丙炔的沸点?用丙炔溴合成丙炔叠氮时 想知道丙炔叠氮的沸点 好分离产品
 胡骁1年前1
胡骁1年前1 -
 手毛很长 共回答了14个问题
手毛很长 共回答了14个问题 |采纳率85.7%丙炔叠氮的沸点确实查不到,但是你要分离产品,他的沸点肯定比丙炔溴要高. 查看原帖1年前查看全部
- 丙醇如何转化为丙炔
 mengxiang8271年前1
mengxiang8271年前1 -
 011222shmily 共回答了14个问题
011222shmily 共回答了14个问题 |采纳率92.9%先用浓HCl溶液与其反应生成氯丙烷
然后用浓NaOH醇溶液脱一分子HCl生成丙烯
然后加Cl2生成1,2-二氯丙烷
然后用浓NaOH醇溶液脱去2分子HCl生成丙炔1年前查看全部
- 丙炔制丙烯方程式
 limshi1年前1
limshi1年前1 -
 sdly911 共回答了19个问题
sdly911 共回答了19个问题 |采纳率100%CH3-C三CH + H2 === CH3CH=CH2
催化剂是Pd和BaSO4的混合物(LINDLAR催化剂)1年前查看全部
- 1L的乙炔和丙炔C含量哪个高
 心中的牧歌1年前3
心中的牧歌1年前3 -
 指间舞蹈 共回答了19个问题
指间舞蹈 共回答了19个问题 |采纳率94.7%1楼:丙炔沸点: -23.3℃ 怎么可能是液态呢
均是气态,故同体积含的乙炔和丙炔的分子数是一致的
乙炔碳的含量是:92.3%
丙炔碳的含量是:90%
很明显乙炔的C含量高1年前查看全部
- 有机物不是碳原子越多熔沸点越高么,密度越大么?那为什么乙炔熔点高于丙炔?
有机物不是碳原子越多熔沸点越高么,密度越大么?那为什么乙炔熔点高于丙炔?
还有是不是不管什么有机物,式量越大熔沸点越高,密度越大?密度和熔沸点一致?
烷烃炔烃烯烃是不是密度都比水轻? aspringday1年前2
aspringday1年前2 -
 有鱼在岸 共回答了19个问题
有鱼在岸 共回答了19个问题 |采纳率100%有机物的熔点取决于分子间的“吸引力”,这种力一般碳原子越多越大,熔沸点越高.但是在极性比较强的分子之间还有电磁力,类似于静电梳子吸引头发,导致极性强的物质熔沸点高于依靠分子量外推的预期数值,乙炔高于丙炔就是如此.
总的来说,式量越大熔沸点越高,密度越大,密度和熔沸点趋势一致.
烷烃炔烃烯烃是不是密度都比水轻.1年前查看全部
- 用丙炔合成2-甲基丙烯酸甲酯欲使原子利用率最高
 huajiangwang1年前1
huajiangwang1年前1 -
 zg7517817 共回答了25个问题
zg7517817 共回答了25个问题 |采纳率92%CO+CH3OH1年前查看全部
- 丙炔和酸性高锰酸钾反应生成什么
 meimeizaixian1年前2
meimeizaixian1年前2 -
 范壶紫 共回答了17个问题
范壶紫 共回答了17个问题 |采纳率88.2%生成二氧化碳、乙酸和二价锰离子1年前查看全部
- 丙炔和氯化氢的加成方程式丙炔和溴水(1:1,1:2)丙炔和氯气(1:1,1:2)丙炔和氢气(1:1,1:2)丙炔和氯化氢
丙炔和氯化氢的加成方程式
丙炔和溴水(1:1,1:2)
丙炔和氯气(1:1,1:2)
丙炔和氢气(1:1,1:2)
丙炔和氯化氢1:1
丙炔和水1:1 轰炸机B521年前1
轰炸机B521年前1 -
 tjj2222 共回答了16个问题
tjj2222 共回答了16个问题 |采纳率93.8%丙炔和溴水(1:1,1:2)
C2H2+2Br2==CHBr2-CHBr2
丙炔和氯气(1:1,1:2)
C2H2+2Cl2==CHCl2-CHCl2
丙炔和氢气(1:1,1:2)
1:1 C2H2+H2== CH2=CH2
1:2 C2H2+2H2== CH3CH3
丙炔和氯化氢1:1
C2H2+HCl== CH2=CHCl
丙炔和水1:1
C2H2+H2O== CH2=CHOH1年前查看全部
- 乙炔与丙炔有转化关系吗
 lmc_5201年前2
lmc_5201年前2 -
 pennylan 共回答了19个问题
pennylan 共回答了19个问题 |采纳率84.2%乙炔与氨基钠反应生成乙炔钠,然后与碘甲烷发生亲核取代反应生成丙炔1年前查看全部
- 1.充分燃烧3L由甲烷、乙烯和丙炔组成的混合气体,生成6LCO2和4.82g水(气体体积均在标准状况下测定),则原混合气
1.充分燃烧3L由甲烷、乙烯和丙炔组成的混合气体,生成6LCO2和4.82g水(气体体积均在标准状况下测定),则原混合气体中甲烷、乙烯和丙炔的体积比可能是()
A1:1:1 B1:2:3 C3:2:1 D3:1:2
2.将烷烃和烯烃按体积比5:1混合,所得混合气体的体积是相同状况下等质量的H2体积的1/16,这该混合气体的组成是
A.甲烷,乙烯B,甲烷,丁烯C丙烷,丙烯D.乙烷,丙烯
第2题平均相对分子质量为什么是32啊? 阿jet1年前2
阿jet1年前2 -
 parttime 共回答了18个问题
parttime 共回答了18个问题 |采纳率88.9%1、选A
设平均化学式为CxHy,则由燃烧方程式:
CxHy+(x+y/4)O2→点燃→xCO2 + y/2H2O
1 x y/2*18
3L/22.4L/mol 6L/22.4L/mol 4.82g
X=2
Y=4
则平均分子式为C2H4
所以原混合气体中乙烯可以是任意体积,
由CH4、C3H4求两者的体积比:
CH4 1 1
2
C3H4 3 1 V(CH4):V(C3H4)=1:1
因此三者的体积比=1:1:1
2、选D
所得混合气体的体积是相同状况下等质量的H2体积的1/16,
则所得混合气体的密度是p是氢气密度的16倍,
根据相对密度D=p1/p2=M1/M2得
M混=16MH2=16*2=32g/mol
甲烷相对分子质量为16
乙烷相对分子质量为30
丙烷相对分子质量为44
乙烯相对分子质量为28
丙烯相对分子质量为42
丁烯相对分子质量为56
A甲烷,乙烯相对分子质量都小于32,不符合题意,
B,甲烷,丁烯平均相对分子质量=(5*16+1*56)/(5+1)=22.7不符合题意;
C丙烷,丙烯相对分子质量都大于32,不符合题意;
D.乙烷,丙烯平均相对分子质量=(5*30+1*42)/(5+1)=32,所以选D1年前查看全部
- 已知14克甲烷和丙炔的混合气体,在标准状况下的体积为11.2升,将其完全燃烧后的混合气体通过浓硫酸,浓...
已知14克甲烷和丙炔的混合气体,在标准状况下的体积为11.2升,将其完全燃烧后的混合气体通过浓硫酸,浓...
已知14克甲烷和丙炔的混合气体,在标准状况下的体积为11.2升,将其完全燃烧后的混合气体通过浓硫酸,浓硫酸增加的质量为多少?A.9g B.18g C.27g D.无法确定 大梦秋寒1年前1
大梦秋寒1年前1 -
 偶假牙 共回答了19个问题
偶假牙 共回答了19个问题 |采纳率89.5%甲烷分子量是16,丙炔是39.标况下11.2升即0.5mol.
设甲烷有xmol.
16x+39(0.5-x)=14,x=11/46,0.5-x=6/23.
一个甲烷有四个H,11/46mol的甲烷能产生11/23mol的水.
一个丙炔有四个H,6/23mol的丙炔能产生12/23mol的水.
浓硫酸吸的气体就是水.所以共23/23mol即1mol的水,所以是18g.选B.1年前查看全部
- 中转有机化学从乙炔或丙炔中选取适当原料及其他无机试剂合成下列化合物1.CH3CHO 2.CH3CH2CH2Br
 迷途小猫咪1年前1
迷途小猫咪1年前1 -
 coco_coco 共回答了22个问题
coco_coco 共回答了22个问题 |采纳率81.8%C2H2 + H2O (催化剂:有硫酸存在下硫酸汞做催化剂)->CH3CHO
CH3CCH + H2 (德林催化剂)->CH3CH=CH2 + HBr (在有光照或过氧化物存在下)->CH3CH2CH2B1年前查看全部
- 乙炔 丙炔 丁炔 这些炔类的结构式有没有什么通式或共同点呢
 may_12241年前2
may_12241年前2 -
 言言c 共回答了19个问题
言言c 共回答了19个问题 |采纳率94.7%有啊
炔烃 通式为:CnH2n-2
如
乙炔(C2H2)、丙炔(C3H4) 、 丁炔(C4H6) 等
炔烃为分子中含有碳碳三键的碳氢化合物的总称,其官能团为碳-碳三键(C≡C),是一种不饱合的碳氢化合物.1年前查看全部
- (1)丙炔的三C原子共面不,它上面的氢呢 (2)笨上连一个乙炔少个氢的键(C三个-CH)原子为何共面
 离人心上冬1年前1
离人心上冬1年前1 -
 gangyu2006 共回答了13个问题
gangyu2006 共回答了13个问题 |采纳率100%丙炔的三个碳原子和氢共面1年前查看全部
- 丙炔如何合成2-己烯
 1z1z1z1年前2
1z1z1z1年前2 -
 kju2c 共回答了17个问题
kju2c 共回答了17个问题 |采纳率94.1%乙炔在液氨和氨钠的条件下生成乙炔钠.然后再用3个C的一卤代烃 和一卤代甲烷反应制得2-己傕 再用Lindlar试剂加成就行了.1年前查看全部
- 有1.3丁二烯和氢气,丙炔,总体体积为5升其中氢气和丙炔在混合气体中的体积分别为X和Y 反应后体积为V升 画出X=0.1
有1.3丁二烯和氢气,丙炔,总体体积为5升其中氢气和丙炔在混合气体中的体积分别为X和Y 反应后体积为V升 画出X=0.15是,V随变化的曲线
当Y=0.2时,V随X变化的曲线 jindianii1年前0
jindianii1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 丙炔与溴的四氯化碳溶液反应的化学方程式
 inforknow_com1年前3
inforknow_com1年前3 -
 流浪和尚 共回答了21个问题
流浪和尚 共回答了21个问题 |采纳率90.5%H2C=CH2+Br2=BrH2C-CH2B1年前查看全部
- 下列说法正确的是( )A.丙炔分子中三个碳原子不可能位于同一直线上B.乙炔分子中碳碳间的三个共价键性质完全相同C.分子
下列说法正确的是( )
A.丙炔分子中三个碳原子不可能位于同一直线上
B.乙炔分子中碳碳间的三个共价键性质完全相同
C.分子组成符合CnH2n-2的链烃一定是炔烃
D.在所有符合通式CnH2n-2炔烃中,乙炔所含氢的质量分数最小 eagle_dx121年前1
eagle_dx121年前1 -
 夏望繁星 共回答了11个问题
夏望繁星 共回答了11个问题 |采纳率90.9%解题思路:A、丙炔中存在C≡C三键直线结构,甲基中的C原子处于乙炔中H原子位置;
B、乙炔分子中碳碳间的三个共价键,有1个σ键、2个π键,其中σ键稳定、π键不稳定;
C、分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,或1个C≡C三键;
D、根据组成通式,计算1个C原子结合的H原子平均数目,H原子数目越大,氢的质量分数越大,据此判断.A、丙炔中存在C≡C三键直线结构,甲基中的C原子处于乙炔中H原子位置,三个C原子处于同一直线,故A错误;
B、乙炔分子中碳碳间的三个共价键,有1个σ键、2个π键,其中σ键稳定、π键不稳定,分子中碳碳间的三个共价键性质不相同,故B错误;
C、分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,为二烯烃,或1个C≡C三键,为炔烃,故C错误;
D、符合通式CnH2n-2炔烃中,1个C原子结合的H原子平均数目为(2-[2/n]),n值越大,(2-[2/n])越大,氢的质量分数越大,故乙炔所含氢的质量分数最小,故D正确;
故选D.点评:
本题考点: 常见有机化合物的结构;乙炔炔烃.
考点点评: 本题考查有机物的空间结构、化学键、组成通式与同分异构体等,难度中等,注意不饱和烃中双键、三键中共价键性质不同.1年前查看全部
- 丙烷、丙烯、丙炔这三种物质的熔沸点逐渐升高,相对密度不断增大.
丙烷、丙烯、丙炔这三种物质的熔沸点逐渐升高,相对密度不断增大.
另外,丙烷的碳原子空间结构是锯齿型的不是简单的线性排列. u61941年前1
u61941年前1 -
 wvomh03 共回答了12个问题
wvomh03 共回答了12个问题 |采纳率100%第一个问题应该是错的,比较分子化合物的熔沸点一般比较其相对分子质量,相对分子质量越大,熔沸点就越高,这只适合那些不存在氢键的分子化合物,如果分子化合物中有氢键那就另当别论了.
关于第二个问题,是对的.烷烃一般成锯齿形,而不是简单的线性排列.1年前查看全部
- 化学方程式(有机物)(1)丙炔与足量的溴加成(2)丁炔在足量氧气中燃烧(3)乙炔、氯化氢制聚氯乙烯
 以ff的名义QJ你1年前0
以ff的名义QJ你1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
大家在问
- 1实证主义和现象学的联系与区别禁止复制粘贴动作.
- 2物理题(正确答案)1.最小分度值也称____________,是指刻度尺上相邻__________间的长度,测量长度要选
- 3一切发声的物体都在——停止,发声也停止.
- 4全神贯注的反义词是狡黠异常吗顺便写下反义词
- 5They speak German.So I think they are ____(German).
- 6解方程组2X+3Y=15M,5X-3Y=-M,X,Y的值
- 7设 x,y∈R ,且3^x=4^y=6^z,求证 1/z - 1/x =1/2y .
- 8用一个数去除30、75和150,正好都能整除,这个数最大是多少?要列出来
- 9人生就像一场戏,因为有缘才相聚,后面是什么
- 10求概率的公式【高中】老师最近讲了,但是我没听.就是C神马的,貌似老师还给分了两类,放回去的和不放回去的求具体例子以及解法
- 11(2009•翔安区质检)一个几何体的三视图如右所示,则这个几何体是( )
- 12当x不等于0时,f(x)=e^(-1/x^2),当x=0时,x=0,证明f(x)的导数在点x=0处连续.
- 13(初三上单词填空)The kids had to stay indoors b___ of the heavy rain
- 14教室里安静极了,大家认真地朗读课文,一点生音也没有.修改病句
- 15(2012•黑龙江)下面的话,描述天气的是( )