(2013•信阳一模)在高速发展的信息时代,我们要学会获取和辨别信息 ××豆腐:
 初步建立2022-10-04 11:39:541条回答
初步建立2022-10-04 11:39:541条回答| ××豆腐: 配料:大豆、食盐、 植物油、辣椒、味精 图一  图二 |
(2)图二中物品使用的主要材料是______.

已提交,审核后显示!提交回复
共1条回复
 candy102 共回答了24个问题
candy102 共回答了24个问题 |采纳率79.2%- 解题思路:(1)人体的六大营养物质是:水、无机盐、蛋白质、脂肪、糖类和维生素,蛋白质、脂肪、糖类是给人体提供能量的物质.大豆中富含蛋白质,食盐属于无机盐,辣椒中含有维生素,植物油属于油脂;
(2)有机合成材料又称有机高分子材料,包括:合成橡胶、合成纤维和塑料.(1)大豆中富含蛋白质,食盐属于无机盐,辣椒中含有维生素,植物油属于油脂,故答案为:蛋白质;无机盐或维生素或油脂.
(2)有机合成材料又称有机高分子材料,包括:合成橡胶、合成纤维和塑料;故答案为:合成橡胶(或合成材料或有机高分子材料).点评:
本题考点: 生命活动与六大营养素;合成材料的使用及其对人和环境的影响.
考点点评: 呵护生命,保障健康,是现代入追求的永恒主题,六大营养素及化学元素与人体健康知识也就成为考查热点,要重点掌握营养素及化学元素的生理作用、代谢过程、食物来源、缺乏症、合理膳食的原则等内容. - 1年前
相关推荐
- (2013•信阳二模)水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32−+O2+xOH−=Fe3O4+S4O
(2013•信阳二模)水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32−+O2+xOH−=Fe3O4+S4O62−+2H2O
下列说法正确的是( )
A.将纳米Fe3O4颗粒分散在水中没有丁达尔现象
B.将纳米Fe3O4颗粒分散在水中,Fe3O4不能透过滤纸
C.每生成1molFe3O4,反应转移的电子为4mol
D.反应物OH-的化学计量数x=2 长天一啸1年前1
长天一啸1年前1 -
 8618535 共回答了17个问题
8618535 共回答了17个问题 |采纳率94.1%解题思路:A.胶体是指分散质粒子直径在1 nm~100 nm之间的分散系;
B.将纳米Fe3O4颗粒分散在水中得到的分散系是胶体;
C.每生成1molFe3O4,则转移电子数为4mol;
D.根据氢原子守恒得x值.A.将纳米Fe3O4颗粒分散在水中得到的分散系是胶体,有丁达尔效应,故A错误;
B.将纳米Fe3O4颗粒分散在水中得到的分散系是胶体,故B错误;
C.反应3Fe2++2S2O32-+O2+4OH-═Fe3O4+S4O62-+2H2O中,Fe和S元素的化合价升高,被氧化,O2为氧化剂,每生成1molFe3O4,反应转移的电子总数为4mol,故C正确;
D.根据氢原子守恒,水的化学计量数为2,则OH-的化学计量数为4,即x=4,故D错误.
故选C.点评:
本题考点: 纳米材料.
考点点评: 本题考查胶体的性质,难度中等,明确各元素的化合价变化是解答该题的关键.1年前查看全部
- (2012•信阳二模)已知:(1)Zn(s)+[1/2]O2(g)═ZnO(s),△H=-348.3kJ/mol
(2012•信阳二模)已知:(1)Zn(s)+[1/2]O2(g)═ZnO(s),△H=-348.3kJ/mol
(2)2Ag(s)+[1/2]O2(g)═Ag2O(s),△H=-31.0kJ/mol
则Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s)的△H等于( )
A.-317.3kJ/mol
B.-379.3kJ/mol
C.-332.8kJ/mol
D.+317.3 kJ/mol 鸳鸯草1年前1
鸳鸯草1年前1 -
 小鸡崽 共回答了14个问题
小鸡崽 共回答了14个问题 |采纳率92.9%解题思路:根据已知的热化学反应方程式和目标反应,利用盖斯定律来计算目标反应的反应热,以此来解答.由(1)Zn(s)+[1/2]O2(g)═ZnO(s),△H=-348.3kJ•mol-1,
(2)2Ag(s)+[1/2]O2(g)═Ag2O(s),△H=-31.0kJ•mol-1,
根据盖斯定律可知,
(1)-(2)可得Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),
则△H=(-348.3kJ•mol-1)-(-31.0kJ•mol-1)=-317.3kJ•mol-1,
故选:A.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 本题考查学生利用盖斯定律计算反应的反应热,明确已知反应和目标反应的关系是解答本题的关键,难度不大.1年前查看全部
- (2013•信阳一模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
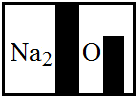 (2013•信阳一模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
(2013•信阳一模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
[提出问题]这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是______.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是______.
[设计实验]为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
[实验结论]实验操作 实验现象 (1)取少量样品于试管中,慢慢滴加BaCl2溶液 出现白色沉淀 (2)静置一段时间后,倾去上层清液,向沉淀中继续滴加稀盐酸 白色沉淀全部溶解,产生大量气泡
(3)该瓶无色溶液是______.生成白色沉淀过程的化学方程式是______.
[实验反思]
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是______.
(5)经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐.简述实验操作和现象.
(6)[综合计算]现取含有氯化钠杂质的纯碱样品25g放入烧杯中,向其中加入50g稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为66.2g(不包括烧杯的质量,且气体的溶解忽略不计).试计算纯碱样品中杂质氯化钠的质量分数. zhaozijing1年前1
zhaozijing1年前1 -
 14541345 共回答了16个问题
14541345 共回答了16个问题 |采纳率93.8%解题思路:根据题干提供的信息进行分析,残缺的标签中钠元素的右下角有数字2,且含有氧元素,故不可能是氯化钠、碳酸氢钠和硝酸钠,可以据此完成(1)(2)两小题;
(3)硫酸钠溶液和碳酸钠溶液都能与氯化钡溶液反应生成白色沉淀,但是碳酸钡沉淀能和盐酸反应产生气体,而硫酸钡不能溶于稀盐酸,可以据此完成解答;
(4)比较碳酸钠和硫酸钠的性质可以知道碳酸钠能与盐酸反应产生气体,而硫酸钠不与盐酸反应,故可以据此解答该题;
(5)碳酸钠的水溶液呈碱性,而硫酸钠的水溶液呈中性,可以使用测定溶液pH的方法或加入指示剂的方法来确定物质的成分,可以据此设计实验来进行判断;
(6)由质量守恒定律可以计算出生成的二氧化碳的质量,然后根据反应的化学方程式可以计算出纯碱样品中碳酸钠的质量,进而计算出样品中氯化钠的质量,最后计算出氯化钠的质量分数即可.(1)根据题干提供的信息进行分析,残缺的标签中Na的右下角有数字2,该物质不可能是氯化钠、碳酸氢钠和硝酸钠;
(2)根据碳酸氢钠(NaHCO3)、硝酸钠(NaNO3)的化学式可以知道中钠元素的右下角没有数字2,故不可能是碳酸氢钠和硝酸钠;
(3)根据实验的现象,加入氯化钡产生了沉淀,产生的沉淀能与盐酸反应产生气体且全部溶解,故该物质是碳酸钠,氯化钡能与碳酸钠反应生成碳酸钡沉淀和氯化钠,其反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl;
(4)碳酸钠能与盐酸反应产生气体,而硫酸钠不与盐酸反应,故可以使用盐酸与样品混合,观察有无气体产生来确定物质的成分;碳酸钠的水溶液呈碱性,而硫酸钠的水溶液呈中性,可以使用测定溶液pH的方法或加入指示剂酚酞的方法来确定物质的成分,可设计实验如下:在玻璃片上放一小片pH试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等.
(6)根据质量守恒定律可以知道生成CO2的质量为:25g+50g-66.2g═8.8g;
设纯碱样品Na2CO3的质量为x
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 8.8g
[106/44]=[x/8.8g]
解得:x═21.2g
纯碱样品中杂质氯化钠的质量分数为:[25g−21.2g/25g]×100%=15.2%
答:纯碱样品中杂质氯化钠的质量分数为15.2%.
故答案为:(1)氯化钠、碳酸氢钠和硝酸钠;
(2)这二者的化学式中Na元素的右下角不会有2;
(3)Na2CO3;BaCl2+Na2CO3═BaCO3↓+2NaCl;
(4)取少量无色溶液样品于试管中,慢慢滴加稀盐酸;
(5)在玻璃片上放一小片pH 试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH 大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等;
(6)15.2%.点评:
本题考点: 缺失标签的药品成分的探究.
考点点评: 对于失去标签的药品成分的探究,要结合所给出问题情景和常见物质的检验、鉴别方法,根据所学的相关知识,认真地进行思考、推断、鉴别出药品的真实身份.1年前查看全部
- (2012•信阳一模)下列化合物:①SO3 ②Fe(OH)3 ③FeCl2&
(2012•信阳一模)下列化合物:①SO3②Fe(OH)3 ③FeCl2④CuS⑤H2SiO3⑥NaHCO3其中不可能通过化合反应制得的是( )
A.①②⑤⑥
B.③④⑤⑥
C.④⑤
D.①②③⑤ uu炎焱1年前1
uu炎焱1年前1 -
 两截人生 共回答了24个问题
两截人生 共回答了24个问题 |采纳率87.5%解题思路:化合反应指由两种或两种以上的物质生成一种新物质的反应反应,结合元素化合物的性质判断.:①二氧化硫与氧气在催化剂、加热的条件下生成SO3 发生化合反应,故①正确;
②氢氧化亚铁与氧气、水反应生成Fe(OH)3,发生化合反应,故②正确;
③铁与氯化铁反应生成FeCl2,发生化合反应,故③正确;
④铜与硫反应生成Cu2S,不能生成CuS,故④错误;
⑤二氧化硅不溶于水,不与水反应,不能化合生成H2SiO3 故⑤错误;
⑥碳酸钠、水、二氧化碳反应生成NaHCO3,发生化合反应,故⑥正确.
故选:C.点评:
本题考点: 含硫物质的性质及综合应用;碳族元素简介;铁的化学性质.
考点点评: 本题考查了元素化合物知识、化学反应类型等,难度不大,掌握元素化合物的知识是关键.1年前查看全部
- (2012•信阳一模)已知X和Y能发生如下反应:X+Y═H2O+盐,下列有关X和Y所属种类的说法中一定不正确的是( )
(2012•信阳一模)已知X和Y能发生如下反应:X+Y═H2O+盐,下列有关X和Y所属种类的说法中一定不正确的是( )
A B C D X 酸性氧化物 碱性氧化物 盐 酸性氧化物 Y 碱 酸 碱 碱性氧化物
A.A
B.B
C.C
D.D 仰泳鱼wz1年前1
仰泳鱼wz1年前1 -
 真心DR123 共回答了16个问题
真心DR123 共回答了16个问题 |采纳率93.8%解题思路:酸性氧化物是能和碱反应生成的是盐和水的氧化物;
碱性氧化物是能和酸反应生成盐和水的氧化物;
碱和盐之间发生的反应是复分解反应,可以生成新的碱和盐,也可以生成盐和水;
酸性氧化物和碱性氧化物化合可以得到盐;A、酸性氧化物能和碱反应生成盐和水,如二氧化碳可以和氢氧化钠反应生成碳酸钠和水,故A正确;
B、碱性氧化物能和酸反应生成盐和水,如氧化铜可以和盐酸反应生成氯化铜和水,故B正确;
C、碱和盐之间发生反应可以生成盐和水,如硫酸氢钠和氢氧化钠反应生成硫酸钠和水,故C正确;
D、酸性氧化物和碱性氧化物化合可以得到盐,酸性氧化物和碱性氧化物都不含H元素,所以不可能生成水,故D错误;
故选D.点评:
本题考点: 酸、碱、盐、氧化物的概念及其相互联系.
考点点评: 本题考查学生化合物之间的反应规律和特点,注意物质的性质以及相关概念的掌握,难度不大.1年前查看全部
- (2009•信阳一模)澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,
(2009•信阳一模)澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性.纳米泡沫碳与金刚石的关系是( )
A.同一种物质
B.同分异构体
C.同位素
D.同素异形体 jj11191年前1
jj11191年前1 -
 五月淡紫色 共回答了17个问题
五月淡紫色 共回答了17个问题 |采纳率76.5%解题思路:A.同一种物质的组成和结构一样,但状态可能不同;
B.同分异构体是分子式相同结构式不同的化合物;
C.质子数相同中子数不同的原子互称同位素,
D.同一元素的不同单质互称同素异形体;A.纳米泡沫碳与金刚石组成元素一样,但结构不一样,不是同一种物质,故A错误;
B.同分异构体是化合物,而纳米泡沫碳与金刚石都是碳元素的不同单质,不是同分异构体,故B错误;
C.同位素是原子,而纳米泡沫碳与金刚石都是碳元素的不同单质,不是同位素,故C错误;
D.纳米泡沫碳与金刚石都是碳元素的不同单质,所以互称同素异形体,故D正确;
故选:D.点评:
本题考点: 同素异形体.
考点点评: 本题考查了基本概念的判断,难点不大,明确这几个概念的区别,同分异构体是化合物,同位素是原子,同素异形体使单质.1年前查看全部
- 为什么河南很多地名都含有“阳”这个字呢,像洛阳,信阳,安阳,南阳什么的
 越少华1年前1
越少华1年前1 -
 撕掉记忆 共回答了28个问题
撕掉记忆 共回答了28个问题 |采纳率85.7%在古代 山的南面,水的背面称之为阳
相反则称之为阴.
古代城市名字里含阴,阳的 一般就是这样取名的.1年前查看全部
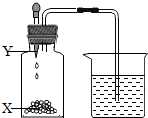
- (2013•信阳一模)如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中,导管口没有气泡产生的是( )
 (2013•信阳一模)如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中,导管口没有气泡产生的是( )
(2013•信阳一模)如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中,导管口没有气泡产生的是( )
A B C D X MnO2 NH4NO3 CaO Mg Y H2O2 H2O H2O 稀HCl
A.A、
B.B、
C.C、
D.D、 提拉Oo米苏1年前1
提拉Oo米苏1年前1 -
 s的猪宝宝 共回答了22个问题
s的猪宝宝 共回答了22个问题 |采纳率86.4%解题思路:根据已有的知识进行分析,导管口没有有气泡产生,则瓶内的压强不能增大,即不能反应生成气体,也不能是瓶内的温度升高.A、MnO2、H2O2混合会产生氧气,会使瓶内气压增大,导管口会有气泡产生,故A错误;B、NH4NO3溶于水是吸热的,会使瓶内的温度降低,压强变小,会出现水倒吸的现象,没有气泡产生,故B正确;C、CaO与水反应会放热,会使...
点评:
本题考点: 反应现象和本质的联系;实验室制取氧气的反应原理;溶解时的吸热或放热现象;金属的化学性质;生石灰的性质与用途.
考点点评: 本题考查了化学知识与物理知识的综合,属于学科交叉题,完成此题,可以依据物质的性质结合物理压强的知识进行.1年前查看全部
- (2012•信阳二模)将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )
(2012•信阳二模)将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )
A.Mg、AlCl3、NaAlO2
B.KNO3、NaCl、CH3COONa
C.NaClO、Na2SO3、BaCl2
D.Ba(NO3)2、FeSO4、NH4HCO3 寒场一雨秋场一1年前1
寒场一雨秋场一1年前1 -
 interzhang003 共回答了14个问题
interzhang003 共回答了14个问题 |采纳率85.7%解题思路:根据盐酸及各选项中的物质所能发生的反应解题.将足量稀盐酸加入题给四种固体混合物中,可能发生的反应有:
A.存在Mg+2HCl=MgCl2+H2↑、NaAlO2+4HCl=AlCl3+NaCl+2H2O,故A不选;
B.只存在CH3COONa+HCl=CH3COOH+NaCl,故B选;
C.存在HCl+NaClO=NaCl+HClO、2HCl+Na2SO3=2NaCl+H2O+SO2↑、2HCl+NaCl=ONaCl+Cl2↑+H2O、HClO+Na2SO3=HCl+Na2SO4,故C不选;
D.存在NH4HCO3+HCl=NH4Cl+H2O+CO2↑、4H++NO3-+3Fe2+=3Fe3++NO↑+2H2O、Ba2++SO42-=BaSO4↓,故D不选;
故选B.点评:
本题考点: 离子反应发生的条件.
考点点评: 本题考查离子反应发生的条件,掌握反应方程式的书写是解题的关键.1年前查看全部
- (2015•信阳一模)如图所示,一根轻杆(质量不计)的一端以O点为固定转轴,另一端固定一个小球,小球以O点为圆心在竖直平
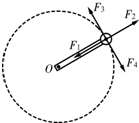 (2015•信阳一模)如图所示,一根轻杆(质量不计)的一端以O点为固定转轴,另一端固定一个小球,小球以O点为圆心在竖直平面内沿顺时针方向做匀速圆周运动.当小球运动到图中位置时,轻杆对小球作用力的方向可能( )
(2015•信阳一模)如图所示,一根轻杆(质量不计)的一端以O点为固定转轴,另一端固定一个小球,小球以O点为圆心在竖直平面内沿顺时针方向做匀速圆周运动.当小球运动到图中位置时,轻杆对小球作用力的方向可能( )
A.沿F1的方向
B.沿F2的方向
C.沿F3的方向
D.沿F4的方向 春虹1年前1
春虹1年前1 -
 haorenbi 共回答了14个问题
haorenbi 共回答了14个问题 |采纳率92.9%小球做匀速圆周运动,根据小球受到的合力提供向心力,则小球受的合力必指向圆心,小球受到竖直向下的重力,还有轻杆的作用力,由图可知,轻杆的作用力如果是F1、F2、F4,与重力的合力不可能指向圆心,只有轻杆的作用力为F3方向,与重力的合力才可能指向圆心.故ABD错误、C正确.
故选:C.1年前查看全部
- (2013•信阳一模)下列对化学反应类型的判断,错误的是( )
(2013•信阳一模)下列对化学反应类型的判断,错误的是( )
A.2H2S+SO2═3S↓+2H2O(复分解反应)
B.CO2+C
2CO(化合反应)高温 .
C.2AgBr
2Ag+Br2↑(分解反应)光照 .
D.2Mg+CO2
2MgO+C(置换反应)点燃 . 老蜜1年前1
老蜜1年前1 -
 bizput3 共回答了20个问题
bizput3 共回答了20个问题 |采纳率90%解题思路:化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”; 分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”;
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应;复分解反应是两种化合物相互交换成分生成两种新的化合物的反应.A、该反应不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应,故选项说法错误.
B、该反应符合“多变一”的特征,属于化合反应,故选项说法正确.
C、该反应符合“一变多”的特征,属于分解反应,故选项说法正确.
D、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项说法正确.
故选A.点评:
本题考点: 反应类型的判定.
考点点评: 本题难度不大,掌握四种基本反应类型的特征并能灵活运用是正确解答本题的关键.1年前查看全部
- (2012•信阳一模)实验是研究化学的基础,如图中所示的实验方法、装置或操作完全正确的是( )
(2012•信阳一模)实验是研究化学的基础,如图中所示的实验方法、装置或操作完全正确的是( )
A.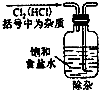
B.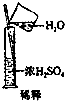
C.
D.
 初步建立1年前1
初步建立1年前1 -
 aqzv 共回答了14个问题
aqzv 共回答了14个问题 |采纳率92.9%解题思路:A、根据洗气装置的特点分析,洗气装置中长导管进气,短导管出气.
B、量筒只能用来量取液体,不能用来溶解固体或稀释液体.
C、实验室用加热氯化铵和氢氧化钙混合物的方法制取氨气,用向下排空气法收集.
D、烧碱有强腐蚀性.A、洗气装置中长导管进气,短导管出气,所以该装置不符合洗气装置特点,故A错误.
B、量筒只能用来量取液体,不能用来溶解固体或稀释液体,且浓硫酸的稀释时,是浓硫酸倒入水中不是水倒入浓硫酸中,故B错误.
C、实验室用加热氯化铵和氢氧化钙混合物的方法制取氨气,且试管口低于试管底,氨气易溶于水,氨气的密度小于空气的密度,所以氨气应采用向下排空气法收集,故C正确.
D、用天平称量药品时,遵循“左物右码“的原则,且强腐蚀性的氢氧化钠应放在烧杯中称量,故D错误.
故选C.点评:
本题考点: 洗气;氨的实验室制法;计量仪器及使用方法;物质的溶解与加热.
考点点评: 本题考查了实验装置或操作的基本知识,难度不大,注意浓硫酸的稀释中应该是:浓硫酸倒入水中不是水倒入浓硫酸中,且不断搅拌防止温度过高.1年前查看全部
- (2014•信阳一模)已知函数f(x)=Asin(ωx+φ),(x∈R,A>0,ω>0,|φ|<[π/2])的部分图象如
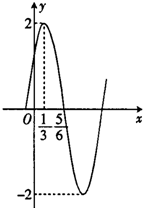 (2014•信阳一模)已知函数f(x)=Asin(ωx+φ),(x∈R,A>0,ω>0,|φ|<[π/2])的部分图象如图所示:
(2014•信阳一模)已知函数f(x)=Asin(ωx+φ),(x∈R,A>0,ω>0,|φ|<[π/2])的部分图象如图所示:
(1)试确定f(x)的解析式;
(2)若f([α/2π])=[1/3],求cos(
−α)的值.2π 3  明天的毛毛虫1年前1
明天的毛毛虫1年前1 -
 legend03zbn 共回答了19个问题
legend03zbn 共回答了19个问题 |采纳率94.7%解题思路:(1)由图可知,A=2,[T/4]=[1/2],可求得ω,再利用[1/3]ω+φ=[π/2]可求得φ,从而可求得f(x)的解析式;
(2)由(1)知f(x)的解析式,结合已知f([α/2π])=[1/3],可求得α的三角函数知,最后利用两角差的余弦计算即可求cos([2π/3]-α)的值.(1)由图可知,A=2,T4=56-13=12,又ω>0,∴T=2πω=2,∴ω=π;由图可知,f(x)=Asin(ωx+φ)经过(13,2),∴13ω+φ=π2,即π3+φ=π2,∴φ=π6,∴f(x)=2sin(πx+π6);(2)∵f(α2π)=13,∴2...
点评:
本题考点: 由y=Asin(ωx+φ)的部分图象确定其解析式;三角函数中的恒等变换应用.
考点点评: 本题考查由y=Asin(ωx+φ)的部分图象确定其解析式,考查三角函数中的恒等变换应用,考查两角差的余弦,属于中档题.1年前查看全部
- (2018•信阳如模)图个表示在某时间段内玉米叶肉细胞中光合作用、有氧呼吸两者之间存在的联系,其中甲~戊表示生理过程,a
(2018•信阳如模)图个表示在某时间段内玉米叶肉细胞中光合作用、有氧呼吸两者之间存在的联系,其中甲~戊表示生理过程,a-d表示相关物质,图如表示该玉米光合作用过程中,测得的CO2释放量和CO2吸收量,其中11、12分别表示相应的面积.请回答下列问题:
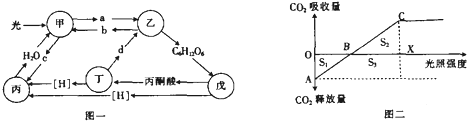
(1)图个中物质d表示______,过程丙进行的部位是______.
(2)在过程甲~戊中,能产生ATP的有______,能产生气体的有______.
(k)在图如中______点都有[H]产生,在图如中不进行图个中甲过程的点为______.
(8)OX段,玉米共吸收的CO2为______(用11、12、1k表示);OB段,玉米固定的CO2为______(用11、12、1k表示). iamcici4131年前1
iamcici4131年前1 -
 ROSE_YTT 共回答了24个问题
ROSE_YTT 共回答了24个问题 |采纳率95.8%解题思路:图一显示了光合作用和呼吸作用之间物质变化和能量变化之间的关系,甲过程是光反应,乙过程是暗反应,丙是有氧呼吸第三步反应,丁是有氧呼吸第二步反应,戊是葡萄糖在细胞基质中的酵解,a是[H]和ATP,b是ADP和Pi,c是氧气,d是二氧化碳.图二显示了光合作用过程中CO2的吸收量和呼吸作用的CO2的释放量之间关系.(1)2中显示3物质是丙酮酸进少步分解的产物,其中另少产物[H]参加下少步反应,而3可以参与暗反应,所以3是CO2;丙过程是有氧呼吸的第三步反应,在线粒体内膜上完成.
(2)能产生TP的过程是;甲光反应,戊、丁、丙分别是有氧呼吸1、2、3步反应都有如TP的产生,乙是暗反应消耗如TP,甲过程光解水产生氧气,丁分解丙酮酸产生CO2.
(3)2二显示的过程能产生[H]的有,有氧呼吸和无氧呼吸,以及光合作用的光反应都能有[H]的产生,即如BC三点.而如点只有呼吸作用,BC二者都有.
(4)2二中,抓住纵坐标意义为CO2的量,另呼吸作用的强度不变可分析.S2应该表示是光照BX以后的积累量.在OB段,积累量应该是负值即S1.
S2+S3 表示玉米光合作用产生的有机物总量即光合作用的二氧化碳总量,而O-X段的CO2吸收量则是光合作用净值所以是:净积累量=光合作用-呼吸作用=(S2+S3)-(S1+S3)=S2-S1,S1+S3 表示玉米呼吸作用消耗的有机物量.
故答案为:
(1)CO2 线粒体内膜
(2)甲、丙、丁、戊,甲、丁
(3)如BC 如
(4)S2-S1 S1点评:
本题考点: 光反应、暗反应过程的能量变化和物质变化;有氧呼吸的过程和意义.
考点点评: 本题综合考察了光合作用的光反应、暗反应以及呼吸作用之间的物质变化和能量变化,而图二首先要分析各个阶段自变量和因变量的变化关系,并结合相关生理过程,把掌握额课本知识应用于图示,就能做好本题.1年前查看全部
- (2012•信阳一模)某固体混合物可能含Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2、NaCl中的一种或
(2012•信阳一模)某固体混合物可能含Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):

请回答
(1)混合物中是否存在FeCl2______(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4______(填“是”或“否”),你的判断依据是______.
(3)写出反应⑤的离子反应方程式;______.
(4)请根据图中数据分析,原固体混合物的成分为______(写化学式). 长春书生1年前1
长春书生1年前1 -
 pwaiyz 共回答了14个问题
pwaiyz 共回答了14个问题 |采纳率78.6%解题思路:依据混合物做实验,结合可能含有的物质的性质,所得现象和有关数据进行分析计算,在过量氢氧化钠溶液中可以生成气体,确定一定含有铵盐,通过碱性干燥剂碱石灰,体积不变,通过浓硫酸体积减少,证明气体是氨气和氢气,判断含有铝;有白色沉淀静置无变化,判断一定无氯化亚铁,一定含有氯化镁;无色溶液加入适量盐酸生成白色沉淀,加入过量盐酸沉淀溶解,只能考虑是氢氧化铝沉淀;根据题干中的实验现象和数据,28.1g固体加入过量的氢氧化钠溶液产生气体,有铵盐和碱反应生成生成的氨气,也可以是金属铝与氢氧化钠溶液反应生成氢气,11.2L气体通过碱石灰无变化,说明气体中无与碱石灰反应的气体,无水蒸气的存在,通过浓硫酸,气体剩余6.72L,体积减少11.2L-6.72L=4.48L,结合混合物可能存在的物质可知,一定含有硫酸铵与氢氧化钠反应生成氨气为4.48L,剩余的气体只能是氢气,体积为6.72L,说明原混合物中一定含有铝;28.1g固体加入过量的氢氧化钠溶液中产生白色沉淀5.8g,久置无变化,说明原混合物中一定唔氯化亚铁,由于氢氧化铝溶于强碱,所以能生成白色沉淀的一定氯化镁生成的氢氧化镁白色沉淀,质量为5.8g;28.1g固体加入过量的氢氧化钠溶液得到无色溶液,加入适量盐酸 会生成沉淀,说明金属铝或氯化铝与过量碱反应生成的偏铝酸钠与盐酸反应生成的氢氧化铝沉淀,加入过量盐酸沉淀溶解进一步证明沉淀是氢氧化铝,综上所述可知:
(1)混合物中不存在FeCl2,故答案为:否;
(2)混合物中一定存在(NH4)2SO4,气体通过浓硫酸会体积减少说明减少的气体是碱性气体,所以依据是气体通过浓硫酸减少4.48L,
故答案为:是;气体通过浓硫酸减少4.48L说明是碱性气体;
(3)反应⑤是氢氧化铝 具有两性和强酸反应,离子方程式为A1(OH)3+3H+=A13++3H2O,故答案为:A1(OH)3+3H+=A13++3H2O;
(4)依据上述分析可得到原混合物中一定含有A1、(NH4)2SO4、MgCl2,一定不含FeCl2,A1Cl3、NaCl不能确定,故答案为:A1、(NH4)2SO4、MgCl2.点评:
本题考点: 几组未知物的检验;镁、铝的重要化合物.
考点点评: 本题考查了物质组成的判断分析方法,主要是铝、铵盐、氯化镁、氢氧化铝、氯化亚铁等物质性质的应用,关键要解决气体的生成与变化判断气体的成分,试剂量的应用和生成沉淀的实质.1年前查看全部
- (2011•信阳二模)图为甲、乙两种植物在不同温度条件下,光合作用效率的变化情形.据图分析正确的是( )
(2011•信阳二模)图为甲、乙两种植物在不同温度条件下,光合作用效率的变化情形.据图分析正确的是( )
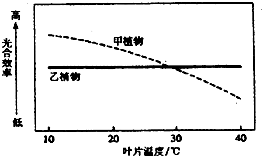
A.温度5℃时,甲植物的光合效率大于乙植物的光合效率
B.温度22℃时,乙植物的光合效率大于甲植物的光合效率
C.温度50℃时,乙植物的光合效率大于甲植物的光合效率
D.甲植物较适合生长在温带地区,乙植物则可以生长在热带地区 pzllb1年前1
pzllb1年前1 -
 mtyecan7 共回答了20个问题
mtyecan7 共回答了20个问题 |采纳率70%解题思路:分析题图:甲植物随着叶片温度的增加,光合速率逐渐降低,乙植物随着叶片温度的增加,光合速率保持不变.A、题中没有显示温度为5℃时的光合速率,A错误;
B、温度为22℃乙植物的光合效率小于甲植物的光合效率,B错误;
C、题中没有显示温度为50℃时的光合速率,C错误;
D、甲植物随着叶片温度的增加,光合速率逐渐降低,乙植物随着叶片温度的增加,光合速率保持不变,甲植物较适合生长在温带地区,乙植物则可以生长在热带地区,D正确.
故选:D.点评:
本题考点: 光反应、暗反应过程的能量变化和物质变化;细胞呼吸的过程和意义.
考点点评: 本题主要考查温度对光合作用的影响,识图读图是解答的关键.1年前查看全部
- (2011•信阳二模)近年来研制的NF3气体可用作氟化氢-氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH
(2011•信阳二模)近年来研制的NF3气体可用作氟化氢-氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2═NF3+3NH4F,下列说法中不正确的是( )
A.NF3的形成过程用电子式可表示为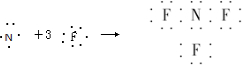
B.NF3的氧化性大于F2
C.NF3分子空间构型为三角锥形
D.NH4F中既有离子键又有极性共价键 secondary-planet1年前1
secondary-planet1年前1 -
 ARCHANC 共回答了15个问题
ARCHANC 共回答了15个问题 |采纳率93.3%解题思路:A、NF3属于共价化合物,N原子和F原子周围有8个电子;
B、根据氧化剂的氧化性大于氧化产物的氧化性判断;
C、根据NH3分子构型判断NF3分子构型;
D、根据NH4Cl化学键类型判断NH4F的化学键类型.A、NF3属于共价化合物,N原子和F原子周围有8个电子,则NF3的形成过程用电子式可表示为
 ,故A正确;
,故A正确;
B、4NH3+3F2═NF3+3NH4F,该反应中F2为氧化剂,NF3为氧化产物,则氧化性NF3的氧化性小于F2,故B错误;
C、NF3分子构型与NH3相似,NH3分子构型是三角锥型的,所以NF3分子构型也是三角锥型的,故C正确;
D、NH4Cl与NH4F含的阳离子相同,阴离子是同一主族元素,所以NH4Cl与NH4F具有相同的化学键,所以NH4F中存在的化学键是离子键、极性共价键,故D正确;
故选B.点评:
本题考点: 用电子式表示简单的离子化合物和共价化合物的形成;判断简单分子或离子的构型;极性键和非极性键.
考点点评: 本题考查物质的结构、化学键、物质的分类、氧化还原反应,该反应中元素的化合价的判断是解答的关键,并注意类推方法的应用,题目难度中等.1年前查看全部
- (2014•信阳二模)下表是人体内的红细胞(未成熟)、胰岛B细胞、浆细胞内所含有的核基因及这些基因表达的情况(“+”表示
(2014•信阳二模)下表是人体内的红细胞(未成熟)、胰岛B细胞、浆细胞内所含有的核基因及这些基因表达的情况(“+”表示该基因能表达,“一”表示该基因未表达).下列有关说法正确的是( )
血红蛋白基因 胰岛素基因 抗体基因 有氧呼吸酶基因 红细胞 + - - + 胰岛B细胞 - ① - + 浆细胞 - - ② ③
A.①②③均表示“+”
B.此表说明细胞分化导致基因的选择性表达
C.三种细胞中mRNA和蛋白质种类完全不同
D.三种细胞的形态、结构和生理功能不同的根本原因是核基因种类不完全相同 Jrimen1年前1
Jrimen1年前1 -
 godnumen 共回答了13个问题
godnumen 共回答了13个问题 |采纳率69.2%解题思路:分析表格:表格中表示人体三种不同细胞中的基因存在及表达情况.三种细胞都存在血红蛋白基因、胰岛素基因、抗体墓因和有氧呼吸酶基因四种基因,但血红蛋白基因只在红细胞中表达;胰岛素基因只在胰岛B细胞中表达;抗体基因只在浆细胞中表达;而有氧呼吸酶基因在三种细胞中均表达.A、血红蛋白基因只在红细胞中表达;胰岛素基因只在胰岛B细胞中表达;抗体基因只在浆细胞中表达;而有氧呼吸酶基因在三种细胞中均表达,则①②③均表示“+”,A正确;
B、此表说明基因的选择性表达导致细胞分化,B错误;
C、三种细胞中mRNA和蛋白质种类不完全相同,有氧呼吸酶相关的信使RNA和蛋白质在所有细胞都表达,C错误;
D、三种体细胞中都具有4种基因,是由于人体细胞都来源于同一个受精卵,含有相同的遗传信息,三种细胞的形态、结构和生理功能不同的根本原因是基因的选择性表达,D错误.
故选:A.点评:
本题考点: 细胞的分化.
考点点评: 本题结合表格中基因表达情况,考查细胞分裂和细胞分化的相关知识,首先要求考生掌握细胞有丝分裂的特点,明确同一个体中所有的体细胞都含有相同的遗传信息;其次根据表中信息,推测相应细胞中表达的基因.1年前查看全部
- (2011•信阳二模)植物细胞的细胞质是不停的流动.根据研究发现同一组织相邻细胞的细胞质流动方式和方向是相同的.某实验小
(2011•信阳二模)植物细胞的细胞质是不停的流动.根据研究发现同一组织相邻细胞的细胞质流动方式和方向是相同的.某实验小组选用菠菜、苔藓、黑藻作为实验材料完成几个实验.
(1)选择合适的材料一次性连续完成观察叶绿体形态、观察细胞质流动、探究气孔开闭机理等三个实验.甲、乙、丙三位同学分别选择菠菜、苔藓、黑藻做实验材料各自完成实验.你认为哪些同学的三个连续实验会成功.理由是什么?______.
(2)甲同学选择菠菜做实验,具体步骤:
①用镊子撕取菠菜______(上、下)表皮组织,带有少许______
②载玻片中央滴一滴清水.将撕取的表皮组织平铺在其上.盖上盖玻片并用滤纸吸收多余的水分.
(3)为了看清细胞质流动情况,常常选择叶绿体作为运动标记.最好选择______作为参照物.原因是______.
(4)你观察到菠菜表皮细胞里______(含有、没有)叶绿体.
(5)细胞质流动速度过快不利于观察叶绿体的形态.在不影响细胞状本情况下,甲同学通过______方法快速降低流动速度.
(6)查资料得知气孔两侧的保卫细胞具有叶绿体.光合作用合成葡萄糖可以立即进入细胞质;保卫细胞吸水膨胀引起气孔开放,失水气孔关闭.甲同学在实验中发现.当光线充足情况下,水分若充足时气孔开放,水分若不足气孔关闭;在光照微弱时,不管水分充足如否,气孔均关闭.根据此现象,你写出假设进行解释:
光照时:______.
无光时:______. 鲨F1年前1
鲨F1年前1 -
 weichaocoke 共回答了17个问题
weichaocoke 共回答了17个问题 |采纳率94.1%解题思路:菠菜、苔藓、黑藻中,由于只有菠菜叶含有气孔,故探究气孔开闭机理只能用菠菜叶;观察细胞质流动情况,常常选择叶绿体作为运动标记.最好选择细胞壁为参照物,因细胞壁固定不动且可以看见.细胞质流动和温度有关,在温度高时流动快,在温度低时流动慢.(1)由于只有菠菜叶含有气孔,故探究气孔开闭机理只能用菠菜叶,故只有甲同学的三个连续实验会成功.
(2)菠菜叶的下表皮易于撕取并带有叶肉细胞,可用于观察叶绿体的形态.
(3)为了看清细胞质流动情况,常常选择叶绿体作为运动标记.最好选择细胞壁为参照物,因细胞壁固定不动且可以看见.
(4)表皮细胞中无叶绿体,而叶肉细胞中含有叶绿体.
(5)细胞质在温度高时流动快,在温度低时流动慢,故甲同学通过降低装片温度方法快速降低流动速度.
(6)据题意可知,保卫细胞吸水膨胀引起气孔开放,失水气孔关闭.当光线充足情况下,水分若充足时气孔开放,水分若不足气孔关闭;在光照微弱时,不管水分充足如否,气孔均关闭.故说明气孔关闭和水分的吸收有关,也和光合作用有关,故可做出出假设:光照时,光合作用产生的单糖是细胞质渗透压增大,引起细胞吸水;无光时,单糖被消耗,细胞质渗透压降低,细胞失水,气孔关闭.
故答案为:(1)甲 只有菠菜叶才具有气孔
(2)①下 叶肉细胞
(3)细胞壁 细胞壁固定不动且可以看见
(4)没有
(5)降低装片温度
(6)光照时,光合作用产生的单糖是细胞质渗透压增大,引起细胞吸水; 无光时,单糖被消耗,细胞质渗透压降低,细胞失水,气孔关闭点评:
本题考点: 观察线粒体和叶绿体;光反应、暗反应过程的能量变化和物质变化.
考点点评: 本题综合考查了有关菠菜的探究实验,意在考查学生的应用和实验探究能力,试题难度中等.1年前查看全部
- (2014•信阳二模)一个胰岛素缺乏的糖尿病患者与健康人一样正常进食(食量相同).下列有关叙述正确的是( )
(2014•信阳二模)一个胰岛素缺乏的糖尿病患者与健康人一样正常进食(食量相同).下列有关叙述正确的是( )
A.血糖调节存在反馈调节
B.胰高血糖素是唯一在血糖浓度高时降血糖的激素
C.调节血糖浓度的激素只有胰岛素和胰高血糖素
D.饭后糖尿病患者血糖迅速大量转化为糖原使血糖浓度恢复正常 jessydizq1年前1
jessydizq1年前1 -
 深海里的鱼 共回答了13个问题
深海里的鱼 共回答了13个问题 |采纳率100%解题思路:1、胰岛素能促进血糖氧化分解、合成糖原、转化成非糖类物质;抑制肝糖原的分解和非糖类物质转化,使得血糖浓度降低.
2、胰高血糖素和肾上腺素能促进肝糖原的分解和非糖类物质转化,使得血糖浓度升高.
3、胰岛素和胰高血糖素互为拮抗关系,胰高血糖素和肾上腺素互为协同关系.A、血糖浓度低促进胰高血糖素的分泌,进而升高血糖,血糖浓度升高时促进胰岛素的分泌,进而降低血糖,属于反馈调节,A正确;
B、胰高血糖素和肾上腺素能促进肝糖原分解和非糖类物质转化,使得血糖浓度升高,B错误;
C、调节血糖的激素有胰岛素、胰高血糖素和肾上腺素,C错误;
D、饭后糖尿病患者血糖浓度升高,大量葡萄糖随着尿量排出体外,但由于胰岛素分泌不足,血糖浓度居高不下,D错误.
故选:A.点评:
本题考点: 体温调节、水盐调节、血糖调节.
考点点评: 本题考查血糖调节的相关知识,意在考查学生分析问题和解决问题的能力,难度不大.1年前查看全部
- (2011•信阳二模)下列有关比较中,大小顺序排列错误5是( )
(2011•信阳二模)下列有关比较中,大小顺序排列错误5是( )
A.热稳定性:PH3>H2S>HBr>NH3
B.物质的熔点:石英>食盐>冰
C.结合H+的能力:CO32->CH3COO->SO42-
D.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 linyuan491年前1
linyuan491年前1 -
 adreamer123 共回答了23个问题
adreamer123 共回答了23个问题 |采纳率82.6%解题思路:A.非金属性越强氢化物越稳定,键能越大氢化物越稳定;
B.根据晶体类型判断,一般熔沸点:原子晶体>离子晶体>分子晶体;
C.酸根离子结合H+能力的强弱是看对应酸的强弱,酸性越弱对应酸根结合H+能力越强;
D.分散系的粒子直径大小关系,浊液>胶体>溶液.A.同一周期从左到右,氢化物稳定性逐渐增强,同一主族,从上到下,氢化物的稳定性逐渐减弱,NH3中的氮原子半径小于HB他,所以N-H键能大于H-B他键能,NH3比HB他稳定,而溴的非金属性大于硫,硫大于磷,所以稳定性NH3>HB他>H2少>PH3,故A错误;
B.石英为原子晶体,食盐为离子晶体,冰为分子晶体,故熔点:石英>食盐>冰,故B正确;
C.硫酸是强酸,醋酸酸性强于碳酸,所以对应酸根离子结合H+的能力:CO32->CH3COO->少Oq2-,故C正确;
D.分散系的粒子直径大小关系,浊液>胶体>溶液,故分散质粒子的直径:Fi(OH)3悬浊液>Fi(OH)3胶体>FiCl3溶液,故D正确;
故选A.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查元素周期律、晶体类型与性质、分散系等,难度中等,主要基础知识的理解掌握.1年前查看全部
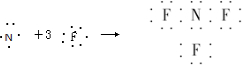
- (2014•信阳一模)如图,一个半圆和长方形组成的铁皮,长方形的边AD为半圆的直径,O为半圆的圆心,AB=1,BC=2,
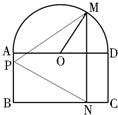 (2014•信阳一模)如图,一个半圆和长方形组成的铁皮,长方形的边AD为半圆的直径,O为半圆的圆心,AB=1,BC=2,现要将此铁皮剪出一个等腰三角形PMN,其底边MN⊥BC.
(2014•信阳一模)如图,一个半圆和长方形组成的铁皮,长方形的边AD为半圆的直径,O为半圆的圆心,AB=1,BC=2,现要将此铁皮剪出一个等腰三角形PMN,其底边MN⊥BC.
(1)设∠MOD=30°,求三角形铁皮PMN的面积;
(2)求剪下的铁皮三角形PMN面积的最大值. ironers1年前1
ironers1年前1 -
 日出时终结 共回答了17个问题
日出时终结 共回答了17个问题 |采纳率82.4%解题思路:(1)设MN交AD交于Q点由∠MOD=30°,利用锐角三角函数可求MQ,OQ,进而可求MN,AQ,代入S△PMN=[1/2]MN•AQ可求
(2)设∠MOQ=θ,由θ∈[0,[π/2]],结合锐角三角函数的定义可求MQ=sinθ,OQ=cosθ,代入三角形的面积公式S△PMN=[1/2]MN•AQ=[1/2](1+sinθ)(1+cosθ)展开利用换元法,转化为二次函数的最值求解(1)设MN交AD交于Q点
∵∠MOD=30°,
∴MQ=[1/2],OQ=
3
2(算出一个得2分)
S△PMN=[1/2]MN•AQ=[1/2]×[3/2]×(1+
3
2)=
6+3
3
8…(6分)
(2)设∠MOQ=θ,∴θ∈[0,[π/2]],MQ=sinθ,OQ=cosθ
∴S△PMN=[1/2]MN•AQ=[1/2](1+sinθ)(1+cosθ)
=[1/2](1+sinθcosθ+sinθ+cosθ)….(11分)
令sinθ+cosθ=t∈[1,
2],
∴S△PMN=[1/2](t+1+
t2−1
2)
θ=[π/4],当t=点评:
本题考点: 两角和与差的正弦函数.
考点点评: 本题主要考查了三角函数的定义的应用及利用三角函数求解函数的最值,换元法的应用是求解的关键1年前查看全部
- (2012•信阳二模)下列物质中按照纯净物,混合物,电解质和非电解质的顺序排列的是( )
(2012•信阳二模)下列物质中按照纯净物,混合物,电解质和非电解质的顺序排列的是( )
A.盐酸,水煤气,醋酸,干冰
B.冰醋酸,盐酸,硫酸钠,乙醇
C.苛性钠,石灰石,铁,硫酸钡
D.胆矾,漂白粉,氯化钾,氯气 gift21年前1
gift21年前1 -
 hamiya 共回答了22个问题
hamiya 共回答了22个问题 |采纳率81.8%解题思路:纯净物是指由同种物质组成的,化合物是指由不同种物质组成的,电解质是指在水溶液里或熔化状态下能够导电的化合物,非电解质是指在水溶液里和熔化状态下都不能够导电的化合物,据此可以分析各个选项中各种的所属类别.A.盐酸、水煤气均为混合物,醋酸、干冰分别属于化合物,则醋酸属于电解质,干冰属于非电解质,故A错误;
B.冰醋酸、盐酸、硫酸钠、乙醇分别属于纯净物、混合物、电解质、非电解质,故B正确;
C.苛性钠、石灰石、铁、硫酸钡分别属于纯净物、混合物、单质、电解质,故C错误;
D.胆矾、漂白粉、氯化钾、氯气分别属于纯净物、混合物、电解质、单质,故D错误.
故选:B.点评:
本题考点: 混合物和纯净物;电解质与非电解质.
考点点评: 本题考查了纯净物、混合物、电解质、非电解质的概念判断及各种物质的成分掌握,难度中等.1年前查看全部
- (2009•信阳一模)下列条件下,两种气体的分子数一定不相等的是( )
(2009•信阳一模)下列条件下,两种气体的分子数一定不相等的是( )
A.相同质量、不同密度的N2O和CO2
B.相同体积、相同密度的CO和C2H4
C.相同温度、相同压强、相同体积的O2和O3
D.相同压强、相同体积、相同质量的NO2和N2O4 三十三画1年前1
三十三画1年前1 -
 tingxue5226 共回答了15个问题
tingxue5226 共回答了15个问题 |采纳率93.3%解题思路:根据N=nNA可知,气体分子数目不相等,则二者物质的量不相等,
A.根据n=[m/M]判断;
B.根据m=ρV,n=[m/M]判断;
C.同温同压下,体积之比等于物质的量之比;
D.根据n=[m/M]判断.根据N=nNA可知,气体分子数目不相等,则二者物质的量不相等,
A.N2O和CO2的摩尔质量相等为44g/mol,根据n=[m/M]可知,二者质量相等,则物质的量相等,含有的分子数目一定相等,故A不选;
B.根据m=ρV可知,相同体积、相同密度的CO和C2H4的质量相等,二者摩尔质量都是28g/mol,根据n=[m/M]可知,二者物质的量相等,含有的分子数目一定相等,故B不选;
C.相同温度、相同压强、相同体积的O2和O3的物质的量之相等,含有分子数目一定相等,故C不选;
D.NO2和N2O4的摩尔质量不同,根据n=[m/M]可知,二者物质的量不同,含有分子数目不同,故D选;
故选:D.点评:
本题考点: 物质的量的相关计算.
考点点评: 本题考查阿伏伽德罗定律及推论,难度不大,注意利用pV=nRT理解阿伏伽德罗定律及推论.1年前查看全部
- (2009•信阳一模)下列实验操作错误的是( )
(2009•信阳一模)下列实验操作错误的是( )
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.测定中和热的实验中,记录NaOH溶液与盐酸均匀混合后溶液的最高温度
C.测定硫酸铜晶体中结晶水的含量时,小火缓慢加热,防止晶体飞溅
D.配制0.1mol•L-1H2SO4溶液时,将浓硫酸直接注入容量瓶中,加水稀释至刻度线 hell_1年前1
hell_1年前1 -
 chongyu 共回答了16个问题
chongyu 共回答了16个问题 |采纳率93.8%解题思路:A.分液时注意防止液体污染;
B.在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的最高温度作为末温度;
C.晶体飞溅或造成误差;
D.容量瓶不能用来稀释溶液.A.为防止液体污染,分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒,故A正确; B.在中和热测定的实验中,需测温度3次,一,盐酸温度,二,氢氧化钠温度,两者取平均值,即初始温度;三,反应之后的最高...
点评:
本题考点: 分液和萃取;配制一定物质的量浓度的溶液;中和热的测定.
考点点评: 本题考查分液、中和热的测定、溶液的配制等,题目难度不大,注意容量瓶不能用来稀释溶液,应先在小烧杯中稀释,D为易错点.1年前查看全部
- (2011•信阳二模)一个用半导体材料制成的电阻器D,其电流I随它两端电压U变化的关系如图中的(a)所示,将它与两个标准
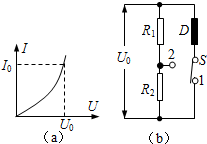 (2011•信阳二模)一个用半导体材料制成的电阻器D,其电流I随它两端电压U变化的关系如图中的(a)所示,将它与两个标准电阻R1、R2组成如图(b)所示电路,当电键S接通位置1时,三个用电器消耗的电功率均为P.将电键S切换到位置2后,电阻器D和电阻R1、R2消耗的电功率分别是PD、P1、P2,下列关系中正确的是( )
(2011•信阳二模)一个用半导体材料制成的电阻器D,其电流I随它两端电压U变化的关系如图中的(a)所示,将它与两个标准电阻R1、R2组成如图(b)所示电路,当电键S接通位置1时,三个用电器消耗的电功率均为P.将电键S切换到位置2后,电阻器D和电阻R1、R2消耗的电功率分别是PD、P1、P2,下列关系中正确的是( )
A.P1>P
B.P1>P2
C.4P1>PD
D.PD+P1+P2>3P haihan151年前1
haihan151年前1 -
 zz边缘 共回答了14个问题
zz边缘 共回答了14个问题 |采纳率92.9%解题思路:根据电阻器D的伏安特性曲线,分析其电阻与电压的关系.根据将电键S切换到位置2后,分析电阻R1、R2电压的变化,分析功率关系.根据电阻器D电阻的变化,判断4P1与PD的关系.分析电路总电阻的变化,判断PD+P1+P2与3P的关系.根据电阻器D的伏安特性曲线,其电阻随电压的增大而减小,电压的减小而增大.设R1=R2=R.
将电键S切换到位置2前,电阻器D和电阻R1、R2的电压分别为U0、
U0
2.由于三个用电器消耗的电功率均为P,由功率公式P=
U2
R,得到此时电阻器D的电阻RD=4R,外电路总电阻为R总=[2R•4R/6R]=[4/3R.将电键S切换到位置2后,电阻器D的电压减小,电阻增大,RD>4R,外电路总电阻R总>R+
R•4R
5R]=1.8R.
A、将电键S切换到位置2后,电阻器D和电阻R1并联的电阻为R并=
RDR
RD+R<R,所以电阻R1的电压小于
U0
2,电阻R1消耗的功率减小,即有P1<P.故A错误.
B、电阻R1的电压小于
U0
2,电阻R2的电压大于
U0
2,则P1>P2.故B错误.
C、将电键S切换到位置2后,电阻器D和电阻R1的电压相等,由功率公式P=
U2
R,由于RD>4R,则4P1>PD.故C正确.
D、由于外电路总增大,而总电压不变,电路的总功率减小,则PD+P1+P2<3P.故D错误.
故选C点评:
本题考点: 闭合电路的欧姆定律.
考点点评: 本题是动态变化分析问题,要抓住电阻器D是由半导体材料制成的,电阻不是定值的特点.1年前查看全部
- 仿写句子.愤怒是人的正常情感之一,当你的尊严被践踏,当你的信阳被玷污,当你的家国被侵占,你能不产生火焰般的愤怒吗?
 ufo6011年前1
ufo6011年前1 -
 idaa11we 共回答了17个问题
idaa11we 共回答了17个问题 |采纳率82.4%悲伤是人的正常情感之一,当你的朋友离你远去,当你的愿望没有达到,当你的努力付之东流,你能不产生寒冰般的失落吗?1年前查看全部
- (2014•信阳二模)如图为两个家族的遗传系谱图,已知甲家庭患色盲,5号无乙家族致病基因,乙家族无色盲基因.下列说法正确
(2014•信阳二模)如图为两个家族的遗传系谱图,已知甲家庭患色盲,5号无乙家族致病基因,乙家族无色盲基因.下列说法正确是( )
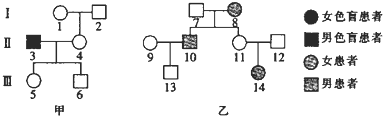
A.乙家族遗传病的致病基因位于X染色体上
B.乙家族中Ⅱ12、Ⅲ13肯定是致病基因携带者
C.Ⅱ11和Ⅱ12这对夫妻再生正常男孩的概率是[3/4]
D.Ⅲ5与Ⅲ13婚配后,后代同时患两种病的概率是[1/2] iyou201年前1
iyou201年前1 -
 锦润 共回答了18个问题
锦润 共回答了18个问题 |采纳率94.4%解题思路:分析甲图:甲家族患色盲,色盲是伴X染色体隐性遗传病(用B、b表示),则Ⅱ3的基因型为XbY;
分析乙图:Ⅱ11和Ⅱ12均不患乙病,但他们有一个患乙病的女儿,即“无中生有为隐性,隐性看女病,女病男正非伴性”,说明乙病为常染色体隐性遗传病(用A、a表示),则Ⅱ11和Ⅱ12的基因型均为Aa.A、由以上分析可知,乙家族遗传病的致病基因位于常染色体上,A错误;
B、乙病为常染色体隐性遗传病,根据Ⅲ14、Ⅱ10可推知Ⅱ12、Ⅲ13肯定是致病基因携带者,B正确;
C、Ⅱ11和Ⅱ12的基因型均为Aa,他们再生正常男孩的概率是[3/4]×[1/2=
3
8],C错误;
D、Ⅲ5的基因型为AAXBXb,Ⅲ13的基因型为AaXBY,他们所生后代患色盲的概率为[1/4],患乙病的概率为0,因此他们的后代同时患两种病的概率是0,D错误.
故选:B.点评:
本题考点: 常见的人类遗传病.
考点点评: 本题结合系谱图,考查人类遗传病,要求考生识记几种常考的人类遗传病的类型及特点,能根据系谱图和题干信息准确判断乙病的遗传方式及相应个体的基因型,再进行相关概率的计算,属于考纲理解和应用层次的考查.1年前查看全部
- (2012•信阳模拟)给出下面结论:
(2012•信阳模拟)给出下面结论:
①命题p:“∃x∈R,x2-3x+2≥0”的否定为¬p:“∀x∈R,x2-3x+2<0”;
②命题:“∀x∈M,P(x)”的否定为:“∃x∈M,P(x)”;
③若¬p是q的必要条件,则p是¬q的充分条件;
④“M>N”是“㏒aM>㏒aN”的充分不必要条件.
其中正确结论的个数为( )
A.4
B.3
C.2
D.1 qingchongju1年前1
qingchongju1年前1 -
 大卫豆腐 共回答了12个问题
大卫豆腐 共回答了12个问题 |采纳率83.3%解题思路:命题p:“∃x∈R,x2-3x+2≥0”的否定为¬p:“∀x∈R,x2-3x+2<0”;命题:“∀x∈M,P(x)”的否定为:“∃x∈M,¬P(x)”;由¬p是q的必要条件,知q⇒¬p,p⇒¬q,故p是¬q的充分条件;“M>N”是“㏒aM>㏒aN”的不充分不必要条件.命题p:“∃x∈R,x2-3x+2≥0”的否定为¬p:“∀x∈R,x2-3x+2<0”,故①正确;
命题:“∀x∈M,P(x)”的否定为:“∃x∈M,¬P(x)”,故②不正确;
∵¬p是q的必要条件,∴q⇒¬p,
∴p⇒¬q,故p是¬q的充分条件,故③正确;
“M>N”是“㏒aM>㏒aN”的不充分不必要条件,故④不正确.
故选C.点评:
本题考点: 命题的真假判断与应用;全称命题;特称命题;必要条件、充分条件与充要条件的判断.
考点点评: 本题考查命题的真假判断,是基础题.解题时要认真审题,仔细解答,注意合理地进行等价转化.1年前查看全部
- (2014•信阳二模)如图为线粒体剖面图,相关叙述正确的是( )
(2014•信阳二模)如图为线粒体剖面图,相关叙述正确的是( )

A.ATP合成酶只分布在①上
B.将线粒体放在蒸馏水中,①②同时被涨破
C.细菌线粒体内的核糖体形成与核仁有关
D.健那绿(铁苏木精)可使线粒体呈现蓝绿色(蓝色) 媛媛02051年前1
媛媛02051年前1 -
 xiaolr7 共回答了17个问题
xiaolr7 共回答了17个问题 |采纳率94.1%解题思路:分析题干和题图可知,该题的知识点是线粒体的结构和功能,线粒体结构与功能相适应的特点,真核细胞与原核细胞的比较,梳理相关知识,然后分析选项进行解答.A、线粒体中线粒体基质和线粒体内膜都是有氧呼吸的场所,因此ATP合成酶分布在线粒体基质和线粒体内膜上,即①②都含有ATP合成酶,A错误;
B、将线粒体放在蒸馏水中,线粒体外膜先涨破,B错误;
C、细菌是原核生物,没有核仁,C错误;
D、健那绿是线粒体的活体染色剂,可以使线粒体呈现蓝绿色,D正确.
故选:D.点评:
本题考点: 线粒体、叶绿体的结构和功能.
考点点评: 对于线粒体结构和功能的理解,把握知识点间的内在联系是解题的关键.1年前查看全部
- (2012•信阳模拟)给出下面结论:
(2012•信阳模拟)给出下面结论:
①命题p:“∃x∈R,x2-3x+2≥0”的否定为¬p:“∀x∈R,x2-3x+2<0”;
②命题:“∀x∈M,P(x)”的否定为:“∃x∈M,P(x)”;
③若¬p是q的必要条件,则p是¬q的充分条件;
④“M>N”是“㏒aM>㏒aN”的充分不必要条件.
其中正确结论的个数为( )
A.4
B.3
C.2
D.1 tredwtv1年前1
tredwtv1年前1 -
 zhanghua996 共回答了12个问题
zhanghua996 共回答了12个问题 |采纳率91.7%命题p:“∃x∈R,x2-3x+2≥0”的否定为¬p:“∀x∈R,x2-3x+2<0”,故①正确;
命题:“∀x∈M,P(x)”的否定为:“∃x∈M,¬P(x)”,故②不正确;
∵¬p是q的必要条件,∴q⇒¬p,
∴p⇒¬q,故p是¬q的充分条件,故③正确;
“M>N”是“㏒aM>㏒aN”的不充分不必要条件,故④不正确.
故选C.1年前查看全部
- 信阳的大眼瞪小眼是什么意思?信阳方言大眼瞪小眼是什么意思?是在和我聊天的时候说的啊,不可能是举足无措的意思 面对问题都没
信阳的大眼瞪小眼是什么意思?
信阳方言大眼瞪小眼是什么意思?
是在和我聊天的时候说的啊,不可能是举足无措的意思 面对问题都没解决方法 就是大眼瞪小眼 也不是歇后语 可可的nn1年前4
可可的nn1年前4 -
 liaaheixine 共回答了19个问题
liaaheixine 共回答了19个问题 |采纳率84.2%举足无措的意思 面对问题都没解决方法 信阳话很深奥的 不同的氛围有不同的意思1年前查看全部
- (2013•信阳一模)实验是科学探究的重要途径,请将下列有关实验问题填写完整.
(2013•信阳一模)实验是科学探究的重要途径,请将下列有关实验问题填写完整.
(1)在粗盐的提纯过程中有三处用到玻璃棒,其中在蒸发过程中要用玻璃棒不断搅拌,其目的是______.
(2)测定某溶液的pH时,先用水将pH试纸润湿会使结果______.(填“偏大”、“偏小”、“不变”或“无法确定”)
(3)除去Na2SO4溶液中少量的Na2CO3,不能选用盐酸的原因是______. 天阿paul1年前1
天阿paul1年前1 -
 pppfff182 共回答了13个问题
pppfff182 共回答了13个问题 |采纳率92.3%解题思路:(1)根据蒸发的注意事项分析;
(2)根据将pH试纸的使用注意事项分析;
(3)根据碳酸钠与盐酸的反应分析.(1)在蒸发过程中要用玻璃棒不断搅拌,其目的是防止因局部温度过高,造成蒸发液飞溅;
(2)测定某溶液的pH时,先用水将pH试纸润湿相当于将待测液稀释.在测定酸液时,pH变大,在测定碱液时,pH变小,在测定中性液时,pH不变.所以,无法确定;
(3)由于碳酸钠与盐酸的反应生成的氯化钠混入溶液中,所以,不能选用盐酸的原因是生成NaCl,引入新的杂质.
故答为:(1)防止因局部温度过高,造成蒸发液飞溅;(2)无法确定;(3)生成NaCl,引入新的杂质.点评:
本题考点: 氯化钠与粗盐提纯;溶液的酸碱度测定;盐的化学性质.
考点点评: 进行物质除杂时,要根据物质的性质进行,可以采用物理或化学方法,要求选用的除杂试剂反应后不能产生新的杂质且不能与原有物质反应,pH试纸在使用时不能润湿.1年前查看全部
- (2013•信阳一模)我们的衣、食、住、行中蕴含着丰富的化学知识.下列说法不正确的是( )
(2013•信阳一模)我们的衣、食、住、行中蕴含着丰富的化学知识.下列说法不正确的是( )
A.食用加碘食盐和强化铁酱油可补充某些人体必需微量元素
B.建造高楼大厦时所用到的钢和生铁属于铁的两种合金
C.衣料中的棉、羊毛等都属于合成有机高分子材料
D.吃松花蛋时,为消除松花蛋中所含碱性物质的涩味,可加入少量食醋 35514671年前1
35514671年前1 -
 小笔芯子 共回答了19个问题
小笔芯子 共回答了19个问题 |采纳率100%解题思路:A、依据铁碘对人体的作用分析解答;
B、依据铁的重要合金-钢和生铁分析判断;
C、依据棉花、羊毛是天然纤维分析判断;
D、依据酸碱反应分析解答;A、铁、碘两种元素均是人体必须的微量元素,因此加碘食盐因含碘和铁强化酱油因含铁都可补充这两种微量元素,故说法正确;
B、生铁和钢是铁的两种最重要合金,故说法正确;
C、衣料中的棉花、羊毛是天然纤维,故说法错误;
D、吃松花蛋时,为消除松花蛋中所含碱性物质的涩味,利用酸碱中和反应,可加入少量食醋和碱性物质反应,故说法正确.
故选C.点评:
本题考点: 人体的元素组成与元素对人体健康的重要作用;合金与合金的性质;中和反应及其应用;有机高分子材料的分类及鉴别.
考点点评: 此题是化学与生活相关问题的考查,解题的关键是利用化学知识对相关问题作出正确的分析.1年前查看全部
- (2013•信阳二模)X、Y、Z、W有如图所示的转化关系,已知焓变:△H=△H1+△H2,则X、Y可能是
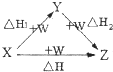 (2013•信阳二模)X、Y、Z、W有如图所示的转化关系,已知焓变:△H=△H1+△H2,则X、Y可能是
(2013•信阳二模)X、Y、Z、W有如图所示的转化关系,已知焓变:△H=△H1+△H2,则X、Y可能是
①C、CO;②AlCl3、Al(OH)3;
③Fe、Fe(NO3)2;④FeBr2、FeBr3;( )
A.①②③
B.①②
C.③④
D.①②③④ 李逸姝1年前1
李逸姝1年前1 -
 抹谷奇遇 共回答了18个问题
抹谷奇遇 共回答了18个问题 |采纳率94.4%①为C
氧气
CO
氧气
CO2的转化,C
氧气
CO2的转化,符合△H=△H1+△H2,故选;
②为AlCl3
NaOH
Al(OH)3
NaOH
NaAlO2,AlCl3
NaOH
NaAlO2的转化,符合△H=△H1+△H2,故选;
③为Fe
硝酸
Fe(NO3)2
硝酸
Fe(NO3)3,Fe
硝酸
Fe(NO3)3,符合△H=△H1+△H2,故选;
④FeBr2
少量Cl2
FeBr3
Cl2
FeCl3、Br2,FeBr2
足量Cl2
FeCl3、Br2,符合△H=△H1+△H2,故选,
以上反应符合有①②③④,
故选D.1年前查看全部
- (2014•信阳二模)“烧芭”(焚烧芭蕉树)是一种传统的农耕文化,在巴西等热带国家盛行.火山喷发是一种自然现象,喷发的岩
(2014•信阳二模)“烧芭”(焚烧芭蕉树)是一种传统的农耕文化,在巴西等热带国家盛行.火山喷发是一种自然现象,喷发的岩浆所到之处寸草不生.甲地发生过“烧芭”现象、乙地发生过火山喷发现象,之后两地均发生了群落的自然演替.关于甲、乙两地群落演替的叙述,错误的是( )
A.甲、乙两地发生的演替类型不同
B.如有人为因素的干扰,甲地不可能恢复到焚烧前的地貌
C.地衣会比苔藓更早地出现在乙地的火山岩上
D.甲、乙两地随着时间延长,生物多样性都能逐渐增多 s8iis111年前1
s8iis111年前1 -
 redsunmen 共回答了19个问题
redsunmen 共回答了19个问题 |采纳率89.5%解题思路:初生演替指在一个从来没有植被覆盖的地面,或者原来存在植被,但是被彻底消灭了的地方发生的演替,如在沙丘、火山岩、冰川泥进行的演替.
次生演替指在原有植被虽已不存在,但原有土壤条件基本保留,甚至还保留了植物的种子或其他繁殖体(如能发芽的地下茎)的地方发生的演替,如火灾后的草原、过量砍伐的森林、弃耕的农田上进行的演替.A、甲地进行的是次生演替,乙地进行的是初生演替,两地演替类型不同,A正确;
B、人类活动往往会使群落演替按照不同于自然演替的速度和方向进行,人为的干扰可使甲地恢复到焚烧前的地貌,B错误;
C、裸岩上群落的演替过程中先驱物种是地衣,地衣分泌有机酸加速岩石风化形成土壤,并积累有机物,这为其他生物的生长提供了条件,C正确;
D、演替的趋势使生物数量越来越多,种类越来越丰富,群落的结构也越来越复杂,稳定性增强,D正确.
故选:B.点评:
本题考点: 群落的演替.
考点点评: 本题考查群落的演替,要求学生能区分初生演替和次生演替、理解演替的过程和演替的结果.1年前查看全部
- (2011•信阳二模)固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3,某同学设计并进行实验对该
(2011•信阳二模)固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3,某同学设计并进行实验对该混合物进行分离,以得到纯净的AlCl3和FeCl3,图甲是该同学设计并进行的实验:
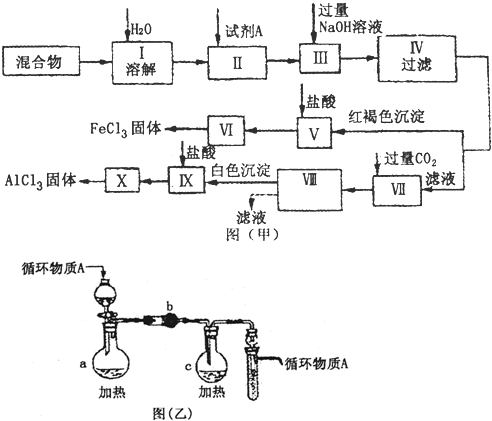
(1)实验操作Ⅱ需加入适宜的试剂,你认为最好选用的试剂是______.
A.KMnO4(H+)溶液B.硝酸C.H2O2 D.浓硫酸
(2)操作V的离子方程式为______;操作Ⅶ的离子方程式为______.
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置(铁架台、加热装置等已略去).
①图乙中,装置a由______、圆底烧瓶、双孔塞和导管组成.
②循环物质A是______.
③装置b中填充的物质可以是______(填编号).
A.碱石灰B.无水氯化钙C.浓硫酸D.五氧化二磷
(4)你认为该同学的实验最后______(填“能”或“不能”)得到纯净的AlCl3和FeCl3.若不能,请你完善该同学的实验步骤设计(用文字叙述):______.(若能,此空不填) hellfire1681年前1
hellfire1681年前1 -
 灵色 共回答了24个问题
灵色 共回答了24个问题 |采纳率91.7%解题思路:由流程可知,混合物溶解后,加试剂A将亚铁离子氧化为铁离子,A为过氧化氢,然后加过量NaOH,过滤后得ⅤⅡ中含硫酸钠、偏铝酸钠,V为Fe(OH)3,Ⅵ为氯化铁溶液,Ⅶ中通入二氧化碳,得到的IX为Al(OH)3,X为氯化铝溶液,以此来解答.由流程可知,混合物溶解后,加试剂A将亚铁离子氧化为铁离子,A为过氧化氢,然后加过量NaOH,过滤后得ⅤⅡ中含硫酸钠、偏铝酸钠,V为Fe(OH)3,Ⅵ为氯化铁溶液,Ⅶ中通入二氧化碳,得到的IX为Al(OH)3,X为氯化铝溶液,
(1)由上述分析可知,氧化亚铁离子不能引入新杂质,只有C符合,故答案为:C;
(2)操作V中加盐酸,该离子方程式为3H++Fe(OH)3═Fe3+3H2O,操作Ⅶ通入二氧化碳,该离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:3H++Fe(OH)3═Fe3+3H2O;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
(3)图乙是操作Ⅵ、X制取无水FeCl3、AlCl3的部分装置,
①由图可知,a为分液漏斗,故答案为:分液漏斗;
②因FeCl3、AlCl3水解生成盐酸易挥发,应在通HCl气流中蒸发,则循环物质为HCl,故答案为:HCl;
③为干燥管,起干燥作用,应为固体干燥剂,且不与HCl反应,只有B、D符合,故答案为:BD;
(4)由流程可知,生成的沉淀没有洗涤,可能混有其它离子,则应在溶解沉淀前洗涤沉淀,所以不能得到纯净的AlCl3和FeCl3,
故答案为:不能;在溶解沉淀前洗涤沉淀.点评:
本题考点: 物质的分离、提纯的基本方法选择与应用;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查物质的分离、提纯,把握流程中各步发生的反应及操作为解答的关键,注意过滤后的沉淀可能不纯及盐类水解应用,题目难度不大.1年前查看全部
- (2013•信阳二模)为确定下列置于空气中的物质是否变质,所选检验试剂(括号内)不能达到目的是( )
(2013•信阳二模)为确定下列置于空气中的物质是否变质,所选检验试剂(括号内)不能达到目的是( )
A.NaOH固体(盐酸)
B.FeCl2溶液(KSCN溶液)
C.KI(淀粉溶液)
D.Na2SO3溶液(氯化钡溶液) panda10101年前1
panda10101年前1 -
 sujiawen 共回答了20个问题
sujiawen 共回答了20个问题 |采纳率75%解题思路:A.变质混有碳酸钠;
B.变质混有铁离子;
C.变质后生成碘单质;
D.变质混有硫酸根离子.A.变质混有碳酸钠,加盐酸生成气体,而NaOH不能,可鉴别是否变质,故A正确;
B.变质混有铁离子,加KSCN溶液,溶液变为红色,而亚铁离子不能,可鉴别是否变质,故B正确;
C.变质后生成碘单质,加淀粉溶液变蓝,而KI不能,可鉴别是否变质,故C正确;
D.变质混有硫酸根离子,亚硫酸根离子、硫酸根离子均与氯化钡溶液反应生成白色沉淀,现象相同,不能鉴别是否变质,故D错误;
故选D.点评:
本题考点: 物质的检验和鉴别的基本方法选择及应用.
考点点评: 本题以物质的变质考查物质的检验,把握发生的化学反应及变质后的生成物为解答的关键,注意离子检验方法及检验中的现象,题目难度不大.1年前查看全部
- (2009•信阳一模)美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是( )
(2009•信阳一模)美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是( )
A.氢铝化合物与水反应生成氢氧化铝和氢气
B.氢铝化合物中铝元素显+3价,氢元素显-1价
C.铝与水蒸气在高温下反应生成氢铝化合物
D.氢铝化合物具有强还原性 関西看板娘1年前1
関西看板娘1年前1 -
 vvvvvv 共回答了19个问题
vvvvvv 共回答了19个问题 |采纳率84.2%解题思路:氢铝化合物性质不稳定能和水反应生成氢氧化铝和氢气,在氧化还原反应中氢铝化合物体现还原性;在化合物中电负性大的显负价,电负性小的元素显正价,据此解答.A.氢铝化合物中氢元素显负价,性质不稳定,易和水反应生成氢氧化铝和氢气而体现还原性,故A正确;
B.在化合物中电负性大的显负价,电负性小的元素显正价,氢元素的电负性大于铝元素,氢铝化合物中铝元素显+3价,氢元素显-1价,故B正确;
C.氢铝化合物易和水反应,所以不能用铝和水蒸气反应制取氢铝化合物,故C错误;
D.氢铝化合物中氢元素显-1价,性质不稳定,易失电子而具有强还原性,故D正确;
故选C.点评:
本题考点: 镁、铝的重要化合物.
考点点评: 本题以铝为载体考查铝的化合物的性质,根据元素电负性、元素化合价和性质的关系来分析解答即可,难度不大.1年前查看全部
- (2012•信阳二模)下列物质中的杂质(括号内为杂质)的检验、除杂的试剂或方法正确的是( )
(2012•信阳二模)下列物质中的杂质(括号内为杂质)的检验、除杂的试剂或方法正确的是( )
物质及其杂质 检验 除杂 A Cl2(HCl) 湿润的淀粉KI试纸 饱和食盐水 B NaHCO3溶液(Na2CO3) Ca(OH)2溶液 过量CO2 C CO2(HCl) AgNO3溶液(含稀硝酸) 饱和Na2CO3溶液 D NO(NO2) 观察颜色或湿润的淀粉KI试纸 水
A.A
B.B
C.C
D.D guangcheny1年前1
guangcheny1年前1 -
 xinghuaking 共回答了22个问题
xinghuaking 共回答了22个问题 |采纳率95.5%解题思路:A.检验HCl应先分离,再检验,用湿润的淀粉KI试纸不能检验HCl;
B.加入Ca(OH)2溶液,NaHCO3和Na2CO3都反应;
C.CO2和HCl都与饱和碳酸钠溶液反应;
D.NO2与水反应生成NO和硝酸.A.湿润的淀粉KI试纸只能检验氯气,不能检验HCl,故A错误;
B.NaHCO3和Na2CO3都与Ca(OH)2溶液反应生成沉淀,不能用来检验,可用氯化钙溶液检验,故B错误;
C.CO2和HCl都与饱和碳酸钠溶液反应,应用饱和碳酸氢钠溶液分离,故C错误;
D.NO2与水反应生成NO和硝酸,可用水除杂,故D正确.
故选D.点评:
本题考点: 物质的分离、提纯的基本方法选择与应用.
考点点评: 本题考查物质的分离、提纯和检验,题目难度中等,注意把握相关物质的性质,根据性质的异同选择实验方法.1年前查看全部
- (2012•信阳一模)已知集合A={y|y=x2-1,x∈R},B={x|log23x>0},则A∩B=( )
(2012•信阳一模)已知集合A={y|y=x2-1,x∈R},B={x|log
x>0},则A∩B=( )2 3
A.{x|x>1}
B.{x|0<x<1}
C.{x|-1≤x<1}
D.{x|x<-1或x>1} 凡间女孩1年前1
凡间女孩1年前1 -
 九阳丹棘 共回答了26个问题
九阳丹棘 共回答了26个问题 |采纳率84.6%解题思路:求二次函数的值域得到集合A,解对数不等式求出集合B,再根据两个集合的交集的定义求出A∩B.集合A={y|y=x2-1,x∈R}={y|y≥-1},B={x|log
2
3x>0}={x|0<x<1},
∴A∩B=[-1,+∞)∩(0,1)=(0,1),
故选B.点评:
本题考点: 指、对数不等式的解法;交集及其运算.
考点点评: 本题主要考查对数不等式的解法,二次函数的值域的求法,两个集合的交集的定义,属于基础题.1年前查看全部
- (2012•信阳二模)下列表述中正确的是( )
(2012•信阳二模)下列表述中正确的是( )
A.任何能使熵值减小的过程都能自发进行
B.已知热化学方程式2SO2(g)+O2(g)⇌2SO3(g),△H=-Q kJ•mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
C.1mol NaOH分别和1mol CH3COOH、1mol HNO3反应,后者比前者△H小
D.在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在SO2−4 ddmajia011年前1
ddmajia011年前1 -
 挑水和尚 共回答了18个问题
挑水和尚 共回答了18个问题 |采纳率100%解题思路:A.反应能否自发进行取决于焓变和熵变的综合判据;
B.反应为可逆反应,不能完全反应;
C.弱酸发生中和反应时,由于弱酸电离吸热,所以放出热量偏小;
D.没有绝对不溶的物质.A.反应能否自发进行取决于焓变和熵变的综合判据,所以不能单独根据熵变判断反应的自发性,故A错误;
B.反应为可逆反应,不能完全反应,将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出的热量小于Q kJ,故B错误;
C.弱酸发生中和反应时,由于弱酸电离吸热,所以放出热量偏小,由于△H为负值,所以1mol NaOH分别和1mol CH3COOH、1molHNO3反应,后者比前者△H小,故C正确;
D.没有绝对不溶的物质,Na2SO4溶液中加入过量的BaCl2后,溶液中存在SO42-,只是浓度很小,故D错误;
故选:C.点评:
本题考点: 焓变和熵变;热化学方程式;反应热的大小比较.
考点点评: 本题考查反应热与焓变,可逆反应的特点,物质的溶解性等,涉及知识点较多,题目难度不大.1年前查看全部
- (2011•信阳二模)某种植物细胞在浓度分别为200mmol•L-1和400mmol•L-1的小分子物质M溶液中,细胞吸
(2011•信阳二模)某种植物细胞在浓度分别为200mmol•L-1和400mmol•L-1的小分子物质M溶液中,细胞吸收M的速率都是10mmol•min-1.对此结果最合理的解释是( )
A.细胞吸收M的方式为自由扩散
B.细胞吸收M的方式为主动运输
C.细胞吸收M需要载体蛋白的参与
D.细胞吸收M物质时所需能量供应不足 开拓85271年前1
开拓85271年前1 -
 峰_god 共回答了32个问题
峰_god 共回答了32个问题 |采纳率87.5%解题思路:物质浓度(在一定浓度范围内)影响运输速率的曲线: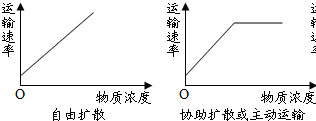
A、自由扩散的动力是浓度差,与外界溶液成正比,与题意中“在浓度分别为200mmol∕L和400mmol∕L的M物质溶液中,细胞吸收M的速率都是10mmol∕min”不符合,A错误;
B、根据题意可知,物质运输的速率与细胞外浓度无关,这可能是由于受到载体蛋白的限制,可能是主动运输,也可能是协助扩散,B错误;
C、“200mmol∕L和400mmol∕L的M物质溶液中,细胞吸收M的速率都是10mmol∕min”,说明物质M运输受到载体数量的限制,C正确;
D、在协助扩散过程中,不需要消耗能量,D错误.
故选:C.点评:
本题考点: 物质跨膜运输的方式及其异同.
考点点评: 本题考查物质跨膜运输的相关知识,意在考查考生能够从题干中获取相关解题信息,并且通过题干的分析明确该物质的运输速率受到载体蛋白的限制,识记主动运输和协助扩散均需要载体蛋白,难度适中.1年前查看全部
- (2013•信阳一模)酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙
 (2013•信阳一模)酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)
(2013•信阳一模)酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)
(1)______;
(2)______;
(3)______. 紫苋1年前1
紫苋1年前1 -
 leilim 共回答了19个问题
leilim 共回答了19个问题 |采纳率78.9%解题思路:根据图象中pH值的变化关系,确定甲乙溶液的名称,并根据图象变化及相关知识确定获得的信息.图象中的pH值的起点小于7,说明甲溶液显酸性,为盐酸,则乙是氢氧化钠溶液;随着加入的乙的量的增加,pH值逐渐增大,与7相交的地方即c点pH值为7,二者恰好中和;
故答案为:(1)甲是盐酸;(2)乙是氢氧化钠溶液;(3)c点表示两溶液恰好中和,c点的pH为7;反应前溶液的pH小于7,随着乙溶液的加入,溶液的pH逐渐增大.(其他合理答案均可).点评:
本题考点: 中和反应及其应用.
考点点评: 本题主要考查了学生依据溶液的pH值变化并结合图象分析、解决问题的能力,难度适中,开放性强.1年前查看全部
- (2011•信阳二模)如图所示,竖直平面上有相互垂直的匀强电场和匀强磁场,电场强度E1=2500N/C,方向竖直向上;磁
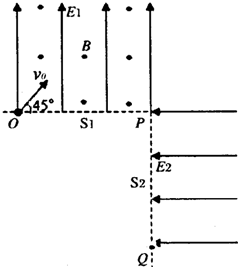 (2011•信阳二模)如图所示,竖直平面上有相互垂直的匀强电场和匀强磁场,电场强度E1=2500N/C,方向竖直向上;磁感应强度B=103T,方向垂直纸面向外;有一质量m=1×10-2kg、电荷量q=4×10-5C的带正电小球自O点沿与水平线成45°以v0=4m/s的速度射入复合场中,之后小球恰好从P点进入电场强度E2=2500N/C,方向水平向左的第二个匀强电场中.不计空气阻力,g取10m/s2.
(2011•信阳二模)如图所示,竖直平面上有相互垂直的匀强电场和匀强磁场,电场强度E1=2500N/C,方向竖直向上;磁感应强度B=103T,方向垂直纸面向外;有一质量m=1×10-2kg、电荷量q=4×10-5C的带正电小球自O点沿与水平线成45°以v0=4m/s的速度射入复合场中,之后小球恰好从P点进入电场强度E2=2500N/C,方向水平向左的第二个匀强电场中.不计空气阻力,g取10m/s2.
求:(1)O点到P点的距离s1;
(2)小球经过P点的正下方Q点时与P点的距离s2. fenzaifei1年前1
fenzaifei1年前1 -
 F人生 共回答了20个问题
F人生 共回答了20个问题 |采纳率95%解题思路:(1)粒子在复合场中电场力和重力平衡,则只在洛仑兹力的作用下做匀速圆周运动,由牛顿第二定律可知粒子的半径,由几何关系可得出两点间的距离;
(2)粒子在电场中,由于重力和电场力的作用做类平抛运动,建立合适的坐标系,则可由运动的合成与分解求得两点间的距离.(1)带电小球在正交的匀强电场和匀强磁场中受到重力G=mg=0.1N;
电场力F1=Eq=0.1N
即G=F1,故小球在正交的电场由A到C做匀速圆周运动.
根据牛顿第二定律可知Bqv0=m
v20
R
解得:R=
mv0
Bq=1m
由几何关系得:s1=
2R=
2m;
(2)带电小球在C点的速度大小仍为v0=4m/s,方向与水平方向成45°.
由于电场力F2=Eq=0.1N
与重力大小相等,方向相互垂直,
则合力的大小为F=0.1
2N,方向与初速度垂直,故小球在第二个电场中作平抛运动.
建立如图所示的坐标系,沿y方向上,小球的加速度a=[F/m]=10
2m/s2;
位移y=[1/2]at2
x方向上有小球的位移x=v0t
由几何关系可知:y=x
即[1/2]at2=v0t,
解得:t=0.4
2s
由几何关系可知,Q到P点的距离为s2=
2点评:
本题考点: 带电粒子在匀强磁场中的运动;牛顿第二定律;带电粒子在匀强电场中的运动.
考点点评: 本题考查带电粒子在复合场中的运动,要注意当粒子在复合场中做匀速 圆周运动时,粒子受到的电场力与重力平衡.1年前查看全部
- (2012•信阳一模)已知函数f(x)=|x-a|.
(2012•信阳一模)已知函数f(x)=|x-a|.
(Ⅰ)若不等式f(x)≤3的解集为{x|-1≤x≤5},求实数a的值;
(Ⅱ)在(Ⅰ)的条件下,求y=f(x)+f(x+5)的最小值. tuq5201年前1
tuq5201年前1 -
 vv幽灵zoooqq 共回答了15个问题
vv幽灵zoooqq 共回答了15个问题 |采纳率100%解题思路:(I)根据含有绝对值不等式的解法法则,可得解集关于常数a的式子,再结合题意比较两解集的区间端点值,即可得到实数a的值;
(II)由(I)得y=f(x)+f(x+5)=|x-2|+|x+3|,利用绝对值不等式的性质,即可求出当-3≤x≤2时,函数的最小值为5.(I)∵|x-a|≤3等价于-3≤x-a≤3,解之得a-3≤x≤a+3.
∴
a−3=−1
a+3=5,解得a=2
(II)∵a=2,f(x)=|x-2|.
∴y=g(x)=f(x)+f(x+5)=|x-2|+|x+3|
∵|x-2|+|x+3|≥|(x-2)-(x+3)|=5
∴当-3≤x≤2时,g(x)=|x-2|+|x+3|的最小值为5.点评:
本题考点: 带绝对值的函数;函数的最值及其几何意义.
考点点评: 本题给出含有绝对值的数,叫我们解关于x的不等式并求另一个函数的最小值,着重考查了带绝对值函数问题的处理方法和函数最值的意义等知识,属于基础题.1年前查看全部
- (2011•信阳二模)人类X染色体和Y染色体大小、形态不完全相同,但是存在着同源区(Ⅱ)和非同源区(Ⅰ、Ⅲ),如图所示.
 (2011•信阳二模)人类X染色体和Y染色体大小、形态不完全相同,但是存在着同源区(Ⅱ)和非同源区(Ⅰ、Ⅲ),如图所示.若等位基因都具有显隐性关系,下列有关叙述错误的是( )
(2011•信阳二模)人类X染色体和Y染色体大小、形态不完全相同,但是存在着同源区(Ⅱ)和非同源区(Ⅰ、Ⅲ),如图所示.若等位基因都具有显隐性关系,下列有关叙述错误的是( )
A.Y染色体Ⅱ片段上显性基因控制的遗传病,男性患病率高于女性
B.Ⅱ片段上基因控制的遗传病,男性患病率可能等于女性患病率
C.Ⅲ片段上基因转移到X染色体上是染色体增加
D.Y染色体Ⅱ片段上的基因若转移到X染色体上的原因可能是染色体结构变异 4364831年前1
4364831年前1 -
 古渡夕阳 共回答了22个问题
古渡夕阳 共回答了22个问题 |采纳率95.5%解题思路:根据题意和图示分析可知:I片段上是位于X染色体上的非同源区段,隐性基因控制的遗传病为伴X染色体隐性遗传病,男性患病率高于女性;同源区段Ⅱ上存在等位基因,Ⅱ片段上基因控制的遗传病,男性患病率可能不等于女必性;Ⅲ片段是位于Y染色体上的非同源区段,Ⅲ片段上基因控制的遗传病为伴Y遗传,患病者全为男性.A、Y染色体Ⅱ片段上显性基因控制的遗传病,后代男性都患病,所以男性患病率高于女性,A正确;
B、Ⅱ片段是X和Y染色体的同源区,其上的单基因遗传病,男女患病率不一定相等,如①XaXa×XaYA后代所有显性个体均为男性,所有隐性个体均为女性;②XaXa×XAYa后代所有显性个体均为女性,所有隐性个体均为男性;③XAXa×XaYa后代男性患病率等于女性患病率,B正确;
C、Ⅲ片段上基因转移到X染色体上是染色体结构变异,相当于易位,染色体没有增加,C错误;
D、Y染色体Ⅱ片段上的基因若转移到X染色体上的原因可能是染色体结构变异,D正确.
故选:C.点评:
本题考点: 伴性遗传;染色体结构变异和数目变异.
考点点评: 本题以性染色体为素材,结合性染色体图,考查伴性遗传的相关知识,重点考查伴X染色体遗传病、伴Y染色体遗传病和X、Y同源区段基因控制的遗传病,特别是X、Y同源区段基因控制的遗传病,要求学生理解相关遗传病的发病情况,能举例说明,并作出准确的判断.1年前查看全部
- (2009•信阳一模)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在
(2009•信阳一模)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在形成的化学键中成为带负电荷的一方,下面是某些短周期元素的x值;
(1)推测x值与原子半径的关系是______;元素素素素 Li Be B C O F x值 0.98 1.57 2.04 2.55 3.44 3.98 元素 Na Al Si P S Cl x值 0.93 1.61 1.90 2.19 2.58 3.16
(2)某有机化合物结构式为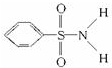 ,其中S-N中,你认为共用电子对偏向______.
,其中S-N中,你认为共用电子对偏向______.
(3)经验规律告诉我们:当成键的两原子相应元素的x差值(△x)即△x>1.7时,一般为离子键,△x<1.7,一般为共价键,试推断:BeCl3中化学键类型是______.
(4)预测元素周期表中x值最小的元素的位置______(放射性元素除外). pianzhou1141年前1
pianzhou1141年前1 -
 八号砖头 共回答了22个问题
八号砖头 共回答了22个问题 |采纳率90.9%解题思路:(1)根据电负性和原子半径在周期表中的递变规律判断;
(2)根据元素的电负性越强,原子吸电子能力越强分析;
(3)根据元素点和性大小计算两种元素的电负性差值,以此判断化合物的类型;
(4)根据电负性的递变规律判断.(1)同一周期周期从左到右,元素的电负性逐渐增大,半径逐渐减小,同一主族从上到下,元素的电负性逐渐减小,原子半径逐渐增大,所以同周期(同主族)中,x值越大,其原子半径越小,体现了元素性质的周期性变化的规律,故答案为:原子半径越小,x值越大;
(2)N元素的电负性大于S元素,吸电子能力较强,则在S-N中,电子对偏向于N元素,故答案为:N原子;
(3)BeCl3中,Be元素的电负性为1.57,Cl元素的电负性小于3.16,则二者差值小于1.7,BeCl3中化学键类型为共价键,故答案为:共价键;
(4)根据同一周期周期从左到右,元素的电负性逐渐增大,同一主族从上到下,元素的电负性逐渐减小,则电负性最小的元素应位于周期表的左下角,排除放射性元素,应为Cs元素,位于第六周期IA族,故答案为:第六周期,第IA族.点评:
本题考点: 共价键的形成及共价键的主要类型;原子结构与元素的性质.
考点点评: 本题考查电负性的递变规律,题目难度中等,注意元素周期律的主要内容,理解电负性的意义和应用.1年前查看全部
- (2014•信阳二模)近来的科学研究发现,小鼠体内HMIGIC基因与肥胖直接相关.具有HMGIC基因缺陷的实验鼠与作为对
(2014•信阳二模)近来的科学研究发现,小鼠体内HMIGIC基因与肥胖直接相关.具有HMGIC基因缺陷的实验鼠与作为对照的小鼠,吃同样多的高脂肪食物,一段时间后,对照组小鼠变得十分肥胖,而具有HMGIC基因缺陷的实验鼠体重仍然保持正常,说明( )
A.基因在DNA上
B.基因在染色体上
C.基因具有遗传效应
D.DNA具有遗传效应 egwar1年前1
egwar1年前1 -
 zw312 共回答了17个问题
zw312 共回答了17个问题 |采纳率82.4%解题思路:分析题干给出的信息可知,同样摄食的情况下,具有HMIGIC基因的小鼠肥胖,具有HMGIC基因缺陷的实验鼠体重正常,这说明肥胖这一性状是由HMGIC基因决定的.A、该题干中没有涉及基因和DNA的关系,A错误;
B、该题干没有涉及染色体与基因的关系,B错误;
C、由题干信息可知,肥胖这一性状是由HMGIC基因决定的,说明基因具有遗传效应,C正确;
D、该实验的研究对象是基因,不是DNA,D错误.
故选:C.点评:
本题考点: 基因与DNA的关系.
考点点评: 通过具体材料理解基因的概念是本题考查的重点.1年前查看全部
大家在问
- 1my weekend 先填写下面的表格然后根据表格信息写一篇英语作文
- 2some后接______名词和_______名词;many后接_________名词;much后接_________名词
- 3as soon as i hear my alrarm clock,i jump out of my bed 替换成--
- 4英语翻译这个座位太硬以至于不能坐
- 5若ab=-1,则称a与b互为负倒数,那么负倒数是它本身的数有几个?
- 6由()及()、扬()避()
- 7一、用两种方法把下列句子变成被动语态Exampie:He gave me a present -->I was give
- 8曲线y=x3上一点B处的切线l交x轴于点A,△OAB(O是原点)是以A为顶点的等腰三角形,则切线l的倾斜角为( )
- 9我十分感激你的帮助 英文这么写地道吗 I appreciate it thanks for your help
- 10如图,AD为△ABC的中线,BE为△ABD的中线.
- 11英语翻译“顺便说一下,给您邮寄的样品A,工厂没有给批号,如有任何问题,请告知.” 以上这句话译成英文,在邮件中出现时怎样
- 12对幸福的理解,200字左右.
- 13月下独酌中写诗人与月共舞的诗句是
- 14有什么关于张家港美食的作文?谢谢啦
- 15nose到底读[n欧Z]还是[N欧S]?请大哥大姐赐教!
