赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O=6C
 紫色红颜Q2022-10-04 11:39:542条回答
紫色红颜Q2022-10-04 11:39:542条回答A.该反应的氧化剂与还原剂物质的量之比为3:1
B.Cu2S在反应中既是氧化剂,又是还原剂
C.Cu是氧化产物,SO2是还原产物
D.每生成38.4g Cu,反应中转移0.6mol电子

已提交,审核后显示!提交回复
共2条回复
 楼民1号 共回答了22个问题
楼民1号 共回答了22个问题 |采纳率95.5%- Cu2S+2Cu2O=6Cu+SO2↑
铜被还原 氧化剂 Cu2S 2Cu2O
S被氧化 还原剂 Cu2S
A.该反应的氧化剂与还原剂物质的量之比为3:1 正确
B.Cu2S在反应中既是氧化剂,又是还原剂 正确
C.Cu是氧化产物,SO2是还原产物
不正确 铜是氧化剂 被还原 还原产物 SO2是氧化产物
D.每生成38.4g Cu,反应中转移0.6mol电子
38.4g Cu 0.6mol 产生0.1mol SO2 S由-2到+4价 转移0.6mol电子 正确 - 1年前
 gaosha007 共回答了3个问题
gaosha007 共回答了3个问题 |采纳率- 1 38.4gCu全部由+1价Cu吸收0.6mol电子而来,因此D正确;
2 Cu元素从高价变到低价,被还原是还原产物,因此C不正确;
3 Cu2S在反应中有一种元素化合价升高有一种元素化合价降低,因此它既是氧化剂,又是还原剂
所以B正确;
4 有2mol的Cu2O和1mol的Cu2S作为氧化剂,有1mol的Cu2S作为还原剂,所以A正确... - 1年前
相关推荐
- 将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄
将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄金”的组成进行了以下探究.
[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物.
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成作了以下三种猜想:
猜想①可能的单质有:C、Zn、Cu
猜想②可能的氧化物有:ZnO、CuO、Cu2O
猜想③可能是单质和氧化物组成的混合物
[论证]乙同学经思考和推理后,首先排除了猜想______(选填①②或③),理由是______.进而再排除了猜想______(选填①②或③);对余下的一种猜想,乙同学又排除了其中的一种物质,依据是______.对余下的两种物质,甲和乙同学用实验鉴定该两种物质确实是“假黄金”的成分. wg026033181年前1
wg026033181年前1 -
 linshi_tmp 共回答了16个问题
linshi_tmp 共回答了16个问题 |采纳率87.5%解题思路:根据ZnCO3高温可分解成金属氧化物;高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质进行分析解答.碳酸锌高温分解的产物之一是氧化锌,与氧化亚铜一起可被过量的碳完全还原为金属,不可能有氧化物存在,而碳在高温时可被氧化为二氧化碳,不可能有碳存在,所以本题答案为:②③,因为C过量,所以可以将氧化物还原成金属.
故答案为:②;因为木炭过量,高温时能将金属氧化物全部还原成金属单质;
③;过量的木炭在高温下可与空气中的氧气反应生成CO2或CO.点评:
本题考点: 实验探究物质的组成成分以及含量.
考点点评: 本题考查了金属氧化物与碳的还原反应以及常见金属的化学性质,完成此题,可以依据课本已有的知识进行知识的迁移.所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.1年前查看全部
- (2005•佛山)将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金
(2005•佛山)将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄金”的组成进行了以下探究.
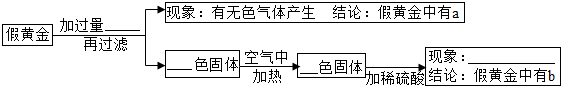
[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;
ZnCO3高温可分解成两种氧化物.
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成作了以下三种猜想:
猜想①可能是单质:C、Zn、Cu
猜想②可能是氧化物:ZnO、CuO、Cu2O
猜想③可能是单质和氧化物组成的混合物
[论证](1)乙同学经过思考和推理后,首先排除了其中的两个猜想______(填①②③序号),理由是______;对余下的一种猜想,乙同学又排除了其中的一种物质,依据是C+O2
CO2点燃 .C+O2.
CO2点燃 .
(2)对余下的两种物质(ab代表),甲和乙同学利用下列实验方案进行验证:______;
(3)写出上述实验过程中发生反应的任意一个化学方程式______;
[结论与应用](4)“假黄金”的成分中a为______;b为______;
生活中真假黄金的鉴别,可采用的一种方法是(要求写出操作、现象和结论)______. hh与馒头的故事1年前1
hh与馒头的故事1年前1 -
 寸长大爷 共回答了14个问题
寸长大爷 共回答了14个问题 |采纳率100%解题思路:ZnCO3高温可分解成两种氧化物,其中一种为氧化锌,生成的氧化锌和赤铜矿(Cu2O)和过量的炭混合后,高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质,锌和铜均在铝的后面,故能全部被还原为金属,得到的锌在氢前,可与酸发生置换反应产生氢气,而铜在氢后,不能与酸发生置换反应生成氢气.(1)碳酸锌高温分解的产物之一是氧化锌,与氧化亚铜一起可被过量的碳完全还原为金属,不可能有氧化物存在,而碳在高温时可被氧化为二氧化碳,不可能有碳存在,所以本题答案为:②③,因为C过量,所以可以将氧化物还原成金属,
C+O2
点燃
.
CO2;
(2)生成的锌在氢前,可与酸发生置换反应产生氢气,而铜在氢后,不能与酸发生置换反应生成氢气,所以可使用HCl进行验证,所以本题答案为:HCl;
(3)加盐酸有气体产生,则是锌与盐酸反应,所以本题答案为:Zn+2HCl═ZnCl2+H2↑;
(4)加入盐酸有气泡产生说明含a,则a为锌,故b为铜,假黄金中含 锌,可与酸反应产生氢气,而真黄金不与酸发生置换反应,所以可采用加酸的方法验证,所以本题答案为:Zn,Cu,加稀盐酸,能与稀盐酸反应产生气体则为假黄金,不能与稀盐酸反应则为真黄金.点评:
本题考点: 金属活动性顺序及其应用;实验探究物质的组成成分以及含量;碳的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了金属氧化物与碳的还原反应以及常见金属的化学性质,完成此题,可以依据课本已有的知识进行知识的迁移.所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.1年前查看全部
- 将碳酸锌,氧化亚铜(赤铜矿),木炭投入炉中冶炼药金,该过程的相关方程式是什么?
将碳酸锌,氧化亚铜(赤铜矿),木炭投入炉中冶炼药金,该过程的相关方程式是什么?
题目让写出该过程体现的三个方程式 古纱1年前1
古纱1年前1 -
 我是创口贴 共回答了15个问题
我是创口贴 共回答了15个问题 |采纳率93.3%ZnCO3+Cu2O+C=加热=Zn+2Cu+2CO2↑
生成铜锌合金,即药金(假黄金)1年前查看全部
- 冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO3)、赤铜矿(主要成分为Cu2O)和木炭粉混合加热至800 ℃左
冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO3)、赤铜矿(主要成分为Cu2O)和木炭粉混合加热至800 ℃左右,即可得到金光闪闪与黄金外观相似的“药金”.
请写出上述过程中发生反应的化学方程式:_________________ bester2101年前1
bester2101年前1 -
 春节 共回答了12个问题
春节 共回答了12个问题 |采纳率83.3%ZnCO3=ZnO+CO2
ZnO+C=Zn+CO
Cu2O+C=2Cu+CO1年前查看全部
- 赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合物加热有以下反应发生:2Cu2O+Cu2S
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合物加热有以下反应发生:2Cu2O+Cu2S
6Cu+SO2↑,填写下列空白:△ .
①在该反应中,氧化剂是______.还原剂是______.
②氧化产物与还原产物的质量比是______. 叫我小公主1年前1
叫我小公主1年前1 -
 xiao0z 共回答了18个问题
xiao0z 共回答了18个问题 |采纳率83.3%解题思路:该反应2Cu2O+Cu2S
6Cu+SO2↑中,Cu元素化合价由+1价变为0价,S元素化合价由-2价变为+4价,得电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂,氧化产物是SO2、还原产物是Cu.△ .①该反应2Cu2O+Cu2S
△
.
6Cu+SO2↑中,Cu元素化合价由+1价变为0价,S元素化合价由-2价变为+4价,所以氧化剂是Cu2O、Cu2S,还原剂是Cu2S,故答案为:Cu2O、Cu2S;Cu2S;
②氧化产物是SO2、还原产物是Cu,根据方程式知,氧化产物和还原产物的物质的量之比为1:6,故答案为:1:6.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应,明确物质中元素化合价是解本题关键,再结合基本概念解答即可,注意Cu2O、Cu2S中Cu元素为+1价,为易错点.1年前查看全部
- 几条化学计算题1 .5000t含磁铁矿(Fe2O3)84%的赤铜矿理论上可练得含铁98%的生铁是多少t 2.若某冶炼厂日
几条化学计算题
1 .5000t含磁铁矿(Fe2O3)84%的赤铜矿理论上可练得含铁98%的生铁是多少t 2.若某冶炼厂日产含碳3%的生铁300t,该厂每天需要含氧化铁80%的赤铁石多少吨?3.某炼钢厂日产含杂质5%的生铁3000t,该炼铜厂每天需要含Fe2O3质量分数为85%的赤铁矿石多少吨(保留整数) 一米阳光8071年前1
一米阳光8071年前1 -
 武士猪 共回答了20个问题
武士猪 共回答了20个问题 |采纳率90%1 Fe2O3 - 2fe 160 112 5000x84% x x= 2940 2940/98%=3000 2 2fe - fe2o3 112 160 300x0.97 x x=415.7 415.7/0.8=520 3 2fe - fe2o3 112 160 3000x0.95 x x=4071 4071/0.85=47891年前查看全部
- 孔雀石 赤铜矿 辉铜矿 最好选那种冶炼铜
 philpszj1年前2
philpszj1年前2 -
 falcon8305 共回答了25个问题
falcon8305 共回答了25个问题 |采纳率92%孔雀石 CuCO3·Cu(OH)2 铜的质量分数57.7%
赤铜矿 Cu2O 铜的质量分数 88.9%
辉铜矿 Cu2S 铜的质量分数 80%
选择赤铜矿.含铜最多1年前查看全部
- 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O═6C
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O═6Cu+SO2↑,关于该反应的说法中,正确的是( )
A. 该反应的氧化剂只有Cu2O
B. Cu2S在反应中既是氧化剂,又是还原剂
C. Cu既是氧化产物又是还原产物
D. 每生成19.2gCu,反应中转移1.8mol电子 bvvc3341年前3
bvvc3341年前3 -
 fsrhbs 共回答了25个问题
fsrhbs 共回答了25个问题 |采纳率84%解题思路:A、化合价降低的元素所在的反应物是氧化剂;
B、化合价降低的元素所在的反应物是氧化剂;化合价升高的元素所在的反应物是还原剂;
C、氧化剂对应的是还原产物,还原剂对应的是氧化产物;
D、根据转移电子的量来分析生成的金属铜的量.A、反应Cu2S+2Cu2O═6Cu+SO2↑中,化合价降低的元素是铜元素,所在的反应物Cu2S、Cu2O是氧化剂,故A错误;
B、硫化铜中硫元素化合价升高,铜元素的化合价升高,所以Cu2S在反应中既是氧化剂,又是还原剂,故B正确;
C、反应物Cu2S、Cu2O中硫元素化合价降为金属铜中的0价,金属铜为还原产物,故C错误;
D、反应Cu2S+2Cu2O═6Cu+SO2↑中,化合价升高了6价,转移了6mol电子,生成金属铜6mol,所以每生成19.2g(即0.3mol)Cu,反应中转移0.3mol电子,故D错误.
故选B.点评:
本题考点: 氧化还原反应;氧化还原反应的电子转移数目计算.
考点点评: 本题考查学生氧化还原反应中的有关概念和电子转移知识,是一道基本知识题目,难度不大.1年前查看全部
- 将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄
将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,即得金光闪闪的“假黄金”.有同学对“假黄金”的组成进行了以下探究.
[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物.
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成作了以下三种猜想:
猜想①可能的单质有:C、Zn、Cu
猜想②可能的氧化物有:ZnO、CuO、Cu2O
猜想③可能是单质和氧化物组成的混合物
[论证]乙同学经思考和推理后,首先排除了猜想______(选填①②或③),理由是______.进而再排除了猜想______(选填①②或③);对余下的一种猜想,乙同学又排除了其中的一种物质,依据是______.对余下的两种物质,甲和乙同学用实验鉴定该两种物质确实是“假黄金”的成分. augurwang1年前1
augurwang1年前1 -
 freeabcd 共回答了25个问题
freeabcd 共回答了25个问题 |采纳率84%解题思路:根据ZnCO3高温可分解成金属氧化物;高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质进行分析解答.碳酸锌高温分解的产物之一是氧化锌,与氧化亚铜一起可被过量的碳完全还原为金属,不可能有氧化物存在,而碳在高温时可被氧化为二氧化碳,不可能有碳存在,所以本题答案为:②③,因为C过量,所以可以将氧化物还原成金属.
故答案为:②;因为木炭过量,高温时能将金属氧化物全部还原成金属单质;
③;过量的木炭在高温下可与空气中的氧气反应生成CO2或CO.点评:
本题考点: 实验探究物质的组成成分以及含量.
考点点评: 本题考查了金属氧化物与碳的还原反应以及常见金属的化学性质,完成此题,可以依据课本已有的知识进行知识的迁移.所以要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.1年前查看全部
- 赤铜矿的成分是Cu 2 O,辉铜矿的成分是Cu 2 S,将赤铜矿与辉铜矿混合加热有以下反应发生:Cu 2 S+2Cu 2
赤铜矿的成分是Cu 2 O,辉铜矿的成分是Cu 2 S,将赤铜矿与辉铜矿混合加热有以下反应发生:Cu 2 S+2Cu 2 O═6Cu+SO 2 ↑,请填写下列空白:
(1)在该反应中,氧化剂是______.
(2)还原剂是______.
(3)氧化产物与还原产物的质量比______. qddxysh1年前1
qddxysh1年前1 -
 琼秋 共回答了17个问题
琼秋 共回答了17个问题 |采纳率82.4%(1)反应Cu 2 S+2Cu 2 O═6Cu+SO 2 ↑中,化合价降低元素是Cu,所在的反应物Cu 2 S、Cu 2 O是氧化剂,故答案为:Cu 2 S、Cu 2 O;
(2)反应Cu 2 S+2Cu 2 O═6Cu+SO 2 ↑中,化合价升高元素是S,所在的反应物Cu 2 S是还原剂,故答案为:Cu 2 S;
(3)氧化剂Cu 2 S、Cu 2 O对应产物Cu是还原产物,还原剂Cu 2 S对应产物SO 2 是氧化产物,氧化产物与还原产物的质量比是1:6,故答案为:1:6.1年前查看全部
- 赤铜矿的主要成分是氧化亚铜(Cu2O),辉铜矿的主要成分是硫化亚铜(Cu2S),将赤铜矿与辉铜矿混合加热有如下反应:Cu
赤铜矿的主要成分是氧化亚铜(Cu2O),辉铜矿的主要成分是硫化亚铜(Cu2S),将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O=6Cu+SO2↑,下列对于该反应的说法正确的是( )
A.该反应中的氧化剂只有Cu2O
B.Cu既是氧化产物又是还原产物
C.Cu2S在反应中既是氧化剂又是还原剂
D.氧化产物与还原产物的物质的量之比为6:1 绝望的水是冰1年前1
绝望的水是冰1年前1 -
 cento 共回答了17个问题
cento 共回答了17个问题 |采纳率88.2%解题思路:Cu2S+2Cu2O=6Cu+SO2↑ 中,得电子化合价降低的反应物的氧化剂,失电子化合价升高的反应物是还原剂,氧化剂对应的产物的还原产物,还原剂对应的产物是氧化产物,根据得失电子数相等确定氧化产物和还原产物的物质的量之比.A.反应中,Cu2S和Cu2O中的+1价Cu元素得电子生成0价的Cu,所以Cu2S和Cu2O都是氧化剂,故A错误;
B.反应中,+1价Cu元素得电子生成0价的Cu,所以Cu是还原产物,故B错误;
C.硫化铜中硫元素化合价升高,铜元素的化合价升高,所以Cu2S在反应中既是氧化剂,又是还原剂,故C正确;
D.根据Cu2S+2Cu2O=6Cu+SO2↑知,还原产物和氧化产物的物质的量之比是6:1,故D错误;
故选C.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,明确元素化合价是解本题的关键,注意该题中反应物都是氧化剂,但Cu2S还是还原剂,为易错点.1年前查看全部
- 将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”.请
将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”.请你参与课外活动小组的同学对“假黄金”进行探究,并回答有关问题:
提出问题:“假黄金”的化学组成是什么?
查阅资料:高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物.
猜想:①“假黄金”可能由C、Zn、Cu三种单质组成;
②“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成;
③“假黄金”可能是单质和氧化物组成的混合物.
论证:他们经思考和推理后,首先排除了猜想______(选填①②或③),你觉得他们的理由是______.进而再排除了猜想______(选填①②或③).对余下的一种猜想,该同学又排除了其中的一种物质,你认为他们的依据是______.
进行实验:他们用实验鉴定了“假黄金”中所含的两种物质,请将实验过程填入下表中:
得出结论:“假黄金”的化学组成是:______.实验方法 观察到的现象 步骤1 步骤2  fwy88881年前1
fwy88881年前1 -
 蓝色郁忧果 共回答了18个问题
蓝色郁忧果 共回答了18个问题 |采纳率94.4%解题思路:根据ZnCO3高温可分解成金属氧化物;高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质进行分析解答.根据查阅资料:ZnCO3高温可分解成金属氧化物;高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;可推知:
②“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成是不可能的;③“假黄金”可能是单质和氧化物组成的混合物是不可能的;
故答案为:②;高温时炭能将金属氧化物还原成金属;③;
对①“假黄金”可能由C、Zn、Cu三种单质组成的猜想,该同学又排除了其中的一种物质为碳,他们的依据是:过量的炭在高温时能与空气中的氧气反应生成CO或CO2,故答案为:过量的炭在高温时能与空气中的氧气反应生成CO或CO2;
实验方法 观察到的现象
步骤1 用一小烧杯取少量“假黄金”,加入适量稀硫酸 有大量气泡产生
步骤2 将上述反应后的剩余固体置于酒精灯火焰上灼烧 固体表面变黑色“假黄金”的化学组成是:锌和铜的合金.故答案为:锌和铜的合金.点评:
本题考点: 科学探究的基本环节;猜想与事实验证.
考点点评: 本题考查学生根据题中所给信息进行分析解题的能力.1年前查看全部
- 赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S+2Cu2O
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S+2Cu2O
6Cu+SO2↑.对于该反应的下列说法正确的是( )△ .
A.该反应中的氧化剂只有Cu2O
B.Cu2O在反应中既是氧化剂又是还原剂
C.Cu既是氧化产物又是还原产物
D.氧化产物与还原产物的物质的量之比为1:6 箐耧男子1年前1
箐耧男子1年前1 -
 漂亮女人123 共回答了21个问题
漂亮女人123 共回答了21个问题 |采纳率90.5%解题思路:反应Cu2S+2Cu2O
6Cu+SO2↑,反应中Cu元素化合价降低,S元素化合价升高,根据元素化合价的变化解答该题.△ .A.Cu2O和Cu2S中Cu元素化合价都降低,都为氧化剂,故A错误;
B.反应中Cu2O只起到氧化剂的作用,故B错误;
C.反应中Cu元素化合价只降低,Cu为还原产物,故C错误;
D.根据方程式可知氧化产物与还原产物的物质的量之比为1:6,故D正确.
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高考高频考点,注意从元素化合价变化的角度认识物质表现出的性质,明确元素化合价为解答该题的关键,题目难度不大.1年前查看全部
- “药金”外观和黄金(Au)相似,常被误认为黄金,不法分子用炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉(C)混合加热
“药金”外观和黄金(Au)相似,常被误认为黄金,不法分子用炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉(C)混合加热至800℃左右,制得金光闪闪的假黄金“药金”以牟取暴利.用上述方法制得的“药金”不可能是黄金,理由是______.
 linnanworl1年前1
linnanworl1年前1 -
 等待是受罪 共回答了15个问题
等待是受罪 共回答了15个问题 |采纳率86.7%解题思路:黄金的成分主要是金,根据质量守恒定律可知,化学反应前后元素的种类不变,那么我们通过分析此题反应前是否存在金(Au)元素来判断能否制得黄金;根据“药金”的制取过程其主要含有的金属是锌和铜.因为黄金的主要成分是金,它是由金元素组成;那么要制取黄金,根据质量守恒定律可知,反应物中一定要有金元素,但是上述材料“炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉(C)混合”,不含有金元素,故不能制取.
故答案为:根据质量守恒定律可知,反应物中一定要有金元素,而“药金”中无金元素点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题考查了对质量守恒定律的应用情况,能够利用该定律解释一些生活中常见的现象;质量守恒定律是初中化学中一个非常重要的定理,也是中考中的热点问题,所以深刻理解质量守恒定律,并能够应用质量守恒定律解决问题对同学来说是非常重要的.1年前查看全部
- (2009•张家界)我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即
(2009•张家界)我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即可得到金光闪闪的“药金”.请回答:
(1)“药金”的主要成分是______;
(2)用上述方法和原料不能制得黄金(Au)的原因是______. xiaohaozi3191年前1
xiaohaozi3191年前1 -
 aigang 共回答了12个问题
aigang 共回答了12个问题 |采纳率83.3%解题思路:(1)在高温条件下,ZnCO3分解为氧化锌和二氧化碳,碳能还原氧化锌和氧化亚铜,生成了锌和铜.据此分析“药金”的主要成分;
(2)根据质量守恒定律分析不制的金的原因.(1)在高温条件下,ZnCO3分解为氧化锌和二氧化碳,碳能还原氧化锌和氧化亚铜,生成了锌和铜.所以,“药金”的主要成分是锌和铜;(2)因为黄金的主要成分是金,它是由金元素组成;要制取黄金,根据质量守恒定律可...
点评:
本题考点: 碳的化学性质;盐的化学性质;质量守恒定律及其应用.
考点点评: 本题考查了对质量守恒定律的应用情况,能够利用该定律解释一些生活中常见的现象;质量守恒定律是初中化学中一个非常重要的定理,也是中考中的热点问题,所以深刻理解质量守恒定律,并能够应用质量守恒定律解决问题对同学来说是非常重要的.1年前查看全部
- 冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO 3 )、赤铜矿(主要成分为Cu 2 O)和木炭粉混合加热至80
冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO 3 )、赤铜矿(主要成分为Cu 2 O)和木炭粉混合加热至800℃左右,即可得到金光闪闪与黄金外观相似的“药金”.
(1)用上述方法不能制得黄金是因为______.
(2)药金的主要成分是______. 只能发10条1年前1
只能发10条1年前1 -
 hxc808 共回答了19个问题
hxc808 共回答了19个问题 |采纳率68.4%(1)因为黄金的主要成分是金,它是由金元素组成;那么要制取黄金,根据质量守恒定律可知,反应物中一定要有金元素,但是上述材料不含有金元素,故不能制取.
(2)根据质量守恒定律,反应前后元素种类不变和“药金”的冶炼材料可知:与黄金外观相似的“药金”主要成分是Zn、Cu.
故正确答案:
(1)在化学反应中原子种类不变Zn、Cu、C、O不可能变成Au;
(2)Zn、Cu1年前查看全部
- 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O
6Cu+SO2↑,关于该反应的说法中正确的是( )△ .
A.该反应的氧化剂只有Cu2O
B.每生成19.2g Cu,反应中转移0.6mol电子
C.Cu既是氧化产物又是还原产物
D.Cu2S在反应中既是氧化剂,又是还原剂 盛夏剩下sil1年前1
盛夏剩下sil1年前1 -
 ywqg888 共回答了21个问题
ywqg888 共回答了21个问题 |采纳率100%解题思路:反应中Cu元素化合价降低,S元素化合价升高,则反应中Cu2S和Cu2O都表现为氧化性,而Cu2S还表现为还原性.A.反应中Cu元素化合价降低,Cu2S和Cu2O都表现为氧化性,都为氧化剂,故A错误;
B.每生成19.2g Cu,n(Cu)=[19.2g/64g/mol]=0.3mol,转移电子为0.3mol×(1-0)=0.3mol,故B错误;
C.Cu元素化合价只降低,为还原产物,故C错误;
D.反应中Cu元素化合价降低,S元素化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,故D正确.
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意元素化合价的判断,题目难度不大.1年前查看全部
- (2011•保康县模拟)将一定量的炉甘石(ZnCO3)和赤铜矿(Cu2O)粉末跟足量炭粉混合,加热至800℃左右,充分反
(2011•保康县模拟)将一定量的炉甘石(ZnCO3)和赤铜矿(Cu2O)粉末跟足量炭粉混合,加热至800℃左右,充分反应后可得到一种外观类似黄金的锌和铜的合金.同学们对上述反应很感兴趣,查阅资料:高温时木炭可将金属活动顺序表中铝以后金属的氧化物还原成金属单质;在高温条件下,ZnCO3可分解成金属氧化物和一种常见气体.试写出生成Zn反应的方程式.ZnCO3
ZnO+CO2↑高温 .ZnCO3;
ZnO+CO2↑高温 .C+2ZnO
2Zn+CO2↑高温 .C+2ZnO.
2Zn+CO2↑高温 . 如仙1年前1
如仙1年前1 -
 尹洪波_ 共回答了16个问题
尹洪波_ 共回答了16个问题 |采纳率87.5%解题思路:根据题意,在高温条件下,ZnCO3可分解成金属氧化物和一种常见气体,由质量守恒定律(反应前后元素种类不变),该金属氧化物为氧化锌,常见气体为二氧化碳;高温时木炭可将金属活动顺序表中铝以后金属的氧化物还原成金属单质,则800℃左右,碳能与氧化锌反应置换反应生成锌和二氧化碳;写出反应的化学方程式即可.在高温条件下,ZnCO3可分解成金属氧化物和一种常见气体,由质量守恒定律(反应前后元素种类不变),该金属氧化物为氧化锌,常见气体为二氧化碳,反应的化学方程式为:ZnCO3
高温
.
ZnO+CO2↑.
高温时木炭可将金属活动顺序表中铝以后金属的氧化物还原成金属单质,则800℃左右,碳能与氧化锌反应置换反应生成锌和二氧化碳,反应的化学方程式为:C+2ZnO
高温
.
2Zn+CO2↑.
故答案为:ZnCO3
高温
.
ZnO+CO2↑;C+2ZnO
高温
.
2Zn+CO2↑.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- 我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即可得到金光
我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即可得到金光
我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和足量木炭粉加热至800℃,即可得到金光闪闪的“药金”.请回答:
(1)“药金”的主要成分是______;
(2)用上述方法和原料不能制得黄金(Au)的原因是______.
 vv的我1881年前1
vv的我1881年前1 -
 feme 共回答了25个问题
feme 共回答了25个问题 |采纳率100%(1)在高温条件下,ZnCO3分解为氧化锌和二氧化碳,碳能还原氧化锌和氧化亚铜,生成了锌和铜.所以,“药金”的主要成分是锌和铜;
(2)因为黄金的主要成分是金,它是由金元素组成;要制取黄金,根据质量守恒定律可知,反应物中一定要有金元素,但是上述反应物中不含有金元素,故不能制取.
故答为:(1)锌和铜;(2)反应物中没有金元素.1年前查看全部
- 赤铜矿和炉甘石和碳混合制取“黄金”的化学式?
 随心梭鱼12341年前4
随心梭鱼12341年前4 -
 贵阳的毛 共回答了16个问题
贵阳的毛 共回答了16个问题 |采纳率87.5%C + 2Cu2O(赤铜矿) = 4Cu + CO2↑
ZnCO3(炉甘石) =ZnO + CO2↑
2ZnO + C = 2Zn + CO2↑
锌和铜合金是金黄色的.1年前查看全部
- 赤铜矿的主要成分是Cu 2 O,辉铜矿的主要成分是Cu 2 S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu 2 S+2C
赤铜矿的主要成分是Cu 2 O,辉铜矿的主要成分是Cu 2 S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu 2 S+2Cu 2 O═6Cu+SO 2 ↑,关于该反应的说法中,正确的是( ) A.该反应的氧化剂只有Cu 2 O B.Cu 2 S在反应中既是氧化剂,又是还原剂 C.Cu既是氧化产物又是还原产物 D.每生成19.2gCu,反应中转移1.8mol电子  高原之鹰6616011年前1
高原之鹰6616011年前1 -
 liebao08 共回答了19个问题
liebao08 共回答了19个问题 |采纳率84.2%A、反应Cu 2 S+2Cu 2 O═6Cu+SO 2 ↑中,化合价降低的元素是铜元素,所在的反应物Cu 2 S、Cu 2 O是氧化剂,故A错误;B、硫化铜中硫元素化合价升高,铜元素的化合价升高,所以Cu 2 S在反应中既是氧化剂,又是还原...1年前查看全部
- (2007•泸州)将炉甘石(主要成分为ZnCO3)、赤铜矿(主要成分是Cu2O)和木炭混合加热到800℃左右,可冶炼出一
(2007•泸州)将炉甘石(主要成分为ZnCO3)、赤铜矿(主要成分是Cu2O)和木炭混合加热到800℃左右,可冶炼出一种外观与通常所说的金子很相似的物质,该物质被称为“药金”.
(1)试分析药金中______(填“有”或“无”)金(Au)元素.
(2)小明将药金进行高温加热,发现药金变为黑色,据此,小明认为药金中含有铜.试写出该反应的化学方程式.2Cu+O2
2CuO△ .2Cu+O2
2CuO△ .
(3)小明为了证明药金是否含有锌:取药金少量于试管中,加入盐酸进行浸泡,发现有气泡产生,用实验验证,该气体为______时,证明药金中含有锌,产生该气体的化学反应方程式为______. ztyh1年前1
ztyh1年前1 -
 ren427 共回答了15个问题
ren427 共回答了15个问题 |采纳率80%解题思路:(1)任何化学变化都遵循质量守恒定律,变化前后元素的种类不变;
(2)铜在加热条件下能与空气中氧气反应生成黑色的氧化铜;
(3)根据金属活动性可知,锌能与稀盐酸反应放出氢气,因此,只需证明放入稀盐酸的药金反应放出的气体为氢气,就可以证明药金中含能与稀盐酸反应的锌.(1)根据质量守恒定律,反应前后元素的种类不变,反应前炉甘石中不含元素Au,所以反应后的生成物“药金”中也一定不含有元素Au;故答案为:无;(2)加热条件下,铜与氧气化合生成黑色的氧化铜;故答案为:2Cu+O2&n...
点评:
本题考点: 碳的化学性质;金属活动性顺序及其应用;酸的化学性质;物质的元素组成;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据质量守恒定律,反应前后元素的种类不变,可由反应物或生成物的组成元素推断生成物或反应物的组成.1年前查看全部
- 将炉甘石(ZnCO 3 )、赤铜矿(Cu 2 O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄
将炉甘石(ZnCO 3 )、赤铜矿(Cu 2 O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”.请你参与课外活动小组的同学对“假黄金”进行探究,并回答有关问题:
提出问题:“假黄金”的化学组成是什么?
查阅资料:高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO 3 高温可分解成金属氧化物.
猜想:①“假黄金”可能由C、Zn、Cu三种单质组成;
②“假黄金”可能由ZnO、CuO、Cu 2 O三种氧化物组成;
③“假黄金”可能是单质和氧化物组成的混合物.
论证:他们经思考和推理后,首先排除了猜想______(选填①②或③),你觉得他们的理由是______.进而再排除了猜想______(选填①②或③).对余下的一种猜想,该同学又排除了其中的一种物质,你认为他们的依据是______.
进行实验:他们用实验鉴定了“假黄金”中所含的两种物质,请将实验过程填入下表中:
得出结论:“假黄金”的化学组成是:______.实验方法 观察到的现象 步骤1 步骤2  发春的猫6661年前1
发春的猫6661年前1 -
 小山一座 共回答了12个问题
小山一座 共回答了12个问题 |采纳率91.7%根据查阅资料:ZnCO 3 高温可分解成金属氧化物;高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;可推知:
②“假黄金”可能由ZnO、CuO、Cu 2 O三种氧化物组成是不可能的;③“假黄金”可能是单质和氧化物组成的混合物是不可能的;
故答案为:②;高温时炭能将金属氧化物还原成金属;③;
对①“假黄金”可能由C、Zn、Cu三种单质组成的猜想,该同学又排除了其中的一种物质为碳,他们的依据是:过量的炭在高温时能与空气中的氧气反应生成CO或CO 2 ,故答案为:过量的炭在高温时能与空气中的氧气反应生成CO或CO 2 ;
实验方法 观察到的现象
步骤1 用一小烧杯取少量“假黄金”,加入适量稀硫酸 有大量气泡产生
步骤2 将上述反应后的剩余固体置于酒精灯火焰上灼烧 固体表面变黑色 “假黄金”的化学组成是:锌和铜的合金.故答案为:锌和铜的合金.1年前查看全部
- 将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”.请
将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800℃左右,充分反应后,即得金光闪闪的“假黄金”.请你参与化学小组同学对“假黄金”进行探究,并回答有关问题:
【提出问题】“假黄金”的化学组成是什么?
【查阅资料】高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物.
【猜想】①“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成;②“假黄金”可能由C、Zn、Cu三种单质组成;③“假黄金”可能是单质和氧化物组成的混合物.
【论证】他们经思考和推理后,首先排除了猜想①.你觉得他们的理由是______.进而再排除了猜想③.对余下的一种猜想,该同学又排除了其中的一种物质炭,你认为他们的依据是______.
进行实验】他们用实验鉴定了“假黄金”中所含的两种物质,请将实验过程填入表中:实验方法 观察到的现象 步骤1 步骤2  摇滚猫m1年前1
摇滚猫m1年前1 -
 awxrfvyhko 共回答了17个问题
awxrfvyhko 共回答了17个问题 |采纳率88.2%解题思路:ZnCO3高温可分解成两种氧化物,其中一种为氧化锌,生成的氧化锌和赤铜矿(Cu2O)和过量的炭混合后,高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质,锌和铜均在铝的后面,故能全部被还原为金属,得到的锌在氢前,可与酸发生置换反应产生氢气,而铜在氢后,不能与酸发生置换反应生成氢气.【论证】因为碳酸锌高温分解的产物之一是氧化锌,根据查阅资料:“高温时炭可将金属活动顺序中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物”;可推知:与氧化亚铜一起可被过量的碳完全还原为金属,不可能有氧化物存在,故①“假黄金”可能由ZnO、CuO、Cu2O三种氧化物组成是不可能的;③“假黄金”可能是单质和氧化物组成的混合物是不可能的;
对②“假黄金”可能由C、Zn、Cu三种单质组成的猜想,该同学又排除了其中的一种物质为碳,他们的依据是:过量的炭在高温时能与空气中的氧气反应生成CO或CO2,故不可能有碳存在;故答案为:过量的炭在高温时能与空气中的氧气反应生成CO或CO2;
【进行实验】
实验方法观察到的现象
步骤1用一小烧杯取少量“假黄金”,加入适量稀硫酸有大量气泡产生
步骤2将上述反应后的剩余固体置于酒精灯火焰上灼烧固体表面变黑色“假黄金”的化学组成是:锌和铜的合金.故答案为:锌和铜的合金.点评:
本题考点: 实验探究物质的组成成分以及含量;金属的化学性质;碳的化学性质.
考点点评: 本题考查学生根据题中所给信息进行分析解题的能力.1年前查看全部
- 古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼
古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.你认为这金光灿灿金属可能是______,炼出它的化学方程式为ZnCO3
ZnO+CO2↑高温 .ZnCO3、
ZnO+CO2↑高温 .C+2Cu2O
4Cu+CO2↑高温 .C+2Cu2O、
4Cu+CO2↑高温 .2ZnO+C
2Zn+CO2↑高温 .2ZnO+C.
2Zn+CO2↑高温 . xieb10011年前1
xieb10011年前1 -
 烧炭闲人 共回答了15个问题
烧炭闲人 共回答了15个问题 |采纳率100%解题思路:根据质量守恒定律:化学反应前后原子的个数和种类不变;反应物中有什么元素,生成物中就有什么元素,我们就可以初步判断在该“黄金”中可能含的元素为铜元素和锌元素.所谓的“黄金”是碳还原的铜锌的合金,其中碳酸锌在高温时可以分解产生氧化锌和二氧化碳,可以据此解答该题.根据质量守恒定律分析,反应物炉甘石(主要成分ZnCO3)赤铜(Cu2O)与木炭粉中存在Zn、Cu、C、O 四种元素,所以生成物中也存在这四种元素,所以可以判断该黄色金属可能为铜和锌的合金,由题意:炉甘石(主要成分ZnCO3)、赤铜(Cu2O)、木碳高温下能得到多种物质,其中ZnCO3高温分解成ZnO和CO2,则反应为:①ZnCO3高温分解成ZnO和CO2的化学方程式为:ZnCO3
高温
.
ZnO+CO2↑;
②木碳高温还原赤铜(含Cu2O)的化学方程式为:C+2Cu2O
高温
.
4Cu+CO2↑;
③木碳高温还原ZnO的化学方程式为:2ZnO+C
高温
.
2Zn+CO2↑;
故答案为:铜锌合金;ZnCO3
高温
.
ZnO+CO2↑;C+2Cu2O
高温
.
4Cu+CO2↑;2ZnO+C
高温
.
2Zn+CO2↑.点评:
本题考点: 质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 对该题的关键是要依据质量守恒定律,所以要求学生一定要牢牢的记住质量守恒定律的真谛.本题根据信息书写化学方程式,在书写时要根据题给条件找准反应物和生成物,注意反应条件和配平.1年前查看全部
- 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O==6
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O==6Cu+SO2↑
每生成19.2gCu,反应中转移1.8mol电子怎么错了 ftalou1年前1
ftalou1年前1 -
 xcurt 共回答了19个问题
xcurt 共回答了19个问题 |采纳率94.7%显然错了,19.2g铜为0.3mol.得到一个铜原子需转移一个电子,0.3mol铜当然是0.3mol的电子转移了 .(矿石中的为+1价,铜单质为0价)1年前查看全部
- Cu2O是赤铜矿的主要成分,Cu2S是辉铜矿的主要成分.铜的冶炼过程通常发生反应:Cu2S+Cu2O=6Cu+SO2↑,
Cu2O是赤铜矿的主要成分,Cu2S是辉铜矿的主要成分.铜的冶炼过程通常发生反应:Cu2S+Cu2O=6Cu+SO2↑,下列有关说法正确的是( )
A.该反应中有三种元素的化合价发生了变化
B.每生成0.1mol Cu,转移0.2 mol 电子
C.Cu2S在反应中既是氧化剂又是还原剂
D.Cu既是氧化产物又是还原产物 野刺梅1年前1
野刺梅1年前1 -
 yiji44 共回答了21个问题
yiji44 共回答了21个问题 |采纳率90.5%解题思路:反应中Cu元素化合价降低,S元素化合价升高,则反应中Cu2S和Cu2O都表现为氧化性,而Cu2S还表现为还原性.A.该反应中Cu元素化合价降低,S元素化合价升高,所以有两种元素化合价变化,故A错误;
B.每生成0.1mol Cu,转移电子=0.1 mol×(1-0)=0.1mol,故B错误;
C.该反应中Cu元素化合价降低,S元素化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,故C正确;
D.该反应中铜元素化合价降低,所以铜是还原产物,故D错误;
故选C.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,题目难度中等,注意把握元素的化合价的变化,为解答该题的关键,从化合价变化的角度理解相关概念.1年前查看全部
- 赤铜矿的成分是Cu 2 O,辉铜矿的成分是Cu 2 S,将赤铜矿与辉铜矿混合加热有以下反应: Cu2S +
赤铜矿的成分是Cu 2 O,辉铜矿的成分是Cu 2 S,将赤铜矿与辉铜矿混合加热有以下反应: Cu2S + 2Cu 2 O 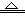 6Cu + SO 2 ↑。对于该反应的下列说法正确的是[ ]
6Cu + SO 2 ↑。对于该反应的下列说法正确的是[ ]A.该反应中的氧化剂只有Cu 2 O
B.Cu 2 O在反应中既是氧化剂又是还原剂
C.Cu既是氧化产物又是还原产物
D.氧化产物与还原产物的物质的量之比为1:6 小狐狸爱人1年前1
小狐狸爱人1年前1 -
 oldwall_chen 共回答了24个问题
oldwall_chen 共回答了24个问题 |采纳率91.7%D1年前查看全部
- 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O═6Cu
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O═6Cu+SO2↑ 下列关于该反应的说法正确的是( )
A.Cu2S在反应中既是氧化剂,又是还原剂
B.Cu既是氧化产物,又是还原产物
C.该反应中氧化剂只有Cu2O
D.每生成19.2g Cu,反应中转移0.6mol电子 荣俊标1年前1
荣俊标1年前1 -
 ksdasda 共回答了16个问题
ksdasda 共回答了16个问题 |采纳率75%解题思路:Cu2S中Cu元素化合价为+1价,S为-2价,Cu2O中Cu元素化合价为+1价,O为-2价,反应Cu2S+2Cu2O═6Cu+SO2↑中,Cu元素化合价降低,S元素化合价升高,以此解答该题.A.Cu2S在反应中Cu元素化合价降低,S元素化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,故A正确;
B.Cu元素化合价降低,Cu为还原产物,故B错误;
C.反应中Cu2S和Cu2O为氧化剂,故C错误;
D.每生成19.2g Cu,即0.3mol,反应中转移0.3mol×(1-0)=0.3mol电子,故D错误.
故选:A.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,侧重于相关概念的考查,为高考高频考点,难度不大,注意从元素化合价的角度认识相关概念和物质的性质.1年前查看全部
- 赤铜矿的主要成分是氧化亚铜(Cu2O),辉铜矿的主要成分是硫化亚铜(Cu2S),将赤铜矿与辉铜矿混合加热有如下反应:Cu
赤铜矿的主要成分是氧化亚铜(Cu2O),辉铜矿的主要成分是硫化亚铜(Cu2S),将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O=6Cu+SO2↑,下列对于该反应的说法正确的是( )
A. 该反应中的氧化剂只有Cu2O
B. Cu既是氧化产物又是还原产物
C. Cu2S在反应中既是氧化剂又是还原剂
D. 氧化产物与还原产物的物质的量之比为6:1 xzw_52111年前4
xzw_52111年前4 -
 ZLCZLN 共回答了13个问题
ZLCZLN 共回答了13个问题 |采纳率92.3%解题思路:Cu2S+2Cu2O=6Cu+SO2↑ 中,得电子化合价降低的反应物的氧化剂,失电子化合价升高的反应物是还原剂,氧化剂对应的产物的还原产物,还原剂对应的产物是氧化产物,根据得失电子数相等确定氧化产物和还原产物的物质的量之比.A.反应中,Cu2S和Cu2O中的+1价Cu元素得电子生成0价的Cu,所以Cu2S和Cu2O都是氧化剂,故A错误;
B.反应中,+1价Cu元素得电子生成0价的Cu,所以Cu是还原产物,故B错误;
C.硫化铜中硫元素化合价升高,铜元素的化合价升高,所以Cu2S在反应中既是氧化剂,又是还原剂,故C正确;
D.根据Cu2S+2Cu2O=6Cu+SO2↑知,还原产物和氧化产物的物质的量之比是6:1,故D错误;
故选C.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,明确元素化合价是解本题的关键,注意该题中反应物都是氧化剂,但Cu2S还是还原剂,为易错点.1年前查看全部
- 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应发生Cu2S+2Cu2O
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应发生Cu2S+2Cu2O
6Cu+SO2↑,关于该反应的下列说法中,正确的是( )△ .
A.该反应的氧化剂中只有Cu2O
B.Cu既是氧化产物,又是还原产物
C.氧化产物与还原产物的物质的量之比为6:1
D.Cu2S在反应中既是氧化剂,又是还原剂 风萧萧20041年前1
风萧萧20041年前1 -
 147258369 共回答了23个问题
147258369 共回答了23个问题 |采纳率82.6%解题思路:反应中Cu元素化合价降低,S元素化合价升高,则反应中Cu2S和Cu2O都表现为氧化性,而Cu2S还表现为还原性.A.反应中Cu元素化合价降低,Cu2S和Cu2O都表现为氧化性,故A错误;
B.Cu元素化合价只降低,为还原产物,故B错误;
C.氧化产物为SO2,还原产物为Cu,氧化产物与还原产物的物质的量之比为1:6,故C错误;
D.反应中Cu元素化合价降低,S元素化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,故D正确.
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,题目难度中等,注意把握元素的化合价的变化,为解答该题的关键,从化合价变化的角度理解相关概念.1年前查看全部
- 自然界中有赤铜矿(主要成分是Cu2O)、辉铜矿(主要成分是Cu2S)等铜的矿物.
自然界中有赤铜矿(主要成分是Cu2O)、辉铜矿(主要成分是Cu2S)等铜的矿物.
(1)Cu2S中铜元素的质量分数为______.
(2)将赤铜矿(Cu2O)和木炭粉混合后加热到约800℃,生成铜和二氧化碳.反应的化学方程式是C+2Cu2O
4Cu+CO2↑800℃ .C+2Cu2O.
4Cu+CO2↑800℃ .
(3)工业上利用辉铜矿炼铜的一个主要反应是在高温下,辉铜矿(Cu2S)与氧气反应,生成铜和二氧化硫,反应的化学方程式是Cu2S+O2
2Cu+SO2↑高温 .Cu2S+O2.
2Cu+SO2↑高温 . cola3281年前1
cola3281年前1 -
 短暂2004 共回答了30个问题
短暂2004 共回答了30个问题 |采纳率93.3%解题思路:(1)根据化合物中元素的质量分数=[相对原子质量×原子个数/相对分子质量]×100%,进行分析解答.
(2)赤铜矿(Cu2O)和木炭粉混合后加热到约800℃,生成铜和二氧化碳,写出反应的化学方程式即可.
(3)在高温下,辉铜矿(Cu2S)与氧气反应,生成铜和二氧化硫,写出反应的化学方程式即可.(1)Cu2S中铜元素的质量分数为[64×2/64×2+32×100%=80%.
(2)赤铜矿(Cu2O)和木炭粉混合后加热到约800℃,生成铜和二氧化碳,反应的化学方程式为:C+2Cu2O
800℃
.
]4Cu+CO2↑.
(3)在高温下,辉铜矿(Cu2S)与氧气反应,生成铜和二氧化硫,反应的化学方程式为:Cu2S+O2
高温
.
2Cu+SO2↑.
故答案为:(1)80%;(2)C+2Cu2O
800℃
.
4Cu+CO2↑;(3)Cu2S+O2
高温
.
2Cu+SO2↑.点评:
本题考点: 元素的质量分数计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握化学式的有关计算、化学方程式的书写方法是正确解答本题的关键.1年前查看全部
- 用一氧化碳还原某赤铜矿样品(只要成分是Cu2O)60g,将反应生成的二氧化碳通入足量的澄清石灰水,
用一氧化碳还原某赤铜矿样品(只要成分是Cu2O)60g,将反应生成的二氧化碳通入足量的澄清石灰水,
用一氧化碳还原某赤铜矿样品(只要成分是Cu2O,还含有不参加反应的杂质)60g,将反应生成的二氧化碳通入足量的澄清石灰水,生成的白色沉淀37.5g.求赤铜矿里Cu2O的质量分数 八直衣兄1年前1
八直衣兄1年前1 -
 刘德才博客 共回答了14个问题
刘德才博客 共回答了14个问题 |采纳率85.7%Cu2O+CO=2Cu+CO2
CO2+Ca(OH)2=CaCO3+H2O
根据方程式每个Cu2O对应一个CaCO3,即质量比:144:100=X:37.5,X=54克.
54*100%/60=90%.1年前查看全部
- 我国古代将炉甘石(主要成分:ZnCO 3 )、赤铜矿(主要成分:Cu 2 O)和足量木炭粉加热至800℃,即可得到金光闪
我国古代将炉甘石(主要成分:ZnCO 3 )、赤铜矿(主要成分:Cu 2 O)和足量木炭粉加热至800℃,即可得到金光闪闪的“药金”.请回答:
(1)“药金”的主要成分是______;
(2)用上述方法和原料不能制得黄金(Au)的原因是______. empemp1年前1
empemp1年前1 -
 珍惜772 共回答了15个问题
珍惜772 共回答了15个问题 |采纳率93.3%(1)在高温条件下,ZnCO 3 分解为氧化锌和二氧化碳,碳能还原氧化锌和氧化亚铜,生成了锌和铜.所以,“药金”的主要成分是锌和铜;
(2)因为黄金的主要成分是金,它是由金元素组成;要制取黄金,根据质量守恒定律可知,反应物中一定要有金元素,但是上述反应物中不含有金元素,故不能制取.
故答为:(1)锌和铜;(2)反应物中没有金元素.1年前查看全部
- 将一定量的炉甘石(ZnCO 3 )和赤铜矿(Cu 2 O)粉末跟足量炭粉混合,加热至800℃左右,充分反应后可得到一种外
将一定量的炉甘石(ZnCO 3 )和赤铜矿(Cu 2 O)粉末跟足量炭粉混合,加热至800℃左右,充分反应后可得到一种外观类似黄金的合金。同学们对这种合金的成分很感兴趣,查阅资料:高温时木炭可将金属活动性顺序中铝以后金属的氧化物还原成金属单质;在高温条件下,ZnCO 3 可分解成金属氧化物和一种常见气体。
(1)写出ZnCO 3 分解反应的化学方程式 ___________。
(2)以下是同学们对该合金成分的几种猜想: a.可能是Zn、Cu b.可能是Zn、Cu、C c.可能是ZnO、CuO、Cu 如果想证明a中Zn的存在,可选用的试剂是____,反应的化学方程式为____。
(3)你认为几种猜想中应首先排除的是____(填“a”“b”或“c”),理由是____。 西伯利亚韩流1年前0
西伯利亚韩流1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO3)、赤铜矿(主要成分为Cu2O)和木炭粉混合加热至800℃左右
冶炼技术在中国有着悠久的历史,我国古代将炉甘石(ZnCO3)、赤铜矿(主要成分为Cu2O)和木炭粉混合加热至800℃左右,即可得到金光闪闪与黄金外观相似的“药金”.
(1)用上述方法不能制得黄金是因为______.
(2)药金的主要成分是______. 小妖精的苹果1年前1
小妖精的苹果1年前1 -
 月牙_牛牛 共回答了21个问题
月牙_牛牛 共回答了21个问题 |采纳率100%解题思路:黄金的成分主要是金,根据质量守恒定律可知,化学反应前后元素的种类不变,那么我们通过分析此题反应前是否存在金(Au)元素来判断能否制得黄金;根据“药金”的制取过程其主要含有的金属是锌和铜.(1)因为黄金的主要成分是金,它是由金元素组成;那么要制取黄金,根据质量守恒定律可知,反应物中一定要有金元素,但是上述材料不含有金元素,故不能制取.
(2)根据质量守恒定律,反应前后元素种类不变和“药金”的冶炼材料可知:与黄金外观相似的“药金”主要成分是Zn、Cu.
故正确答案:
(1)在化学反应中原子种类不变Zn、Cu、C、O不可能变成Au;
(2)Zn、Cu点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题考查了对质量守恒定律的应用情况,能够利用该定律解释一些生活中常见的现象;质量守恒定律是初中化学中一个非常重要的定理,也是中考中的热点问题,所以深刻理解质量守恒定律,并能够应用质量守恒定律解决问题对同学来说是非常重要的.1年前查看全部
大家在问
- 1公正的小裁判.(对的打“√”,错的打“×”)
- 2为什么温度降低,气压变小
- 3(2014•长宁区一模)甲、乙、丙、丁是初中化学常见的化合物.甲和乙中含有碳元素,甲能做建筑材料.它们之间有如图所示的转
- 46下语文8课多音字
- 5已知角A的正弦值,怎样用计算器算A的度数?是余弦或正切呢?
- 619.某生物基因型为A/a、Bc/bC,所产生的配子中abc占10﹪,则b、c之间的交换值为【 】
- 7我刚到这儿 英文怎么说I've just been here.
- 8"这一切都是人类一手造成的"的英语怎么写?
- 9已知:在△ABC中,∠ACB=90°,点P是线段AC上一点,过点A作AB的垂线,交BP的延长线于点M,MN⊥AC于点N,
- 10一水合氨和氨水什么区别
- 11七年级英语暑假课堂(N版)每课一练部分答案请求.
- 12在学习了八年级物理第七、八章的知识后,小强同学得出了以下四个结论,你认为错误的一项是( )
- 13(2013•崇安区二模)下列化学用语正确的是( )
- 14为什么?密度计的刻度是上宽下窄?
- 15给我几个比较级的句子.
