碘化亚铁溶液中通入氯气两者的物质的量之比为5:7方程式?
 漂泊的翅膀2022-10-04 11:39:541条回答
漂泊的翅膀2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
相关推荐
- 碘化亚铁与氯气反应 ,氯气少量及过量
碘化亚铁与氯气反应 ,氯气少量及过量
我找别的网页,有氯气多了 2FeI2+3Cl2=2FeCl3+2I21.氯气少了 FeI2+Cl2=FeCl2+I2
2.5Cl2 + 4FeI2 == 2FeCl3 + 2FeCl2 + 4I2
3.氯气不足3Cl2+6FeI2=4FeI3+2FeCl3 氯气过量:3Cl2 + 2FeI2 = 2FeCl3 + 2I2
哪个是对的啊 nlut1年前1
nlut1年前1 -
 冬之浪子 共回答了21个问题
冬之浪子 共回答了21个问题 |采纳率85.7%如果不考虑I2被Cl2氧化的话,那麼少量Cl2只能把I2氧化,发生FeI2+Cl2=FeCl2+I2.过量以後Cl2继续氧化Fe2+,发生2FeCl2+Cl2=2FeCl3,加起来总反应就是2FeI2+3Cl2=2FeCl3+2I2
如果再考虑I2被Cl2氧化,则再发生5Cl2+I2+6H2O=2HIO3+10HCl.1年前查看全部
- 氯气与碘化亚铁6:5反应的化学方程式以及4:3反应化学方程式
 糖sherry糖1年前2
糖sherry糖1年前2 -
 一个大ii 共回答了17个问题
一个大ii 共回答了17个问题 |采纳率88.2%氯气与碘化亚铁6:5反应:
5 FeI2 + 6 Cl2 = 5 I2 + 2 FeCl3 + 3 FeCl2
2 Fe2+ + 10 I- + 6 Cl2 = 5 I2 + 2 Fe3+
氯气与碘化亚铁4:3反应:
3 FeI2 + 4 Cl2 = 3 I2 + FeCl2 + 2 FeCl3
2 Fe2+ 6 I- + 4 Cl2 = 3 I2 + 2 Fe3+ + 6 Cl-1年前查看全部
- 足量的氯气与碘化亚铁反应的离子反应方程式以及足量的氯气与溴化亚铁的离子反映方程式?
 2523440161年前1
2523440161年前1 -
 燕子岭322 共回答了21个问题
燕子岭322 共回答了21个问题 |采纳率100%溴化亚铁与氯气等物质的量反应的化学方程式和离子方程式应如何快速写出?
关键抓住:氯气要先氧化亚铁离子,然后再氧化溴离子.
2Fe^2+^2Br-^+2Cl2====2Fe^3+^+Br2^+4Cl-
化学方程式,你对照写.1年前查看全部
- 碘化亚铁与氯气以5:7的物质的量反应
 chengjingtaoer1年前2
chengjingtaoer1年前2 -
 乡下yy 共回答了27个问题
乡下yy 共回答了27个问题 |采纳率85.2%因为I-和Fe2+是I-的还原性比较强所以Cl2先跟I-反应.就假设FeI2是5mol,Cl2是7mol,那麼Fe2+是5mol而I-是10mol.
2I-+Cl2=I2+2Cl-
2 1
10 n1=5mol,因此当I-全部被氧化之後还剩馀2mol的Cl2.
2Fe2++Cl2=2Fe3++2Cl-
2 1
n2=4 2mol
当Cl2完全消耗掉之後还剩馀1molFe2+在溶液.所以总共方程是
5FeI2+7Cl2=FeCl2+5I2+4FeCl31年前查看全部
- 碘化亚铁与氯气的计算题已知Fe3+ +2I-=2Fe2++I2 现有2L 0.5mol/L 的FeI2溶液,往其中通入一
碘化亚铁与氯气的计算题
已知Fe3+ +2I-=2Fe2++I2 现有2L 0.5mol/L 的FeI2溶液,往其中通入一定量标况下的氯气.反应过程体积不变,反应结束后,Cl-浓度是Fe2+浓度的5倍,求通入氯气的体积? 答案是:28L 求过程 天空的雾1年前1
天空的雾1年前1 -
 牧野流星 共回答了18个问题
牧野流星 共回答了18个问题 |采纳率100%题目方程式告诉你的是通入Cl2先氧化I-,再氧化Fe2+
2I- +Cl2=2Cl- +I2
2Fe2+ +Cl2= 2Fe3+ +2Cl-
2L 0.5mol/L 的FeI2溶液
含有Fe2+ 2*0.5=1mol I- 2mol
首先全部还原I-需要1molCl2,得到2molCl-,此时消耗Cl2 22.4L
然后设再参加反应的Cl2为xmol
那么有(1-2x):(2+2x)=1:5
x=0.25
因此最后总共需要Cl2 1.25*22.4=28L1年前查看全部
- 离子反应,碘化亚铁和少量氯气反应,为什么碘离子不反应
 菠蘿油王子1年前2
菠蘿油王子1年前2 -
 我喜欢百事可乐 共回答了20个问题
我喜欢百事可乐 共回答了20个问题 |采纳率95%还原性亚铁离子大于碘离子,氯气少量的情况下先于亚铁离子反应1年前查看全部
- 过量氯气通入碘化亚铁方程式怎么写
过量氯气通入碘化亚铁方程式怎么写
为什么这么写2Fe2+ + 4I- + 3Cl2 = 2Fe3 + 2I2 + 6Cl-
2Cl2+2Fe2+ +2I-=I2+2Fe3+ +4Cl- 78_99991年前3
78_99991年前3 -
 chyu5677 共回答了19个问题
chyu5677 共回答了19个问题 |采纳率94.7%一个碘化亚铁电离出一个Fe2+和两个I- ,二者又都能和Cl2反应,所以Cl2过量就以碘化亚铁为基准,写为2Fe2+ + 4I- + 3Cl2 = 2Fe3 + 2I2 + 6Cl-;Cl2不足以Cl2为基准,兼顾生成物Fe3+和I2,写为2Cl2+2Fe2+ +2I-=I2+2Fe3+ +4C...1年前查看全部
- 在溴化亚铁溶液和碘化亚铁溶液中分别加入少量氯水,分别发生了什么反应?
在溴化亚铁溶液和碘化亚铁溶液中分别加入少量氯水,分别发生了什么反应?
反应的方程式分别是什么? sweetsecho331年前2
sweetsecho331年前2 -
 hh一号1 共回答了18个问题
hh一号1 共回答了18个问题 |采纳率88.9%还原性:I->Fe2+>Br-
6FeBr2+3Cl2(少)=4FeBr3+2FeCl3
-----只氧化Fe2+
FeI2+Cl2(少)=FeCl2+I2
-----只氧化I-1年前查看全部
- 碘化亚铁溶液中通入少量氯气反应方程式
碘化亚铁溶液中通入少量氯气反应方程式
1.碘化亚铁溶液中通入 少量氯气 反应方程式
2.碘化亚铁溶液中通入 过量氯气 反应方程式 明天的梦想1年前2
明天的梦想1年前2 -
 fengyefengyu 共回答了18个问题
fengyefengyu 共回答了18个问题 |采纳率100%因为I-的还原性大于Fe2+
所以若通入少量氯气会全部与碘离子反应,若是过量氯气才生成Fe3+
碘化亚铁溶液中通入 少量氯气
Cl2 + 2 I- = I2 + 2 Cl-
Cl2 + FeI2 = FeCl2 + I2
碘化亚铁溶液中通入 过量氯气
2 Fe2+ + 4 I- + 3 Cl2 = 2 Fe3+ + I2 + 6 Cl-
3 Cl2 + 2 FeI2 = 2 FeCl3 + 2 I2
1年前查看全部
- 氯气与碘化亚铁 (2:3)怎么反应
 禹彤1年前3
禹彤1年前3 -
 淡淡花田 共回答了13个问题
淡淡花田 共回答了13个问题 |采纳率92.3%由于铁离子可以氧化 碘离子 所以氯气先和碘离子发生反应
氯气和碘离子的反应是1:1的
所以 碘离子过量
这个反应最后生成FeCl2+I21年前查看全部
- 下列离子方程式正确的是( ) A.向碘化亚铁溶液中通入少量氯气 2Fe 2+ +Cl 2 =2F
下列离子方程式正确的是( )
A.向碘化亚铁溶液中通入少量氯气 2Fe 2+ +Cl 2 =2Fe 3+ +2Cl - B.向硫酸氢钠溶液中滴入氢氧化钡溶液至中性 2H + +SO 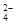 +Ba 2+ +2OH - =BaSO 4 ↓+2H 2 O
+Ba 2+ +2OH - =BaSO 4 ↓+2H 2 OC.向次氯酸钙溶液中通入过量二氧化硫 Ca 2+ +2ClO - +SO 2 +H 2 O=CaSO 3 ↓+2HClO D.将氢氧化铁粉末加入氢碘酸中 Fe(OH) 3 +3H + =Fe 3+ +3H 2 O  y8wa9gew1年前1
y8wa9gew1年前1 -
 josisi 共回答了16个问题
josisi 共回答了16个问题 |采纳率93.8%B
正确答案:B
A、应为:Cl 2 +2I ― =I 2 +2Cl ―
B、正确
C、应为:Ca 2+ +ClO - +SO 2 +H 2 O=CaSO 4 ↓+2H + +Cl ―
D、应为:2Fe(OH) 3 +2I ― +6H+ 2 =Fe 3+ +6H 2 O+I 2 :、1年前查看全部
- 碘化亚铁与氯气反应的情况碘化亚铁如果是固体 不是溶液 会反应吗
 nigeldong1年前3
nigeldong1年前3 -
 xi_mi_gao 共回答了21个问题
xi_mi_gao 共回答了21个问题 |采纳率85.7%光照或加热就会.1年前查看全部
- 溴化亚铁、碘化亚铁分别与过量和少量氯气反应.(共四个方程式),谢谢、急用.
 零下_1年前1
零下_1年前1 -
 旺旺19841122 共回答了22个问题
旺旺19841122 共回答了22个问题 |采纳率95.5%6FeBr2+3Cl2=4FeBr3+2FeCl3(少)
2FeBr2+3Cl2=2FeCl3+2Br2(多)
FeI2+Cl2=FeCl2+I2(少)
2FeI2+3Cl2=2FeCl3+2I2(多)1年前查看全部
- 碘化亚铁中滴加少量溴水溴先氧化的是碘离子,溴化亚铁中滴加氯水为什么先氧化亚铁离子,
碘化亚铁中滴加少量溴水溴先氧化的是碘离子,溴化亚铁中滴加氯水为什么先氧化亚铁离子,
他们的还原性怎么排 大周华健1年前1
大周华健1年前1 -
 yybbs 共回答了17个问题
yybbs 共回答了17个问题 |采纳率94.1%还原性I->Fe2+>Br->Cl-
氧化性Cl2>Br2>Fe3+>I2
所以在碘化亚铁中滴加少量溴水,先氧化I-;溴化亚铁中滴加氯水,先氧化Fe2+1年前查看全部
- 2.5摩尔的氯气与2摩尔的碘化亚铁反应的化学方程式.
2.5摩尔的氯气与2摩尔的碘化亚铁反应的化学方程式.
2I~+Cl2=I2+2Cl~为离子符号】 啊庆1年前1
啊庆1年前1 -
 ecnuyf 共回答了20个问题
ecnuyf 共回答了20个问题 |采纳率75%5Cl2 + 4FeI2 =2FeCl2 + 2FeCl3 + 4I2
5 4
2.5 2
离子方程式:5Cl2 + 2Fe2+ + 8I- =2Fe3+ + 10Cl- + 4I21年前查看全部
- 氯气能不能和碘化亚铁反应生成氯化铁和碘化铁,为什么
 沧海笑robert1年前1
沧海笑robert1年前1 -
 wislimin 共回答了23个问题
wislimin 共回答了23个问题 |采纳率91.3%不可以,Cl2优先氧化I-,再说FeI3不存在,自身发生氧化还原.2Fe3+ + 2I- =2Fe2+ + I21年前查看全部
- 碘化亚铁与少量稀硝酸反应的化学方程式与离子式,求详解,如何写的过程
 根据我多年的经验1年前6
根据我多年的经验1年前6 -
 缴_枪_不_杀 共回答了19个问题
缴_枪_不_杀 共回答了19个问题 |采纳率100%碘离子还原性强于亚铁离子,HNO3先与碘离子反应.若HNO3量略多再与亚铁离子反应
6I- +2NO3 - +8H+ =3I2 +2NO↑+4H2O
3Fe2+ 十NO3- 十 4H+ =3Fe3+ 十NO↑十2H2O1年前查看全部
- 一定量氯气和碘化亚铁反应时,三价铁离子和二价铁离子浓度相等时的化学方程式
 终要长大1年前2
终要长大1年前2 -
 sunshlee 共回答了15个问题
sunshlee 共回答了15个问题 |采纳率80%2Cl2+2Fe2+ +2I-=====2Fe3+ +I2 +4Cl-1年前查看全部
- 少量氯气分别和溴化亚铁、碘化亚铁反应离子方程式 有把握的帮帮忙!
 小鸟xiaochong1年前3
小鸟xiaochong1年前3 -
 爱上一只不回家的羊 共回答了22个问题
爱上一只不回家的羊 共回答了22个问题 |采纳率95.5%解决这一个题型的话关键在于,氯气与三种离子反应的顺序,依次为,碘离子,二价铁,溴离子.再跟据氯气用量决定最后和几种离子反应.1年前查看全部
- 碘化亚铁溶液中通入过量氯气反应的现象是什么?方程式和例子反应式怎么写?
 wuqulong1年前1
wuqulong1年前1 -
 年迈的狼 共回答了16个问题
年迈的狼 共回答了16个问题 |采纳率81.3%呀,我是飞柔望极春愁,刚才没看清楚.应该是(2Fe2+)+4I-+3Cl2=(2Fe3+)+I2+6Cl- 2FeI2+3Cl2=2FeCl3+2I21年前查看全部
- 下列离子方程式正确的是( )A.过量氯气通入碘化亚铁溶液中:Cl2+Fe2++2I-=2Cl-十Fe3++I2B.向N
下列离子方程式正确的是( )
A.过量氯气通入碘化亚铁溶液中:Cl2+Fe2++2I-=2Cl-十Fe3++I2
B.向NaHCO3溶液中加入少量澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-
C.H218O中投入少量Na2O2固体:2H218O+2 Na2O2=4Na++4OH-+18O2↑
D.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:H++SO42-+Ba2++OH-═BaSO4↓+H2O jiangzhe001年前1
jiangzhe001年前1 -
 junjun_2005 共回答了19个问题
junjun_2005 共回答了19个问题 |采纳率89.5%解题思路:A.碘离子、亚铁离子均被氧化;
B.反应生成碳酸钙、水、碳酸钠;
C.只有过氧化钠中O得失电子;
D.至SO42-恰好完全沉淀,以1:1反应生成硫酸钡、水、NaOH.A.过量氯气通入碘化亚铁溶液中的离子反应为3Cl2+2Fe2++4I-=6Cl-+2Fe3++2I2,故A错误;
B.向NaHCO3溶液中加入少量澄清石灰水的离子反应为2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-,故B正确;
C.H218O中投入少量Na2O2固体的离子反应为2H218O+2 Na2O2=4Na++4OH-+218OH-+O2↑,故C错误;
D.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀的离子反应为H++SO42-+Ba2++OH-═BaSO4↓+H2O,故D正确;
故选BD.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应考查,注重基础知识的夯实,题目难度不大.1年前查看全部
- xmol氯气通入含amol碘化亚铁溶液中充分反应,写出该反应的化学方程式(已知a
 zjxyyp6591年前4
zjxyyp6591年前4 -
 lxslfree 共回答了21个问题
lxslfree 共回答了21个问题 |采纳率90.5%aFeI2+xCl2=(3a-2x)FeCl2+(2x-2a)FeCl3+aI2
即当a=x 没有FeCl3
当x=1.5a没有FeCl2
所以a1年前查看全部
- 氯气和碘化亚铁反应 请写出当有一半的亚铁离子变成铁离子时的方程式.
 遗忘是一种幸福1年前2
遗忘是一种幸福1年前2 -
 泊无地 共回答了19个问题
泊无地 共回答了19个问题 |采纳率89.5%Fe2+离子被氧化了,则I-已经全部被氧化了.
1 mol的 FeI2 就得到 0.5 的Fe3+ ,和1 mol的 I2 ,
根据得失电子守恒,Cl2为 (0.5+2)/2==1.25 mol ,Cl- 就是 2.5 mol
则 方程为 0.5Fe2+ +2I- + 1.25Cl2 ==0.5Fe3+ +I2 +2.5Cl-
乘以4 化为整数就是 : 2Fe2+ +8I- + 5Cl2 ==2Fe3+ +4I2 +10Cl-1年前查看全部
- 1mol碘化亚铁与1.2mol氯气反应.请讲一下反应过程和离子方程式.
 彦云1年前4
彦云1年前4 -
 人间八月天 共回答了21个问题
人间八月天 共回答了21个问题 |采纳率100%Cl2>Br2>Fe3+>I2>S,故先有2I-+CL2=I2+2CL-(氧化出1mol I2,剩0.2molCL2)
再有2FE2+CL2=2FE3+2CL-(氧化出0.2mol FE3+,剩0.8mol FE3+)1年前查看全部
- 向碘化亚铁溶液中通入足量Cl2的方程式是2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-对吗?错的话请解释原因
 简单红茶1年前3
简单红茶1年前3 -
 清辉玉碧寒 共回答了14个问题
清辉玉碧寒 共回答了14个问题 |采纳率85.7%错,有2点都错了,楼上只说了1点
首先,CL2通入FEI2中应该首先和I-发生反应
因为还原性 I- 强于 FE2+
所以楼上说错了,应该是先和碘离子反应完了才和铁离子反应
又足量氯气和以上物质反应,则FEI2应该就是不足量的
不足量的物质写离子方程式 各离子应满足化学式的计量关系,所以你写错了,正确的应该是
足量氯气和FEI2反应
3CL2 + 4I- + 2FE2+ = 2FE3+ + 2I2沉淀 +6CL-1年前查看全部
- 少量或过量的氯气通入碘化亚铁的离子方程式.
 可乐一虾之暗1年前1
可乐一虾之暗1年前1 -
 一遍激活 共回答了17个问题
一遍激活 共回答了17个问题 |采纳率94.1%少量Cl2气,只与I(-)反应,不与Fe(2+)反应:
Cl2 + 2I(-) = 2Cl(-) + I2
过量Cl2,Fe(2+)也参与反应,且I2会继续氧化(对中学生来说难度不小了):
7Cl2 + 4I(-) + 2Fe(2+) = 2Fe(3+) + 2IO3(-) + 14Cl(-)1年前查看全部
- 1mol碘化亚铁与1.2mol氯气反应.请讲一下反应过程和离子方程式.
 卡车Q1年前2
卡车Q1年前2 -
 杯子把儿 共回答了17个问题
杯子把儿 共回答了17个问题 |采纳率94.1%2FE2+CL2=2FE3+2CL-(氧化出1mol FE3+,剩0.2molCL2)
2I-+CL2=I2+2CL-(氧化出0.2mol I2,剩下1.6mol I-)1年前查看全部
- 氯气和碘化亚铁在水中能否反应?为什么?
 tangliuji1年前1
tangliuji1年前1 -
 wbrock 共回答了15个问题
wbrock 共回答了15个问题 |采纳率100%能反应方程式分为两种情况!第一种氯气不足氯气与碘化亚铁比例小于1,Cl2+2I-=I2+2Cl-,比例大于1,3Cl2+2Fe2++4I-=2Fe3++6Cl-+2I21年前查看全部
- 碘化亚铁溶液通入少量氯气会发生反应吗?会生成什么?
 橄榄树下的人1年前1
橄榄树下的人1年前1 -
 liyunone 共回答了18个问题
liyunone 共回答了18个问题 |采纳率83.3%上面的答案是错的
会反应,但生成碘单质和氯化亚铁
因为碘离子的还原性大于亚铁离子大于溴离子,所以若通入少量氯气会全部与碘离子反应,若是过量氯气才生成3价的铁离子1年前查看全部
- 为什么碘化亚铁中加入氯水呈黄色
 哂麽鬪荹箽1年前4
哂麽鬪荹箽1年前4 -
 c_heng 共回答了20个问题
c_heng 共回答了20个问题 |采纳率95%因为,氯水中的氯把碘化亚铁中的亚铁氧化成了三价的铁离子,三价铁显黄色.1年前查看全部
- 碘化亚铁和氯水反映,和碘化亚铁和氯气反映 的化学方程式怎么不一样.怎么回事啊?
 cejack1年前3
cejack1年前3 -
 mengyuan_2008 共回答了17个问题
mengyuan_2008 共回答了17个问题 |采纳率88.2%氯水的成分:分子:H2O Cl2 HClO 离子:H+ Cl- ClO- OH-
氯气的成分:Cl2
成分不同,发生的反应自然不同,1年前查看全部
- 碘化亚铁与氯水反应生成什么求迅速!题目中是FeI2 是碘化铁?
 lvskiller1年前2
lvskiller1年前2 -
 谁胡说八道 共回答了19个问题
谁胡说八道 共回答了19个问题 |采纳率94.7%1:氯气少量Cl2 + 2Fe2+ = 2Fe3+ + 2Cl-
2:氯气过量2Cl2 + 2Fe2+ + 2I- = 2Fe3+ + I2 + 4Cl-1年前查看全部
- 除去氯化亚铁中的碘化亚铁选用什么试剂
 我们家的殿菲哥1年前2
我们家的殿菲哥1年前2 -
 kuoge 共回答了15个问题
kuoge 共回答了15个问题 |采纳率86.7%1加过量FeCl3 2Fe3+ + 2I-===I2 + 2Fe2+
2 加过量Fe粉 2Fe3+ + Fe==3Fe2+
3 过滤 弃去滤渣即可1年前查看全部
- 将少量氯水滴加到碘化亚铁溶液中,为什么只有碘离子被氧化,亚铁离子为什么不被氧化?
 JACKHDT1年前3
JACKHDT1年前3 -
 kejiazhouq 共回答了23个问题
kejiazhouq 共回答了23个问题 |采纳率95.7%氯水具有氧化性,碘离子和亚铁离子具有还原性,他们的还原性不同,碘的强于亚铁的,所以要碘离子完全被氯水还原之后有剩余的才能和亚铁反应,所以少量氯水滴加到碘化亚铁溶液中,只有碘离子被氧化,发生氧化还原反应1年前查看全部
- 化学知识 求解!请问 碘化亚铁 与溴 单质 分别过量 应该如何反应 请写出方程式 谢谢
 wenlongxlc1年前5
wenlongxlc1年前5 -
 93019301 共回答了9个问题
93019301 共回答了9个问题 |采纳率88.9%若碘化亚铁过量:
FeI2+Br2==FeBr2+I2
若溴过量:2FeI2+3Br2==2FeBr3+2I2
原因:这是因为氧化性Br2>Fe3+>I2,因此如果碘化亚铁过量,溴优先将碘离子氧化,但如果溴过量,他就把二价铁离子也氧化了
若还有问题,欢迎追问哦1年前查看全部
- 氯气渐渐通入碘化亚铁的反应分布的.
 lei99991年前2
lei99991年前2 -
 139739zhusi 共回答了21个问题
139739zhusi 共回答了21个问题 |采纳率90.5%上面的答案是错的会反应,但生成碘单质和氯化亚铁因为碘离子的还原性大于亚铁离子大于溴离子,所以若通入少量氯气会全部与碘离子反应,若是过量氯气才生成31年前查看全部
- 有书上说铁与碘反应可以生成碘化亚铁,但是这不是与"亚铁离子的还原性比碘离子弱相矛盾吗?
有书上说铁与碘反应可以生成碘化亚铁,但是这不是与"亚铁离子的还原性比碘离子弱相矛盾吗?
在铁与碘的反应中,铁把碘还原了 abcazpq1年前1
abcazpq1年前1 -
 加号 共回答了17个问题
加号 共回答了17个问题 |采纳率100%没矛盾啊,如果在碘化亚铁中加入少量氧化剂,碘离子先被氧化成单质碘.1年前查看全部
- 请问 碘化亚铁 与溴 单质 分别过量 应该如何反应 请写出方程式
 HBLinx1年前3
HBLinx1年前3 -
 Crystal25 共回答了19个问题
Crystal25 共回答了19个问题 |采纳率94.7%若碘化亚铁过量:
FeI2+Br2==FeBr2+I2
若溴过量:2FeI2+3Br2==2FeBr3+2I2
原因:这是因为氧化性Br2>Fe3+>I2,因此如果碘化亚铁过量,溴优先将碘离子氧化,但如果溴过量,他就把二价铁离子也氧化了
若还有问题,欢迎追问哦1年前查看全部
- 氯气通入到碘化亚铁溶液中发生的化学反应
氯气通入到碘化亚铁溶液中发生的化学反应
分氯气少量,足量和过量 jason2007i91年前1
jason2007i91年前1 -
 renbing_ok 共回答了20个问题
renbing_ok 共回答了20个问题 |采纳率90%少量 2 I- + Cl2 = I2 + 2 Cl-过量 3 Cl2 + 4 I- + 2 Fe2+ = 6 Cl- +2 I2 +2 Fe3+ 足量I2+5Cl2+6H2O=2IO3- +10Cl- +12H+1年前查看全部
- 等物质的量的氯气和碘化亚铁离子反应方程式怎么写的?
等物质的量的氯气和碘化亚铁离子反应方程式怎么写的?
急求.望各路好汉伸手相助 50806_vv1年前2
50806_vv1年前2 -
 xinwu587 共回答了14个问题
xinwu587 共回答了14个问题 |采纳率85.7%1mol的氯气和2mol的碘离子生成2mol的氯离子和1mol碘单质,因为碘离子还原性比亚铁强.1年前查看全部
- 碘化亚铁与少量氯水反应的方程式
 whbjx1年前1
whbjx1年前1 -
 mm需尚武 共回答了18个问题
mm需尚武 共回答了18个问题 |采纳率94.4%先和碘离子反应,后和二价铁离子反应
2I-+Cl2=I2+2Cl-1年前查看全部
- 在溴化亚铁和碘化亚铁中通入氯气,可能发生的反应
 不做mm1年前1
不做mm1年前1 -
 修山民 共回答了21个问题
修山民 共回答了21个问题 |采纳率81%向溴化亚铁溶液通入足量的氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
向溴化亚铁溶液通入少量氯气:2Fe2++Cl2=2Fe3++2Cl-
向碘化亚铁溶液通入足量氯气:2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-
向碘化亚铁溶液通入少量氯气:2I-+Cl2=I2+2Cl-
记着:氧化性由强到弱为:Cl2>Br2>Fe3+>I2
还原性则相反.氧化剂先和还原性强的还原剂反应,在和还原性弱的反应.
所以氯气先和二价铁离子反应再和溴离子反应.
在碘化亚铁中就先和碘离子反应
少量 2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
足量2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 6Cl- + 2Br21年前查看全部
- 有书上说铁与碘反应可以生成碘化亚铁,但是这不是与"亚铁离子的还原性比碘离子弱相矛盾吗?
 天客游涯1年前1
天客游涯1年前1 -
 wxdan12 共回答了11个问题
wxdan12 共回答了11个问题 |采纳率90.9%没问题啊,碘化亚铁一个是亚铁,一个是典离子,还原性强弱有什么关系?不是问一个亚铁一个是典或者一个铁离子一个典离子啊
如果在碘化亚铁中加入少量氧化剂,碘离子先被氧化成单质碘.1年前查看全部
- 在水溶液中碘化亚铁为什么不能和氯气反应?请从氧化还原的角度来解释.
在水溶液中碘化亚铁为什么不能和氯气反应?请从氧化还原的角度来解释.
已知氯化铁的还原性>碘单质 大龄女yy1年前1
大龄女yy1年前1 -
 百合咚儿 共回答了20个问题
百合咚儿 共回答了20个问题 |采纳率100%可以反应的
在水溶液中,碘离子还原性大于二价铁,所以氯气会先把碘离子氧化,然后氧化二价铁,如果氯气足够,最终的产物是氯化铁,单质碘!1年前查看全部
- 氯气为什么不能和碘化亚铁反应
 宿命1年前1
宿命1年前1 -
 pilmegt 共回答了10个问题
pilmegt 共回答了10个问题 |采纳率100%你说的没错,但你别忘了还有一个氧化性更弱的碘离子,如果是过量的氯气,那么氯气在和碘离子反应后就和亚铁离子反应1年前查看全部
- 氯气为什么不能和碘化亚铁反应
 飞雪飘客1年前1
飞雪飘客1年前1 -
 表妹25 共回答了12个问题
表妹25 共回答了12个问题 |采纳率91.7%你说的没错,但你别忘了还有一个氧化性更弱的碘离子,如果是过量的氯气,那么氯气在和碘离子反应后就和亚铁离子反应1年前查看全部
- a mol碘化亚铁和b mol氯气反应的化学方程式
 上不去了1年前2
上不去了1年前2 -
 吾忘我 共回答了20个问题
吾忘我 共回答了20个问题 |采纳率90%2aFeI2+3bCl2=2bFeCl3+2aI21年前查看全部
- 碘化亚铁和氯气反应的方程式子是什么?
 johe991年前1
johe991年前1 -
 家中女人 共回答了19个问题
家中女人 共回答了19个问题 |采纳率89.5%碘离子还原性强于亚铁离子,先被氧化
所以氯气不足时只有碘离子被氧化,氯气足量时碘离子、亚铁离子都被氧化,氯气过量时甚至能被碘单质氧化成碘酸根离子1年前查看全部
- 氯气与碘化亚铁反应是不是有两个方程式
氯气与碘化亚铁反应是不是有两个方程式
一个是那个置换反应
一个是那个氯气把 Fe2+和I-都氧化生成氯化铁和碘单质的那个(这个不太确定 如果要是没有这个 请说明为什么) 温州飞云江1年前1
温州飞云江1年前1 -
 wbwdy 共回答了19个问题
wbwdy 共回答了19个问题 |采纳率84.2%不足量的话置先换出碘单质
足量的话不仅置换出碘,还把亚铁离子氧化成铁离子1年前查看全部
大家在问
- 1有A、B两个物体,叠放,上A下B,都是20N,当拉力为10牛时,两物体一起做匀速直线运动,B受到的阻力是多少?
- 2如图,已知AD为三角形ABC的高,E为AC上的一点,B交AD于F,且有BF=AC,FD=CD.求证:BE垂直AC
- 3已知a属于(0,π/4)B属于(0,π)且tan(a-B)=1/2,tanB=-1/7,求tan(2a-B)的值及角2a
- 4如果空气中没有二氧化碳,将会出现什么样的后果?
- 5关于匀变速直线运动的一道题目求解答
- 6I hope you get better soon.这个句子有错吗?
- 7①铁锅作炊具主要是利用铁的______性.
- 8on earth you want?
- 9教下2道数学题~谢咯1、一个同学进行多边形内角和计算时求得内角和为2748度、当发现错了后、重新检查发现少加了一个内角,
- 10阅读教材相关内容,简述人类进化经历的几个主要阶段。 1.南方古猿(1)时间:距今约100万年~400万年前。
- 111 巴西的矿产资源主要分布在哪部?其中铁矿石主要分布的地形区是什么?
- 1250g镁,锌,铝的混合物与适量的稀硫酸反应,结晶成晶体(不含结晶水)218g,则反应中H2的质量
- 13英语翻译
- 14在科学探究中,提出的假设总是与实验结果相一致。(这句话是否正确?试试说明理由)
- 15高一物理题.关于加速度的一跳伞员从高空离开直升机落下,开始未打开伞,先做匀加速直线运动,落下一段距离后才打开伞,打开伞后

