(2013•册亨县模拟)下列反应中属于复分解反应的是( )
 LIZHUJIAN372022-10-04 11:39:541条回答
LIZHUJIAN372022-10-04 11:39:541条回答A.NaOH+HCl=NaCl+H2O
B.2H2O
| ||
C.2Mg+O2
| ||
D.Zn+H2SO4=ZnSO4+H2↑

已提交,审核后显示!提交回复
共1条回复
 水玲珑杨静 共回答了20个问题
水玲珑杨静 共回答了20个问题 |采纳率75%- 解题思路:复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,据此进行分析判断.
A、该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项正确.
B、该反应符合“一变多”的特征,属于分解反应,故选项错误.
C、该反应符合“多变一”的特征,属于化合反应,故选项错误.
D、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误.
故选D.点评:
本题考点: 复分解反应及其应用.
考点点评: 本题难度不大,掌握复分解反应的特征(换成分、价不变)并能灵活运用是正确解答本题的关键. - 1年前
相关推荐
- (2013•册亨县模拟)(1)某试验小组在研究二氧化碳的性质时,利用如图所示试验装置进行试验.回答下列问题.
(2013•册亨县模拟)(1)某试验小组在研究二氧化碳的性质时,利用如图所示试验装置进行试验.回答下列问题.
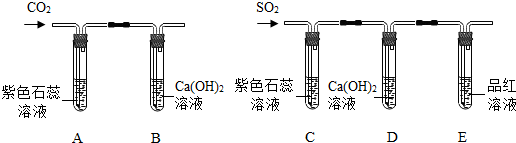
A中的现象是______;
B中反应的化学方程式是______.
(2)该小组利用对比的方法研究二氧化硫的性质,进行如下探究.
【提出问题】二氧化硫与二氧化碳均属于非金属氧化物,是否具有相似的化学性质呢?
【查阅资料】二氧化硫具有漂白性,其原因是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,实验室常用红色的品红溶液检验二氧化硫的存在.
【试验探究】试验装置如图所示.
①装置C中紫色石蕊溶液变红,是由于二氧化硫与水反应生成了亚硫酸(H2SO3);装置D中澄清石灰水变浑浊,该反应的化学方程式是______.
②装置E的试管中溶液变无色,取该溶液加热,溶液又变为红色,其原因是______.
③此装置有一个明显的不足之处是______.
④活性炭也能使品红溶液褪色,其褪色原理与二氧化硫使品红溶液褪色的原理不相同,其理由______
【反思提高】某同学将二氧化硫通入到紫色的酸性高锰酸钾溶液中,观察到溶液由紫色变为无色,由此他得出的结论是:二氧化硫能将酸性高锰酸钾溶液漂白.请你设计试验证明此结论是否正确(要求写出操作、现象、结论)______.
【试验结论】二氧化硫与二氧化碳有相似的化学性质,但二氧化硫还具有某些特殊的化学性质. 老驴驴1年前1
老驴驴1年前1 -
 抚凌云自惜 共回答了18个问题
抚凌云自惜 共回答了18个问题 |采纳率94.4%解题思路:(1)依据二氧化碳溶于水生成碳酸,二氧化碳与石灰水反应生成碳酸钙的知识分析解决;
(2)①根据二氧化硫能与石灰水反应生成白色的亚硫酸钙的知识解决;
②依据题干中有关二氧化硫的使溶液褪色的原理分析判断;
③依据二氧化硫是有毒气体,需进行尾气处理的知识分析判断;
④从两者使物质褪色的变化类型分析判断;
【反思提高】根据二氧化硫的漂白原理进行分析判断即可(1)二氧化碳溶于水生成碳酸,碳酸能使石蕊变红,二氧化碳与石灰水反应生成碳酸钙沉淀和水,所以溶液变浑浊;
(2)①结合题干中的叙述可知:二氧化硫能与石灰水反应生成白色的亚硫酸钙和水,其方程式为:SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫的使溶液褪色的原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以取该溶液加热,溶液又变为红色,其原因是二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③二氧化硫是有毒气体,不能排放到空气中污染空气,所以该装置需进行尾气处理以防空气污染;
④两者使物质褪色的变化类型不同:活性炭的吸附溶液褪色的过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】二氧化硫的漂白原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以可进行如下设计:将褪色的溶液加热,观察溶液颜色的变化,若溶液恢复为原来的颜色,则结论正确,否则错误.
故答案为:(1)溶液变红,CO2+Ca(OH)2═CaCO3↓+H2O;
(2)①SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③没有进行尾气处理;
④活性炭的吸附过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】将褪色后的溶液加热,观察溶液颜色变化,若溶液恢复为紫色,则此结论是正确的;若溶液不能恢复为紫色,则此结论不正确.点评:
本题考点: 二氧化碳的化学性质;实验探究物质的性质或变化规律.
考点点评: 此题是一道实验设计题,解题的关键是掌握二氧化碳的性质并进行知识的大胆迁移,只有这样才能顺利解题.1年前查看全部
- (2013•册亨县模拟)4支排球队进行单循环比赛(参加比赛的每两支球队之间都要进行一场比赛),则总的比赛场数为_____
(2013•册亨县模拟)4支排球队进行单循环比赛(参加比赛的每两支球队之间都要进行一场比赛),则总的比赛场数为______场.
 不寐听江1年前0
不寐听江1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•册亨县模拟)我校九年级(1)班共有54人,据统计,参加读书节活动的18人,参加科技节活动的占全班总人数的[1
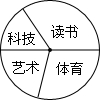 (2013•册亨县模拟)我校九年级(1)班共有54人,据统计,参加读书节活动的18人,参加科技节活动的占全班总人数的[1/6],参加艺术节活动的比参加科技节活动的多3人,其他同学参加体育节活动.则在扇形图中表示参加体育节活动人数的扇形的圆心角是______度.
(2013•册亨县模拟)我校九年级(1)班共有54人,据统计,参加读书节活动的18人,参加科技节活动的占全班总人数的[1/6],参加艺术节活动的比参加科技节活动的多3人,其他同学参加体育节活动.则在扇形图中表示参加体育节活动人数的扇形的圆心角是______度.  rr者小穆1年前1
rr者小穆1年前1 -
 爱吃鱼的老虎0535 共回答了15个问题
爱吃鱼的老虎0535 共回答了15个问题 |采纳率86.7%解题思路:因为参加科技节活动的占全班总人数的[1/6],参加艺术节活动的比参加科技节活动的多3人,所以可求出这两项活动的人数,则参加体育活动的人数可求,再除以总人数即可得到其在扇形中所占百分比,故其圆心角度数可求.参加科技节活动的人数为54×[1/6]=9人,
则参加艺术节活动的人数为9+3=12人,
所以参加体育活动的人数为54-18-9-12=15人,
其所占百分比为15÷54=28%,
则参加体育节活动人数的扇形的圆心角360°×28%=100.8°.
故答案为:100.8.点评:
本题考点: 扇形统计图.
考点点评: 本题考查扇形统计图及相关计算.在扇形统计图中,每部分占总部分的百分比等于该部分所对应的扇形圆心角的度数与360°的比.1年前查看全部
- (2013•册亨县模拟)化学与工农业生产、日常生活密切相关,回答下列问题.
(2013•册亨县模拟)化学与工农业生产、日常生活密切相关,回答下列问题.
(1)蔬菜、水果中富含的______能调节新陈代谢,维持人的身体健康.
(2)加钙牛奶中的“钙”是指钙______,身体中一旦缺钙,可能患有的疾病是______.
(3)下列物品中,所使用的主要材料属于天然纤维的是______
A.塑料保鲜膜B.橡胶手套C.棉布围裙D.玻璃杯
(4)化肥KH2PO4 属于______肥料,磷酸二氢钙的化学式为______. xuhuiweida1年前1
xuhuiweida1年前1 -
 o15732 共回答了23个问题
o15732 共回答了23个问题 |采纳率91.3%解题思路:(1)根据蔬菜、水果中富含维生素考虑;(2)加钙牛奶中的“钙”是指这一类原子的总称,根据缺钙得症状考虑;(3)根据天然纤维与三大合成材料的区别考虑;(4)根据肥料的鉴别方法和化学式的书写考虑.(1)蔬菜、水果中富含维生素,能调节新陈代谢,维持人的身体健康;
(2)加钙牛奶中的“钙”是指具有相同核电荷数的这一类原子的总称,所以属于钙元素;儿童缺钙易得佝偻病,成年人缺钙易得骨质疏松症;
(3)三大合成材料是:塑料、合成纤维、合成橡胶,塑料保鲜膜属于塑料,属于合成材料;橡胶手套属于合成橡胶,属于合成材料;玻璃杯属于无机非金属材料,棉布围裙属于天然纤维;
(4)KH2PO4 含有钾和磷两种营养素属于复合肥;由于磷酸二氢根显-1价,钙元素显+2价,根据正价在前,负价在后,十字交叉再约简,所以化学式是:
Ca(H2PO4)2.
故答案为:(1)维生素;(2)元素;佝偻病或骨质疏松;(3)C;(4)复合;Ca(H2PO4)2.点评:
本题考点: 生命活动与六大营养素;常见化肥的种类和作用;有机高分子材料的分类及鉴别;人体的元素组成与元素对人体健康的重要作用.
考点点评: 本题考查了常见食品中的营养物质,身体中缺乏元素的症状,材料的分类,化学肥料的分类和化学式的书写,题目比较简单.1年前查看全部
- (2013•册亨县模拟)如图1是某学生绘制的元素周期表的一部分. 1H
(2013•册亨县模拟)如图1是某学生绘制的元素周期表的一部分.

根据相关信息与知识回答下列问题.1H
氢2He
氦3Li
锂4Be
铍5B
硼6C
炭7N
氮8O
氧9F
氟10Ne
氖11Na
钠12Mg
镁13Al
铝14Si
硅15P
磷16S
硫17Cl
氯18Ar
氩
(1)1869年,俄国化学家______发现了元素周期律并编制了元素周期表.
(2)氦、氖、氩等稀有气体的化学性质很不活泼,原因是______.
(3)写出原子序数分别为8、13两种元素组成的化合物的化学式:______.
(4)仔细阅读和观察上表,其中有一种常见元素的元素名称书写有误,写出其正确的元素名称:______.
(5)上述元素在周期表中处于同一周期的依据是______.
(6)硫与氧气的反应(S+O2
SO2)如图2所示.点燃 .
设N个氧气分子的质量为32g,则64g氧气与足量硫粉完全反应生成的二氧化硫分子数为______N. Marshall_nb1年前1
Marshall_nb1年前1 -
 峰峰Dyiyi 共回答了20个问题
峰峰Dyiyi 共回答了20个问题 |采纳率100%解题思路:(1)根据化学家的贡献判断;
(2)根据最外层电子数决定了元素的化学性质分析;
(3)根据化合价书写化学式的方法;
(4)根据元素名称的特点进行解答;
(5)根据元素周期与电子层数的关系考虑;
(6)由硫与氧气的反应,可知其各物质的质量关系;N个氧气分子的质量为32g,完全反应生成的二氧化硫分子数为N个;则可求则64g氧气与足量硫粉完全反应生成的二氧化硫分子数.(1)门捷列夫发现元素周期律并编制出元素周期表,故答案为:门捷列夫;
(2)最外层电子数决定了元素的化学性质,氦、氖、氩等稀有气体的化学性质很不活泼是因为它们原子的最外层电子数均为8(氦是2),是稳定结构,故答案为:原子的最外层电子成稳定结构;
(3)原子序数是8的元素是氧,化合价为-2价,原子序数为13的元素是铝,化合价为+3价,所以氧化铝的化学式为Al2O3,故答案为:Al2O3;
(4)化学元素汉字名称的偏旁可辨别元素的种类,固态非金属元素名称有“石”字旁,所以表中碳元素写错.故答案为:碳;
(5)原子所处的周期数与该原子核外的电子层数相同,所以在周期表中处于同一周期的原子,核外电子层数相同.
故答案为:原子核外电子层数相同;
(6)由硫与氧气的反应(S+O2
点燃
.
SO2),可知其各物质的质量关系;N个氧气分子的质量为32g,完全反应生成的二氧化硫分子数为N个;64g氧气含有2N个氧气分子,故64g氧气与足量硫粉完全反应生成的二氧化硫分子数为2N.
故答案为:2.点评:
本题考点: 元素周期表的特点及其应用;微粒观点及模型图的应用.
考点点评: 本题考查学生根据元素周期表,辨别元素种类的方法,最外层电子数相同的元素化学性质相似进行分析解题,将元素周期律灵活应用的能力.1年前查看全部
- (2013•册亨县模拟)4的算术平方根是( )
(2013•册亨县模拟)4的算术平方根是( )
A.-4
B.4
C.-2
D.2 就是不停1年前1
就是不停1年前1 -
 ksn96112 共回答了21个问题
ksn96112 共回答了21个问题 |采纳率90.5%解题思路:根据算术平方根的定义解答即可.∵22=4,
∴4的算术平方根是2,
即
4=2.
故选D.点评:
本题考点: 算术平方根.
考点点评: 本题考查了算术平方根的定义,是基础题,熟记概念是解题的关键.1年前查看全部
- (2013•册亨县模拟)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
(2013•册亨县模拟)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
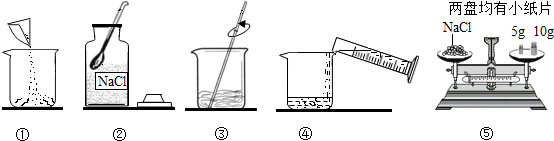
(1)用如图表示的序号表示配制溶液的正确操作顺序______.
(2)图②中,有一种塑料仪器,其名称是______.
(3)称量NaCl时,天平平衡后的状态如图所示,游码标尺示数见图,则称取得NaCl质量为______.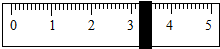
(4)根据计算需要量取水的体积是______(水的密度为1g/mL).量取读数时,如图视线角度正确的是______.(选填字母序号)
 tengfeiclever1年前1
tengfeiclever1年前1 -
 barbaraqu 共回答了19个问题
barbaraqu 共回答了19个问题 |采纳率89.5%解题思路:(1)据配制一定溶质质量分数的溶液的步骤回答;
(2)药匙是塑料仪器;
(3)称量物的质量=砝码的质量+游码的质量;
(4)由溶质的质量分数计算溶液的质量,溶剂的质量=溶液的质量-溶质的质量,并据水的密度计算其体积,利用量筒量取液体读数时视线要与液体凹液面的最低处保持水平.(1)配制溶质质量分数为10%的NaCl溶液的步骤是:计算、称量、量取、溶解;
(2)药匙是塑料仪器;
(3)根据称量物的质量=砝码的质量+游码的质量可知:称取得NaCl质量为10g+5g+3.2g=18.2g;
(4)所配溶液的质量为:[18.2g/10%]=182g,所以需要水的质量是182g-18.2g=163.8g,水的密度为1g/mL,即需要水的体积为163.8mL;量取读数时,视线角度正确的是D;
故答案为:(1)②⑤①④③;(2)药匙;(3)18.2g;(4)163.8mL;D.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 了解并会熟练应用配制溶液的相关知识、及溶质的质量分数、量筒的使用等知识,即可顺利解答.1年前查看全部
大家在问
- 1怎样笔不离纸地画四条直线,并通过下面这九个点?一定要笔不离纸呀!
- 2如图,四边形ABCD的对角线AC,BD交于点O,MN分别是AB,CD的中点,连接MN交BD,AC于P,Q,角OPQ=角O
- 3解方程:x-2/5X(x-15)=69
- 4have a hard time with 和 have problems with可以互换么
- 5父子的果园 作文
- 6_____my teacher,after all 10 years.was my unforgettable mome
- 7(2012•蒙城县模拟)图A给出物体AB及像A′B′的位置,请在图中画出凸透镜及其焦点F的大致位置.
- 8一种液体A,B的比例是5:4,现有30的量,如何去分配A,B之间的配比量,请帮忙计算下公式
- 9______do you like him?He _____ so serious.每空一词,麻烦做下
- 10写一篇英语作文《How do you spend your winten vocation》
- 11直线y=−12x被圆C:x2+y2-2x-4y-4=0截得的弦长为( )
- 12rain and tears are the same
- 13⒈再小数乘法算试中,小数连乘按照(?)的顺序来计算,乘加、乘减中,先算(?)再算(?),有括号的先算(?).⒉计算“29
- 14新人学英语,音标等等什么的本人都很差,可以说是一事无成的样子,但不能这样过下去吧!
- 15帮我改篇作文 字数到550 一个字不能少
