亚铁离子和浓硫酸反应的离子方程式.亚铁离子和稀硝酸、浓硝酸的反应条件以及和浓硫酸的反应条件
 明哲熙2022-10-04 11:39:541条回答
明哲熙2022-10-04 11:39:541条回答
亚铁离子和浓硫酸反应的离子方程式.亚铁离子和稀硝酸、浓硝酸的反应条件以及和浓硫酸的反应条件
1、亚铁离子和浓硫酸反应的离子方程式
2、亚铁离子和稀硝酸、浓硝酸的反应条件以及和浓硫酸的反应条件
1、亚铁离子和浓硫酸反应的离子方程式
2、亚铁离子和稀硝酸、浓硝酸的反应条件以及和浓硫酸的反应条件

已提交,审核后显示!提交回复
共1条回复
 王石三 共回答了18个问题
王石三 共回答了18个问题 |采纳率94.4%- 1.2Fe2+ + 4H+ + SO4^2- == 2Fe3+ + SO2(气体) + 2H2O
2.亚铁离子和稀硝酸、浓硝酸及浓硫酸的反应都是溶液中自发进行的氧化还原反应,不需要条件. - 1年前
相关推荐
- 怎么区分铁离子和亚铁离子
 七七水妖1年前1
七七水妖1年前1 -
 天-堂-水 共回答了21个问题
天-堂-水 共回答了21个问题 |采纳率90.5%三价铁离子的特效鉴别方法是,在溶液中滴加KSCN溶液:得到红色溶液,证明容易中含有Fe3+.
如果这两种离子存在与同一溶液中,鉴别方法:先取一份,加硫氰化钾溶液,变血红色,有铁离子存在;再取另一份,加酸性高锰酸钾,褪色,说明有亚铁离子存在.1年前查看全部
- 铁在反应中怎样区分亚铁离子还是铁离子
铁在反应中怎样区分亚铁离子还是铁离子
区分生成物 不好意识打错了 那它会不会只给你一 个方程司 而不告诉你 颜色呢? porcelethch1年前1
porcelethch1年前1 -
 feison 共回答了15个问题
feison 共回答了15个问题 |采纳率86.7%如果是在考试中出现这类问题,就通过反应物质的氧化性强弱和量来确定:反应物如果氧化性弱,如氢离子,则产生的是亚铁离子,如果氧化性强,如高锰酸根离子,且量足够多,则产生铁离子,如果量不够多,通过计算来确定结果为亚铁离子还是铁离子与亚铁离子共存(铁离子氧化性很强,能氧化Fe)1年前查看全部
- 含有三价铁离子的溶液都是黄色的,但是实际是红褐色的 含有亚铁离子的溶液都是浅绿色的,但是实际是白色的
含有三价铁离子的溶液都是黄色的,但是实际是红褐色的 含有亚铁离子的溶液都是浅绿色的,但是实际是白色的
这两句话对吗?,我是初中生!
如果不对,请告诉我含有三价铁离子或亚铁离子的溶液是什么颜色的? goat_yang1年前4
goat_yang1年前4 -
 闭着嘴刷牙 共回答了22个问题
闭着嘴刷牙 共回答了22个问题 |采纳率86.4%不对.三氯化铁的溶液是黄色的,而氢氧化铁是红褐色的.含有氯化亚铁的溶液是浅绿色的,但氢氧化亚铁是白色的.
事实上,你看到的颜色是络合离子的颜色,比如氯化铁的颜色就是铁和氯离子结合的颜色,这个可能比较深.普遍地说,三价铁离子是浅紫色的,二价铁离子是浅绿色的.上面说了,氯化铁的颜色是那样的.
但愿对你有所帮助1年前查看全部
- 检验亚铁离子时直接加入氯水不就行了吗?为什么要先加kscn呢?
 kktelcom1年前1
kktelcom1年前1 -
 双子亭 共回答了25个问题
双子亭 共回答了25个问题 |采纳率96%氯水有强氧化性,会把亚铁直接氧化成三价铁,这样就检验不出亚铁了1年前查看全部
- 除去亚铁离子中混有的铁离子用什么试剂 离子方程式是什么?
 一铲三1年前2
一铲三1年前2 -
 smilenancy 共回答了15个问题
smilenancy 共回答了15个问题 |采纳率66.7%加入过量的铁粉后过滤.
2Fe3+ +Fe=3Fe2+1年前查看全部
- 亚铁离子和硫离子反应的化学方程式怎么写?
 宝贝不说话1年前4
宝贝不说话1年前4 -
 l95447 共回答了24个问题
l95447 共回答了24个问题 |采纳率91.7%Fe2+ + S2-=========FeS(沉淀)
硫化亚铁沉淀可溶于强酸1年前查看全部
- 亚硫酸根、亚铁离子、溴离子、碘离子的还原性强弱排列
 rdx_7810161年前2
rdx_7810161年前2 -
 e124238142 共回答了22个问题
e124238142 共回答了22个问题 |采纳率77.3%还原性:SO32->I->Fe2+>Br-1年前查看全部
- 通常情况下既有氧化性,又有还原性的例子是 A铁 B亚铁离子 C碘离子 D铜离子
通常情况下既有氧化性,又有还原性的例子是 A铁 B亚铁离子 C碘离子 D铜离子
打错了C是铁离子 kuxx1年前3
kuxx1年前3 -
 唐伯虎點蚊香_ll 共回答了17个问题
唐伯虎點蚊香_ll 共回答了17个问题 |采纳率100%化合价高的只有氧化性,没有还原性;化合价低的没有氧化性,只有还原性;中间化合价的既有氧化性,又有还原性
所以选B亚铁离子1年前查看全部
- 回收纯银,废液里含有Ag离子,锌离子,亚铁离子
回收纯银,废液里含有Ag离子,锌离子,亚铁离子
费液(加过量X;操作I)得溶液C和固体A 然后固体A(加过量Y;操作II)得固体B和溶液D 然后溶液D(蒸发结晶)得固体E
回收的纯银存在于字母:中 X和Y的化学式是什么 gybfbb6go7cb81年前1
gybfbb6go7cb81年前1 -
 zwn126 共回答了17个问题
zwn126 共回答了17个问题 |采纳率100%X Fe
Y HCl1年前查看全部
- 氢离子、亚铁离子、氯离子、硝酸根离子为什么不能在同一溶液中共存
 azdxr4281年前2
azdxr4281年前2 -
 夜月悄悄 共回答了18个问题
夜月悄悄 共回答了18个问题 |采纳率100%氢离子 硝酸根=硝酸.硝酸有强氧化性,亚铁离子有还原性,二者发生氧化还原反应,不能共存1年前查看全部
- 检验盐铁离子和铁离子1.如何检验?用什么试剂?2. 检验亚铁离子时,为什么要先加入KSCN再加入氯水?谢谢
 宏立1231年前1
宏立1231年前1 -
 口丁牙牙 共回答了12个问题
口丁牙牙 共回答了12个问题 |采纳率83.3%检验亚铁离子:
方法一:待测液中先加入KSCN,没有明显现象(证明待测液中无三价铁离子),然后滴加氯水或者硝酸或者双氧水,溶液变血红色,说明加入氧化剂之后有三价铁离子,也就说明最初有亚铁离子.
方法二:待测液中加入氢氧化钠溶液,立刻生成白色沉淀,该白色沉淀迅速变为灰绿色,最后变为红褐色,证明待测液中含有亚铁离子.
检验三价铁离子
方法一:待测液中加入硫氰化钾,溶液变为血红色,证明待测液中有三价铁离子.
方法二:待测液中加入氢氧化钠溶液,生成红褐色沉淀.证明待测液中有三价铁离子.
方法三:待测液中滴加苯酚溶液,液体变紫色,证明待测液中含有三价铁离子.1年前查看全部
- 镁离子 钡离子 铁离子 亚铁离子 铝离子
镁离子 钡离子 铁离子 亚铁离子 铝离子
加氢氧化钠溶液无沉淀的是?
加过量氢氧化钠溶液仍有白色沉淀的是?
的溶液不宜长期保存. bobovii0021年前2
bobovii0021年前2 -
 521恋上下宇天 共回答了17个问题
521恋上下宇天 共回答了17个问题 |采纳率94.1%钡离子无沉淀,因为钡离子和氢氧根离子可以稳定共存.
产生白色沉淀且稳定存在的是镁离子;铁离子应该是红色沉淀.
由于亚铁离子不宜稳定存在,所以其沉淀会迅速转化为红色.
加入过量氢氧化钠使铝离子变成NaAlO3,是一种可溶性物质1年前查看全部
- 高一化学铁部分内容(两个填空)为除去废水中的亚铁离子,常先将废水中的( ),再调节溶液的铁离子转化为( )析出
 desheng161年前1
desheng161年前1 -
 90_09_99 共回答了16个问题
90_09_99 共回答了16个问题 |采纳率81.3%亚铁离子转换为铁离子、FE(OH)31年前查看全部
- 一道高中化学必修一的题已知ABCD均为可溶于水的固体,组成它们的离子如下阳离子:钠离子 亚铁离子 3价铁离子 铝离子阴离
一道高中化学必修一的题
已知ABCD均为可溶于水的固体,组成它们的离子如下
阳离子:钠离子 亚铁离子 3价铁离子 铝离子
阴离子:氢氧根离子 氯离子 硝酸根离子 硫酸根离子
1.B溶液与适量的Ba(OH)2溶液反应生成白色沉淀,加入过量的Ba(OH)2溶液,沉淀量减少,但不消失.
2.在呈黄色的A溶液中滴加硝酸银溶液,无明显现象.
3.向C溶液中滴加KSCN溶液,溶液不显红色,再滴加氯水,溶液呈红色.
所以,ABCD的化学式分别是?
能不能附上解析
谢谢了.... linuo开心果1年前6
linuo开心果1年前6 -
 亮亮爱的两只青蛙 共回答了16个问题
亮亮爱的两只青蛙 共回答了16个问题 |采纳率87.5%阳离子:Na+ 、Fe2+ 、Fe3+、Al3+
阴离子:OH-、Cl-、NO3-、SO4 2-
1.B与Ba(OH)2反应,先沉淀,后部分溶解,溶解说明有Al3+,部分溶解说明有两种沉淀,一种是AL(OH)3 ,另一种可能是氢氧化亚铁和硫酸钡,但下面出现二价Fe、所以没有二价铁.
则,B为Al2(SO4)3
2.黄色说明有Fe3+,加AgNO3无现象,说明无Cl-、无OH-.那么阴离子只能是NO3-.
则,A为Fe(NO3)3
3.加KSCN不红,再加氯水红,Fe2+的典型反应,此时阴离子还剩下OH-、Cl-,但Fe2+和OH-不共存,所以阴离子只能是Cl-
则,C为FeCl2
最后,根据1.2.3.得D为NaOH
所以、A为Fe(NO3)3,
B为Al2(SO4)3
C为FeCl2
D为NaOH1年前查看全部
- 如何确认溶液中同时含有亚铁离子和三价铁离子
如何确认溶液中同时含有亚铁离子和三价铁离子
偶然看到了一道题目,如题.屡想屡碰壁,往大虾们出手相助!
无其他条件,就是确认他俩同时存在
同时鄙视刷分用户
Fe(SCN)3溶液,不是沉淀。
貌似亚铁离子能使KMnO4褪色,但是三价铁离子不行,是不
RE 529699897:怎么除?用铜粉还原?这样又会生成亚铁离子,干扰。 lncserchen1年前4
lncserchen1年前4 -
 yijia1314 共回答了25个问题
yijia1314 共回答了25个问题 |采纳率88%楼主说话真是言简意赅啊~
三价铁都知道是用啥,我就不说了,问题是怎么检验二价铁
那么,可以从还原性角度入手,因此,滴入高锰酸钾溶液,褪色了,就含有二价铁
当两个特征反应同时发生,则同时含有1年前查看全部
- 什么情况下亚铁离子被氧化为铁离子
什么情况下亚铁离子被氧化为铁离子
说明加上实例,最好再说明一下,除了给氢氧化铁里加氧气和水变为氢氧化铁外还有什么方法? liuyuliang681年前1
liuyuliang681年前1 -
 意郿 共回答了21个问题
意郿 共回答了21个问题 |采纳率95.2%其实只要是比Fe3+强的氧化剂都可以把Fe2+氧化成Fe3+:
你说的:4Fe(OH)2+O2+2H2O=4 Fe(OH)3 氧气氧化了亚铁离子
还有:2Fe2+ + Cl2 = 2Fe3+ + 2Cl- 氯气氧化了亚铁离子
MnO4 - + 5Fe 2+ + 8H + = Mn 2+ + 5Fe 3+ + 4H2O 酸性高锰酸钾氧化了亚铁离子
3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO + 4H2O 硝酸氧化了亚铁离子
H2O2 + 2Fe2+ +2H+ = 2Fe3+ +2H2O 双氧水也行(这个不引入新的杂质)1年前查看全部
- 碘离子可以还原亚铁离子,碘单质可以氧化铁离子
碘离子可以还原亚铁离子,碘单质可以氧化铁离子
那么该两个反应互为可逆反应吗? jiaqing111年前4
jiaqing111年前4 -
 zzc6688 共回答了14个问题
zzc6688 共回答了14个问题 |采纳率92.9%哇噻……老大……是碘离子(I-)还原铁离子(Fe3+)吧,但是碘单质(I2)是氧化不了亚铁离子(Fe2+)的.这应该是个不可逆反应……1年前查看全部
- 亚铁离子和次氯酸根离子和水反应的离子方程式配平(生成物是氢氧化铁 铁离子 氯离子)
亚铁离子和次氯酸根离子和水反应的离子方程式配平(生成物是氢氧化铁 铁离子 氯离子)
FE2+ + CLO- + H2O === FE(OH)3 + FE3+ + CL- 蚊子09171年前2
蚊子09171年前2 -
 luojunty 共回答了17个问题
luojunty 共回答了17个问题 |采纳率82.4%6Fe2+ + 3ClO- + 3H2O === 2Fe(OH)3↓ + 4Fe3+ + 3Cl-1年前查看全部
- 亚铁离子,硝酸根离子,铵根离子能否共存?
 krico971年前1
krico971年前1 -
 liuxw051129 共回答了14个问题
liuxw051129 共回答了14个问题 |采纳率100%少量可以
大量不行1年前查看全部
- 在用k3[fe(cn)]检验亚铁离子时为什么要滴加氯化氢溶液
 lyh5301年前1
lyh5301年前1 -
 梦幻靓哥 共回答了17个问题
梦幻靓哥 共回答了17个问题 |采纳率100%亚铁离子本身水解能力很强,为了避免测试结果不准,加如氯化氢抑制亚铁离子的水解,提高(如果真存在的话)亚铁离子的浓度,使检验容易.1年前查看全部
- 已知氯离子、亚铁离子、H2O2、碘离子、SO2 均具有还原性,且在酸性溶液中还原性依次增强,则下列反应不能
已知氯离子、亚铁离子、H2O2、碘离子、SO2 均具有还原性,且在酸性溶液中还原性依次增强,则下列反应不能
发生的是( ) A.2Fe3+ +SO2 +2H2O ==2Fe2+ +SO4 2- +4H+ B.2Fe2+ +CI2 ==2Fe3+ +2CI- C.H2O2 +H2SO4==SO2 +O2 +2H2O D.I2(碘气)+SO2 +2H2O ==2HI +H2SO4 月影飘临1年前4
月影飘临1年前4 -
 dyjj1314 共回答了12个问题
dyjj1314 共回答了12个问题 |采纳率91.7%选 C.
如果 C能发生,则 H2SO4是氧化剂,H2O2是还原剂,SO2 是还原产物,O2 是氧化产物.
根据还原性:还原剂>还原产物,则 还原性:H2O2>SO2.
但根据题意,还原性 H2O2<SO2.与此矛盾.
所以 C 不合题意.
ABD都可以.
A说明还原性 SO2>Fe2+
B说明还原性Fe2+>Cl-
D说明还原性SO2> I-
与题设都不矛盾.1年前查看全部
- 关于氧化性还原性的问题我想知道铁离子和卤素单质的氧化性比较还有亚铁离子和卤素离子的还原性比较能扩充是最好的我看了很多答案
关于氧化性还原性的问题
我想知道铁离子和卤素单质的氧化性比较
还有亚铁离子和卤素离子的还原性比较
能扩充是最好的
我看了很多答案都参差不齐的, lb2ucat1年前3
lb2ucat1年前3 -
 75757095 共回答了22个问题
75757095 共回答了22个问题 |采纳率95.5%因为溴单质可以将铁氧化成溴化铁,所以溴单质的氧化性强于铁离子.因为铁离子可氧化碘单质生成碘化亚铁,所以铁离子氧化性强于碘单质,据此又可推知亚铁离子的还原性强于碘离子.综合起来有——氧化性:氟>氯>溴>铁离子>碘 还原性:亚铁离子>碘离子>溴离子1年前查看全部
- 铁遇到什么物质可以直接变成三价铁离子?遇到什么物质可以变成二价亚铁离子
铁遇到什么物质可以直接变成三价铁离子?遇到什么物质可以变成二价亚铁离子
如题 涉外客栈1年前1
涉外客栈1年前1 -
 sheilawx 共回答了15个问题
sheilawx 共回答了15个问题 |采纳率80%在空气中生锈,置换硫酸、盐酸等1年前查看全部
- 离子价电子排布记得在网上查时,有说亚铁离子是从最外层开始失电子,那其他过渡金属是不是都是这样?为什么?不是最外层能量不是
离子价电子排布
记得在网上查时,有说亚铁离子是从最外层开始失电子,那其他过渡金属是不是都是这样?为什么?不是最外层能量不是最少的啊. jian606_11171年前1
jian606_11171年前1 -
 oumeng215 共回答了14个问题
oumeng215 共回答了14个问题 |采纳率92.9%不太好讲,要看该能级的电离能,个人见解;亚铁离子从稳定性而言我觉得先失去最外层似乎不是稳定的,但是可这样认为,这样的失去电子可能是因为在溶液中水合导致.若先失去外层电子,水合后的亚铁离子应该能量比水加上亚铁离子低很多.其他的也是类似分析.对于金属离子得失电子我尚未见到什么很有力的证据能说明一定是如何进行的,只能猜测其可能的.最外层的能量不能说“少”只能说是绝对值较小,正常情况下能级是和负的电子所在层的平方呈反比(这只是浅显的说),这对应的能量事实上就是电离能,详细写说明的话就是当电子能量大于这个电离能的情况,电子的能谱变成连续的,将不受到原子核库仑力的束缚.一般来说就是上述规律,但是伴随着电子的屏蔽、钻穿、能级交错,以及相对论效应,上述命题就不是完全正确的了.1年前查看全部
- 在化学式中铁离子 铁原子 亚铁离子怎样区分
 FancyOne1年前1
FancyOne1年前1 -
 jingzhouxue 共回答了20个问题
jingzhouxue 共回答了20个问题 |采纳率80%铁离子 铁原子 亚铁离子的区别:主要是化合价不一样
1、铁离子,Fe3+,是三价的,就是说外层电子缺了三个
2、铁原子,Fe,是0价的,单质铁中含有的都是铁原子
3、亚铁离子,Fe2+,是二价的
不知你问的是不是这个意思?!1年前查看全部
- 铁离子具有什么性 亚铁离子具有什么性
 cpc194621年前1
cpc194621年前1 -
 狗狗克里夫 共回答了21个问题
狗狗克里夫 共回答了21个问题 |采纳率95.2%铁离子具有(氧化)性.亚铁离子具有(氧化性和还原)性 ,但以还原性为主.
解析:铁离子中铁的化合价是+3价,处于最高价,只有还原性.亚铁离子中的铁是+2价,介于0价和+3价之间,所以具有氧化性和还原性1年前查看全部
- 写出2个亚铁离子的符号,
 xjhrh1年前2
xjhrh1年前2 -
 晴天之前的雨 共回答了23个问题
晴天之前的雨 共回答了23个问题 |采纳率73.9%2Fe2+;
2+在Fe的右上角;
亚铁离子是+2价的Fe离子;
2个是写在前面的;
有问题请追问~~1年前查看全部
- 用化学符号表示硫离子S2-S2-2个氮分子2N22N2+2价的锌元素+2Zn+2Zn4个亚铁离子4Fe2+4Fe2+2个
用化学符号表示
硫离子S2-S2-2个氮分子2N22N2+2价的锌元素+2 Zn
4个亚铁离子4Fe2+4Fe2++2 Zn
2个磷酸根离子2PO43-2PO43-氧化铁中铁元素的化合价为+3价
2O3+3 Fe
2O3+3 Fe
 NeNe氯离子的结构示意图
NeNe氯离子的结构示意图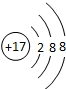
 .
.  最小的善1年前1
最小的善1年前1 -
 fgs_sc 共回答了18个问题
fgs_sc 共回答了18个问题 |采纳率72.2%①离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后:故硫离子S2-
②分子的表示方法:正确书写物质的化学式,故2个氮分子2N2
③元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后;+2价的锌元素
+2
Zn
④离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后:4个亚铁离子表示为4Fe2+;2个磷酸根离子表示为2PO43-
⑤元素化合价的表示方法:氧化铁中铁元素的化合价为+3价表示为
+3
Fe2O3
⑥ Ne;氯离子的结构示意图
Ne;氯离子的结构示意图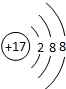
故答为:S2-; 2N2;
+2
Zn; 4Fe2+; 2PO43-;
+3
Fe2O3; Ne 1年前查看全部
1年前查看全部
- 为什么测量亚铁离子浓度用高锰酸钾滴定亚铁离子更合适 而不是亚铁离子滴定高锰酸钾
 rr阿蒙1年前1
rr阿蒙1年前1 -
 markey 共回答了25个问题
markey 共回答了25个问题 |采纳率100%用高锰酸钾滴定亚铁离子终点是无色变红色,容易观察.
亚铁离子滴定高锰酸钾终点是红色变无色,不容易观察.1年前查看全部
- 2个氢原子 五氧化二磷 3个亚铁离子 硝酸钾中氮元素的化合价
 ㄥ七七ㄟ1年前2
ㄥ七七ㄟ1年前2 -
 greatleadery 共回答了14个问题
greatleadery 共回答了14个问题 |采纳率85.7%2H
P2O5
3Fe^2+
KNO3 +51年前查看全部
- 硝酸亚铁和水反应么亚铁离子有强还原性,硝酸有强氧化性,和水能生成氢氧化铁,铁离子和no么?如果不能的话请说明下原因,那k
硝酸亚铁和水反应么
亚铁离子有强还原性,硝酸有强氧化性,和水能生成氢氧化铁,铁离子和no么?如果不能的话请说明下原因,
那kmno4为什么没有氢离子也有强还原性 66chen661年前1
66chen661年前1 -
 qq1115201111 共回答了18个问题
qq1115201111 共回答了18个问题 |采纳率88.9%不反应.
这里不是HNO3,只是NO3-.NO3-要有大量H+的条件下才具有强氧化性.
高锰酸钾是高锰酸钾,NO3-是NO3-.拿2种不同的物质来比较,没意思.1年前查看全部
- 化学除去亚铁离子一定要转变为氢氧化铁吗?氢氧化亚铁不行吗?
 fristsl1年前5
fristsl1年前5 -
 mingmichael 共回答了21个问题
mingmichael 共回答了21个问题 |采纳率95.2%因为Fe(OH)2是絮状沉淀,不容易除去,
一般除去Fe2+都要氧化为Fe3+
溶液中有Cu2+存在的时候更要这样.因为如果有Cu2+,Fe2+开始沉淀的时候Cu2+也已经沉淀.
但Fe3+沉淀完全时,Cu2+并不会沉淀1年前查看全部
- 大学化学问题,关于莫尔盐为什么莫尔盐的氧化还原稳定性比一般的亚铁盐高?(常作为亚铁离子的标准试剂使用)
 旭日一派1年前1
旭日一派1年前1 -
 晨mu 共回答了23个问题
晨mu 共回答了23个问题 |采纳率95.7%大概是因为铵离子在水溶液中能创造出酸性环境,在酸性条件下,亚铁离子的还原能力比在碱性环境下差很多.由此可以推断出,没有明显氧化能力的弱碱阳离子的硫酸盐(只要不与亚铁离子反应的阴离子盐皆可,例如高氯酸盐)与硫酸亚铁混合,都将稳定二价铁离子.1年前查看全部
- 亚铁离子与碘离子反应离子方程式
 林觉1年前4
林觉1年前4 -
 qjmm88 共回答了19个问题
qjmm88 共回答了19个问题 |采纳率84.2%还原性强弱:I->Fe2+>Br->Cl-
首先我们知道存在这个反应:2Fe3+ + 2I- = 2Fe2+ + I2,所以亚铁离子和碘离子是不反应的.1年前查看全部
- 2个亚铁离子 用符号怎么表示?
 lacina2061年前3
lacina2061年前3 -
 aijia1314 共回答了19个问题
aijia1314 共回答了19个问题 |采纳率84.2%2Fe2+.1年前查看全部
- 碘离子为什么不和亚铁离子反应?铁离子和碘离子反应生成物为什么是亚铁离子而不是铁,碘离子的还原性那么强?(这个才是重点)
 四楼米粉1年前5
四楼米粉1年前5 -
 扬谷的天空 共回答了16个问题
扬谷的天空 共回答了16个问题 |采纳率87.5%先假设碘离子和三价铁能生成铁单质和碘单质,肯定那么根据还原剂的还原性大于还原产物的还原性就有还原性碘离子大于铁单质,可事实是金属的还原性肯定大于碘离子,所以假设不成立,产物只能是二价的铁,这就符合还原性的顺序碘离子大于二价铁大于溴离子大于氯离子大于氢氧根,如果是高一和高二学生这是最好的解释1年前查看全部
- 某无色的溶液中可能含有大量的碘离子,亚硫酸根离子,铵根离子,铜离子,亚铁离子,向该溶液中加入少量的溴水
某无色的溶液中可能含有大量的碘离子,亚硫酸根离子,铵根离子,铜离子,亚铁离子,向该溶液中加入少量的溴水
0 - 离问题结束还有 0 小时
,溶液呈无色,则下列关于溶液的组成判断正确的是( )
1.肯定不含碘离子2.肯定不含铜离子、亚铁离子3.肯定含有亚硫酸根离子4.可能含有碘离子5铵根离子可能存在
A 1235 B135 C 2345 D 34 jihaichao1年前1
jihaichao1年前1 -
 jessica--- 共回答了16个问题
jessica--- 共回答了16个问题 |采纳率81.3%肯定不含碘离子
对,如果有I-,有单质碘生成,溶液有颜色.
2.肯定不含铜离子、亚铁离子
对,如果有铜离子、亚铁离子,溶液有颜色.
3.肯定含有亚硫酸根离子
对,只有两种阴离子,没有I-,肯定有SO32-.
4.可能含有碘离子
错,不可能有
5铵根离子可能存在
对,有NH4+
选A1年前查看全部
- 如何证明铁离子溶液中含有亚铁离子?
 kkkkbing1年前1
kkkkbing1年前1 -
 coohacker 共回答了19个问题
coohacker 共回答了19个问题 |采纳率89.5%滴加少量的KMnO4溶液,若褪色,证明有亚铁离子1年前查看全部
- [高中化学]过量亚铁离子与稀硝酸反应的化学方程式
 丁子张1年前3
丁子张1年前3 -
 eoo9 共回答了22个问题
eoo9 共回答了22个问题 |采纳率81.8%3Fe2+ + 4H+ + NO3- == 3Fe3+ + NO↑ + 2H2O1年前查看全部
- 用化学用语填空:(1)空气中含量最多的气体______;(2)2个亚铁离子______(3)氧化铁中铁元素的化合价+3F
用化学用语填空:
(1)空气中含量最多的气体______;
(2)2个亚铁离子______
(3)氧化铁中铁元素的化合价
2O3+3 Fe .
2O3+3 Fe
(4)写出符号“4NO2”中数字表示的含义:
①“4”表示______;
②“2”表示______. XMX77585211年前1
XMX77585211年前1 -
 ww专用ee沙发 共回答了23个问题
ww专用ee沙发 共回答了23个问题 |采纳率95.7%解题思路:(1)空气中含量最多的气体是氮气.
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字.
(3)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
(4)①标在分子符号前面的数字表示分子的个数.
②标在化学式中元素右下角的数字表示一个分子中所含原子的数目.(1)空气中含量最多的气体是氮气,氮气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:N2.
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个亚铁离子可表示为:2Fe2+.
(3)氧化铁中氧元素显-2价,铁元素显+3价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化铁中铁元素的化合价为+3价可表示为:
+3
Fe2O3.
(4)①标在分子符号前面的数字表示分子的个数,“4NO2”中“4”表示二氧化氮分子的个数为4.
②标在化学式中元素右下角的数字表示一个分子中所含原子的数目,4NO2中的“2”表示1个二氧化氮分子中含有2个氧原子.
故答案为:(1)N2;(2)2Fe2+;(3)
+3
Fe2O3;(4)①二氧化氮分子的个数为4;②1个二氧化氮分子中含有2个氧原子.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(分子符号、化学式、化合价、离子符号等)的书写和理解能力.1年前查看全部
- →用化学符号和数字表示:三个水分子,两个硫原子,两个铜离子,三个硫酸根离子,四个亚铁离子,四个铁原子,铁元素的化合价为+
→用化学符号和数字表示:三个水分子,两个硫原子,两个铜离子,三个硫酸根离子,四个亚铁离子,四个铁原子,铁元素的化合价为+3,3个二氧化硫分子,钙离子,+5价的磷元素.
 西门停电1年前1
西门停电1年前1 -
 sqli1506 共回答了16个问题
sqli1506 共回答了16个问题 |采纳率87.5%3H2O;2S;2Cu2+;3SO4(右上角标2-);4Fe2+;4Fe;Fe(正上方标+3);3SO2;Ca2+;P((正上方标+5)1年前查看全部
- 硫酸亚铁溶液加铁钉防止溶液里的亚铁离子被氧化
硫酸亚铁溶液加铁钉防止溶液里的亚铁离子被氧化
通常用氯化铁溶液腐蚀铜箔制造印刷线路板,在硫酸亚铁溶液里加铁定或铁粉来防止溶液离得亚铁离子被氧化,说出其中的道理,分析发生的化学反应. rt19821年前2
rt19821年前2 -
 可怜水 共回答了24个问题
可怜水 共回答了24个问题 |采纳率95.8%因为如果亚铁离子被氧化会生产铁离子,铁和铁离子反应生产亚铁离子.方程式:Fe+2Fe3+ = 3Fe2+1年前查看全部
- 溶液中既有亚铁离子,又有铁离子的验证实验方法是什么啊?
 avazouli1年前1
avazouli1年前1 -
 memorable417 共回答了11个问题
memorable417 共回答了11个问题 |采纳率63.6%取两份溶液.一份加KSCN有血红色,表示有三价铁
另一份加铁氰化钾K3[Fe(CN)6]生成蓝色沉淀,表示有二价铁.1年前查看全部
- 推断题哈,我推断出溶液有亚铁离子和铁离子,哪种试剂可以验证溶液里有亚铁离子.
推断题哈,我推断出溶液有亚铁离子和铁离子,哪种试剂可以验证溶液里有亚铁离子.
A稀硫酸.B铁 c硫氰化钾 d酸性高锰酸钾.
请说清楚每个选项的原因, 晴天绿雪1年前4
晴天绿雪1年前4 -
 5237355yj 共回答了19个问题
5237355yj 共回答了19个问题 |采纳率94.7%亚铁离子具有还原性,高锰酸钾有氧化性,所以亚铁离子与高锰酸钾混合后,高锰酸钾溶液会褪色,所以可以用来检验亚铁离子.选D
硫氰化钾是专门用来检验铁离子的,它俩混合后溶液会变成血红色(生成硫氰化铁络合物),这是很重要的一个知识点,一定要记住.
稀硫酸与两个都不反应.铁与亚铁离子也不反应,所以都观察不到明显现象.1年前查看全部
- 请问酸化的高锰酸钾与亚铁离子反应褪色原理是什么
请问酸化的高锰酸钾与亚铁离子反应褪色原理是什么
考试时遇到题目 酸化的高锰酸钾溶液能否鉴别亚铁离子和铁离子
我是这么想的 类比H+、NO3-、Fe3+两两共存但不能三者同时共存 MnO4-强氧化性 所以酸化之后引入H+ 氧化性更强足以氧化Fe2+ 使之变为Fe3+ 类比铜和硝酸反应生成氮氧化物 我认为与Fe2+反应的现象是产生黑色沉淀二氧化锰 而与Fe3+不会反应 所以可以鉴别
回家之后查了一下,答案确实是可以鉴别,结果是高锰酸钾溶液褪色,
我想知道这个褪色的现象之下是怎样的反应原理?
老师提到过稀硫酸与铜不反应 但加入硝酸盐即引入NO3-后就可以反应 生成氮氧化物 铜既有还原性也有氧化性两个性质都不是特别强 H+加上NO3-具有强氧化性
亚铁离子也既有氧化性也有还原性两个性质都不是特别突出 H+加上MnO4-也具有强氧化性 是不是酸化的高锰酸钾溶液与亚铁离子反应会生成锰的氧化物?那明显的现象不应该是褪色而应该是黑色沉淀啊?
如果是我所想的那样的话 请问褪色的反应方程式是什么?
如果我想的不对的话 可以告诉我哪里不对以及褪色的反应原理吗?
定量的东西说多了可能不明白 请尽量用定性的方式解释 未雨时1年前1
未雨时1年前1 -
 骷髅舞曲骷髅舞曲 共回答了23个问题
骷髅舞曲骷髅舞曲 共回答了23个问题 |采纳率95.7%高锰酸钾在酸性、中性、碱性条件下都有氧化性,但依次减弱,其还原产物分别为2价锰离子、二氧化锰、锰酸根.
根据电子得失守恒配平,所以 2KMnO4+8H2SO4+10FeSO4=5Fe2(SO4)3+K2SO4+2MnSO4+8H2O
因此褪色.1年前查看全部
- 含硝酸跟离子的溶液中,有氨根离子、钡离子、亚铁离子、溴离子.在这溶液中,为什么能大量共存?亚铁不是会水解吗?
 谷熙1年前2
谷熙1年前2 -
 clematis 共回答了18个问题
clematis 共回答了18个问题 |采纳率88.9%NH4+ + H2O ==可逆== NH3 H2O + H+
Fe2+ + 2H2O ==可逆== Fe(OH)2 + 2H+
NH4+ 和 Fe2+ 在溶液中都会发生小程度的水解,它们产生的H+会互相抑制对方的水解,减弱水解的程度,此时可以认为NH4+和Fe2+可以大量共存
若是将其中一种离子换成弱酸银离子如HCO3-
HCO3- + H2O ==可逆== H2CO3 + OH-
这个时候产生的OH-会和阳离子水解产生的H+反应,使得阴阳离子双方的水解程度增大,此时不能共存1年前查看全部
- 用化学语填空 3 个亚铁离子……
用化学语填空 3 个亚铁离子……
用化学语填空 3 个亚铁离子……
地壳中含量最高的元素是…… 心香-yy1年前1
心香-yy1年前1 -
 aliao166 共回答了25个问题
aliao166 共回答了25个问题 |采纳率96%3Fe2+ O1年前查看全部
- 用化学符号怎么表示下列内容?钾离子 钠离子 银离子 钙离子 镁离子 钡离子 锌离子 铝离子 铜离子 亚铁离子 铁离子 氢
用化学符号怎么表示下列内容?
钾离子 钠离子 银离子 钙离子 镁离子 钡离子 锌离子 铝离子 铜离子 亚铁离子 铁离子 氢离子 硫离子 氯离子 氧离子 氟离子
铵根离子 氢氧根离子 硫酸根离子 氯酸根离子 碳酸根离子
硫酸根离子
盐酸 硫酸 硝酸 碳酸 氯酸
氢氧化钠 氢氧化钾 氢氧化钙 氢氧化镁 氢氧化钡 氢氧化锌
氢氧化铝 氢氧化铜 氢氧化铁 氢氧化亚铁
氯化钠 氯化镁 氯化铝 氯化铜 氯化钡 氯化钙 氯化亚铁
氯化铁 氯化锌 氯化银
硫酸铜 硫酸钠 硫酸钾 硫酸铝 硫酸钡 硫酸钙 硫酸亚铁
碳酸钠 碳酸钙 碳酸铵 碳酸钡 碳酸铝
硝酸根 硝酸铵 硝酸钠 硝酸镁 硝酸铝
拜托拉…………
帮帮忙!我才刚刚学呀~!…………
帮帮你们的学妹拉 张无忌俺小弟1年前1
张无忌俺小弟1年前1 -
 chenglu2007 共回答了19个问题
chenglu2007 共回答了19个问题 |采纳率94.7%钾离子K+ 钠离子Na+ 银离子Ag+ 钙离子Ca2+ 镁离子Mg2+ 钡离子Ba2+ 锌离子Zn2+ 铝离子Al3+ 铜离子Cn2+ 亚铁离子Fe2+ 铁离子Fe3+ 氢离子H+ 硫离子S2- 氯离子Cl- 氧离子O2- 氟离子F-
铵根离子NH4+ 氢氧根离子OH- 硫酸根离子SO4 2- 氯酸根离子ClO3- 碳酸根离子 CO3 2-
硫酸根离子 SO4 2-
盐酸HCl 硫酸H2SO4 硝酸HNO3 碳酸H2CO3 氯酸HClO3
氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙Ca(OH)2 氢氧化镁Mg(OH)2 氢氧化钡Ba(OH)2 氢氧化锌 Zn(OH)2
氢氧化铝Al(OH)3 氢氧化铜Cu(OH)2 氢氧化铁Fe(OH)3 氢氧化亚铁Fe(OH)2
氯化钠NaCl 氯化镁MgCl2 氯化铝AlCl3 氯化铜CuCl2 氯化钡BaCl2 氯化钙CaCl2 氯化亚铁FeCl2 氯化铁FeCl3 氯化锌ZnCl2 氯化银AgCl
硫酸铜CuSO4 硫酸钠Na2SO4 硫酸钾K2SO4 硫酸铝Al2(S04)3 硫酸钡BaSO4 硫酸钙CaSO4 硫酸亚铁 FeSO4
碳酸钠Na2CO3 碳酸钙CaCO3 碳酸铵(NH4)2CO3 碳酸钡BaCO3 碳酸铝Al2(CO3)3
硝酸根NO3- 硝酸铵NH4NO3 硝酸钠NaNO3 硝酸镁Mg(NO3)2 硝酸铝Al(NO3)31年前查看全部
- 若某溶液中有 亚铁离子 和 碘离子 共存,要氧化碘离子 而又不氧化 亚铁离子,可以加入的试剂是 1 氯气 2 高锰酸钾
若某溶液中有 亚铁离子 和 碘离子 共存,要氧化碘离子 而又不氧化 亚铁离子,可以加入的试剂是 1 氯气 2 高锰酸钾 3氯化铁 4氯化氢
选哪个?为什么? 锦色华年谁与共1年前2
锦色华年谁与共1年前2 -
 smartegg 共回答了20个问题
smartegg 共回答了20个问题 |采纳率100%选第3个氯化铁.
氯气和高锰酸钾同属于强氧化剂,能把碘和亚铁离子都氧化.
而FeCL3中的Fe3+能与I-发生反应:2Fe3++2I-=2Fe2+ + I2
使得碘离子被氧化,你看方程式,Fe3+自身被还原为Fe2+,那Fe3+肯定不能氧化亚铁离子了.
至于氯化氢,它没有氧化性,加进去没用,
还有什么不会的可以继续Hi我1年前查看全部
大家在问
- 12分之b,负4分之b的3次方,6分之b的5次方,负8分之b的7次方.第n个式子为(n为正整数)
- 2小明打篇论文,第一天打了全部的2/5,第二天打了剩下的5/7,第三天打了1200字,正好打完,求这篇论文字数
- 3为测定某纯碱样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5
- 4两架飞机从南极同时出发,分别沿东经40度和西经20度向北行进,会发生什么情况?
- 5解释multiple point of view
- 6读某地区聚落分布示意图,回答小题。
- 7我叔叔正在给我爸打电话的英文翻译句子
- 8如何上好小学阅读指导课
- 9这个周四下午一点上课可以吗英语怎么说
- 10小明周末去看奶奶,在超市他用74元钱买了苹果,梨,香蕉三种水果已知苹果每千克5元,梨每千克5.5元,香蕉每千克4元,三种
- 11流体力学发展到现在为什么还要进行风洞试验?风洞试验能解决哪些理论计算解决不了的问题?
- 12Hoping so bad that you'll let me in.这个句子属于同位语从句吗?
- 13英语单选题———Aren't you a student ------____.I study in a middle
- 14山地迎风坡的自然带是如何分布的
- 15(2012•滨州一模)蜜蜂的雄峰是由未受精的卵细胞发育来的,雄峰在产生精子时染色体数目不减半.蜂王和一雄峰杂交后,让F1
