碳元素性质活泼,可以跟多数元素形成共价键这句话错的吗?
 叫你xx唱xx2022-10-04 11:39:541条回答
叫你xx唱xx2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 风-781123 共回答了18个问题
风-781123 共回答了18个问题 |采纳率94.4%- 碳元素性质不活泼,它的单质如石墨、金刚石都很稳定.
- 1年前
相关推荐
- 如何证明石墨和木炭中均含有碳元素
 chalkz1年前1
chalkz1年前1 -
 疗喁觋路 共回答了24个问题
疗喁觋路 共回答了24个问题 |采纳率87.5%将石墨和木炭分别放在纯氧气中燃烧,生成产物只有二氧化碳(用澄清石灰水来检验它),则证明它们是碳元素组成的单质.1年前查看全部
- 甲烷和乙醇的燃烧产物都是二氧化碳和水,是否可以由此证明甲烷和乙醇是由碳元素和氢元素组成的碳氢化合物
甲烷和乙醇的燃烧产物都是二氧化碳和水,是否可以由此证明甲烷和乙醇是由碳元素和氢元素组成的碳氢化合物
不要证明氧气,只要证明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物.
就像我问的,该怎么写 ctj5211年前4
ctj5211年前4 -
 怡人晴天 共回答了24个问题
怡人晴天 共回答了24个问题 |采纳率100%可以由此证明
原理是:元素守恒1年前查看全部
- 甲烷和乙醇的燃烧产物都是二氧化碳和水,是否可以由此证明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物
 acuiweihua1年前4
acuiweihua1年前4 -
 别咬我疼 共回答了20个问题
别咬我疼 共回答了20个问题 |采纳率90%不行,肯定不行,燃烧时可能引入氧,不能排除是否有氧哈
hydrocarbon 烃,是仅由碳和氢两种元素组成的有机化合物称为碳氢化合物,又叫烃.1年前查看全部
- 碳元素和某非金属元素R可形成化合物CRx,已知CRx分子中各原子原子核外最外层电子数之和为16,核外电子总数为38,则R
碳元素和某非金属元素R可形成化合物CRx,已知CRx分子中各原子原子核外最外层电子数之和为16,核外电子总数为38,则R的元素符号为——,x值为——
 阿宏1年前1
阿宏1年前1 -
 看不穿酒悟 共回答了20个问题
看不穿酒悟 共回答了20个问题 |采纳率90%R的元素符号为—S—,x值为—2—1年前查看全部
- 请问怎样证明足球烯由碳元素组成
 wqcz78791年前1
wqcz78791年前1 -
 GUO88888888 共回答了10个问题
GUO88888888 共回答了10个问题 |采纳率90%燃烧它
把气体排进石灰水中
有沉淀1年前查看全部
- 组成细胞的重要化合物种都含有碳元素吗
组成细胞的重要化合物种都含有碳元素吗
应该是有机化合物里都有碳元素吧
请说明有机物还是有机化合物 小葱--1年前4
小葱--1年前4 -
 DoRe米 共回答了12个问题
DoRe米 共回答了12个问题 |采纳率100%有机物都是化合物,都有碳元素.1年前查看全部
- 关于碳元素的分子晶体和原子晶体有哪些?
 爱上纽ss1年前4
爱上纽ss1年前4 -
 两面的人生 共回答了16个问题
两面的人生 共回答了16个问题 |采纳率93.8%原子晶体有金刚石,石墨
分子晶体富勒烯(C60此类)
CO2是分子晶体.1年前查看全部
- 某CO和CO2的混合气体中,碳元素的质量分数为36%,取5g该气体混合物通过足量炽热的氧化铜,再将气体通入足
 大胆浆糊1年前1
大胆浆糊1年前1 -
 heran1038 共回答了25个问题
heran1038 共回答了25个问题 |采纳率84%5g该气体混合物,碳元素的质量分数为36%,C的质量=5*36%=1.8克,碳元素的物质的量=1.8/12=0.15mol.
设CO和CO2物质的量分别为X,Y:
28X+44Y=5
X+Y=0.15,X=0.1mol,Y=0.05mol
即含有CO=0.1*28=2.8克,CO2=0.05*44=2.2克.1年前查看全部
- 碳元素和氢元素的质量比都是12:1的三种烃A.B.C,
碳元素和氢元素的质量比都是12:1的三种烃A.B.C,
碳元素和氢元素的质量比都是12:1的三种烃A.B.C,A呈气态,B和C呈液态.A.B.C相对分子质量之比为1:3:4.A和C既能使溴的四氯化碳褪色,又能使高锰酸钾酸性溶液褪色;B既不能使溴的四氯化碳褪色,也不能使高锰酸钾酸性溶液褪色.A.C都能发生加聚反应,A的加聚物具有导电性,C的加聚物则是使用较为广泛的塑料.
1.写出A.B.C的分子式
2.写出A.C分别加聚所的产物的结果简式 小小大财迷1年前3
小小大财迷1年前3 -
 下雨天的松风声 共回答了19个问题
下雨天的松风声 共回答了19个问题 |采纳率100%碳元素和氢元素的质量比都是12:1,A、B、C通式为(CH)n.
A既能使溴的四氯化碳溶液褪色,又能使高锰酸钾酸性溶液褪色;A的加聚产物具有导电性.
故A应该为乙炔C2H2.乙炔的加聚产物中碳链上单键双键一个隔一个,这种结构可以导电.(知识点)
A、B、C相对分子质量之比为1:3:4.故B分子式为C6H6,C为C8H8.
B为液态,既不能使溴的四氯化碳溶液褪色,也不能使高锰酸钾酸性溶液褪色.故B有稳定结构,应该为苯.
C既能使溴的四氯化碳溶液褪色,又能使高锰酸钾酸性溶液褪色(有双键或三键);C的加聚产物是使用较为广泛的塑料.
故C应该为苯乙烯.(聚苯乙烯为常用塑料)1年前查看全部
- 碳元素以什么形式进入动物
 蒸米糕1年前4
蒸米糕1年前4 -
 布丁哆哆 共回答了15个问题
布丁哆哆 共回答了15个问题 |采纳率93.3%有机物1年前查看全部
- 某甲醛【HCHO]溶液中,氢元素的质量分数为10%,那么碳元素的质量分数是多少?
 x379911年前1
x379911年前1 -
 钟馗007 共回答了14个问题
钟馗007 共回答了14个问题 |采纳率71.4%601年前查看全部
- 某钢样品的含碳量为0.24%(其他杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和F
某钢样品的含碳量为0.24%(其他杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和FeC的质量分数范围是()
 经济发展1年前1
经济发展1年前1 -
 ricexu 共回答了26个问题
ricexu 共回答了26个问题 |采纳率84.6%设该钢样品中Fe2C和FeC的质量分数分别为X、Y
根据碳原子守恒和质量分数之比=质量之比得到如下关系式:
Fe2C~C
124 12
X 0.24%
124:12=X:0.24%
X=2.48%
Fe3C~C
180 12
Y 0.24%
Y=3.6%
答:该钢样品中Fe2C和FeC的质量分数范围为2.48%~3.6%
希望我的回答能对你的学习有帮助!1年前查看全部
- 求氮元素和碳元素分别的最高价含氧酸分子式
 天下第七唐唐1年前2
天下第七唐唐1年前2 -
 事后一支烟 共回答了13个问题
事后一支烟 共回答了13个问题 |采纳率100%氮元素高价含氧酸分子式:HNO3
碳元素高价含氧酸分子式:H2CO31年前查看全部
- 甲苯和甘油组成的混合物中,若碳元素的质量分数为60%,则氢元素的质量分数为____
 真水无香MM1年前1
真水无香MM1年前1 -
 liudaxianr 共回答了28个问题
liudaxianr 共回答了28个问题 |采纳率100%甲苯化学式为C7H8 甘油为C3H8O3
两者的摩尔质量都是92 H在其中都是8
所以两者中H的质量分数都是8/92=8.69%
所以不论他们以什么比例混合 H元素的质量分数都是8/92=8.69%
这题的条件 碳元素的质量分数为60% 是多余的……
不过根据这个条件 用十字交叉法可以算出本题中甲苯:甘油=2:31年前查看全部
- 氮元素和碳元素都能在生物群落与无机环境之间不断循环,为什么还要在农田中不断施加氮肥呢?
氮元素和碳元素都能在生物群落与无机环境之间不断循环,为什么还要在农田中不断施加氮肥呢?
谢谢了
 三教九家多学派1年前1
三教九家多学派1年前1 -
 cylfly15 共回答了15个问题
cylfly15 共回答了15个问题 |采纳率100%氮元素在自然界中的稳定存在状态是硝酸盐,而植物需要的是氨基酸必需的铵态氮,所以需要补充铵态氮肥.1年前查看全部
- 30克醋酸含有几克碳元素
 Sid_Hell1年前2
Sid_Hell1年前2 -
 亲娘咧真费解啊 共回答了18个问题
亲娘咧真费解啊 共回答了18个问题 |采纳率83.3%醋酸:ch3c00h
故质量为30/60*24=12g1年前查看全部
- 下列实验结论正确的是 ①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成 ②既可说明二氧化碳的密度比空气大,又
下列实验结论正确的是
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成, 又可推导出水分子中氢原子和氧原子个数之比为2:1
④既可说明二氧化碳能溶于水,又说明了二氧化碳能与水反应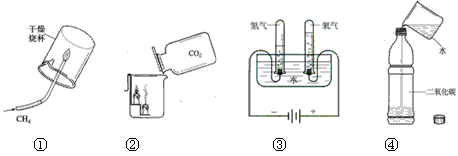 [ ]
[ ]A.①②③
B.②③
C.②③④
D.①②③④ putiansun1年前1
putiansun1年前1 -
 coffeea 共回答了16个问题
coffeea 共回答了16个问题 |采纳率93.8%B1年前查看全部
- 已知甲醛的水溶液中,碳元素的质量分数是10%,甲醛的质量分数为多少?
 edlf1年前1
edlf1年前1 -
 观摩演出 共回答了11个问题
观摩演出 共回答了11个问题 |采纳率90.9%甲醛HCHO中碳元素质量分数=12/30 = 40%
而甲醛的水溶液中,碳元素的质量分数是10%
所以甲醛质量分数 = 10%/40% = 25%1年前查看全部
- 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.
(1)很多天然矿石中含有碳元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是______.
(2)天然气的主要成分是甲烷,天然气燃烧的化学方程式:CH4+2O2
CO2+2H2O点燃 .CH4+2O2.
CO2+2H2O点燃 .
(3)木炭还原氧化铜的化学方程式:C+2CuO
2Cu+CO2↑高温 .C+2CuO.
2Cu+CO2↑高温 . qqzyt90991年前1
qqzyt90991年前1 -
 masor 共回答了22个问题
masor 共回答了22个问题 |采纳率90.9%解题思路:(1)根据在化合物中正负化合价代数和为零进行解答本题.
(2)熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则,就能写出正确的化学方程式.
(3)熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则,就能写出正确的化学方程式.(1)碳酸根显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)=0,则x=+2.故填:+2;(2)甲烷在空气中燃烧生成二氧化碳和水,故方程式为:CH4+2O2 点燃 . CO2+2H2...
点评:
本题考点: 有关元素化合价的计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力和书写化学方程式的能力.1年前查看全部
- 有氮气,一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%.使该混合气体通过足量的灼热氧化铁充分反应后,再
有氮气,一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%.使该混合气体通过足量的灼热氧化铁充分反应后,再将气体通入过量的石灰水中,能得到白色沉淀的质量为A.30g B.50g C.100g D.150g
 xuser8567781年前1
xuser8567781年前1 -
 zhangsunny 共回答了17个问题
zhangsunny 共回答了17个问题 |采纳率94.1%根据混合气体中碳元素的质量分数,计算出碳元素的质量,而这些质量的碳元素转化为二氧化碳后又与氢氧化钙反应转化为碳酸钙中的碳元素,所以依据质量守恒定律可知混合物中的碳元素质量与碳酸钙中碳元素的质量相等.
氮气、一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%,故碳元素的质量为40g×30%=12g,12g的碳元素转化为二氧化碳后又与氢氧化钙反应转化为碳酸钙中的碳元素,所以依据质量守恒定律可知混合物中的碳元素质量与碳酸钙中碳元素的质量相等.
设碳酸钙的质量是x
x×
12
100
=12g
x=100g
同学你好
有帮助请点采纳或者右上角好评~
祝你新的一年学习进步,马到成功!1年前查看全部
- 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
(1)C 60 分子能与F 2 发生加成反应,其加成产物为______,C 60 分子的晶体中,在晶胞的顶点和面心均含有一个C 60 分子,则一个C 60 晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp 3 杂化,石墨中碳原子的杂化类型为sp 2 杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm 3 ,Cu的相对原子质量为M,阿伏伽德罗常数N A ,则Cu的原子半径为______.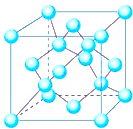
 吹海风的海1年前1
吹海风的海1年前1 -
 zhanshu1983 共回答了18个问题
zhanshu1983 共回答了18个问题 |采纳率94.4%(1)C 60 分子含有30个共价键,发生加成反应时一个C 60 分子中含有的碳碳双键个数和氟气分子个数相同,1molC 60 分子中30mol碳碳双键,所以需要30mol氟气,所以其加成产物的化学式为:C 60 F 60 ;C 60 晶体为面心立方排布,所以每个C 60 晶胞有4个C 60 分子 (面心3个,顶点1个),所以一个C 60 晶胞=
4×60
N A ×12 =
2880
N A g ,
故答案为:C 60 F 60 ;
2880
N A g ;
(2)a、水分子间存在氢键,且氢键有方向性,导致水分子形成冰时存在较大的空隙,密度比水小,干冰分子之间只存在范德华力,形成的分子晶体是密堆积,密度比水大,故a正确;
b、冰融化时氢键被破,干冰分子之间只存在范德华力,融化时破坏范德华力,氢键比范德华力强,故晶体的熔点冰>干冰,故b错误;
c、水分子间存在氢键,且氢键有方向性,导致水分子形成冰时存在较大的空隙,干冰分子之间只存在范德华力,形成的分子晶体是密堆积,晶体中的空间利用率:干冰>冰,故c正确;
d、干冰分子之间存在范德华力,水分子间存在氢键,晶体中分子间相互作用力类型不相同,故d错误.
故选:ac;
(3)a、金刚石中碳原子与四个碳原子形成4个共价单键,构成正四面体,碳原子的杂化类型为sp 3 杂化;石墨中的碳原子与相邻的三个碳原子以σ键结合,形成平面正六边形结构,碳原子的杂化类型为sp 2 杂化,故a正确;
b、sp 2 杂化中,s轨道的成分比sp 3 杂化更多,而且石墨的碳原子还有大π键所以形成的共价键更短,更牢固,即石墨的层内共价键键长比金刚石的键长短,故b错误;
c、石墨的层内共价键键长比金刚石的键长短,作用力更大,破坏化学键需要更大能量,所以晶体的熔点金刚石<石墨,故c错误;
d、金刚石中碳原子与四个碳原子形成4个共价单键,构成正四面体,键角为109°28′,石墨中的碳原子用sp 2 杂化轨道与相邻的三个碳原子以σ键结合,形成正六角形的平面层状结构,键角为120°,故d错误;
e、金刚石中碳原子与四个碳原子形成4个共价单键,构成正四面体,石墨中的碳原子用sp 2 杂化轨道与相邻的三个碳原子以σ键结合,形成正六角形的平面层状结构,而每个碳原子还有一个2p轨道,其中有一个2p电子.这些p轨道又都互相平行,并垂直于碳原子sp 2 杂化轨道构成的平面,形成了大π键.因而这些π电子可以在整个碳原子平面上活动,类似金属键的性质,石墨为层状结构,层与层之间通过范德华力连接,说明晶体中含有共价键、金属键、范德华力,故e正确;
f、金刚石是原子晶体,石墨为层状结构,层与层之间通过范德华力连接,石墨为混合型晶体,不属于原子晶体,故f错误;
故选:ae;
(4)由金刚石的晶胞结构可知,晶胞内部有4个C原子,面心上有6个C原子,顶点有8个C原子,在BN晶体中,每个B原子和4个N原子形成共价键,所以B原子周围最近的N原子所构成的立体图形为正四面体;B原子的配位数是4,B原子与N原子之间共价键的数目是12,所以B原子与N原子之间共价键的数目与配位键的数目比为 3:1,一个晶胞中N原子数目为 4,
故答案为:正四面体;3:1;4;
(5)铜是29号元素,核外电子排布式为1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 ,原子结构示意图为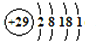
;
金属铜采用面心立方最密堆积,晶胞内Cu原子数目为8×
1
8 +6×
1
2 =4,令铜原子的半径为rcm,则晶胞的棱长为
为
2
2 ×4rcm=2
2 rcm,所以 (2
2 r ) 3 ρ=4
M
N A ,r=
2
4 ×
3
4M
ρ N A
cm,
故答案为: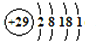
;12;
2
4 ×
3
4M
ρ N A
.1年前查看全部
- 甲烷和乙醇的燃烧产物都是二氧化碳和水,是否可以由此证明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物.
甲烷和乙醇的燃烧产物都是二氧化碳和水,是否可以由此证明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物.
how to do?
我知道答案是不可以证明的.请用化学方程式说明! camplaw1年前7
camplaw1年前7 -
 探新鲜 共回答了17个问题
探新鲜 共回答了17个问题 |采纳率94.1%不可以
因为
CH8+O2=CO2+H2O
C2H5OH+O2=CO2+H2O(我不再配平了,不然看不清)
除去反应物中的氧元素,就剩下碳元素,氢元素了
因为氧气中只有氧元素
所以甲烷是含有碳元素,氢元素的组成的碳氢化合物
但是乙醇不是
它含有氧元素1年前查看全部
- 流向分解者的碳元素是否全部被转化成了无机物排向大气?
 三灌帮白花紫露草1年前3
三灌帮白花紫露草1年前3 -
 fengzi57 共回答了13个问题
fengzi57 共回答了13个问题 |采纳率100%也可以转化为甲烷等有机物排向大气、转化油脂(石油)渗入地下、转化为自身及后代的身体、转化为初级分解物由其他分解者继续分解……1年前查看全部
- 1纯碱不是碱而是( )2由碳元素组成的碳酸盐的物理性质和化学性质,还有其他特殊性质.3由碳元素组成的有机物的物理性质和化
1纯碱不是碱而是( )
2由碳元素组成的碳酸盐的物理性质和化学性质,还有其他特殊性质.
3由碳元素组成的有机物的物理性质和化学性质,还有其他特殊性质.
4高温煅烧碳酸钙制备二氧化碳气体不宜采用的原因
5一块岩石(主要成分是碳酸钙)中发现一段古树的化石(主要成分是碳),欲将化石取出 ,可用的试剂是( ),该反映的化学方程式( ).
6根据H,O,S,Na元素,学出有关物质的化学式:盐( ) lgmql1321年前1
lgmql1321年前1 -
 水月青云 共回答了14个问题
水月青云 共回答了14个问题 |采纳率92.9%1、纯碱不是碱而是盐 2、由碳元素组成的碳酸盐的物理性质和化学性质,还有其他特殊性质 只有碳酸钠和碳酸钾可溶,其余大部分难溶或微溶;可以与酸反应出二氧化碳;特殊性质的决定应该不是由碳元素决定,而是又金属离子...1年前查看全部
- 某种二氧化碳和一氧化碳组成的混合气体中,碳元素的质量分数的合理范围
 何况健少年01年前1
何况健少年01年前1 -
 小鬼0526 共回答了17个问题
小鬼0526 共回答了17个问题 |采纳率82.4%27.3%-42.9%,分别是全都是二氧化碳和全都是一氧化碳时碳的质量分数,介于两者中间都有可能1年前查看全部
- 一氧化碳、二氧化碳、二氧化硫三种气体混合的气体中,已知碳元素的质量占三种气体总和的24%,求二氧化硫在其中的质量的百分数
 5k7h1年前1
5k7h1年前1 -
 z3232085 共回答了14个问题
z3232085 共回答了14个问题 |采纳率85.7%S=6%-22% 是个范围1年前查看全部
- 在酒精中 碳元素的百分含量 要式子
在酒精中 碳元素的百分含量 要式子
H-1 C-12 O-16 S-32 啦啦肥1年前2
啦啦肥1年前2 -
 夏雨辞的母贵性 共回答了19个问题
夏雨辞的母贵性 共回答了19个问题 |采纳率84.2%LS;那个C的相对原子质量应该是12
w(C2H5OH)=(2*12)/(2*12+5+16+1)=52.17%1年前查看全部
- 在苯和苯酚组成的混合物中,碳元素的质量分数为90%,则该混合物中氧元素的质量分数是
 xiaoben52001年前1
xiaoben52001年前1 -
 笑着飘零的秋叶 共回答了17个问题
笑着飘零的秋叶 共回答了17个问题 |采纳率94.1%苯是C6H6
苯酚是C6H6O
C和H的比例是1::1质量比是12:1
则H的质量分数是90%/12=7.5%
则O的质量分数是100%-90%-7.5%=2.5%1年前查看全部
- 等质量的碳酸钠(化学式Na2CO3)碳酸氢钠(化学式NaHCO3)中,碳元素的质量比为( )
等质量的碳酸钠(化学式Na2CO3)碳酸氢钠(化学式NaHCO3)中,碳元素的质量比为( )
A. 1:1
B. 42:53
C. 55:42
D. 85:106 voke1年前3
voke1年前3 -
 yy阳光9929 共回答了18个问题
yy阳光9929 共回答了18个问题 |采纳率94.4%解题思路:设碳酸钠和碳酸氢钠的质量均为mg,然后根据:化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数,分别算出碳酸钠和碳酸氢钠中碳元素的质量,两者相比即可得出结果.设碳酸钠和碳酸氢钠的质量均为mg,碳酸氢钠和碳酸氢钠所含碳元素的质量比为:(mg×[碳原子的相对原子质量×碳原子的原子数/碳酸钠的相对分子质量]×100%):(mg×[碳原子的相对原子质量×碳原子的原子数/碳酸氢钠的相对分子质量]×100%)=[12m/106]:[12m/84]=42:53
故选B.点评:
本题考点: 化合物中某元素的质量计算.
考点点评: 本题难度不是很大,考查根据化学式的有关计算进行分析解题的能力,掌握化合物中元素的质量的计算方法是解题的关键.1年前查看全部
- 1、两个集气瓶中分别盛有纯净的一 氧化碳和二氧化碳气体,测得其中碳元素的质量比为 2 :1,则两瓶气体的质量比为
1、两个集气瓶中分别盛有纯净的一 氧化碳和二氧化碳气体,测得其中碳元素的质量比为 2 :1,则两瓶气体的质量比为
2、X、Y 元素能形成两种化合物 C1,C2.C1 中含X 元素 75%,含 Y 元素 25%,C2 中含 X 元素 80%,含 Y 元素20%.若 C1 XY4,则 C2
3、由碳、氧两种元素组成的物质中,碳与氧的质量比为 3 :5,则该物质可能是( ).
A.由 CO 或 CO2 单独组成的纯净物
B.由 CO 和 CO2 共同组成的混合物
C.由 CO 和 C 共同组成的混合物
D.由 CO2 和 O2 共同组成的混合物
4、某氮肥是含有杂质的硝酸铵(NH4NO3),其中氮元素的质量分数为 38%,这种氮肥中可能含有的杂质是( ).
A.NH4HCO3 B.NH4Cl
C.CO(NH2)2 D.(NH4)2SO4 qinzhi12261年前1
qinzhi12261年前1 -
 l5mfgn 共回答了25个问题
l5mfgn 共回答了25个问题 |采纳率80%第一题:碳元素的质量比为 2 : 1,所以 碳原子它们的摩尔量之比为2:1 因为一 氧化碳和二氧化碳都是含有一个碳原子, 所以一 氧化碳和二氧化碳的摩尔量之比为2:1 然后就 分别乘以一 氧化碳和二氧化碳各自的 相对分子质量 也就是分别为28 和44 结果就是 28乘以2 : 44乘以1 答案为14:11
第二题: 首先你的明白 C1 里含%75 的X是什么意思~ 它是说 质量分数%75
后面的也都是指质量分数 , 你分别假设X、Y的相对原子质量 为x和y
由于C1的化学式是XY4 那么 你就可以由上面的质量分数 算出x和y
列式如下 x 4y
-------= 75% 还有一个是 --------=25%
x+4y x+4y
解得 x=12 y =1 所以X是碳 Y 是氢
然后你就设 c2里 碳原子n个 氢原子z个 那么
12 * n z*1
-----------=80% ----------= 20% 同样解方程组~
12n+z*1 12n+ z*1
解得c2为 C2H6 叫乙烷!
好累~
第三题: 用极限的方法和 假设的思想 加入全是 CO2那么 碳氧的比是
12:32 即3:8 再假设 全是CO那么 比就是 3:4 所以你说 答案是什么~
呵呵 C 其他的自己可以同样的思想去做.
第四题~ 和第三题的方法一样啊~
你先算出硝酸铵(NH4NO3) 中 N 的 质量分数 再
看它 与 38% 哪个大~ 如果大于38% 那么和它混合的肯定的是含N小于 38%的物质~
终于回答完了~~~ 给我分哈~ 早饭还没吃呢~1年前查看全部
- 煤的一种干馏产品,碳元素的质量分数为90.6%,其蒸气密度是空气的3.66倍,能使高锰酸钾褪色,但不能是溴...
煤的一种干馏产品,碳元素的质量分数为90.6%,其蒸气密度是空气的3.66倍,能使高锰酸钾褪色,但不能是溴...
煤的一种干馏产品,碳元素的质量分数为90.6%,其蒸气密度是空气的3.66倍,能使高锰酸钾褪色,但不能是溴水褪色,这是什么东西?要推理过程. 乡里乡亲啊1年前1
乡里乡亲啊1年前1 -
 夜凉如清水 共回答了21个问题
夜凉如清水 共回答了21个问题 |采纳率85.7%其蒸气密度是空气的3.66倍,那么其物质的量为29*3.66=106 又碳元素的质量分数为90.6%,碳元素质量为106*90.6%=96 其余为氢元素,其化学方程式为C8H10,也就是二甲苯.至于究竟是1,4二甲苯还是别的类型就不得而知了.1年前查看全部
- “碳元素是各种化合物中含量最多的元素”这句话为什么错?
 ff少年1年前3
ff少年1年前3 -
 随风1102 共回答了18个问题
随风1102 共回答了18个问题 |采纳率88.9%解析:
由C元素形成的化合物种类最多(绝大多数为有机化合物).
在地壳中含量最多的元素是O元素,大约占总质量的一半.
概念错误.1年前查看全部
- 1.医用葡萄糖(C 2 H 12 O 6)注射液是用葡萄糖和水配制而成的,测得葡萄糖溶液中碳元素的质量分数为2%,则该注
1.医用葡萄糖(C 2 H 12 O 6)注射液是用葡萄糖和水配制而成的,测得葡萄糖溶液中碳元素的质量分数为2%,则该注射液中溶质的质量分数为多少?
——————————————————
2.背溶解性表有什么用啊?
————————————————
C6H12O6 dabin111年前1
dabin111年前1 -
 欲爆的rr 共回答了15个问题
欲爆的rr 共回答了15个问题 |采纳率100%C占葡萄糖溶液2%
C6 H12 O6中C的质量分数为(12*6)/(12*6+12+16*6)=40%
那么C6 H12 O6占溶质的质量分数是2%/40%,再换算成百分比等于5%
该注射液中溶质的质量分数为5%
背溶解性表可以让你记住哪些物质是沉淀,哪些物质溶于水
也就是物质在水中的溶解性
主要用来判断一些离子是否可以共存,或者检查溶液中是否存在某种离子
知道了吗啊?1年前查看全部
- h2o ch2o c2h4o 的混合物,测得其中碳元素的质量百分含量为X%则氢元素的质量百分含量应为?
 江75961年前1
江75961年前1 -
 暗夜yy 共回答了21个问题
暗夜yy 共回答了21个问题 |采纳率81%凌空飞翼 :你的题目可能有问题?把C2H4O改成C2H4O2才可以解.
(1-X%)是H、O的质量百分含量,把H2O、CH2O、C2H4O2改写为H2O、C(H2O)、C2(H2O)2,可以看出H、O两元素按1:8比例组成.则氢元素的质量百分含量应为(1-X%)×1/91年前查看全部
- (2011•钦州)航天探测发现:金星周围的大气层3含有三氧化二碳(的23你),则的23你3碳元素的化合价为( )
(2011•钦州)航天探测发现:金星周围的大气层3含有三氧化二碳(的23你),则的23你3碳元素的化合价为( )
A.+1
B.+2
C.+3
D.+4 zyhyy1年前1
zyhyy1年前1 -
 刘健349 共回答了17个问题
刘健349 共回答了17个问题 |采纳率82.4%解题思路:金星周围的大气层中含有三氧化二碳(C2O3),已知氧元素的化合价为-2价,根据化合价的原则:化合物中正负化合价的代数和为零,故可知C2O3中碳元素的化合价.已知氧元素的化合价为-2价,根据化合价的原则:化合物手正负化合价的代数和为零,则设C2O多手碳元素的化合价为7,则27+多×(-2)=0,故7=+多,故可知C2O多手碳元素的化合价为+多价.
故选C.点评:
本题考点: 化学式的书写及意义;常见元素与常见原子团的化合价;有关元素化合价的计算.
考点点评: 掌握根据化合价的原则:化合物中正负化合价的代数和为零,求未知化合价的方法.1年前查看全部
- 化学问题对于本分子说法错误的是( )A.苯分子是碳元素和氢元素组成的.B.苯分子中碳元素和氢元素的个数比是1:1C.苯分
化学问题
对于本分子说法错误的是( )
A.苯分子是碳元素和氢元素组成的.
B.苯分子中碳元素和氢元素的个数比是1:1
C.苯分子是由碳原子、氢原子构成的
D.一个苯分子有42个电子
哪位帮忙解释一下?
谢谢啦~~~O(∩_∩)O~
马上中考
在线等
大家帮帮啦~~~~~~~~~~
( ^_^ )/~~
那个......b应该是
B.苯分子中碳原子和氢原子的个数比是1:1 酸辣菜苔1年前0
酸辣菜苔1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 碳元素和氮元素属于不同种元素原因是 碳12原子和碳13原子是不同种原子的原因是
 traveller771年前1
traveller771年前1 -
 籽念 共回答了19个问题
籽念 共回答了19个问题 |采纳率94.7%碳元素和氮元素属于不同种元素原因是 碳原子和氮原子所含的质子数不同
碳12原子和碳13原子是不同种原子的原因是 碳12原子和碳13原子所含的中子数不同1年前查看全部
- 碳元素所形成的化合物的种类是所有化合物中最多的.已知碳元素与某非金属元素R可形成化合物CRX,且知在一个CRX分子中各原
碳元素所形成的化合物的种类是所有化合物中最多的.已知碳元素与某非金属元素R可形成化合物CRX,且知在一个CRX分子中各原子的电子数之和为74,则R的原子序数和X的值分别是( )
A. 16,2
B. 35,4
C. 17,4
D. 26,3 但愿月圆1年前4
但愿月圆1年前4 -
 大智无谋 共回答了14个问题
大智无谋 共回答了14个问题 |采纳率85.7%解题思路:根据原子中质子数=原子序数=核外电子数进行分析,表示出一个R原子中的电子数和x的关系,然后分别代入选项所提供的数值进行验证即可.已知一个碳原子中有6个电子,设一个R原子的电子数为a,那么一个R原子中所含的电子数(即原子序数)为a=[74−6/x]=[68/x],即ax=68,然后分别代入选项数据,只有a=17,x=4时符合条件.
故选C点评:
本题考点: 分子、原子、离子、元素与物质之间的关系;原子的定义与构成;原子的有关数量计算.
考点点评: 了解原子中各种粒子之间的关系是解题关键,在原子中:核电荷数=质子数=原子序数=核外电子数.1年前查看全部
- (2012•河东区一模)在CO和CO2的混合气体中,碳元素的质量分数是36%,将该气体10g通过足量灼热的CuO粉末,完
(2012•河东区一模)在CO和CO2的混合气体中,碳元素的质量分数是36%,将该气体10g通过足量灼热的CuO粉末,完全反应后,气体通入足量的澄清石灰水中,得到白色沉淀的质量是( )
A.10g
B.13.4g
C.30g
D.40g liufeng2820011年前1
liufeng2820011年前1 -
 晔蓝 共回答了20个问题
晔蓝 共回答了20个问题 |采纳率85%解题思路:根据混合气体的质量与碳元素的质量分数可计算碳元素的质量,然后利用碳元素的质量守恒来计算生成碳酸钙的质量.根据质量守恒混合气体中碳元素的质量即为碳酸钙中碳元素的质量;
则生成碳酸钙的质量为:10g×36%÷
12
40+12+16×3=30g
故选C.点评:
本题考点: 质量守恒定律及其应用;化合物中某元素的质量计算;混合物中某元素的质量计算.
考点点评: 本题考查学生利用物质发生的化学反应,借助元素在物质的存在形式,巧妙利用元素守恒的方法来计算,注重学科思维方法在解题中的应用.1年前查看全部
- 利巴韦林是有机物还是无机物?C H N O的质量比是多少?碳元素的质量分数为?
 doncenter1年前0
doncenter1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 多少克乙酸乙酯中含有的碳元素与88gCO2中含有的碳元素的质量相等?
 ice-alex1年前2
ice-alex1年前2 -
 枫起风落 共回答了10个问题
枫起风落 共回答了10个问题 |采纳率80%88gCO2中有2摩尔C ,而一摩尔乙酸乙酯中含有4摩尔C,所以需要0.5摩尔乙酸乙酯.
0.5*88=44克1年前查看全部
- 甲烷和乙醇的燃烧产物都是水和二氧化碳,是否可以证明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物
 花开浅浅1年前4
花开浅浅1年前4 -
 skyfree7210 共回答了18个问题
skyfree7210 共回答了18个问题 |采纳率94.4%不可以
甲烷和乙醇的燃烧产物都是二氧化碳和水,只能由此证明甲烷和乙醇都含有有碳元素和氢元素,但不能证明有没有氧元素.1年前查看全部
- 碳元素是组成许多物质的基本元素.
 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.
(1)下列含碳元素的物质中,属于有机物的是______
A.碳酸钙B.乙醇(C2H5OH)C.二氧化碳
(2)化石燃料主要包括煤、______和天然气,它们都含有碳元素,其中天然气的主要成分是______(写化学式).
(3)“碳海绵”是已知最轻的固体材料(如图所示),由碳元素组成,具有多孔结构,弹性好.它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状.下列关于碳海绵的说法不正确的是______
A.具有吸附性
B.可重复使用
C.可处理海上石油泄漏
D.会与吸入的石油发生化学反应. tt31021年前1
tt31021年前1 -
 天下一贼 共回答了18个问题
天下一贼 共回答了18个问题 |采纳率72.2%解题思路:(1)据有机物的概念和特殊情况分析;
(2)据化石燃料的种类和天然气的主要成分分析;
(3)根据题意,“碳海绵”是已知最轻的固体材料(如图所示),由碳元素组成,具有多孔结构,弹性好.它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状,据此结合碳单质的物理性质进行分析判断即可.(1)除一氧化碳、二氧化碳、碳酸以及碳酸盐外,含碳元素的化合物称为有机物,因此,乙醇(C2H5OH ) 属于有机;
(2)化石燃料主要包括煤、石油和天然气,其中天然气的主要成分是CH4
(3)A、由题意,“碳海绵”是已知最轻的固体材料(如图所示),由碳元素组成,具有多孔结构,有很强的吸附能力(不吸水),具有吸附性,故选项说法正确.
B、由题意,将吸入的石油挤出后仍可恢复原状,可知碳海绵可重复使用,故选项说法正确.
C、由题意,它对石油有很强的吸附能力(不吸水),可处理海上石油泄漏,故选项说法正确.
D、根据题意,碳海绵吸附物质的过程属于物理变化,故选项说法错误.
故选:D.
故答案为:(1)B(1分)(2)石油(1分)CH4(1分)(3)D(1分)点评:
本题考点: 有机物与无机物的区别;碳单质的物理性质及用途;化石燃料及其综合利用.
考点点评: 本题难度不大,物质的性质决定物质的用途,理解题意、掌握常见碳单质的性质并能灵活运用是正确解答本题的关键.1年前查看全部
- 三种化合物A、B、C具有相同的最简式.经测定其分子中只含碳氢两种元素,且碳元素质量分数均为92.3%.已知A、B、C分子
三种化合物A、B、C具有相同的最简式.经测定其分子中只含碳氢两种元素,且碳元素质量分数均为92.3%.已知A、B、C分子量之比为1:3:4,A在常温下为气态,B、C为芳香烃,B不能使溴水褪色,C能使溴水褪色.
(1)写出A、B、C的结构简式.
(2)由C可合成一种塑料,写出该反应的化学方程式.
(3)C与氢气按物质的量1:1加成后的产物,可否被酸性高锰酸钾溶液氧化?若能,写出氧化产物的结构简式. 一天到晚乱飞的猪1年前1
一天到晚乱飞的猪1年前1 -
 hhh22647 共回答了19个问题
hhh22647 共回答了19个问题 |采纳率73.7%解题思路:(1)根据碳元素的质量分数计算出氢元素的质量分数,然后确定三者的最简式,再根据B、C为芳香烃及B不能使溴水褪色得出B为苯,然后分别确定A、C,并写出A、B、C的结构简式;(2)C为苯乙烯,苯乙烯能够发生加聚反应生成聚苯乙烯,据此写出反应的化学方程式;(3)苯乙烯与氢气按照物质的量1:1发生加成反应生成乙苯,乙苯能够被酸性高锰酸钾溶液氧化成苯甲酸,写出苯甲酸的结构简式.(1)A、B、C具有相同的最简式,分子中只含碳、氢两种元素,碳元素质量分数均为92.3%,则氢元素的质量分数为:1-92.3%=7.7%,则其分子中C、H原子数之比为:[92.3%/12]:[7.7%/1]=1:1,所以A、B、C的结构简式为CH;
B、C为芳香烃,B不能使溴水褪色,C能使溴水褪色,则B一定为苯,分子式为:C6H6,结构简式为: ;已知A、B、C分子量之比为1:3:4,则A的分子式为C2H2,即A为乙炔,结构简式为:CH≡CH;C的分子式为C8H8,C为芳香烃、能够使溴水褪色,则C只能为苯乙烯,结构简式为:
;已知A、B、C分子量之比为1:3:4,则A的分子式为C2H2,即A为乙炔,结构简式为:CH≡CH;C的分子式为C8H8,C为芳香烃、能够使溴水褪色,则C只能为苯乙烯,结构简式为: ,
,
答:A、B、C的结构简式分别为:CH≡CH、 、
、 ;
;
(2)一定条件下,苯乙烯发生聚合反应生成聚苯乙烯,反应方程式为:n
催化剂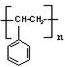 ,
,
答:该反应的化学方程式为n
催化剂 ;
;
(3)苯乙烯与氢气按照物质的量1:1与氢气加成生成乙苯: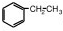 ,乙苯为苯的同系物,连接苯环的碳原子含有H,能够被酸性高锰酸钾溶液氧化生成苯甲酸,苯甲酸的结构简式为:
,乙苯为苯的同系物,连接苯环的碳原子含有H,能够被酸性高锰酸钾溶液氧化生成苯甲酸,苯甲酸的结构简式为: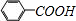 ,
,
答:乙苯能够被酸性高锰酸钾溶液氧化,氧化产物为苯甲酸,结构简式为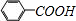 .
.点评:
本题考点: 有关有机物分子式确定的计算;有机物实验式和分子式的确定.
考点点评: 本题考查了有机物分子式、结构简式的计算、有机物结构与性质,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,明确常见有机物结构与性质为解答本题的关键.1年前查看全部
- 碳元素的单质有哪些
 cui30267411年前5
cui30267411年前5 -
 咖啡香Fortune 共回答了17个问题
咖啡香Fortune 共回答了17个问题 |采纳率88.2%金刚石、石墨、C60、碳纳米管
另还有:C50、C72等等
(有些人可能要说:木炭、活性炭、焦炭、炭黑都是碳元素的单质——它们事实上是含有少量杂质的石墨)1年前查看全部
- 关于“地球上的生命是在碳元素的基础上建立起来的”原因的叙述,错误的是( )
关于“地球上的生命是在碳元素的基础上建立起来的”原因的叙述,错误的是( )
A. 碳元素在生物体内含量最多
B. 碳原子含有4个价电子
C. 碳原子之间能以共价键结合
D. 许多含碳有机物能连接成链或环 fossil-20041年前1
fossil-20041年前1 -
 CJJfpp 共回答了14个问题
CJJfpp 共回答了14个问题 |采纳率100%解题思路:组成细胞的大量元素有:C、H、O、N、P、S、K、Ca、Mg,其中C、H、O、N是组成细胞的基本元素,C是组成细胞的最基本元素,因为碳链是构成生物大分子的基本骨架.据此答题.地球上的生命是在碳元素的基础上建立起来的.说明了碳原子的重要性.组成细胞的基本元素有:C、H、O、N,其中C是组成细胞的最基本元素,并非因它的含量高,而是因为碳原子含有4个价电子,易形成共价键,从而形成碳链构成生物大分子的基本骨架.
故选:A.点评:
本题考点: 碳原子的结构特点.
考点点评: 本题结合材料,考查组成细胞的元素的相关知识,要求考生识记组成细胞的元素的种类、含量和作用,明确C是组成生物体的最基本的元素,再选出正确的答案,属于考纲识记层次的考查.1年前查看全部
- 石蜡只是由碳元素和氢元素两种元素组成的么?
 天使之珠1年前1
天使之珠1年前1 -
 pphail 共回答了21个问题
pphail 共回答了21个问题 |采纳率85.7%是.碳氢化合物.1年前查看全部
- 由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
A. 15.6%
B. 26.7%
C. 30%
D. 无法确定 ljmgdjsj1年前1
ljmgdjsj1年前1 -
 为你哭丧 共回答了18个问题
为你哭丧 共回答了18个问题 |采纳率100%解题思路:乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,根据碳元素的质量百分含量可计算出C2H4的质量分数,进而计算的质量分数,进而计算氧元素的质量百分含量.乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,
已知:ω(C)=60%,则ω(C2H4)=60%×[28/24]=70%,
则ω(H2O)=1-70%=30%,
所以:ω(O)=30%×[16/18]=26.7%,
故选B.点评:
本题考点: 元素质量分数的计算.
考点点评: 本题考查元素质量分数的计算,题目难度不大,注意利用分子式的转化,将乙醇的分子式可作C2H4•H2O.1年前查看全部
- 碳元素原子最外层4个电子,易得还是失电子
 jenny1801年前3
jenny1801年前3 -
 玫瑰的王子 共回答了22个问题
玫瑰的王子 共回答了22个问题 |采纳率90.9%既不易得电子,也不易失电子,所以碳的单质很稳定1年前查看全部
大家在问
- 1童趣中 神游 啥意思?
- 2已知二次函数f(x)满足f(2-x)=f(x),且在y轴上的截距为-1,被x轴截得线段长为4根号2,求f(x
- 3英语中定语都可以做什么成分?
- 4锌与等体积等PH的盐酸和醋酸反应
- 5既然胃蛋白酶属于蛋白质,那么为什么胃蛋白酶不会互相分解呢?
- 6兰 用英语读什么?
- 7已知如图在四边形ABCD中,E,FG,H分别是AB,CD,AC,BD的中点.求证:四边形EGFH是平行四边形
- 8三点水加懒去掉竖心旁您念什么
- 9三点水加心念什么,请用拼音打出来 .
- 10三点水加各心念啥
- 11共价键的强弱怎么判断
- 12共价键强弱判断
- 13共价键的强弱判断是根据电负性差值的大小.还是根据原子半径?那你怎么判断:H-F和H-O 他们的大小..不是根据电负性或原
- 14当m为何值时,关于x的方程5m+2x=二分之一+x的解比关于x的方程x(m+1)=m(1+x)的解大2
- 15用水银,酒精,煤油制作的温度计有什么区别?
