碳正离子
 comoneon2022-10-04 11:39:541条回答
comoneon2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 普鲁弗 共回答了25个问题
普鲁弗 共回答了25个问题 |采纳率88%- 碳正离子是一种带正电的极不稳定的碳氢化合物.分析这种物质对发现能廉价制造几十种当代必需的化工产品是至关重要的.欧拉教授发现了利用超强酸使碳正离子保持稳定的方法,能够配制高浓度的碳正离子和仔细研究它.他的发现已用于提高炼油的效率、生产无铅汽油和研制新药物.
- 1年前
相关推荐
- 问懂有机化学的几个问题(都与生成的碳正离子中间体稳定性有关)
问懂有机化学的几个问题(都与生成的碳正离子中间体稳定性有关)
(1) 比较CH3CH=CHCH3 和H2C=CHCH(CH3)2 两者与H2SO4反应的活性大小
(2) CH3CH=CHCH(CH3)2 + H2SO4 →
那个H2SO4产生的—OSO3基团到底是加在左边还是右边的碳上啊?
(3) CH3CH=CHC=CHCH(CH3)2 + HCl →
〡
CH3
如果发生1,4加成的话 —C1加在左边还是右边的碳上? zxx42971年前2
zxx42971年前2 -
 我威如天的yy3 共回答了19个问题
我威如天的yy3 共回答了19个问题 |采纳率78.9%(1),CH3CH=CHCH3对称,H2C=CHCH(CH3)2 中,第二个C有形式正电,易与H-OSO3加成.
(2),CH3-的推电子能力比-CH(CH3)2强,第二个双键C有形式正电,带形式负电的—OSO3易加在第二个双键C上.
(3),同上,CH3-的推电子能力比-CH(CH3)2强,第二个双键C有形式正电,带形式负电的Cl易加在右边的碳上.1年前查看全部
- 有双键的碳正离子和无双键的那个更稳定?例如c-c-c-和c=c-c-
 小丁93971年前1
小丁93971年前1 -
 nyyfxx 共回答了17个问题
nyyfxx 共回答了17个问题 |采纳率88.2%双键不稳定.1年前查看全部
- 关于重排碳正离子和不稳定的环都有可能重排,但是这些重排(尤其是碳正离子)往往需要一定条件,那么这般在什么条件下会重排呢?
关于重排
碳正离子和不稳定的环都有可能重排,但是这些重排(尤其是碳正离子)往往需要一定条件,那么这般在什么条件下会重排呢?(主要是SN1机理中的碳正离子)请举出具体例子 huaihuaizy1年前2
huaihuaizy1年前2 -
 蚊子妞 共回答了19个问题
蚊子妞 共回答了19个问题 |采纳率94.7%分子中共价键结合顺序发生改变的反应.这种改变可导
致碳架或官能团位置发生变化,有时因为伴有进一步变化而
得到分子组成与反应物并不相同的重排产物,按反应机理 ,
重排反应可分为:基团迁移重排反应和周环反应.
基团迁移重排反应 反应物分子中的一个基团在分子范
围内从某位置迁移到另一位置的反应.常见的迁移基团是烃
基.迁移基团的原来位置称为迁移起点,迁移后的位置称为
迁移终点,这类反应又可按价键断裂方式分为异裂和均裂 ,
前者重要得多,其中尤以缺电子重排最为重要.
缺电子重排反应是反应物分子先在迁移终点形成一个缺
电子活性中心,从而促使迁移基团带着键裂的电子对发生迁
移,并通过进一步变化生成稳定产物.以频哪酮重排反应为
例,反应物分子中的一个羟基与酸作用形成锌盐后失水变为
缺电子活性中心正碳离子,促使邻位带羟基碳原子上的一个
甲基带着电子对发生1,2-迁移,同时羟 基氧原子 上未共用
电子对转移至碳?氧之间构成双键,最后失去质子而得产物
(见上反应式).在迁移终点形成一个富电子活性中心后 ,
促使迁移基团不带键裂电子对而转移,叫富电子重排反应 ,
例如法沃斯基重排:a - 卤代酮 在强碱作用 下重排,生成碳
架不同的羟酸酯,反应通过富电子活性中心负碳离子进行 :
环反应 反应物因分子内共价键协同变化而发生重排
的反应,有电环化反应和δ迁移反应.例如环丁烯经加热发
生逆向电环化而得1,3-丁二烯,1,3-己二烯经加热发生氢
原子1,5-迁移而得2,4-己二烯.这类重排在合成中应用最
多的是属于3,3-迁移的科 普重排和克 莱森重排.科普重排
是1,5-二烯受热重排为另一个1,5-二烯的反应.例如内消
旋-3,4-二甲基-1,5-己二烯经加热几乎定量地转变为(Z ,
E)-2,6-辛二烯:
克莱森重排反应是参与反应的体系中有一个氧原子代替
了碳原子.例如,苯基烯丙醚经加热重排生成的环己二烯酮,
随即异构化为邻烯丙基苯酚.1年前查看全部
- 碳正离子稳定性比较?见 下图的两个碳正离子 比较稳定性
 xiaoyanzi2001年前2
xiaoyanzi2001年前2 -
 荆天 共回答了19个问题
荆天 共回答了19个问题 |采纳率78.9%碳正离子稳定性:3级>2级>1级,带点的C连的C多的稳定
这里两个同级,应该就比较附近的C,左边的稳定吧(没画的部分我当H理解)1年前查看全部
- 碳正离子中带正电荷的碳未杂化的p轨道上有几个电子?
 浪子十年1年前1
浪子十年1年前1 -
 peng1118 共回答了16个问题
peng1118 共回答了16个问题 |采纳率93.8%应该是0个,也就是说这个p轨道是空轨道.这样想,以甲基正离子为例,甲烷上一个H如果发生均裂(即共用电子对中的两个电子各自物归原主,平均分配,分裂后两部分都不产生电性),形成一个甲基,此时C原子杂化方式sp3,但是一条p轨道上只有1个电子,这是甲基,甲基失去一个电子后形成甲基正离子,C正离子是以SP2杂化,那条原来只有一个电子的p轨道上的唯一一个电子失去了,形成空轨道.1年前查看全部
- 下列碳正离子最稳定的是?如题,选项为:(A)苄基正离子(B)对甲氧基苄基正离子(C)对氯苄基正离子(D)对硝基苄基正离子
下列碳正离子最稳定的是?
如题,选项为:
(A)苄基正离子
(B)对甲氧基苄基正离子
(C)对氯苄基正离子
(D)对硝基苄基正离子
一头雾水.看书看碳正离子很抽象,做题时就更加抽象.该如何判断?以简单明了的方法?让我明白怎么判断和选出答案即可. 明白着好1年前1
明白着好1年前1 -
 飞哥128 共回答了20个问题
飞哥128 共回答了20个问题 |采纳率90%碳正离子肯定是缺电子,看附近的基团是什么样的.如果是吸电子的,就会更不稳定,如果是推电子的,就会稳定.至于基团吸或者推电子的强弱:常见的吸电子基团(吸电子诱导效应用-I表示) NO2 > CN > F > Cl > Br > I > C三C...1年前查看全部
- 叔丁基碳正离子为什么会有未杂化的空p轨道?
 oo为131年前1
oo为131年前1 -
 豆末糖 共回答了17个问题
豆末糖 共回答了17个问题 |采纳率94.1%C:1s22s22p2 p轨道分为px,py,pz,用了2个进行杂化就剩下一个了.1年前查看全部
- 为什么碳正离子的稳定性顺序是这个样的
 padavid1年前2
padavid1年前2 -
 兔兔and狗狗 共回答了22个问题
兔兔and狗狗 共回答了22个问题 |采纳率95.5%首先 A,C,D比较,都含有双键,且都形成p-π共轭,但D是叔C正离子,而A是仲碳正离子,C是伯碳正离子,碳正离子稳定性 叔>仲>伯
所以D>A>C
B没有共轭体系 最不稳定
所以稳定性D>A>C>B1年前查看全部
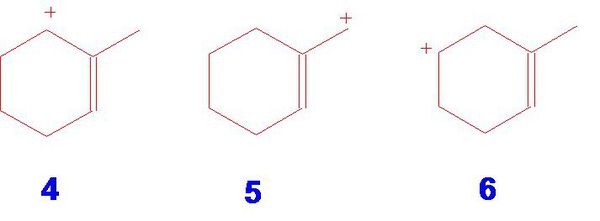
- 有机化学题,判碳正离子的稳定性4和5怎么比较?都是稀丙位上的碳正离子.还有6?CH2=CH2-Cl 与CH2=
有机化学题,判碳正离子的稳定性
4和5怎么比较?都是稀丙位上的碳正离子.
还有6?
CH2=CH2-Cl 与CH2=CH2-CH3与CH2=CH2哪个反应活性大?
烯烃的活性是否与连有的基团有关,是吸电子基,还是给电子基?
 猪猪爱上树1年前4
猪猪爱上树1年前4 -
 jsxjywj 共回答了26个问题
jsxjywj 共回答了26个问题 |采纳率84.6%4比较稳定,因为4中有临近环上的超共轭作用存在,稳定碳正离子.而5则是在端上,相比之下,4 就稳定些.
CH2=CH2-Cl (a),CH2=CH2-CH3 (b),CH2=CH2 (c)的活性需要分是亲电反应还是亲核反应:
如果是亲核反应,则比较电子密度大小,电子密度小的就活性大,活性顺序:a>b>c
如果是亲电反应,则电子密度大,活性大,顺序:c>b>a1年前查看全部
- 1mol CH3+(碳正离子)中的电子数为多少?
 keleji3331年前1
keleji3331年前1 -
 叶落城市-京 共回答了11个问题
叶落城市-京 共回答了11个问题 |采纳率90.9%一个C原子有6个电子
一个H原子有1个电子
因为CH3带有一个单位正电荷
所以1mol CH3+(碳正离子)中的电子数 = 6+1*3-1 = 8NA1年前查看全部
- 怎样区别一个有机物中的碳是碳正离子还是碳负离子?
 江上孤客1年前4
江上孤客1年前4 -
 westkingking 共回答了14个问题
westkingking 共回答了14个问题 |采纳率92.9%我认为你可以完完全全无视1L和3L的内容 他们连题目都没看懂
碳正离子的形成过程大概是这样的:
C+上原本连有一个电负性较大的或者吸电子的基团(如-Br -OH等)
那么这个基团就会将它连接的碳上的电子吸引过去 使该碳稍微显正电性
吸电子基团在适当溶液中还可能带着一对电子离去(例如Br-)
那么剩下的烃基就形成了碳正离子
例子:CH2=CH-CH2Br CH3-CO-CH-COOCH2CH3(-) + CH3CH2OH + Na+1年前查看全部
- 碳自由基的稳定性和碳正离子稳定性相同吗?
 syl_tianya1年前4
syl_tianya1年前4 -
 ldsh82 共回答了16个问题
ldsh82 共回答了16个问题 |采纳率93.8%1.5.4 碳正离子、碳负离子和碳自由基的结构与稳定性
在反应过程中,成键的碳原子由于共价键的断裂方式不同可以形成带有正电荷、负电荷或一个未成对电子的碳原子,这些碳原子分别被称为碳正离子(carbon cations)、碳负离子(carbon anions)或碳自由基(carbon radicals).
实验事实表明碳正离子和碳自由基具有平面结构,而碳负离子则呈角锥状,因此杂化轨道理论指出在碳正离子和碳自由基中,碳原子都采用sp2杂化方式,并使用3个sp2杂化轨道形成3个σ键,形成一个平面的分子.不同的是,在碳正离子中,2p轨道上没有电子,而在碳自由基中,2p轨道上有一个单电子.
碳负离子的结构与碳正离子或碳自由基不同,因为带负电荷的碳原子最外层有3对成键电子和1对未成键电子,这样的4对电子需要采取相互远离的方式排列,因此碳负离子采用sp3杂化轨道成键,未成键电子对与3个共价键形成一个四面体结构.碳正离子、碳自由基和碳负离子的结构对比如下图所示.
碳正离子、碳自由基和碳负离子的结构与稳定性直接受到与之相连接的基团的影响.它们稳定性的一般规律如下:
(1)苄基型或烯丙型一般较稳定;
(2)碳正离子或碳自由基是:3°>2°>1°;
(3)碳负离子则是1°>2°>3°.1年前查看全部
- 关于碳正离子稳定性是怎样比较的
 花吻1年前1
花吻1年前1 -
 黑_瞳 共回答了25个问题
黑_瞳 共回答了25个问题 |采纳率88%看碳正离子上连接的集团
1.如果连接烷基、H等,由于碳正离子是Sp2杂化,有空的p轨道,会和烷基的C-Hsigma形成超共轭,进而分散碳正离子的电荷,使之稳定.所以,连接的烷基越多越稳定,即叔碳正离子>仲碳正离子>伯碳正离子>甲基.
2.如果连接的卤素,以Cl为例,cl的电负性大于c,有吸电子的诱导,同时是2s2 2px2 spy2 2pz,即有未成对电子,有碳正离子是Sp2 杂化,有空的p轨道,cl未成对的电子可以到空轨道上去,则可以分散正电荷,总的效果是使碳正离子更不稳定.
3如果是烯丙型和苄基型的碳正离子,由于p-pai共轭,可以分散电荷,是碳正离子更稳定1年前查看全部
- 在CH3-CH+-Cl(正电荷在CH上)碳正离子中,氯的孤电子对和正电荷形成的是什么共轭效应?
 乌榄肉松饭1年前1
乌榄肉松饭1年前1 -
 twinsenwells 共回答了15个问题
twinsenwells 共回答了15个问题 |采纳率93.3%p-p共轭效应:Cl上的孤电子对(主要是p轨道上)与C上的p空轨道(C正离子上有一个p空轨道)1年前查看全部
- 讨论影响碳正离子和碳自由基稳定性的因素(考虑诱导效应,共轭效应,超共轭效应),并要举例说明。谢谢
 张冠李戴LQWJ1年前1
张冠李戴LQWJ1年前1 -
 loveyouwei 共回答了14个问题
loveyouwei 共回答了14个问题 |采纳率78.6%你看看邢其毅版的有机化学上册介绍自由基的那部分,分的很详细。1年前查看全部
- 比较下列碳正离子稳定性,为什么?
比较下列碳正离子稳定性,为什么?
C6H5*CHCH3 C6H5CH2*CH2 *C(CH3)3 *CH(CH3)2
看的懂吧,手机打字的说
星号右边的是要比较的碳正离子,答案是第一个最镇定,为什么? weilun_ho1年前2
weilun_ho1年前2 -
 yem3631 共回答了15个问题
yem3631 共回答了15个问题 |采纳率93.3%碳正离子的稳定取决于连接的烃基取代基的多少,因为烃基越多,对正电荷的分散越有利;第一个是苄基的碳正离子,因为有苯环的存在(富电子的),所以碳正离子稳定性很好.1年前查看全部
- 怎么比较有机反应中自由基的稳定性和碳正离子的稳定性啊?
 五指1年前1
五指1年前1 -
 ckwcln 共回答了21个问题
ckwcln 共回答了21个问题 |采纳率95.2%自由基的稳定性和碳正离子的稳定性的规律相同,中心碳原子(带自由基或正电的碳原子)上连的供电取代基(如烷基,烷氧基等)越多,则自由基或者、碳正离子越稳定.1年前查看全部
- 碳正离子重排的一道题该化合物与两分子HCL加成时,上面那一部分是怎样进行碳正离子重排的?最后的生成产物又是什么?比如H首
碳正离子重排的一道题

该化合物与两分子HCL加成时,上面那一部分是怎样进行碳正离子重排的?最后的生成产物又是什么?
比如H首先加到哪个C上,比如六元环是如何一步一步形成的... wemustbe1年前2
wemustbe1年前2 -
 fys1985 共回答了25个问题
fys1985 共回答了25个问题 |采纳率84%形成六元环,双键移位
解题思路:1.碳正一定是先存在于多支链碳上,所以这里只能有两种选择
2.重排以后形成的六元环更趋于稳定,共扼双键的转移
这个要贴图了,太麻烦
电子云的转移自己可以画一下,其实就是先形成右边的碳正,然后左边的双键移位和右边的双键连接形成单键,这个双键转移到右边去形成新的双键,而正电荷会转移到左边,左边最后会夺走一个电荷而形成最终的产物1年前查看全部
- 关于E1反应中碳正离子重排的问题
关于E1反应中碳正离子重排的问题
关于下面这句:
醇分子内脱水生成烯,主要按E1机理进行,由于碳正离子的生成,易发生分子重排;但用Al2O3(氧化铝)等lewis酸(即电子受体)脱水,不发生重排.
我知道如果用质子酸,是可以发生碳正离子重排的.为什么用lewis酸就不会发生重排了呢? 多嘴猫1年前1
多嘴猫1年前1 -
 潘多拉007 共回答了19个问题
潘多拉007 共回答了19个问题 |采纳率89.5%用Al2O3(氧化铝)等lewis酸A 并不是不会发生重排,而是不易发生重排.
用Al2O3(氧化铝)催化脱水是将醇的蒸汽通过350-400度的氧化铝,由于醇与生成物烯烃与催化剂的接触时间较短,可以减少异化物等副反应.
当然情况不限于上面这种
重排反应与碳正离子直接消去H+是相互竞争的
温度升高,或者-OH…A基团的离去性较好都是更有利于直接E1的.
以上是我个人理解,不知可否帮上你?1年前查看全部
- 每摩尔物质含有阿伏加德罗常数(NA)个微粒.这是对的不?1molCH3+(碳正离子)中含有电子数为8NA.
每摩尔物质含有阿伏加德罗常数(NA)个微粒.这是对的不?1molCH3+(碳正离子)中含有电子数为8NA.
这是为什么?电子数也就是微粒数吧?这也是1mol丫.为什么不是NA个,而是8NA? Jorgy1年前3
Jorgy1年前3 -
 zz995100 共回答了18个问题
zz995100 共回答了18个问题 |采纳率88.9%电子数是分子中所有原子所含的电子数之和.
1个CH3+含有1个C和3个H.
1个C含有6个电子,1个H含有1个电子,所以是6+3=9,因为还带有一个单位的正电荷,所以需要减去一个电子,是9-1=8.
所以电子是8mol,数目是8NA.1年前查看全部
- 比较下列碳正离子的稳定性A. A>B>C>DB. B>A>D>C
比较下列碳正离子的稳定性
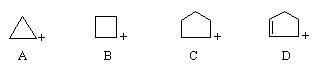
A. A>B>C>DB. B>A>D>CC. C>A>C>DD. D>C>B>A求解析谢谢 saohoo1年前1
saohoo1年前1 -
 coming516 共回答了12个问题
coming516 共回答了12个问题 |采纳率91.7%应该选D,我只知道稀丙基碳正离子最稳定,D就是稀丙基碳正离子,所以应该选D,但另外几个稳定性的排列我就不知道了.1年前查看全部
- 给电子基团可使碳正离子稳定,那么更容易发生亲核反应还是亲电反应,为什么?
 若宁1年前2
若宁1年前2 -
 libaim8900 共回答了17个问题
libaim8900 共回答了17个问题 |采纳率100%你这个问题问的.
进攻基团为正电荷就是亲电,为电子对或负电荷基团就是亲核.
你都说了是自己形成正离子,还用再说吗?别的基团进攻当然是容易亲核反应,异性相吸嘛;它自己进攻那就是亲电反应.1年前查看全部
- 碳正离子、碳负离子、碳自由基的电子排布是不是都是一样的?
碳正离子、碳负离子、碳自由基的电子排布是不是都是一样的?
都是1s22s22p2吗? weiyue8861年前2
weiyue8861年前2 -
 bingyun 共回答了17个问题
bingyun 共回答了17个问题 |采纳率76.5%不是.三者都是SP2杂化,不同的是剩余的一个P轨道中,碳正离子是空的,碳负离子有两个电子,自由基有一个电子.1年前查看全部
- 碳正离子稳定性判断第24题.主要是3,4分不清.
碳正离子稳定性判断
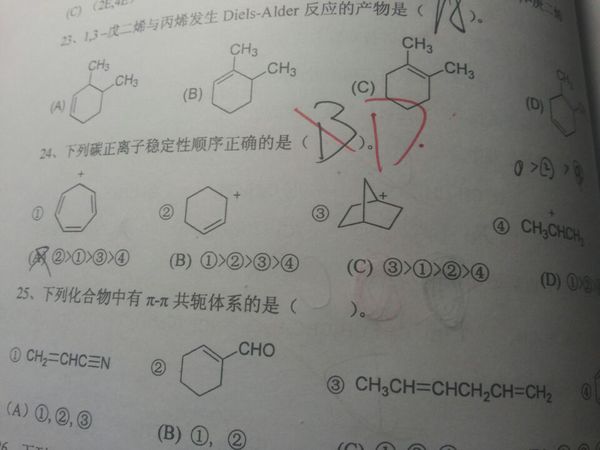 第24题.主要是3,4分不清.
第24题.主要是3,4分不清.  6273131年前1
6273131年前1 -
 风摧醉兰 共回答了22个问题
风摧醉兰 共回答了22个问题 |采纳率95.5%1最稳定,芳香性,2共振结构,3烷基供电子,4最不稳定,受环张力影响,桥碳正离子极不稳定1年前查看全部
- 为什么环戊基乙烯加HCl时碳正离子重排到2°碳上?旁边有3°碳呀?
为什么环戊基乙烯加HCl时碳正离子重排到2°碳上?旁边有3°碳呀?
产物为1-甲基-2-氯环戊烷,为什么不重排到3°碳?
产物中改为环己烷…… 淡墨生尘1年前6
淡墨生尘1年前6 -
 fy13393 共回答了19个问题
fy13393 共回答了19个问题 |采纳率84.2%这个碳正离子稳定性好像没能得到加强,暂时不知怎么解释...那位五元环108°的肯定是错误的,因为环戊烷的五个碳不在一个平面内,环己烷也是...1年前查看全部
- 烯烃不对称亲电加成的产物取决于电子云密度还是生成的碳正离子稳定性?比如说1-丁烯与H2O的加成产物是什么
 爱蕙1年前1
爱蕙1年前1 -
 乐涩夭夭 共回答了23个问题
乐涩夭夭 共回答了23个问题 |采纳率91.3%取决于碳正离子的稳定性.
1-丁烯加水生成2-丁醇.1年前查看全部
- 碳正离子的稳定性比较(3),请说明理由
 荞麦包108号1年前1
荞麦包108号1年前1 -
 抱不平啊 共回答了20个问题
抱不平啊 共回答了20个问题 |采纳率90%1.如果连接烷基、H等,由于碳正离子是Sp2杂化,有空的p轨道,会和烷基的C-Hsigma形成超共轭,进而分散碳正离子的电荷,使之稳定.所以,连接的烷基越多越稳定,即叔碳正离子>仲碳正离子>伯碳正离子>甲基.
2.如果连接的卤素,以Cl为例,cl的电负性大于c,有吸电子的诱导,同时是2s2 2px2 spy2 2pz,即有未成对电子,有碳正离子是Sp2 杂化,有空的p轨道,cl未成对的电子可以到空轨道上去,则可以分散正电荷,总的效果是使碳正离子更不稳定.
3如果是烯丙型和苄基型的碳正离子,由于p-pai共轭,可以分散电荷,是碳正离子更稳定1年前查看全部
- 为什么三级碳正离子会比二级、一级碳正离子稳定呢?
 rrr1234561年前3
rrr1234561年前3 -
 飘渺眼花 共回答了24个问题
飘渺眼花 共回答了24个问题 |采纳率91.7%碳正离子相连的烷基数不同,连有的烷基数目越多,相应的碳正离子越稳定,可见烷基能分散部分正电荷,它是推电子集团
与烷基相连的碳正离子为sp2杂化,它有一空的p轨道,烷基的C-H 西格马键与空的p轨道发生重叠,结果C-H键中的电子部分离域到空的p轨道中,分散了正电荷,稳定了碳正离子.这种电子离域现象称为共轭.有 西格马轨道参与的共轭成为超共轭.
叔丁基正离子有9个C-H键参与超共轭,因此最稳定,二极碳正离子有六个C-H键参与超共轭,稳定性次之,一级碳正离子只有三个C-H键参与,因此稳定性又低些
引自 有机化学1年前查看全部
- 碳正离子是什么?
 小强松1年前1
小强松1年前1 -
 幽人_yy 共回答了27个问题
幽人_yy 共回答了27个问题 |采纳率92.6%碳正离子是一种带正电的极不稳定的碳氢化合物.分析这种物质对发现能廉价制造几十种当代必需的化工产品是至关重要的.欧拉教授发现了利用超强酸使碳正离子保持稳定的方法,能够配制高浓度的碳正离子和仔细研究它.他的发现已用于提高炼油的效率、生产无铅汽油和研制新药物.1年前查看全部
- 碳正离子及在有机合成中的结构,产生,应用
 ff猪1年前1
ff猪1年前1 -
 泡沫红茶3287 共回答了29个问题
泡沫红茶3287 共回答了29个问题 |采纳率93.1%碳正离子是共价键的异裂或有机金属化合物的分解产生的,其结构是中心碳原子采取sp2杂化和三个基团相连,剩下一个空轨道.碳正离子的活性很高是重要的亲电试剂,应用例子有,格利亚试剂1年前查看全部
- 亲核顺序和碳正离子稳定性问题H2O OH- ARO- RCOO- RO- ROH亲核性强弱比较另外还有刑其毅基础有机化学
亲核顺序和碳正离子稳定性问题
H2O OH- ARO- RCOO- RO- ROH
亲核性强弱比较
另外还有刑其毅基础有机化学 P249 习题6-4 碳正离子稳定性比较
小弟先谢过各位前辈了
刑其毅基础有机化学 是第三版
另外我想问下为什么ArO->RCOO-
谢谢这位前辈了,还能讲下碳正离子的吗 后面都是桥头碳,怎么比较 nihaome8121年前2
nihaome8121年前2 -
 chyenqiwen 共回答了23个问题
chyenqiwen 共回答了23个问题 |采纳率91.3%大部分时候只要比较碱性,碱性强的亲核性强.只有一种情况,即同主族原子,和碱性顺序是相反的,比如亲核性I->Br->Cl-碱性Cl->Br->I-,亲核性HS->OH-碱性OH->HS-,这是周期大的变形性好所致.
在这里不存在那种特殊情况,所以只要管碱性.显然应该是RO->OH->ArO->RCOO->ROH>H2O.
那个碳正离子的,第一个是最稳定的,因为后面几个都是桥头碳形成的正离子,桥头碳的刚性结构不容易形成sp2杂化的120°键角所以不稳定.
因为羧酸酸性比苯酚强啊,显然羧酸根碱性比苯酚弱,亲核性一样.
都是桥头碳,就要看形成120°键角的能力谁强了,原来的键角接近109.5°,这个要靠想象...1年前查看全部
- 比较下列碳正离子稳定性
 奔驰5系列1年前2
奔驰5系列1年前2 -
 小-聊 共回答了19个问题
小-聊 共回答了19个问题 |采纳率89.5%应该是A要稳定些
原因如下:
首先环丙烯正离子是符合休克而规则(4n+2),可以判断出具有芳香性,而具有芳香性的物质就是那些高度不饱和但是化学性质稳定的物质所具有的性质,比如说苯.相比之下,丙烯正离子就不是那么稳定了.
直链碳正离子由于分子中广泛存在着σ与P的超共轭现象,若共轭键越多就越稳定,因此支链连在碳正离子上越多就越稳定.比如说叔碳正离子比仲碳正离子稳定.另外如果存在不饱和键,就可能出现P和π的超共轭现象,使的稳定性提高.
从这个角度上看,应该是环状要稳定点,因为环状结构他的超共轭体系可能会更多.1年前查看全部
- 下列碳正离子最稳定的是
 shaoquanhui1年前3
shaoquanhui1年前3 -
 依旧在从前 共回答了17个问题
依旧在从前 共回答了17个问题 |采纳率94.1%答案为B,因为碳正离子为sp2的平面结构,所以D中桥头结构,不容易形成平面碳正离子,B为烯丙基稳定结构,而A会发生重排,更不稳定.1年前查看全部
- 碳正离子稳定性+ +F-CH2CHCH2CH3 ,Cl-CH2CHCH2CH3 哪个碳正离子更稳定,为啥?
 在乎拥有1年前2
在乎拥有1年前2 -
 与我常在 共回答了20个问题
与我常在 共回答了20个问题 |采纳率80%后者更稳定,F电负性比Cl的强,拉电子效应更强,使电荷分散变弱,通常,给电子基团越多,给电子效应越强,碳正离子越稳定,F使亚甲基的给电子效应削弱的比CL大,所以更加不稳.1年前查看全部
- 碳正离子中,最稳定的是?
 dugujiujia1年前1
dugujiujia1年前1 -
 mzx_2013 共回答了14个问题
mzx_2013 共回答了14个问题 |采纳率100%看碳正离子的稳定性就是比较其碳正离子的正电荷分散程度.
如果碳正离子旁边有可以发生共轭的体系,那么其正电荷可以很有效的分散,如果连有甲基,就会有超共轭效应,使碳正离子更加稳定.
所以最稳定的是B.
希望对你有所帮助!1年前查看全部
- 碳正离子是否属于路易斯酸?
 caojianbin1年前1
caojianbin1年前1 -
 DONGHUANGJIE 共回答了13个问题
DONGHUANGJIE 共回答了13个问题 |采纳率84.6%在有机化学中,能吸收电子云的分子或原子团称为路易斯酸,碳正离子可以,则应是1年前查看全部
- 碳正离子是路易斯酸吗
 leegeo1年前1
leegeo1年前1 -
 donny999 共回答了28个问题
donny999 共回答了28个问题 |采纳率78.6%路易斯酸是有空轨道的物质,C+有一个空轨道所以是路易斯酸.1年前查看全部
- 苄基型碳正离子稳定还是乙烯基型碳正离子稳定,理由是什么?
 ipveo4411年前2
ipveo4411年前2 -
 ls03lwei 共回答了18个问题
ls03lwei 共回答了18个问题 |采纳率88.9%苄基型碳正离子稳定
电子离域范围更大1年前查看全部
- 苯甲基碳正离子和乙基碳正离子的稳定性比较
 二过头1年前2
二过头1年前2 -
 asd7890 共回答了16个问题
asd7890 共回答了16个问题 |采纳率81.3%后者.你应该知道苯基是吸电子基团 所以会导致碳正离子的极化现象更严重 而相反乙基是推离子基团 所以会减弱碳正离子的极化现象更稳定.1年前查看全部
- 怎样判断碳正离子的稳定性
 shang0010020031年前2
shang0010020031年前2 -
 iamwayne 共回答了26个问题
iamwayne 共回答了26个问题 |采纳率88.5%伯,仲,叔,季的问题
伯>仲>叔>季
伯C就是和三个H相连的C
仲C就是和两个H相连的C
叔C就是只和一个H相连的C
季C就是C上一个H都不连1年前查看全部
- 碳正离子的稳定性怎么判断啊
 user60001年前1
user60001年前1 -
 亚热带的忧伤 共回答了17个问题
亚热带的忧伤 共回答了17个问题 |采纳率88.2%1.如果连接烷基、H等,由于碳正离子是Sp2杂化,有空的p轨道,会和烷基的C-Hsigma形成超共轭,进而分散碳正离子的电荷,使之稳定.所以,连接的烷基越多越稳定,即叔碳正离子>仲碳正离子>伯碳正离子>甲基.2.如果连接的卤素,以Cl为例,cl的电负性大于c,有吸电子的诱导,同时是2s2 2px2 spy2 2pz,即有未成对电子,有碳正离子是Sp2 杂化,有空的p轨道,cl未成对的电子可以到空轨道上去,则可以分散正电荷,总的效果是使碳正离子更不稳定.3如果是烯丙型和苄基型的碳正离子,由于p-pai共轭,可以分散电荷,是碳正离子更稳定1年前查看全部
- 怎么判断有机反应中是否产生碳正离子?即怎样判断一个反应是SN1还是SN2类型.
 龙飞猪舞1年前1
龙飞猪舞1年前1 -
 sd1219582 共回答了18个问题
sd1219582 共回答了18个问题 |采纳率72.2%这个不好判断,一般三级卤代烃亲核取代反应中有碳正离子,但多数情况,卤代烃的亲核取代反应不会完全进行某一类型反应只会以某一类型反应为主.
建议参考邢其毅有机化学第六章的相关内容1年前查看全部
- 碳正离子有三个sp2杂化轨道与其他原子形成西格马键,还有一个空的p轨道,这样我们可不可以认为碳原子有
碳正离子有三个sp2杂化轨道与其他原子形成西格马键,还有一个空的p轨道,这样我们可不可以认为碳原子有
4个p轨道呢? 3928108791年前1
3928108791年前1 -
 dd也蛛蛛 共回答了18个问题
dd也蛛蛛 共回答了18个问题 |采纳率94.4%不可以,因为那三个sp2杂化轨道不是p轨道1年前查看全部
- 小弟问一下关于 碳正离子 有机化学中碳正离子是什么?他是怎么形成的?
 rommelyanan1年前4
rommelyanan1年前4 -
 气球鸟 共回答了17个问题
气球鸟 共回答了17个问题 |采纳率94.1%碳正离子是一种带正电的极不稳定的碳氢化合物.分析这种物质对发现能廉价制造几十种当代必需的化工产品是至关重要的.欧拉教授发现了利用超强酸使碳正离子保持稳定的方法,能够配制高浓度的碳正离子和仔细研究它.他的发现已用于提高炼油的效率、生产无铅汽油和研制新药物.
碳正离子与自由基一样,是一个活波的中间体.碳正离子有一个正电荷,最外层有6个电子.带正电荷的碳原子以SP2杂化轨道与3个原子(或原子团)结合,形成3个σ键,与碳原子处于同一个平面.碳原子剩余的P轨道与这个平面垂直.碳正离子是平面结构.
1963年有报道,直接观察到简单的碳正离子,证明了它的平面结构,为它的存在及其结构提供了实验依据.
根据带正电荷的碳原子的位置,可分为一级碳正离子,二级碳正离子和三级碳正离子.
碳正离子的结构与稳定性直接受到与之相连接的基团的影响.它们稳定性的一般规律如下:
(1)苄基型或烯丙型一般较稳定;
(2)其它碳正离子是:3°>2°>1°;
碳正离子越稳定,能量越低,形成越容易,加成速度也越快,可见碳正离子的稳定性决定烯烃加成的取向.1年前查看全部
- 卤代烃消去时是否有可能产生重排产物?到处都看不到确切结论但是如果是E1的话,碳正离子应该有可能重排吧
 烟笛1年前1
烟笛1年前1 -
 swm_f_d4dh_v6e58 共回答了20个问题
swm_f_d4dh_v6e58 共回答了20个问题 |采纳率100%当然可能重排啦,在做题中,如果判定为E1一定要考虑重排1年前查看全部
- 碳正离子稳定性判断
 中康保健1年前1
中康保健1年前1 -
 uu209 共回答了18个问题
uu209 共回答了18个问题 |采纳率77.8%电子云密度增加后就会使苯环与碳正离子产生p-π共轭,从而稳定性明显高于ccl3(氯的电负性高于碳,因此电子云密度明显偏向于氯,使苯环上的电子云密度降低1年前查看全部
- 对甲基苯甲基碳正离子,对硝基苯甲基碳正离子,对甲氧基苯甲基碳正离子,苯甲基碳正离子稳定性比较,
 超值等你拿1年前1
超值等你拿1年前1 -
 kyle_chen 共回答了11个问题
kyle_chen 共回答了11个问题 |采纳率100%如下,稳定性一次下降
对甲氧基苯甲基碳正离子,对甲基苯甲基碳正离子,苯甲基碳正离子,对硝基苯甲基碳正离子
原因如下
碳离子的稳定性可以根据正电荷的分散程度来判断,也就是说,正离子越分散,正电荷越稳定.苯环提供的电子越多,正离子越稳定.苯环上电子越多,才能提供的电子越多.苯环取代基给的电子越多,苯环上电子才会越多,吸电子越多,苯环上电子越少.甲氧基给电子能力大于甲基,而硝基是吸电子基团,所以稳定性如上1年前查看全部
- 什么是路易斯酸?碳正离子是否属于路易斯酸?
 逃离爱的束缚1年前1
逃离爱的束缚1年前1 -
 hdch 共回答了18个问题
hdch 共回答了18个问题 |采纳率88.9%路易斯酸指亲电试剂或电子受体,碳正离子有亲电性,所以是路易斯酸1年前查看全部
- 在亲核加成、取代反应和亲电加成、取代反应中,什么反应生成碳负离子,什么反应生成碳正离子?说说机理
 许-风-雨1年前1
许-风-雨1年前1 -
 jovial237 共回答了15个问题
jovial237 共回答了15个问题 |采纳率100%亲电加成,亲核加成就是根据生成的中间体才得名的.
亲电加成反应中形成的中间体是碳正离子,由于碳正离子带正电荷,能够吸引带负电的电子或带负电的试剂.因此才命名为亲电(电子)加成.
亲核加成反应中形成的中间体是碳负离子,碳负离子带负电荷,能够吸引裸露的原子核(带正电)以及带正电的试剂.它的命名就是亲核(原子核)加成.
至于取代反应,一般都是共价键均裂生成自由基中间体;在加成反应里也有一类是自由基加成反应,中间体也是自由基.
希望能够帮助到你~
如有疑惑,欢迎追问1年前查看全部
大家在问
- 1一个正方形里面加两条对角线怎么一笔画成
- 2卤素灯与白炽灯,节能灯和LED灯的区别
- 3in the sunday 和 on sundays都不是都指每个星期太天?意思一样否?
- 4今年小林的爷爷,爸爸和小林本人的年龄和为110岁.
- 5十分悬赏 !文章运用拟人的修辞手法,细腻地表达了作者真挚的情感,品味下列句子妙处
- 6(2007•湘潭)读等高线地形图,回答12~13题.
- 7请英语牛人帮我翻译这句话要通顺,不要借助翻译工具
- 8一次函数综合习题已知直线l1:y=-x+11,将直线l1向下平移3个单位长度,得到直线l2,设直线l2与y轴相交于点A,
- 9过点A(1,0)的直线L与中心在原点, 过点Q(1,0)的直线l与中心在原点,焦点在x轴上且离心率为根号2/2的椭圆
- 10鉴于情况紧急,甲(O型)曾为乙(A型)输过两次血,第一次输血未发生凝集反应,而第小次输血却发生了凝集反应,则第小次输血发
- 11If you think the price of pork is too high, you _____ as wel
- 12我喜欢上了你,可是你却喜欢上了别人,我还怎么办 翻译成英语
- 13(2012•广陵区二模)“钾泻盐”的化学式为MgSO4•KCl•xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与
- 14初中生活 作文
- 15介词+which/whom引导定语从句中介词怎么选啊
