氩元素的原子序数为什么是18..
 kikifeng2022-10-04 11:39:543条回答
kikifeng2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 dengqingpeng 共回答了18个问题
dengqingpeng 共回答了18个问题 |采纳率100%- 元素的核外电子是根据构造原理填入各级轨道的,1s 2s 2p 3s 3p 4s 3d……
s层只能容纳2个自旋方向相反的电子,p层能容纳6个电子(三个简并轨道,每个容纳2个自旋方向相反的电子),所以排到Ar时排了18个电子,K、L能级排满,3s、3p也是满的,符合稳定构型;又因为质子数等于电子数,所以原子序数是18 - 1年前
 72645jun 共回答了1个问题
72645jun 共回答了1个问题 |采纳率- 你要问门捷列夫
- 1年前
 okeva 共回答了290个问题
okeva 共回答了290个问题 |采纳率- 原子序数就是根据元素的质子数排列的,氩的质子数为18,原子序数也就是18了
- 1年前
相关推荐
- (2010•泉州)下表是元素周期表中第三周期的部分元素(氩元素除外),在化学反应中,从左到右原子失电子能力逐渐减弱,得电
(2010•泉州)下表是元素周期表中第三周期的部分元素(氩元素除外),在化学反应中,从左到右原子失电子能力逐渐减弱,得电子能力逐渐增强.
根据上表得出以下结论,其中不正确的是( )11 Na
钠
22.9912 Mg
镁
24.3113 Al
铝
26.9814 Si
硅
28.0915 P
磷
30.9716 S
硫
32.0717 Cl
氯
35.45
A.失电子能力:Na>Al
B.得电子能力:S<Cl
C.磷的相对原子质量是30.97
D.镁和硅两种元素属于非金属元素 jonly7771年前1
jonly7771年前1 -
 担杆岛 共回答了17个问题
担杆岛 共回答了17个问题 |采纳率94.1%解题思路:根据在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类和性质,也发生规律性的变化,解答本题.A、在电子层数相等的条件下,质子数越少,失电子能力越强,所以失电子能力:Na>Al,故A正确;
B、在电子层数相等的条件下,质子数越多,得电子能力越强,所以得电子能力:S<Cl,故B正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C正确;
D、根据图示信息可以知道,镁为金属元素,硅为非金属元素,故D错误.
故选D.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 了解元素周期表的特点及其应用;了解原子结构示意图与离子结构示意图的特点.1年前查看全部
- 由硫元素的原子和氩元素的原子组成的化合物的化学式是什么?
 jiaotu1年前1
jiaotu1年前1 -
 缇儿 共回答了22个问题
缇儿 共回答了22个问题 |采纳率90.9%它们不能形成化合物.
氩是稀有气体元素,没有化合态,即没有化合物1年前查看全部
- 下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强.
下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强.下列说法不正确的是( ) 11 Na
钠
22.9912 Mg
镁
24.3113 Al
铝
26.9814 Si
硅
28.0915 P
磷
30.9716 S
硫
32.0717 Cl
氯
35.45
11 Na
钠
22.99
12 Mg
镁
24.31
13 Al
铝
26.98
14 Si
硅
28.09
15 P
磷
30.97
16 S
硫
32.07
17 Cl
氯
35.45
A.硫元素原子的核外电子数为16
B.得电子能力:S<Cl
C.磷的相对原子质量是30.97
D.钠原子结构示意图为
 瓦那人1年前1
瓦那人1年前1 -
 rhpwdbnbg 共回答了19个问题
rhpwdbnbg 共回答了19个问题 |采纳率94.7%A、硫元素的原子序数为16,核外电子数和原子序数相等,故A说法正确;
B、在电子层数相等的条件下,质子数越多,得电子能力越强,故B说法正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C说法正确;
D、钠原子的最外层电子数应该为1个电子,故D说法不正确.
故选D.1年前查看全部
- 下列元素是周期表中的第三周期元素(氩元素除外),在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强。
下列元素是周期表中的第三周期元素(氩元素除外),在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强。下列说法不正确的是

A.硫元素原子的核外电子数为16 B.得电子能力:S < Cl C.磷的相对原子质量是30.97 D.钠元素的原子结构示意图为: 
 荒漠一孤烟1年前1
荒漠一孤烟1年前1 -
 洽洽口味 共回答了18个问题
洽洽口味 共回答了18个问题 |采纳率88.9%D
A、硫元素的原子序数为16,核外电子数和原子序数相等,故A说法正确;
B、在电子层数相等的条件下,质子数越多,得电子能力越强,故B说法正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C说法正确;
D、钠原子的最外层电子数应该为1个电子,故D说法不正确.
故选D.1年前查看全部
- 化学式cl氯元素的意义还有氩元素Ar的意义五氧化二磷P2O5的意义钡元素Ba2+的意义会哪个答哪个
 unicornliu1年前5
unicornliu1年前5 -
 JamesNorlan 共回答了15个问题
JamesNorlan 共回答了15个问题 |采纳率80%Ar:氩气、1个氩原子、氩元素
Ba2+:带2个单位正电荷的钡离子1年前查看全部
- 一道化学题目关于元素的12.有三种短周期元素,最外层电子数之和为17,质子数之和为31.如果这三种元素中有一种是氩元素,
一道化学题目关于元素的
12.有三种短周期元素,最外层电子数之和为17,质子数之和为31.如果这三种元素中有一种是氩元素,则关于另外两种元素的说法不正确的是
A.如果一种元素是金属元素,则另一种元素一定是稀有元素
B.如果一种元素的单质通常情况下是气体,则另一种元素的单质通常情况下是固体
C.如果一种元素的气态氢化物是三角锥形分子,则另一种元素的气态氢化物一定是"V"型分子
D.如果一种元素的最高正价是+3,则另一种元素的单质有两种常见的同素异形体 zhang034671年前3
zhang034671年前3 -
 bvbb 共回答了17个问题
bvbb 共回答了17个问题 |采纳率100%氩最外电子8 质子18
余下最外电子和9 质子13
满足这个组合的有碳 氮
硼 氧
铍 氟
Li Ne
带进去对照,a不对,铍 氟
b对,四组都是
c不对三角锥形分子是NH3 CH4是正四面体
d对 硼 氧 氧有O3 O21年前查看全部
- 按要求完成各题(1)用元素符号或化学式填空:①氩元素______;②4个二氧化硫分子______;③氮气______;&
按要求完成各题
(1)用元素符号或化学式填空:
①氩元素______;②4个二氧化硫分子______;③氮气______; ④氨气______;
(2)标出下列划线元素的化合价:
2 H2O • S •
2O H2K •
O4S •
(3)指出下列符号中“2”的含义:
①2O______; ②O2-______;③O2______; ④2CH4______. 未激活7241年前1
未激活7241年前1 -
 小虫_sgq 共回答了18个问题
小虫_sgq 共回答了18个问题 |采纳率88.9%解题思路:(1)①根据元素符号的书写方法进行解答;
②根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,进行解答;
③氮气由双原子分子构成;
④正确书写氨气的化学式即可;
(2)根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,进行解答;
(3)根据标在元素符号前面的数字表示原子的个数;标在元素符号右上角的数字表示离子所带电荷数;标在元素符号右下角的数字表示一个分子中所含原子的个数;标在化学式前面的数字表示分子的个数;进行解答.(1)①根据元素符号的书写方法,氩元素符号为:Ar;故答案为:Ar;
②根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此4个二氧化硫分子表示为:4SO2;故答案为:4SO2;
③氮气由双原子分子构成;氮气的 化学式为:N2 ;故答案为:N2 ;
④氨气的化学式为:NH3 ;故答案为:NH3;
(2)根据元素化合价的表示方法,单质中元素的化合价为0,
0
O2,H2
−2
S;
+1
K2O; H2
+6
SO4;
故答案为:,
0
O2,H2
−2
S;
+1
K2O; H2
+6
SO4;
(3)根据标在元素符号前面的数字表示原子的个数;2O中“2”的含义表示:2个氧原子;故答案为:2个氧原子;
标在元素符号右上角的数字表示离子所带电荷数;因此O2-中“2”的含义:一个氧离子带2个单位的负核电荷;
故答案为:一个氧离子带2个单位的负核电荷;
标在元素符号右下角的数字表示一个分子中所含原子的个数;因此中“2”的含义为:一个氧分子中含有2个氧原子;故答案为:一个氧分子中含有2个氧原子;
标在化学式前面的数字表示分子的个数;因此2CH4 中“2”的含义:2个甲烷分子;故答案为:2个甲烷分子.点评:
本题考点: 化学符号及其周围数字的意义;化学式的书写及意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.1年前查看全部
- (2011•玄武区一模)下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减
(2011•玄武区一模)下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强.下列说法不正确的是( )
11 Na
钠
22.9912 Mg
镁
24.3113 Al
铝
26.9814 Si
硅
28.0915 P
磷
30.9716 S
硫
32.0717 Cl
氯
35.45
A.硫元素原子的核外电子数为16
B.得电子能力:S<Cl
C.磷的相对原子质量是30.97
D.钠原子结构示意图为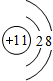
 whitebird_zz1年前1
whitebird_zz1年前1 -
 比目鱼9172 共回答了17个问题
比目鱼9172 共回答了17个问题 |采纳率94.1%解题思路:根据在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类和性质,也发生规律性的变化,解答本题.A、硫元素的原子序数为16,核外电子数和原子序数相等,故A说法正确;
B、在电子层数相等的条件下,质子数越多,得电子能力越强,故B说法正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C说法正确;
D、钠原子的最外层电子数应该为1个电子,故D说法不正确.
故选D.点评:
本题考点: 元素周期表的特点及其应用;原子的定义与构成;原子结构示意图与离子结构示意图;原子的有关数量计算.
考点点评: 了解元素周期表的特点及其应用;了解原子结构示意图与离子结构示意图的特点.1年前查看全部
- (1)用元素符号或化学式填空①氩元素______; ②4个氢分子______; ③7个银离子____
(1)用元素符号或化学式填空
①氩元素______; ②4个氢分子______; ③7个银离子______;
④3个硫酸根离子______; ⑤氯化亚铁______;⑥碳酸钡______;
(2)写出下列符号中2表示的意义
①2Al3+:______;②Mg2+:______;
③Cu2+:______;④H2O:______. huairen231年前1
huairen231年前1 -
 yan2 共回答了18个问题
yan2 共回答了18个问题 |采纳率88.9%解题思路:(1)本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
(2)离子符号前加数字表示离子个数,右上角数字表示离子所带的电荷数,右下角数字表示分子中原子个数.(1)①元素用元素符号表示,只有一个字母组成的元素符号要大写,由两个字母组成的元素符号第一个要大写,第二个要小写,故氩元素可表示为:Ar;
②分子的表示方法:正确书写物质的化学式,若表示多个该分子,就在其化学式前加上相应的数字,所以4个氢分子可表示为:4H2;
③表示粒子个数的数字写在符号前面;写离子符号时要在元素符号或原子团的右上角标上离子所带电荷数,是“1”时省略,且数值在前,正、负号在后;1个银离子含有1个银原子且带有1个单位的正电荷.因此7个银离子表示为7Ag+.
④离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.表示多个离子在离子符号前面加数字,故3个硫酸根离子符号为3SO42-;
⑤氯化亚铁是由显+2价的铁元素和显-1价的氯元素组成的,根据化合价原则,氯化亚铁可表示为:FeCl2;
⑥碳酸钡是由显+2价钡元素和-2价的碳酸根组成,根据化合价原则,其化学式可表示为:BaCO3;
(2)①离子符号前加数字表示离子个数,故2Al3+中的2表示2个铝离子;
②右上角数字表示离子所带的电荷数,故Mg2+中的2表示镁离子带2个单位的正电荷;
③右上角数字表示离子所带的电荷数,故Cu2+中的2表示铜离子带2个单位的正电荷;
④右下角数字表示分子中原子个数,故H2O中的2表示一个水分子中含有2个氢原子;
故答案为:(1)①Ar;②4H2;③7Ag+;④3SO42-;⑤FeCl2;⑥BaCO3;(2)①2个铝离子;②镁离子带2个单位的正电荷;③铜离子带2个单位的正电荷;④一个水分子中含有2个氢原子;点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.1年前查看全部
- (2011•玄武区一模)下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减
(2011•玄武区一模)下图是元素周期表中的第三周期元素(氩元素除外).在化学反应中,从左到右各元素原子失电子能力逐渐减弱,得电子能力逐渐增强.下列说法不正确的是( )
A.硫元素原子的核外电子数为16
B.得电子能力:S<Cl
C.磷的相对原子质量是30.97
D.钠原子结构示意图为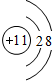
 ppp_1111年前1
ppp_1111年前1 -
 13926755669 共回答了14个问题
13926755669 共回答了14个问题 |采纳率92.9%A、硫元素的原子序数为16,核外电子数和原子序数相等,故A说法正确;
B、在电子层数相等的条件下,质子数越多,得电子能力越强,故B说法正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C说法正确;
D、钠原子的最外层电子数应该为1个电子,故D说法不正确.
故选D.1年前查看全部
- 按要求完成各题(1)用元素符号或化学式填空:①氩元素______;②4个二氧化硫分子______;③氮气______;&
按要求完成各题
(1)用元素符号或化学式填空:
①氩元素______;②4个二氧化硫分子______;③氮气______; ④氨气______;
(2)标出下列划线元素的化合价:
2 H 2O • S •
2 O H 2K •
O 4S •
(3)指出下列符号中“2”的含义:
①2O______; ②O 2- ______;③O 2 ______; ④2CH 4 ______. 乔珂藜1年前1
乔珂藜1年前1 -
 壁赏观 共回答了22个问题
壁赏观 共回答了22个问题 |采纳率90.9%(1)①根据元素符号的书写方法,氩元素符号为:Ar;故答案为:Ar;
②根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此4个二氧化硫分子表示为:4SO 2 ;故答案为:4SO 2 ;
③氮气由双原子分子构成;氮气的 化学式为:N 2 ;故答案为:N 2 ;
④氨气的化学式为:NH 3 ;故答案为:NH 3 ;
(2)根据元素化合价的表示方法,单质中元素的化合价为0,
0
O 2 ,H 2
-2
S ;
+1
K 2 O; H 2
+6
S O 4 ;
故答案为:,
0
O 2 ,H 2
-2
S ;
+1
K 2 O; H 2
+6
S O 4 ;
(3)根据标在元素符号前面的数字表示原子的个数;2O中“2”的含义表示:2个氧原子;故答案为:2个氧原子;
标在元素符号右上角的数字表示离子所带电荷数;因此O 2- 中“2”的含义:一个氧离子带2个单位的负核电荷;
故答案为:一个氧离子带2个单位的负核电荷;
标在元素符号右下角的数字表示一个分子中所含原子的个数;因此中“2”的含义为:一个氧分子中含有2个氧原子;故答案为:一个氧分子中含有2个氧原子;
标在化学式前面的数字表示分子的个数;因此2CH 4 中“2”的含义:2个甲烷分子;故答案为:2个甲烷分子.1年前查看全部
- (2013•大连)如图是氩元素在元素周期表中的有关信息,下列说法错误的是( )
 (2013•大连)如图是氩元素在元素周期表中的有关信息,下列说法错误的是( )
(2013•大连)如图是氩元素在元素周期表中的有关信息,下列说法错误的是( )
A.元素符号是Ar
B.属于金属元素
C.原子核外有18个电子
D.相对原子质量是39.95 樱花飘浪1年前1
樱花飘浪1年前1 -
 曾经此岸迷离 共回答了27个问题
曾经此岸迷离 共回答了27个问题 |采纳率88.9%解题思路:根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.A、根据元素周期表中的一格中获取的信息,氩元素的元素符号是Ar,故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的名称是氩,属于非金属元素,故选项说法错误.
C、根据元素周期表中的一格中获取的信息,氩元素的原子序数为18,根据原子序数=核外电子数,则氩元素的原子核外有18个电子,故选项说法正确.
D、根据元素周期表中的一格中获取的信息,可知该元素的相对原子质量为39.95,故选项说法正确.
故选B.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.1年前查看全部
- 下列元素是周期表中的第三周期元素(氩元素除外),下列说法不正确的是( )
下列元素是周期表中的第三周期元素(氩元素除外),下列说法不正确的是( )
11 Na
钠
22.9912 Mg
镁
24.3113 Al
铝
26.9814 Si
硅
28.0915 P
磷
30.9716 S
硫
32.0717 Cl
氯
35.45
A.硫元素原子的核外电子数为16
B.硅元素属于非金属元素
C.磷的相对原子质量是30.97
D.钠元素的原子结构示意图为:
 海棠溪照1年前1
海棠溪照1年前1 -
 csuyhl 共回答了20个问题
csuyhl 共回答了20个问题 |采纳率90%解题思路:根据在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类和性质,也发生规律性的变化,解答本题.A、硫元素的原子序数为16,核外电子数和原子序数相等,故A说法正确;
B、由硅元素的名称可知硅元素属于非金属元素,故B说法正确;
C、根据图示信息可以知道磷元素的相对原子质量为30.97,故C说法正确;
D、钠原子的最外层电子数应该为1个电子,故D说法不正确.
故选D.点评:
本题考点: 元素周期表的特点及其应用;原子结构示意图与离子结构示意图.
考点点评: 了解元素周期表的特点及其应用;了解原子结构示意 图与离子结构示意图的特点.1年前查看全部
- 在自然界中,为什么氩元素总是以单质形式存在?
 tqtivit1年前3
tqtivit1年前3 -
 huijuan_2006 共回答了26个问题
huijuan_2006 共回答了26个问题 |采纳率88.5%因为氩元素十分稳定,几乎不和任何物质反应.1年前查看全部
- 用元素符号或化学式填空:①氩元素______②4个二氧化硫分子______③氮气______④3个硫酸根离子______
用元素符号或化学式填空:①氩元素______②4个二氧化硫分子______③氮气______④3个硫酸根离子______ ⑤碳酸钡______⑥氖气______ ⑦三个亚铁离子______ ⑧氧化镁中镁元素的化合价为+2价
O+2 Mg .
O+2 Mg  allenshaw1年前1
allenshaw1年前1 -
 迷途叶子 共回答了20个问题
迷途叶子 共回答了20个问题 |采纳率100%解题思路:①根据元素符号的书写方法进行书写即可.
②根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,进行书写.
③根据单质化学式的书写方法进行书写即可.
④根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行书写.
⑤据化合物化学式的书写进行书写即可.
⑥根据单质化学式的书写方法进行书写即可.
⑦根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行书写.
⑧据化合价的书写原子书写即可.①钙元素的元素符号为:Ar.
②由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则4个二氧化硫分子可表示为:4SO2.
③氮气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:N2.
④由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个硫酸根离子可表示为:3SO42-.
⑤钡元素显+2价,碳酸根的化合价为-2价,十字交叉后表示为:BaCO3
⑥由原子直接构成的物质用元素符号表示,故氖气可表示为Ne
⑦由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个亚铁离子可表示为:3Fe2+.
⑧镁元素为+2价,氧元素为-2价,化合价十字交叉后2被约掉,所以氧化镁的化学式为MgO,然后再在镁元素的正上方标出其化合价即可.
故答案为:①Ar;②4SO2;③N2;④3SO42-.⑤BaCO3.⑥Ne.⑦3Fe2+.⑧
+2
MgO点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(元素符号、分子符号、化学式、离子符号等)的书写和理解能力.1年前查看全部
- 氩元素,氮气,硫酸钡元素符号或者化学式
 pengdegen1年前3
pengdegen1年前3 -
 忧郁的热带1 共回答了15个问题
忧郁的热带1 共回答了15个问题 |采纳率100%氩元素 Ar,
氮气 N2,
硫酸钡 BaSO41年前查看全部
- 用元素符号或化学式填空:①氩元素______;
用元素符号或化学式填空:
①氩元素______;
②4个二氧化硫分子______;
③氮气______;
④7个银原子______;
⑤3个硫酸根离子______;
⑥碳酸镁______;
⑦氧化铝中铝元素的化合价
2O3+3 Al .
2O3+3 Al  clsb1年前1
clsb1年前1 -
 zlg19811209 共回答了17个问题
zlg19811209 共回答了17个问题 |采纳率82.4%解题思路:书写元素符号时,第一个字母要大写,第二个字母要小写;化学符号周围的数字表示不同的意义:符号前面的数字,表示原子或分子个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价.一个二氧化硫分子是由一个硫原子和两个氧原子构成的,一个氮气分子是由两个氮原子构成的;一个硫酸根离子带两个单位的负电荷,碳酸镁中镁元素的化合价是+2价,碳酸根的化合价是-2价;氧化铝中铝元素的化合价是+3价.书写元素符号时,第一个字母要大写,第二个字母要小写;符号前面的数字,表示原子、离子或分子个数;一个二氧化硫分子是由一个硫原子和两个氧原子构成的,一个氮气分子是由两个氮原子构成的;一个硫酸根离子带两个单位的负电荷,碳酸镁中镁元素的化合价是+2价,碳酸根的化合价是-2价;氧化铝中铝元素的化合价是+3价;故答案为:①Ar ②4SO2③N2 ④7Ag ⑤3SO42- ⑥MgCO3⑦
+3
Al2O3点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本考点考查了化学式和离子符号的书写,化学式书写的一般规律是:正前负后,然后利用十字交叉法;元素符号、化学式、化学方程式等化学用语的书写是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.1年前查看全部
- 用化学符号填空:(1)钠元素______;钙元素______;镁元素______;氩元素______;高锰酸钾_____
用化学符号填空:
(1)钠元素______;钙元素______;镁元素______;氩元素______;高锰酸钾______;氯酸钾______.
(2)人的呼吸作用主要是消耗空气中的______;雨雪等自然现象证明空气中有______;石灰水露置在空气中一段时间,表面会形成一层白色薄膜,是因为空气中含有______;以空气为原料可以生产尿素(一种氮肥),说明空气中有______. 张臻1年前1
张臻1年前1 -
 chenne 共回答了22个问题
chenne 共回答了22个问题 |采纳率77.3%解题思路:(1)根据元素符号和化学式书写的注意事项考虑;
(2)根据空气中各成分的用途和性质来回答本题.(1)元素符号的写法是遵循一大二小的原则,化学式书写要根据正价在前,负价在后,先约简再交叉,检验时根据正负化合价代数和为零来检查;
(2)人的呼吸作用主要是吸入氧气呼出二氧化碳,所以主要是消耗空气中氧气;雨雪是水的固态,所以雨雪等自然现象证明空气中有水蒸气;由于二氧化碳能使澄清石灰水变浑浊,所以石灰水露置在空气中一段时间,表面会形成一层白色薄膜,是因为空气中含有二氧化碳;由于尿素是一种氮肥,空气中的成分中只有氮气含有氮元素,所以说明空气中含有氮气.
故答案为:
(1)Na;Ca;Mg;Ar;KMnO4 ;KClO3;
(2)O2;H2O;CO2;N2.点评:
本题考点: 化学符号及其周围数字的意义;空气的成分及各成分的体积分数.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,又考查了空气中各成分及其性质,考查全面,注重基础,题目难度较易.1年前查看全部
- 用数字和化学符号填空:①氩元素______②4个二氧化硫分子______③3个硫酸根离子______④氯酸钾中氯元素的化
用数字和化学符号填空:
①氩元素______②4个二氧化硫分子______③3个硫酸根离子______④氯酸钾中氯元素的化合价为+5价K
O3+5 Cl K.
O3+5 Cl  三哥哥1年前1
三哥哥1年前1 -
 zhzhjnjn000 共回答了21个问题
zhzhjnjn000 共回答了21个问题 |采纳率81%解题思路:书写元素符号时,第一个字母要大写,第二个字母要小写;化学式书写的一般规律是:正前负后,然后利用十字交叉法.化学符号周围的数字表示不同的意义:符号前面的数字,表示原子、离子或分子个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价.设氯酸钾中氯元素的化合价为x,+1+x+(-2)×3=0,x=+5.(1)书写元素符号时,第一个字母要大写,第二个字母要小写,故答案为:Ar
(2)符号前面的数字,表示分子个数,一个二氧化硫分子是由一个硫原子和两个氧原子构成的,故答案为:4SO2
(3)符号前面的数字,表示离子个数,一个硫酸根离子带两个单位的负电荷,故答案为:3SO42-
(4)设氯酸钾中氯元素的化合价为x,+1+x+(-2)×3=0,x=+5,故答案为:K
+5
ClO3点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本考点考查了化学式和离子符号的书写,同时考查了有关化合价的计算,元素符号、化学式、化学方程式等化学用语的书写是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.1年前查看全部
- 由氢,氮,氧,氩元素组成的化合物的化学式
 kld19861年前1
kld19861年前1 -
 甲状腺功能减退症 共回答了17个问题
甲状腺功能减退症 共回答了17个问题 |采纳率82.4%H2O NO2 N2O5 HNO31年前查看全部
- 氩元素能构成分子还是原子
 luzhifei10161年前1
luzhifei10161年前1 -
 1984ZZ 共回答了12个问题
1984ZZ 共回答了12个问题 |采纳率91.7%当然是分子!1年前查看全部
- 氟,氖,氯和氩元素有什么共同特点
氟,氖,氯和氩元素有什么共同特点
镍、铜、钯、银元素有什么共同特点
碳、氮、氧元素有什么共同特点 拨通1年前1
拨通1年前1 -
 良渚玉琮 共回答了22个问题
良渚玉琮 共回答了22个问题 |采纳率90.9%氟,氖,氯和氩元素:单质在常温下都是气态.
镍、铜、钯、银元素都是金属元素.
碳、氮、氧元素:都属于非金属元素.1年前查看全部
大家在问
- 1扩句:同学们讨论问题
- 2夏天的诗在报刊杂志或课外书里描写夏天的好诗
- 3摘栗子的英文和过去式写作文要用!十万火急!
- 4高一重力势能一物体重60kg从高为H的地方自由下落以水面为零势能面水面以上高度为H 水面下的高度为h (g取10)求1:
- 5英语翻译1,他从过去的经验得知,她不会轻易放弃的.2 要想让他们彻底了解当地文化是不可能的.3,在那时,每天下班他会去拐
- 6六(3)班共有56名同学去江海风情园,共乘坐10只船,其中大船坐6人,小船坐4人,大船、小船各有多少只?(用假设的策略)
- 7一个平行四边形,如果高增加5Ccm,底不变,面积就增加45c㎡;如果高不变,底减少5cm,面积就减少30c㎡.原来平行四
- 8把一个重10n,体积为1.2立方分米的物体浸没在水中,该物体静止后所受的浮力是
- 9我自学的 搞不清楚
- 10今年考上所高中,想预习数学,可自学几天都稀里糊涂,题目大多数也不会怎么办
- 11复分解反应反应物条件是:当反应物为盐盐或盐碱时反应物必须溶于水.那为什么酸发生复分解反应时不需要溶于水?
- 12wide high tall huge immense geat 的区别.
- 13英语翻译1.许多人都被这次灾难震惊.(number,shock) 2.看上去他们之间的一切都结束(seem,as if)
- 14On turning on the computer,_______
- 15语文学科提分今年升初三,我语文大概90多分,基础满分25我平均每次15分,阅读记叙文答的一般,说明文扣2分,作文每次都4
