车用乙醇汽油是把变性燃料乙醇和汽油按一定比例混配形成的.经多项检测表明,她不影响汽车的行驶性能,还可减少污染.下列有关乙
 笑花主人CCC2022-10-04 11:39:541条回答
笑花主人CCC2022-10-04 11:39:541条回答A.乙醇汽油是一种纯净物
B.乙醇汽油作燃料不会产生碳氧化物等有害气体
C.乙醇和汽油都可作溶剂,也可相互溶解
D.乙醇和乙二醇互为同系物

已提交,审核后显示!提交回复
共1条回复
 Tahity 共回答了26个问题
Tahity 共回答了26个问题 |采纳率84.6%- 解题思路:A.只由一种物质组成的物质是纯净物,由两种或者两种以上物质组成的物质是混合物;
B.汽油的组成元素:C、H、O,还含有少量的S;
C.乙醇和汽油相互溶解;
D.同系物的概念:结构相似,符合同一通式,在组成上相差一个或n个CH2.A.因乙醇汽油的主要成分为乙醇和汽油,是混合物,故A错误;
B.因汽油的组成元素:C、H、O,还含有少量的S,燃烧产物有碳氧化物和二氧化硫,故B错误;
C.因乙醇和汽油都是常见的有机溶剂且有机溶剂之间往往相溶,故C正确;
D.因同系物要求:结构相似,符合同一通式,在组成上相差一个或n个CH2;而乙醇中有1个羟基,乙二醇中含有2个羟基,结构不相相似,故D错误;
故选C.点评:
本题考点: 化石燃料与基本化工原料.
考点点评: 本题需要强调的是同系物的概念,结构相似,若有官能团,必须官能团种类和数目都相同,题目难度不大. - 1年前
相关推荐
- 车用乙醇汽油就是在汽油中加入10%乙醇混合而成的一种燃料.下列对车用乙醇汽油的叙述错误的是
车用乙醇汽油就是在汽油中加入10%乙醇混合而成的一种燃料.下列对车用乙醇汽油的叙述错误的是
A乙醇汽油是一种新型化合物
B汽车使用乙醇汽油达到节能减排的目的
C用玉米、木薯发酵可以制得乙醇
D广西生产木薯,使用车用乙醇可以促进广西农村经济的发展
请详细分析每个答案的原因,谢谢!
 天影王小乖1年前1
天影王小乖1年前1 -
 接头的暗语 共回答了20个问题
接头的暗语 共回答了20个问题 |采纳率100%选A
A错
车用乙醇汽油就是在汽油中加入10%乙醇混合而成,这只是单纯把两种液体混合在一起,没有发生化学反应,只是一种混合物,不是化合物.
B 对,加入乙醇后汽油的燃烧量减少了,而乙醇燃烧后只生成二氧化碳和水,对环境危害极小,达到节能减排的目的.
C对,乙醇可以由含淀粉、糖的植物产品发酵制取.
D制取乙醇要使用大量木薯,所以有助经济发展.
不懂请追问,满意请采纳.谢谢!1年前查看全部
- (2009•南汇区模拟)我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列相关叙述错误的是(
(2009•南汇区模拟)我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列相关叙述错误的是( )
A.使用乙醇汽油能减少有害气体的排放
B.乙醇汽油是一种新型的化合物
C.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得,属于可再生能源
D.甲醇、乙醇都能以任意比例和水互溶 muslin1年前1
muslin1年前1 -
 豆子8210 共回答了16个问题
豆子8210 共回答了16个问题 |采纳率75%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法制乙醇和乙烯与水直接反应.A、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源.故A正确;
B、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成.由此可知乙醇汽油是混合物.故B错误;
C、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等.乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇.故C正确;
D、甲醇、乙醇都是有机物,能以任意比例和水互溶,故D正确.
故选B.点评:
本题考点: 使用化石燃料的利弊及新能源的开发.
考点点评: 使用车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产.1年前查看全部
- (2010•静安区二模)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
(2010•静安区二模)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
①乙醇和汽油均属于______(填“有机物”或“无机物”);
②在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质w.现测得反应前后各物质的质量如下:
根据质量守恒定律,得出表中x的值为______;物质 乙醇 氧气 二氧化碳 水蒸气 W 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
③根据表中数据,可确定未知物w中所含______元素,其组成元素的质量比为______;
④为了使乙醇汽油燃烧过程中少产生w,应采取的措施是______(任写一种). 晓暮_zz中1年前1
晓暮_zz中1年前1 -
 拥砌翠筠侵坐冷 共回答了17个问题
拥砌翠筠侵坐冷 共回答了17个问题 |采纳率94.1%解题思路:(1)欲正确解答本题,须知有机物和无机物的概念和区别;
(2)欲正确解答本题,须根据质量守恒定律,反应前物质的质量=反应后物质的质量进行计算;
(3)欲正确解答本题,需根据化学方程式配平的原则,写出方程式,即可得出W的化学式,然后根据化学式进行计算即可.
(4)欲正确解答本题,须知CO气体的产生与什么有关,进而采取相应的措施.(1)有机物即碳氢化合物(烃)及其衍生物,简称有机物.无机物是无机化合物的简称,通常指不含碳元素的化合物.汽油为油品的一大类,是四碳至十二碳复杂烃类的混合物,符合有机物的特征.从乙醇的化学式可知,它也属于有机物.故答案为:有机物.
(2)根据质量守恒定律,反应前物质的质量=反应后物质的质量.故x=23g+40g-(22g+27g)=14g,故答案为:14.
(3)根据乙醇和氧气的质量关系和化学方程式配平的原则可得反应的化学方程式为:2C2H5OH+5O2
点燃
.
6H2O+2CO2+2CO,故未知物w中所含的元素为C、O;其组成元素的质量比为12:16=3:4.故选C、O,3:4.
(4)在反应过程中之所以生成CO气体,是因为燃烧不充分,要使乙醇汽油燃烧过程中少产生CO气体,需加大空气的进入量,在氧气充足的情况下让其充分燃烧.故答案为:加大空气的进入量.点评:
本题考点: 物质的构成和含量分析;有机物与无机物的区别;元素质量比的计算;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查学生对有机物和无机物的概念和区别、质量守恒定律、化学方程式配平的原则的认识,以及运用化学式进行计算的能力.1年前查看全部
- 石油资源紧张是制约中国发展轿车工业,尤其是制约轿车进入家庭的重要因素.为此,我国在某些省市已开始推广“车用乙醇汽油”,即
石油资源紧张是制约中国发展轿车工业,尤其是制约轿车进入家庭的重要因素.为此,我国在某些省市已开始推广“车用乙醇汽油”,即在汽油中加少量乙醇(C 2 H 5 OH),写出乙醇完全燃烧的化学方程式______.  wszdan31561年前1
wszdan31561年前1 -
 wangyingfeng 共回答了17个问题
wangyingfeng 共回答了17个问题 |采纳率88.2%乙醇和氧气在点燃的条件下生成二氧化碳和水,故答案为:C 2 H 5 OH+3O 2
点燃
.
2CO 2 +3H 2 O.1年前查看全部
- (5分)"车用乙醇汽油"的推广和使用将会缓解石油资源紧张。乙醇(化学式为C 2 H 5 OH)完全燃烧生成CO 2 和H
(5分)"车用乙醇汽油"的推广和使用将会缓解石油资源紧张。乙醇(化学式为C 2 H 5 OH)完全燃烧生成CO 2 和H 2 O.
(1)写出乙醇完全燃烧的化学方程式 。
(2)乙醇燃烧时如果氧气量不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO和CO 2 ,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号) 。
正确连接后的装置仍存在不足,请指出其不足之处 。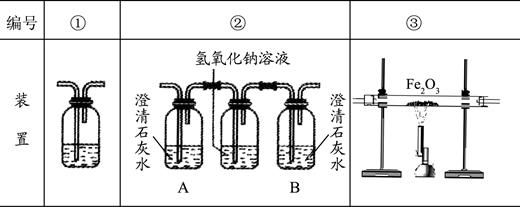
(3)装置②中A、B两瓶均盛有澄清的石灰水,其作用分别是 。
(4)写出装置①中所盛溶液名称及该溶液的作用 。 求祝福1年前1
求祝福1年前1 -
 寻觅黎明 共回答了20个问题
寻觅黎明 共回答了20个问题 |采纳率90%1年前查看全部
- 我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
A.使用乙醇汽油能减少有害气体的排放
B.燃烧中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型的化合物
D.燃烧乙醇汽油可以减少对大气的污染,是因为它不含硫元素和氮元素 richardrr1年前1
richardrr1年前1 -
 maomaodxx 共回答了17个问题
maomaodxx 共回答了17个问题 |采纳率88.2%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法制乙醇和乙烯与水直接反应,乙醇汽油同样会产生污染,其在不完全燃烧的情况下会产生含硫气体和一氧化碳,都属于污染型气体.A、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源.故A叙述正确;
B、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等.乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇.故B叙述正确;
C、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成.由此可知乙醇汽油是混合物.故C叙述不正确;
D、由选项A可知乙醇汽油可以减少对空气的污染,但乙醇汽油同样会产生污染,其在不完全燃烧的情况下会产生含硫气体和一氧化碳,都属于污染型气体,而不是汽油不含硫、氮元素,故选项错误.
故选CD点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;常用燃料的使用与其对环境的影响.
考点点评: 使用车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产.1年前查看全部
- 2003年11月12日《新闻联播》报道:河南省天冠集团20万t车用乙醇汽油工程顺利投产,车用乙醇汽油是由乙醇与汽油按1:
2003年11月12日《新闻联播》报道:河南省天冠集团20万t车用乙醇汽油工程顺利投产,车用乙醇汽油是由乙醇与汽油按1:9比例混合而成.下列有关推广使用乙醇汽油的说法不正确的是( ) A.汽油是以石油为原料加工而成 B.乙醇是由粮食中的淀粉转化而成 C.可节省石油资源,减轻大气污染,改善大气环境 D.乙醇是一种不可再生的能源  xamxat9891年前1
xamxat9891年前1 -
 梧桐2004 共回答了16个问题
梧桐2004 共回答了16个问题 |采纳率87.5%A、汽油是以石油为原料加工而成.故A正确.
B、乙醇是由粮食中的淀粉转化而成.故B正确.
C、汽油中加入乙醇,可节省石油资源,从而降低大气污染物的排放,可改善大气环境.故C正确.
D、乙醇可由粮食发酵制的,所以乙醇是可再生的资源.故D错误.
故选D.1年前查看全部
- (2010•长宁区一模)车用乙醇汽油是将乙醇(C2H6O)和汽油按一定比例混合而成的一种汽车燃料.
(2010•长宁区一模)车用乙醇汽油是将乙醇(C2H6O)和汽油按一定比例混合而成的一种汽车燃料.
(1)乙醇由三三种元素组成,它的式量是4646;
(2)乙醇中各元素的质量之比是12:3:812:3:8;
(3)乙醇中质量分数最大的元素是碳元素碳元素;
(4)工业上用陈化粮(过期粮食)来生产乙醇,过程如下:陈化粮
葡萄糖(C6H12O6)淀粉酶
乙醇+二氧化碳酒化酶
其中葡萄糖转化为乙醇的化学方程式是C6H12O6
2C2H6O+2CO2↑C6H12O6酒化酶
2C2H6O+2CO2↑.酒化酶
(5)乙醇不完全燃烧会生成H2O(气)、CO2和CO.在乙醇质量未知的情况下,若要知道所生成气体的总质量,下列做法能达到目的是D、E、F、GD、E、F、G.
A.只测定CO的质量 B.只测定H2O的质量C.只测定CO2的质量
D.分别测定H2O、CO2的质量E.分别测定H2O、CO的质量
F.分别测定CO、CO2的质量G.分别测定H2O、CO2、CO的质量. polesun1231年前1
polesun1231年前1 -
 dine 共回答了18个问题
dine 共回答了18个问题 |采纳率100%(1)由乙醇的化学式为C2H6O,则该物质是由C、H、O三种元素组成的,其相对分子质量为12×2+1×6+16=46,故答案为:三;46;
(2)由乙醇的化学式为C2H6O,碳、氢、氧元素的质量比为12×2:1×6:16=12:3:8,故答案为:12:3:8;
(3)因相对分子质量为46,,12×2>16>1×6,则碳元素的质量分数最大,故答案为:碳元素;
(4)由陈化粮
淀粉酶
葡萄糖(C6H12O6)
酒化酶
乙醇+二氧化碳,则葡萄糖分解生成乙醇和二氧化碳,反应为C6H12O6
酒化酶
2C2H6O+2CO2↑,
故答案为:C6H12O6
酒化酶
2C2H6O+2CO2↑;
(5)因单独测定一种生成物的质量无法计算CO2和CO的质量,对于D中测定H2O、CO2的质量,由氢原子守恒可知乙醇的量,也可知碳原子的总量,
则再由二氧化碳的量可计算一氧化碳的量,即可以测定混合气体的质量;E中由氢原子守恒可知乙醇的量,也可知碳原子的总量,则再由一氧化碳
的量可计算二氧化碳的量,即可以测定混合气体的质量,D与E的方法相同;因混合气体为CO2和CO,则F、G都可以直接测定出,
故答案为:D、E、F、G.1年前查看全部
- 我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
A.使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源
B.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型的化合物
D.推广乙醇汽油可以减少石油的消耗,缓解石油紧缺 lei_141年前1
lei_141年前1 -
 随野山庄捉刀人 共回答了17个问题
随野山庄捉刀人 共回答了17个问题 |采纳率82.4%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法制乙醇和乙烯与水直接反应,生产乙醇是主要的制乙醇方法.石油是不可再生能源,乙醇汽油是目前世界上可再生能源的发展重点.由多种物质【由多种纯净物(单质或化合物)】混合而成的是混合物.A、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源.故A叙述正确;
B、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等.乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇.故B叙述正确;
C、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成.由此可知乙醇汽油是混合物.故C叙述不正确;
D、石油是不可再生能源,乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点.推广乙醇汽油可以减少石油的消耗,缓解石油紧缺.故D叙述正确.
故选C.点评:
本题考点: 资源综合利用和新能源开发;物质的简单分类;常用燃料的使用与其对环境的影响.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 2003年11月12日《新闻联播》报道:河南省天冠集团20万吨车用乙醇汽油]:程顺利投产,车用乙醇汽油是由乙醇与汽油按1
2003年11月12日《新闻联播》报道:河南省天冠集团20万吨车用乙醇汽油]:程顺利投产,车用乙醇汽油是由乙醇与汽油按1:9比例混合而成.下列有关推广使用乙醇汽油的说法不正确的是( )
A.可大大降低油料价格
B.有助于减轻大气污染,改善大气环境
C.乙醇是一种不可再生的能源
D.有助于促进粮食转化,提高农民收入 gemmer19791年前1
gemmer19791年前1 -
 诗人的舌头 共回答了14个问题
诗人的舌头 共回答了14个问题 |采纳率92.9%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法可制乙醇,所以乙醇是可再生资源,汽油中加入乙醇可减小污染物的排放但对油料的价格影响不大,据此分析解答即可;A、乙醇汽油是由乙醇与汽油按1:9比例混合而成,乙醇含量较小且乙醇价格也不太低,所以使用乙醇汽油并不能大大降低油料价格;
B、汽油中加入乙醇可减小矿物燃料的燃烧,从而降低大气污染物的排放,可改善大气环境;
C、乙醇可由粮食发酵制的,所以乙醇是可再生的资源;
D、制取乙醇可消耗大量的粮食,从而有助于促进粮食转化,提高农民收入;
故选AC点评:
本题考点: 常用燃料的使用与其对环境的影响;常见能源的种类、能源的分类.
考点点评: 此题是对乙醇汽油的考查,根据使用车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,而且还可以促进农业生产便可顺利解题.1年前查看全部
- 车用乙醇汽油是在汽油中加入适量乙醇形成的燃料,使用这种汽车燃料,不但节省了石油资源(乙醇属于 &
车用乙醇汽油是在汽油中加入适量乙醇形成的燃料,使用这种汽车燃料,不但节省了石油资源(乙醇属于 能源),也减少了汽车尾气的污染。乙醇俗称 ,它在空气中充分燃烧的反应化学方程式为 。  liyl1231年前0
liyl1231年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( ) A.使用乙醇汽油能减少
我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( ) A.使用乙醇汽油能减少有害气体的排放 B.燃烧中的乙醇可以通过粮食发酵或化工合成等方法制得 C.乙醇汽油是一种新型的化合物 D.燃烧乙醇汽油可以减少对大气的污染,是因为它不含硫元素和氮元素  tuwei1681年前1
tuwei1681年前1 -
 平平121 共回答了22个问题
平平121 共回答了22个问题 |采纳率95.5%A、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源.故A叙述正确;
B、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等.乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇.故B叙述正确;
C、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成.由此可知乙醇汽油是混合物.故C叙述不正确;
D、由选项A可知乙醇汽油可以减少对空气的污染,但乙醇汽油同样会产生污染,其在不完全燃烧的情况下会产生含硫气体和一氧化碳,都属于污染型气体,而不是汽油不含硫、氮元素,故选项错误.
故选CD1年前查看全部
- (2008•来宾)从2008年4月1日起,来宾等市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C2H5OH)混合而成,
(2008•来宾)从2008年4月1日起,来宾等市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C2H5OH)混合而成,其中乙醇约占10%.
(1)乙醇充分燃烧的化学方程式为C2H50H+302
2C02+3H20点燃 .C2H50H+302.
2C02+3H20点燃 .
(2)使用乙醇汽油的优点是______(写出一点即可) CCCollie1年前1
CCCollie1年前1 -
 lihaibo0906 共回答了14个问题
lihaibo0906 共回答了14个问题 |采纳率85.7%解题思路:根据反应物和生成物及其质量守恒定律可以书写化学方程式;乙醇燃烧生成二氧化碳和水,不污染环境.(1)乙醇充分燃烧的化学方程式为:C2H50H+302
点燃
.
2C02+3H20.
(2)使用乙醇汽油的优点是节约原油、环保等.故填:节约原油、环保等.点评:
本题考点: 常用燃料的使用与其对环境的影响;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和节能环保的重要性,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料.下列叙述错误的是( )
A.使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源
B.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型燃料
D.燃烧乙醇汽油可以减少对大气的污染,是因为它不含硫元素和氮元素 zhai9090901年前1
zhai9090901年前1 -
 53dd 共回答了19个问题
53dd 共回答了19个问题 |采纳率84.2%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法制乙醇和乙烯与水直接反应,生产乙醇是主要的制乙醇方法.石油是不可再生能源,乙醇汽油是目前世界上可再生能源的发展重点.由多种物质【由多种纯净物(单质或化合物)】混合而成的是混合物.A、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源.故A叙述正确;
B、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等.乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇.故B叙述正确;
C、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成.由此可知乙醇汽油是一种新型燃料.故C叙述正确;
D、由选项A可知乙醇汽油可以减少对空气的污染,但乙醇汽油同样会产生污染,其在不完全燃烧的情况下会产生含硫气体和一氧化碳,都属于污染型气体,而不是汽油不含硫、氮元素,故选项错误.
答案:D点评:
本题考点: 常用燃料的使用与其对环境的影响;甲烷、乙醇等常见有机物的性质和用途.
考点点评: 使用车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产.1年前查看全部
- 车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合而成的一种汽车燃料.
车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合而成的一种汽车燃料.
(1)乙醇分子中,组成元素的原子个数比C:H:O为______.
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W.现测得反应前后各物质的质量如下:
①根据质量守恒定律,得出表中x的值为______;物质 乙醇 氧气 二氧化碳 水蒸气 W 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
②根据表中数据,可确定未知物W中各组成元素的质量比为______;
(3)通常可燃物中碳元素质量分数越高,燃烧产生W越多.则相同条件下,乙醇和汽油分别燃烧时,产生W较多的是______;为了使乙醇汽油燃烧过程中少产生W,应采取的措施是______(任写一种). longsing19861年前1
longsing19861年前1 -
 lixiaoxin 共回答了18个问题
lixiaoxin 共回答了18个问题 |采纳率83.3%(1)根据乙醇(C 2 H 5 OH)的化学式可知,组成元素的原子个数比C:H:O为2:6:1.故答案为:2:6:1.
(2)①据质量守恒定律可得,x=23g+40g-(22g+27g)=14g;
②根据乙醇(C 2 H 5 OH)的化学式可知,C:H:O元素的质量比为:(12×2):6:16=24:6:16=12:3:8,
看一看反应物:乙醇中碳质量为23g×
12
23 =12克,氧的质量为23g×
8
23 =8克,氢的为23g×
3
23 =3克;
氧气质量为40克.故反应物中氧原子共有48克.
看生成物:碳的质量为22g×
12
44 =6克,氢的为27g×
2
18 =3克,氧的质量为22g+27g-6g-3g=40克.
生成物中碳的质量为:12g-6g=6g,氧的质量为:48g-40g=8g,氢的质量为:3g-3g=0.
故W中含有碳6克,氧8克.
故答案为3:4(或4:3).
(3)①从乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 )的化学式可以看出,汽油中碳元素的质量分数>乙醇中碳元素的质量分数,根据已知条件可知,产生W较多的是汽油;
②由题意“在密闭容器中”可知,乙醇再不完全燃烧时产生W较多,因此,为了使乙醇汽油燃烧过程中少产生W,应采取的措施可以是:加大助燃物(氧气)的质量,使其成分燃烧;提高乙醇在乙醇汽油中的比例等.
故答案为:①汽油;②增大氧气量,使之充分燃烧(或提高乙醇在乙醇汽油中的比例等,合理即可).1年前查看全部
- 据中央电视台2001年4月15日的报道,我国推广使用车用乙醇汽油的工作将全面启动.车用乙醇汽油是在汽油中加入适量的乙醇形
据中央电视台2001年4月15日的报道,我国推广使用车用乙醇汽油的工作将全面启动.车用乙醇汽油是在汽油中加入适量的乙醇形成的混合燃料.使用这种汽油不但不影响汽车的行驶性能,而且可减少有害气体的排放,是一种改善环境的清洁能源.同时,燃料乙醇主要是以粮食作为原料,这对解决我国粮食过剩,促进农业生产良性循环也具有十分重要的意义.
根据上述报道回答:
(1)乙醇能代替汽油作为燃料,是因为乙醇中含有______元素和______元素;
(2)燃烧乙醇比燃烧汽油减少了对大气的污染,是因为乙醇中不含有______元素;
(3)乙醇是由粮食中的淀粉转化而成的,淀粉是绿色植物通过光合作用由______和______两种物质转化而成的. lgh2101年前1
lgh2101年前1 -
 w010101 共回答了16个问题
w010101 共回答了16个问题 |采纳率81.3%解题思路:(1)乙醇的结构简式为CH3CH2OH,乙醇燃烧后的产物对环境无污染.乙醇是可再生能源,汽油提取自石油,属于不可再生资源;
(2)乙醇可代替汽油做燃料,是因为它含有碳和氢元素,它减少了对大气的污染,是因为它不含硫元素;
(3)光合作用是植物、藻类利用叶绿素等光和色素和某些细菌利用其细胞本身,在可见光的照射下,将二氧化碳和水(细菌为硫化氢和水)转化为有机物,并释放出氧气(细菌释放氢气)的生化过程.(1)乙醇能代替汽油作为燃料,是因为乙醇中含有碳元素和氢元素;
(2)燃烧乙醇比燃烧汽油减少了对大气的污染,是因为乙醇中不含有硫元素;
(3)淀粉是绿色植物通过光合作用由二氧化碳和水两种物质转化而成的.
故答案为:(1)碳,氢;
(2)硫;
(3)二氧化碳,水.点评:
本题考点: 资源综合利用和新能源开发;自然界中的碳循环;物质的元素组成;常用燃料的使用与其对环境的影响.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合而成的一种汽车燃料。
车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合而成的一种汽车燃料。
(1)乙醇分子中,组成元素的原子个数比C:H:O为___________。
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W。现测得反应前后各物质的质量如下: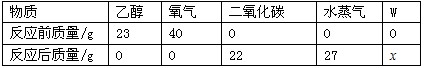
①根据质量守恒定律,得出表中x的值为_________;
②根据表中数据,可确定未知物W中各组成元素的质量比为__________;
(3)通常可燃物中碳元素质量分数越高,燃烧产生W越多。则相同条件下,乙醇和汽油分别燃烧时,产生W较多的是_________;为了使乙醇汽油燃烧过程中少产生W,应采取的措施是______(任写一种)。 蒾眩薬1年前1
蒾眩薬1年前1 -
 suosuo1314 共回答了16个问题
suosuo1314 共回答了16个问题 |采纳率100%(1)2:6:1
(2)①14
②3:4(或4:3)
(3)汽油;增大氧气量,使之充分燃烧(或提高乙醇在乙醇汽油中的比例等,合理即可)1年前查看全部
- 据央视报道,自2006年12月1日起在武汉九市进行车用乙醇汽油封闭推广行动.车用乙醇汽油是把变性燃料乙醇和汽油按一定比例
据央视报道,自2006年12月1日起在武汉九市进行车用乙醇汽油封闭推广行动.车用乙醇汽油是把变性燃料乙醇和汽油按一定比例混配形成的一种新型汽车燃料.经多项检测结果表明,它不影响汽车的行驶性能,还可以减少有害气体的排放量.在美国、巴西等国早已推广使用.下列有关乙醇汽油的说法正确的是( ) A.乙醇汽油是一种纯净物 B.乙醇汽油作燃料不会产生碳氧化物等有害气体,其优点是可以减少对环境的污染 C.乙醇和汽油都可作溶剂,也可相互溶解 D.乙醇和乙二醇互为同系物  lk_1520311年前1
lk_1520311年前1 -
 ggtea 共回答了16个问题
ggtea 共回答了16个问题 |采纳率87.5%A、因乙醇汽油的主要成分为乙醇和汽油,是混合物,故A错误;
B、因汽油的组成元素:C、H、O,还含有少量的S,燃烧产物有碳氧化物和二氧化硫,其中二氧化硫污染环境,乙醇的组成元素:C、H、O,燃烧产物有碳氧化物,所以乙醇汽油作燃料仍会产生碳氧化物等有害气体,但可以减少对环境的污染,故B错误;
C、因乙醇和汽油都是常见的有机溶剂且有机溶剂之间往往相溶,故C正确;
D、因同系物要求:结构相似,符合同一通式,在组成上相差一个或n个CH 2 ;而乙醇中有1个羟基,乙二醇中含有2个羟基,结构不相相似,故D错误;
故选:C.1年前查看全部
- 生活中处处有化学,按要求填空:(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染。乙醇在空气中燃烧的化学方程式为
生活中处处有化学,按要求填空:
(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染。乙醇在空气中燃烧的化学方程式为 。
(2)用二氧化碳灭火器灭火的原理是 。
(3)把煤做成蜂窝煤状就有利于燃烧,其原因是 。 散步的鱼儿1231年前0
散步的鱼儿1231年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 2001年6月21日,河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗
2001年6月21日,河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗名酒精,它是以玉米、小麦、薯类等为原料经发酵、蒸馏而制成的。乙醇进一步脱水,再加上适量汽油后形成变性燃料乙醇。而车用乙醇汽油就是把变性燃料乙醇和汽油按一定比例混配形成的车用燃料。结合有关知识,完成以下问题:
(1)乙醇的结构简式为_____________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C 5 —C 11 范围内,如戊烷,其分子式为__________________,结构简式及其同分异构体分别为_____________、_____________、_____________。
(2)乙醇可由含淀粉〔(C 6 H 10 O 5 ) n 〕的农产品,如玉米、小麦、薯类等经发酵、蒸馏而得。请写出由淀粉制乙醇的化学方程式:
①淀粉+水 葡萄糖(C 6 H 12 O 6 )
葡萄糖(C 6 H 12 O 6 )
②葡萄糖 乙醇
乙醇
(3)淀粉可由绿色植物经光合作用等一系列生物化学反应得到,即水和二氧化碳经光合作用生成葡萄糖,由葡萄糖再生成淀粉。进行光合作用的场所是_____________,发生光合作用生成葡萄糖的化学方程式是
__________________________________________________________。
(4)乙醇充分燃烧的产物为__________________和__________________。
(5)车用乙醇汽油称为环保燃料,其原因是__________________________________________。 frankly9021年前1
frankly9021年前1 -
 bluezxc 共回答了13个问题
bluezxc 共回答了13个问题 |采纳率92.3%1年前查看全部
- 生活中处处有化学,按要求填空:(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染.乙醇在空气中燃烧的化学方程式为___
生活中处处有化学,按要求填空:
(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染.乙醇在空气中燃烧的化学方程式为______.
(2)用二氧化碳灭火器灭火的原理是______.
(3)把煤做成蜂窝煤状就有利于燃烧,其原因是______. 阳光下的暴风雪1年前1
阳光下的暴风雪1年前1 -
 wangbo05390 共回答了17个问题
wangbo05390 共回答了17个问题 |采纳率94.1%(1)乙醇燃烧生成二氧化碳和水,故答案:C 2 H 5 OH+3O 2
点燃
.
2CO 2 +3H 2 O;
(2)二氧化碳灭火器灭火的原理是在常温下用压缩体积的办法使二氧化碳气体液化装入钢瓶里的,液态二氧化碳在常温下会迅速汽化,并吸收大量的热.所以灭火故答案为:隔绝氧气并降温到着火点以下.
(3)增大氧气的浓度或增大可燃物与氧气的接触面积可以促进燃料的燃烧,把块煤做成蜂窝煤是为了增大煤与氧气的接触面积,从而促进煤的燃烧.
答案:
(1)C 2 H 5 OH+3O 2
点燃
.
2CO 2 +3H 2 O
(2)隔绝空气并降低可燃物的温度至着火点以下
(3)增大与空气的接触面积1年前查看全部
- (2012•青浦区二模)“车用乙醇汽油“的推广和使用将会缓解石油资源紧张.乙醇(化学式为C2H5OH)完全燃烧生成CO2
(2012•青浦区二模)“车用乙醇汽油“的推广和使用将会缓解石油资源紧张.乙醇(化学式为C2H5OH)完全燃烧生成CO2和H2O.
(1)写出乙醇完全燃烧的化学方程式C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2.
2CO2+3H2O点燃 .
(2)乙醇燃烧时如果氧气量不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO和CO2,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号)______.正确连接后的装置仍存在不足,请指出其不足之处______.
(3)装置②中A、B两瓶均盛有澄清的石灰水,其作用分别是______.
(4)写出装置①中所盛溶液名称及该溶液的作用______.编号 ① ② ③ 装置 
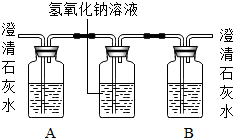
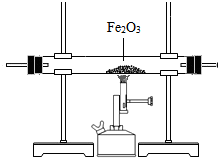
 colorwindlk1年前1
colorwindlk1年前1 -
 taozeng 共回答了17个问题
taozeng 共回答了17个问题 |采纳率94.1%解题思路:根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式;一氧化碳有毒,能够污染环境;澄清的石灰水遇二氧化碳变浑浊;氢氧化钠溶液能吸收二氧化碳气体.例如,澄清的石灰水遇二氧化碳变浑浊,可以用来检验二氧化碳气体是否存在.(1)乙醇燃烧的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O.
(2)通过②可以检验是否有二氧化碳,如果含有二氧化碳可以通过氢氧化钠溶液除去;通过③可以检验是否有一氧化碳;通过①可以检验是否有二氧化碳生成.故填:②③①.
一氧化碳有毒,能够污染环境,应该对尾气中的一氧化碳进行处理.故填:没有尾气处理装置.
(3)装置②中A、B两瓶均盛有澄清的石灰水,其作用分别是:A检验燃烧产物中有二氧化碳;B证明燃烧产物中的二氧化碳是否被氢氧化钠溶液完全吸收.故填:A检验燃烧产物中有二氧化碳;B证明燃烧产物中的二氧化碳是否被氢氧化钠溶液完全吸收.
(4)装置①中所盛溶液名称及该溶液的作用:澄清的石灰水;作用是证明③中反应有二氧化碳生成,从而说明原燃烧产物中有一氧化碳.故填:澄清的石灰水;作用是证明③中反应有二氧化碳生成,从而说明原燃烧产物中有一氧化碳.点评:
本题考点: 常用燃料的使用与其对环境的影响;常见气体的检验与除杂方法;二氧化碳的检验和验满;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和各种物质的性质等方面的知识,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 燃油税于今年实施,目前使用的车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合
燃油税于今年实施,目前使用的车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 表示)按一定比例混合而成的一种汽车燃料.
(1)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W.现测得反应前后各物质的质量如下:
①根据质量守恒定律,得出表中x的值为______;物质 乙醇 氧气 二氧化碳 水蒸气 W 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
②根据表中数据,可确定未知物W中的化学式为______;
(2)通常可燃物中碳元素质量分数越高,燃烧产生 W越多.则相同条件下,乙醇和汽油分别燃烧时,产生W较多的是______;为了使乙醇汽油燃烧过程中少产生 W,应采取的措施是______(任写一种). 谜女郎1年前1
谜女郎1年前1 -
 还是健 共回答了23个问题
还是健 共回答了23个问题 |采纳率91.3%(1)①据质量守恒定律可得,x=23+40-(22+27)=14;
②根据乙醇(C 2 H 5 OH)的化学式可知,C:H:O元素的质量比为:(12×2):6:16=24:6:16=12:3:8,
看一看反应物:乙醇中碳质量为23g×
12
23 =12g,氧的质量为23g×
8
23 =8g,氢的质量为23g×
3
23 =3g;
氧气质量为40克,故反应物中氧元素的质量共是48克.
看生成物:碳的质量为22g×
12
44 =6g,氢的质量为27g×
2
18 =3g,氧的质量为22g+27g-6g-3g=40g.
生成物中碳的质量为:12g-6g=6g,氧的质量为:48g-40g=8g,氢的质量为:3g-3g=0.
故W中含有碳6克,氧8克,因此W中碳氧原子个数比是
6g
12 :
8g
16 =1:1,所以W的化学式是CO;
(2)从乙醇(C 2 H 5 OH)与汽油(以C 8 H 18 )的化学式可以看出,汽油中碳元素的质量分数>乙醇中碳元素的质量分数,根据已知条件可知,产生W较多的是汽油;
由题意“在密闭容器中”可知,乙醇再不完全燃烧时产生W较多,因此,为了使乙醇汽油燃烧过程中少产生W,应采取的措施可以是:增大氧气量,使之充分燃烧;提高乙醇在乙醇汽油中的比例等.
故答案为:(1)①14; ②CO;(2)汽油;增大氧气量,使之充分燃烧.1年前查看全部
- (10分)河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗名酒精,它是
(10分)河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗名酒精,它是以玉米、小麦、薯类等为原料经发酵、蒸馏而制成的。乙醇进一步脱水,再加上适量汽油后形成变性燃料乙醇。而车用乙醇汽油就是把变性燃料乙醇和汽油按一定比例混配形成的车用燃料。结合有关知识,完成以下问题:
(1)乙醇的结构简式为_________________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C 5 —C 11 范围内,如戊烷,其分子式为_________________,其同分异构体结构简式分别为_______________________、________________________、_______________________。
(2)乙醇可由含淀粉〔(C 6 H 10 O 5 ) n 〕的农产品(如玉米、小麦、薯类等)经发酵、蒸馏而得,这就是酿酒。酿酒主要有两步:①淀粉+水 葡萄糖(C 6 H 12 O 6 ) ②葡萄糖
葡萄糖(C 6 H 12 O 6 ) ②葡萄糖 乙醇。
乙醇。
请写出淀粉生成葡萄糖的化学方程式:___________________________________。
(3)乙醇充分燃烧的产物为_____________和_____________。
(4)车用乙醇汽油称为环保燃料,其原因是________________________________。 afiend1年前1
afiend1年前1 -
 朝三暮四女 共回答了18个问题
朝三暮四女 共回答了18个问题 |采纳率94.4%(1)1×5=5分 C 2 H 5 OH C 5 H 12 CH 3 CH 2 CH 2 CH 2 CH 3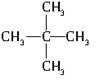
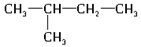
(2)(C 6 H 10 O 5 ) n (淀粉)+nH 2 O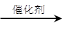 nC 6 H 12 O 6 (葡萄糖)(2分)
nC 6 H 12 O 6 (葡萄糖)(2分)
(3)CO 2 H 2 O(2分)
(4)能有效降低汽车尾气带来的严重大气污染,改善环境(1分)
(1)乙醇中含有羟基,所以结构简式为C 2 H 5 OH。根据烷烃的通式CnH2n+2可知,戊烷的分子式是C 5 H 12 。戊烷有三种同分异构体,分别是CH 3 CH 2 CH 2 CH 2 CH 3 、CH 3 CH 2 CH(CH 3 ) 2 、C(CH 3 ) 4 。
(2)淀粉水解即生成葡萄糖,方程式为(C 6 H 10 O 5 ) n +nH 2 O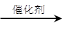 nC 6 H 12 O 6
nC 6 H 12 O 6
(淀粉) (葡萄糖)
(3)根据乙醇的组成元素可知,乙醇完全燃烧的生成物是CO 2 和水。
(4)根据乙醇的燃烧产物可知,乙醇汽油之所以称为环保燃料,其原因是由于能有效降低汽车尾气带来的严重大气污染,改善环境。1年前查看全部
- 2003年11月12日《新闻联播》报道:河南省天冠集团20万t车用乙醇汽油工程顺利投产,车用乙醇汽油是由乙醇与汽油按1:
2003年11月12日《新闻联播》报道:河南省天冠集团20万t车用乙醇汽油工程顺利投产,车用乙醇汽油是由乙醇与汽油按1:9比例混合而成.下列有关推广使用乙醇汽油的说法不正确的是( )
A.汽油是以石油为原料加工而成
B.乙醇是由粮食中的淀粉转化而成
C.可节省石油资源,减轻大气污染,改善大气环境
D.乙醇是一种不可再生的能源 东风知俺欲1年前1
东风知俺欲1年前1 -
 猪猪和猴猴 共回答了24个问题
猪猪和猴猴 共回答了24个问题 |采纳率91.7%解题思路:乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.发酵法可制乙醇,所以乙醇是可再生资源,汽油中加入乙醇可减小污染物的排放但对油料的价格影响不大.据此分析解答即可.A、汽油是以石油为原料加工而成.故A正确.
B、乙醇是由粮食中的淀粉转化而成.故B正确.
C、汽油中加入乙醇,可节省石油资源,从而降低大气污染物的排放,可改善大气环境.故C正确.
D、乙醇可由粮食发酵制的,所以乙醇是可再生的资源.故D错误.
故选D.点评:
本题考点: 常用燃料的使用与其对环境的影响;石油加工的产物;常见能源的种类、能源的分类.
考点点评: 此题是对乙醇汽油的考查,根据使用车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,而且还可以促进农业生产便可顺利解题.1年前查看全部
- 车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
①乙醇和汽油均属于______(填“有机物”或“无机物”);
②在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质w.现测得反应前后各物质的质量如下:
根据质量守恒定律,得出表中x的值为______.物质 乙 醇 氧 气 二氧化碳 水蒸气 w 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x  秋如月1年前1
秋如月1年前1 -
 luihui0535 共回答了15个问题
luihui0535 共回答了15个问题 |采纳率86.7%解题思路:①根据物质的组成分析物质的类别;
①根据质量守恒定律定律分析x的值①乙醇和汽油都是含有碳元素的化合物,属于有机物;
②因为反应物为乙醇和氧气,质量共23+40=63克,根据质量守恒定律可知,生成物的质量应为63克,所以x的值为:63-22-27=14克.
故答为:①有机物②14点评:
本题考点: 有机物与无机物的区别;质量守恒定律及其应用.
考点点评: 本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.1年前查看全部
- 石油是一种不可再生能源,为了人类的可持续发展,人们正在积极寻找新能源,研究和推广“车用乙醇汽油”就是一例.乙醇(化学式为
石油是一种不可再生能源,为了人类的可持续发展,人们正在积极寻找新能源,研究和推广“车用乙醇汽油”就是一例.乙醇(化学式为C 2 H 5 OH)完全燃烧生成CO 2 和H 2 O.
(1)写出乙醇完全燃烧的化学方程式:______.
(2)乙醇燃烧时如果氧气不足,可能还有CO生成.如图中装置④所盛的固体药品是白色无水硫酸铜,它遇水蒸气变蓝色.用以下装置验证乙醇燃烧产物有 CO,CO 2 ,H 2 O,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号):______.
(3)实验时可观察到装置②中A瓶石灰水变浑浊,C瓶的石灰水不变浑浊.A瓶溶液的作用是______;B瓶溶液的作用是______;C瓶溶液的作用是______.编号 ① ② ③ ④ 装置 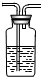
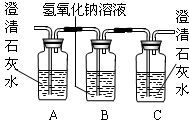
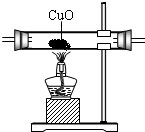
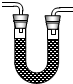
(4)装置③的作用是______,装置①中所盛的是______溶液.
(5)尾气应如何处理?______. 30新用户注册1年前1
30新用户注册1年前1 -
 37094479 共回答了11个问题
37094479 共回答了11个问题 |采纳率100%(1)乙醇完全燃烧的化学方程式:C 2 H 5 OH+30 2
点燃
.
2CO 2 +3H 2 O.
(2)通过④可以检验水的存在,通过②可以检验二氧化碳的存在,并且能够除去二氧化碳气体,通过③①能够检验一氧化碳的存在.故填:④②③①.
(3)A瓶溶液的作用是验证CO 2 的存在;B瓶溶液的作用是除去混合气体中的CO 2 ;C瓶溶液的作用是证明CO 2 已被除尽.故填:验证CO 2 的存在;除去混合气体中的CO 2 ;证明CO 2 已被除尽.
(4)装置③的作用是将CO氧化成CO 2 ,装置①中所盛的是澄清石灰水溶液.故填:将CO氧化成CO 2 ;澄清石灰水.
(5)一氧化碳具有可燃性,可以通过点燃的方法除去一氧化碳.故填:点燃.1年前查看全部
- 下列有关环境保护的叙述不正确的是( ) A.为了减少环境污染,提倡有限制的使用塑料制品. B.使用车用乙醇汽油,减少对
下列有关环境保护的叙述不正确的是( )
A.为了减少环境污染,提倡有限制的使用塑料制品. B.使用车用乙醇汽油,减少对不可再生能源的开发利用. C.禁止煤的使用,防止酸雨的形成. D.为了提高生活质量应减少PM 2.5 烟尘排放.  红桑牡丹1年前1
红桑牡丹1年前1 -
 puppet9527 共回答了13个问题
puppet9527 共回答了13个问题 |采纳率92.3%C
1年前查看全部
- (2014•集美区模拟)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
(2014•集美区模拟)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
(1)写出乙醇在氧气中完全燃烧的化学方程式C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2;
2CO2+3H2O点燃 .
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质w.
现测得反应前后各物质的质量如下:
根据质量守恒定律,得出表中x的值为______;物质 乙 醇 氧 气 二氧化碳 水蒸气 w 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
(3)为了使乙醇汽油燃烧过程中少产生w,应采取的措施是______.
(4)根据表中数据,可确定未知物w中含有______元素,其组成元素的质量比为______. 成而文1年前1
成而文1年前1 -
 兰花小馆十二点 共回答了16个问题
兰花小馆十二点 共回答了16个问题 |采纳率100%解题思路:(1)乙醇完全燃烧生成二氧化碳和水,写出反应的化学方程式即可;
(2)据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.据此答题;
(3)欲正确解答本题,须知CO气体的产生与什么有关,进而采取相应的措施;
(4)欲正确解答本题,需根据化学方程式配平的原则,写出方程式,即可得出W的化学式,然后根据化学式进行计算即可.(1)乙醇完全燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O.故填:C2H5OH+3O2
点燃
.
2CO2+3H2O;
(2)据质量守恒定律:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.可得:23g+40g=22g+27g+x,解得x=23g+40g-(22g+27g)=14g;故填:14;
(3)在反应过程中之所以生成CO气体,是因为燃烧不充分,要使乙醇汽油燃烧过程中少产生CO气体,需加大空气的进入量,在氧气充足的情况下让其充分燃烧.故填:加大空气的进入量;
(4)根据乙醇和氧气的质量关系和化学方程式配平的原则可得反应的化学方程式为:2C2H5OH+5O2
点燃
.
6H2O+2CO2+2CO,故未知物w中所含的元素为C、O;其组成元素的质量比为12:16=3:4.故填:C、O;3:4.点评:
本题考点: 常用燃料的使用与其对环境的影响;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查学生对质量守恒定律、化学方程式配平的原则的认识,以及运用化学式进行计算的能力.1年前查看全部
- (2006•荆州)车用乙醇汽油是将燃料乙醇和汽油以一定的比例混合而成的一种汽油燃料,那么乙醇汽油属于( )
(2006•荆州)车用乙醇汽油是将燃料乙醇和汽油以一定的比例混合而成的一种汽油燃料,那么乙醇汽油属于( )
A.氧化物
B.纯净物
C.混合物
D.化合物 Iacta_alea_est1年前1
Iacta_alea_est1年前1 -
 vovlo2005 共回答了23个问题
vovlo2005 共回答了23个问题 |采纳率95.7%解题思路:乙醇汽油是由乙醇和汽油两种物质组成的,属于混合物.乙醇属于纯净物,汽油是由多种烷烃组成的,属于混合物,乙醇和汽油组成的物质属于混合物.
故选C.点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;纯净物和混合物的判别.
考点点评: 解答本题要分析物质是由几种物质组成的,如果是由多种物质组成的就属于混合物.1年前查看全部
- 我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料。下列相关叙述错误的是 [
我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料。下列相关叙述错误的是 [ ]A.使用乙醇汽油能减少有害气体的排放
B.乙醇汽油是一种新型的化合物
C.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得,属于可再生能源
D.甲醇、乙醇都能以任意比例和水互溶 一个茸茸1年前1
一个茸茸1年前1 -
 我就很从容 共回答了15个问题
我就很从容 共回答了15个问题 |采纳率86.7%B1年前查看全部
- 填空 计算车用乙醇汽油是将乙醇与汽油按一定比例混合而成的一种汽车燃料,在密闭容器中,将乙醇置于氧气中燃烧,若生成物均为化
填空 计算
车用乙醇汽油是将乙醇与汽油按一定比例混合而成的一种汽车燃料,在密闭容器中,将乙醇置于氧气中燃烧,若生成物均为化合物,测得反应前后部分物质的质量如下:
物质 乙醇 氧气 X Y
反应前质量/g 30 40 0 0
反应后质量/g 7 0 22 14
根据表中的数据,可确定未知物Y种各组成元素的质量比是多少? 下看民1年前1
下看民1年前1 -
 jasminezl 共回答了9个问题
jasminezl 共回答了9个问题 |采纳率100%参加反应的乙醇为30-7=23克 H O C 元素含量分别为:3克 8克 12克
参加反应的氧气为40克 0 元素含量为40克
生成的水=30+40-7-22-14=27克 H O 元素含量为 3克 24克
根据质量守恒定律
XY 共含
C 12克 12/12=1
O (8+40-24)克=24克 24/16=1.5
H (3-3)克=0克
可知,XY中一种为CO2,一种为CO
十字交叉法(氧碳比)
CO2 2 1.5-1=0.5
1.5
CO 1 2-1.5=0.5
即CO2与CO的系数比为1:1
所以X,Y 分别为CO2 ,CO
Y中各组成元素的质量比C:O=12:16=3:41年前查看全部
- 石油是一种不可再生能源,为了人类的可持续发展,人们正在积极寻找新能源,研究和推广“车用乙醇汽油”就是一例.乙醇(化学式为
石油是一种不可再生能源,为了人类的可持续发展,人们正在积极寻找新能源,研究和推广“车用乙醇汽油”就是一例.乙醇(化学式为C2H5OH)完全燃烧生成CO2和H2O.
(1)写出乙醇完全燃烧的化学方程式:C2H5OH+302
2CO2+3H2O点燃 .C2H5OH+302.
2CO2+3H2O点燃 .
(2)乙醇燃烧时如果氧气不足,可能还有CO生成.如图中装置④所盛的固体药品是白色无水硫酸铜,它遇水蒸气变蓝色.用以下装置验证乙醇燃烧产物有 CO,CO2,H2O,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号):______.
(3)实验时可观察到装置②中A瓶石灰水变浑浊,C瓶的石灰水不变浑浊.A瓶溶液的作用是______;B瓶溶液的作用是______;C瓶溶液的作用是______.编号 ① ② ③ ④ 装置 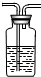
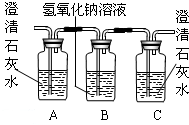
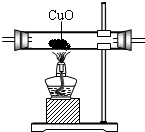
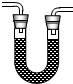
(4)装置③的作用是______,装置①中所盛的是______溶液.
(5)尾气应如何处理?______. 1x1y1年前1
1x1y1年前1 -
 青岛火鸟 共回答了15个问题
青岛火鸟 共回答了15个问题 |采纳率93.3%解题思路:(1)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(2)通过④可以检验水的存在,通过②可以检验二氧化碳的存在,并且能够除去二氧化碳气体,通过③①能够检验一氧化碳的存在;
(3)A中变浑浊说明含有二氧化碳,C瓶的石灰水不变浑浊说明二氧化碳已经被氢氧化钠溶液完全吸收;
(4)在加热条件下一氧化碳能和氧化铜反应生成铜和二氧化碳,通过澄清的石灰水遇二氧化碳变浑浊可以检验原混合气体中含有一氧化碳;
(5)一氧化碳有毒,能够污染环境,可以用燃烧的方法把一氧化碳除去.(1)乙醇完全燃烧的化学方程式:C2H5OH+302
点燃
.
2CO2+3H2O.
(2)通过④可以检验水的存在,通过②可以检验二氧化碳的存在,并且能够除去二氧化碳气体,通过③①能够检验一氧化碳的存在.故填:④②③①.
(3)A瓶溶液的作用是验证CO2的存在;B瓶溶液的作用是除去混合气体中的CO2;C瓶溶液的作用是证明CO2已被除尽.故填:验证CO2的存在;除去混合气体中的CO2;证明CO2已被除尽.
(4)装置③的作用是将CO氧化成CO2,装置①中所盛的是澄清石灰水溶液.故填:将CO氧化成CO2;澄清石灰水.
(5)一氧化碳具有可燃性,可以通过点燃的方法除去一氧化碳.故填:点燃.点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;常见气体的检验与除杂方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 2003年11月12日《新闻联播》报道:河南省天冠集团20万吨车用乙醇汽油]:程顺利投产,车用乙醇汽油是由乙醇与汽油按1
2003年11月12日《新闻联播》报道:河南省天冠集团20万吨车用乙醇汽油]:程顺利投产,车用乙醇汽油是由乙醇与汽油按1:9比例混合而成.下列有关推广使用乙醇汽油的说法不正确的是( )
A.可大大降低油料价格
B.有助于减轻大气污染,改善大气环境
C.乙醇是一种不可再生的能源
D.有助于促进粮食转化,提高农民收入 痕无雪踏1年前1
痕无雪踏1年前1 -
 suxuan 共回答了18个问题
suxuan 共回答了18个问题 |采纳率94.4%A、乙醇汽油是由乙醇与汽油按1:9比例混合而成,乙醇含量较小且乙醇价格也不太低,所以使用乙醇汽油并不能大大降低油料价格;
B、汽油中加入乙醇可减小矿物燃料的燃烧,从而降低大气污染物的排放,可改善大气环境;
C、乙醇可由粮食发酵制的,所以乙醇是可再生的资源;
D、制取乙醇可消耗大量的粮食,从而有助于促进粮食转化,提高农民收入;
故选AC1年前查看全部
- 我大力推广车用乙醇汽油的意义是什么
我大力推广车用乙醇汽油的意义是什么
急 binbinche1年前5
binbinche1年前5 -
 月鸟月 共回答了16个问题
月鸟月 共回答了16个问题 |采纳率75%为了减少环境污染,节约能源呀~使用纯汽油的话,各种废弃排量很高~而且油资源减少很快.乙醇是可再生的,且燃烧只产生少量二氧化碳和水,污染小.1年前查看全部
- 车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油按一定比例混合而成的一种汽车燃料.
车用乙醇汽油是将乙醇(C 2 H 5 OH)与汽油按一定比例混合而成的一种汽车燃料.
①乙醇和汽油均属于______(填“有机物”或“无机物”);
②在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质w.现测得反应前后各物质的质量如下:
根据质量守恒定律,得出表中x的值为______;物质 乙醇 氧气 二氧化碳 水蒸气 W 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
③根据表中数据,可确定未知物w中所含______元素,其组成元素的质量比为______;
④为了使乙醇汽油燃烧过程中少产生w,应采取的措施是______(任写一种). xiaomu081年前1
xiaomu081年前1 -
 宁波慈城 共回答了21个问题
宁波慈城 共回答了21个问题 |采纳率90.5%(1)有机物即碳氢化合物(烃)及其衍生物,简称有机物.无机物是无机化合物的简称,通常指不含碳元素的化合物.汽油为油品的一大类,是四碳至十二碳复杂烃类的混合物,符合有机物的特征.从乙醇的化学式可知,它也属于有机物.故答案为:有机物.
(2)根据质量守恒定律,反应前物质的质量=反应后物质的质量.故x=23g+40g-(22g+27g)=14g,故答案为:14.
(3)根据乙醇和氧气的质量关系和化学方程式配平的原则可得反应的化学方程式为:2C 2 H 5 OH+5O 2
点燃
.
6H 2 O+2CO 2 +2CO,故未知物w中所含的元素为C、O;其组成元素的质量比为12:16=3:4.故选C、O,3:4.
(4)在反应过程中之所以生成CO气体,是因为燃烧不充分,要使乙醇汽油燃烧过程中少产生CO气体,需加大空气的进入量,在氧气充足的情况下让其充分燃烧.故答案为:加大空气的进入量.1年前查看全部
- 从2008年4月1日起,某市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C 2 H 5 OH)混合而成,其中乙醇约占1
从2008年4月1日起,某市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C 2 H 5 OH)混合而成,其中乙醇约占10%.
(1)乙醇充分燃烧的化学方程式为______.
(2)使用乙醇汽油的优点是______(写出一点即可) hdbadboy1年前1
hdbadboy1年前1 -
 雨凤 共回答了24个问题
雨凤 共回答了24个问题 |采纳率91.7%(1)乙醇充分燃烧生成了二氧化碳和水,化学方程式为:C 2 H 5 OH+30 2
点燃
.
2C0 2 +3H 2 0.
(2)使用乙醇汽油的优点是节约能源、环保等.
故答为:(1)C 2 H 5 OH+30 2
点燃
.
2C0 2 +3H 2 0,
(2)节约能源.1年前查看全部
- (2014•顺义区一模)乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少
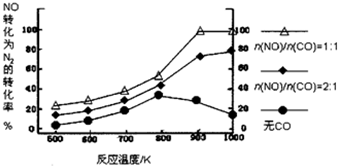 (2014•顺义区一模)乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放.但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题.
(2014•顺义区一模)乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放.但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题.
(1)NOx排入空气中,形成酸雨,造成空气污染.NOx中有一种红棕色气体,其溶于水的方程式是______.
(2)已知NO2和N2O4的结构式分别是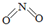 和
和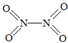 .
.
写出NO2转化N2O4的热化学方程式______.物质 NO2 N2O4 化学键 N=O N-N N=O 键能(kJ/mol) 466 167 438
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放.
①写出用CO还原NO生成N2的化学方程式______.
②在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和
比例变化情况如图.n(NO) n(CO)
为达到NO转化为N2的最佳转化率,应该选用的温度和
比例分别为______、______;该反应的△H______0(填“>”、“<”或“=”).n(NO) n(CO)
(4)用CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质.CH4与NO发生反应的化学方程式为______. fjzsj231年前1
fjzsj231年前1 -
 utopiadf 共回答了17个问题
utopiadf 共回答了17个问题 |采纳率100%解题思路:(1)二氧化氮是红棕色的气体,可以和水之间反应生成硝酸和一氧化氮;
(2)旧键的断裂吸收能量,新键的生成释放能量,根据吸收和释放能量的多少判断反应的吸放热,焓变值等于二者之间的能量差;
(3)①CO还原NO生成N2和二氧化碳,据此书写方程式;
②根据图象分析n(NO)/n(CO)=1时,在相同温度下氮气的转化率最高;n(NO)/n(CO)=1时,温度在900K左右氮气的转化率最高;
(4)CH4与NO发生反应生成的无毒物质是氮气、二氧化碳和水.(1)NOx中有只有二氧化氮是红棕色气体,可以和水之间反应生成硝酸和一氧化氮,其溶于水的方程式是3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
(2)NO2转化N2O4的过程中,旧键的断裂吸收能量为2×466kJ=932kJ,新键的生成释放能量为:167+438×4=1919kJ,该反应是放热的,放出的热量是1919kJ-932kJ=987kJ,所以2NO2(g)=N2O4(g),△H=-987kJ/mol,
故答案为:2NO2(g)=N2O4(g),△H=-987kJ/mol;
(3)①CO还原NO生成N2和二氧化碳,化学方程式为:2CO+2NO=N2+2CO2,
故答案为:2CO+2NO=N2+2CO2;
②根据图象分析n(NO)/n(CO)=1时,在相同温度下氮气的转化率最高;n(NO)/n(CO)=1时,温度在900K左右氮气的转化率最高,温度越高,氮气的转化率越大,所以平衡正向进行,该反应是吸热的,
故答案为:900K;1:1;>;
(4)CH4与NO发生反应生成的无毒物质是氮气、二氧化碳和水,化学方程式为:CH4+4NO=2N2+CO2+2H2O.
故答案为:CH4+4NO=2N2+CO2+2H2O.点评:
本题考点: 氮的氧化物的性质及其对环境的影响;化学平衡的影响因素;转化率随温度、压强的变化曲线.
考点点评: 本题涉及热化学、化学键键能和化学反应的焓变值间的关系以及化学平衡的移动等方面的知识,属于综合知识的考查,难度不大.1年前查看全部
- 附加题:车用乙醇汽油是将乙醇(C2H5OH)与汽油(以C8H18表示)按一定比例混合而成的一种汽车燃料.
附加题:车用乙醇汽油是将乙醇(C2H5OH)与汽油(以C8H18表示)按一定比例混合而成的一种汽车燃料.
(1)乙醇分子中,组成元素的原子个数比C:H:O为______.
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W.现测得反应前后各物质的质量如下:
①根据质量守恒定律,得出表中x的值为______;物质 乙醇 氧气 二氧化碳 水蒸气 W 反应前质量/g 23 40 0 0 0 反应后质量/g 0 0 22 27 x
②根据表中数据,可确定未知物W中各组成元素的质量比为______;
(3)通常可燃物中碳元素质量分数越高,燃烧产生W越多.则相同条件下,乙醇和汽油分别燃烧时,产生W较多的是______;为了使乙醇汽油燃烧过程中少产生W,应采取的措施是(任写一种)______. 李上松1年前1
李上松1年前1 -
 刷25 共回答了13个问题
刷25 共回答了13个问题 |采纳率100%解题思路:(1)由乙醇的化学式可以得到乙醇中各元素的原子个数比.
(2)①根据质量守恒定律中物质质量守恒可以计算出x的值;
②根据质量守恒定律中元素种类不变、元素质量不变可以计算出W的组成元素和元素质量比.
(3)汽油中碳元素的质量分数比乙醇中的大,因此,相同条件下分别燃烧汽油比乙醇生成较多的W;
可以通过增大氧气量(或提高乙醇在乙醇汽油中的比例等)等措施减少乙醇汽油燃烧过程中W的产生.(1)乙醇中碳、氢、氧的原子个数比为2:6:1
(2)①x的值为
23+40-22-27=14
②23g乙醇中碳、氢、氧三种元素的质量分别为
23g×[12×2/46]=12g、23g×[1×6/46]=3g、23g×[16/46]=8g
22g二氧化碳中碳、氧两种元素的质量分别为
22g×[12/44]=6g、22g×[16×2/44]=16g
27g水中氢、氧两种元素的质量分别为
27g×[1×2/18]=3g、27g×[16/18]=24g
12g-6g=6g,说明W中含有6g碳元素;
8g+40g-16g-24g=8g,说明W中含有8g氧元素.
因此W中碳、氧两种元素的质量比为
6g:8g=3:4
(3)汽油中碳元素的质量分数比乙醇中的大,因此,相同条件下分别燃烧汽油比乙醇生成较多的W;
可以通过增大氧气量(或提高乙醇在乙醇汽油中的比例等)等措施减少乙醇汽油燃烧过程中W的产生.点评:
本题考点: 根据化学反应方程式的计算;化学式的书写及意义;元素质量比的计算;化合物中某元素的质量计算;质量守恒定律及其应用;完全燃烧与不完全燃烧.
考点点评: 本题主要考查质量守恒定律和有关化学式的计算,难度较大.1年前查看全部
- 从2008年4月1日起,某市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C2H5OH)混合而成,其中乙醇约占10%.
从2008年4月1日起,某市开始使用车用乙醇汽油,乙醇汽油是由汽油和乙醇(C2H5OH)混合而成,其中乙醇约占10%.
(1)乙醇充分燃烧的化学方程式为C2H5OH+302
2C02+3H20点燃 .C2H5OH+302.
2C02+3H20点燃 .
(2)使用乙醇汽油的优点是______(写出一点即可) 褪了色的卡纸1年前1
褪了色的卡纸1年前1 -
 nihaoya8888 共回答了26个问题
nihaoya8888 共回答了26个问题 |采纳率96.2%解题思路:由反应物和生成物及反应条件根据质量守恒定律可以书写化学方程式;乙醇燃烧生成二氧化碳和水,不污染环境,节约能源.(1)乙醇充分燃烧生成了二氧化碳和水,化学方程式为:C2H5OH+302
点燃
.
2C02+3H20.
(2)使用乙醇汽油的优点是节约能源、环保等.
故答为:(1)C2H5OH+302
点燃
.
2C02+3H20,
(2)节约能源.点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了乙醇的相关知识,书写化学方程式时要先正确写出反应物和生成物的化学式,然后配平,注明反应条件.1年前查看全部
- 为了节省石油资源和有效地减少汽车尾气对环境的污染,我国正在逐步推广使用在汽油中加入适量乙醇作为汽车燃料(车用乙醇汽油).
为了节省石油资源和有效地减少汽车尾气对环境的污染,我国正在逐步推广使用在汽油中加入适量乙醇作为汽车燃料(车用乙醇汽油).乙醇的化学式是C2H5OH,在物质分类中属于 ______化合物(填“无机”或“有机”),乙醇中碳元素和氢元素的质量比是 ______,乙醇燃烧时生成二氧化碳和水,写出该反应的化学方程式C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2.
2CO2+3H2O点燃 . 靓女迷1年前1
靓女迷1年前1 -
 tryer2003 共回答了29个问题
tryer2003 共回答了29个问题 |采纳率89.7%解题思路:根据乙醇的化学式是C2H5OH,可以得知乙醇的组成元素,据此可判断物质是否属于有机物及计算出组成元素C、H的质量比;组成元素质量比为元素的相对原子质量与原子个数之积的比;
利用“乙醇燃烧时生成二氧化碳和水”的信息,用化学方程式表示反应.乙醇的化学式是C2H5OH,可以得知乙醇由C、H、O三种元素组成,为含C元素的化合物,属于有机物;
故答案为:有机物;
乙醇C2H5OH中C、H元素质量比=(12×2):(1×6)=4:1;
故答案为:4:1;
乙醇C2H5OH燃烧,即与氧气在点燃条件下生成二氧化碳和水;
故答案为:C2H5OH+3O2
点燃
.
2CO2+3H2O.点评:
本题考点: 有机物的特征、分类及聚合物的特性;元素质量比的计算.
考点点评: 化学式表示一种物质,表示该物质的元素组成;化学式表示构成物质的一个分子,表示物质的分子构成.1年前查看全部
- 为了节省石油资源和有效地减少汽车尾气对环境的污染,我国正在逐步推广使用在汽油中加入适量乙醇作为汽车燃料(车用乙醇汽油).
为了节省石油资源和有效地减少汽车尾气对环境的污染,我国正在逐步推广使用在汽油中加入适量乙醇作为汽车燃料(车用乙醇汽油).乙醇的化学式是C 2 H 5 OH,在物质分类中属于 ______化合物(填“无机”或“有机”),乙醇中碳元素和氢元素的质量比是 ______,乙醇燃烧时生成二氧化碳和水,写出该反应的化学方程式 ______.  lenovotea1年前1
lenovotea1年前1 -
 靓娇美qq 共回答了22个问题
靓娇美qq 共回答了22个问题 |采纳率100%乙醇的化学式是C 2 H 5 OH,可以得知乙醇由C、H、O三种元素组成,为含C元素的化合物,属于有机物;
故答案为:有机物;
乙醇C 2 H 5 OH中C、H元素质量比=(12×2):(1×6)=4:1;
故答案为:4:1;
乙醇C 2 H 5 OH燃烧,即与氧气在点燃条件下生成二氧化碳和水;
故答案为:C 2 H 5 OH+3O 2
点燃
.
2CO 2 +3H 2 O.1年前查看全部
- 车用乙醇汽油是在汽油中加入适量的乙醇而形成的混合燃料.使用这种汽油不但不影响汽车的行驶性能,而且可减少有害气体的排放,这
车用乙醇汽油是在汽油中加入适量的乙醇而形成的混合燃料.使用这种汽油不但不影响汽车的行驶性能,而且可减少有害气体的排放,这对解决***粮食转化,促进农业生产良性循环具有十分重要的意义.根据上述报道回答:
(1)乙醇能代替汽油作为燃料,是因为乙醇中含有______元素和______元素;
(2)燃烧乙醇比燃烧汽油减少了对大气的污染,这是因为乙醇中不含有______元素和______元素;
(3)乙醇主要是粮食中的淀粉等转化而成的,淀粉是绿色植物通过光合作用由水和二氧化碳两种物质转化而成的.植物光合作用可简单表示为:水+二氧化碳
淀粉+氧气.由此判断:淀粉中一定含有______元素和______元素.叶绿体 光  lj79_621年前1
lj79_621年前1 -
 fxx84 共回答了14个问题
fxx84 共回答了14个问题 |采纳率85.7%(1)乙醇能代替汽油作为燃料,是因为乙醇中含有碳元素和氢元素.
故填:碳;氢.
(2)因为乙醇中不含有硫元素和氮元素,燃烧时不能产生二氧化硫、氮氧化物,减少了对大气的污染.
故填:硫;氮.
(3)由水+二氧化碳
叶绿体
光 淀粉+氧气可知,水中的氢元素和二氧化碳中的碳元素转化到了淀粉中,所以淀粉中一定含有碳元素和氢元素,是否含有氧元素无法确定.
故填:碳;氢.1年前查看全部
- 生活中处处有化学,按要求填空:(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染.乙醇在空气中燃烧的化学方程式为C2H
生活中处处有化学,按要求填空:
(1)车用乙醇汽油可节省石油资源,减少汽车尾气的污染.乙醇在空气中燃烧的化学方程式为C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2.
2CO2+3H2O点燃 .
(2)用二氧化碳灭火器灭火的原理是______.
(3)把煤做成蜂窝煤状就有利于燃烧,其原因是______. 02ah1年前1
02ah1年前1 -
 weidongben 共回答了21个问题
weidongben 共回答了21个问题 |采纳率100%解题思路:(1)根据乙醇燃烧生成二氧化碳和水分析.
(2)可燃物燃烧的条件是:与空气接触、达到着火点、本身可燃,缺一不可燃燃烧,控制其中一个或二个条件就可灭火.
(3)煤做成蜂窝状增大了煤与氧气的接触面积.(1)乙醇燃烧生成二氧化碳和水,故答案:C2H5OH+3O2
点燃
.
2CO2+3H2O;
(2)二氧化碳灭火器灭火的原理是在常温下用压缩体积的办法使二氧化碳气体液化装入钢瓶里的,液态二氧化碳在常温下会迅速汽化,并吸收大量的热.所以灭火故答案为:隔绝氧气并降温到着火点以下.
(3)增大氧气的浓度或增大可燃物与氧气的接触面积可以促进燃料的燃烧,把块煤做成蜂窝煤是为了增大煤与氧气的接触面积,从而促进煤的燃烧.
答案:
(1)C2H5OH+3O2
点燃
.
2CO2+3H2O
(2)隔绝空气并降低可燃物的温度至着火点以下
(3)增大与空气的接触面积点评:
本题考点: 常用燃料的使用与其对环境的影响;书写化学方程式、文字表达式、电离方程式;完全燃烧与不完全燃烧;几种常用的灭火器.
考点点评: 本题考查了当今的能源问题的知识侧重基础,解题时一定要注意审题要仔细,细节决定成败,细心是必须的,仔细审题是正确解答问题的关键.1年前查看全部
大家在问
- 1经度与距离是不是用111*cos&.&指纬度距离.这算出来是纬度1度的长度
- 2仿写句子!1.童年是一幅五彩缤纷的画,描绘着金色的梦想:童年是__________________,__________
- 3《月光启蒙》为什么题目叫“月光启蒙”
- 4已知A=3x,B是一个多项式,小马虎在计算B+A时,误把B+A看成了B乘A,结果得到x的平方+3分
- 5一个数除以“0”,这个算式就等于“0”.______.(判断对错)
- 6氯化铜溶液的颜色.有CuCl3这种物质吗?
- 7大正方形边长为a,小正方形边长为b,求阴影部分的面积,当知道a为8时,b为4时,阴影部分的面积是多少? 急求!
- 8什么物质可以吸收氢气,一氧化碳?分别用什么装置?
- 9将下列句子按顺序排列.A.GreatB.Now,where are my keys?C.OK.And where's m
- 10山东教育出版社英语八年级下册单词表 1.2单元就可以.
- 11乌鸦的叫声怎么形容
- 121.《走一步,再走一步》文中最生动细腻,几乎贯穿整个故事的,是对“我”的哪个方面的描写?
- 13英语高手求翻译工英语帮我翻译一下下面4句.我们应该少用电子产品.电子产品对人有影响.我们应该合理利用电子产品.现在我们无
- 14There wii be an English party tonight 改同义句
- 15阅读下面文言文,完成1-4题。 甘罗