偏二甲肼是火箭推进器的常用燃料,根据偏二甲肼的化学式C2H8N2,你知道哪些信息?请至少写出三点.
 liyongxiaohu2022-10-04 11:39:541条回答
liyongxiaohu2022-10-04 11:39:541条回答C2
2是右下角的下标H8也一样

已提交,审核后显示!提交回复
共1条回复
 朝闻游子 共回答了19个问题
朝闻游子 共回答了19个问题 |采纳率94.7%- 是有机物,
是碳氢化合物的衍生物
燃烧后可生成NO2,CO2,H2O
有氨基
这是04年左右的高考原题,具体的我忘了 - 1年前
相关推荐
- 2010年10月1日18时59分57秒,“嫦娥二号”卫星发射升空.嫦娥二号用的火箭它的一子级和二子级使用偏二甲肼和N2O
 2010年10月1日18时59分57秒,“嫦娥二号”卫星发射升空.嫦娥二号用的火箭它的一子级和二子级使用偏二甲肼和N2O4作为推进剂,反应式为(CH3)2NNH2+2N2O4=2CO2+4H2O+3N2,三子级则使用效能更高的液氢(H2)和液氧(O2).下列说法正确的( )
2010年10月1日18时59分57秒,“嫦娥二号”卫星发射升空.嫦娥二号用的火箭它的一子级和二子级使用偏二甲肼和N2O4作为推进剂,反应式为(CH3)2NNH2+2N2O4=2CO2+4H2O+3N2,三子级则使用效能更高的液氢(H2)和液氧(O2).下列说法正确的( )
A.N2O4在反应中被氧化
B.反应中1molN2O4得到4mole-
C.(CH3)2NNH2具有还原性
D.液氢与液氧的反应中转移的电子数为2NA 藤皋惠介1年前1
藤皋惠介1年前1 -
 wusula 共回答了15个问题
wusula 共回答了15个问题 |采纳率73.3%解题思路:(CH3)2NNH2中,C元素化合价为-2价,N元素化合价为-2价,N2O4中N元素化合价为+4价,反应(CH3)2NNH2+2N2O4=2CO2+4H2O+3N2中,C元素化合价由-2价升高到+4价,N元素化合价既升高又降低,反应中N2O4为氧化剂,(CH3)2NNH2为还原剂,以此解答该题.A.N2O4在反应中N元素化合价降低,得电子,被还原,故A错误;
B.反应中N元素化合价由+4价降低到0价,1molN2O4得到8mole-,故B错误;
C.(CH3)2NNH2中,C元素化合价为-2价,N元素化合价为-2价,反应中C元素化合价由-2价升高到+4价,N元素化合价由-2价升高高0价,表现为还原性,故C正确;
D.液氢与液氧的反应中,因反应物的物质的量未知,则转移的电子的物质的量不能确定,故D错误.
故选C.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握题给信息,明确元素的化合价为解答该题的关键,难度中等.1年前查看全部
- 发射“嫦娥二号”的长三丙火箭由三个子级构成,其中一子级上部装有液体四氧化二氮(N2O4).下部装有液体偏二甲肼(C2H8
发射“嫦娥二号”的长三丙火箭由三个子级构成,其中一子级上部装有液体四氧化二氮(N2O4).下部装有液体偏二甲肼(C2H8N2).发动机内燃烧的化学方程式为:C2H8N2+2N2O4→3N2+2CO2+4H2O.该反应中( )
A.C2H8N2发生还原反应
B.C2H8N2是氧化剂
C.N2O4发生氧化反应
D.N2O4是氧化剂 liyf1121年前1
liyf1121年前1 -
 abbyxiao 共回答了12个问题
abbyxiao 共回答了12个问题 |采纳率83.3%解题思路:根据燃烧的化学方程式为C2H8N2+2N2O4→3N2+2CO2+4H2O,利用元素的化合价变化来分析氧化剂和还原剂,若反应物中某元素的化合价升高,则该物质为还原剂,还原剂在反应中发生氧化反应.偏二甲肼的化学式为C2H8N2,H为+1价,C为-1价,N为-3价,
则反应C2H8N2+2N2O4→3N2+2CO2+4H2O中,
C2H8N2中N元素的化合价和C元素的化合价升高,N2O4中N元素的化合价降低,
则C2H8N2作还原剂,发生氧化反应;N2O4作氧化剂,发生还原反应;
故选:D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应反应中氧化剂、还原剂的判断及氧化反应、还原反应,明确元素的化合价即可解答,本题难点在于分析偏二甲肼(C2H8N2)元素的化合价.1年前查看全部
- 偏二甲肼的是一种火箭燃料,它是由碳、氮、氢三种元素组成,其结构式如图.请按下列要求答题.
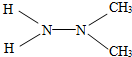 偏二甲肼的是一种火箭燃料,它是由碳、氮、氢三种元素组成,其结构式如图.请按下列要求答题.
偏二甲肼的是一种火箭燃料,它是由碳、氮、氢三种元素组成,其结构式如图.请按下列要求答题.
(1)根据苷胺酸的化学式C2H5NO2的形式,写出偏二甲肼的化学式;
(2)求其相对分子量;
(3)求偏二甲肼中碳、氮、氢三种元素的质量比;
(4)求偏二甲肼中氮元素的质量分数. 脑袋忘在家1年前1
脑袋忘在家1年前1 -
 茅山剑客 共回答了17个问题
茅山剑客 共回答了17个问题 |采纳率82.4%解题思路:(1)根据苷胺酸的化学式C2H5NO2的形式,写出偏二甲肼的化学式.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数=[相对原子质量×原子个数/相对分子质量]×100%,进行分析解答.(1)根据苷胺酸的化学式C2H5NO2的形式,可知偏二甲肼的化学式为:C2N2H8;
(2)偏二甲肼的相对分子质量=12×2+14×2+1×8=60;
(3)偏二甲肼中碳、氮、氢三种元素的质量比=(12×2):(14×2):(1×8)=6:7:2;
(4)偏二甲肼中氮元素的质量分数=[14×2/12×2+14×2+1×8]×100%=35%.
故答案为:(1)C2N2H8;(2)60;(3)6:7:2;(4)35%.点评:
本题考点: 化学式的书写及意义;相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.1年前查看全部
- 一个化学问题偏二甲肼(C2H8N2)在点燃条件下与四氧化二氮(N2O4)反应,需不需要氧气?
 leo8503161年前3
leo8503161年前3 -
 v恍若隔世v 共回答了20个问题
v恍若隔世v 共回答了20个问题 |采纳率90%需要氧气.C2H8N2+N2O4+2O2====2CO2+4H2O+2N21年前查看全部
- 天旱时,可用单级小火箭发射碘化银进行人工降雨.小火箭使用的主要燃料名叫“偏二甲肼”.现取3.0g偏二甲肼在O2中充分燃烧
天旱时,可用单级小火箭发射碘化银进行人工降雨.小火箭使用的主要燃料名叫“偏二甲肼”.现取3.0g偏二甲肼在O2中充分燃烧后生成4.4gCO2、3.6gH2O和1.4gN2三种物质,由此可知偏二甲肼由______种元素组成,其中碳元素的质量分数为______.偏二甲肼的相对分子质量为60,则其化学式为______.
 不专一1年前1
不专一1年前1 -
 完美地体现了她 共回答了21个问题
完美地体现了她 共回答了21个问题 |采纳率95.2%解题思路:①根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据偏二甲肼在O2中充分燃烧后生成物质所含有的元素的质量,即可推断出偏二甲肼所含有的元素;
②根据二氧化碳的质量和二氧化碳中碳元素的质量分数,就可计算出偏二甲肼中碳的质量,再根据“[偏二甲肼中碳的质量/偏二甲肼的质量]×100%”计算即可;
③根据偏二甲肼中各元素的质量比得出C、H、N元素的原子个数比,结合偏二甲肼的相对分子质量为60,进而得出偏二甲肼中C、H、N元素的原子个数,即可写出化学式.①偏二甲肼中碳元素的质量为:4.4g×[12/44]=1.2g;偏二甲肼中H元素的质量为:3.6g×[2/18]=0.4g;偏二甲肼中N元素的质量为:1.4g;偏二甲肼中氧元素的质量为:3.0g-1.2g-0.4g-1.4g=0;故偏二甲肼由C、H、N三种元素组成;
②偏二甲肼中碳元素的质量分数为:[1.2g/3.0g]×100%=40%;
③偏二甲肼中C、H、N元素的质量比为;1.2g:0.4g:1.4g=12:4:14,则C、H、N元素的原子个数比为1:4:1;又因为偏二甲肼的相对分子质量为60,则偏二甲肼中C的个数为2,H的个数为8,N的个数为2,那么,其化学式为:C2H8N2.
故答案为:三,40%,C2H8N2.点评:
本题考点: 质量守恒定律及其应用;元素的质量分数计算;有关化学式的计算和推断.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 2014年12月2日“嫦娥三号”成功发射.其运载火箭的常规燃料是四氧化二氮(N2O4)和偏二甲肼(C2H8N2),飞船的
2014年12月2日“嫦娥三号”成功发射.其运载火箭的常规燃料是四氧化二氮(N2O4)和偏二甲肼(C2H8N2),飞船的低温燃料是液氧和液氢.下列有关说法不正确的是( )
A.N2O4属于氧化物
B.C2H8N2属于有机物
C.液氢作燃料时发生反应为2H2+O2
2H2O点燃 .
D.液氧变成氧气的过程属于化学变化 laughlast1年前1
laughlast1年前1 -
 颜色问题 共回答了17个问题
颜色问题 共回答了17个问题 |采纳率94.1%解题思路:A、根据氧化物的概念进行分析判断.
B、根据有机物的含义进行分析判断.
C、根据方程式书写方法进行分析.
D、根据化学变化的概念进行分析判断.A、N2O4是由两种元素组成,且含有氧的化合物,属于氧化物,故选项说法正确.
B、C2H8N2是含有碳元素的化合物,属于有机物,故选项说法正确.
C、液氢作燃料时发生反应为2H2+O2
点燃
.
2H2O,故选项说法正确.
D、液氧变成氧气的过程没有新物质生成,属于物理变化,故选项说法错误.
故选:D.点评:
本题考点: 从组成上识别氧化物;有机物与无机物的区别;化学变化和物理变化的判别;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义进行分析问题、解决问题的能力.1年前查看全部
- 偏二甲肼与氧气反应化学方程式
 潇洒哥龙1年前3
潇洒哥龙1年前3 -
 苏州那些事 共回答了25个问题
苏州那些事 共回答了25个问题 |采纳率96%C2N2H8+4O2=(等号上写点燃)2CO2+4H2O+N21年前查看全部
- 关于可变化合价的知识在一些常见的化学物质中,如高锰酸钾、过氧化钠、次氯酸、偏二甲肼中,前面的“高”“过”“次”“偏”是否
关于可变化合价的知识
在一些常见的化学物质中,如高锰酸钾、过氧化钠、次氯酸、偏二甲肼中,前面的“高”“过”“次”“偏”是否是元素可变化合价的表示方式?
是不是可变化合价中每种不同的化合价都能用不同的汉字表示?(如高锰酸钾中的“高”代表的是锰的最高化合价+7)
那一共有多少种前缀?怎样标注?请以不同化合价的氯元素的氧化物的水化物举例说明, 缘定今生52571年前1
缘定今生52571年前1 -
 今天的小鱼 共回答了19个问题
今天的小鱼 共回答了19个问题 |采纳率94.7%高,一般指元素的最高价化合物
过,一般是由于同种元素原子构成双原子或多原子原子团,计算化合价时,一般把原子团的化合价平分到每个原子上来考虑,所以表面上甚至会出现几分之几这种价态.
亚,比一般化合价低,而“次”比“亚”更低.
偏,正,异……是有机物表示同分异构体结构的方法,与化合价无关.有机物一般不讲化合价而讲结构,因为有机物中化合价对于实际问题没什么意义1年前查看全部
- 嫦娥一号在飞行过程中用偏二甲肼(化学式为C2H8N2)作燃料,四氧化二氮(N2O4)作为助燃剂,其反应会生成三种地球大气
嫦娥一号在飞行过程中用偏二甲肼(化学式为C2H8N2)作燃料,四氧化二氮(N2O4)作为助燃剂,其反应会生成三种地球大气中存在的没有污染的气体,则其反应的方程式是:C2H8N2+2N2O4
3N2+2CO2+4H2O点燃 .C2H8N2+2N2O4.
3N2+2CO2+4H2O点燃 . tnqb1年前1
tnqb1年前1 -
 hzmato 共回答了21个问题
hzmato 共回答了21个问题 |采纳率85.7%解题思路:根据题中的叙述找出反应物、生成物,然后依据方程式的书写规则进行书写.偏二甲肼和四氧化二氮在点燃的条件下生成氮气、水和二氧化碳,故答案为:C2H8N2+2N2O4
点燃
.
3N2+2CO2+4H2O;点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;空气的成分及各成分的体积分数.
考点点评: 在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.1年前查看全部
- 偏二甲肼(C2H8N2)是“嫦娥一号”运载火箭发动机推进剂之一. 下列关于偏二甲肼的说法正确的是( )
偏二甲肼(C2H8N2)是“嫦娥一号”运载火箭发动机推进剂之一. 下列关于偏二甲肼的说法正确的是( )
A. 偏二甲肼分子中含有氮气分子
B. 偏二甲肼由碳、氢、氮三种元素组成
C. 偏二甲肼中碳、氢、氮各元素的质量比为12:1:14
D. 一个偏二甲肼分子由1个碳原子、4个氢原子和1个氮原子构成 ncyd1191年前1
ncyd1191年前1 -
 wtwolf 共回答了28个问题
wtwolf 共回答了28个问题 |采纳率92.9%解题思路:A、根据纯净物中只含有一种分子进行解答;
B、根据偏二甲肼的化学式 C2H8N2 进行分析其元素组成;
C、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
D、根据标在元素符号右下角的数字表示一个分子中所含原子的个数,进行解答.A、偏二甲肼为纯净物,里面只含有偏二甲肼分子,不含其它分子,故A错误;
B、根据偏二甲肼的化学式 C2H8N2 可知偏二甲肼由C,H,N三种元素组成;故B正确;
C、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,所以偏二甲肼中碳、氢、氮各元素的质量比为:12×2:8:14×2=6:2:7;故C错误;
D、根据标在元素符号右下角的数字表示一个分子中所含原子的个数,所以一个偏二甲肼分子由2个碳原子、8个氢原子和2个氮原子构成,;故D错误;
故选B.点评:
本题考点: 元素质量比的计算;分子和原子的区别和联系;物质的元素组成.
考点点评: 本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系在解题中应用.1年前查看全部
- (2014•金牛区模拟)运载“玉兔号”月球车的火箭使用的是偏二甲肼(C2H8N2)作燃料,下列说法不正确的是( )
(2014•金牛区模拟)运载“玉兔号”月球车的火箭使用的是偏二甲肼(C2H8N2)作燃料,下列说法不正确的是( )
A.偏二甲肼由碳、氢、氮三种元素组成
B.偏二甲肼的相对分子质量为60
C.偏二甲肼中碳、氢、氮元素质量比2:8:2
D.偏二甲肼中碳元素的质量分数为25% 玉火粉身1年前0
玉火粉身1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 2013年6月11日,“神舟十号”在酒泉发射升空,并取得圆满成功.“神舟十号”的运载火箭所用燃料是偏二甲肼(C2H8N2
2013年6月11日,“神舟十号”在酒泉发射升空,并取得圆满成功.“神舟十号”的运载火箭所用燃料是偏二甲肼(C2H8N2)和四氧化二氮(N2O4).在火箭升空过程中,燃料发生反应:C2H8N2+2N2O4→2CO2+3N2+4H2O提供能量.下列有关叙述正确的是( )
A.该燃料绿色环保,在燃烧过程中不会造成任何环境污染
B.该反应中只是氮元素之间的氧化还原反应,偏二甲肼是氧化剂
C.N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物
D.每有0.6mol N2生成,转移电子数目为3.2NA kkmbl1年前1
kkmbl1年前1 -
 BBT_海鸥 共回答了17个问题
BBT_海鸥 共回答了17个问题 |采纳率88.2%解题思路:C2H8N2中C元素化合价为-1价,N为-3价,N2O4中N元素化合价为+4价,反应C2H8N2+2N2O4→2CO2+3N2+4H2O中,C元素化合价由-1价升高到+4价,N元素化合价分别由-3价、+4价变为0价,以此解答该题.A.四氧化二氮可污染环境,故A错误;
B.反应中C元素化合价由-1价升高到+4价,故B错误;
C.C元素化合价升高,则CO2为氧化产物,故C错误;
D.由方程式可知,每有0.6mol N2生成,则消耗0.4molN2O4,则转移电子的物质的量为0.4mol×4×2=3.2mol,则每有0.6mol N2生成,转移电子数目为3.2NA,故D正确.
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意元素化合价的判断,为解答该题的关键,从元素化合价的角度解答该类题目,难度不大.1年前查看全部
- (2013•昆明)2013年6月11日,“神舟十号”成功发射.运载“神舟十号”飞船的火箭使用偏二甲肼(C2H8N2)作燃
(2013•昆明)2013年6月11日,“神舟十号”成功发射.运载“神舟十号”飞船的火箭使用偏二甲肼(C2H8N2)作燃料,下列说法正确的是( )
A.偏二甲肼由碳、氢、氮三种元素组成
B.偏二甲肼的相对分子质量为58
C.偏二甲肼中碳、氢、氮元素质量比2:8:2
D.偏二甲肼中碳元素的质量分数为50% 娃哈哈iad1年前0
娃哈哈iad1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 偏二甲肼是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.
偏二甲肼是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.
它是一种含C、H、N的化合物,其摩尔质量为60g/mol.其中所含碳元素的质量分数为40%;所含氢元素的质量分数为13.3%;其余为N
(1)30kg偏二甲肼的物质的量为:
(2)C、H、N三种元素的原子个数比为:
(3)偏二甲肼的分子式为: 冷余11年前1
冷余11年前1 -
 nb903 共回答了18个问题
nb903 共回答了18个问题 |采纳率88.9%C的个数=40%*60/12=2
H的个数=13.3%*60/1=8
根据摩尔质量,得出N的个数 C2H8Nx 24+8+14x=60 x=2
(1)30000/60=500mol
(2)1:4:1
(3)C2H8N21年前查看全部
- (2014•河西区一模)2013年6约11日,“神舟十号”成功发射,运载“神舟十号”飞船的火箭使用偏二甲肼(C2H8N2
(2014•河西区一模)2013年6约11日,“神舟十号”成功发射,运载“神舟十号”飞船的火箭使用偏二甲肼(C2H8N2)作燃料.
(1)偏二甲肼中碳、氢、氮元素质量比为______.
(2)300kg偏二甲肼中含有氢元素的质量为______kg. zhangyong1631年前1
zhangyong1631年前1 -
 把它涂黑 共回答了12个问题
把它涂黑 共回答了12个问题 |采纳率83.3%解题思路:(1)偏二甲肼中各元素(C、H、N)的质量比=(碳的相对原子质量×碳原子个数):(氢的相对原子质量×氢原子个数):(氮的相对原子质量×氮原子个数);
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.(1)偏二甲肼中各元素(C、H、N)的质量比=(12×2):(1×8):(14×2)=24:8:28=6:2:7;
(2)300kg的偏二甲肼含氮元素的质量为300kg×[1×8/12×2+1×8+14×2]×100%=40kg.
故答案为:(1)6:2:7;(2)40.点评:
本题考点: 元素质量比的计算;化合物中某元素的质量计算.
考点点评: 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.1年前查看全部
- 2010年10月1日,我国成功发射“嫦娥二号”卫星,嫦娥二号卫星由长征三号火箭承载发射.火箭燃料为偏二甲肼(C 2 H
2010年10月1日,我国成功发射“嫦娥二号”卫星,嫦娥二号卫星由长征三号火箭承载发射.火箭燃料为偏二甲肼(C 2 H 8 N 2 ),它是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是( ) A.偏二甲肼(C 2 H 8 N 2 )的摩尔质量为60 B.6.02×10 23 个偏二甲肼(C 2 H 8 N 2 )分子的质量约为60g C.1mol偏二甲肼(C 2 H 8 N 2 )的质量为60g/mol D.60g偏二甲肼(C 2 H 8 N 2 )中含有N A 个氮原子  网虫1231年前1
网虫1231年前1 -
 受伤的刀 共回答了27个问题
受伤的刀 共回答了27个问题 |采纳率77.8%A、偏二甲肼(C 2 H 8 N 2 )的摩尔质量为60g/mol,相对分子质量为60,故A错误;
B、6.02×10 23 个偏二甲肼的物质的量为1mol,质量为1mol×60g/mol=60g,故B错误;
C、1mol偏二甲肼(C 2 H 8 N 2 )的质量为60g,60g/mol是偏二甲肼的摩尔质量,故C错误;
D、60g偏二甲肼(C 2 H 8 N 2 )的物质的量为
60g
60g/mol =1mol,每个偏二甲肼(C 2 H 8 N 2 )分子中含有2个氮原子,所以含有氮原子数目为1mol×2×N A mol -1 =2N A ,故D正确.
故选:D.1年前查看全部
- 火箭 偏二甲肼与四氧化二氮燃烧要不要加氧气
火箭 偏二甲肼与四氧化二氮燃烧要不要加氧气
我要详细回答 不少了 产物是氮气和二氧化碳!没有水吗 土豆5241年前3
土豆5241年前3 -
 与云一起飞翔 共回答了18个问题
与云一起飞翔 共回答了18个问题 |采纳率88.9%2N2H4+N2O4=3N2+4H2O 这是一个氧化还原反应 N2H4中N是-2价 N2O4中N是+4价 然后2mol的N2H4中游4mol的-2价N氧化成了0价的N ,N2O4中2mol+4价的N被还原成0价 这样就已经平衡了 所以就不需要再加入氧气了1年前查看全部
- (2002•济南)天旱时,可用单级小火箭发射碘化银进行人工降雨.小火箭使用的主要燃料名叫“偏二甲肼”.现取3.0g偏二甲
(2002•济南)天旱时,可用单级小火箭发射碘化银进行人工降雨.小火箭使用的主要燃料名叫“偏二甲肼”.现取3.0g偏二甲肼在O2中充分燃烧后生成4.4gCO2、3.6gH2O和1.4gN2三种物质,由此可知偏二甲肼由______种元素组成,其中碳元素的质量分数为______.偏二甲肼的相对分子质量为60,则其化学式为______.
 fgwh1年前1
fgwh1年前1 -
 guangvicky 共回答了27个问题
guangvicky 共回答了27个问题 |采纳率92.6%解题思路:①根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据偏二甲肼在O2中充分燃烧后生成物质所含有的元素的质量,即可推断出偏二甲肼所含有的元素;
②根据二氧化碳的质量和二氧化碳中碳元素的质量分数,就可计算出偏二甲肼中碳的质量,再根据“[偏二甲肼中碳的质量/偏二甲肼的质量]×100%”计算即可;
③根据偏二甲肼中各元素的质量比得出C、H、N元素的原子个数比,结合偏二甲肼的相对分子质量为60,进而得出偏二甲肼中C、H、N元素的原子个数,即可写出化学式.①偏二甲肼中碳元素的质量为:4.4g×[12/44]=1.2g;偏二甲肼中H元素的质量为:3.6g×[2/18]=0.4g;偏二甲肼中N元素的质量为:1.4g;偏二甲肼中氧元素的质量为:3.0g-1.2g-0.4g-1.4g=0;故偏二甲肼由C、H、N三种元素组成;
②偏二甲肼中碳元素的质量分数为:[1.2g/3.0g]×100%=40%;
③偏二甲肼中C、H、N元素的质量比为;1.2g:0.4g:1.4g=12:4:14,则C、H、N元素的原子个数比为1:4:1;又因为偏二甲肼的相对分子质量为60,则偏二甲肼中C的个数为2,H的个数为8,N的个数为2,那么,其化学式为:C2H8N2.
故答案为:三,40%,C2H8N2.点评:
本题考点: 质量守恒定律及其应用;元素的质量分数计算;有关化学式的计算和推断.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 偏二甲肼是火箭推进器的常用燃料,根据偏二甲肼的化学式,写出3点信息.
 dzdz3331年前1
dzdz3331年前1 -
 脸色单纯 共回答了15个问题
脸色单纯 共回答了15个问题 |采纳率93.3%楼主你漏写了偏二甲肼的化学式.
偏二甲肼的化学式是C2H8N2.
根据为个化学式可得的信息是:
1.是有机物;
2.其组成中含有碳、氢、氮三种元素;
3.每个偏二甲肼分子含有2个碳原子、8个氢原子、2个氮原子;
4.燃烧后可生成N2,CO2,H2O1年前查看全部
- (2011•张掖)发射“嫦娥一号”的长三甲火箭燃料是偏二甲肼(x),氧化剂是四氧化二氮(N2O4),反应的化学方程式为X
(2011•张掖)发射“嫦娥一号”的长三甲火箭燃料是偏二甲肼(x),氧化剂是四氧化二氮(N2O4),反应的化学方程式为X+2N2O4═3N2+2CO2+4H2O,则X的化学式为( )
A. H2
B. CH4
C. C2H8N
D. C2H8N2 wylovermb1年前3
wylovermb1年前3 -
 缘来缘去缘未了 共回答了15个问题
缘来缘去缘未了 共回答了15个问题 |采纳率86.7%解题思路:本题根据反应的化学方程式为X+2N2O4═3N2+2CO2+4H2O,利用质量守恒定律来确定X的化学式.根据质量守恒定律,化学反应前后原子的种类、数目不变,
由化学方程式为X+2N2O4═3N2+2CO2+4H2O可知,
该反应中,反应物中含有4个N,8个O;生成物中已有6个N,2个C,8个O和8个H,还差2个N,2个C,8个H在X中,
则X的化学式为C2H8N2.
故选:D.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题考查利用化学方程式来确定物质的化学式,学生应灵活运用质量守恒定律,理解质量守恒定律中的元素守恒、原子守恒在解题中的重要作用.1年前查看全部
- (2009•徐汇区二模)火箭燃料偏二甲肼(C2H8N2)与四氧化二氮(N2O4)反应的化学方程式为:C2H8N2+2N2
(2009•徐汇区二模)火箭燃料偏二甲肼(C2H8N2)与四氧化二氮(N2O4)反应的化学方程式为:C2H8N2+2N2O4→3N2+2CO2+4R,则R的化学式为______,其中氧化剂的化学式为______.
 赤脚跑海南1年前1
赤脚跑海南1年前1 -
 nn难测 共回答了24个问题
nn难测 共回答了24个问题 |采纳率83.3%解题思路:根据质量守恒定律可知,反应前后元素的种类、原子种类、原子个数不变,然后分别算出各类原子的个数即可得到答案.氧化剂是指元素的化合价降低的物质.根据质量守恒定律可知,反应前后元素的种类、原子种类、原子个数不变.反应前碳原子是2个,氢原子是8个、氮原子是6个、氧原子是8个;反应后氮原子是6个、碳原子是2个、氧原子是4个.反应前后相差数目是:氢原子是8个...
点评:
本题考点: 有关化学式的计算和推断;氧化反应.
考点点评: 学会利用质量守恒定律计算某种物质的化学式,即反应前后原子的种类、原子个数均不变,;理解氧化剂的概念并会判断谁是氧化剂.1年前查看全部
- 火箭燃料偏二甲肼(C 2 H 8 N 2 )与四氧化二氮(N 2 O 4 )反应的化学方程式为:C 2 H 8 N 2
火箭燃料偏二甲肼(C 2 H 8 N 2 )与四氧化二氮(N 2 O 4 )反应的化学方程式为:C 2 H 8 N 2 +2N 2 O 4 →3N 2 +2CO 2 +4R,则R的化学式为______,其中氧化剂的化学式为______.  xdx20091年前1
xdx20091年前1 -
 Graceheart 共回答了22个问题
Graceheart 共回答了22个问题 |采纳率95.5%根据质量守恒定律可知,反应前后元素的种类、原子种类、原子个数不变.反应前碳原子是2个,氢原子是8个、氮原子是6个、氧原子是8个;反应后氮原子是6个、碳原子是2个、氧原子是4个.反应前后相差数目是:氢原子是8个、氧原子是4个,因为R的系数是4,所以一个R分子有两个氢原子和一个氧原子,即R是水.N 2 O 4 中N元素的化合价是+4价,N 2 中N元素的化合价是0价,因此N元素的化合价是降低的,即N 2 O 4 是氧化剂.
故答案为:H 2 O,N 2 O 4 .1年前查看全部
- 在火箭发射时,偏二甲肼和四氧化二氮发生剧烈反应,释放出大量热,并产生大量氮气,二氧化碳和水蒸气.写出该反应的化学式.
 saycloudy1年前3
saycloudy1年前3 -
 yejiao 共回答了13个问题
yejiao 共回答了13个问题 |采纳率84.6%2N2H4+N2O4=3N2+4H2O
这行吗1年前查看全部
- 偏二甲肼与四氧化二氮反应 四氧化二氮是氧化剂还是还原剂
 at2301年前1
at2301年前1 -
 65ngf76laiqian 共回答了16个问题
65ngf76laiqian 共回答了16个问题 |采纳率87.5%根据C2H8N2 + 2N2O4=2CO2↑ + 4H2O + 3N2↑
如果没记错的话..偏二甲肼中的N应该是-2价的,四氧化二氮中的N应该是+4价的
那么可以看出,四氧化二氮是氧化剂,偏二甲肼是还原剂
纯手打..1年前查看全部
- (2004•上海)偏二甲肼(C2H8N2)是运载飞船的火箭所使用的燃料之一,该燃料发生反应的化学方程式为:C2H8N2+
(2004•上海)偏二甲肼(C2H8N2)是运载飞船的火箭所使用的燃料之一,该燃料发生反应的化学方程式为:C2H8N2+4O2
N2+2X+4H2O,其中X为______(填化学式).点燃 . 梦里发呆1年前1
梦里发呆1年前1 -
 何捷辉 共回答了18个问题
何捷辉 共回答了18个问题 |采纳率88.9%解题思路:根据化学变化前后原子的种类、数目不变,由反应的化学方程式C2H8N2+4O2
N2+2X+4H2O,推断反应中生成X的分子构成,然后确定X物质的化学式.点燃 .由反应的化学方程式C2H8N2+4O2
点燃
.
N2+2X+4H2O,可知:
反应前 反应后
C原子 2 0
H原子 8 8
N原子 2 2
O原子 8 4
根据化学变化前后原子的种类、数目不变,可判断2个X分子中含有2个C原子和4个O原子,则每个X分子由1个C原子、2个O原子构成,物质X的化学式为CO2;
故答案为:CO2.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.1年前查看全部
- 偏二甲肼(C 2 H 8 N 2 )是神州八号火箭发动机燃料,燃烧时氧化剂是四氧化二氮,反应的化学方程式为C 2 H 8
偏二甲肼(C 2 H 8 N 2 )是神州八号火箭发动机燃料,燃烧时氧化剂是四氧化二氮,反应的化学方程式为C 2 H 8 N 2 +2N 2 O 4
2CO 2 ↑+4X+3N 2 ↑,下列有关说法正确的是( )点燃 . A.偏二甲肼分子中含有氮气分子 B.偏二甲肼由2个碳原子、8个氢原子和2个氮原子构成 C.偏二甲肼中碳、氢、氮各元素的质量比为1:4:1 D.X的化学式为H 2 O  loloyou1年前1
loloyou1年前1 -
 chxtcs 共回答了13个问题
chxtcs 共回答了13个问题 |采纳率92.3%A、化学式中元素符号右下角的数字表示一个分子中含有该元素原子的个数,一个偏二甲肼分子中含有2个氮原子,故A错误;
B、一个偏二甲肼分子由2个碳原子、8个氢原子和2个氮原子构成的,故B错误;
C、偏二甲肼中碳、氢、氮各元素的质量比为:(12×2):(1×8):(14×2)=6:2:7,故C错误;
D、由反应的方程式,根据质量守恒定律反应前后原子的种类、数目不变,可推出X的化学式为H 2 O,故D正确.
故选D.1年前查看全部
- 承担神舟七号飞船发射任务的长征二号F运载火箭,使用液态四氧化二氮(N2O4)和偏二甲肼(C2H8N2)作为推进剂.
承担神舟七号飞船发射任务的长征二号F运载火箭,使用液态四氧化二氮(N2O4)和偏二甲肼(C2H8N2)作为推进剂.
(1)N2O4中的氮元素的化合价是______价.四氧化二氮常温下就能转化成二氧化氮(NO2),NO2与N2O4比较,不同点是______.
A.氮元素的化合价 B.分子中原子的个数
C.物质中氮元素的质量分数D.组成元素
(2)四氧化二氮与偏二甲肼的反应为:C2H8N2+2N2O4=2CO2↑+3R↑+4H2O↑,R的化学式为______. kkkk阵线1年前1
kkkk阵线1年前1 -
 yunrs 共回答了23个问题
yunrs 共回答了23个问题 |采纳率91.3%解题思路:(1)根据化合物中各元素的化合价代数和为0,利用物质的化学式N2O4,计算其中N元素的化合价;利用两物质的化学式NO2与N2O4,分别计算氮元素的化合价、氮元素的质量分数及相对分子质量,判断组成元素与分子中原子的个数;选出其中不同的选项.(2)根据化学变化前后原子的种类、数目不变,由反应的化学方程式C2H8N2+2N2O4═2CO2↑+3R↑+4H2O↑,推断反应中R的分子构成,确定R物质的化学式.(1)设化合物中N元素的化合价为x,依据化合物中各元素的化合价代数和为0,有x×2+(-2)×4=0,解得x=+4;
根据两物质的化学式NO2与N2O4,可得知两物质都由N、O两种元素组成且其中N、O原子个数比相等都为1:2,则两物质中氮元素的化合价、氮元素的质量分数也相等;物质NO2的分子中含3个原子而物质N2O4的分子中含有6个原子;故选B;
(2)由反应的化学方程式C2H8N2+2N2O4═2CO2↑+3R↑+4H2O↑,可得知C、H、N、O原子的个数分别为
反应前 反应后
C原子 2 2
H原子 8 8
N原子6 0
O原子 8 8
根据化学变化前后原子的种类、数目不变,可判断物质R的3个分子中含有6个N原子,则每个R的分子由2个N原子构成,则物质R的化学式为N2;
故答案为:(1)+4;B
(2)N2;点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查根据反应的化学方程式推断物质的化学式及根据物质的化学式可进行的相关计算等基础知识与技能.1年前查看全部
- 发射“嫦娥二号”的长三丙火箭由三个子级构成,其中一子级上部装有液体四氧化二氮(N 2 O 4 ).下部装有液体偏二甲肼(
发射“嫦娥二号”的长三丙火箭由三个子级构成,其中一子级上部装有液体四氧化二氮(N 2 O 4 ).下部装有液体偏二甲肼(C 2 H 8 N 2 ).发动机内燃烧的化学方程式为:C 2 H 8 N 2 +2N 2 O 4 →3N 2 +2CO 2 +4H 2 O.该反应中( ) A.C 2 H 8 N 2 发生还原反应 B.C 2 H 8 N 2 是氧化剂 C.N 2 O 4 发生氧化反应 D.N 2 O 4 是氧化剂  漆黑夜空1年前1
漆黑夜空1年前1 -
 西贝赤赤 共回答了19个问题
西贝赤赤 共回答了19个问题 |采纳率84.2%偏二甲肼的化学式为C 2 H 8 N 2 ,H为+1价,C为-1价,N为-3价,
则反应C 2 H 8 N 2 +2N 2 O 4 →3N 2 +2CO 2 +4H 2 O中,
C 2 H 8 N 2 中N元素的化合价和C元素的化合价升高,N 2 O 4 中N元素的化合价降低,
则C 2 H 8 N 2 作还原剂,发生氧化反应;N 2 O 4 作氧化剂,发生还原反应;
故选:D.1年前查看全部
- 帮忙解一道初三化学题取3.0克偏二甲肼在氧气中充分燃烧后生成4.4克CO2、3.6克H2O和1.4克N2三种物质,由此可
帮忙解一道初三化学题
取3.0克偏二甲肼在氧气中充分燃烧后生成4.4克CO2、3.6克H2O和1.4克N2三种物质,由此可知偏二甲肼由( )种元素组成,其中碳元素的质量分数为( ) 3.0克偏二甲肼中,碳原子有( )mol,氢原子有( )mol,氮原子有( )mol
最好有解题过程,谢谢
 雨不亭1年前1
雨不亭1年前1 -
 寒冰ZJK 共回答了24个问题
寒冰ZJK 共回答了24个问题 |采纳率91.7%4.4g CO2中含有4.4/44 * 12 = 1.2g C元素
3.6g H2O中含有3.6/18 * 2 = 0.4g H元素
1.4g N2中含有1.4g N元素
因为1.2 + 0.4 + 1.4 = 3g
说明偏二甲肼中只含有C/H/N三种元素
所以偏二甲肼由 3 种元素组成,其中碳元素的质量分数 = 1.2/3 = 40%
碳原子有1.2/12 = 0.1mol,
氢原子有0.4/1 = 0.4mol,
氮原子有1.4/14 = 0.1mol1年前查看全部
- 偏二甲肼和四氧化二氯反应生成二氧化碳水和一种常见的气体单质的反应方程式(偏二甲肼的化学式:C2H8N2)
 yuruoshuang1年前1
yuruoshuang1年前1 -
 jxhvszy 共回答了16个问题
jxhvszy 共回答了16个问题 |采纳率87.5%是四氧化二氮……
氮气
C2H8N2+2N2O4=2CO2+4H2O+3N2,右边全是气体(高温下水自然是蒸汽)1年前查看全部
- 求偏二甲肼的化学式(要有过程啊)
求偏二甲肼的化学式(要有过程啊)
发射小火箭使用的主要原料叫“偏二甲肼”。一直该化合物由3种元素组成,其中氢元素质量分数约为13.3%,氮元素质量分数约为46.7%,碳元素的质量分数为40.0%且每个分子中含有2个碳原子,
试回答
求出偏二甲肼的化学式 玉玉仔1年前4
玉玉仔1年前4 -
 lunur 共回答了13个问题
lunur 共回答了13个问题 |采纳率76.9%碳元素的质量分数为40.0%且每个分子中含有2个碳原子,可求出:偏二甲肼的相对分子质量为2*12/40%=60;
所以H有:60*13.3%/1=8个
所以N有:60*46.7%/14=2个
所以C2H8N21年前查看全部
- “嫦娥三号”月球探测卫星成功发射是我国航天事业的有一个里程碑.运载“嫦娥三号”的火箭使用偏二甲肼(C 2 H 8 N 2
“嫦娥三号”月球探测卫星成功发射是我国航天事业的有一个里程碑.运载“嫦娥三号”的火箭使用偏二甲肼(C 2 H 8 N 2 )作燃料,下列说法正确的是( )
A.偏二甲肼中含有N 2 分子 B.偏二甲肼的相对分子质量为58 C.偏二甲肼中碳、氢、氮元素质量比2:8:2 D.偏二甲肼中氢元素原子质量分数最小  鬼风才疙瘩1年前1
鬼风才疙瘩1年前1 -
 快乐之新 共回答了19个问题
快乐之新 共回答了19个问题 |采纳率89.5%D
1年前查看全部
- 发射“嫦蛾一号”的火箭用偏二甲肼(C 2 H 8 N 2 )和四氧化二氮(N 2 O 4 )作常规推进剂,其完全反应的化
发射“嫦蛾一号”的火箭用偏二甲肼(C 2 H 8 N 2 )和四氧化二氮(N 2 O 4 )作常规推进剂,其完全反应的化学方程式:C 2 H 8 N 2 +2N 2 O 4 =3X+2CO 2 +4H 2 O,则X的化学式为 ( )
A.N 2 B.H 2 C.O 2 D.CO  金鱼的vv1年前1
金鱼的vv1年前1 -
 外研社123 共回答了22个问题
外研社123 共回答了22个问题 |采纳率95.5%A
1年前查看全部
- (2009•莆田)2008年9月25日,中国“神舟七号”飞船载人航天再次取得成功.火箭推进器的常用燃料是偏二甲肼[C2H
(2009•莆田)2008年9月25日,中国“神舟七号”飞船载人航天再次取得成功.火箭推进器的常用燃料是偏二甲肼[C2H8N2],该物质是由______种元素组成,它的分子中碳、氢、氮原子的个数比为______(填最简整数比).
 jixm1年前1
jixm1年前1 -
 一直都爱你 共回答了14个问题
一直都爱你 共回答了14个问题 |采纳率64.3%解题思路:根据偏二甲肼的化学式分析其元素组成和每个分子中元素原子个数比.由题意知偏二甲肼的化学式为C2H8N2,其元素组成为C、H、N三种,分子中右下角的数字表示原子个数,所以碳、氢、氮原子的个数比为2:8:2即1:4:1.
故答案为:(1)3;
(2)1:4:1.点评:
本题考点: 化学式的书写及意义.
考点点评: 该题以“神舟七号”飞船的燃料偏二甲肼为背景,考查化学式的意义,生动活泼,有利于学生兴趣的培养.1年前查看全部
- 2009年3月1日16时13分,“嫦娥一号”成功撞击月球.发射“嫦娥一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(
2009年3月1日16时13分,“嫦娥一号”成功撞击月球.发射“嫦娥一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进荆,其完全反应的化学方程式:C2H8N2+2N2OX=3N2+2CO2+4H2O,则X的值为( )
A.1
B.2
C.3
D.4 vantaxy1年前1
vantaxy1年前1 -
 _rqw_f93etu3_e9e 共回答了26个问题
_rqw_f93etu3_e9e 共回答了26个问题 |采纳率92.3%解题思路:由题意,根据“完全反应的化学方程式:C2H8N2+2N2OX=3N2+2CO2+4H2O”,结合质量守恒定律的元素守恒,可知反应前后的元素种类不变,原子个数相等,则可推测x的值.由“完全反应的化学方程式:C2H8N2+2N2OX=3N2+2CO2+4H2O”,结合质量守恒定律的元素守恒,则:反应前:碳原子2个,氢原子8个,氮原子6个,氧原子2x个;反应后:碳原子2个,氢原子8个,氮原子6个,氧原子8个,故氧原子2x=8,故x=4.
故选D.点评:
本题考点: 质量守恒定律及其应用;有关化学式的计算和推断.
考点点评: 本题是运用化学中的基本思想质量守恒思想,通过计算反应前后原子的个数,从而培养了学生的处理问题的能力.1年前查看全部
- 2003年10月15日,中国“神州五号”飞船载人航天取得成功.偏二甲肼是火箭推进器的常用燃料.根据偏二甲肼的化学式
2003年10月15日,中国“神州五号”飞船载人航天取得成功.偏二甲肼是火箭推进器的常用燃料.根据偏二甲肼的化学式
C2H8N2,你知道哪些信息?(即化学式表示的意义,回答不要求涉及反应.)请写出三点:
(1)相对原子质量______.(2)______(3)______. 绿葡萄嘟嘟1年前1
绿葡萄嘟嘟1年前1 -
 异域娃娃 共回答了16个问题
异域娃娃 共回答了16个问题 |采纳率81.3%解题思路:相对分子质量为构成分子的各原子的相对原子质量之和;化学式表示的意义有:①表示一种物质,②表示该物质的元素组成,③表示物质的一个分子,④表示物质的分子的构成等.偏二甲肼的相对原子质量为:12×2+1×8+14×2=60.
由偏二甲肼的化学式(C2H8N2)的化学式可知:表示偏二甲肼这种物质;表示偏二甲肼是由碳、氢、氮三种元素组成的;表示1个偏二甲肼分子;表示1个偏二甲肼分子是由2个碳原子、8个氢原子和2个氮原子构成的.
故答案为:(1)60;(2)表示偏二甲肼是由碳、氢、氮三种元素组成的;(3)1个偏二甲肼分子等.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题难度不大,考查化学式的含义,掌握化学式的含义并能灵活运用是正确解答本题的关键.1年前查看全部
- 发射神州九号飞船时,使用的燃料是偏二甲肼,它和四氧化二氮反应的化学方程式为:2N2O4+R═3N2+2CO2+4H2O,
发射神州九号飞船时,使用的燃料是偏二甲肼,它和四氧化二氮反应的化学方程式为:2N2O4+R═3N2+2CO2+4H2O,则R的化学式是( )
A.C3H5O
B.C2H8N2
C.C2H8
D.C2H5N newminer1年前1
newminer1年前1 -
 Mr000Bean 共回答了22个问题
Mr000Bean 共回答了22个问题 |采纳率95.5%解题思路:由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物R的化学式.根据反应的化学方程式2N2O4+R═3N2+2CO2+4H2O,反应物中氮、氧原子个数分别为4、8,反应后的生成物中氮、氧、碳、氢原子个数分别为6、8、2、8,根据反应前后原子种类、数目不变,则每个R分子由2个碳原子、8个氢原子和2个氮原子构成,则物质R的化学式为C2H8N2.
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式是正确解题的关键.1年前查看全部
- 偏二甲肼与四氧化二氮反应生成氮气,为什么会污染空气?
 marry8881年前2
marry8881年前2 -
 yuan8888 共回答了23个问题
yuan8888 共回答了23个问题 |采纳率87%充分燃烧的产物不会污染空气.但不完金燃烧产坐的一氧化碳及剩余的燃料或氧化剂都是大气污染物.其中N2O4会部分分解为NO2.NO2等氮氧化物在紫外线的作用下能强烈地破坏臭氧层,威力不下于氟氯代烷.1年前查看全部
- 火箭推进剂主要是偏二甲肼(C2H8N2) 它在空气中燃烧时会产生大气污染物,该污染物是什么?
 事实证明俞1年前1
事实证明俞1年前1 -
 yaxiange 共回答了26个问题
yaxiange 共回答了26个问题 |采纳率92.3%碳及一氧化碳1年前查看全部
- 偏二甲肼是火箭推进器的常用燃料与N2O4点燃反应的化学方程式
 aimiren1年前1
aimiren1年前1 -
 gogo547 共回答了19个问题
gogo547 共回答了19个问题 |采纳率89.5%C2H8N2+2N2O4=2CO2+3N2+4H2O
C2H8N2+2N2O4=2CO2+3N2+4H2O是正确的1年前查看全部
- 火箭常用偏二甲肼(C2H8N2)、液态氢等作为燃料,而用液态氧、四氧化二氮(N2O4)等作助燃剂.下列有关偏二甲肼的说法
火箭常用偏二甲肼(C2H8N2)、液态氢等作为燃料,而用液态氧、四氧化二氮(N2O4)等作助燃剂.下列有关偏二甲肼的说法不正确的是( )
A.偏二甲肼的相对分子质量是60
B.一个偏二甲肼分子是由2个碳原子、8个氢原子和2个氮原子构成的
C.偏二甲肼中碳、氢、氮三种元素的质量比为2:8:2
D.偏二甲肼中碳元素的质量分数为40% weistudio1年前0
weistudio1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 偏二甲肼的相对分子质量为?
 cynthiacat1年前1
cynthiacat1年前1 -
 SHAN112233 共回答了22个问题
SHAN112233 共回答了22个问题 |采纳率86.4%中文名:偏二甲肼
别称:1,1-二甲基肼;二甲基肼
化学式:C2H8N2
分子量:60.11年前查看全部
- 发射“嫦娥一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学方程式:C2H8N
发射“嫦娥一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学方程式:C2H8N2+2N2O4═3X+2CO2+4H2O,则X的化学式为( )
A.N2
B.H2
C.O2
D.CO 玄海小师父1年前1
玄海小师父1年前1 -
 灰猫仕 共回答了19个问题
灰猫仕 共回答了19个问题 |采纳率94.7%解题思路:根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式.在化学反应前后除X外,其他各原子相差的个数分别是:C:2-2=0,H:8-4×2=0,N:2+2×2-0=6,O:2×4-2×2-4×1=0,所以3个X分子中共含有6个N原子,每个X分子中含有2个N原子,即X的化学式为N2.
故选:A.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 利用质量守恒定律推断化学方程式中未知的化学式,是常见的有关化学式的计算题,根据质量守恒定律,化学反应前后原子的种类和数目不变,即可推断出化学式.1年前查看全部
- 偏二甲肼的蒸汽密度为氢气的30倍,既偏二甲肼的摩尔质量为氢气的30倍
偏二甲肼的蒸汽密度为氢气的30倍,既偏二甲肼的摩尔质量为氢气的30倍
为什么当偏二甲肼的蒸汽密度为氢气的30倍时候,
偏二甲肼的摩尔质量为氢气的30倍? friday1年前2
friday1年前2 -
 guaichang 共回答了22个问题
guaichang 共回答了22个问题 |采纳率72.7%密度是质量/体积,同样的状况下,体积是一样的,所以质量比就=密度比了,这里要注意是在相同情况下哈1年前查看全部
- 2010年10月1日,我国成功发射“嫦娥二号”卫星,嫦娥二号卫星由长征三号火箭承载发射.火箭燃料为偏二甲肼(C2H8N2
2010年10月1日,我国成功发射“嫦娥二号”卫星,嫦娥二号卫星由长征三号火箭承载发射.火箭燃料为偏二甲肼(C2H8N2),它是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是( )
A.偏二甲肼(C2H8N2)的摩尔质量为60
B.6.02×1023个偏二甲肼(C2H8N2)分子的质量约为60g
C.1mol偏二甲肼(C2H8N2)的质量为60g/mol
D.60g偏二甲肼(C2H8N2)中含有NA个氮原子 x4yja1年前1
x4yja1年前1 -
 jie5771 共回答了23个问题
jie5771 共回答了23个问题 |采纳率91.3%解题思路:A、摩尔质量的单位是g/mol等,以g/mol为单位数值上等于其相对分子质量.
B、6.02×1023个偏二甲肼的物质的量为1mol,根据m=nM计算质量.
C、质量的单位为g等,根据m=nM计算质量.
D、根据n=[m/M]计算60g偏二甲肼(C2H8N2)的物质的量,每个偏二甲肼(C2H8N2)分子中含有2个氮原子,再根据N=nNA计算氮原子数目.A、偏二甲肼(C2H8N2)的摩尔质量为60g/mol,相对分子质量为60,故A错误;
B、6.02×1023个偏二甲肼的物质的量为1mol,质量为1mol×60g/mol=60g,故B正确;
C、1mol偏二甲肼(C2H8N2)的质量为60g,60g/mol是偏二甲肼的摩尔质量,故C错误;
D、60g偏二甲肼(C2H8N2)的物质的量为[60g/60g/mol]=1mol,每个偏二甲肼(C2H8N2)分子中含有2个氮原子,所以含有氮原子数目为1mol×2×NAmol-1=2NA,故D正确.
故选:B.点评:
本题考点: 物质分子中的原子个数计算;摩尔质量.
考点点评: 考查对摩尔质量的理解及常用化学计量计算,难度较小,注意公式的灵活运用与概念的理解.1年前查看全部
- 火箭使用的燃料是偏二甲肼[(CH3)2NNH2],火箭升空时发生的化学反应为C2H8N2+2N2O4=2CO2↑+3N2
火箭使用的燃料是偏二甲肼[(CH3)2NNH2],火箭升空时发生的化学反应为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑.下列有关该反应的说是( D ) A.该反应的氧化剂是偏二甲肼 B.该反应进行时只有放热过程没有吸热过程 C.该反应中氮元素的化合价升高 D.该反应中每生成1 mol CO2转移8 mol e—
 hnmabfaut2__5_a21年前8
hnmabfaut2__5_a21年前8 -
 表录乌有 共回答了22个问题
表录乌有 共回答了22个问题 |采纳率100%A选项错误:氧化剂是指在化学反应后元素的化合价降低的物质.在反应式中,明显四氧化二氮的氮元素化合价从+4降到了0(氮气),所以该反应的氧化剂是四氧化二氮
B选项错误:反应开始时要点燃使反应物能相互反应,此时吸热
C选项错误:氮元素所指不明确.四氧化二氮中氮元素化合价是下降的.
D选项正确:四氧化二氮中氮由+4到氮气中氮的0价,电子转移4.由方程式2N2O4---2CO2可知,四氧化二氮与二氧化碳的物质的量之比为1:1.生成1molco2,相当于消耗等物质的量的N2O4,电子转移数为:4*1*2=8mol
注意:
1 有机物一般不去考虑化合价,因为构型复杂,很多时候加和甚至不为零,无法以此作为评判标准,这就是考虑D选项时为什么不选偏二甲肼的缘故
2 化学反应的实质是反应物中化合物化学键的断裂和生成物中化合物化学键的生成的过程,概括说来就是“旧键的断裂和新键的生成”,键是需要先断裂的,而破坏键的作用需要大量能量,也就是吸热,可以说没什么反应能单纯的放热1年前查看全部
- 发射“嫦娥二号”的长征火箭由三个子级构成。其中一子级上部装有液体四氧化二氮(N 2 O 4 ),下部装有液体偏二甲肼(C
发射“嫦娥二号”的长征火箭由三个子级构成。其中一子级上部装有液体四氧化二氮(N 2 O 4 ),下部装有液体偏二甲肼(C 2 H 8 N 2 )高能燃料。发动机内燃烧的化学方程式为:C 2 H 8 N 2 +2N 2 O 4 =3N 2 ↑+2CO 2 ↑+4H 2 O↑,该反应中
A.C 2 H 8 N 2 发生还原反应 B.C 2 H 8 N 2 是氧化剂 C.N 2 O 4 发生氧化反应 D.N 2 O 4 是氧化剂  zjxfyhj1年前1
zjxfyhj1年前1 -
 shenjdaoke 共回答了26个问题
shenjdaoke 共回答了26个问题 |采纳率92.3%D
1年前查看全部
- (2006•泉州)“神舟六号”载人航天飞船的火箭发射时是以偏二甲肼(C2H8N2)为燃料、以N2O4为助燃物的.请你回答
(2006•泉州)“神舟六号”载人航天飞船的火箭发射时是以偏二甲肼(C2H8N2)为燃料、以N2O4为助燃物的.请你回答有关问题:
(1)C2H8N2是由______等元素组成的化合物.
(2)1个C2H8N2分子共含有______个原子.2C2H8N2的相对分子质量总和等于______.
(3)C2H8N2燃烧能推进燃料舱升空是由于反应中释放出巨大的______.
(4)C2H8N2完全燃烧产物有三种在空气中都含有,其中一种是氮单质,请写出C2H8N2完全燃烧的产物中任意一种物质的化学式:______. caobbvaobb1年前1
caobbvaobb1年前1 -
 zrdhdo 共回答了21个问题
zrdhdo 共回答了21个问题 |采纳率90.5%解题思路:由化学式可以直接得出组成元素.每个分子中含有的原子个数等于各原子的个数之和.相对分子质量等于各原子的相对原子质量之和.燃料之所以称之为燃料是因为燃烧能放出能量.含碳化合物在完全燃烧时,碳元素全部转化为二氧化碳,氢元素转化为水.(1)偏二甲肼中是由碳、氢、氮三种元素组成.
(2)一个偏二甲肼中含有的原子个数为:2+8+2=12
2个C2H8N2的相对分子质量总和为:2(12×2+1×8+14×2)=120
(3)C2H8N2做燃料是因为能放出大量的热
故答案为:能量
(4)含碳化合物中完全燃烧时,碳元素转化为CO2而氢元素转化为H2O.题目中还告诉有一种是氮单质.
故答案为:N2或CO2或H2O点评:
本题考点: 有关化学式的计算和推断;元素在化学变化过程中的特点;化学式的书写及意义;质量守恒定律及其应用.
考点点评: 熟记化学式的意义,是解决化学式中的计算的前提.1年前查看全部
- 偏二甲肼和双氧水反应化学式
 不是谁都能爱你1年前1
不是谁都能爱你1年前1 -
 心事如烟 共回答了15个问题
心事如烟 共回答了15个问题 |采纳率93.3%C2H8N2+8H2O2=2CO2(气体符号)+12H2O+N2(气体符号)1年前查看全部
大家在问
- 1区别:last/remain表持续;recycling/recycled material表可回收金属
- 25.4比1又5分之3的比值是()化成最简整数比是().
- 3(2013•烟台)分解因式:a2b-4b3=______.
- 4(2013•莱芜)如图表示切开的苹果.有关叙述正确的是( )
- 5首字母填空1.Most Englishmen will open a door for a w_____ and so
- 6the Bund is where old Shanghai meets new Shanghai 叫什么句型
- 7一辆自行车车外轮直径是0.6米,平均每分钟转140周,这辆自行车5分钟可以行多少千米?
- 8After graduation he asked to be sent to the place____
- 9一根钢材,第一次截去20%,第二次截去4米,还剩全长的五分之三,这根钢材原来长几米
- 10猫头鹰(转载) 作文
- 11英语翻译1.我有一个比萨饼,你要来些吗?I have a pizza.Would you ________ ______
- 12only i can touch you,let myself occupy you,forever是什么意思
- 13双线桥法中箭头不代表电子移动方向,代表什么
- 14求有氧呼吸过程公式求有氧呼吸\无氧呼吸 用中文+字母表达 太多化学元素不认识了...
- 15什么是QA测试
