(2010•鲤城区质检)一个圆锥形零件的母线长为a,底面的半径为r,则这个圆锥形零件的全面积为______.
 xu_heng20012022-10-04 11:39:541条回答
xu_heng20012022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 郭剑2002 共回答了20个问题
郭剑2002 共回答了20个问题 |采纳率85%- 解题思路:圆锥全面积=底面积+侧面积=π×底面半径2+π×底面半径×母线长.
圆锥形零件的全面积为:πr2+πar.
点评:
本题考点: 圆锥的计算.
考点点评: 本题考查圆锥全面积公式的运用,掌握公式是关键. - 1年前
相关推荐
- (2010•鲤城区质检)下图是实验室制取某些气体的装置图,请根据要求回答问题.
(2010•鲤城区质检)下图是实验室制取某些气体的装置图,请根据要求回答问题.

(1)写出图中带序号仪器的名称:a______;b______.
(2)实验室发生和收集氧气可采用______(填标号,下同)和______装置组合,产生氧气的化学方程式是2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4;利用该装置组合收集氧气时,判断集气瓶中的氧气是否收集满的方法是______.
K2MnO4+MnO2+O2↑△ .
(3)已知乙炔(C2H2)是一种密度比空气小,不易溶于水的可燃性气体.实验室常用电石(主要成分是CaC2)与水反应制取乙炔,该反应放出大量的热,同时生成氢氧化钙.实验室制取乙炔的化学方程式是______,发生和收集乙炔的装置组合可以是______(填标号,下同)和______.保存电石应注意的问题是______. 飛翔的翅膀1年前1
飛翔的翅膀1年前1 -
 abcd765268 共回答了16个问题
abcd765268 共回答了16个问题 |采纳率87.5%解题思路:(1)ab均为实验室常用的仪器,熟记常见仪器即可解答;
(2)根据实验室制取氧气的反应原理,收集方法和验满方法解答;
(3)实验室制取乙炔气体:考虑反应物的状态、反应条件和生成的气体的密度、水溶性;根据反应物,推测生成物,正确书写化学方程式;(1)仪器名称:a 试管;b 集气瓶.
(2)实验室用高锰酸钾制取氧气时,要选择加热固体的发生装置,氧气密度比空气大且不易溶于水,可用排水法或向上排空气法收集氧气,故反应的化学方程式为 2KMnO4
△
.
K2MnO4+MnO2+O2↑;用向上排空气法收集氧气的验满的方法是将带火星的木条放在集气瓶口,看是否复燃.
(3)电石(主要成分是CaC2)与水反应生成乙炔,同时生成氢氧化钙,化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑,反应物是固体和液体,条件不需加热,乙炔密度比空气小,不易溶于水,故发生和收集乙炔的装置组合可以是 B和 C或E.电石能与水反应,故保存电石应注意的问题是 要注意防潮.
故答案为:(1)a 试管;b 集气瓶.
(2)A,D,2KMnO4
△
.
K2MnO4+MnO2+O2↑;将带火星的木条放在集气瓶口,看是否复燃.
(3)CaC2+2H2O═Ca(OH)2+C2H2↑,B和 C或E.要注意防潮.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常用仪器的名称和选用;实验室制取氧气的反应原理;氧气的检验和验满;书写化学方程式、文字表达式、电离方程式.
考点点评: 了解气体制取装置的选择和连接方法;掌握氧气的制取装置、制取原理和检验方法;正确书写有关化学方程式.1年前查看全部
- (2010•鲤城区质检)一定温度下,往质量均为100g的四份水中分别加入不同质量的硝酸钾,充分搅拌后,测得有关数据如下表
(2010•鲤城区质检)一定温度下,往质量均为100g的四份水中分别加入不同质量的硝酸钾,充分搅拌后,测得有关数据如下表所示:该温度下,硝酸钾的溶解度是( )
加入硝酸钾的质量/g 20 30 40 50 形成溶液的质量/g 120 130 140 140
A.20g
B.30g
C.40g
D.50g zhangcxt1年前1
zhangcxt1年前1 -
 含羞草10 共回答了15个问题
含羞草10 共回答了15个问题 |采纳率100%解题思路:首先知道:溶液的质量=溶质的质量+溶剂的质量;再明白固体物质的溶解度是指:在一定温度下,该物质在100g溶剂里到达饱和状态时所溶解的质量.最后观察图表判断硝酸钾在该温度下的溶解度.观察图表可知,当分别加入20g、30g、40g、50g硝酸钾时,加入40g和50g硝酸钾时的溶液的质量相同,所以可知硝酸钾在该温度下的溶解度是40g.我们据此作出判断ABCD的正确与否.
A、20g不是此温度下的溶解度,故错误;
B、30g不是此温度下的溶解度,故错误;
C、40g是此温度下的溶解度,故正确;
D、50g不是此温度下的溶解度,故错误;
故选C点评:
本题考点: 固体溶解度的概念.
考点点评: 同学们一定记住固体物质溶解度的概念,即在一定温度下,该物质在100g溶剂(通常溶剂为水)里到达饱和状态时所溶解的质量.1年前查看全部
- (2010•鲤城区质检)如图是某商场一楼与二楼之间的手扶电梯示意图.其中AB、CD分别表示一楼、二楼地面的水平线,∠AB
 (2010•鲤城区质检)如图是某商场一楼与二楼之间的手扶电梯示意图.其中AB、CD分别表示一楼、二楼地面的水平线,∠ABC=140°,一楼高(h)为3.5m,则乘手扶电梯从起点(B)到终点(C)有______米(结果精确到0.1).
(2010•鲤城区质检)如图是某商场一楼与二楼之间的手扶电梯示意图.其中AB、CD分别表示一楼、二楼地面的水平线,∠ABC=140°,一楼高(h)为3.5m,则乘手扶电梯从起点(B)到终点(C)有______米(结果精确到0.1).  qingxunan1年前0
qingxunan1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2010•鲤城区质检)已知直线y=x+4与y轴交于点C,与x轴交于点A.
 (2010•鲤城区质检)已知直线y=x+4与y轴交于点C,与x轴交于点A.
(2010•鲤城区质检)已知直线y=x+4与y轴交于点C,与x轴交于点A.
(1)求线段AC的长度;
(2)若抛物线y=−
x2+bx+c过点C、A,且与x轴交于另一点B,将直线AC沿y轴向下平移m个单位长度,若平移后的直线与x轴交于点D,与抛物线交于点N(N在抛物线对称轴的左边),与直线BC交于点E.1 2
①是否存在这样的m,使得△CAD是以AC为底的等腰三角形?若存在,请求出点N的坐标;若不存在,请说明理由;
②在直线AC平移的过程中,是否存在m值,使得△CDE的面积最大.若存在,请求出m值,若不存在,请说明理由. 薄荷卿卿1年前1
薄荷卿卿1年前1 -
 zhanghang1 共回答了20个问题
zhanghang1 共回答了20个问题 |采纳率95%解题思路:(1)根据直线AC的解析式,可得到A、C的坐标,进而利用勾股定理求得线段AC的长.
(2)①根据A、C的坐标,可利用待定系数法确定该抛物线的解析式,然后用m表示出平移后的直线解析式,由(1)知△OAC是等腰直角三角形,若△CAD是以AC为底的等腰三角形,那么点D必为线段CA的垂直平分线与x轴的交点,即D、O重合,由此求得m的值,进而可确定平移后的直线解析式,联立抛物线的解析式,即可求得N点的坐标.
②此题应分两种情况考虑:
1)当D在B点左侧时,即0<m≤6时;过E作EF⊥x轴于F,根据抛物线和平移后的直线解析式,可得到B、D的坐标,进而可求得BD、BA的长,由于平移前后的直线互相平行,则可证得△BDE∽△BAC,因此BD:BA=EF:OC,由此可求得EF的表达式,进而可求出△BDC和△BDE的面积,那么两个三角形的面积差即为△CDE的面积,由此可得关于S、m的函数关系式,根据函数的性质即可判断出S是否具有最大值以及对应的m的值;
2)当D在B点右侧时,即m>6时,方法同上. (1)当x=0时,y=4,
(1)当x=0时,y=4,
∴C(0,4)(1分)
当y=0时,x=-4,
∴A(-4,0)(2分)
在Rt△AOC中,OA=OC=4,∠AOC=90°,
∴AC=
OA2+OC2=
42+42=4
2.(3分)
(2)①抛物线经过点A、C,则:
−
1
2×(−4)2−4b+c=0
c=4,
解得
b=−1
c=4;
∴抛物线所对应的函数关系式为y=−
1
2x2−x+4;(4分)
∵△CAD是以AC为底的等腰三角形,
∴点D在AC的垂直平分线上,
此时点D与原点重合,即D(0,0),(5分)
∴m=OC=4;
则平移后的直线所对应的函数关系式为y=x,(6分)
∵点N是抛物线y=−
1
2x2−x+4与直线y=x的交点,
∴设点N(a,a),
则a=−
1
2a2−a+4,
解得a=−2±2
3;
∵点N在抛物线对称轴的左侧,
∴N(−2−2
3,−2−2
3);(7分)
②设△CDE的面积为S,
在y=−
1
2x2−x+4中,令y=0,
解得x=-4或x=2,
∴B(2,0),AB=6,
当点D在点B的左侧时,即当0<m≤6时(如图),
平移后的直线为y=x+4-m,
当y=0时,x=m-4.
∴D(m-4,0),
∴BD=2-(m-4)=6-m;(8分)
过点E作EF⊥AB于点F,
由DE∥AC,得∠BDE=∠CAD,
∴△BDE∽△BAC,
∴[EF/OC=
BD
BA],∴[EF/4=
6−m
6],
解得EF=
12−2m
3;(9分)
∴S=S△BCD−S△BDE=
1
2•(6−m)×4−
1
2•(6−m)•
12−2m
3=−
1
3m2+2m=−
1
3(m−3)2+3;
∴抛物线的开口向下,对称轴为直线m=3,
∵顶点(3,3)的横坐标在范围0<m≤6内,
∴当m=3,S有最大值为3;(10分)
当点D在点B的右侧时,即当m>6时(如图),
平移后的直线所对应的函数关系式为y=x+4-m,
当y=0时,x=m-4,
∴D(m-4,0),
∴BD=m-4-2=m-6;
过点E作EG⊥AB于点G,
由DE∥AC,得∠BDE=∠CAD,
∴△BDE∽△BAC,
∴[EG/OC=
BD
BA],∴[EG/4=
m−6
6],
解得EG=
2m−12
3;(11分)
∴S=S△BCD+S△BDE=
1
2•(m−6)×4+
1
2•(m−6)•
2m−12
3=
1
3m2−2m=
1
3(m−3)2−3;
∴抛物线开口向上,对称轴为m=3,
∵在抛物线对称轴的右侧,S随着m的增大而增大,
∴当m>6时,S没有最大值;(12分)
综上得,在直线AC平移的过程中,存在m值,当m=3,S有最大值为3,使得△CDE的面积最大.(13分)点评:
本题考点: 二次函数综合题.
考点点评: 此题考查的知识点有:勾股定理、二次函数解析的确定、相似三角形的判定和性质以及图形面积的求法等重要知识;在求图形面积的最大(小)问题时,将其转化为二次函数的最值问题是常用的方法.1年前查看全部
- (2010•鲤城区质检)下图是某个化学反应的微观模拟示意图(反应后的微粒没有表示完整).
(2010•鲤城区质检)下图是某个化学反应的微观模拟示意图(反应后的微粒没有表示完整).

(1)若要将反应后的微料表示完整,反应后的方框内应填入下图中的______(填标号).
(2)该微观模拟示意图所表示反应的化学方程式是2H2O
2H2↑+O2↑;通电 .2H2O,该反应属于______(选填“化合”、“分解”、“置换”或“复分解”)反应.
2H2↑+O2↑;通电 .
(3)请根据图中包含的信息,提炼出一点有关物质构成奥秘的知识:______. wddwn1年前1
wddwn1年前1 -
 raineral 共回答了20个问题
raineral 共回答了20个问题 |采纳率95%解题思路:根据不同的圆点表示的元素可知反应前是水分子,则通电后会生成氢气与氧气,符合一变多的变化特性,右框中只含有氢分子所以应补充氧分子的图示,该变化反映出水分子或其他分子的构成情况.(1)该反应反应前的分子是水分子所以生成的分子应该是氢分子与氧分子,所以应该在右框加入氧的分子,及氧的双原子分子.
(2)该微观示意图反映的是水的电解过程,产物是氢气与氧气,符合“一变多”的分解反应的特征.
(3)从图示可以得到水分子氢分子氧分子的结构,进而可知分子是由原子构成的,分子可以直接构成物质.
故答案为:(1)③(2)2H2O
通电
.
2H2↑+O2↑;分解(3)分子可以直接构成物质.点评:
本题考点: 微粒观点及模型图的应用;反应类型的判定;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了微观粒子的有关问题,化学反应的类型、物质的构成等方面均是由微观图示反映的信息得出的,解题的关键是知识与图示的结合.1年前查看全部
- (2010•鲤城区质检)2010年上海世博会福建馆以“潮涌海西,魅力福建”为主题,其外形就像一艘破浪远航的巨轮(如图).
 (2010•鲤城区质检)2010年上海世博会福建馆以“潮涌海西,魅力福建”为主题,其外形就像一艘破浪远航的巨轮(如图).则此图的左视图为( )
(2010•鲤城区质检)2010年上海世博会福建馆以“潮涌海西,魅力福建”为主题,其外形就像一艘破浪远航的巨轮(如图).则此图的左视图为( )
A.
B.
C.
D.
 tbq12171年前1
tbq12171年前1 -
 华欧商务英语翻译 共回答了12个问题
华欧商务英语翻译 共回答了12个问题 |采纳率75%解题思路:找到从左面看所得到的图形即可.从左面看可得到棱长正好组合为一个长方形,故选A.
点评:
本题考点: 简单组合体的三视图.
考点点评: 本题考查了三视图的知识,左视图是从物体的左面看得到的视图.1年前查看全部
- (2010•鲤城区质检)下列物质属于纯净物的是( )
(2010•鲤城区质检)下列物质属于纯净物的是( )
A.浮有冰的水
B.自来水
C.矿泉水
D.硬水 waizd1年前1
waizd1年前1 -
 xawf 共回答了23个问题
xawf 共回答了23个问题 |采纳率82.6%解题思路:纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质.据此逐项分析即可.A、浮有冰的水中只含有水一种物质,属于纯净物.故选项正确;
B、自来水中含有水、钙镁的化合物等多种物质,属于混合物.故选项错误;
C、矿泉水中含有水、微量的矿物质等多种物质,属于混合物,故选项错误;
D、硬水中含有水、钙镁的化合物等物质,属于混合物.故选项错误.
故选A.点评:
本题考点: 纯净物和混合物的判别.
考点点评: 解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物,如果有多种物质就属于混合物.1年前查看全部
- (2010•鲤城区质检)下列化学实验基本操作错误的是( )
(2010•鲤城区质检)下列化学实验基本操作错误的是( )
A.
读取液体体积
B.
检查装置气密性
C.
加热液体试剂
D.
倾倒液体试剂 utadaye1年前1
utadaye1年前1 -
 agnew 共回答了17个问题
agnew 共回答了17个问题 |采纳率94.1%解题思路:根据量筒使用、气密性检查方法、给液体加热及倾倒液体试剂的操作方法解答.A、用量筒最取液体,读数时视线应与液体凹液面最低处保持相平,故A正确;
B、将导管插入水中,用手握住试管外壁,导管口有气泡产生,说明气密性良好,故B正确;
C、给试管中液体加热时,试管内液体不能超过试管容积的[1/3],故C错误;
D、倾倒液体试剂时瓶塞倒放,标鉴向着手心,瓶口紧挨试管口,都正确,故D正确.
故选C.点评:
本题考点: 测量容器-量筒;液体药品的取用;给试管里的液体加热;检查装置的气密性.
考点点评: 熟悉实验基本操作是解答本题关健.1年前查看全部
- (2010•鲤城区质检)下列式子错误的是( )
(2010•鲤城区质检)下列式子错误的是( )
A.3x2y•x3y2=3x5y3
B.
=3−21 32
C.(m4)3=m7
D.
−32
=−22 2  fafa8531年前1
fafa8531年前1 -
 iceking9 共回答了27个问题
iceking9 共回答了27个问题 |采纳率85.2%解题思路:根据单项式的乘法法则;负整数指数次幂等于正整数次幂的倒数;幂的乘方,底数不变指数相乘,合并同类二次根式的法则对各选项计算后利用排除法求解.A、3x2y•x3y2=3x5y3,正确;
B、
1
32=3−2,正确;
C、(m4)3=m4×3=m12,故本选项错误;
D、
2−3
2=−2
2,正确.
故选C.点评:
本题考点: 二次根式的加减法;同底数幂的乘法;幂的乘方与积的乘方;负整数指数幂.
考点点评: 本题考查了合并同类二次根式、同底数幂的乘法、幂的乘方和单项式的乘法,需熟练掌握并区分清楚,才不容易出错.1年前查看全部
- (2010•鲤城区质检)甘氨酸(C2H5NO2)是组成绿色荧光蛋白的一种成分.下列有关甘氨酸说法错误的是( )
(2010•鲤城区质检)甘氨酸(C2H5NO2)是组成绿色荧光蛋白的一种成分.下列有关甘氨酸说法错误的是( )
A.是一种有机物
B.由四种元素组成
C.碳和氢两种元素的质量比为12:1
D.分子中碳氢两种原子的个数比为2:5 秋竹的种子1年前1
秋竹的种子1年前1 -
 心寥寥 共回答了22个问题
心寥寥 共回答了22个问题 |采纳率100%解题思路:化学式表示的意义:
表示一种物质;表示该物质的组成元素;表示一个分子;表示一个分子由几个原子构成等.A、甘氨酸是含有碳元素的化合物,属于有机物.正确;
B、甘氨酸是由碳元素、氢元素、氮元素和氧元素等四种元素组成的.正确;
C、碳和氢两种元素的质量比为:24:5.错误;
D、分子中碳氢两种原子的个数比为2:5.正确.
故选C.点评:
本题考点: 化学式的书写及意义;有机物的特征、分类及聚合物的特性;元素质量比的计算.
考点点评: 本题主要考查化学式的含义,解答时要注意理解宏观组成和微观构成的区别,宏观方面一般用组成表示,微观方面一般用构成表示.1年前查看全部
- (2010•鲤城区质检)右图是从元素周期表中截取的原子序数1-18的四种不同元素.下列有关说法正确的是( )
(2010•鲤城区质检)右图是从元素周期表中截取的原子序数1-18的四种不同元素.下列有关说法正确的是( )
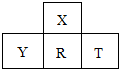
A.X与R在同一周期
B.Y与T在同一主族
C.原子序数:Y<R
D.核电子荷数:Y>R g26412211年前1
g26412211年前1 -
 忏悔的dddd光 共回答了23个问题
忏悔的dddd光 共回答了23个问题 |采纳率91.3%解题思路:在元素周期表中,每个横行表示1个周期,由上往下递增;在同一个周期中,由左向右原子序数增大;每个竖列表示1个族.A、因为X与R不在同一横行中,所以X与R不在同一周期.错误;
B、T元素可能是稀有气体元素,稀有气体元素不属于主族元素.错误;
C、Y和R在同一周期,R的原子序数大于Y的原子序数.正确;
D、R的核电荷数大于Y的核电荷数.错误.
故选C.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题考查学生对元素周期表的理解,解答时要从原子序数、核电荷数的概念方面进行分析、判断,从而得出正确的结论.1年前查看全部
- (2010•鲤城区质检)如图,已知点A1(a,1)在直线l:y=33x上,以点A1为圆心,以233为半径画弧,交x轴于点
(2010•鲤城区质检)如图,已知点A1(a,1)在直线l:y=
x上,以点A1为圆心,以3 3 2 3
为半径画弧,交x轴于点B1、B2,过点B2作A1B1的平行线交直线l于点A2,在x轴上取一点B3,使得A2B3=A2B2,再过点B3作A2B2的平行线交直线l于点A3,在x轴上取一点B4,使得A3B4=A3B3,按此规律继续作下去,则①a=3 3 ;②△A4B4B5的面积是3 64 3 3 .64 3 3 
 粤粤1年前1
粤粤1年前1 -
 vanilla_hazelnut 共回答了20个问题
vanilla_hazelnut 共回答了20个问题 |采纳率95%解题思路:①将点A1(a,1)代入直线1中可求的a的值.
②先求出△A1B1B2的面积,然后根据相似三角形可以求出下一个三角形的面积,以此类推可求出△A4B4B5的面积. 如图所示:
如图所示:
①将点A1(a,1)代入直线1中,可得
3
3a=1,
所以a=
3.
②△A1B1B2的面积为:S=
1
2×1×
2
3
3=
3
3;
因为△OA1B1∽△OA2B2,所以2A1B1=A2B2,又因为两线段平行,可知△A1B1B2∽△A2B2B3,所以△A2B2B3的面积为S1=4S;
以此类推,△A4B4B5的面积等于64S=
64
3
3.点评:
本题考点: 一次函数综合题.
考点点评: 本题主要考查对于一次函数的应用以及三角形面积的求法,此外还用到相似三角形方面的知识.1年前查看全部
- (2010•鲤城区质检)参加高强度体育活动后,为能较迅速恢复体能,可饮用下列物质中的( )
(2010•鲤城区质检)参加高强度体育活动后,为能较迅速恢复体能,可饮用下列物质中的( )
A.纯净水
B.矿泉水
C.葡萄糖水
D.食盐水 cwj123zlj1年前1
cwj123zlj1年前1 -
 trytoforget 共回答了19个问题
trytoforget 共回答了19个问题 |采纳率94.7%解题思路:根据六大营养素的作用解答.葡萄糖能直接给人体供能.葡萄糖能直接给人体供能,可以迅速增加体能.
故选C点评:
本题考点: 生命活动与六大营养素.
考点点评: 明确六大营养素及作用是解答本题关健.1年前查看全部
- (2010•鲤城区质检)请结合所学的知识,回答下列航空航天领域的相关问题:
(2010•鲤城区质检)请结合所学的知识,回答下列航空航天领域的相关问题:
(1)大多数飞船是由运载火箭送上太空的.火箭发射升空时,燃料燃烧将化学能先转化为______能.
(2)飞船的许多结构部件含有铝合金.铝合金属于______(填标号)
a.金属材料 b.无机非金属材料 c.合成材料 d.复合材料
(3)航天员进行太空漫步所穿着的舱外航天服中装配有氧气,此时氧气的主要作用是______.
(4)在太空舱里,nife2o4可促进宇航员呼出的co2转化为o2,而自身的质量和化学性质保持不变,nife2o4是这一反应的______剂.
(5)2011年***首个火星探测器“荧火一号”将踏***问火星的旅程.太阳能帆板是探测器的重要部件,其制作材料之一的高纯硅(si)是在高温条件下,用氢气与四氯化硅(sicl4)反应制得,反应同时得到一种化合物,该反应的化学方程式sicl4+2h2
si+4hcl高温 .sicl4+2h2.
si+4hcl高温 . sugerchan1年前1
sugerchan1年前1 -
 doudoutang1 共回答了16个问题
doudoutang1 共回答了16个问题 |采纳率93.8%解题思路:解:(1)根据能量的转化解答;
(2)根据金属材料的范围解决此题
(3)根据氧气的性质与用途解答;
(4)根据催化剂的概念解决此题.
(5)根据化学方程式的书写及相关信息解答.(1)飞船发射升空时,所用的燃料燃烧是将化学能转化为热能.
(2)金属材料包括金属及合金,所以铝合金属于金属材料.
(3)航天员进行太空漫步所穿着的舱外航天服中装配有氧气,此时氧气的主要作用供给呼吸;
(4)因为NiFe2O4自身的质量和化学性质保持不变,符合催化剂的特征,所以NiFe2O4是这一反应的催化剂.
(5)氢气与四氯化硅(SiCl4)在高温条件下反应生成硅和氯化氢,该反应的化学方程式为SiCl4+2H2
高温
.
Si+4HCl.
故答案为:(1)化学能;(2)D;(3)供给呼吸;(4)催化剂(5)SiCl4+2H2
高温
.
Si+4HCl;点评:
本题考点: 物质发生化学变化时的能量变化;氧气的用途;催化剂的特点与催化作用;金属材料及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题综合考查了航天领域的知识,氧气的用途,化学方程式的书写及化学反应中能量的转化,属于基础知识考查.1年前查看全部
- (2010•鲤城区质检)因式分解:4b3+8ab2+4a2b=______.
 13qe1年前1
13qe1年前1 -
 爱为你存在 共回答了13个问题
爱为你存在 共回答了13个问题 |采纳率76.9%解题思路:此多项式有公因式,应先提取公因式4b,再对余下的多项式进行观察,有3项,可利用完全平方公式继续分解.4b3+8ab2+4a2b,
=4b(b2+2ab+a2),
=4b(b+a)2.点评:
本题考点: 提公因式法与公式法的综合运用.
考点点评: 本题考查了提公因式法与公式法进行因式分解,一个多项式有公因式首先提取公因式,然后再用其他方法进行因式分解,同时因式分解要彻底,直到不能分解为止.1年前查看全部
- (2010•鲤城区质检)以下疾病可能与缺钙有关的是( )
(2010•鲤城区质检)以下疾病可能与缺钙有关的是( )
A.智力低下
B.骨质疏松
C.贫血
D.甲状腺肿大 win04591年前1
win04591年前1 -
 藏家 共回答了16个问题
藏家 共回答了16个问题 |采纳率81.3%解题思路:可根据元素对人体健康的作用及元素缺乏症进行解答.幼儿及青少年缺钙会得佝偻病和发育不良,老年人缺钙会发生骨质疏松,容易骨折.
A、缺锌会引起智力低下;
B、缺钙会引起骨质疏松;
C、缺铁会引起贫血;
D、缺碘会引起甲状腺肿大;
故选B点评:
本题考点: 人体的元素组成与元素对人体健康的重要作用.
考点点评: 人体所需的各种元素来说,都有一个合理摄入量的问题:不能太少,也不能过量;因为摄入不足或摄入过量均不利于人体健康.要记住各种元素对人体的作用.1年前查看全部
- (2010•鲤城区质检)白醋(含3%-5%的醋酸)是常用的调味品.现有4%的白醋500g,该溶液中含溶质醋酸______
(2010•鲤城区质检)白醋(含3%-5%的醋酸)是常用的调味品.现有4%的白醋500g,该溶液中含溶质醋酸______g;若再加水500g稀释后所得溶液溶质醋酸的质量分数为______.
 dongbaohua1年前1
dongbaohua1年前1 -
 VanGog 共回答了16个问题
VanGog 共回答了16个问题 |采纳率87.5%解题思路:根据溶质的质量分数=
×100%计算溶质醋酸的质量;溶液在进行加水稀释时,稀释前后溶液中溶质的质量不变,根据此等量关系,溶质的质量 溶液的质量 溶质醋酸的质量为500g×4%=20g
稀释前后溶质的质量不变,所以有:稀释后溶质的质量分数=[500g×4%/500g+500g]×100%=2%
故答案为:20、2%点评:
本题考点: 有关溶质质量分数的简单计算.
考点点评: 欲使溶液的溶质质量分数减小一半,可通过加入与溶液质量相等的水进行稀释的方法实现.1年前查看全部
- (2010•鲤城区质检)小红同学在西汉《淮南子•万毕术》一书中看到了湿法炼铜的文字记载:“曾青得铁则化铜”.为了能对古代
(2010•鲤城区质检)小红同学在西汉《淮南子•万毕术》一书中看到了湿法炼铜的文字记载:“曾青得铁则化铜”.为了能对古代湿法炼铜有更深入的认识,小红与同学们展开了以下的学习与交流.
(1)请按金属活动性的顺序,将铁和铜的元素符号填在下图的方框内.
(2)若曾青为硫酸铜.请用化学方程式表示“曾青得铁则化铜”所包含的化学反应:CuSO4+Fe=FeSO4+CuCuSO4+Fe=FeSO4+Cu.
(3)为模拟古代湿法炼铜的过程,同学们设计了以下的实验方案:
请问:步骤①中,加入过量细铁粉的目的是使硫酸铜全部反应使硫酸铜全部反应,该步骤所得的金属混合物成分是铜和铁铜和铁(填物质名称);步骤②中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑Fe+H2SO4=FeSO4+H2↑. 等着挖秦陵1年前1
等着挖秦陵1年前1 -
 小菜的yy 共回答了23个问题
小菜的yy 共回答了23个问题 |采纳率87%(1)金属活动顺序表中,铁在氢前,铜在氢后,故答案为;Fe、Cu
(2)在金属活动顺序表中,铁在铜前边,所以铁会把铜从其盐溶液中置换出来,故选CuSO4+Fe=FeSO4+Cu
(3)该实验的流程是:过量的铁粉把硫酸铜中所有的Cu2+都置换出来,得到铁和铜的混合物,然后加入足量的稀硫酸或稀盐酸,把所有的铁粉消耗完,最后经过滤、洗涤、干燥,即可得到纯净的铜.
故答案为:使硫酸铜全部反应;铜和铁;Fe+H2SO4=FeSO4+H2↑或Fe+2HCl=FeCl2+H2↑.1年前查看全部
- (2010•鲤城区质检)探究课上,老师进行了钠在二氧化碳中燃烧的实验.实验后,同学们发现集气瓶底有黑色颗粒,瓶壁上有白色
(2010•鲤城区质检)探究课上,老师进行了钠在二氧化碳中燃烧的实验.实验后,同学们发现集气瓶底有黑色颗粒,瓶壁上有白色物质.
[提出问题]钠在二氧化碳中燃烧生成的黑色颗粒和白色物质是什么?
[探究活动一]探究黑色颗粒的成分
[猜想与假设]同学们根据二氧化碳中含有______,猜想黑色颗粒成分可能是炭黑.
[设计并进行实验]
实验过程,观察到黑色颗粒逐渐减少,澄清石灰水变浑浊.
[得出结论]上述实验证明同学们的猜想是______(选填“正确”或“错误”)的.硬质玻璃管内发生反应的化学方程式为C+O2
CO2点燃 .C+O2.
CO2点燃 .
[探究活动二]探究白色物质的成分
[猜想与假设]同学们对白色物质的成分做出以下猜想:
Ⅰ是氧化钠;Ⅱ是碳酸钠;Ⅲ是氢氧化钠.
小雨同学通过对物质组成元素的分析,认为“猜想Ⅲ”是错误的.原因是______.
林阳同学认为白色物质的成分还可能是______(填化学式,下同)和______的混合物.
[查阅资料]氧化钠是白色固体,能与水反应生成氢氧化钠.
[验证猜想](1)请写出证明白色物质中含有碳酸钠的实验步骤和现象:______.
(2)填写证明白色物质不含氧化钠的实验报告.
[交流与讨论]综合上述探究活动的结果,请写出钠在二氧化碳中燃烧的化学方程式实验步骤 实验现象 实验结论 ①除去溶液中的碳酸钠.
取少量白色物质于试管中,加水溶解,再加入足量的氯化钙溶液.白色沉淀生成 产生沉淀的化学方程式是
______②证明白色物质中不含氧化钠.
取少量实验①所得的溶液于另一试管中,加入______.______ 不含氧化钠 4Na+3CO2
C+2Na2CO3点燃 .4Na+3CO2.
C+2Na2CO3点燃 . fdsfdd1年前1
fdsfdd1年前1 -
 zjk11010 共回答了13个问题
zjk11010 共回答了13个问题 |采纳率69.2%解题思路:(1)根据质量守恒定律可知反应前后元素种类不变;根据能够使澄清石灰水变浑浊的气体是二氧化碳,又因为二氧化碳是由黑色粉末与氧气反应得到的物质,所以黑色物质是碳,方程式是根据方程式的书写方法来考虑;根据质量守恒定律可知反应前后元素种类不变来考虑,氢氧化钠是否正确;由于可能是氧化钠、碳酸钠,所以有一种考虑方法就是可能是二者的混合物;判断碳酸钠的存在,就是判断碳酸根离子的存在,所以加入盐酸有气体产生即可;
(2)加入足量的氯化钙溶液发生了碳酸钠与氯化钙反应的方程式.由于氧化钠是白色固体,能与水反应生成氢氧化钠,氯化钙与碳酸钠已经反应完了,所以把碳酸根离子除去后.再加入酚酞试液变红说明溶液显碱性,能够证明碳酸根离子的存在即可,碳酸根离子与酸反应能产生二氧化碳和水;钠与二氧化碳反应的实例可知生成物中含有碳和碳酸钠,所以方程式的书写要考虑书写方法.[猜想与假设]由于黑色颗粒成分可能是炭黑,并且反应物是碳和二氧化碳,在反应前后元素种类是不变的;所以生成炭黑是由于生成物中含有碳元素;由于是黑色颗粒是与氧气反应,并且生成二氧化碳,说明反应物中含有碳元素;硬质玻璃管内发生反应的反应物是碳和氧气,生成物是二氧化碳;由于反应前后元素种类不变,所以不可能含有氢氧化钠,因为二氧化碳和碳中不含有氢元素所以生成物中不可能含有氢氧化钠;所以生成物可能是二者的混合物;(1)鉴别碳酸根离子主要是判断它们与碳酸根离子是否产生气体、沉淀和水;(2)由于碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,氯化钠显中性,消耗了碳酸钠并消耗了原料; 由于氧化钠是白色固体,能与水反应生成氢氧化钠,氯化钠是显中性,所以将固体溶于水,不变色说明没有氧化钠等物质的支持;根据钠和二氧化碳反应生成碳和碳酸钠可知反应物中含有钠和碳酸钠.
故答案为:
[猜想与假设]碳元素;[得出结论]正确;C+O2
点燃
.
CO2;反应物中没有氢元素;Na2O;Na2CO3;
(1)加入盐酸,有气泡产生;
(2)Na2CO3+CaCl2═2NaCl+CaCO3↓;无色酚酞试液;溶液不变色;4Na+3CO2
点燃
.
C+2Na2CO3.点评:
本题考点: 实验探究物质的组成成分以及含量;证明碳酸盐;盐的化学性质;碳的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据所做题目的已知可知反应后生成物已知条件可推出反应物的特点,检验碳酸根离子的存在就是加入盐酸看是否有氯化钙的生成.1年前查看全部
- (2010•鲤城区质检)如图,六边形ABCFED是轴对称图形,CD所在的直线是它的对称轴,若∠ADC+∠BCD=130°
 (2010•鲤城区质检)如图,六边形ABCFED是轴对称图形,CD所在的直线是它的对称轴,若∠ADC+∠BCD=130°,则∠E+∠F的大小是( )
(2010•鲤城区质检)如图,六边形ABCFED是轴对称图形,CD所在的直线是它的对称轴,若∠ADC+∠BCD=130°,则∠E+∠F的大小是( )
A.130°
B.220°
C.260°
D.230° 雪山飞鹄pbdq1年前1
雪山飞鹄pbdq1年前1 -
 力力70 共回答了20个问题
力力70 共回答了20个问题 |采纳率95%解题思路:知道六边形ABCFED是轴对称图形,可知∠FCD+∠EDC=130°,进而知道∠E+∠F.∵六边形ABCFED是轴对称图形,CD所在的直线是它的对称轴,
∴∠FCD+∠EDC=∠ADC+∠BCD=130°,
∴∠E+∠F=230°,
故选D.点评:
本题考点: 轴对称的性质.
考点点评: 本题是考查图形的对称、旋转、分割以及分类的数学思想.1年前查看全部
大家在问
- 1无法理解这句话:减小压强,向体积增大的方向移动?
- 2/tu:/的英语是什么啊
- 3王老师把5万元存入银行,整存整取三年,年利率是4.41%,到期时他可以取出本金和税后利息共多少元?
- 4小明在用已经校零的弹簧测力计测量一个物体的重力时,误将物体挂在了拉环上,如图所示,当物体静止时,弹簧测力计的示数是2N,
- 5你的梦想是什么?读了17梦想的力量,你有什么感受,你准备怎样为梦想而努力?
- 6什么是英语语法翻译法?
- 7如图,AB=8cm,O为线段AB上的任意一点,C为AO的中点,D为OB的中点,你能求出线段CD的长吗?并说明理由.
- 8英语翻译1.legend bar is a show bar主要表演new jazz,pole-dance,bell-d
- 9下面是一盒药片的说明书.题(1)成人一天服用药片多少克?(2)儿童每天服药的有效成分是多少克?
- 10关于x,y的方程组x+y=a,xy=b只有一个解,求实数a,b满足的条件,并求出这组解
- 11人体和高等动物生命活动的调节过程很复杂,某同学总结出4种不同的生理调节过程,用图表示如下.你认为该同学总结正确的是(
- 12at once,without delay用一个英语单词表达
- 13我一直以来很困惑电流的一个事情,比如说一个半导体,他原来里面的自由电子数目很少,说不太容易导电?、,那往里面掺杂一个杂志
- 14i gave up what might have been a maginificent career as a pa
- 15求中秋节随想 500~600字 本人六年 在9号之前要
