求高二上学期化学知识点.习题[要有解释]
 冯洪江2022-10-04 11:39:541条回答
冯洪江2022-10-04 11:39:541条回答
求高二上学期化学知识点.习题[要有解释]
主要要化学平衡、水的电离,弱电解质的电离、平衡、水解…
主要要化学平衡、水的电离,弱电解质的电离、平衡、水解…

已提交,审核后显示!提交回复
共1条回复
 南南罗兰 共回答了19个问题
南南罗兰 共回答了19个问题 |采纳率94.7%- 化学平衡
1.定义:
化学平衡状态:一定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再改变,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态.
化学平衡的特征
逆(研究前提是可逆反应)
等(同一物质的正逆反应速率相等)
动(动态平衡)
定(各物质的浓度与质量分数恒定)
变(条件改变,平衡发生变化)
判断平衡的依据
判断可逆反应达到平衡状态的方法和依据
例举反应 mA(g)+nB(g) pC(g)+qD(g)
混合物体系中各成分的含量①各物质的物质的量或各物质的物质的量的分数一定平衡
②各物质的质量或各物质质量分数一定 平衡
③各气体的体积或体积分数一定 平衡
④总体积、总压力、总物质的量一定 不一定平衡
正、逆反应
速率的关系 ①在单位时间内消耗了m molA同时生成m molA,即V(正)=V(逆) 平衡
②在单位时间内消耗了n molB同时消耗了p molC,则V(正)=V(逆) 平衡
③V(A):V(B):V(C):V(D)=m:n:p:q,V(正)不一定等于V(逆) 不一定平衡
④在单位时间内生成n molB,同时消耗了q molD,因均指V(逆) 不一定平衡
压强 ①m+n≠p+q时,总压力一定(其他条件一定) 平衡
②m+n=p+q时,总压力一定(其他条件一定) 不一定平衡
混合气体平均相对分子质量Mr ①Mr一定时,只有当m+n≠p+q时 平衡
②Mr一定时,但m+n=p+q时 不一定平衡
温度 任何反应都伴随着能量变化,当体系温度一定时(其他不变) 平衡
体系的密度 密度一定 不一定平衡
其他 如体系颜色不再变化等 平衡
(二)影响学平衡移动的因素
1、浓度对化学平衡移动的影响
(1)影响规律:在其他条件不变的情况下,增大反应物 的浓度或减少生成物的浓度,都可以使平衡向正方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向逆方向移动
(2)增加固体或纯液体的量,由于浓度不变,所以平衡_不移动_
(3)在溶液中进行的反应,如果稀释溶液,反应物浓度__减小__,生成物浓度也_减小_, V正_减小__,V逆也_减小__,但是减小的程度不同,总的结果是化学平衡向反应方程式中化学计量数之和_大_的方向移动.
2、温度对化学平衡移动的影响
影响规律:在其他条件不变的情况下,温度升高会使化学平衡向着___吸热反应______方向移动,温度降低会使化学平衡向着_放热反应__方向移动.
3、压强对化学平衡移动的影响
影响规律:其他条件不变时,增大压强,会使平衡向着__体积缩小___方向移动;减小压强,会使平衡向着___体积增大__方向移动.
注意:(1)改变压强不能使无气态物质存在的化学平衡发生移动
气体减压或增压与溶液稀释或浓缩的化学平衡移动规律相似
催化剂对化学平衡的影响:由于使用催化剂对正反应速率和逆反应速率影响的程度是等同的,所以平衡__不移动___.但是使用催化剂可以影响可逆反应达到平衡所需的_时间_.
勒夏特列原理(平衡移动原理):如果改变影响平衡的条件之一(如温度,压强,浓度),平衡向着能够减弱这种改变的方向移动.
化学平衡常数
(一)定义:在一定温度下,当一个反应达到化学平衡时,___生成物浓度幂之积与反应物浓度幂之积的比值是一个常数____比值. 符号:__K__
(二)使用化学平衡常数K应注意的问题:
表达式中各物质 的浓度是__变化的浓度___,不是起始浓度也不是物质的量.
K只与__温度(T)___有关,与反应物或生成物的浓度无关.
3、反应物或生产物中有固体或纯液体存在时,由于其浓度是固定不变的,可以看做是“1”而不代入公式.
稀溶液中进行的反应,如有水参加,水的浓度不必写在平衡关系式中.
化学平衡常数K的应用:
化学平衡常数值的大小是可逆反应__进行程度__的标志.K值越大,说明平衡时_生成物___的浓度越大,它的___正向反应__进行的程度越大,即该反应进行得越__完全___,反应物转化率越_高___.反之,则相反. 一般地,K>_105__时,该反应就进行得基本完全了.
可以利用K值做标准,判断正在进行的可逆反应是否平衡及不平衡时向何方进行建立平衡.(Q:浓度积)
Q_〈__K:反应向正反应方向进行;
Q__=_K:反应处于平衡状态 ;
Q_〉__K:反应向逆反应方向进行
利用K值可判断反应的热效应
若温度升高,K值增大,则正反应为__吸热___反应
若温度升高,K值减小,则正反应为__放热___反应
*
等效平衡
概念:在一定条件下(定温、定容或定温、定压),只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的百分含量均相同,这样的化学平衡互称为等效平衡.
分类
(1)定温,定容条件下的等效平衡
第一类:对于反应前后气体分子数改变的可逆反应:必须要保证化学计量数之比与原来相同;同时必须保证平衡式左右两边同一边的物质的量与原来相同.
第二类:对于反应前后气体分子数不变的可逆反应:只要反应物的物质的量的比例与原来相同即可视为二者等效.
(2)定温,定压的等效平衡
只要保证可逆反应化学计量数之比相同即可视为等效平衡.
化学反应进行的方向
反应熵变与反应方向:
熵:物质的一个状态函数,用来描述体系的混乱度,符号为S. 单位:J*mol-1*K-1
体系趋向于有序转变为无序,导致体系的熵增加,这叫做熵增加原理,也是反应方向判断的依据..
(3)同一物质,在气态时熵值最大,液态时次之,固态时最小.即S(g)〉S(l)〉S(s)
反应方向判断依据
在温度、压强一定的条件下,化学反应的判读依据为:
ΔH-TΔS〈0 反应能自发进行
ΔH-TΔS=0 反应达到平衡状态
ΔH-TΔS〉0 反应不能自发进行
注意:(1)ΔH为负,ΔS为正时,任何温度反应都能自发进行
(2)ΔH为正,ΔS为负时,任何温度反应都不能自发进行
水溶液中的离子平衡
一、弱电解质的电离
定义:电解质: 在水溶液中或熔化状态下能导电的化合物,叫电解质
非电解质 在水溶液中或熔化状态下都不能导电的化合物
强电解质 在水溶液里全部电离成离子的电解质
弱电解质 在水溶液里只有一部分分子电离成离子的电解质
电解质与非电解质本质区别:
电解质——离子化合物或共价化合物 非电解质——共价化合物
注意:①电解质、非电解质都是化合物 ②SO2、NH3、CO2等属于非电解质
③强电解质不等于易溶于水的化合物(如BaSO4不溶于水,但溶于水的BaSO4全部电离,故BaSO4为强电解质)——电解质的强弱与导电性、溶解性无关.
电离平衡:在一定的条件下,当电解质分子电离成 离子的速率 和离子结合成 时,电离过程就达到了 平衡状态 ,这叫电离平衡.
影响电离平衡的因素:
温度:电离一般吸热,升温有利于电离.
B、浓度:浓度越大,电离程度 越小 ;溶液稀释时,电离平衡向着电离的方向移动.C、同离子效应:在弱电解质溶液里加入与弱电解质具有相同离子的电解质,会 减弱 电离.D、其他外加试剂:加入能与弱电解质的电离产生的某种离子反应的物质时,有利于电离.
电离方程式的书写:用可逆符号 弱酸的电离要分布写(第一步为主)
电离常数:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数.叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱. )
表示方法:AB A++B- Ki=[ A+][ B-]/[AB]
影响因素:
a、电离常数的大小主要由物质的本性决定.
b、电离常数受温度变化影响,不受浓度变化影响,在室温下一般变化不大.
C、同一温度下,不同弱酸,电离常数越大,其电离程度越大,酸性越强.如:H2SO3>H3PO4>HF>CH3COOH>H2CO3>H2S>HClO
二、水的电离和溶液的酸碱性
水电离平衡::
水的离子积:KW = c[H+]?c[OH-]
25℃时, [H+]=[OH-] =10-7 mol/L ; KW = [H+]*[OH-] = 1*10-14
注意:KW只与温度有关,温度一定,则KW值一定
KW不仅适用于纯水,适用于任何溶液(酸、碱、盐)
2、水电离特点:(1)可逆 (2)吸热 (3)极弱
3、影响水电离平衡的外界因素:
①酸、碱 :抑制水的电离 KW〈1*10-14
②温度:促进水的电离(水的电离是 吸 热的)
③易水解的盐:促进水的电离 KW 〉 1*10-14
4、溶液的酸碱性和pH:
(1)pH=-lgc[H+]
(2)pH的测定方法:
酸碱指示剂—— 甲基橙 、 石蕊 、 酚酞 .
变色范围:甲基橙 3.1~4.4(橙色) 石蕊5.0~8.0(紫色) 酚酞8.2~10.0(浅红色)
pH试纸 —操作 玻璃棒蘸取未知液体在试纸上,然后与标准比色卡对比即可 .
注意:①事先不能用水湿润PH试纸;②广泛pH试纸只能读取整数值或范围
三 、混合液的pH值计算方法公式
强酸与强酸的混合:(先求[H+]混:将两种酸中的H+离子物质的量相加除以总体积,再求其它) [H+]混 =([H+]1V1+[H+]2V2)/(V1+V2)
强碱与强碱的混合:(先求[OH-]混:将两种酸中的OH 离子物质的量相加除以总体积,再求其它) [OH-]混=([OH-]1V1+[OH-]2V2)/(V1+V2) (注意 :不能直接计算[H+]混)
强酸与强碱的混合:(先据H+ + OH- ==H2O计算余下的H+或OH-,①H+有余,则用余下的H+数除以溶液总体积求[H+]混;OH-有余,则用余下的OH-数除以溶液总体积求[OH-]混,再求其它)
稀释过程溶液pH值的变化规律:
强酸溶液:稀释10n倍时,pH稀 = pH原+ n (但始终不能大于或等于7)
弱酸溶液:稀释10n倍时,pH稀 〈 pH原+n (但始终不能大于或等于7)
强碱溶液:稀释10n倍时,pH稀 = pH原-n (但始终不能小于或等于7)
弱碱溶液:稀释10n倍时,pH稀 〉 pH原-n (但始终不能小于或等于7)
不论任何溶液,稀释时pH均是向7靠近(即向中性靠近);任何溶液无限稀释后pH均接近7
稀释时,弱酸、弱碱和水解的盐溶液的pH变化得慢,强酸、强碱变化得快.
强酸(pH1)强碱(pH2)
混和计算规律
1、若等体积混合
pH1+pH2=14 则溶液显中性pH=7
pH1+pH2≥15 则溶液显碱性pH=pH2-0.3
pH1+pH2≤13 则溶液显酸性pH=pH1+0.3
2、若混合后显中性
pH1+pH2=14 V酸:V碱=1:1
pH1+pH2≠14 V酸:V碱=1:10〔14-(pH1+pH2)〕
六、酸碱中和滴定:
盐类的水解(只有可溶于水的盐才水解)
盐类水在水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合生成弱电解质的反应.
水解的实质: 水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合,破坏水的电离,是平衡向右移动,促进水的电离.
盐类水解规律:
①有 弱 才水解,无弱不水解,越弱越水解;谁 强显谁性,两弱都水解,同强显中性.
②多元弱酸根,浓度相同时正酸根比酸式酸根水解程度大,碱性更强. (如:Na2CO3 >NaHCO3)
盐类水解的特点:(1)可逆(与中和反应互逆) (2)程度小 (3)吸热
影响盐类水解的外界因素:
①温度:温度越 高 水解程度越大 (水解吸热,越热越水解)
②浓度:浓度越小,水解程度越 大 (越稀越水解)
③酸碱:促进或抑制盐的水解(H+促进 阴离子 水解而 抑制 阳离子水解;OH -促进阳离子水解而抑制阴离子水解)
酸式盐溶液的酸碱性:
①只电离不水如HSO4- 显 酸 性
②电离程度>水解程度,显 酸 性 (如: HSO3- 、H2PO4-)
③水解程度>电离程度,显 碱 性 (如:HCO3- 、HS- 、HPO42-)
双水解反应:
构成盐的阴阳离子均能发生水解的反应.双水解反应相互促进,水解程度较大,有的甚至水解完全.使得平衡向右移.
常见的双水解反应完全的为:Fe3+、Al3+与AlO2-、CO32-(HCO3-)、S2-(HS-)、SO32-(HSO3-);S2-与NH4+;CO32-(HCO3-)与NH4+其特点是相互水解成沉淀或气体.双水解完全的离子方程式配平依据是两边电荷平衡,如:2Al3+ + 3S2- + 6H2O == 2Al(OH)3↓+ 3H2S↑
盐类水解的应用:
水解的应用 实例 原理
1、净水
明矾净水 Al3++3H2O Al(OH)3(胶体)+3H+
△
去油污 用热碱水冼油污物品 CO32-+H2O HCO3-+OH-
药品的保存 ①配制FeCl3溶液时常加入少量盐酸 Fe3++3H2O Fe(OH)3+3H+
②配制Na2CO3溶液时常加入少量NaOH CO32-+H2O HCO3-+OH-
4、制备无水盐 由MgCl2`6H2O制无水MgCl2 在HCl气流中加热 若不然,则:
MgCl2`6H2O Mg(OH)2+2HCl+4H2O
Mg(OH)2 MgO+H2O
泡沫灭火器 用Al2(SO4)3与NaHCO3溶液混合 Al3++3HCO3-=Al(OH)3↓+3CO2↑
6、比较盐溶液中离子浓度的大小 比较NH4Cl溶液中离子浓度的大小 NH4++H2O NH3`H2O+H+
c(Cl-)>c(NH4+)>c(H+)>c(OH)-
水解平衡常数 (Kh)
对于强碱弱酸盐:Kh =Kw/Ka(Kw为该温度下水的离子积,Ka为该条件下该弱酸根形成的弱酸的电离平衡常数)
对于强酸弱碱盐:Kh =Kw/Kb(Kw为该温度下水的离子积,Kb为该条件下该弱碱根形成的弱碱的电离平衡常数)
电离、水解方程式的书写原则
多元弱酸(多元弱酸盐)的电离(水解)的书写原则:分步书写
注意:不管是水解还是电离,都决定于第一步,第二步一般相当微弱.
多元弱碱(多元弱碱盐)的电离(水解)书写原则:一步书写
溶液中微粒浓度的大小比较
☆☆基本原则:抓住溶液中微粒浓度必须满足的三种守恒关系:
①电荷守恒::任何溶液均显电 中 性,各阳离子浓度与其所带电荷数的乘积之和=各阴离子浓度与其所带电荷数的乘积之和
②物料守恒: (即原子个数守恒或质量守恒)
某原子的总量(或总浓度)=其以各种形式存在的所有微粒的量(或浓度)之和
③质子守恒:即水电离出的H+浓度与OH-浓度相等. - 1年前
相关推荐
- {访高人}高二平面基本性质正三角形ABO的边长为a,在画它的水平放置的直观图时,建立如图所示的直角坐标系xOy,则它的直
{访高人}高二平面基本性质
正三角形ABO的边长为a,在画它的水平放置的直观图时,建立如图所示的直角坐标系xOy,则它的直观图的面积是___________.
------------------{图在这}↓↓↓↓↓

√6/16×a² 清晰完整 dl07141年前1
dl07141年前1 -
 hzy160435 共回答了13个问题
hzy160435 共回答了13个问题 |采纳率84.6%现在的底边 = a,腰 = a,高 = a×sin60°= (√3)a/2
角度倾斜45°后,并缩短一半后,
高变成了斜边为(√3)a/4的小直角三角形的斜边,
小直角三角形的高 = h = (√3)a/4×sin45°
= (√3)a/4×(√2)/2
= (√6)a/8
此小直角三角形的高 = 直观图的高
所以,
直观图的底 = a
直观图的高 = (√6)a/8
直观图的面积 = ½×a×(√6)a/8 = (√6)a²/161年前查看全部
- 一道高二化学等效平衡题,本人尚未学到,目前正自学这部分内容,有些地方有点不明白,
一道高二化学等效平衡题,本人尚未学到,目前正自学这部分内容,有些地方有点不明白,
将3molA和1molB混合于一体积可变的密闭容器P中,以此时温度、压强和体积作为起始条件,发生如下反应:3A(g)+B(g)= 2C(g)+D(g),达到平衡时C的浓度为w mol/L.,则
(1)保持原始起始温度和体积不变,要使平衡后C浓度仍为w mol/L,应按下列哪种配比向容器Q中充入有关物质?
A 3molA+1molB B 4molC+2molD C 1.5molA+0.5molB+1molC+0.5molD D 无法判断
(2)现将2molC和2molD按起始温度和体积充入容器Q中,保持温度和体积不变,平衡时C的浓度为V mol/L,则V和w的关系是
A.V>w B.V thids1年前1
thids1年前1 -
 小西小西西 共回答了17个问题
小西小西西 共回答了17个问题 |采纳率100%1里我要是没记错的话好像是体积和温度不变的前提下对于反应体积变化不为零的反应全折成反应物必须是同样的量才是等效平衡.而对于体积和压强不变的前提下则是等于同样的比值即可.所以这两种不同条件下等效平衡的比较是不同的.
能说A和C达到的是同一个平衡,B相当于在AC的基础上增加了反应物因此平衡正向移动.我觉得也是能得出来AC的平衡程度要低于P容器中的,但是加多少能够达到P中的那个反应程度,这个确实算不出来,所以无法判断.
2的话在2molC1molD的时候就比w的时候反应程度低,又加了生成物反应程度更低,所以C剩的更多,所以V要大.
简单的讲……就是我能比大小,但是要加多少能把缺的这么多恰好添上,在现有的这些数据基础上我算不出来.1年前查看全部
- 高二上学期的数学难吗?谢谢
 zxylly20011年前3
zxylly20011年前3 -
 安安1204 共回答了24个问题
安安1204 共回答了24个问题 |采纳率91.7%嗯...个人认为不算太难~
总共有3章~
第六章:关于不等式的,这一章还算简单...
第七章:关于直线和圆的方程,这儿可能有点儿难,因为本人就不喜欢这种几何~公式挺多的~!
第八章:关于圆锥曲线方程的,里面包括椭圆,双曲线和抛物线,好好学还是比较简单的~1年前查看全部
- 高二上学期数学和物理3-1较难的地方(哪一章或哪一节)
 罗乾1年前3
罗乾1年前3 -
 小子天空 共回答了15个问题
小子天空 共回答了15个问题 |采纳率80%必修5主要是数列很重要.经常会出压轴题.
物理3-1.磁场也就是第三章比较难,经常会跟电场混在一起,第二章其实很多都有初中的基础了,在基础上加深了而已,而第一章电场主要是概念问题,第三章题目明显比前两章难.1年前查看全部
- 谁会做高二数学练习册p25、26页上24,25,26题啊
谁会做高二数学练习册p25、26页上24,25,26题啊
1 zxcv1451年前1
zxcv1451年前1 -
 睡睡与WDSL 共回答了17个问题
睡睡与WDSL 共回答了17个问题 |采纳率88.2%你确定你学过有一张打星号的东西?自己去看看
24.通项是10的n次方+2的(N-1)次方.第一项是10+1,一个用等差数列前n项和公式,一个用等比数列前n项和公式.再加起来.
25.通项为1-(10的-n次方).然后n个1加一起,再用等比数列前n项和公式,加一起.
26.通项为1/3(1/(3n-2)-1/(3n+1)).Sn=1/3(1-1/4+1/4-1/7+.+1/(3n-5)-1/(3n-2)+1/(3n-2)-1/(3n+1)).中间的抵消,只剩1/3(1)-1/(3n+1)).
阿门上帝保佑你看了不会烦1年前查看全部
- 高二物理公式t=2mv/Eq的推导过程
 公子楚的小野花花1年前2
公子楚的小野花花1年前2 -
 leeleleele 共回答了25个问题
leeleleele 共回答了25个问题 |采纳率96%Eqs=1/2mv^2
s=vt/2
带电粒子在匀强电场中从静止开始作匀加速运动?
那个2没推出来...1年前查看全部
- 高二物理不理解为什么静电平衡书本上是这样的,将金属导体放入电场为E0的电场中然后自由电子如图那样运动构成与外界等大相反的
高二物理不理解为什么静电平衡
 书本上是这样的,将金属导体放入电场为E0的电场中然后自由电子如图那样运动构成与外界等大相反的内电场导致E=0.但是当内部这样左边是负右边是正时,他们产生的场强也是匀强电场吗?不然的话不就是内部的场强是中间小,向两边递增了,内部各处电场都不相等,怎么同时和外部恒定的电场E0平衡?
书本上是这样的,将金属导体放入电场为E0的电场中然后自由电子如图那样运动构成与外界等大相反的内电场导致E=0.但是当内部这样左边是负右边是正时,他们产生的场强也是匀强电场吗?不然的话不就是内部的场强是中间小,向两边递增了,内部各处电场都不相等,怎么同时和外部恒定的电场E0平衡?还有就是书上说导体中如果合电场不为0,自由电子就会移动,因此合电场为0,如果导体中某部分的电子受外部电场全都转移地方了,那么这部分的电场就算不为0,也没有电子转移了吧?
 tom4011年前1
tom4011年前1 -
 喜欢你没道理 共回答了22个问题
喜欢你没道理 共回答了22个问题 |采纳率72.7%这个也比较好理那是因为将金属放在静电场中时,由于金属是由带正电的原子核与带负电的自由电子构成,在外电场的作用下,自由电子移向一端,这样金属导体一段出现正电一端出现负电,两端出现电势差在内部形成了电场,当外部的电场比内部的强,自由电子就会移动,直到内部的场强与外部大小相等是,自由电子才能停止移动,此时就达到了一种静电平衡,也可以从力学的角度理就是金属内部的自由电子在外电场的作用下受力方向与外电场的方向相反,所以就移动,但是移动的结果使得自由电子集中到一端时,金属内部的两端出现电势差,所以内部就产生电场,对于内部的自由电子就受两个力,一个是外部的电场力,一个是内部的电场力,当外部的电场力大于内部的电场力时,自由电子就会不停的移向一端,使得两端的电势差增大,场强继续增强,知道某一时刻就会与外电场大小相等,方向相反,此时,内部的自由电子受力平衡,内部任意一点的合场强为零,即静电平衡1年前查看全部
- 紧急!高二数列问题!已知数列{an}是等差数列且a1=1,a1+a2+a3=12,设Sn是等比数列{bn}的前n项和,b
紧急!高二数列问题!
已知数列{an}是等差数列且a1=1,a1+a2+a3=12,设Sn是等比数列{bn}的前n项和,b1=1/a1、b2=1/a2,求lim(n→∞)Sn.
(我算到an=2n+1,后面怎么做?)
我算到an=2n,后面怎么做 ? 打错了,是a1=2. superzone1年前1
superzone1年前1 -
 阿魔熊 共回答了14个问题
阿魔熊 共回答了14个问题 |采纳率92.9%由a1=1
a1+a3=2a2
a1+a2+a3=12
得到:a2=4
a3=7
所以,b1=1
b2=1/4
q=1/4
bn=(1/4)^(n-1)
所以,
1-(1/4)^n
sn=---------
3/41年前查看全部
- 高二数学已知函数f(x)=kx+7\kx+4kx+3,若倒Ax∈R,f(x)有意义,则k的取值范围是()
高二数学已知函数f(x)=kx+7kx+4kx+3,若倒Ax∈R,f(x)有意义,则k的取值范围是()
更正kx+7是分子,kx²+4kx+3是分母 绍兴书画社zz1年前3
绍兴书画社zz1年前3 -
 花儿谢了 共回答了24个问题
花儿谢了 共回答了24个问题 |采纳率100%任意实数x都使f(x)有意义,x=0时,恒成立;x等于零时,只要满足分母不等于零即可,就是分母所在二次函数的判别式小于等于0,即k^2-4*k*3小于等于01年前查看全部
- 某高中有学生2000人,其中高一年级有1000人,高二年级有500人,高三年级有500人,先采用分层抽样的方法抽取一个容
某高中有学生2000人,其中高一年级有1000人,高二年级有500人,高三年级有500人,先采用分层抽样的方法抽取一个容量为72的样本,那么高二年级抽取的学生个数应为多少人?
 春天一把火1年前1
春天一把火1年前1 -
 qwwk 共回答了15个问题
qwwk 共回答了15个问题 |采纳率100%72÷2000=3.6%
500×3.6%=18(人)1年前查看全部
- 高二英语下册第5单元阅读的翻译
 逍遥68121年前3
逍遥68121年前3 -
 cycqq 共回答了11个问题
cycqq 共回答了11个问题 |采纳率90.9%你是今年高二吗 What is the title of this unit?1年前查看全部
- 高二必修四三角函数.已知函数f(x)=2-cos^2x+2sinxcosx-3sin^x.求f(x)最小正周期.当x属于
高二必修四三角函数.
已知函数f(x)=2-cos^2x+2sinxcosx-3sin^x.求f(x)最小正周期.当x属于〔四分之派,二分之派〕、求f(x)值域. 口口棉花糖1年前3
口口棉花糖1年前3 -
 最爱最爱小ll 共回答了22个问题
最爱最爱小ll 共回答了22个问题 |采纳率90.9%f(x)=2-1+sin2x-2sin²x=sin2x+cos2x+1=√2sin(2x+π/4)+1
x+π/4∈(π/2,3π/4),f(x)∈(2,√2+1) ,最小正周期是π1年前查看全部
- ★☆高人进)高二直观图斜二侧如果一个水平放置的平面图形的直观图是一个腰长为1的等腰直角三角形,那么原平面图形的周长是?
 丁丁丁当当当1年前1
丁丁丁当当当1年前1 -
 yanghou 共回答了20个问题
yanghou 共回答了20个问题 |采纳率90%设直观图为RT等腰三角形ABC,〈A=90度,
则A点对应点是从B点作垂线,截长度A'B=2AB,连结A'C,三角形A'BC就是原三角形,A'B=2,BC=√2,A'C=√(A'B^2+BC^2)=√6,
故原三角形周长=2+√2+√6.1年前查看全部
- 有关电势的一道高二物理题的几个疑惑求解答
有关电势的一道高二物理题的几个疑惑求解答
如图所示,导体棒AB靠近带正电的导体Q放置.用手接触B端,移去手指再移去Q,导体带何种电荷 __________ .若手的接触点改在A端,情况又如何___________

答案是负电荷,负电荷
我想问的是第二个空,若手的接触点改在A端,因为A带负电荷,那么A的电势就比大地小了.所以A的负电荷要往大地移动,移开手和Q后电荷均匀分布,则导体就带正电了.这是我所理解的.错在哪里呢?
其次,根据我的理解,A的电势比大的小,B的电势比大地大,这不是和导体AB是等势体的结论矛盾了吗?
还有一个问题,为什么等势体的电场线不能从自身的正极指向负极呢?
 豆浆店白展糖1年前1
豆浆店白展糖1年前1 -
 23asp 共回答了15个问题
23asp 共回答了15个问题 |采纳率93.3%你的错在A端与B端的电势是相等的,它们是导体啊,导体上各点都是等电势的,电势高低并不与带电荷的正负有绝对关系,是与电场的分布有关的,你可以试着画一画电场线再分析这个题
而且电场是保守场,沿着电场线电势降低,如过等势体自身上连有同一根电场线,那就会在其自身上产生电势差,自然有问题1年前查看全部
- 高二物理汞柱移动问题中,将玻璃管加热,与将部分气体加热有区别吗?
高二物理汞柱移动问题中,将玻璃管加热,与将部分气体加热有区别吗?
采纳的有分。 奈可优优1年前1
奈可优优1年前1 -
 我爱海云 共回答了15个问题
我爱海云 共回答了15个问题 |采纳率100%有区别,加热部分空气时,只有加热的这部分空气气压增大.而加热导管时,却是所有气体受热,压强增大(液体变化莫认忽略).1年前查看全部
- 高二下学期的数学题目1一个正方体,它的表面涂满了红色,在它的相邻三个面上各切两刀,可得27个小立方块,从中任取2个,其中
高二下学期的数学题目1
一个正方体,它的表面涂满了红色,在它的相邻三个面上各切两刀,可得27个小立方块,从中任取2个,其中恰有1个一面涂有红色,另一个两面涂有红色的概率为
我不要答案,我要过程 我不懂的是为什么1面红色6个。2面的12个。。。解释下1 忝睚1年前1
忝睚1年前1 -
 bdxxdb 共回答了15个问题
bdxxdb 共回答了15个问题 |采纳率86.7%一面红色6个
2面红色12个
3面红色8个
没红色面1个
一面是红色的概率:6/27;
2面红色的概率:12/27;
总概率:(6/27)*(12/27);
答案:(6/27)*(12/27)
我晕,你切一下.看看只有一面带红色的是不是6个?就是6个面中间的那块1年前查看全部
- 跪求高人! 高二有机化学题有由两种有机物组成的液态混合物 ,向其中加入NaOH溶液震荡后静置,溶液分为两层.用分液漏斗分
跪求高人! 高二有机化学题
有由两种有机物组成的液态混合物 ,向其中加入NaOH溶液震荡后静置,溶液分为两层.用分液漏斗分离后,向原混合溶液中加入盐酸,有浑浊现象,说明溶液中有____(写名称)有关化学方程式_____________
大概都有什么和什么的反应啊0.0? 急求!
将原上层溶液滴入浓硫酸 和浓硝酸组成的混合溶液中 并将容器放入50~60度的水浴中加热 得到呈黄色油状液体 病有苦杏仁味 证明原混合溶液中有______ 该反应化学方程式______________________________ 痛哭的人19841年前2
痛哭的人19841年前2 -
 坡哥 共回答了27个问题
坡哥 共回答了27个问题 |采纳率88.9%(1)苯酚,NaOH+苯酚=苯酚钠+H2O 应将等号改成单箭头,我这上面不好打单箭头
(2)苯,反应方程式是甲苯和一个硝酸在浓硫酸做催化剂的条件下加热得到硝基苯和水,硝基苯有苦杏仁味1年前查看全部
- 高二物理---欧姆挡中为啥红进黑出?
高二物理---欧姆挡中为啥红进黑出?
电流不是从正极出吗,可为啥红表笔连的是负极?
还有,除了在欧姆当中,其他电表中也是红进黑出吗? QQAZ1231年前0
QQAZ1231年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 海淀区高二上学期化学先学哪本书?
 1388641年前1
1388641年前1 -
 雨辰风浅 共回答了23个问题
雨辰风浅 共回答了23个问题 |采纳率87%文科生学《化学与生活》,理科生继续学有机.1年前查看全部
- 一根铁丝可围成一个长十五dm宽七dm高二dm的长方体模型如果用这根铁丝围成一个正方体的棱长应该是多少分米?
 羊知冬1年前3
羊知冬1年前3 -
 失落的燃烧 共回答了19个问题
失落的燃烧 共回答了19个问题 |采纳率94.7%81年前查看全部
- 请教一个高二下学期物理问题(带电粒子在磁场中的运动)
请教一个高二下学期物理问题(带电粒子在磁场中的运动)
在一定宽度的范围内,用场强为E(竖直向下)的电场使得初速度为v的,垂直电场方向入射的正离子偏转为 β角.若换做同样宽度的匀强磁场,使该离子穿过磁场时也偏转 β角,求该磁场强度.
答案是Ecos β /v..
.或者给个思路也好啊..我完全没思路啊 septwolfs1年前1
septwolfs1年前1 -
 luyoutianyou 共回答了16个问题
luyoutianyou 共回答了16个问题 |采纳率100%1年前查看全部
- 求证一道高二数学不等式证明题求证:函数f(x)=1/(x+根号x)在其定义域上是减函数
 dce_win1年前4
dce_win1年前4 -
 tripleli 共回答了18个问题
tripleli 共回答了18个问题 |采纳率88.9%定义域x>0
在定义域内,任取01年前查看全部
- 高二圆锥曲线的综合题过原点的一条直线与椭圆C:x²/a²+y²/b²=1(a>b>0)交椭圆于A,B两点,P为椭圆上异于
高二圆锥曲线的综合题
过原点的一条直线与椭圆C:x²/a²+y²/b²=1(a>b>0)交椭圆于A,B两点,P为椭圆上异于A,B的另一点
(1)求椭圆的离心率
(2)过点A切平行于X轴的直线交椭圆于另一点D,直线PA,PD分别交y轴于M,N两点,若OM向量·ON向量=2,求椭圆C的方程
直线PA,PB的斜率乘积为-1/2 陈精1年前1
陈精1年前1 -
 泉诚 共回答了19个问题
泉诚 共回答了19个问题 |采纳率94.7%题目不完整1年前查看全部
- 高二物理安培力问题如图所示,用两条一样的弹簧秤吊着一根铜棒,铜棒所在的虚线框范围内有垂直纸面的匀强磁场,棒中通入自左向右
高二物理安培力问题
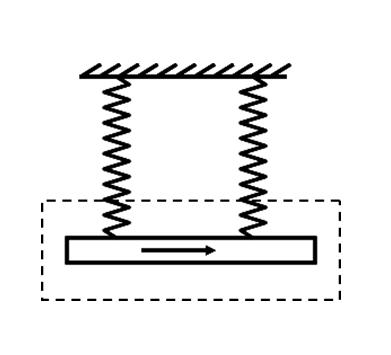
如图所示,用两条一样的弹簧秤吊着一根铜棒,铜棒所在的虚线框范围内有垂直纸面的匀强磁场,棒中通入自左向右的电流.当棒静止时,弹簧秤示数为F1;若将棒中电流反向,当棒静止时,弹簧秤的示数为F2,且F2>F1,根据上面所给的信息,可以确定 ( )
A磁场的方向 B磁感应强度的大小
C安培力的大小 D铜棒的重力如图
 lywapp1年前1
lywapp1年前1 -
 痛苦seu 共回答了21个问题
痛苦seu 共回答了21个问题 |采纳率90.5%图呢1年前查看全部
- 怎样让英语成绩变得稳定我上高二了,英语成绩一直不稳定,请各位传授一下你们的宝贵意见,
 fxc8105b1年前4
fxc8105b1年前4 -
 遗憾生活 共回答了13个问题
遗憾生活 共回答了13个问题 |采纳率100%首先基础语法得弄清,一般《五年高考三年模拟》的语法不错,你要每天看点,还要经常复习.这叫大语法.小语法你要跟着老师走,要建立个语法本,如果以前没建可以借同学的抄一下.还有每天要做两篇阅读,然后弄懂你错的地方.同时培养语感.难度适中.而且单词也要背,至少书上的都得会.然后有时间背背《新概念三》,扩展词汇量.作文每周至少两篇.找老师改改.总之,你得用功.加油!1年前查看全部
- 高二溶液的酸碱度习题若1体积硫酸恰好与10体积pH=11的NaOH溶液完全反应 则两者物质的量浓度纸币为多少
 今生红颜1年前2
今生红颜1年前2 -
 sanweizai 共回答了22个问题
sanweizai 共回答了22个问题 |采纳率100%你看我这个思路可以不啊.我物质的量浓度单位是mol/L,氢离子和氢氧根离子的物质的量是1:1,体积比是1:10,浓度之比就是10:1,硫酸是2元酸,所以硫酸与氢氧化钠的物质的量浓度之比就是5:1了1年前查看全部
- 怎样提高英语阅读速度?我是一名高二的文科生,英语成绩130左右.可是我每一次英语考试时间都非常紧张,有的时候刚好做完,有
怎样提高英语阅读速度?
我是一名高二的文科生,英语成绩130左右.可是我每一次英语考试时间都非常紧张,有的时候刚好做完,有的时候甚至做不完.ABCDE,5篇阅读我大概要用55分钟才做的完,我觉得太慢了,但是我做出来的题目基本上是对的.我想在保证正确率的情况下,提高阅读速度,请各位哥哥姐姐给我一些建议! xiyang_xiyang1年前1
xiyang_xiyang1年前1 -
 喝椰子水看妹妹 共回答了21个问题
喝椰子水看妹妹 共回答了21个问题 |采纳率90.5%平常心对待,平常的时候多看看与英语相关的书籍,可以提高你的速度1年前查看全部
- [提问]高二化学会考的一道计算题~会的进
[提问]高二化学会考的一道计算题~会的进
将碳酸钠和碳酸氢钠的固体混合物44.52g,全部投入到250ml a mol/L盐酸中,待完全溶解后,放出的气体在标准状况下的体积为 b L.(反应前后溶液的体积变化和生成的气体在水中的溶解度忽略不计)
试计算(结果精确到0.01)
(1)若测得反应后的溶液呈中性,则其中Na离子物质的量为 mol.
(2)若酸过量,并测得b=11.2 L,则原混合物中含碳酸氢钠的质量为 g.
(3)若反应后的溶液呈强酸性,则b的取值范围是 .
请对答案进行以下讲解,最好可以把三个小题的答案都写下来!Thank you! suede8181年前1
suede8181年前1 -
 saitsmokey 共回答了21个问题
saitsmokey 共回答了21个问题 |采纳率81%(1)呈中性说明刚好完全反应,则n(Na+)=n(Cl-)=a mol/L×0.25L=0.25a mol
(2)0.11g
真的很遗憾,这上面讲化学题真的不方便!又没法上传图片,如果可以我在别的地方给你把解题详细过程给你写出来,剪了,粘贴在这上面就可以了!1年前查看全部
- 高二双曲线的性质(及!)已知三角形ABC中的两个顶点B(0,6),C(0,-6),AB边与 AC边所在的直线的斜率之积是
高二双曲线的性质(及!)
已知三角形ABC中的两个顶点B(0,6),C(0,-6),AB边与 AC边所在的直线的斜率之积是4/9,求顶点A的轨迹(请写出过程, dreamyubo1年前1
dreamyubo1年前1 -
 毛手套 共回答了24个问题
毛手套 共回答了24个问题 |采纳率83.3%先设A(x,y)
然后根据题意,得到:[(6-y)/(-x)]*[(-6-y)/(-x)]=4/9
然后整理,就得到x,y的等式了.1年前查看全部
- 如何巧妙背单词!我英语基础等于零,到我现在已经高二可,我想从背单词开始,亲们!
 CQVITAMIN1年前4
CQVITAMIN1年前4 -
 aliz7 共回答了19个问题
aliz7 共回答了19个问题 |采纳率94.7%网上方法很多的啊,平时老师也会说的啊.
我一般用音标(会念就会写)、联想(和已经记忆了的东西产生联系)、词缀(背了词缀单词可以自己推断意思)…还有死记法…这些我觉得足够了
不过最重要的是重复,我一般单词背7遍才能保证熟悉度.祝成功1年前查看全部
- 我听别人说高二开始的电学和初中的没什么联系啊,几乎重新学的,可是我看到高二的欧姆定律那一章还是有什么串联并联啊..*而且
我听别人说高二开始的电学和初中的没什么联系啊,几乎重新学的,可是我看到高二的欧姆定律那一章还是有什么串联并联啊..*而且好像还没怎么细讲,就大体讲一下基础的就直接.(我最不行的..)我电路图根本就是瞎的嘛,现在给我一个最简单的电路图我一定搞不清楚.
欧姆定律.从现在开始学可以吗?直接看高二的参考书还是看以前的? happyant19771年前2
happyant19771年前2 -
 99zpd 共回答了13个问题
99zpd 共回答了13个问题 |采纳率84.6%关系不大
高中物理很难
数学基础不好的
千万别选1年前查看全部
- 高二英语必修五 单词音标不用英文
 余遇海豚1年前1
余遇海豚1年前1 -
 zwqmy 共回答了19个问题
zwqmy 共回答了19个问题 |采纳率89.5%我有书,给你照下来可以吗 追问: = = 我也有书我就是想要书里的 音标 全部抄出来然后打印来‘默写, 回答: 你有书,那你就抄下来吧,我初中也抄过单词,然后默写呢 追问: = = 就不想抄而且自己字不好看抄了可能自己看不懂,O(∩_∩)O 回答: 额,那你是想让别人给你抄?然后给你发过去? 追问: = = 也可以打在 word文档 发给我 不过我觉得这两种基本不会实现 只是来碰碰运气 回答: 有书的基本都是高二三的学生,谁会 有时间给你 抄,没书的自然就不行了,所以学习要靠自己,你要是真想学习,想 背单词 ,找父母或同学考你不就行了,想学习的话总会有办法的.你要是觉得我说的对,请采纳,写这么多也挺累的1年前查看全部
- 高二化学【急】高分追加]下列各组微粒半径比值最小的是A.O2-/F- B.Al3+/S2- C.Na/Na+ D.S/C
高二化学【急】高分追加]
下列各组微粒半径比值最小的是
A.O2-/F- B.Al3+/S2- C.Na/Na+ D.S/Cl
【答案】:B
我想知道详细的过程和原因,谢谢. 爱兮1年前1
爱兮1年前1 -
 那一刀的疼痛 共回答了21个问题
那一刀的疼痛 共回答了21个问题 |采纳率85.7%AB比较,铝离子和氧离子的电子数相同,但铝的质子数多,电子对离子半径有扩大作用,而质子则有收缩作用,所以铝比氧的小.同理硫比氟的大,比值最小.C选项,只相差一个电子,半径比更接近1,而且用上述法分析,电子数与质子数只差1,作用效果不明显.同理D中质子数只差一,也不明显,1年前查看全部
- 高二物理带电粒子在复合场中运动 (8)(9)
高二物理带电粒子在复合场中运动

(8)(9)

 舞翼蝶1年前1
舞翼蝶1年前1 -
 zhy_1984 共回答了20个问题
zhy_1984 共回答了20个问题 |采纳率90%当粒子与EF相切时,不能从EF射出,此时d=r+rcosθ,再由qvb=mv2/r解得临界速度,当速度比这个速度大时就能从EF边射出1年前查看全部
- 请教高二数学高手!已知直线L的倾斜角为a,且2sina-cosa/5cosa+3sina=3/11,求直线L的斜率.希望
请教高二数学高手!
已知直线L的倾斜角为a,且2sina-cosa/5cosa+3sina=3/11,求直线L的斜率.
希望有过程啊! 小惜20031年前1
小惜20031年前1 -
 linly_777 共回答了21个问题
linly_777 共回答了21个问题 |采纳率95.2%K=tan(a)
原式分子分母同时除以 cos(a),得到2*tan(a)-1/5+3*tan2(a)=3/11,
即可求得直线的斜率tan(a)=2.
得到斜率为2.1年前查看全部
- 【高二化学】有机化学式子的判断》》》
【高二化学】有机化学式子的判断》》》
某有机物X的分子式为C9H14,经催化加氢后得到分子式为C9H18的饱和化合物
由题目分析,有机物X经加氢后只能得到C9H18的饱和有机物,这表明有机物X中含有一个碳环. 海与天交接点1年前2
海与天交接点1年前2 -
 wang550618 共回答了18个问题
wang550618 共回答了18个问题 |采纳率77.8%因为C9H18是饱和化合物 既然加氢了就说明双键三键什么的都没了,但得到的是C9H18,如果是直链的话,饱和的应该是C9H20
这样就只有一种可能,有一个碳环,因为碳环也算一个不饱和度1年前查看全部
- 高二数学运算(含对数运算)(lg3)*2^(n-1)=lg[(Xn+2)/(Xn-2)]求Xn
 la流浪记1年前2
la流浪记1年前2 -
 termno 共回答了15个问题
termno 共回答了15个问题 |采纳率100%因为(lg3)*2^(n-1)=lg[(Xn+2)/(Xn-2)]
所以3^(2^(n-1))=(Xn+2)/(Xn-2)
所以9^(n-1)=1+1/(Xn-2)
所以Xn-2=1/(9^(n-1)-1)
所以Xn=……1年前查看全部
- 高二物理静电场专题大题.问第3小问中损失的机械能是怎么想的?
 北飲狂刀1年前2
北飲狂刀1年前2 -
 乔灌争辉 共回答了10个问题
乔灌争辉 共回答了10个问题 |采纳率90%这个应该这么理解,如果没损失机械能的话,碰撞之后应该回到P点,正因为谁损失了只能回到Q点,损失了多少,就是在QP这段你还需要做的功对不对.1年前查看全部
- 高二古典概型如果从一排10盏灯中关掉3盏灯,那么关掉的是互不相邻的三盏灯的概率是_______(说明过程)
 zwjch19751年前3
zwjch19751年前3 -
 inzyc 共回答了18个问题
inzyc 共回答了18个问题 |采纳率88.9%逐个考虑呗.
共有10*9*8/6=120种情况
一、第一个关1
(1)再关3,第三盏灯可以关5~10,共6种情况
(2)再关4,第三盏灯可以关6~10,共5种情况
(3)再关5,第三盏灯可以关7~10,共4种情况
(4)再关6,第三盏灯可以关8~10,共3种情况
(5)再关7,第三盏灯可以关9~10,共2种情况
(6)再关8,第三盏灯可以关10,共1种情况
共21种情况
同理
二、第一个关2 共15种情况
三、第一个关3 共10种情况
四、第一个关4 共6种情况
五、第一个关5 共3种情况
六、第一个关6 共1种情况
关掉的是互不相邻的三盏灯共:21+15+10+6+3+1=56种情况
概率为:56/120=7/151年前查看全部
- 高二教材多用电简化电路图,测电流时图中1、2哪个量程大?为什么?求详解!
高二教材多用电简化电路图,测电流时图中1、2哪个量程大?为什么?求详解!

?t=1319964427484接在1,2位置处时哪个的电流大,哪个的量程大?求详解!
 查无些人1年前1
查无些人1年前1 -
 中日苏蒙 共回答了11个问题
中日苏蒙 共回答了11个问题 |采纳率90.9%测电流时图中1 量程大
电流表是表头同分流电阻并联而成的.分流电阻的阻值越小,分流约明显,即只有电流很大时,表头(微安表)才能满偏,故,此时的量程最大.
该题图中档位打到1时,还有一个电阻同表头串联分压.故,只有电流更大时,表头才能满偏.所以,在图中的1位,电流的量程最大.1年前查看全部
- 求自贡市05-06,07-08,09-10学年度上期末高二化学试题(理科)答案
求自贡市05-06,07-08,09-10学年度上期末高二化学试题(理科)答案
大哥大姐些帮忙查一下!
 sukicoo1年前1
sukicoo1年前1 -
 谁不想团结 共回答了17个问题
谁不想团结 共回答了17个问题 |采纳率100%汗.我觉得你还不如找你同学些要呢.百度上面要遇到自贡的 简直少之又少1年前查看全部
- 高二数学的数列的通项公式,求教怎么解
 wittyjuven1年前0
wittyjuven1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 高二英语填词请帮我把最后两个空填好,不要受我前面误导,有错的帮我纠正,
 jssqzyd1年前2
jssqzyd1年前2 -
 日啤酒爱好者的娘 共回答了16个问题
日啤酒爱好者的娘 共回答了16个问题 |采纳率93.8%elies advertising1年前查看全部
- 高手们!高二数学关于圆的填空题一道~等待中!……
高手们!高二数学关于圆的填空题一道~等待中!……
两圆x^2+y^2=9与(x-6)^2+y^2=1的外公切线的方程为______
求过程,谢谢~
stampzh - 职场新人 三级这么做的理由是? spysun1年前3
spysun1年前3 -
 165146116 共回答了21个问题
165146116 共回答了21个问题 |采纳率85.7%画图,作两条外公切线,并设它们交于点P,切点为A,B,圆心为O,C.
则|CB|/|AO|=|PC|/|PO|
即:1/3|=|PC|/|PO|
所以点P分有向线段CO的比λ=-1/3,而点O(0,0),C(6,0)
∴点P坐标为(9,0)
设外公切线的方程为:x=my+9,圆心O(0,0)到外公切线的距离为3.
∴|-9|/√(1+m²)=3
解得m=±2√2
∴两圆x^2+y^2=9与(x-6)^2+y^2=1的外公切线的方程为:x-2√2y-9=0和x+2√2y-9=01年前查看全部
- 高二生物 激素调节 急对人体内水平衡调节的叙述,正确的是:A.在神经调节和激素调节的共同作用下,主要通过肾脏来完成B.喝
高二生物 激素调节 急
对人体内水平衡调节的叙述,正确的是:
A.在神经调节和激素调节的共同作用下,主要通过肾脏来完成
B.喝啤酒过多时,垂体分泌的抗利尿激素减少
我怎么觉的都对啊?~ chl349421年前1
chl349421年前1 -
 冷月tyf 共回答了16个问题
冷月tyf 共回答了16个问题 |采纳率93.8%抗利尿激素是由下丘脑分泌的.
这个错误的确不明显.1年前查看全部
- 电池容量与放电状态有关?电池容量与放电状态有关吗?高二物理课本这样写的:"同样的电池,小电流,间断性放电就比大电流,连续
电池容量与放电状态有关?
电池容量与放电状态有关吗?
高二物理课本这样写的:
"同样的电池,小电流,间断性放电就比大电流,连续放电的容量大"
如果是真的,那是为什么?
还有电池的体积越大,容量越大,其内阻就越小,为什么? 亿家缘1年前2
亿家缘1年前2 -
 月末幽灵 共回答了19个问题
月末幽灵 共回答了19个问题 |采纳率89.5%什么垃圾课本啊,纯粹误导学生.
容量是电芯固有的,只是小电流能发挥95%容量,大电流可能只能85%.
另外,大体积说明里面化学物质多,可以反应的时间就长,容量自然大.
内阻,粗的导线比细的内阻小,是一样的道理.1年前查看全部
- 高二立体几何3有一根长5厘米,底面半径为0.5厘米的圆柱形铁管,用一段铁丝在铁管上缠绕4圈,并使铁丝的两个端点落在圆柱的
高二立体几何3
有一根长5厘米,底面半径为0.5厘米的圆柱形铁管,用一段铁丝在铁管上缠绕4圈,并使铁丝的两个端点落在圆柱的同一母线的两端,则铁丝的最短长度为多少 zzh96881年前1
zzh96881年前1 -
 真爱你的云168 共回答了23个问题
真爱你的云168 共回答了23个问题 |采纳率82.6%我是首师大数学系的,中学知识早忘了,仅作为参考.
lz仔细想一想,你把圆柱侧面展开,长宽分别为∏、5
绕四圈又要铁丝首尾都在母线上,那么不妨让侧面延长四倍.
这样这四倍的侧面所形成的矩形的对角线就是所求:长:4∏,宽:5
用勾股定理求出:√(16∏^2+25)1年前查看全部
- 【高二化学一轮复习】终于突破瓶颈
【高二化学一轮复习】终于突破瓶颈
I'm so happy that 我的化学终于突破瓶颈了,it's to say that 很多以前要看很久或者看解析都看不懂的题目现在可以比较轻松甚至是很轻松地做出来了。I want to ask you that 对于现在这种情况应该怎么做才能把化学学到最好甚至变成优势提分的科目呢?
ps:现在我居然会觉得化学是一门很有趣的学科(我是不是疯了oh my gad~)With the help of you ,I think i can do better . bear45871年前2
bear45871年前2 -
 pundary 共回答了15个问题
pundary 共回答了15个问题 |采纳率86.7%多做题 不知道的就翻书= = 顺其自然就好吧 我高中的时候也是这样的 高一化学不好 到高二就开始变成优势学科了 高三复习的时候基本对于那个知识点在哪本书上大概多少页我都知道了 加油吧 骚年= =
来自华中科技大学化学与化工院 = =1年前查看全部
大家在问
- 1若方程x的平方+ax+3=0有两个实数根,一个根大于1,一个根小于1,求a的取值范围
- 2形容雨的词语,5个以上
- 3修一条路,甲需12天完成,乙需18天完成.甲先修了两天,剩下的由甲乙合作,完成之后,甲修了多少天?
- 4(x+a)(x+b)=x2+(a+b)x+ab 这个公式怎么推算出来的?
- 5求help sb with sth的例句(要好的)
- 6鸡兔共有100只.鸡的脚数比兔的脚数多18只.鸡兔各有多少只?
- 7like,what,holidays,you,do to do on连词成句
- 8水解植物蛋白是食品添加剂吗?
- 9签字,用英文如何说
- 10如图,在平行四边形ABCD中,对角线AC、BD相交于点O,BC=18,E为OD的中点,连结CE并延长交AD于点F,求DF
- 11Can you see _____________? A.what he’s reading B.what is he
- 12梯形ABCD中,AD平行于BC,角B=90度,AD=2,AB=3,BC=6,动点P自点A起,沿A-B-C匀速运动.
- 13阅读下文(8分)林尽水源,便得一山,山有小口,仿佛若有光。便舍船,从口入。初极狭,才通人。复行数十步,豁然开朗。土地平旷
- 14二分之一a²-ab+二分之一b²分解因式 -2x的三次方 +4x²-2x
- 15Y1=2X-1与Y2=2分之3-2分之1X的图像 1 、 求交点坐标 2、当X取何值时Y1>Y2,y1<y2


