高铁酸钾在酸性水溶液中分解的离子方程式 .用高铁酸钾与镁组成的碱性电
 桑斥2022-10-04 11:39:541条回答
桑斥2022-10-04 11:39:541条回答高铁酸钾在酸性水溶液中分解的离子方程式 .用高铁酸钾与镁组成的碱性电池的电极反应.

已提交,审核后显示!提交回复
共1条回复
 随便看看撒 共回答了22个问题
随便看看撒 共回答了22个问题 |采纳率86.4%- 化学:4 K2FeO4 + 10 H2SO4 = 4 K2SO4 + 2 Fe2(SO4)3 + 3 O2 ↑+ 10H2O
离子:4 FeO42- + 20 H+ = 4 Fe3+ + 3 O2 ↑+ 10H2O
正极:2 FeO42- + 6 e- + 8 H2O = 2 Fe(OH)3 + 10 OH-
负极:3 Mg - 6e- + 6 OH- = 3 Mg(OH)2
总反应:3 Mg + 2 FeO42- + 8 H2O = 3 Mg(OH)2 + 2 Fe(OH)3 + 4 OH- - 1年前
相关推荐
- 锌和高铁酸钾组成的碱性电池,正负极方程式咋写?正负极的生成物咋判断是什么?、
 二十而狂1年前2
二十而狂1年前2 -
 归零57 共回答了25个问题
归零57 共回答了25个问题 |采纳率88%楼上很完美,只有一个地方错误,就是高铁酸钾一定存在於强碱溶液中,因此氢氧化锌一定会溶解.
负极:Zn-2e-+4OH-=ZnO22-+2H2O
正极:FeO42-+3e-+4H2O=Fe(OH)3+5OH-
总:3Zn+2K2FeO4+2KOH+2H2O=3K2ZnO2+2Fe(OH)31年前查看全部
- 二氧化铅与高铁酸钾谁的氧化性强氯气溶于酒精呢,现象
 dlj77777771年前2
dlj77777771年前2 -
 chris_zhuge 共回答了16个问题
chris_zhuge 共回答了16个问题 |采纳率87.5%高铁酸钾强,无论从电机电势还是从客观的化学反应!
高铁酸钾遇到稀硫酸,立刻分解产生O2,
而二氧化铅遇到稀硫酸,则不会分解!
E(FeO4 2-/Fe3+)==2.2V
E(PbO2/Pb2+)==1.458V
以上参考了大连理工大学无机化学和三校无机化学课本!
氯气溶于酒精呈浅黄绿色!1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂。下列反应可制取K 2 FeO 4 :
高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂。下列反应可制取K 2 FeO 4 :
2Fe(OH) 3 +3Cl 2 +10KOH 2 K 2 FeO 4 +KCl+8H 2 O
K 2 FeO 4 +KCl+8H 2 O
对于该反应,下列说法正确的是A.该反应是置换反应 B.钾元素化合价降低 C.Fe(OH) 3 发生还原反应 D.Cl 2 是氧化剂  我是北斗我怕谁1年前1
我是北斗我怕谁1年前1 -
 不懂乱猜 共回答了17个问题
不懂乱猜 共回答了17个问题 |采纳率88.2%
1年前查看全部
- (1)高铁酸钾与水反应是其将水氧化了吗?但也可能是水做催化剂,高铁酸钾自身发生氧化还原反应,毕竟含四个氧
(1)高铁酸钾与水反应是其将水氧化了吗?但也可能是水做催化剂,高铁酸钾自身发生氧化还原反应,毕竟含四个氧
(2)能将水氧化的物质除了氟气,氟氧化物,氟氙化物,还有什么? aa就来1年前1
aa就来1年前1 -
 cfr138 共回答了20个问题
cfr138 共回答了20个问题 |采纳率90%(1)高铁酸盐钾是六价铁盐,具有很强的氧化性,溶于水中能释放大量的原子氧,从而非常有效地杀灭水中的病菌和病毒.与此同时,自身被还原成新生态的Fe(OH)3.这是一种品质优良的无机絮凝剂,能高效地除去水中的微细悬浮物.更为重要的是它在整个对水的消毒和净化过程中,不产生任何对人体有害的物质.高铁酸盐被科学家们公认为绿色消毒剂.
高铁酸钾极易溶于水,形成类似于高锰酸钾溶液紫红色的溶液.此溶液极不稳定,数分钟后明显分解,变为棕黄色浑浊溶液,高铁酸钾可氧化水而自身分解:
4K2FeO4+4H2O=2Fe2O3+8KOH+3O2
2K2FeO4+5H2O=2Fe(OH)3+4KOH+3/2O2
所以,是高铁酸钾把水氧化了.如果水是催化剂,那水不参加变化,或变化前后都是水.
(2)还有强金属,如钠、钾等1年前查看全部
- 氢氧化钠和氢氧化钾的区别:高铁酸钾的制备中为什么既用氢氧化钠又用氢氧化钾?
 浅吻你的额头1年前1
浅吻你的额头1年前1 -
 seeme1984 共回答了23个问题
seeme1984 共回答了23个问题 |采纳率100%因为要制取高铁酸钠,所以加氢氧化钠.被氧化为高铁酸钠后加氢氧化钾,因为钾比钠活泼,生成氢氧化钠和高铁酸钾.最后降压抽滤,使高铁酸钾析出.1年前查看全部
- (2009•香坊区一模)高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、杀菌
(2009•香坊区一模)高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、杀菌、灭藻的新型、高效的多功能水处理剂.干燥的高铁酸钾在198℃以下是稳定的,受热易分解为氧化铁、金属氧化物和氧气.根据上述信息,请回答下列问题:
(1)高铁酸钾的物理性质是有紫色光泽的晶体有紫色光泽的晶体.
(2)保存高铁酸钾时应注意避免潮湿和受热避免潮湿和受热.
(3)写出高铁酸钾受热分解的化学方程式4K2FeO4
2Fe2O3+4K2O+3O2↑4K2FeO4△ .
2Fe2O3+4K2O+3O2↑.△ .  ylin1181年前1
ylin1181年前1 -
 夕城美朱 共回答了10个问题
夕城美朱 共回答了10个问题 |采纳率100%(1)高铁酸钾的物理性质有:有紫色光泽的晶体.故填:有紫色光泽的晶体.
(2)保存高铁酸钾时应注意避免潮湿和受热.故填:避免潮湿和受热.
(3)高铁酸钾受热分解的化学方程式为:4K2FeO4
△
.
2Fe2O3+4K2O+3O2↑.1年前查看全部
- 高铁酸钾是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:
 yy561年前1
yy561年前1 -
 badoudou 共回答了10个问题
badoudou 共回答了10个问题 |采纳率80%(1)温度较低 2分
(2)2,3,10;2,6,3,5 3分
(3)AC 2分
(4)5.6m/33 L 3分
(5)在pH=11.50的溶液中,OH-浓度大,使FeO42-+10H2O 4Fe(OH)3+
8OH-+3O2↑平衡向左移动(合理答案也给分). 2分1年前查看全部
- 高铁酸钾是一种理想的绿色水处理剂,工业上可通过如下反应制得:Fe(OH)3+ClO-+OH-一FeO42-+Cl-+H2
高铁酸钾是一种理想的绿色水处理剂,工业上可通过如下反应制得:Fe(OH)3+ClO-+OH-一FeO42-+Cl-+H2O(未配平),在上述反应中( )
A. FeO4 2-是还原产物
B. ClO-是还原剂
C. 1molFe(OH)3得到3mol电子
D. 配平后OH-的化学计量数为4 ryan9231年前1
ryan9231年前1 -
 星夜一人 共回答了18个问题
星夜一人 共回答了18个问题 |采纳率88.9%解题思路:氧化还原反应中,得电子化合价降低的反应物是氧化剂,氧化剂对应的产物是还原产物,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物;氧化还原反应中得失电子相等,据此分析解答.A、该反应中,反应前后氯元素的化合价由+1价→-1价,氯元素得电子化合价降低,所以ClO-作氧化剂,还原产物是
Cl-,FeO42-是氧化产物,故A错误.
B、该反应中,反应前后氯元素的化合价由+1价→-1价,氯元素得电子化合价降低,所以ClO-作氧化剂,故B错误.
C、该反应中,一个Fe(OH)3生成FeO42-,铁元素失去3个电子,所以1molFe(OH)3失去3mol电子,故C错误.
D、该反应中,一个Fe(OH)3生成FeO42-,铁元素失去3个电子,一个ClO-生成Cl-得到2个电子,根据得失电子相等,该反应方程式为 2Fe(OH)3+3 ClO-+4OH-=2FeO42-+3Cl-+5H2O,故D正确.
故选D.点评:
本题考点: 氧化还原反应方程式的配平;氧化还原反应的电子转移数目计算.
考点点评: 本题考查了氧化还原反应中还原剂和氧化剂、氧化产物和还原产物的判断等知识点,难度不大,注意氧化还原反应方程式的配平依据是得失电子相等.1年前查看全部
- (2010•平谷区一模)高铁酸钾(K2FeO4)是一种新型高效水处理剂.下列关于该物质的叙述,正确的是( )
(2010•平谷区一模)高铁酸钾(K2FeO4)是一种新型高效水处理剂.下列关于该物质的叙述,正确的是( )
A.它是一种氧化物
B.组成中含有两种非金属元素
C.它是一种混合物
D.K2FeO4中铁元素的化合价为+6 embraceor1年前1
embraceor1年前1 -
 昨天的风0609 共回答了15个问题
昨天的风0609 共回答了15个问题 |采纳率80%解题思路:A、根据氧化物的组成特点,由高铁酸钾的化学式K2FeO4,判断该物质是否属于氧化物;
B、由高铁酸钾的化学式K2FeO4,判断组成元素中属于非金属元素的种类;
C、根据高铁酸钾的化学式K2FeO4,由物质组成的组成,判断物质分类;
D、利用化合物中各元素化合价代数和为0,由K、O元素的化合价,可计算其中铁元素的化合价.A、氧化物是由两种元素组成且含有氧元素的化合物,根据高铁酸钾的化学式K2FeO4,高铁酸钾由K、Fe、O三种元素组成,该物质不属于氧化物;故A不正确;
B、根据高铁酸钾的化学式K2FeO4,高铁酸钾由K、Fe、O三种元素组成,其中只有O元素一种非金属元素;故B不正确;
C、根据高铁酸钾的化学式K2FeO4,高铁酸钾由K、Fe、O三种元素组成的化合物,而非混合物;故C不正确;
D、设化合物K2FeO4中铁元素的化合价为x,依据化合物中各元素化合价代数和为0,有(+1×2)+x+(-2×4)=0,解得x=+6;故D正确;
故选D.点评:
本题考点: 有关元素化合价的计算;从组成上识别氧化物;纯净物和混合物的判别;元素的简单分类.
考点点评: 根据化合物中各元素化合价代数和为0,利用化合物的化学式可计算其中未知的元素化合价.1年前查看全部
- (2011•上海)高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是( )
(2011•上海)高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是( )
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 我只是ff啊1年前1
我只是ff啊1年前1 -
 wzlshui 共回答了16个问题
wzlshui 共回答了16个问题 |采纳率100%解题思路:根据高铁酸钾的化学式 K2FeO4,从物质所含元素的化合价来分析氧化性还原性问题,利用离子的水解产物的性质来分析净水原因.高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,
故选:A.点评:
本题考点: 重要的氧化剂;常见的生活环境的污染及治理.
考点点评: 本题考查净水剂的净水原理,明确强氧化性及离子水解是解答的关键,并明确具有强氧化性的物质,能使蛋白质变性,从而起到杀菌消毒的作用来解答.1年前查看全部
- 高铁酸钾受热分解的文字表达式
 水上的诺言1年前2
水上的诺言1年前2 -
 Beautiful34 共回答了25个问题
Beautiful34 共回答了25个问题 |采纳率92%干燥的高铁酸钾在198℃以下是稳定的,受热易分解为氧化铁,金属氧化物和氧气
4K2FeO4=2Fe2O3+3O2↑ +4K2O1年前查看全部
- 关于电解法制取高铁酸钾本人想用电解法制高铁酸钾,谁能帮我详细描述一下方法?比如氢氧化钠的浓度,温度,电流强度,以及电解时
关于电解法制取高铁酸钾
本人想用电解法制高铁酸钾,谁能帮我详细描述一下方法?比如氢氧化钠的浓度,温度,电流强度,以及电解时出现的现象,要详细点的, robertech1年前1
robertech1年前1 -
 shuisheng 共回答了24个问题
shuisheng 共回答了24个问题 |采纳率95.8%百度文库里面有《电解法制备高铁酸钾的研究》.
是硕士论文(^o^)/!
结论:
较优条件:阳极电极材料:低碳钢;16mol/L氢氧化钠溶液;35℃;电极面积与电解液的比值为0.6平方厘米/ml,电流密度为100mA/平方厘米的条件为最佳.加入极少量KCl活化电极.在电解液中加入硅酸钠来提高高铁酸根的稳定性.
现象:电流密度为100mA/平方厘米的条件下,电解一开始研究电极表面就有大量的氧气气泡生成,同时辅助电极表面有大量的氢气气泡,在铂片电解液的附近出现了气泡,研究电极表面出现紫色溶液,整个电解池迅速变为紫色,同时伴有致密的氧气气泡从液面冒出.1年前查看全部
- 请问怎么制取高铁酸钾?请写出化学方程式(还有高铁酸钾和水反应的化学方程式)
 wojiaomyn1年前1
wojiaomyn1年前1 -
 benfeek 共回答了21个问题
benfeek 共回答了21个问题 |采纳率90.5%生产方法
次氯酸盐氧化法
将NaOH加入反应釜中,加水溶解后冷却到20℃,通氯气充分饱和.然后过滤,除去固体NaCl.滤液备用(波浪为有效氯含量为70%~80%的次氯酸钠溶液).
将滤液转移到氧化反应釜中,在20~30℃下一边搅拌一边滴加Fe(NO3)3溶液.反应一段时间后取样测终点.当反应液中[Fe3+}<0.5mg/ml时即为氧化终点.到达终点后再继续搅拌一小时.然后加入40%的水溶液,静止后将析出的NaCl过滤除去.滤液备用.
将滤液转移至转化釜中,加入50%的KOH水溶液,在20~30℃下反应2h.析出的褐紫色沉淀便是K2FeO4.过滤,用冰水和丙三醇洗涤滤饼,真空干燥,包装即可.
高温过氧化钠法
将过氧化钠和硫酸亚铁依次投入反应釜中,其投料比为3∶1(mol).密闭反应器,在氮气流中,加热反应,在700℃下反应一小时.得到Na2FeO4粉末,将其溶于NaOH溶液,快速过滤.滤液转移至转化釜中,加入等摩尔KOH固体,析出K2FeO4结晶.用95%乙醇洗涤,真空干燥得成品.
化学氧化法
将氯气通人氢氧化钠溶液生成饱和次氯酸钠浓碱溶液,缓慢加入硝酸铁氧化反应生成高铁酸钠,用氢氧化钾转化成高铁酸钾,抽滤得粗品,再用氢氧化钾溶解,重结晶,用苯和95%乙醇进行脱碱、乙醚洗涤,干燥制得高铁酸钾产品,可立即使用或储存于隔绝空气的容器中.其
2NaOH+Cl2→NaCIO+NaCl+H2O
Fe(N03)3+3NaOH→Fe(OH)3+3NaNO3
2Fe(OH)3+3NaClO+4NaOH→2Na2FeO4+3NaCI+5H2O
Na2FeO4+2KOH→K2FeO4+2NaOH
电解法将三氯化铁和氢氧化钠溶液,在隔膜型电解槽,以铁阳极电解氧化,先生成铁的氧化一氢氧化物络合物,在卤素离子存在下,电化学转化为高铁酸盐离子,与Na+>^结合成高铁酸钠,含量可达50~80 g/L.用50%氢氧化钾溶液,按氢氧化钾与高铁酸钠摩尔比值3:1反应生成高铁酸钾,抽滤,用异丙醇脱碱、洗涤,经干燥制得高铁酸钾,放入密闭干燥器中保存.其
Fe+8OH->^[Cl->^]→[FexOy?n H2O]^[Cl->^]→FeO42->^+4H2O+6e^
FeCl3+8OH->^^[Cl->^]→[FexOy?n H2O] ^[Cl->^]→FeO42->^+4H2O+3Cl->^+3e->^
6Na+>^6H2O+6e→6NaOH+3H2↑
Na2FeO4+2KOH→K2FeO4+2NaOH
高铁酸钾极易溶于水生成浅紫红色溶液,静置时会逐渐分解放出氧气并沉淀出三氧化二铁,分解过程也会使溶液的pH值升高.
4K2Fe4+4H2O=2Fe2O3+8KOH+3O21年前查看全部
- (2011•江苏一模)高铁酸钾是一种高效的多功能的水处理剂.工业上常采用NaClO氧化法生产,原理为:3NaClO+2F
(2011•江苏一模)高铁酸钾是一种高效的多功能的水处理剂.工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O,Na2FeO4+2KOH=K2FeO4+2NaOH,主要的生产流程如下:

(1)写出反应①的离子方程式______.
(2)流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4)______Ksp(Na2FeO4)(填“>”或“<”或“=”).
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响.
①工业生产中最佳温度为______℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为______.
②若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:______.
③若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:______.
(4)K2FeO4 在水溶液中易水解:4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑.在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).
A.H2OB.CH3COONa、异丙醇C.NH4Cl、异丙醇D.Fe(NO3)3、异丙醇. 飘的水1年前1
飘的水1年前1 -
 尚笑酷房 共回答了14个问题
尚笑酷房 共回答了14个问题 |采纳率92.9%解题思路:(1)氯气是酸性气体,能和烧碱溶液反应生成NaCl和NaClO;
(2)从难溶电解质的沉淀转化的角度分析;
(3)①寻找最佳温度要具备的条件:该温度下反应速率快,生成高铁酸钾的产率较大两方面;
②从盐类的水解角度分析;
③根据反应物和生成物书写反应的离子方程式;
(4)选择的洗涤剂应能抑制K2FeO4的水解,并注意减少K2FeO4的溶解.(1)氯气是酸性气体,能和烧碱溶液反应,反应实质为:Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;(2)根据反应Na2FeO4+2KOH=K2FeO4+2NaOH可知,反应生成溶解度更小的物质,说明此温度下Ksp(K2FeO4...
点评:
本题考点: 制备实验方案的设计;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查物质的制备方案的设计,题目难度中等,解答本题时注意把握题给信息,学习中注重知识迁移能力的培养.1年前查看全部
- 高铁酸钾(K2FeO4)具有很强的氧化性,是一种新型的高效水处理剂.
高铁酸钾(K2FeO4)具有很强的氧化性,是一种新型的高效水处理剂.

(1)高铁酸钾具有强氧化性的原因是______.
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为______,______.
(3)制备K2FeO4可以采用干式氧化法或湿式氧化法.
①干式氧化的初始反应是2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中每生成2mol Na2FeO4时转移电子______mol.
②湿式氧化法的流程如图:
上述流程中制备Na2FeO4的化学方程式是______.
(4)高铁电池是正在研制中的可充电电池,图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有______、______.
(5)探究高铁酸钾的某种性质.
【实验1】将适量K2FeO4固体分别溶解于pH为 4.74、7.00、11.50的水溶液中,配得FeO42-浓度为1.0mmol•L-1(1mmol•L-1=10-3mol•L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图2(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
【实验2】将适量K2FeO4溶解于pH=4.74的水溶液中,配制成FeO42-浓度为0mmol•L-1的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.则
①实验1的目的是______;
②实验2可得出的结论是______;
③高铁酸钾在水中的反应为4FeO42-+10H2O⇌4Fe(OH)3+8OH-+3O2↑.由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是______. 8227love1年前1
8227love1年前1 -
 majcos 共回答了19个问题
majcos 共回答了19个问题 |采纳率84.2%解题思路:(1)高铁酸钾中的铁是正6价,处于高价态,具有强氧性;
(2)高铁酸钾是具有强氧性,还原产物铁离子水解生成氢氧化铁胶体,吸附杂质的作用;
(3)①2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,6molNa2O2中12mol的负一价氧,2mol的有变成0价,还有10mol变成-2价,而铁是正2价变为正6价,所以每生成2mol Na2FeO4时转移电子10mol;
②Fe(NO3)3被NaClO氧化成Na2FeO4;
(4)高铁电池由图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有放电时间长,工作电压稳定等优点;
(5)①在其它条件相同的情况下研究在FeO42-不同PH溶液中的稳定性;
②研究温度改变,FeO42-的稳定性;
③用平衡移动的原理解释.(1)高铁酸钾中的铁是正6价,处于高价态,具有强氧性,故答案为:其中的铁元素为+6价,易得电子;
(2)高铁酸钾是具有强氧性,还原产物铁离子水解生成氢氧化铁胶体,吸附杂质的作用,故答案为:高铁酸钾有强氧化性,能杀菌消毒;产生的Fe(OH)3有吸附性,有絮凝作用;
(3)①2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,6molNa2O2中12mol的负一价氧,2mol的有变成0价,还有10mol变成-2价,而铁是正2价变为正6价,所以每生成2mol Na2FeO4时转移电子10mol,故答案为:10;
②Fe(NO3)3被NaClO氧化成Na2FeO4,故答案为:2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O;
(4)高铁电池由图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有放电时间长,工作电压稳定等优点,
故答案为:放电时间长;工作电压稳定;
(5)①在其它条件相同的情况下研究在FeO42-不同PH溶液中的稳定性,故答案为:研究在FeO42-不同PH溶液中的稳定性(或反应的速率);
②研究温度改变,FeO42-的稳定性,故答案为:温度越高,FeO42-越不稳定(或与水反应的速率越快);
③用平衡移动的原理解释,pH=11.50的溶液中OH-离子浓度大,使平衡向左移动,故答案为:pH=11.50的溶液中OH-离子浓度大,使平衡向左移动.点评:
本题考点: 物质的量或浓度随时间的变化曲线;化学电源新型电池.
考点点评: 本题考查元素化合物知识结合化学反应的速率以及平衡的移动等知识的综合考查,难度大,学生不容易接受.1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、去浊、脱色、除臭为一体的新型高效水处理剂.下列关于该物质的叙述正
高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、去浊、脱色、除臭为一体的新型高效水处理剂.下列关于该物质的叙述正确的是( )
A. 它是一种氧化物
B. K2FeO4中铁元素的化合价为+6价
C. 它是一种混合物
D. 该物质含有两种非金属元素 WSL5301年前4
WSL5301年前4 -
 叮铃鱼 共回答了20个问题
叮铃鱼 共回答了20个问题 |采纳率95%解题思路:可以根据高铁酸钾的化学式进行相关的判断,氧化物是指含有两种元素且其中一种是氧元素的化合物,根据化合价规则即可求得高铁酸钾中铁元素的化合价.A、高铁酸钾含有钾、铁、氧三种元素,不是氧化物,故A错误;
B、根据化合物中各元素正负化合价的代数和为零,设铁元素的化合价为x,则有(+1)×2+x+(-2)×4=0,解得x=+6,故B正确;
C、高铁酸钾是纯净物不是混合物,故C错误;
D、高铁酸钾含有氧这一种非金属元素,故D错误;
故选B.点评:
本题考点: 物质的简单分类;从组成上识别氧化物;纯净物和混合物的判别;物质的元素组成;有关元素化合价的计算.
考点点评: 本题主要考查了氧化物的概念以及化合价规则,完成此题,可以依据已有的知识进行.1年前查看全部
- 近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂.高铁酸钾在水处理过程中涉及到的化学过程正确的有:①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应( )
A. ①②③④
B. ①③④⑥
C. ②③④⑤
D. ②③⑤⑥ 湖底草生长1年前1
湖底草生长1年前1 -
 liushupei2008 共回答了25个问题
liushupei2008 共回答了25个问题 |采纳率92%解题思路:高铁酸钾具有强氧化性,可致蛋白质发生氧化而变性,高铁酸钾被还原生成Fe3+,水解生成具有吸附性的Fe(OH)3胶体而达到净水作用.高铁酸钾具有强氧化性,可致蛋白质发生氧化而变性,则不涉及蛋白质的盐析,故②错误;
高铁酸钾被还原生成Fe3+,水解生成具有吸附性的Fe(OH)3胶体而达到净水作用,涉及胶体聚沉、盐类水解,不涉及颜色反应,则⑤错误,
所以涉及的有①③④⑥,
故选B.点评:
本题考点: "三废"处理与环境保护;胶体的重要性质;氨基酸、蛋白质的结构和性质特点.
考点点评: 本题考查高铁酸钾的性质以及反应原理,题目难度不大,解答该题的关键是把握相关物质的性质及应用,学习中注意积累.1年前查看全部
- 高铁酸钾在水中能消毒杀菌的原因?能净水的原因?
 田汉1年前4
田汉1年前4 -
 snow520kt 共回答了21个问题
snow520kt 共回答了21个问题 |采纳率90.5%KFeO4具有强氧化性(杀菌消毒)
还原产物Fe3+水解产物Fe(OH)3能净水1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3
高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3 +3Cl 2 +10KOH
2K 2 FeO 4 +6KCl+8H 2 O对于该反应,下列说法正确的是( )0-30℃ . A.该反应是置换反应 B.钾元素化合价降低 C.Fe(OH) 3 发生还原反应 D.Cl 2 是氧化剂  xiesuan1年前1
xiesuan1年前1 -
 没有果实 共回答了17个问题
没有果实 共回答了17个问题 |采纳率94.1%A、反应物、生成物的种类、种数不符合置换反应概念,不是置换反应,故A错误;
B、钾元素化合价反应前后都为+1价,故B错误;
C、铁元素化合价由+3价升高为+6价,Fe(OH) 3 发生氧化反应,故C错误;
D、氯元素的化合价由0将为-1价,发生还原反应,氯气是氧化剂,故D正确.
故选:D.1年前查看全部
- (2009•香坊区一模)高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、杀菌
(2009•香坊区一模)高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、杀菌、灭藻的新型、高效的多功能水处理剂.干燥的高铁酸钾在198℃以下是稳定的,受热易分解为氧化铁、金属氧化物和氧气.根据上述信息,请回答下列问题:
(1)高铁酸钾的物理性质是______.
(2)保存高铁酸钾时应注意______.
(3)写出高铁酸钾受热分解的化学方程式4K2FeO4
2Fe2O3+4K2O+3O2↑△ .4K2FeO4.
2Fe2O3+4K2O+3O2↑△ . 孔最1年前1
孔最1年前1 -
 lxxx586780 共回答了16个问题
lxxx586780 共回答了16个问题 |采纳率81.3%解题思路:高铁酸钾的颜色、光泽、状态等性质不需要通过化学变化表现出来,属于物理性质;
干燥的高铁酸钾在较低温度下是稳定的;
根据反应物和生成物及其质量守恒定律可以书写化学方程式.(1)高铁酸钾的物理性质有:有紫色光泽的晶体.故填:有紫色光泽的晶体.
(2)保存高铁酸钾时应注意避免潮湿和受热.故填:避免潮湿和受热.
(3)高铁酸钾受热分解的化学方程式为:4K2FeO4
△
.
2Fe2O3+4K2O+3O2↑.点评:
本题考点: 化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要能够区分物理性质和化学性质的区别,同时书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- 铁是重要的金属元素,用途极广.(1)高铁酸钾(K2FeO4)具有很强的氧化性,常用作净水剂,对环境无不良影响,被人们称为
铁是重要的金属元素,用途极广.
(1)高铁酸钾(K2FeO4)具有很强的氧化性,常用作净水剂,对环境无不良影响,被人们称为“绿色化学”试剂.工业上,可用铁作阳极,电解KOH溶液制备K2FeO4,其阳极的电极反应式为______.
(2)某高效净水剂可由Fe(OH)SO4聚合得到.工业上以FeSO4、NaNO2和稀硫酸为原料来制备Fe(OH)SO4,反应中有NO生成,化学方程式为______.
(3)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ/mol
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ/mol
高炉炼铁过程中发生的主要反应为:
[1/3]Fe2O3(s)+CO(g)⇌[2/3] Fe(s)+CO2(g)△H=a kJ/mol,则a=kJ/mol.
已知该反应在不同温度下的平衡常数如下表:
在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时v正______v逆(填“等于”、“大于”或“小于”).经过l0min,在1000℃达到平衡,则该时间范围内反应的平均反应速率v(CO2)=______.欲提高上述反应中CO的平衡转化率,可采取的措施是______;温度/℃ 1000 1115 1300 平衡常数 4.0 3.7 3.5
A.提高反应温度B.移出部分CO2C.加入合适的催化剂D.减小容器的容积
(4)一定温度下的难溶电解质在水溶液中达到溶解平衡时.已知下表数据,对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是______.
A.向该溶液中加少量铁粉不能观察到红色固体析出物质 Fe(OH)2 Cu(OH)2 Fe(OH)3 Ksp/25℃ 8.0×10-16 2.2×10-20 4.0×10-38 完全沉淀时的PH值 ≥9.6 ≥6.4 3~4
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
C.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,可得到纯净的CuSO4溶液
D.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀. zhqi86861年前1
zhqi86861年前1 -
 月夜的忘忧 共回答了21个问题
月夜的忘忧 共回答了21个问题 |采纳率85.7%解题思路:(1)铁失去电子,在碱性溶液中生成高铁酸根离子,同时有水生成;
(2)此反应为氧化还原反应,反应物中既有氧化剂又有还原剂,依据化合价升降相等配平即可;
(3)依据热化学方程式计算,反应焓变;依据计算得到浓度商和该温度下平衡常数比较判断反应进行方向,依据平衡常数计算生成二氧化碳,结合反应速率概念计算二氧化碳的化学反应速率;欲提高上述反应中CO的平衡转化率,需要反应正向进行;
(4)A.因为Fe3+的氧化性强于Cu2+,所以投入少量铁粉,先发生的反应是:2Fe3++Fe=3Fe2+;
B.Cu2+、Fe2+、Fe3+发生水解,因此它们的物质的量会减少;
C.溶液中混有CuCl2;
D.根据Ksp的大小判断溶解性.(1)铁失去电子,在碱性溶液中生成高铁酸根离子,同时有水生成,阳极的电极反应式为Fe-6e-+8OH-═FeO42-+4H2O,故答案为:Fe-6e-+8OH-═FeO42-+4H2O;
(2)FeSO4→Fe(OH)SO4 ,Fe由+2变为+3,故FeSO4为还原剂,NaNO2→NO,N由+3变为+2,故NaNO2为氧化剂,稀硫酸既不做氧化剂也不做还原剂.FeSO4→Fe(OH)SO4 和NaNO2→NO化合价升降相等,故FeSO4和NaNO2化学计量数相等,依据原子守恒配平可得:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑
故答案为:2FeSO4+2NaNO2+H2SO4=2Fe(OH)SO4+Na2SO4+2NO↑;
(3)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ/mol
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ/mol
依据盖斯定律①×[1/3]-②得到高炉炼铁过程中发生的主要反应为:[1/3]Fe2O3(s)+CO(g)⇌[2/3] Fe(s)+CO2(g)△H=-9.5 kJ/mol,则a=-9.5kJ/mol
在一个容积为:10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,Q=
1mol
10L
1mol
10L=1<K=4,说明费用正向进行,v正>v逆;
设反应一氧化碳物质的量为x
[1/3]Fe2O3(s)+CO(g)⇌[2/3] Fe(s)+CO2(g)
起始量 (mol) 1 1
变化量(mol) x x
平衡量(mol)1-x 1+x
[1+x/1−x]=4
x=0.6
经过l0min,在1000℃达到平衡,则该时间范围内反应的平均反应速率v(CO2)=
0.6mol
10L
10min=0.006mol/L•min;
欲提高上述反应中CO的平衡转化率,应使平衡正向进行;
A.反应是放热反应,提高反应温度,平衡逆向进行,一氧化碳转化率减小,故A不符合;
B.移出部分CO2平衡正向进行,一氧化碳转化率增大,故B符合;
C.加入合适的催化剂,改变反应速率不改变化学平衡,一氧化碳转化率不变,故C不符合;
D.反应前后气体体积不变,减小容器的容积增大压强,平衡不变,一氧化碳转化率不变,故D不符合;
故选B.
(4)A.因为Fe3+的氧化性强于Cu2+,所以投入少量铁粉,先发生的反应是:2Fe3++Fe=3Fe2+,不能观察到红色固体析出,故A正确;
B.因为Cu2+、Fe2+、Fe3+对应的碱全是弱碱,所以这三种离子在溶液中都会发生水解,因此它们的物质的量会减少,故B正确;
C.加入氯水,可以把亚铁离子全氧化成三价,但它的还原产物Cl-肯定还在溶液中,而且在调节pH时加入的试剂也会在溶液中有所保留,所以得到的溶液中不可能只含CuSO4一种溶质,故C错误;
D.从表格中可以看出,Fe(OH)3的Ksp是最小的,所以它最先出现沉淀,故D正确;
故选C.点评:
本题考点: 电解原理;化学平衡常数的含义;化学平衡的影响因素;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查了电解原理,化学平衡影响因素,平衡常数、反应速率概念分析应用,热化学方程式和盖斯定律计算,沉淀溶解平衡的理解应用,掌握基础是关键,题目难度中等.1年前查看全部
- 高铁酸钾在不同条件下发生的反应如下……
 zhapmin20041年前1
zhapmin20041年前1 -
 吴始吴终 共回答了23个问题
吴始吴终 共回答了23个问题 |采纳率78.3%酸性;Mno4 - Mn2+;a;反应为28KMnO4+5K2S+24KOH=28KMnO4+3K2SO4+2S+12H20
花了我一点时间求采纳1年前查看全部
- 化学与环境.材料,信息,能源关系密切相关,下列说话不正确的事A高铁酸钾
化学与环境.材料,信息,能源关系密切相关,下列说话不正确的事A高铁酸钾
2.化学与环境、材料、信息、能源关系密切,下列说法中不正确的是( )
A.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水
B."光化学烟雾"、"臭氧空洞"的形成都与氮氧化合物 有关
C.尽量使用含12C的产品,减少使用含13C或14C的产品符合"促进低碳经济"宗旨
D.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会 "断路 yun02171年前2
yun02171年前2 -
 狼狼猪 共回答了17个问题
狼狼猪 共回答了17个问题 |采纳率88.2%C不正确的
A选项,高铁酸钾是一种强氧化剂,氧化后生成的絮状沉淀可以吸附沉淀过滤,不影响饮水.
B"光化学烟雾"、"臭氧空洞"的形成就是与氮氧化合物有关.也是形成酸雨的一个原因
C不正确,12C指的是质量数是12的碳原子,13C和14C具有一定的放射性.但是使用12C可不是执行"促进低碳经济"宗旨
D二氧化硅是酸性氧化物,与强碱反应 2NaOH+SiO2=NaSiO3+H2O
不懂请问1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
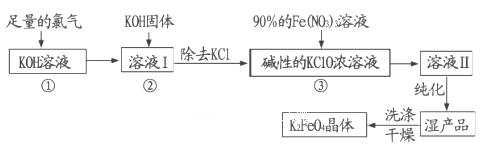
请同答下列问题:
(l)写出向KOH溶液中通入足量Cl 2 发生反应的离子方程式_______ 。
(2)在溶液I中加入KOH固体的目的是______(填编号)。
(3)从溶液Ⅱ中分离出K 2 FeO 4 后,还会有副产品KNO 3 ,KCl,则反应③中发生的离子反应方程式为_______。每制得59.4克K 2 FeO 4 ,理论上消耗氧化剂的物质的量为____ mol。A.为下一步反应提供碱性的环境 B.使KClO 3 转化为KClO C.与溶液I中过量的Cl 2 继续反应,生成更多的KClO D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(4)高铁酸钾(K 2 FeO 4 )作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:_______ FeO 4 2 - +_______ H 2 O="_______" Fe(OH) 3 (胶体)+_______O 2 ↑+_______OH - 。
(5)从环境保护的角度看,制备K 2 FeO 4 较好的方法为电解法,其装置如图所示。电解过程中阳极的电极反应式为________。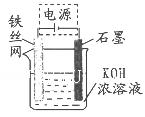
(6)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:3Zn(OH) 2 +2Fe(OH) 3 +4KOH-----3Zn+2K 2 FeO 4 +8H 2 O,放电时电池的负极反应式为________ 。 lvchaohahaha1年前1
lvchaohahaha1年前1 -
 huang123tao 共回答了11个问题
huang123tao 共回答了11个问题 |采纳率81.8%1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下 (1)反应①应在温度
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下 
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl 2 反应生成的是KClO 3 。写出在温度较高时KOH 与Cl 2 反应的化学方程式______________________,当反应中转移5mol电子时,消耗的氯气是
___________mol。
(2)在反应液I中加入KOH固体的目的是___________(填编号)。
A.与反应液I中过量的Cl 2 继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO 3 转化为KClO
(3)从溶液II中分离出K 2 FeO 4 后,还会有副产品KNO 3 、KCl,则反应③中发生的离子反应方程式为
___________________________。
(4)如何判断K 2 FeO 4 晶体已经洗涤干净______________________。
(5)高铁酸钾(K 2 FeO 4 )作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,其离子反应是:
____FeO 4 2- +____H 2 O→_____Fe(OH) 3 (胶体)+_____O 2 ↑+______完成并配平方程式将完整的离子方程式写在下方:______________________。 追求真理吧1年前1
追求真理吧1年前1 -
 venus88 共回答了23个问题
venus88 共回答了23个问题 |采纳率91.3%(1)6KOH+3Cl 2 ==KClO 3 +5KCl+3H 2 O;3
(2)AC
(3)2Fe 3+ +3ClO - +10OH - ==2FeO 4 2- +3Cl - +5H 2 O
(4)取最后一次的洗涤液,加硝酸银溶液,无白色沉淀则已被洗净
(5)4FeO 4 2- +10H 2 O=4Fe(OH) 3 (胶体)+3O 2 ↑+8OH -1年前查看全部
- 高铁酸钾与水反应生成的一种红褐色的氢氧化物是什么
 田下有力1年前3
田下有力1年前3 -
 琴伊 共回答了17个问题
琴伊 共回答了17个问题 |采纳率76.5%高铁酸盐钾是六价铁盐,具有很强的氧化性
高铁酸钾极易溶于水,形成类似于高锰酸钾溶液紫红色的溶液.此溶液极不稳定,数分钟后明显分解:
4Fe04 2- + 10H2O = 4Fe(OH)3(沉淀)+ 8OH- + 3O2(气体)
红褐色氢氧化物是氢氧化铁1年前查看全部
- 课本上的化合价与好多题不符,如课本上的铁化合价是+2+3价,可高铁酸钾中铁的化合价为+6.为什么,是课本上的化合价只是参
课本上的化合价与好多题不符,如课本上的铁化合价是+2+3价,可高铁酸钾中铁的化合价为+6.为什么,是课本上的化合价只是参考吗?
 oras9031年前3
oras9031年前3 -
 littlebasin 共回答了20个问题
littlebasin 共回答了20个问题 |采纳率90%同种元素 不同化合价 很正常
元素的“化合价”是元素的一种重要性质,这种性质只有跟其他元素相化合时才表现出来.就是说,当元素以游离态存在时,即没有跟其他元素相互结合成化合物时,该元素是不表现其化合价的,因此单质中元素的化合价为“0”.例如Zn、C、H2等.
因为两个单质组成的化合物有时不同如:H2O H2O2等等,但是它们的化合价总和必须为0,所以在有些物质化合价不变的同时,有些物质的化合价就要做相应的改变,就出现了一种物质多种化合价
有网友提供通俗的说法:
首先化合价是因为原子电子发现变化了,于是原子的电荷情况也就发生变化了.表现出来就是化合价了.
显然同一种原子,跟不同原子接触时,它的变化情况是不同的.因为双方间争夺电子的能力是有差异的.这相当于有一盘面包,一般是你抢得最多的,可是来了一个更强的,结果你一个都没抢到,这并不是你抢的能力变差了,而是别人更强了.
所以就有了不同的化合价了.关键在于外面的环境.跟哪个原子在一起才是关键~1年前查看全部
- 高铁酸钾的消毒效率是二氧化氯的几倍
 ShiRr1年前1
ShiRr1年前1 -
 gg土冒ggqq 共回答了12个问题
gg土冒ggqq 共回答了12个问题 |采纳率75%电子守恒1年前查看全部
- 高铁酸钾{K2FeO4}受热分解为氧化铁,金属氧化物,氧气.
 KierKafka1年前1
KierKafka1年前1 -
 abc近距离 共回答了15个问题
abc近距离 共回答了15个问题 |采纳率93.3%4K2FeO4 === 2Fe2O3 + 4K2O + 3O2
等号上面写 加热1年前查看全部
- 高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是( )
高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是( )
A. 有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B. 有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C. 有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D. 有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 回忆烟草的味道1年前1
回忆烟草的味道1年前1 -
 人间不系舟 共回答了18个问题
人间不系舟 共回答了18个问题 |采纳率94.4%解题思路:根据高铁酸钾的化学式 K2FeO4,从物质所含元素的化合价来分析氧化性还原性问题,利用离子的水解产物的性质来分析净水原因.高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,
故选:A.点评:
本题考点: 重要的氧化剂;常见的生活环境的污染及治理.
考点点评: 本题考查净水剂的净水原理,明确强氧化性及离子水解是解答的关键,并明确具有强氧化性的物质,能使蛋白质变性,从而起到杀菌消毒的作用来解答.1年前查看全部
- 高铁酸钾与水反应能生成氧气吧?
 4608909251年前1
4608909251年前1 -
 guojia50 共回答了19个问题
guojia50 共回答了19个问题 |采纳率94.7%不可以,FeMnO4和水无法反应1年前查看全部
- 硫酸铁+氢氧化钠+氯气反应=高铁酸钾+硫酸钾+氯化钾+(?) 写出括号内的物质并配平
 李四1233211年前1
李四1233211年前1 -
 永远过客 共回答了16个问题
永远过客 共回答了16个问题 |采纳率75%Fe2(SO4)3+16KOH+3CL2==2K2FeO4+3K2SO4+6KCL+8H2O1年前查看全部
- AAAAAAAAA湿法氧化:在溶液中用次氯酸钠、氢氧化铁和氢氧化钾制高铁酸钾,参加反应的氧化剂和还原剂的物质
AAAAAAAAA湿法氧化:在溶液中用次氯酸钠、氢氧化铁和氢氧化钾制高铁酸钾,参加反应的氧化剂和还原剂的物质
湿法氧化:在溶液中用次氯酸钠、氢氧化铁和氢氧化钾制高铁酸钾,参加反应的氧化剂和还原剂的物质的量之比是多少?
最好用得失电子守恒法解答. wallawiq1年前1
wallawiq1年前1 -
 philofd 共回答了20个问题
philofd 共回答了20个问题 |采纳率85%NaClO----NaCl 氯元素化合价总降2价
Fe(OH)3------K2FeO4 铁元素化合价总升3价
根据得失电子守恒 氧化剂NaClO和还原剂Fe(OH)3的物质的量之比是3:21年前查看全部
- 高铁酸钾(K 2 FeO 4 )是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌、灭
高铁酸钾(K 2 FeO 4 )是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌、灭藻的新型、高效的多功能水处理剂。干燥的高铁酸钾在198℃以下是稳定的,受热易分解,受潮易与水反应生成氢氧化铁、氢氧化钾和氧气。根据上述信息,请回答下列问题:
(1)请写出高铁酸钾的一条物理性质是:_____________。
(2)保存高铁酸钾时应注意:____________。
(3)请写出高铁酸钾的一种用途:_______________。
(4)完成高铁酸钾与水反应的化学方程式。
 viviana11221年前1
viviana11221年前1 -
 yan1977 共回答了11个问题
yan1977 共回答了11个问题 |采纳率100%(1)紫色光泽的固体粉末
(2)防潮、避免放在高温环境中
(3)杀菌(合理即可)
(4)3;O 21年前查看全部
- 高铁酸钾铁元素的化合价我算的怎么是-4 答案上怎么是-6?
 wnsky5291年前1
wnsky5291年前1 -
 四月雏菊 共回答了21个问题
四月雏菊 共回答了21个问题 |采纳率85.7%K2FeO4
K+1,O-2,则Fe+6
+1*2+(-2*4)+x=0
x=+61年前查看全部
- 谁能告诉我从高铁酸钾组成元素角度作为净水剂的优点
 linqing081年前3
linqing081年前3 -
 黄晓鸿 共回答了15个问题
黄晓鸿 共回答了15个问题 |采纳率100%高铁酸钾组成元素有:钾K、铁Fe、氧O
以上元素是人体必需元素,经高铁酸钾净化的水对人体的危害小;铁为最高价态,氧化性强,净水效果好.
所以,优点是对人体危害小,净水效果好.1年前查看全部
- (2005•荆州)高铁酸钾是一种亲型、高效、多功能的“绿色”水处理剂,其化学式为K2FeO4,已知其中K元素为+1价,O
(2005•荆州)高铁酸钾是一种亲型、高效、多功能的“绿色”水处理剂,其化学式为K2FeO4,已知其中K元素为+1价,O元素为-2价,则Fe元素的化合价为( )
A.+2
B.+4
C.+5
D.+6 tom51681年前1
tom51681年前1 -
 q68040967 共回答了16个问题
q68040967 共回答了16个问题 |采纳率87.5%解题思路:已知K元素为+1价,O元素为-2价,根据在化合物中,各元素的化合价代数和为零即可求得Fe元素的化合价.在K2FeO4中K元素为+1价,O元素为-2价;
则设铁元素化合价为x,
则(+1)×2+x+(-2)×4=0;
解得:x=+6;
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.1年前查看全部
- 高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂.高铁酸钾是具有紫色光泽的粉末;干燥的高铁酸钾在198℃以下是稳
高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂.高铁酸钾是具有紫色光泽的粉末;干燥的高铁酸钾在198℃以下是稳定的,在受潮或受热时都易发生分解.根据上述信息,请回答下列问题.
(1)高铁酸钾的物理性质是有紫色光泽的粉末有紫色光泽的粉末.
(2)高铁酸钾在保存时应注意避免受潮,受热受潮,受热.
(3)高铁酸钾与水反应的化学方程式如下,请在方框内填入化学计量数,在横线上填写化学式.
4K2FeO4+10H2O═4Fe(OH)3↓+8KOH+3O23O2↑. yu6275272951年前1
yu6275272951年前1 -
 liaodl1975 共回答了20个问题
liaodl1975 共回答了20个问题 |采纳率90%(1)物质的颜色、光泽、状态等方面的性质不需要通过化学变化表现出来,属于物理性质.故填:有紫色光泽的粉末.
(2)高铁酸钾在受潮或受热时都易发生分解,所以高铁酸钾在保存时应注意避免受潮,受热.故填:受潮,受热.
(3)根据质量守恒定律可知,高铁酸钾和水反应生成氢氧化铁、氢氧化钾和氧气.故填:3O2.1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂。下列反应可制取K 2 FeO 4 ;
高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂。下列反应可制取K 2 FeO 4 ;
2Fe(OH) 3 +3Cl 2 +10KOH 2K 2 FeO 4 +6KCl+8H 2 O 对于该反应,下列说法正确的是 [ ]
2K 2 FeO 4 +6KCl+8H 2 O 对于该反应,下列说法正确的是 [ ]A.该反应是置换反应
B.钾元素化合价降低
C.Fe(OH) 3 发生还原反应
D.Cl 2 是氧化剂 maryzz1年前1
maryzz1年前1 -
 124356 共回答了13个问题
124356 共回答了13个问题 |采纳率84.6%D1年前查看全部
- 高铁酸钾(K2FeO4)是一种新型的自来水处理剂,有强氧化性,可消毒杀菌,其还原产物能吸附水中杂质
高铁酸钾(K2FeO4)是一种新型的自来水处理剂,有强氧化性,可消毒杀菌,其还原产物能吸附水中杂质
这句话那里错了 筱簃1年前2
筱簃1年前2 -
 心痛到无以复加 共回答了14个问题
心痛到无以复加 共回答了14个问题 |采纳率100%印象中,因为正6价的铁有强氧化性,因而可以用来杀菌消毒,不记得它能吸附水中杂质啊······另外,十二水硫酸铝钾(明矾)的水解产物氢氧化铝能吸附水中杂质,但不能杀菌消毒.1年前查看全部
- 高铁酸钾和水反应,生成氢氧化铁,氢氧化钾,氧气,这个反应中,生成氧气是负二价氧离子失电子,那么电子去哪了?其他元素中哪个
高铁酸钾和水反应,生成氢氧化铁,氢氧化钾,氧气,这个反应中,生成氧气是负二价氧离子失电子,那么电子去哪了?其他元素中哪个变价了?
 我怕了two1年前1
我怕了two1年前1 -
 zczc3242320 共回答了15个问题
zczc3242320 共回答了15个问题 |采纳率100%高铁酸钾中 铁是正六价1年前查看全部
- 高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂.高铁酸钾是具有紫色光泽的粉末;干燥的高铁酸钾在198℃以下是稳
高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂.高铁酸钾是具有紫色光泽的粉末;干燥的高铁酸钾在198℃以下是稳定的,在受潮或受热时都易发生分解.根据上述信息,请回答下列问题.
(1)高铁酸钾的物理性质是有紫色光泽的粉末有紫色光泽的粉末.
(2)高铁酸钾在保存时应注意避免受潮,受热受潮,受热.
(3)高铁酸钾与水反应的化学方程式如下,请在方框内填入化学计量数,在横线上填写化学式.
4K2FeO4+10H2O═4Fe(OH)3↓+8KOH+3O23O2↑. 宁静之声1年前1
宁静之声1年前1 -
 同在A组的 共回答了9个问题
同在A组的 共回答了9个问题 |采纳率88.9%解题思路:(1)物质的物理性质是指不需要通过化学变化表现出来的性质.
(2)高铁酸钾的热稳定性差,遇水容易发生化学反应.
(3)根据质量守恒定律可以确定物质的化学式.(1)物质的颜色、光泽、状态等方面的性质不需要通过化学变化表现出来,属于物理性质.故填:有紫色光泽的粉末.
(2)高铁酸钾在受潮或受热时都易发生分解,所以高铁酸钾在保存时应注意避免受潮,受热.故填:受潮,受热.
(3)根据质量守恒定律可知,高铁酸钾和水反应生成氢氧化铁、氢氧化钾和氧气.故填:3O2.点评:
本题考点: 化学性质与物理性质的差别及应用;空气中常见酸碱盐的质量或性质变化及贮存法;有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查高铁酸钾的性质和化学方程式的书写等方面的知识,物质之间发生化学变化时都遵循质量守恒定律.1年前查看全部
- 新型净水剂-高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2F
新型净水剂-高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O
②Na2FeO4+2KOH═K2FeO4+2NaOH.下列说法不正确的是( )
A.反应①为氧化还原反应,反应②为复分解反应
B.反应①中氧化产物与还原产物物质的量之比为2:9
C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒
D.若有2mol FeCl3发生反应,转移电子的物质的量为6 mol 天寒地动1年前1
天寒地动1年前1 -
 YoungD 共回答了18个问题
YoungD 共回答了18个问题 |采纳率100%解题思路:反应2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O中,Fe元素化合价升高,由+3价升高到+6价,被氧化,Cl元素化合价由+1价降低到-1价,被还原,NaClO为氧化剂,FeCl3为还原剂,Na2FeO4+2KOH═K2FeO4+2NaOH为复分解反应,元素化合价没有发生变化,以此解答.A.反应①Fe和Cl元素化合价发生变化,为氧化还原反应,反应②元素化合价没有发生变化,为复分解反应,故A正确;
B.反应2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O中,NaClO为氧化剂,FeCl3为还原剂,由方程式可知,氧化产物与还原产物物质的量之比为2:3,故B错误;
C.由化合价代数和为0的原则可知K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒,故C正确;
D.反应2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O中,Fe元素化合价升高,由+3价升高到+6价,则若有2mol FeCl3发生反应,转移电子的物质的量为6 mol,故D正确.
故选B.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意从元素化合价的角度认识氧化还原反应中物质所表现出的性质,明确元素的化合价为解答该类题目的关键,难度中等.1年前查看全部
- 制备高铁酸钾反应中的还原剂在哪?
制备高铁酸钾反应中的还原剂在哪?
FeO3+3KNO3+4kOH=2K2FeO4+3KNO2+2H2O 春残1年前1
春残1年前1 -
 吹二 共回答了13个问题
吹二 共回答了13个问题 |采纳率92.3%Fe2O3
Fe从正三价升到正六价1年前查看全部
- 氯化铁与次氯酸钾反应生成高铁酸钾和什么
 harry30251年前1
harry30251年前1 -
 至爱桃子 共回答了20个问题
至爱桃子 共回答了20个问题 |采纳率95%2FeCl3+3KClO+10KOH=2K2FeO4+9KCl+5H2O1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、脱色、除臭等为一的新型高效水处理剂.下列关于该物质的说法正确的是
高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、脱色、除臭等为一的新型高效水处理剂.下列关于该物质的说法正确的是( )
A.高铁酸钾是由2个钾原子、一个铁原子和4个氧原子构成的
B.高铁酸钾是一种混合物
C.高铁酸钾中含有两种金属元素
D.高铁酸钾分子是由6个原子构成的 qq521425q1年前1
qq521425q1年前1 -
 一定是猪 共回答了16个问题
一定是猪 共回答了16个问题 |采纳率87.5%解题思路:A、根据物质的构成进行分析;
B、根据混合物的概念进行分析;
C、由高铁酸钾的化学式K2FeO4,判断组成元素的种类;
D、根据分子的构成分析.A、宏观物质不能说是由几个原子构成的,应说一个高铁酸钾分子是由2个钾原子、一个铁原子和4个氧原子构成的,故A不正确;
B、根据高铁酸钾是由一种物质组成的,是一种纯净物;故B不正确;
C、根据高铁酸钾的化学式K2FeO4,高铁酸钾由K、Fe、O三种元素组成的化合物,含有两种金属元素;故C正确;
D、一个高铁酸钾分子是由7个原子构成的;故D不正确.
故选:C.点评:
本题考点: 化学式的书写及意义;纯净物和混合物的判别;元素的简单分类.
考点点评: 本题主要考查了物质的分类和化学式的意义,完成此题,可以依据已有的知识进行.1年前查看全部
- 高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
(1)高铁酸钾中铁元素的化合价为________,推测它具有的化学性质是________。
(2)在次氯酸钠(NaClO,84消毒液的主要成分)溶液中加入烧碱固体形成碱性环境,将研磨的硝酸铁少量多次地加入到上述溶液中,冰浴中反应1 h。发生的离子反应为2Fe3++3ClO-+10OH-===2FeO2-4+3Cl-+5H2O,氧化剂是________。将KOH加入到反应后的溶液搅拌半小时。静置,抽滤粗产品。该反应的化学方程式为2KOH+Na2FeO4===K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度________(填:大于、小于或等于)高铁酸钾的溶解度。
(3)在强碱性溶液中,高铁酸钾能将亚铬酸钾(KCrO2)氧化为铬酸钾(K2CrO4),生成的铬酸盐溶解酸化后,得到的重铬酸钾(K2Cr2O7)用(NH4)2Fe(SO4)2的标准溶液滴定,以二苯胺磺酸钠为指示剂。到达滴定终点时,溶液由紫色变为淡绿色(+6价铬转化成+3价铬),有关离子方程式为FeO2-4+CrO-2+2H2O===CrO2-4+Fe(OH)3↓+OH-,2CrO2-4+2H+===Cr2O2-7+H2O,2Cr2O2-7+6Fe2++14H+===2Cr3++6Fe3++7H2O
现称取5.00g高铁酸钾样品于烧杯中,加入适量氢氧化钾溶液,加入稍过量的KCrO2,充分反应后,转移到250 mL容量瓶中,定容,量取25.00 mL,再用稀硫酸酸化,用0.1000 mol•L-1的(NH4)2Fe(SO4)2标准溶液滴定,用去标准溶液33.33 mL。计算上述实验制得的样品中,高铁酸钾的质量分数为________;
(4)明矾、硫酸铁、高铁酸钾都能净水,简述高铁酸钾净水原理:
________________________________________________________________________。 yiguzhou1年前1
yiguzhou1年前1 -
 晴天5658 共回答了2个问题
晴天5658 共回答了2个问题 |采纳率50%太长了1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3
高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3 +3Cl 2 +10KOH=2K 2 FeO 4 +6KCl+8H 2 O,对于该反应,下列说法正确的是( ) A.该反应是复分解反应 B.钾元素化合价降低 C.Cl 2 是还原剂 D.Fe(OH) 3 发生氧化反应  正茂ii1年前1
正茂ii1年前1 -
 沙茶牛肉片 共回答了17个问题
沙茶牛肉片 共回答了17个问题 |采纳率94.1%A.Fe和Cl的化合价发生变化,属于氧化还原反应,故A错误;
B.K元素的化合价没有发生变化,故B错误;
C.Cl元素的化合价降低,被还原,Cl 2 是氧化剂,故C错误;
D.Fe元素的化合价升高,被氧化,Fe(OH) 3 发生氧化反应,故D正确.
故选D.1年前查看全部
大家在问
- 1一个生日蛋糕,切成五等份的每一块比切成七等份的每一块重80克,这个生日蛋糕重多少克?
- 2《两小儿辨日》“孔子不能决也”,我能“决”!请你分析“两小儿”的难题.
- 3A、B两地相距5000千米,甲、乙两车分别从A、B两地同时出发,相向而行,甲速度为120千米\时,
- 4(1)一条直线可以把平面分成两个部分(或区域),如图,两条直线可以把平面分成几个部分?三条直线可以把平面分成几个部分?试
- 5很小很小的小螃蟹吃什么分两种说吧 一种是刚脱离母螃蟹的 宽0.5毫米(吃什么、住的环境);还有一种是宽1.2厘米的(吃什
- 6礼轻情意重的英文A—— —— means a lot
- 7丌分之s是单项式吗,兀(R^2+r^2)是多项式吗
- 8要一篇英语励志小短文,120字左右的,今天要!
- 9英语翻译4.Critical accounting estimates and judgements in applyi
- 10(2011•沙湾区二模)等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生
- 11诗人独酌的原因是(),诗中三人指?
- 12I busy doing homework.busy后一定要加ing么
- 13牛顿运动定律 内容及其影响?
- 14与人体内环境及稳态有关的叙述,正确的是( )
- 15下面是对汽车的某些配置和行驶有关规定的表述,其中与物体惯性无关的是( )

