次氯酸盐在碱性条件下能否氧化亚硫酸根?
 苏墨荷2022-10-04 11:39:544条回答
苏墨荷2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 大堡礁红树林 共回答了13个问题
大堡礁红树林 共回答了13个问题 |采纳率76.9%- 可以,只不过在酸性条件下氧化性最强.亚硫酸根有还原性,次氯酸根有氧化性.次氯酸是氯气通入碱中制得,如漂粉精 生成次氯酸根和氯离子(碱性环境),然而在酸性环境下氯离子和次氯酸根又能归盅反应,生氯气.
- 1年前
 河头的榕树 共回答了8个问题
河头的榕树 共回答了8个问题 |采纳率- 能 次氯酸盐碱性条件下也有强氧化性,次氯酸钠就是碱性的,可以将亚硫酸根氧化为硫酸根。
- 1年前
 149092743 共回答了8个问题
149092743 共回答了8个问题 |采纳率- 能 SO32- + ClO- = SO42- + Cl-
亚硫酸根有还原性,次氯酸根有氧化性
次氯酸是氯气通入碱中制得,如漂粉精 生成次氯酸根和氯离子(碱性环境),然而在酸性环境下氯离子和次氯酸根又能归盅反应,生氯气 碱性能 - 1年前
 hekailawyer 共回答了13个问题
hekailawyer 共回答了13个问题 |采纳率- 能的
- 1年前
相关推荐
- (2014•永州三模)镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池
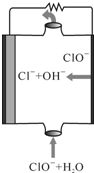 (2014•永州三模)镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )
(2014•永州三模)镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )
A.电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl-
B.放电过程中OH-移向正极
C.镁电池中镁均为负极,发生氧化反应
D.镁-过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O 锦言1年前1
锦言1年前1 -
 夕阳倦了 共回答了29个问题
夕阳倦了 共回答了29个问题 |采纳率93.1%解题思路:该燃料电池中,镁易失电子作负极、次氯酸根离子得电子发生还原反应,负极电极反应式为Mg-2e-=Mg 2+,正极电极反应式为:ClO-+H2O+2e-=Cl-+2OH-,放电时,电解质溶液中阴离子向负极移动.A.镁在负极上失电子生成镁离子,次氯酸根离子在正极上得电子和水生成氯离子和氢氧根离子,所以电池反应式为:Mg+ClO-+H2O=Mg(OH)2+Cl-,故A正确;
B.放电过程中氢氧根离子向负极移动,故B错误;
C.镁失电子发生氧化反应而作负极,故C正确;
D.酸性介质中,正极上双氧水得电子发生还原反应,电极反应式为H2O2+2H++2e-═2H2O,故D正确;
故选B.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池原理,明确正负极上发生的反应是解本题关键,再结合离子移动方向来分析解答,题目难度不大.1年前查看全部
- 镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO - + H 2 O
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO - + H 2 O + 2e - = Cl - + 2OH - ,关于该电池的叙述正确的是
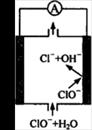
A.该电池中镁为负极,发生还原反应 B.电池工作时,OH - 向正极移动 C.电池工作时,正极周围溶液的pH将不断变小 D.该电池的总反应为:Mg + ClO - + H 2 O = Mg(OH) 2 ↓+ Cl -  Anna18281年前1
Anna18281年前1 -
 mike_829 共回答了20个问题
mike_829 共回答了20个问题 |采纳率80%D
1年前查看全部
- 高氯酸盐,氯酸盐,亚氯酸盐,次氯酸盐,氯气,它们的氧化性强弱之比
高氯酸盐,氯酸盐,亚氯酸盐,次氯酸盐,氯气,它们的氧化性强弱之比
不懂的别扯淡 做你的宠物1年前1
做你的宠物1年前1 -
 snow654321 共回答了15个问题
snow654321 共回答了15个问题 |采纳率93.3%楼上,提问的不是说了,不懂的别捣乱
溶液中比较电极电势,并且必须是相同条件下
事实上含氧酸氧化性次氯酸大于亚氯酸大于氯酸大于高氯酸1年前查看全部
- 氯气与碱反应生成次氯酸盐和金属氯化物
氯气与碱反应生成次氯酸盐和金属氯化物
这句话 9407121年前1
9407121年前1 -
 qogtyu 共回答了19个问题
qogtyu 共回答了19个问题 |采纳率94.7%Cl2+2NaOH=NaClO+NaCl+H2O
对1年前查看全部
- 高中化学氯气一章中次氯酸钠和次氯酸钙(次氯酸盐本身是否具有漂白性?)
高中化学氯气一章中次氯酸钠和次氯酸钙(次氯酸盐本身是否具有漂白性?)
最近听老师和同学说了很多答案,都被弄模糊了,有人说有漂白性,是因为次氯酸钠和次氯酸钙水解成了次氯酸,那么是次氯酸起漂白作用吗?也就是说,次氯酸钙和次氯酸钠本身无漂白作用? horsemz1年前1
horsemz1年前1 -
 恋冰蓝草 共回答了18个问题
恋冰蓝草 共回答了18个问题 |采纳率94.4%你要搞清楚是怎麼漂白的 水解没错 生成了次氯酸 次氯酸又会分解出“原子氧” 这个”原子氧“才是有漂白作用的 所以他们本身都不能漂白 水解之後并产生了”原子氧“才行1年前查看全部
- 次氯酸盐怎样在使用过程中变成次氯酸的?化学学霸们,帮帮忙呗
 她视为1年前1
她视为1年前1 -
 井里de宝贝 共回答了8个问题
井里de宝贝 共回答了8个问题 |采纳率25%二氧化碳1年前查看全部
- 实验室制氯气(次氯酸盐)反应方程式是什么?
 口袋里的零钱1年前2
口袋里的零钱1年前2 -
 linda7798 共回答了17个问题
linda7798 共回答了17个问题 |采纳率76.5%Cl- +ClO- +2H+ ==Cl2+H2O1年前查看全部
- 次氯酸盐可以完全电离吗次氯酸不是弱酸吗为啥 CL2+2OH(-)====CL(-)+CLO(-)+H2O
 花折叶1年前1
花折叶1年前1 -
 陈浩畅 共回答了18个问题
陈浩畅 共回答了18个问题 |采纳率88.9%可以.和醋酸钙类似啦.醋酸也是弱酸,但醋酸钙是强电解质,能够完全电离1年前查看全部
- 怎么样区别氯酸盐和次氯酸盐
 zzmm1年前1
zzmm1年前1 -
 换皮 共回答了27个问题
换皮 共回答了27个问题 |采纳率88.9%如果两者盐都是可溶的
可以直接配成溶液,因为次氯酸为弱酸
次氯酸盐就是显弱碱性的
氯酸盐溶液为中性的
即加酚酞溶液
如果不是可溶的,步骤麻烦1年前查看全部
- 次氯酸盐的化学性质它有什么化学性质
 Zyniker1年前1
Zyniker1年前1 -
 panmuqing 共回答了17个问题
panmuqing 共回答了17个问题 |采纳率94.1%次氯酸盐是次氯酸的盐,含有次氯酸根离子ClO−,其中氯的氧化态为+1.次氯酸盐常以溶液态存在,不稳定,会发生歧化反应生成氯酸盐和氯化物.见光分解为氯化物和氧气.
次氯酸盐是一种常用的漂白剂和消毒剂.在人体组织中,在亚铁血红素的髓过氧化物酶的催化作用下,过氧化物与氯化物反应可产生C lO-或HC lO.这种在血球内产生的C lO-/HC lO或C l2(HOC l的分解产物)在生物大分子的氧化损伤过程中所起的作用已成为目前生物化学研究的热点问题之一.1年前查看全部
- 次氯酸盐与空气中的水、二氧化碳反应生成不稳定的次氯酸的化学方程式
 lhy09191年前4
lhy09191年前4 -
 ktv001ktv001 共回答了25个问题
ktv001ktv001 共回答了25个问题 |采纳率100%2NaCIO + H2O + CO2 = Na2CO3 + 2 HCIO1年前查看全部
- (1)已知Fe(OH)3能与次氯酸盐发生如下反应(未配平):Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2
(1)已知Fe(OH)3能与次氯酸盐发生如下反应(未配平):Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2O
①已知有10.7g Fe(OH)3参加反应,共转移了0.3NA个电子,则n=______,FeO4n-中铁元素的化合价为______.
②根据所学的知识,推测FeO4-能和下列______(填序号)物质反应.
A.KMnO4 B.SO2 C.H2S D.O2
(2)一定条件下,向含硝酸的废水中加入CH3OH,将HNO3还原成N2.若该反应消耗32g CH3OH,转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是______. tcsujdr1年前1
tcsujdr1年前1 -
 阴阳两茫茫 共回答了11个问题
阴阳两茫茫 共回答了11个问题 |采纳率81.8%解题思路:(1)反应中Fe元素化合价升高,被氧化,Cl元素化合价降低,被还原,结合氧化还原反应中氧化剂、还原剂得失电子数目相等计算;
(2)32gCH30H转移6mol电子,即1mol还原剂参加反应转移6mol电子,根据消耗甲醇的量和转移电子的量来书写方程式,并确定氧化剂和还原剂的量的多少;.(1)①n(Fe(OH)3)=[10.7g/107g/mol]=0.1mol,设Fe被氧化生成的FeO4n-中Fe元素化合价为x,
则0.1mol×(x-3)=0.3mol,x=6,由化合价代数和为0可知,n=2,
故答案为:2;+6;
②FeO42-中Fe为+6价,具有强氧化性,可与还原性物质反应,B、C符合,
故答案为:B、C;
(2)消耗32g(1mol)CH3OH转移6mol电子,由CH3OH中碳原子的化合价升高6,所以反应后碳的化合价为+4,产物为CO2,根据质量守恒和化合价升降总数相等得:5CH3OH+6HNO3═5CO2+3N2+13H2O,反应中氧化剂是硝酸,还原剂是甲醇,参加反应的还原剂和氧化剂的物质的量之比是5:6,
故答案为:5:6.点评:
本题考点: 氧化还原反应的计算.
考点点评: 本题考查氧化还原反应的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意从元素化合价的角度解答该题,难度中等.1年前查看全部
- 各高锰酸盐 和次氯酸盐的溶解度 包括难容的不容的 溶
 外强中干1年前1
外强中干1年前1 -
 68nanquan 共回答了17个问题
68nanquan 共回答了17个问题 |采纳率76.5%常见的次氯酸盐都可溶
高锰酸钙 溶于液氨
高锰酸铯 微溶于水
钠盐钾盐都溶1年前查看全部
- 次氯酸和次氯酸盐的一个问题次氯酸盐分别从金属活动性最强到最弱,和次氯酸形成的盐氧化性有什么变化?(比如KClO,CaCl
次氯酸和次氯酸盐的一个问题
次氯酸盐分别从金属活动性最强到最弱,和次氯酸形成的盐氧化性有什么变化?
(比如KClO,CaClO,NaClO一直排下去到AuClO)氧化性有什么变化? yuyan57191年前2
yuyan57191年前2 -
 潘趣酒 共回答了18个问题
潘趣酒 共回答了18个问题 |采纳率94.4%这个问题比较新颖
几乎没人问
他们的氧化性,可以默认为相近,都是氯元素(+1)的强氧化性1年前查看全部
- 为什么弱酸盐能电离?弱酸在写离子方程的时候不是不拆开嘛,为什么弱酸盐比如次氯酸盐就拆开了呢?
 syscqt1年前1
syscqt1年前1 -
 xinjiangyrc 共回答了15个问题
xinjiangyrc 共回答了15个问题 |采纳率80%简单点的解释就是:弱酸拆不开是因为氢离子与酸根之间的作用力(共价键)不易断开,而弱酸盐的阳离子则和酸根是离子形式结合,在水中就能都全部分开.1年前查看全部
- 次氯酸盐的溶解度都怎么样啊?磷酸盐呢?能不能给各详细点的盐溶解性总结?(特别是那些弱酸盐)
 tonytqp1年前1
tonytqp1年前1 -
 fage850521 共回答了19个问题
fage850521 共回答了19个问题 |采纳率78.9%磷酸的二氢盐都是可溶的;
磷酸盐和磷酸氢盐只溶钾、钠、铵
常见的次氯酸盐都可溶1年前查看全部
- 氯水,次氯酸盐不具有漂白性为什么可用于漂白
 金蚕子1年前1
金蚕子1年前1 -
 小叫天 共回答了18个问题
小叫天 共回答了18个问题 |采纳率94.4%hclo具有漂白性.
给你一个方成式
cl2+h2o生成hcl+hclo(双向箭头)1年前查看全部
- 84是酸性还是碱性的84消毒液是酸性的还是碱性的84消毒液—— 次氯酸盐,次氯酸盐和空气中的水和二氧化碳接触,反应,生成
84是酸性还是碱性的
84消毒液是酸性的还是碱性的
84消毒液—— 次氯酸盐,次氯酸盐和空气中的水和二氧化碳接触,反应,生成碳酸盐和次氯酸,而次氯酸不稳定,易分解生成盐酸和原子状态的氧“O”.原子状态的氧具有强氧化性,能够杀灭细菌,病毒等. zwfzxy1年前1
zwfzxy1年前1 -
 琪lyx 共回答了20个问题
琪lyx 共回答了20个问题 |采纳率85%84消毒液是有次氯酸钠和次氯酸的氧化性消毒的 故显酸性1年前查看全部
- 次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
次氯酸盐是一些 ,和 的有效成分,如次氯酸钠是84消毒液的有效成分,次氯酸钙是漂白粉的有效成分,
他们与 反应生成次氯酸,起到漂白的作用,有关反应方程式为 . wang13yu101年前3
wang13yu101年前3 -
 月伴弯 共回答了20个问题
月伴弯 共回答了20个问题 |采纳率90%消毒剂 漂白剂
CO2和水
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
2NaClO + H2O+CO2=2HClO + Na2CO31年前查看全部
- 水杨酸次氯酸盐光度测氨氮时,国标说要50g水杨酸等等.怎么样能让水杨酸完全溶解呢?
水杨酸次氯酸盐光度测氨氮时,国标说要50g水杨酸等等.怎么样能让水杨酸完全溶解呢?
我每次实验都不能让水杨酸完全溶解.能不能等比例缩小水杨酸,氢氧化钠,酒石酸钾钠的用量? 糊涂一生02021年前1
糊涂一生02021年前1 -
 IST远程qq 共回答了18个问题
IST远程qq 共回答了18个问题 |采纳率94.4%若水杨酸未能全部溶解,可再加入数毫升氢氧化钠溶液,直至完全溶解为止,最后溶液的PH为6.0~6.5.水杨酸与氢氧化钠时,最后的PH为6.0~6.5不好掌握,为此,本人把水杨酸改为水杨酸柠檬酸,取柠檬酸10克,加入10ml水溶解,另取5...1年前查看全部
大家在问
- 1求老师解答:为下列的加粗字注音.
- 2句型转换This is the plan that was suggested at the meeting yeste
- 3高二数学必修二答疑若点A、B是平面α内的两点,点C是直线AB上的点,则C必在α内,这一命题用符号语言可以表述为_____
- 4用动词的适当形式填空1.She _________(go) to school at seven o’clock.2.I
- 5一道数学题(快)自然科学兴趣小组的同学采集的动物标本数量是植物标本数量的70%,已知动物标本比植物标本少24件.两种标本
- 6小孔成像的实验报告怎么写太阳光照射在树荫里,射下来的光在地面上形成了光斑,探究这些光斑的形状和什么有关的实验报告
- 7移液管中的溶液可以直接加入容量瓶吗?
- 8改错He is younger and stronger than you do.为什么要删去do
- 9庹 【拼音】:[tuǒ] 【字义】:1.中国一种约略计算长度的单位,以成人两臂左右伸直的长度为标准,约合五市
- 10baggage到底是可数名词还是不可数名词?
- 11下列有关孟德尔豌豆的七对相对性状杂交实验的说法中错误的是
- 12孟德尔遗传定律与基因自由组合定律有什么区别
- 13据报载,美国宇航员阿姆斯特朗在月球上烙下了人类第一只脚印,迈出了人类征服宇宙的一大步,在月
- 14化学与生物哪个更难?
- 15已知数列(An)中的相邻两项A2k-1与A2k是关于x的方程x^2-(3k+2^k)x+3k*2^k=0的两个根,且A2
