(2005•资阳区)物质在发生化学反应的过程中,构成物质的下列粒子一定发生变化的是( )
 筑梦开始2022-10-04 11:39:541条回答
筑梦开始2022-10-04 11:39:541条回答A.分子
B.原子
C.原子核
D.电子

已提交,审核后显示!提交回复
共1条回复
 殿下Deoo妃 共回答了13个问题
殿下Deoo妃 共回答了13个问题 |采纳率69.2%- 解题思路:在化学反应里,分子可以再分,原子不能再分,原子是化学变化中的最小粒子,原子是由原子核和核外电子构成.
A、化学变化的实质是有新物质生成,有新物质生成也就有新分子生成,即分子一定变;故A正确;
B、原子是化学变化中的最小粒子,在化学变化中不能再分;故B不正确;
C、原子是由原子核和核外电子构成.原子在化学变化中不能再分,原子核也不能分;故C不正确;
D、原子是由原子核和核外电子构成.原子在化学变化中不能再分,核外电子也不能分;故D不正确;
故选A点评:
本题考点: 分子和原子的区别和联系;质量守恒定律及其应用.
考点点评: 此题主要考查分子与原子区别与联系,原子的定义及组成,此题基础性较好. - 1年前
相关推荐
- (2005•资阳区)下列饮食与健康关系的说法不正确 的是( )
(2005•资阳区)下列饮食与健康关系的说法不正确 的是( )
A.食物中缺乏维生素C,会引起坏血病
B.用加碘盐作调味剂,可预防大脖子病
C.适量补充硫酸亚铁,可预防缺铁性贫血
D.不吃肉类,可保持苗条身材,有利健康 e_1181年前1
e_1181年前1 -
 乐乐wu 共回答了17个问题
乐乐wu 共回答了17个问题 |采纳率94.1%解题思路:可根据微量元素及营养素与人体健康的关系及生理作用进行分析.A、缺乏维生素C会患坏血病,所以要多吃蔬菜和水果,正确.
B、碘是合成甲状腺激素的主要元素,缺乏会患大脖子病,正确.
C、铁元素是合成血红蛋白的主要元素,缺乏会患贫血,所以正确.
D、油脂是重要的功能物质,还是维持生活活动的备用能源,应当适量食用,所以错误.
故选D点评:
本题考点: 微量元素、维生素与健康的关系及摄取方法;生命活动与六大营养素.
考点点评: “民以食为天”,在生活水平不断提高的今天,人们把对健康饮食的追求提上了生活的日程,所以对六大营养素的考查也成了热点之一,特别是六大营养素包括的种类、代谢过程、生理功能、食物来源、缺乏症,摄入时的注意事项等.1年前查看全部
- (2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
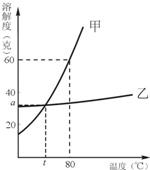 (2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
(2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
(1)将40g甲物质溶解到100g、80℃的热水中,形成的溶液属于(填饱和或不饱和)______溶液;该溶液中溶质的质量分数为______;
(2)甲、乙两物质溶解度相同时的温度是______℃,此温度下的溶解度是______;
(3)不同温度下物质的溶解度不同,两物质随温度变化溶解度变化较大的是______物质. ttl_19841年前1
ttl_19841年前1 -
 yangdy 共回答了17个问题
yangdy 共回答了17个问题 |采纳率100%(1)由甲物质的溶解度曲线可知,80℃时甲物质的溶解度为60g,因此,此时100g水可以完全溶解40g甲且为不饱和溶液;
所得溶液的溶质质量分数=[40g/100g+40g]×100%≈28.6%;
(2)利用曲线图,两物质溶解度曲线在t℃时交于一点,说明此时两物质的溶解度相等,都为a g;
(3)由甲、乙两物质的溶解度曲线可知,甲物质的溶解度曲线曲线为“陡升型”而乙物质的溶解度曲线为“缓升型”,说明甲物质的溶解度随温度变化而有较大的变化;
故答案为:(1)不饱和;28.6%;
(2)t;a g;
(3)甲.1年前查看全部
- (2005•资阳区)味精是谷氨酸钠和氯化钠混合的一种调味剂.某品牌味精包装袋上有如图所示的内容.学校初三“学化学、用化学
(2005•资阳区)味精是谷氨酸钠和氯化钠混合的一种调味剂.某品牌味精包装袋上有如图所示的内容.学校初三“学化学、用化学”兴趣小组同学,设想通过测定味精中NaCl的含量,来探究该味精的有效成分谷氨酸钠是否大于或等于80%的标注含量.他们的实验操作是:用天平准确称量5.88g该味精样品,全部溶解于适量水中,滴加足量的AgNO3溶液,再加入少量稀硝酸(排除杂质干扰检测),将产生的沉淀过滤、洗涤、干燥、称量,得到白色固体AgCl 2.87g.
请你根据他们获得的实验数据,完成探究活动最后的数据分析(要有分析过程)、结果判断工作,最终得出正确的判断结果.XX牌味精
成分:谷氨酸钠(C5H7NO4Na2)≥80%
氧化钠(NaCl)≤20%
净重:100g
生产日期:XX年X月X日
XX味精厂 雨夜清枫1年前1
雨夜清枫1年前1 -
 楚楚爱穆乖 共回答了18个问题
楚楚爱穆乖 共回答了18个问题 |采纳率83.3%解题思路:根据反应的化学方程式,可由生成沉淀氯化银的质量计算出该味精产生中所含氯化钠的质量,味精样品的质量与所计算氯化钠的质量差即为样品中谷氨酸钠的质量,用谷氨酸钠的质量与样品质量比可计算出该味精的有效成分谷氨酸钠的含量,用该含量与包装袋中所标注含量对比,判断谷氨酸钠是否大于或等于80%的标注含量.设味精氯化钠的质量为x
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5
x 2.87g
[58.5/x]=[143.5/2.87g] x=1.17g
该味精的有效成分谷氨酸钠的质量分数=[5.88g−1.17g/5.88g]×100%=80.10%>80%
因此,味精的有效成分谷氨酸钠为80.10%,符合包装袋上谷氨酸钠≥80%的标注含量
答:味精的有效成分谷氨酸钠为80.10%,符合包装袋上谷氨酸钠≥80%的标注含量.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 把化学方程式的计算与生活用品相结合,用计算结果判断生活用品标注是否符合实际,使计算具有现实意义.1年前查看全部
- (000z•资阳区)“绿色化学”是当今化学科学所追求的,了是指化学反应中的反应物全部转化成了人们需要的产物,且没有不需要
(000z•资阳区)“绿色化学”是当今化学科学所追求的,了是指化学反应中的反应物全部转化成了人们需要的产物,且没有不需要的物质或有害物质产生,所得到的产物对环境和人类健康都没有不良影响.小列化学反应类型中,最可能体现“绿色化学”理念的是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应 疯人恶嘴1年前1
疯人恶嘴1年前1 -
 yanghuacong 共回答了22个问题
yanghuacong 共回答了22个问题 |采纳率90.9%解题思路:A、化合反应是指,有两种或两种以上物质反应生成了一种物质.
B、分解反应是指,由一种物质参加反应生成两种或两种以上的其它物质的反应;
C、置换反应是指,由一种单质和一种化合物反应生成另一种单质和另一种化合物;
D、复分解反应是指,两种化合物相互交换成分生成另外两种化合物的反应.通过化和反应的概念看出反应物的各种原子都转化到产品里,没有损失,这个反应符合绿色化学工艺;而由分解反应、置换反应、复分解反应的定义看出反应物的各种原子没有都转化到产品里,还能生成其0物质,甚至是有害物质,反应物有损失,这个反应不符合绿色化学工艺.
故选A点评:
本题考点: 绿色化学;反应类型的判定.
考点点评: 本题考查学生对绿色化学概念的理解,解题时除了要有绿色化学(环境友好型化学)的意识外,还要通过读题搞清绿色化学工艺的含义,即“反应物中的原子全部转化为欲得到的产物,原子的利用率为100%”,然后再逐项判断.1年前查看全部
- (2005•资阳区)我国制碱工业的先驱侯德榜发明了侯氏制碱法,为我国制碱工业的发展做出了极大的贡献.纯碱(化学式为Na2
(2005•资阳区)我国制碱工业的先驱侯德榜发明了侯氏制碱法,为我国制碱工业的发展做出了极大的贡献.纯碱(化学式为Na2CO3)是常见的工业用碱,也是许多化工产品的生产原料,在生活和生产中得到广泛应用.
(1)纯碱不是碱,在化学物质分类中属于______类物质;
(2)石灰石、大理石的主要成分是______,在组成上与纯碱具有相同的组成部分,因而,它们都能与盐酸反应产生(填具体物质)______气体;
(3)纯碱溶液与石灰水反应可制得少量NaOH溶液,写出反应的化学方程式:______;在反应基本类型中,该反应属于______反应. 小黑96111年前1
小黑96111年前1 -
 liyayadong 共回答了20个问题
liyayadong 共回答了20个问题 |采纳率95%解题思路:(1)碱类物质和盐类物质的区别是:碱是有金属阳离子和氢氧根离子构成的化合物,而盐是有金属阳离子和酸根离子构成的化合物;
(2)碳酸盐都能和盐酸反应生成二氧化碳气体;
(3)复分解反应是两种化合物相互交换成分生成另外两种化合物.条件是生成物中需有气体或沉淀或水生成.(1)纯碱是Na2CO3,是有金属阳离子和酸根离子构成的化合物,所以纯碱是盐而不是碱;
(2)大理石和石灰石的主要成分都是碳酸钙;碳酸钙和纯碱都具有碳酸根,都能和稀盐酸反应放出二氧化碳气体;
(3)纯碱和石灰水反应生成碳酸钙沉淀和氢氧化钠,方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,此反应满足复分解反应的条件有沉淀生成,故属于复分解反应.
故答案为:
(1)盐类
(2)CaCO3,二氧化碳
(3)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,复分解点评:
本题考点: 碳酸钠、碳酸氢钠与碳酸钙;常见的氧化物、酸、碱和盐的判别;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题考查有碱和盐的区别、碳酸盐的性质、复分解反应等知识点,难度较小,比较容易作答,属于基础型题.1年前查看全部
- (2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4)
(2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4),由此判断作物秸秆含有碳碳元素和氢氢元素;在农村,燃烧沼气可用于做饭、点灯,其能量转化形式是由化学能转化成热能和光能化学能转化成热能和光能;沼气作为资源再利用的燃料,对环境而言属于比较清洁的清洁的(填清洁或不清洁) 燃料.
 chn00781年前1
chn00781年前1 -
 kkmkjjj 共回答了14个问题
kkmkjjj 共回答了14个问题 |采纳率92.9%植物秸秆经微生物作用产生沼气,沼气的主要组成元素是碳元素和氢元素,由此判断作物秸秆含有碳元素和氢元素.故填:碳;氢.
燃烧沼气可用于做饭、点灯,其能量转化形式是由化学能转化成热能和光能.故填:化学能转化成热能和光能.
甲烷燃烧能生成水和二氧化碳,对环境污染较小,是一种比较清洁的能源.故填:清洁的.1年前查看全部
- (2005•资阳区)水是常见的溶剂,许多物质可以在水中溶解,因而,在生活中常用水洗菜、洗碗、洗衣服.但不同的物质在水中溶
(2005•资阳区)水是常见的溶剂,许多物质可以在水中溶解,因而,在生活中常用水洗菜、洗碗、洗衣服.但不同的物质在水中溶解性不同,有的物质在水中就难以溶解.在生活中可向水中填加助溶剂溶解一些难溶于水的物质.根据你的生活经验,当衣服上有油污时,可向洗衣服的水中添加下列物质作助溶剂的是( )
A.食盐
B.白酒
C.食醋
D.洗涤剂 勇敢的小心1年前1
勇敢的小心1年前1 -
 瘦水陀螺 共回答了27个问题
瘦水陀螺 共回答了27个问题 |采纳率88.9%解题思路:生活中或实验室中洗涤的原理主要有三种,一是利用化学反应把不溶物变成可溶物而洗去,二是利用乳化作用原理,把油污变成细小的油滴,形成乳浊液而洗去,三是利用溶解原理,把物质溶解于水形成溶液而洗去,在洗涤时,要根据被洗涤的物质成分选择合适的原理和方法.食盐、白酒、食醋都不具备上述的洗涤原理,故错.
D、洗涤剂中有乳化剂,具有乳化作用,能将油污变成细小的油滴,从而形成乳浊液而被洗掉,故对.
故选D点评:
本题考点: 溶解现象与溶解原理;乳化现象与乳化作用.
考点点评: 根据洗涤剂的去污原理回答,乳化原理.1年前查看全部
- (2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4)
(2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4),由此判断作物秸秆含有碳碳元素和氢氢元素;在农村,燃烧沼气可用于做饭、点灯,其能量转化形式是由化学能转化成热能和光能化学能转化成热能和光能;沼气作为资源再利用的燃料,对环境而言属于比较清洁的清洁的(填清洁或不清洁) 燃料.
 志不同道不合1年前1
志不同道不合1年前1 -
 狂徒DOMO 共回答了15个问题
狂徒DOMO 共回答了15个问题 |采纳率66.7%植物秸秆经微生物作用产生沼气,沼气的主要组成元素是碳元素和氢元素,由此判断作物秸秆含有碳元素和氢元素.故填:碳;氢.
燃烧沼气可用于做饭、点灯,其能量转化形式是由化学能转化成热能和光能.故填:化学能转化成热能和光能.
甲烷燃烧能生成水和二氧化碳,对环境污染较小,是一种比较清洁的能源.故填:清洁的.1年前查看全部
- (2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4)
(2005•资阳区)农村许多作物的秸秆,过去都是一烧了之,现在可铡碎后放入沼气池,经微生物作用产生沼气(主要成分CH4),由此判断作物秸秆含有______元素和______元素;在农村,燃烧沼气可用于做饭、点灯,其能量转化形式是由______;沼气作为资源再利用的燃料,对环境而言属于比较______(填清洁或不清洁) 燃料.
 信封1年前1
信封1年前1 -
 wuweishizhen 共回答了18个问题
wuweishizhen 共回答了18个问题 |采纳率94.4%解题思路:根据生成物可以判断反应物的元素组成;
化学能、热能、光能等能量之间可以相互转化;
甲烷燃烧能生成水和二氧化碳,是一种比较清洁的能源.植物秸秆经微生物作用产生沼气,沼气的主要组成元素是碳元素和氢元素,由此判断作物秸秆含有碳元素和氢元素.故填:碳;氢.
燃烧沼气可用于做饭、点灯,其能量转化形式是由化学能转化成热能和光能.故填:化学能转化成热能和光能.
甲烷燃烧能生成水和二氧化碳,对环境污染较小,是一种比较清洁的能源.故填:清洁的.点评:
本题考点: 甲烷、乙醇等常见有机物的性质和用途;物质的元素组成;物质发生化学变化时的能量变化.
考点点评: 解答本题要充分理解质量守恒定律的内容,要掌握能量之间的转化关系,理解节能环保的重要性.1年前查看全部
- (2005•资阳区)氢气是未来的理想能源,下列微小粒子能保持氢气化学性质的是( )
(2005•资阳区)氢气是未来的理想能源,下列微小粒子能保持氢气化学性质的是( )
A.H+
B.H2
C.H
D.H2O 李智5211年前1
李智5211年前1 -
 小懿1128 共回答了15个问题
小懿1128 共回答了15个问题 |采纳率100%解题思路:分子是保持物质化学性质的最小微粒,原子是化学变化中的最小微粒.氢气是由分子构成的物质,保持氢气化学性质的粒子是氢分子.
故选B.点评:
本题考点: 分子的定义与分子的特性.
考点点评: 本题主要考查了分子的性质及应用方面的知识.此题还能提示学生对原子、离子知识的梳理.1年前查看全部
- (2005•资阳区)通过学习我们知道,氢气、单质碳和一氧化碳在一定条件下,都能夺取氧化物中的氧,而具有还原性.下列反应方
(2005•资阳区)通过学习我们知道,氢气、单质碳和一氧化碳在一定条件下,都能夺取氧化物中的氧,而具有还原性.下列反应方程式能表示炼铁高炉中,将铁还原出来的反应是( )
A.3H2+Fe2O3
2Fe+3H2O△ .
B.3C+2Fe2O3
4Fe+3CO2高温 .
C.3CO+Fe2O3
2Fe+3CO2高温 .
D.C+CO2
2CO高温 . 雨夜长歌1年前1
雨夜长歌1年前1 -
 siva_0 共回答了15个问题
siva_0 共回答了15个问题 |采纳率100%解题思路:在炼铁高炉中是发生的一氧化碳与氧化铁的反应,把铁从氧化铁中置换出来,利用这一知识解决问题.在炼铁高炉中发生反应的还原剂是一氧化碳,一氧化碳会与氧化铁发生还原反应,把铁从其氧化物中置换出来,生成铁与二氧化碳,氢气与碳还原氧化铁的反应在高炉中不会发生,碳与二氧化碳的反应会发生但不是还原铁的反应.
故选C点评:
本题考点: 铁的冶炼;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题是对炼铁知识的考查,只要知道炼铁高炉中发生的具体反应就能解决问题,属基础知识考查题.1年前查看全部
- (2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
 (2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
(2005•资阳区)右图为甲、乙两种物质的溶解度曲线图,根据溶解度曲线图回答下列问题:
(1)将40g甲物质溶解到100g、80℃的热水中,形成的溶液属于(填饱和或不饱和)不饱和不饱和溶液;该溶液中溶质的质量分数为28.6%28.6%;
(2)甲、乙两物质溶解度相同时的温度是tt℃,此温度下的溶解度是a ga g;
(3)不同温度下物质的溶解度不同,两物质随温度变化溶解度变化较大的是甲甲物质. lanshui11年前1
lanshui11年前1 -
 ideabai 共回答了17个问题
ideabai 共回答了17个问题 |采纳率82.4%解题思路:(1)根据溶解度曲线可以查找指定温度时物质的溶解度,利用图示的曲线,查出80℃时物质甲的溶解度,判断将40g甲物质放入100g水中是否达到饱和;并计算此时所得溶液的溶质的质量分数;
(2)两条溶解度曲线的交点,表示在该点所示的温度下,两种物质的溶解度相等;利用曲线图,查出两物质溶解度曲线交于一点时的温度及此时的溶解度,溶解度以g为单位;
(3)根据溶解度曲线的坡度越大,说明溶解度受温度影响越大;反之,说明受温度影响较小.利用两物质的溶解度曲线,判断随温度变化溶解度变化较大的物质.(1)由甲物质的溶解度曲线可知,80℃时甲物质的溶解度为60g,因此,此时100g水可以完全溶解40g甲且为不饱和溶液;
所得溶液的溶质质量分数=
40g
100g+40g×100%≈28.6%;
(2)利用曲线图,两物质溶解度曲线在t℃时交于一点,说明此时两物质的溶解度相等,都为a g;
(3)由甲、乙两物质的溶解度曲线可知,甲物质的溶解度曲线曲线为“陡升型”而乙物质的溶解度曲线为“缓升型”,说明甲物质的溶解度随温度变化而有较大的变化;
故答案为:(1)不饱和;28.6%;
(2)t;a g;
(3)甲.点评:
本题考点: 固体溶解度曲线及其作用;饱和溶液和不饱和溶液.
考点点评: 根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;根据溶解度曲线,比较在一定温度范围内的物质的溶解度大小.1年前查看全部
- (2005•资阳区)关于C60的下列说法,不正确 的是( )
(2005•资阳区)关于C60的下列说法,不正确 的是( )
A.分子结构象足球
B.一个分子中有60个碳原子
C.C60、金刚石和石墨均属碳的不同单质
D.属于化合物 浙江横店1年前1
浙江横店1年前1 -
 bobolaw 共回答了18个问题
bobolaw 共回答了18个问题 |采纳率88.9%解题思路:A、可回忆课本C60的结构和俗称进行解答.
B、根据分子化学式的意义进行分析.
C、根据单质的概念进行分析.
D、根据化合物的概念进行分析.A、C60俗称足球烯,回忆课本其结构,可知选项正确.
B、化学式可表示分子中原子的组成及个数,一个C60分子有60个碳原子组成,正确.
C、三种物质都是有一种元素组成的纯净物,所以都属于单质,正确.
D、化合物是有不同元素组成的纯净物,C60是由一种元素组成的,是单质,所以选项错误.
故选D点评:
本题考点: 碳元素组成的单质;单质和化合物的判别;原子的有关数量计算.
考点点评: 本题主要考查了单质和化合物的概念及分子式是意义,对的C60结构学生可能陌生,平时对课本的插图要有所了解.1年前查看全部
- (2005•资阳区)在物质发生化学变化的过程中,一定有( )
(2005•资阳区)在物质发生化学变化的过程中,一定有( )
A.热的放出
B.发光现象
C.气体产生
D.新物质生成 zym1985371年前1
zym1985371年前1 -
 魔天使 共回答了23个问题
魔天使 共回答了23个问题 |采纳率87%解题思路:化学变化中经常伴有的现象并不是化学变化中一定会出现的,化学变化的本质依据是看有无其他物质生成.A、B、C都只是化学变化中经常伴有的现象,如:放热、发光、变色、放出气体、生成沉淀等;但并不是任何化学变化都一定有此现象,但物质发生化学变化时一定会生成新物质;
故选D.点评:
本题考点: 化学变化的基本特征.
考点点评: 考查学生对化学变化的现象的理解和对化学变化本质的认识.1年前查看全部
- (2005•资阳区)实验室制取少量氧气,可用二氧化锰作催化剂,分解过氧化氢制取.如图所示的实验装置(其中仪器①是带活塞的
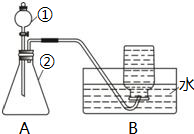 (2005•资阳区)实验室制取少量氧气,可用二氧化锰作催化剂,分解过氧化氢制取.如图所示的实验装置(其中仪器①是带活塞的长颈漏斗)可进行氧气的制取和收集.
(2005•资阳区)实验室制取少量氧气,可用二氧化锰作催化剂,分解过氧化氢制取.如图所示的实验装置(其中仪器①是带活塞的长颈漏斗)可进行氧气的制取和收集.
(1)写出上述实验室制取氧气反应的化学方程式:2H2O2
2H2O+O2↑MnO2 .2H2O2
2H2O+O2↑MnO2 .
(2)用装置A作制氧气的气体发生装置,催化剂放入仪器(选填仪器代号,后同)______中,过氧化氢装入仪器______中;用此装置作为该反应制氧气的发生装置,其优越性是______;
(3)实验室常用B装置进行气体的收集,可得到相对较纯净的气体,具备什么条件的气体可用此装置进行收集?______. 小足过河1年前1
小足过河1年前1 -
 多爱我一点 共回答了19个问题
多爱我一点 共回答了19个问题 |采纳率94.7%解题思路:(1)熟记常用的化学方程式.
(2)固体药品应放在锥形瓶中;液体药品应放在分液漏斗中;从操作是否简单、是否节约药品、生成物是否方便使用等角度进行分析.
(3)气体的收集装置主要由气体的密度和溶水性决定,另外还要考虑气体是否与水反应、是否与空气反应、是否会污染空气等等.(1)过氧化氢以二氧化锰为催化剂生成水和氧气.故答案为:2H2O2
MnO2
.
2H2O+O2↑
(2)二氧化锰是固体,应放在锥形瓶中,过氧化氢溶液是液体,应放在分液漏斗中;使用分液漏斗能随时添加液体药品,能控制反应的发生和停止,还能节约药品.故答案为:②①能控制反应的发生和停止,节约药品
(3)只有不溶于水,不与水发生反应的气体才能用排水法收集.故答案为:不溶于水,不与水反应点评:
本题考点: 氧气的制取装置;常用气体的收集方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 实验室制取气体的发生装置和收集装置要会灵活应用.根据所制取的气体要会选择发生装置和收集装置,对于某一个发生装置和收集装置又能确定要使用该装置应满足什么条件.1年前查看全部
大家在问
- 1整式化简中,如果有0,0能省略吗?
- 2菜豆和黄瓜等植物的种子内没有胚乳,这是因为( )
- 3抛物线y=2x平方+5可以看做是由抛物线y=()沿y轴向()平移()个单位长度得到的.
- 4How was he able to change的意思
- 5图书馆在一楼,我喜欢在那儿看书英文
- 6有一个长方体纸箱,底面是正方形,如果把它的侧面展开,正好是个边长60厘米的正方形,问这个纸箱的容积?
- 7想一想,算一算.(1) 9 10 ÷3表示把______平均分成______份,求其中的1份是多少,也就是求 9 10
- 8电压表测电源电压的所有情况(初中)
- 9本周英语题库:用be动词的正确形式填空
- 10"我只有对你有感觉"用英文怎么说
- 11英语语法题?_________ has been done.A.Ninety nine percents of the
- 12五年级第一学期期终冲刺百分百专题复习三词语答案
- 13大学英语1You speak,write a letter,and make a telephone call.Your
- 143x的4次方+6x的平方减9进行十字相乘法
- 15如图,ad是三角形abc的角平分线,且AC=AB+BD,角c30度,求角∠bac的度数.
