(2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,
 恐龙太太2022-10-04 11:39:543条回答
恐龙太太2022-10-04 11:39:543条回答

已提交,审核后显示!提交回复
共3条回复
 ff5077 共回答了20个问题
ff5077 共回答了20个问题 |采纳率95%- 解题思路:首先在Rt△ABC中利用∠A=30°、AB=12,求得BC=6、AC的长,然后根据四边形CDEF是矩形得到EF∥AC从而得到△BEF∽△BAC,设AE=x,则BE=12-x.利用相似三角形成比例表示出EF、DE,然后表示出有关x的二次函数,然后求二次函数的最值即可.
在Rt△ABC中,∠A=30°,AB=12,
∴BC=6,AC=AB•cos30°=12×
3
2=6
3.
∵四边形CDEF是矩形,
∴EF∥AC.
∴△BEF∽△BAC.
∴[EF/AC=
BE
BA].
设AE=x,则BE=12-x.
EF=
6
3(12−x)
12=
3
2(12−x).
在Rt△ADE中,DE=
1
2AE=
1
2x.
矩形CDEF的面积S=DE•EF=
1
2x•
3
2(12−x)=−
3
4x2+3点评:
本题考点: 相似三角形的应用;二次函数的最值.
考点点评: 本题考查了相似三角形的应用及二次函数的应用,解题的关键是从几何问题中整理出二次函数模型,并利用二次函数的知识求最值. - 1年前
 蓝色水滴2007 共回答了239个问题
蓝色水滴2007 共回答了239个问题 |采纳率- 由基本不等式新制克制,E为AB中点时最大最大值为12S=18*3^1/2
- 1年前
 浓妆妖怪欧吉桑 共回答了314个问题
浓妆妖怪欧吉桑 共回答了314个问题 |采纳率- 设AE=X
S=根3/2 X(6-x/2)
求出当X=多少时,S的最大值即可 - 1年前
相关推荐
- (2012•和平区二模)烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示.则符合该变化的一组物
 (2012•和平区二模)烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示.则符合该变化的一组物质是( )
(2012•和平区二模)烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示.则符合该变化的一组物质是( ) 选项 x y A NaOH溶液 稀HCl(过量) B 稀H2SO4 BaCl2溶液(少量) C Ca(OH)2 CO2(适量) D Ca(OH)2 Na2CO3
A.A
B.B
C.C
D.D 逸云菲1年前1
逸云菲1年前1 -
 我结巴 共回答了17个问题
我结巴 共回答了17个问题 |采纳率82.4%解题思路:当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性;
根据图中pH的变化情况可以判断加入物质的种类.A、氢氧化钠溶液显碱性,pH大于7,当加入过量的稀盐酸时,溶液的pH逐渐减小至小于7.与图不符合;
B、稀硫酸显酸性,pH小于7,x不是稀硫酸.与图不符合;
C、氢氧化钙溶液显碱性,pH大于7,当加入适量二氧化碳时,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,溶液的pH逐渐减小至等于7.与图符合;
D、氢氧化钙溶液显碱性,pH大于7,当加入碳酸钠溶液时,氢氧化钙能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠显碱性,即使溶液的pH减小,也不会减小到7.与图不符合.
故选:C.点评:
本题考点: 碱的化学性质;酸的化学性质.
考点点评: 解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.1年前查看全部
- (2014•和平区二模)某校进入高中数学竞赛复赛的学生中,高一年级有6人,高二年级有12人,高三年级有24人,现采用分层
(2014•和平区二模)某校进入高中数学竞赛复赛的学生中,高一年级有6人,高二年级有12人,高三年级有24人,现采用分层抽样的方法从这些学生中抽取7人进行采访
(Ⅰ)求应从各年级分别抽取的人数:
(Ⅱ)若从抽取的7人中再随机抽取2人做进一步了解
(i)列出所有可能的抽取结果;
(ii)求抽取的2人均为高三年级学生的概率. sunshouxin0011年前1
sunshouxin0011年前1 -
 小鱼吐oO 共回答了10个问题
小鱼吐oO 共回答了10个问题 |采纳率80%解题思路:(Ⅰ)根据方差抽样的定义即可求应从各年级分别抽取的人数:
(Ⅱ)根据古典概型的概率公式即可求出对应的概率.(Ⅰ)∵高一,高二,高三的人数比为6:12:24=1:2:4,
则用分层抽样的方法从这些学生中抽取7人,则高一,高二,高三的人数分别为1,2,4.
(Ⅱ)若从抽取的7人中高一学生记为a,高二的两个学生记为b,c,高三的两个学生记为A,B,C,D,
则抽取2人的结果是(a,b),(a,c),(a,A),(a,B),(a,C),(a,D),
(b,c),(b,A),(b,B),(b,C),(b,D),
(c,A),(c,B),(c,C),(c,D),
(A,B),(A,C),(A,D),(B,C),(B,D),(C,D),共21种结果.
抽取的2人均为高三年级学生(A,B),(A,C),(A,D),(B,C),(B,D),(C,D),共6种结果.
则抽取的2人均为高三年级学生的概率P=[6/21=
2
7].点评:
本题考点: 分层抽样方法.
考点点评: 本题主要考查分层抽样的应用以及古典概率的计算,利用列举法是解决本题概型的基本方法.1年前查看全部
- (2010•和平区一模)下图是某种加钙食盐标签的一部分,请仔细阅读后回答以下问题:
(2010•和平区一模)下图是某种加钙食盐标签的一部分,请仔细阅读后回答以下问题:

(1)包装标签上______元素被称为“智力之花”,可预防甲状腺肿大.
(2)若已知该食盐中钙元素的质量分数为1%,则食盐中碳酸钙的质量分数为______.
(3)由于标签上氯化钠的含量已模糊不清,为了测定食盐中氯化钠的含量,某同学取100.0g样品加水溶解过滤后,加入足量的硝酸银,生成了白色的氯化银沉淀220.8g.试计算该食盐中氯化钠的质量分数(精确到0.1%).______. ceylon_tea1年前1
ceylon_tea1年前1 -
 恐怖聆听者 共回答了20个问题
恐怖聆听者 共回答了20个问题 |采纳率100%解题思路:(1)欲正确解答本题须知碘在人体中的作用;
(2)根据已知条件计算出该食盐中钙元素的质量,再根据碳酸钙中钙元素的质量分数计算出食盐中碳酸钙的质量,然后求出食盐中碳酸钙的质量分数
(3)根据题给条件计算出该食盐中氯化钠的质量,再计算出食盐中氯化钠的质量分数(1)碘是人体内的一种必需微量元素,是甲状腺激素必不可少的成分,当人体缺碘时,甲状腺得不到足够的碘,甲状腺激素及甲状腺球蛋白的合成将会受到影响,使甲状腺组织产生代偿性增生,形成甲状腺肿大症,称为地方性甲状腺肿大,所以被称为智力之花;
(2)该食盐中钙元素的质量为:500g×1%=5g,
则食盐中碳酸钙的质量为:5g÷[40/100]=12.5g,
食盐中碳酸钙的质量分数为:12.5g÷500g×100%=2.5%
(3)根据生成的氯化银的质量可以求出氯化钠的质量,进而求出它的质量分数
故答案为:(1)碘
(2)2.5%
(3)设100g食盐样品中氯化钠的质量为x..
NaCl+AgNO3=NaNO3+AgCl↓
58.5 143.5
x220.8g
[58.5/x =
143.5
220.8g]
解得:x=90.0g
氯化钠的质量分数=[90.0g/100g]×100%=90.0%点评:
本题考点: 缺失标签的药品成分的探究;有关溶质质量分数的简单计算;根据化学反应方程式的计算.
考点点评: 本题主要考查学生对碘在人体中的作用的认识,以及根据化学方程式进行计算的能力,注意根据化学方程式进行计算的主要依据化学方程式,所以务必要保证化学方程式的书写正确.1年前查看全部
- (p03p•和平区模拟)甲数÷乙数=3p…30.当甲数与乙数同时扩大3倍时,那么余数是( )
(p03p•和平区模拟)甲数÷乙数=3p…30.当甲数与乙数同时扩大3倍时,那么余数是( )
A.120
B.90
C.60
D.30 淡淡的蓝_lucky1年前1
淡淡的蓝_lucky1年前1 -
 我家傻笨笨 共回答了16个问题
我家傻笨笨 共回答了16个问题 |采纳率87.5%甲数÷乙数=1他…90.当甲数与乙数同时扩大9倍时,那么余数也扩大9倍,为90×9=90;
故选:B.1年前查看全部
- (2013•和平区模拟)在盛有稀硫酸的烧杯中,分别加入下列物质,最终只存在无色液体的是( )
(2013•和平区模拟)在盛有稀硫酸的烧杯中,分别加入下列物质,最终只存在无色液体的是( )
A.BaCl2溶液、NaOH溶液
B.CuO粉末、Na2SO4溶液
C.Fe2(SO4)3溶液、NaNO3溶液
D.Na2CO3溶液、KOH溶液 无晴雨1年前1
无晴雨1年前1 -
 cony9000 共回答了14个问题
cony9000 共回答了14个问题 |采纳率92.9%解题思路:A、稀硫酸可与BaCl2溶液反应生成硫酸钡白色沉淀;
B、硫酸可与CuO粉末反应生成蓝色溶液硫酸铜;
C、Fe2(SO4)3溶液是黄色溶液;
D、硫酸与Na2CO3溶液反应生成无色硫酸钠溶液,与KOH溶液反应生成无色的硫酸钾溶液.依据题意,在盛有稀硫酸的烧杯中,分别加入下列物质后,最终只存在无色液体,所以所加物质无论与硫酸是否反应,但最终液体应是无色的;
A、稀硫酸可与BaCl2溶液反应生成硫酸钡白色沉淀,最终不是溶液.不符合题意;
B、硫酸可与CuO粉末反应生成蓝色溶液硫酸铜,最终液体不是无色的,不符合题意;
C、Fe2(SO4)3溶液是黄色溶液,最终液体不是无色的,不符合题意;
D、硫酸与Na2CO3溶液反应生成无色硫酸钠溶液,与KOH溶液反应生成无色的硫酸钾溶液,最终液体是无色的,符合题意;
故选D.点评:
本题考点: 酸的化学性质.
考点点评: 含有铜离子的溶液显蓝色,含有铁离子的溶液显黄色,硫酸钡是白色沉淀,了解这些知识及硫酸的化学性质才能正确解答该题.1年前查看全部
- (2010•和平区一模)氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性.区别
(2010•和平区一模)氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性.区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味 痴心爱你1年前1
痴心爱你1年前1 -
 13月32号嫁你 共回答了11个问题
13月32号嫁你 共回答了11个问题 |采纳率81.8%A、NH4C1与KCl均是白色粉末,通过观察外观不能区分,故错误;
B、NH4HCO3与KCl,均能溶于水,故不能区分,故错误;
C、K2S04与Ca3(P04)2,均无气味,闻气味不能区分,故错误;
D、铵盐遇碱会放出氨气,氨气有刺激性气味,则(NH4)2SO4与K2S04前者放氨气,后者没有,故可区分,故正确.
故选D1年前查看全部
- (2008•和平区一模)下列关于种群和物种的叙述不正确的是( )
(2008•和平区一模)下列关于种群和物种的叙述不正确的是( )
A.一个物种可以分为多个种群
B.同一物种的个体都是生活在一起的
C.两个种群件的生殖隔离一旦形成,这两个种群就属于两个物种
D.种群是生物进化的基本单位 yanglifanyang1年前1
yanglifanyang1年前1 -
 lizzy714 共回答了19个问题
lizzy714 共回答了19个问题 |采纳率94.7%解题思路:本题是对种群和物种概念的理解的考查,物种是分布在一定的自然区域内,具有一定的形态结构和生理功能,而且在自然状态下能够相互交配和繁殖,并能够产生可育后代的一群生物个体,种群是指生活在同一地域内的所有同种生物个体的综合,物种可以包含很多种群,但同一种群只能是一个物种.A、一个物种可以生活中不同的地域中,因此一个物种可以分为很多种群,A正确;
B、同一个物种的个体可以生活中不同的地域中,B错误;
C、生殖隔离是物种形成的标志,两个种群件的生殖隔离一旦形成,这两个种群就属于两个物种,C正确;
D、现代生物进化理论认为种群是生物进化的基本单位,D正确.
故选:B.点评:
本题考点: 物种的概念与形成;现代生物进化理论的主要内容.
考点点评: 本题的知识点是物种和种群概念之间的关系,新物种形成的标志,生物进化的单位,对于物种、种群和新物种形成的标志的理解是解题的关键.1年前查看全部
- (2013•和平区一模)在宏观和微观之间建立联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
(2013•和平区一模)在宏观和微观之间建立联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
事实 解释 A 水和过氧化氢化学性质不同 分子构成不同 B NaOH和Ca(OH)2化学性质相似 电离时生成的阴离子都是OH- C 由碳元素组成的金刚石坚硬而石墨很软 原子排列方式不同 D 水电解生成氢气和氧气 水分子是由氢分子和氧分子构成的
A.A
B.B
C.C
D.D 凄凄雪荷1年前1
凄凄雪荷1年前1 -
 moononline 共回答了12个问题
moononline 共回答了12个问题 |采纳率75%解题思路:A、根据水和过氧化氢化学性质不同是因为分子构成不同进行解答;
B、根据NaOH和Ca(OH)2都属于碱,电离时生成的阴离子都是OH-所以化学性质相似进行解答;
C、根据金刚石坚硬而石墨很软是因为碳原子排列方式不同进行解答;
D、根据水分子是由氢原子和氧原子构成的进行解答.A、水是由水分子构成,过氧化氢是由过氧化氢分子构成,所以化学性质不同是因为分子构成不同,故A正确;B、NaOH和Ca(OH)2都属于碱,电离时生成的阴离子都是OH-所以化学性质相似,故B正确;C、金刚石坚硬而石墨很软...
点评:
本题考点: 利用分子与原子的性质分析和解决问题;酸的化学性质.
考点点评: 掌握利用分子和原子的性质分析和解决问题的方法;熟练记忆分子和原子的性质;同种粒子的性质相同,不同种粒子的性质不同.1年前查看全部
- (2013•和平区模拟)下列说法正确的是( )
(2013•和平区模拟)下列说法正确的是( )
A.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O;c(NH4+) 由大到小的顺序是:①>②>③>④
B.某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a
C.物质的量浓度相等的 H2S 和 NaHS 混合溶液中:c (Na+)+c(H+)=c (S2-)+c (HS-)+c (OH-)
D.AgCl悬浊液中存在平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 远实1年前1
远实1年前1 -
 ecl3adadf6a84 共回答了11个问题
ecl3adadf6a84 共回答了11个问题 |采纳率90.9%解题思路:A、铵根离子水解程度小结合的离子对铵根离子的水解的影响分析判断;
B、水电离出的c(H+)=1×10-amol/L,若a>7时水的电离被抑制,酸或碱都能抑制水的电离;
C、依据溶液中的电荷守恒分析判断;
D、程度溶解平衡温度不变,溶度积不变,加入氯化钠平衡左移,离子浓度乘积不变;A、相同物质的量浓度的下列溶液中,①NH4Al(SO4)2溶液中铝离子水解显酸性抑制铵根离子的水解,②NH4Cl溶液中氯离子不影响铵根离子水解、③CH3COONH4溶液中醋酸根水解显碱性,促进铵根离子的水解、④NH3•H2O溶液中存在电离平衡电离程度较小,所以铵根离子浓度大小顺序是:①>②>③>④,故A正确;
B、某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,说明水的电离被抑制,酸或碱都能抑制水的电离,所以PH可以是a,也可以是14-a,故B错误;
C、物质的量浓度相等的 H2S 和 NaHS 混合溶液中存在电荷守恒为:c (Na+)+c(H+)=2c (S2-)+c (HS-)+c (OH-),故C错误;
D、AgCl悬浊液中存在平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,但温度不同溶度积不同,所以氯离子浓度增大,银离子浓度减少,溶液中离子的总浓度不变,故D错误;
故选A.点评:
本题考点: 盐类水解的应用;弱电解质在水溶液中的电离平衡;难溶电解质的溶解平衡及沉淀转化的本质;离子浓度大小的比较.
考点点评: 不同考查了盐类水解的离子浓度大小比较,水的电离平衡影响因素,溶液中电荷守恒的应用,沉淀溶解平衡的溶度积常数的应用.1年前查看全部
- (2012•和平区一模)在平面直角坐标系中,O为坐标原点,已知抛物线C1:y=x2,点A(2,4).
(2012•和平区一模)在平面直角坐标系中,O为坐标原点,已知抛物线C1:y=x2,点A(2,4).
(Ⅰ)求直线OA的解析式;
(Ⅱ)直线x=2与x轴相交于点B,将抛物线C1从点O沿OA方向平移,与直线x=2交于点P,顶点M到A点时停止移动,设抛物线顶点M的横坐标为m.
①当m为何值时,线段PB最短?
②当线段PB最短时,相应的抛物线上是否存在点Q,使△QMA的面积与△PMA的面积相等?若存在,请求出点Q的坐标;若不存在,请说明理由;
(Ⅲ)将抛物线C1作适当的平移,得抛物线C2:y=x2-x+c,若点D(x1,y1),E(x2,y2)在抛物线C2上,且D、E两点关于坐标原点成中心对称,求c的取值范围. benbenbeno1年前0
benbenbeno1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•和平区一模)分析下列研究豌豆种子形状的材料,结合相关知识回答问题:
(2008•和平区一模)分析下列研究豌豆种子形状的材料,结合相关知识回答问题:
材料一:七8上九年,孟德尔发现,用圆形种子的植株与皱缩种子植株进行杂交,子一代(f七)全部为圆形.f七自花授粉后,得到的子二代(f2)有圆形和皱缩两种形状的种子.其中九474颗是圆形的,七***0颗是皱缩的,两者之比为2.9上:七.
材料二:20世纪80年代的研究发现,豌豆的成熟种子圆形与皱缩的差异与淀粉代谢有关.七990年,m.p.bhatta五ha3yya等二指出,在皱缩种子形成的过程中,合成淀粉所需的一种分支酶(ub七j)活性完全丧失,所以种子含有较多游离的蔗糖,而淀粉含量1.这样,会有较多的水分进入种子.当种子发育完成时,水分减1可导致种子体积减小.进一步的研究发现,与圆形种子相比,皱缩种子的ub七Ⅰ基因在一个外显子中插入了800个碱基对.
(七)孟德尔提出了______解释了材料一的试验结果.若将f2植株全部自花授粉,可以预测未来收获的种子中,圆形和皱缩形种子的比例约为______.若想通过“测交”试验来验验材料一中f七产生的花粉基因类型及比例,需要对表现型为______的植株进行去雄处理;
(2)根据材料二提供的信息,你认为豌豆种子皱缩这一性状出现的根本原因是______. polkiuy1年前1
polkiuy1年前1 -
 labyrinth3 共回答了15个问题
labyrinth3 共回答了15个问题 |采纳率100%解题思路:根据题意分析可知:圆形种子的植株与皱缩种子植株进行杂交,子一代自花授粉后,得到的子二代约3:1,所以符合基因的分离定律.基因突变是指DNA分子中发生碱基对的替换、增添和缺失而引起基因结构的改变.(1)根据得到的子二代(她2)中,圆形种子:皱缩种子=口:1,可推测豌豆种子形状是由三对等位基因控制.因此孟德尔提出多基因的分离定律解释多材料三的试验结果.设圆形的基因型为AA和Aa,则皱缩的基因型为aa.因此...
点评:
本题考点: 基因的分离规律的实质及应用;基因突变的特征.
考点点评: 本题考查基因的分离定律和基因突变的相关知识,意在考查学生的识记能力和判断能力,运用所学知识综合分析问题的能力.1年前查看全部
- (2013•和平区一模)电阻可忽略的光滑平行金属导轨,两导轨间距L=0.75m,导轨倾角为30°,导轨上端ab接一阻值R
 (2013•和平区一模)电阻可忽略的光滑平行金属导轨,两导轨间距L=0.75m,导轨倾角为30°,导轨上端ab接一阻值R=1.5Q的电阻,磁感应强度B=0.8T的匀强磁场垂直轨道平面向上.阻值r=0.5Q,质量m=0.2kg的金属棒与轨道垂直且接触良好,从轨道上端ab处由静止开始下滑至底端,在此过程中金属棒产生的焦耳热Qr=0.1J.(取g=10m/s2)求:
(2013•和平区一模)电阻可忽略的光滑平行金属导轨,两导轨间距L=0.75m,导轨倾角为30°,导轨上端ab接一阻值R=1.5Q的电阻,磁感应强度B=0.8T的匀强磁场垂直轨道平面向上.阻值r=0.5Q,质量m=0.2kg的金属棒与轨道垂直且接触良好,从轨道上端ab处由静止开始下滑至底端,在此过程中金属棒产生的焦耳热Qr=0.1J.(取g=10m/s2)求:
(1)金属棒在此过程中克服安培力的功W安;
(2)金属棒下滑速度v=2m/s时的加速度a. samguday1年前1
samguday1年前1 -
 sophietyliu 共回答了16个问题
sophietyliu 共回答了16个问题 |采纳率100%解题思路:(1)根据功能关系知道:金属棒在此过程中克服安培力的功W安等于整个电路中产生的焦耳热.由于R=3r,由焦耳定律分析得知R上产生的焦耳热是棒上产生的焦耳热的3倍,即可求得W安;(2)金属棒下滑过程中,受到重力、轨道的支持力和安培力,根据F=BIL、I=BLvR+r求得安培力F,根据牛顿第二定律列式可求得加速度.(1)由题知,R=3r,通过R的电流与金属棒的电流又相同,所以在棒下滑过程中,R上产生的焦耳热为QR=3Qr=0.3J
根据功能关系得:金属棒在此过程中克服安培力的功W安=QR+Qr=0.4J
(2)金属棒下滑速度v=2m/s时,所受的安培力为F=BIL=B
BLv
R+rL=
B2L2v
R+r
由牛顿第二定律得:mgsin30°-
B2L2v
R+r=ma
得a=gsin30°-
B2L2v
m(R+r)
代入解得,a=3.2m/s2
答:
(1)金属棒在此过程中克服安培力的功W安为0.4J
(2)金属棒下滑速度v=2m/s时的加速度a是3.2m/s2.点评:
本题考点: 导体切割磁感线时的感应电动势;牛顿第二定律.
考点点评: 本题关键要分析功能关系,并对金属棒正确受力分析,应用安培力公式、牛顿第二定律等,即可正确解题.1年前查看全部
- (2014•和平区一模)估测你站立时对地面的压强;根据你的体重可以得到你对地面的压力,在测量你站立时鞋底和地面的接触面积
 (2014•和平区一模)估测你站立时对地面的压强;根据你的体重可以得到你对地面的压力,在测量你站立时鞋底和地面的接触面积,为简单起见,假设双脚站立时,整个鞋印范围都与地面接触(如图).测量时,在方格纸上画出鞋底的轮廓,看鞋底占有多少小格(不满一个时,大于半格的算一格,小于半格的不算).再乘以每个小格的面积,若某同学的质量为50kg,图中每个小格的边长是1cm,他鞋底的总面积是______,他站立时对地面的压强是______.
(2014•和平区一模)估测你站立时对地面的压强;根据你的体重可以得到你对地面的压力,在测量你站立时鞋底和地面的接触面积,为简单起见,假设双脚站立时,整个鞋印范围都与地面接触(如图).测量时,在方格纸上画出鞋底的轮廓,看鞋底占有多少小格(不满一个时,大于半格的算一格,小于半格的不算).再乘以每个小格的面积,若某同学的质量为50kg,图中每个小格的边长是1cm,他鞋底的总面积是______,他站立时对地面的压强是______.  推荐记忆1年前1
推荐记忆1年前1 -
 瑞雪ff 共回答了23个问题
瑞雪ff 共回答了23个问题 |采纳率87%解题思路:(1)数出鞋底占有的方格数(大于或等于半格的算一格),求出鞋底与地面的接触面积;
(2)水平面上物体的压力和重力相等,根据G=mg求出该同学站立时对地面的压力,根据p=[F/S]求出对地面的压强.(1)鞋底占有的方格数为51格,一小格的面积为1cm×1cm=1cm2,人站立时与地面的接触面积:S=2×51×1cm2=102cm2=1.02×10-2m2,(2)该同学站立时对地面的压力:F=G=mg=50kg×9.8N/kg=490N,对地面的压强:p=FS=490N...
点评:
本题考点: 压强的大小及其计算.
考点点评: 本题考查了压力、压强的计算,关键是根据图象读出该同学对面压力的受力面积和受力面积为双脚桌底面积,计算过程中要注意单位的统一.1年前查看全部
- (2012•和平区三模)物质的性质决定物质的用途.下列物质的用途主要由其化学性质决定的是( )
(2012•和平区三模)物质的性质决定物质的用途.下列物质的用途主要由其化学性质决定的是( )
A.用干冰做致冷剂保存食品
B.压缩空气给轮胎充气
C.用石墨做铅笔芯
D.二氧化碳用作气体肥料 yangfuqiu1年前1
yangfuqiu1年前1 -
 尚平凡 共回答了17个问题
尚平凡 共回答了17个问题 |采纳率88.2%解题思路:物质的物理性质是指不需要通过化学变化表现出来的性质.例如,颜色、状态、气味、密度、硬度、熔点、沸点等.物质的化学性质是指通过化学变化表现出来的性质.例如,稳定性、氧化性、还原性、毒性、可燃性等.A、干冰做致冷剂是利用干冰升华吸热,使周围环境温度降低,是物理性质;
B、压缩空气给轮胎充气利用气体微粒间的间隔大,增大压强间隔变小,利用气体易被压缩的性质,是物理性质;
C、用石墨做铅笔芯是利用石墨质软,在纸上划能留下痕迹,利用的是硬度,是物理性质;
D、二氧化碳用作气体肥料是利用二氧化碳是光合作用的原料,能与水在光和叶绿体的作用下转化成淀粉和氧气,是化学性质.
故选D.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 掌握物理性质和化学性质的定义,理解物理性质和化学性质的本质区别----是否通过化学变化表现出来,了解二者包括的内容是解决这类问题的关键.1年前查看全部
- (2012•和平区一模)根据下列五种微粒的结构示意图,回答下列问题:
(2012•和平区一模)根据下列五种微粒的结构示意图,回答下列问题:

(1)图中微粒共能表示______ 种元素,这几种元素共同组成化合物的化学式______.
(2)图中表示的阴离子是(用离子符号表示)______. daniel81821年前1
daniel81821年前1 -
 wangxinyanqq 共回答了20个问题
wangxinyanqq 共回答了20个问题 |采纳率100%解题思路:(1)根据五种微粒的结构示意图的质子数判读元素的种类,根据元素组成物质,写出化学式;
(2)根据微粒的结构示意图中核内质子数与核外电子数之间的关系分析,当核内质子数小于核外电子数时,为阴离子.(1)由五种微粒的结构示意图可知,微粒共由三种质子数,能表示3种元素,分别是氢、氧、钠三种元素,这三种元素可组成氢氧化钠这种物质,化学式是:NaOH;(2)由五种微粒的结构示意图可知,在C微粒中,核内质子数=8...
点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 了解原子结构示意图与离子结构示意图的区别和联系;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称.1年前查看全部
- (2005•和平区一模)如图(甲)所示,正方形导体框的边长为l,总电阻为R,导体框置于如图(乙)变化的匀强磁场中,求导体
(2005•和平区一模)如图(甲)所示,正方形导体框的边长为l,总电阻为R,导体框置于如图(乙)变化的匀强磁场中,求导体框中生热的热功率.

 malon1年前1
malon1年前1 -
 真的是想不通 共回答了24个问题
真的是想不通 共回答了24个问题 |采纳率95.8%解题思路:根据法拉第电磁感应定律求出感应电动势的大小,结合热功率的公式求出导线框中生热的热功率.由图乙可知,穿过导体框的磁通量是均匀增大的,磁通量的变化率为
[△Φ/△t=
△B
△tS=
0.5
5l2=
l2
10(Wb/s) ①
由法拉第电磁感应定律E=n
△Φ
△t=
l2
10]V②
导体框中生热的热功率为P=
E2
R=
l4
100RW ③
答:导体框中生热的热功率为
l4
100R.点评:
本题考点: 法拉第电磁感应定律;闭合电路的欧姆定律;电功、电功率.
考点点评: 解决本题的关键掌握法拉第电磁感应定律,以及掌握热功率的公式.1年前查看全部
- (语文s版)五年级下册第三单元和平区卷纸答案
 菊花奖1年前1
菊花奖1年前1 -
 忘情E夜 共回答了19个问题
忘情E夜 共回答了19个问题 |采纳率84.2%里面有:看音写词,选音,选择(病句),改写句子.阅读:说明文,课外阅读.1年前查看全部
- 谁知道六年级下册和平区卷纸语文的整张卷纸所有题
 stony84611年前1
stony84611年前1 -
 俄从草原来 共回答了15个问题
俄从草原来 共回答了15个问题 |采纳率93.3%1、算出总面积
总面积=4*2/2+5*2/2+6*2/2+5*2=25(平方米)
2、算出每块砖的面积
每块砖的面积=0.5*0.5=0.25(平方米)
3、算出需要多少块砖
25/0.25=100块
4、得出答案
100*25=2500元
一共需要2500元1年前查看全部
- (2012•和平区三模)下列说法中正确的是( )
(2012•和平区三模)下列说法中正确的是( )
A.同种溶质的饱和溶液一定比它的不饱和的浓度大
B.饱和溶液降低温度析出晶体后就变为不饱和溶液
C.某饱和溶液温度升高时,若溶液的质量不变,则溶质的质量分数不变
D.固体溶质的饱和溶液温度降低时必定有晶体析出 地狱哈哈天使1年前1
地狱哈哈天使1年前1 -
 流星1314 共回答了23个问题
流星1314 共回答了23个问题 |采纳率82.6%解;A、因为如果不是在同一温度下,会出现不饱和溶液比不饱和溶液还浓的现象,故A错误;
B、根据饱和溶液的含义,既然饱和溶液降低温度有晶体析出,说明还有不溶解的,故仍为饱和溶液,故B错误;
C、把饱和溶液温度升高时,若溶液质量不变,说明溶质和溶剂的质量都没变,则溶液质量分数也不变,故C正确;
D、根据固体物质受温度的影响可知,有些物质的溶解度随温度降低而增大,例如氢氧化钙,所以固体溶质的饱和溶液温度降低时不一定有晶体析出,故D错误.
故选:C.1年前查看全部
- (2008•和平区三模)已知数列{an}的通项公式an=log2n+1n+2(n∈N*),设前n项和为Sn,则使Sn<-
(2008•和平区三模)已知数列{an}的通项公式an=log2
(n∈N*),设前n项和为Sn,则使Sn<-5成立的自然数n的最小值是______.n+1 n+2  我就是mm1年前1
我就是mm1年前1 -
 frgrthnf 共回答了24个问题
frgrthnf 共回答了24个问题 |采纳率87.5%解题思路:根据题中已知数列{an}的通项公式求出其前n项和的Sn的表达式,然后令Sn<-5即可求出n的取值范围,即可知n有最小值.由题意可知;an=log2 [n+1/n+2](n∈N*),
设{an}的前n项和为Sn=log2 [2/3]+log2 [3/4]+…+log2 [n/n+1]+log2 [n+1/n+2],
=[log22-log23]+[log23-log24]+…+[log2n-log2(n+1)]+[log2(n+1)-log2(n+2)]
=[log22-log2(n+2)]=log2 [2/n+2]<-5,
即 [2/n+2]<2-5
解得n>62,
∴使Sn<-5成立的自然数n有最小值为63,
故答案为:63.点评:
本题考点: 数列的求和.
考点点评: 本题主要考查了数列与函数的综合应用,考查了学生的计算能力和对数列的综合掌握,解题时注意整体思想和转化思想的运用,属于中档题.1年前查看全部
- (2010•和平区二模)如图,PA、PB、EF分别切⊙O于A、B、D,若PA=10cm,则△PEF的周长是______
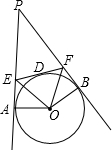 (2010•和平区二模)如图,PA、PB、EF分别切⊙O于A、B、D,若PA=10cm,则△PEF的周长是______ cm,若∠P=35°,则∠AOB=______(度),∠EOF=______(度).
(2010•和平区二模)如图,PA、PB、EF分别切⊙O于A、B、D,若PA=10cm,则△PEF的周长是______ cm,若∠P=35°,则∠AOB=______(度),∠EOF=______(度).  骑在墙头红杏1年前1
骑在墙头红杏1年前1 -
 他的小vv儿 共回答了20个问题
他的小vv儿 共回答了20个问题 |采纳率80%解题思路:由PA、PB、EF分别切⊙O于A、B、D,根据切线长定理可得PA=PB=10cm,ED=EA,FD=DB,则PE+EF+PF=PE+ED+PF+FD=PA+PB,即可得到△PEF的周长;根据切线的性质得到∠PAO=∠PBO=90°,根据四边形的内角和为360度即可计算出∠AOB;连OD,根据切线的性质得到∠ODE=∠ODF=90°,易证得Rt△OAE≌Rt△ODE,Rt△OFD≌Rt△OFB,得∠1=∠2,∠3=∠4,即有∠EOF=∠2+∠3=[1/2]∠AOB.∵PA、PB、EF分别切⊙O于A、B、D,
∴PA=PB=10cm,ED=EA,FD=DB,
∴PE+EF+PF=PE+ED+PF+FD
=PA+PB
=20(cm);
∵PA、PB为⊙O的切线,
∴∠PAO=∠PBO=90°,
而∠P=35°,
∴∠AOB=360°-90°-90°-35°=145°;
连OD,如图,
∴∠ODE=∠ODF=90°,
易证得Rt△OAE≌Rt△ODE,Rt△OFD≌Rt△OFB,
∴∠1=∠2,∠3=∠4,
∴∠2+∠3=[1/2]∠AOB=72.5°,
∠EOF=72.5°.
故答案为20;145;72.5.点评:
本题考点: 切线长定理.
考点点评: 本题考查了切线长定理:从圆外一点引圆的两条切线,切线长相等;也考查了切线的性质:圆的切线垂直于过切点的半径.1年前查看全部
- (2013•和平区一模)如图所示,灯泡L标有“12V 6W”的字样,R1是定值电阻,R2上标有“2
 (2013•和平区一模)如图所示,灯泡L标有“12V6W”的字样,R1是定值电阻,R2上标有“24Ω 1A”,电源电压为12V.则下列说法正确的是(灯泡L的电阻不变)( )
(2013•和平区一模)如图所示,灯泡L标有“12V6W”的字样,R1是定值电阻,R2上标有“24Ω 1A”,电源电压为12V.则下列说法正确的是(灯泡L的电阻不变)( )
A.灯泡L的阻值为24Ω
B.当灯泡L正常发光时电流表的示数为0.9 A
C.变阻器滑片在b端时,同时闭合开关S、S1,则灯泡L正常发光
D.当开关S闭合、S1断开时,灯泡L消耗的最小功率是1.5 W 优游双鱼1年前1
优游双鱼1年前1 -
 kawai_zhuzhu 共回答了21个问题
kawai_zhuzhu 共回答了21个问题 |采纳率85.7%解题思路:(1)由灯泡的铭牌可知额定电压和额定功率,根据I=[P/U]求出灯泡的额定电流,根据欧姆定律求出灯泡的电阻;
(2)当开关S闭合、S1断开,变阻器滑片在b端时,电路为灯泡的简单电路,此时灯泡两端的电压和额定电压相等、正常发光,电流表的示数和灯泡的额定电流相等;
当滑片位于a端时,灯泡与滑动变阻器的最大阻值串联,电路中的电阻最大、电路中的电流最小、根据P=I2R可知灯泡的实际功率最小,根据电阻的串联和欧姆定律求出电路中的电流,根据电功率公式求出小灯泡消耗的最小功率;
(3)同时闭合开关S、S1,变阻器滑片在b端时,灯泡与电阻R1并联在电源的两端,根据额定电压下灯泡正常发光可知灯泡正常发光.(1)灯泡的额定电流I额=
P额
U额=[6W/12V]=0.5A,所以B错误;
电阻RL=
U额
I额=[12V/0.5A]=24Ω,故A正确;
(2)同时闭合开关S、S1,变阻器滑片在b端时,灯泡与电阻R1并联在电源的两端;
此时灯泡两端的电压和额定电压相等,所以此时灯泡正常发光,故C正确;
(3)当开关S闭合、S1断开时,滑片位于a端时,灯泡与滑动变阻器的最大阻值串联,此时灯泡消耗的电功率最小,
电路中的电流I=[U
RL+R2=
12V/24Ω+24Ω]=0.25A,
小灯泡消耗的最小功率PL=I2RL=(0.25A)2×24Ω=1.5W,故D正确.
故选ACD.点评:
本题考点: 欧姆定律的应用;电功率的计算.
考点点评: 本题考查了串联电路的特点和并联电路的特点以及欧姆定律、电功率公式的应用,关键是开关闭合、断开时和滑片位于不同位置时电路连接方式的辨别.1年前查看全部
- (2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,
(2012•和平区一模)一块三角形废料如图所示,∠A=30°,∠C=90°,AB=12.用这块废料剪出一个矩形CDEF,其中,点D、E、F分别在AC、AB、BC上.要使剪出的矩形CDEF面积最大,点E应选在何处?

 蚺後弦1年前1
蚺後弦1年前1 -
 zorro521 共回答了20个问题
zorro521 共回答了20个问题 |采纳率80%解题思路:首先在Rt△ABC中利用∠A=30°、AB=12,求得BC=6、AC的长,然后根据四边形CDEF是矩形得到EF∥AC从而得到△BEF∽△BAC,设AE=x,则BE=12-x.利用相似三角形成比例表示出EF、DE,然后表示出有关x的二次函数,然后求二次函数的最值即可.在Rt△ABC中,∠A=30°,AB=12,
∴BC=6,AC=AB•cos30°=12×
3
2=6
3.
∵四边形CDEF是矩形,
∴EF∥AC.
∴△BEF∽△BAC.
∴[EF/AC=
BE
BA].
设AE=x,则BE=12-x.
EF=
6
3(12−x)
12=
3
2(12−x).
在Rt△ADE中,DE=
1
2AE=
1
2x.
矩形CDEF的面积S=DE•EF=
1
2x•
3
2(12−x)=−
3
4x2+3点评:
本题考点: 相似三角形的应用;二次函数的最值.
考点点评: 本题考查了相似三角形的应用及二次函数的应用,解题的关键是从几何问题中整理出二次函数模型,并利用二次函数的知识求最值.1年前查看全部
- (2014•和平区模拟)若复数[a/1−i]+[1−i/2](i为虚数单位)的实部与虚部互为相反数,则实数a的值为(
(2014•和平区模拟)若复数[a/1−i]+[1−i/2](i为虚数单位)的实部与虚部互为相反数,则实数a的值为( )
A.2
B.1
C.-1
D.0 熟悉的身影1年前0
熟悉的身影1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•和平区一模)已知正六边形的半径是4,则这个正六边形的周长为______.
 flybird7891年前1
flybird7891年前1 -
 wl0722 共回答了19个问题
wl0722 共回答了19个问题 |采纳率84.2%解题思路:根据正六边形的半径可求出其边长为4,进而可求出它的周长.正六边形的半径为2cm,则边长是4,因而周长是4×6=24.
故答案为:24.点评:
本题考点: 正多边形和圆.
考点点评: 此题主要考查了正多边形和圆的有关计算,正六边形的半径与边长相等是需要熟记的内容.1年前查看全部
- (2012•和平区二模)已知抛物线y1=a(x-2)2-4(a≠0)经过点(0,-3),顶点为M,将抛物线y1向上平移b
(2012•和平区二模)已知抛物线y1=a(x-2)2-4(a≠0)经过点(0,-3),顶点为M,将抛物线y1向上平移b个单位可使平移后得到的抛物线y2经过坐标原点,抛物线y2的顶点为A,与x轴的另一个交点为B.

(1)求a的值;
(2)①b=______,②抛物线y2的函数表达式是y2=[1/4](x-2)2-1y2=[1/4](x-2)2-1;
(3)①点P是y轴上一点,当|PA-PB|的值最大时,求点P的坐标;
②点E是x轴上一点,在抛物线y2上是否存在点F,使O(原点)、M、E、F四点构成以OM为一边的平行四边形?若存在,请求出点F的坐标;若不存在,请说明理由. nkelove1年前1
nkelove1年前1 -
 fyxlf 共回答了20个问题
fyxlf 共回答了20个问题 |采纳率85%解题思路:(1)将(0,-3)代入y1=a(x-2)2-4(a≠0)中,即可求得a的值.
(2)抛物线y1经过(0,-3),向上平移后经过原点即可(0,0),因此抛物线向上平移了3个单位,根据“上加下减”的平移规律即可得出y2的函数表达式.
(3)①当P、A、B三点不在同一直线上时,能构成△PAB,由三角形三边关系定理不难看出|PA-PB|<AB;若P、A、B三点共线时,|PA-PB|=AB,显然当|PA-PB|的值最大时,P、A、B三点共线,所以直接求出直线AB的解析式,该直线与y轴的交点即为符合条件的P点;
②点O、M已经确定了具体坐标,且OM是平行四边形的边,所以只考虑另一边EF即可,由于点E在x轴上,且OM
EF,所以可分两种情况讨论:∥ .
Ⅰ、点F在x轴下方,此时MF必与OB平行,即MF平行于x轴,此时M、F两点的纵坐标相同,由题意(y2由y1向上平移所得)可知,点F不可能在y2上,这种情况不成立;
Ⅱ、点F在x轴下方,由于平行四边形是中心对称图形,那么此时M、F的纵坐标互为相反数,可据此确定点F的坐标.(1)抛物线y1=a(x-2)2-4(a≠0)经过点(0,-3),可得:
-3=a(0-2)2-4,
解得:a=[1/4].
(2)∵经过(0,-3)的抛物线y1向上平移,经过(0,0)得到抛物线y2,
∴向上平移了3个单位,即b=3;
故抛物线y2:y2=[1/4](x-2)2-4+3=[1/4](x-2)2-1.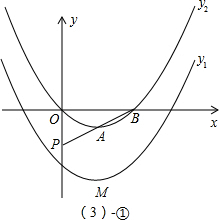 (3)①∵|PA-PB|≤AB,且当且仅当P、A、B共线时取等号,
(3)①∵|PA-PB|≤AB,且当且仅当P、A、B共线时取等号,
∴|PA-PB|的值最大时,P、A、B共线;
由(2)的抛物线解析式知:A(2,-1)、B(4,0),设直线AB的解析式:y=kx+b,有:
2k+b=−1
4k+b=0,
解得
k=
1
2
b=−2
故直线AB:y=[1/2]x-2,则P(0,-2).
②易知M(2,-4),分两种情况讨论:
Ⅰ、点F在x轴下方时,由于OM是平行四边形的边,则MF∥x轴,即F点的纵坐标为-4,显然点F不可能在抛物线y2上,此种情况不成立;
Ⅱ、点F在x轴上方时,由于平行四边形是中心对称图形,所以F点的纵坐标为4;
当y2=4时,[1/4](x-2)2-1=4,解得:x=2±2
5
则F(2-2点评:
本题考点: 二次函数综合题.
考点点评: 此题主要考查了二次函数解析式的确定、函数图象的平移规律、三角形三边关系定理以及平行四边形的判定等重要知识;(3)的难度较大,利用几何知识找出解题的思路是解题的关键,着重体现了数形结合的重要性.1年前查看全部
- (2011•和平区二模)某只含CaCl2和Na2SO4杂质的粗盐样品,加水得到混合物A后,某实验小组的同学设计如下实验步
(2011•和平区二模)某只含CaCl2和Na2SO4杂质的粗盐样品,加水得到混合物A后,某实验小组的同学设计如下实验步骤,请按要求回答有关问题.

(1)在混合物A中先加入过量BaCl2溶液除去的物质是______;成分搅拌后,再加过量Na2CO3溶液可除去的物质是______(2)在溶液C中加入的足量试剂X是______;发生反应的化学方程式是______(3)操作①和②的分离方法分别是______、______(4)写出③的化学方程式2NaCl
2Na+Cl2↑通电 .2NaCl.
2Na+Cl2↑通电 . liangys08291年前1
liangys08291年前1 -
 红尘做客 共回答了17个问题
红尘做客 共回答了17个问题 |采纳率88.2%解题思路:(1)根据氯化钡能与硫酸钠反应,碳酸钠能与氯化钙、氯化钡反应分析
(2)根据碳酸钠能与盐酸反应分析
(3)根据分离混合物的方法分析
(4)根据书写方程式原则书写(1)氯化钡能与硫酸钠反应生成硫酸钡沉淀和氯化钠,因此加入氯化钡溶液是除去硫酸钠的;碳酸钠能与氯化钙反应产生碳酸钙沉淀,能与氯化钡反应产生碳酸钡沉淀,因此加入碳酸钠溶液的目的是除去原混合物中的氯化钙以及过量的氯化钡;
(2)溶液C中含有过量的碳酸钠和氯化钠,加入试剂x将碳酸钠转化成氯化钠,因此加入的x是盐酸,反应的化学方程式为2HCl+Na2CO2=2NaCl+CO2↑+H2O;
(3)操作①是将固体与液体分离,用过滤法,操作②是将氯化钠溶液中氯化钠结晶析出,应用蒸发溶剂的方法.
(4)氯化钠在通电条件下生成钠和氯气,化学方程式为:2NaCl
通电
.
2Na+Cl2↑
故答案为:(1)Na2SO4; CaCl2、BaCl2(2)盐酸; 2HCl+Na2CO2=2NaCl+CO2↑+H2O(3)过滤、蒸发(4)2NaCl
通电
.
2Na+Cl2↑点评:
本题考点: 氯化钠与粗盐提纯;盐的化学性质.
考点点评: 本题主要考了在粗盐提纯的试验中对杂质进行转换的探究,除去杂质的同时不能引入新的杂质.1年前查看全部
- 高分求公司地址英文(15分)地 址:太原市和平区平山路118号甲-8开户行:交行云口第二支行以及税号的英文,要书面的.急
高分求公司地址英文(15分)
地 址:太原市和平区平山路118号甲-8
开户行:交行云口第二支行
以及税号的英文,要书面的.
急等,求真. wj40569433381年前1
wj40569433381年前1 -
 都市亦丛林9 共回答了15个问题
都市亦丛林9 共回答了15个问题 |采纳率100%Add:Jia-eight,No.118 Pingshan Lu,Heping District,Taiyuan City,Shanxi Province...
Bank account:The second branch of Yunkou,BANK OF COMMUNICATION
另:你的地址还差邮政编码1年前查看全部
- (2009•和平区二模)如图是生活中常用的剪指甲工具,小京在剪指甲时机械效率为90%.若指甲平均厚度为0.2mm,剪断一
 (2009•和平区二模)如图是生活中常用的剪指甲工具,小京在剪指甲时机械效率为90%.若指甲平均厚度为0.2mm,剪断一次指甲时,刀口与指甲间的平均作用力为4.5N.则( )
(2009•和平区二模)如图是生活中常用的剪指甲工具,小京在剪指甲时机械效率为90%.若指甲平均厚度为0.2mm,剪断一次指甲时,刀口与指甲间的平均作用力为4.5N.则( )
A.剪断一次指甲的过程需要做的额外功是1J
B.剪断一次指甲的过程需要做的有用功是1J
C.剪断一次指甲的过程需要做的有用功是1×10-2J
D.剪断一次指甲的过程需要做的总功是1×10-3J shllzb1年前1
shllzb1年前1 -
 anna_ping 共回答了24个问题
anna_ping 共回答了24个问题 |采纳率79.2%解题思路:(1)由题干中数据知道指甲的厚度,即剪断一次指甲刀口与指甲间作用力移动的距离,利用W=Fs求剪断一次指甲做的有用功;
(2)知道指甲刀的效率,利用效率公式求剪断一次指甲做的总功;
(3)利用W总=W有用+W额求出剪断一次指甲做多少额外功.(1)剪断一次指甲对指甲做的有用功:
W有用=Fs=4.5N×0.2×10-3m=9×10-4J,故B、C错误;
(2)∵指甲刀的效率:
η=
W有
W总
∴剪断一次指甲做的总功:
W总=
W有
η=
9×10−4J
90%=1×10-3J,故D正确;
(3)剪断一次指甲做多少额外功:
W额=W总-W有用=1×10-3J-9×10-4J=1×10-4J,故A错误.
故选D点评:
本题考点: 有用功和额外功;功的计算.
考点点评: 本题综合考查了功的计算、机械效率的计算,涉及到用所学知识计算身边的指甲刀的有关物理量,与实际生活联系,有意义!1年前查看全部
- (2013•和平区一模)某初中校共有学生1200名,各年级男、女生人数如下表:
(2013•和平区一模)某初中校共有学生1200名,各年级男、女生人数如下表:
已知在全校学生中随机抽取l名,抽到七年级女生的概率是0.17.七年级 八年级 九年级 女生 a 216 b 男生 198 222 c
(Ⅰ)求a的值;
(Ⅱ)现用分层抽样的方法在全校抽取200名学生,问应在九年级抽取多少名学生?
(Ⅲ)已知175≤b≤183,求九年级中女生不少于男生的概率. figo_sq1年前1
figo_sq1年前1 -
 jy00573066 共回答了23个问题
jy00573066 共回答了23个问题 |采纳率100%解题思路:(Ⅰ)直接用总体容量乘以概率得到七年级女学生数;
(Ⅱ)利用图表中的数值求出九年级的学生数,乘以样本容量和总体容量的比值得到九年级抽取的学生数;
(Ⅲ)由九年级中女学生数的取值范围,结合九年级学生总人数得到男学生数的取值情况,列出九年级中女生人数及男生人数的所有可能结果,查出女生不少于男生的可能结果,然后利用古典概型概率公式求概率.解(Ⅰ)由题意,得a=1200×0.17=204;
(Ⅱ)由(Ⅰ)及已知条件,得
七年级共有学生:204+198=402(名).
八年级共有学生:216+222=438(名).
所以九年级共有学生:1200-402-438=360(名).
所以应在九年级抽取学生数:360×[200/1200]=60(名).
(Ⅲ)由(Ⅱ)可知九年级共有学生360名.
则九年级中女生人数及男生人数的所有可能结果为:
(175,185),(176,184),(177,183),(178,182),(179,181),(180,180),(181,179),
(182,178),(183,177)共9中.
其中女生不少于男生的可能结果为:(180,180),(181,179),(182,178),(183,177)共4种.
所以九年级中女生不少于男生的概率为:P=[4/9].点评:
本题考点: 列举法计算基本事件数及事件发生的概率;分层抽样方法.
考点点评: 本题考查了分层抽样方法,考查了利用列举法计算基本事件及事件发生的概率,解答的关键在于列举时做到不重不漏,是基础题.1年前查看全部
- (2012•和平区模拟)如图所示,电流表示数为I,电压表示数为U,R1、R2为已知阻值的电阻,则( )
 (2012•和平区模拟)如图所示,电流表示数为I,电压表示数为U,R1、R2为已知阻值的电阻,则( )
(2012•和平区模拟)如图所示,电流表示数为I,电压表示数为U,R1、R2为已知阻值的电阻,则( )
A.[U/I]=R1+R2
B.[I/U]=[1R1 1 R2  我本鸿鹄1年前1
我本鸿鹄1年前1 -
 lonelygo 共回答了14个问题
lonelygo 共回答了14个问题 |采纳率92.9%解题思路:由电路图可知,两电阻串联,电压表测电源的电压,电流表测电路中的电流;
(1)串联电路的总电阻等于各分电阻之和,根据欧姆定律可知电路中的总电阻等于总电压和总电流的比值;
(2)串联电路中各用电器消耗的总功率等于各用电器消耗的电功率之和,还等于总电压和总电流的乘积;
(3)纯电阻电路中,用电器消耗的电功率可以用P=I2R和P=
求得.U2 R 由电路图可知,两电阻串联,电压表测电源的电压,电流表测电路中的电流;
(1)∵串联电路的总电阻等于各分电阻之和,
∴根据欧姆定律可得:
U/I]=R1+R2,[I/U]=[1
R1+R2,故A正确,B不正确;
(2)∵串联电路中各用电器消耗的总功率等于各用电器消耗的电功率之和,
∴根据P=UI和P=I2R可得:P=UI=I2R1+I2R2,故C正确;
根据P=UI和P=
U2/R]可得:P=
U2
R1+R2=I2R1+I2R2,故D正确.
故选ACD.点评:
本题考点: 欧姆定律的应用;电阻的串联;电功率的计算.
考点点评: 本题考查了电阻的串联特点和欧姆定律的、电功率公式的应用,灵活的运用好电功率公式和知道公式使用的范围是关键.1年前查看全部
- (2010•和平区一模)通过一年对化学的学习,你已经掌握了实验室制取气体的有关规律.请结合图回答问题:
(2010•和平区一模)通过一年对化学的学习,你已经掌握了实验室制取气体的有关规律.请结合图回答问题:

(1)写出图中标号仪器的名称①______,②______.
(2)用加热高锰酸钾的方法制取氧气,应选用发生装置和收集装置是______.
(3)欲制取并收集二氧化碳,所选用的装置是______.
(4)实验室常用锌粒和稀硫酸反应制取氢气.若用C装置制取氢气(C装置气密性良好),在有孔塑料板上放置的药品是锌粒.反应进行过程中,关闭该装置中的弹簧夹后,可以观察到的现象是______. lcs53331年前1
lcs53331年前1 -
 牙齿流了很多血 共回答了19个问题
牙齿流了很多血 共回答了19个问题 |采纳率100%解题思路:根据图示即可知道仪器的名称,气体制取装置的选择取决于反应物的状态和反应的条件,收集装置的选择取决于气体的水溶性和密度,使用C装置制取氢气,夹住弹簧夹则固体和液体会自相分离,达到反应停止的目的.(1)据图可知,①是酒精灯,②是分液漏斗,故填:酒精灯,分液漏斗;
(2)使用高锰酸钾制取氧气,高锰酸钾是固体,反应需要加热,使用固体加热型发生装置,故使用A装置制取氧气,由于氧气的密度比空气大,使用向上排空气法收集氧气,由于氧气不易溶于水,可以使用排水法收集氧气,故填:ADF;
(3)实验室使用石灰石与稀盐酸制取二氧化碳,石灰石是固体,稀盐酸是液体,常温下反应就能进行,使用液固常温型气体发生装置,故可以使用BC,由于二氧化碳的密度比空气大,故使用向上排空气法收集,故填:BCD;
(4)使用C装置制取氢气,夹住弹簧夹则固体和液体会自相分离,达到反应停止的目的,会观察到试管中的酸液液面下降,长颈漏斗中的酸液上升,锌与稀硫酸分离,反应停止,故填:试管中的酸液液面下降,长颈漏斗中的酸液上升,锌与稀硫酸分离,反应停止点评:
本题考点: 常用气体的发生装置和收集装置与选取方法.
考点点评: 本题考查了气体发生装置和收集装置的选择,完成此题,可以依据反应物的状态和反应的条件以及气体的密度和水溶性进行.1年前查看全部
- (2010•和平区一模)若正项数列{an}满足a1=2,a2n+1-3an+1an-4a2n=0,则数列{an}的通项a
(2010•和平区一模)若正项数列{an}满足a1=2,
-3an+1an-4a 2n+1
=0,则数列{an}的通项an=______.a 2n llyzhy1年前1
llyzhy1年前1 -
 不谢的情致 共回答了18个问题
不谢的情致 共回答了18个问题 |采纳率88.9%解题思路:由
-3an+1an-4a 2n+1
=0,分解因式得出(an+1−4an)(an+1+ an)=0,得出an+1−4an=0,所以{an}是以4为公比的等比数列,通项公式易求.a 2n由
a2n+1-3an+1an-4
a2n=0,分解因式得出(an+1−4an)(an+1+ an)=0,由于{an}为正项数列,所以只能是an+1−4an=0,所以{an}是以4为公比的等比数列,首项a1=2,通项公式为an=2•4n-1=22n-1
故答案为:22n-1点评:
本题考点: 数列递推式.
考点点评: 本题考查数列的递推公式和等比数列的判断,等比数列通项公式.考查转化、计算能力,本题得出an+1−4an=0是关键.1年前查看全部
- (2014•和平区模拟)复数i32i−1(i为虚数单位)的虚部是( )
(2014•和平区模拟)复数
(i为虚数单位)的虚部是( )i3 2i−1
A.[1/5i cbr954rr1年前1
cbr954rr1年前1 -
 Henry307 共回答了23个问题
Henry307 共回答了23个问题 |采纳率95.7%解题思路:利用两个复数相除,分子和分母同时乘以分母的共轭复数,求出复数z,即可得复数z的虚部.i3
2i−1=
−i(−2i−1)
(2i−1)(−2i−1)=[2+i/5]=[2/5+
1
5i
故复数
i3
2i−1](i为虚数单位)的虚部是[1/5]
故选B点评:
本题考点: 复数代数形式的乘除运算.
考点点评: 本题主要考查了复数的基本概念,以及复数代数形式的乘除运算,同时考查了计算能力,属于基础题.1年前查看全部
- (2012•和平区模拟)已知矩形纸片OBCD,OB=2,OD=1.如图①②,将该纸片放置在平面直角坐标系中,折叠该纸片,
(2012•和平区模拟)已知矩形纸片OBCD,OB=2,OD=1.如图①②,将该纸片放置在平面直角坐标系中,折叠该纸片,使顶点O与边CD上的点E重合.

(Ⅰ)如图①,折痕FG分别与OD、OB交于点F、G,且OF=
,求点E的坐标;2 3
(Ⅱ)如图②,折痕FG分别与CD、OB交于点F、G,过O、D、E三点的圆恰与直线BC相切于点N,OE与FG交于点P.
①求点E的坐标;
②求折痕FG的长. 建猪文化1年前1
建猪文化1年前1 -
 zhangkuan123 共回答了15个问题
zhangkuan123 共回答了15个问题 |采纳率86.7%(Ⅰ)∵OD=1,OF=
2
3,
∴DF=OD−OF=1−
2
3=
1
3.
∵折叠后点O与点E重合,
∴△EFG≌△OFG.
∴EF=OF=
2
3.
∵四边形OBCD是矩形,
∴∠ODC=90°.
在Rt△DEF中,DE=
EF2−DF2=
(
2
3)2−(
1
3)2=
3
3.
∴点E的坐标为(
3
3,1).
(Ⅱ)①如图所示,连接NP,并延长交OD于点M,
∵折叠后点O与点E重合,且FG是折痕,
∴PO=PE.
∵∠ODC=90°,
∴OE是过O、D、E三点的圆的直径,点P是圆心.
∵BC切⊙P于点N, ∴∠DOB=∠OBC=∠BNM=90°.
∴∠DOB=∠OBC=∠BNM=90°.
∴四边形OBNM是矩形.
∴MN=OB=2,且MN∥OB.
∵DC∥OB,∴DC∥MN.
∴△OMP∽△ODE.
∴
MP
DE=
OP
OE=
1
2.
∴MP=
1
2DE.
设DE=x,则MP=
1
2x,PN=2−
1
2x.
在⊙P中,PE=PN=2−
1
2x,
∴OE=2PE=4-x.
在Rt△ODE中,由OD2+DE2=OE2,
得12+x2=(4-x)2.
解得x=
15
8.
即DE=
15
8.
∴点E的坐标(
15
8,1).
②PE=2−
1
2x=
17
16.
∵折叠后点O与点E重合,且FG是折痕,
∴OE⊥FG.
∴∠EPF=∠EDO=90°.
∵∠FEP=∠OED,
∴△EFP∽△EOD.
∴
FP
OD=
PE
DE.
∴FP=
PE•OD
DE=
17
16×1
15
8=
17
30.
∵DC∥OB,
∴∠FEP=∠GOP,∠EFP=∠OGP.
∠FEP=∠GOP
∠EFP=∠OGP
PE=OP,
∴△FEP≌△GOP(AAS).
∴FP=GP.
∴FG=2FP=
17
15.
∴折痕FG的长是
17
15.1年前查看全部
- (2006•和平区二模)一艘潜水艇的体积为6000m3,其内部水箱的容积是2000m3,当它在水下匀速航行时,水箱正好灌
(2006•和平区二模)一艘潜水艇的体积为6000m3,其内部水箱的容积是2000m3,当它在水下匀速航行时,水箱正好灌满水,此时潜水艇受到的浮力是多少?当潜水艇排完水箱中水时,潜水艇匀速航行时受到的浮力是多少?(海水密度为1.03×103kg/m3,g=10N/Kg)
 东在南方1年前1
东在南方1年前1 -
 赌坊962号 共回答了19个问题
赌坊962号 共回答了19个问题 |采纳率94.7%解题思路:已知潜水艇的体积,根据浮力公式可求潜水艇受到的浮力,此时潜水艇悬浮,受到的浮力等于现在自身的重力,等于潜水艇的重力与一箱水的重力之和;
当潜水艇排完水箱中水时,潜水艇航行时受到的浮力等于潜水艇的重力.水箱正好灌满水,此时潜水艇受到的浮力F浮=ρgV排=1.03×103kg/m3×10N/kg×6000m3=6.18×107N,
一箱水的重力G水=m水g=ρV箱g=1.03×103kg/m3×2000m3×10N/kg=2.06×107N,
所以潜水艇的自重为G潜=F浮-G水=6.18×107N-2.06×107N=4.12×107N,
当潜水艇排完水箱中水时,潜水艇航行时受到的浮力F浮1=G潜=4.12×107N.
故答案为:当它在水下匀速航行时,水箱正好灌满水,此时潜水艇受到的浮力是6.18×107N,
当潜水艇排完水箱中水时,潜水艇匀速航行时受到的浮力是4.12×107N.点评:
本题考点: 浮力大小的计算;阿基米德原理.
考点点评: 本题考查浮力、重力等的计算,关键是公式及其变形的灵活运用,难点是知道物体漂浮或悬浮时浮力等于自身的重力.1年前查看全部
- (2012•和平区一模)如图,木块竖立在小车上,随小车一起以相同的速度向右做匀速直线运动,下列分析正确的( )
(2012•和平区一模)如图,木块竖立在小车上,随小车一起以相同的速度向右做匀速直线运动,下列分析正确的( )

A.木块没有受到小车的摩擦力
B.木块的运动速度越快,惯性越大
C.木块对小车的压力与小车对木块的支持力是一对作用力和反作用力
D.当小车受到阻力突然停止运动时,如果木块与小车接触面光滑,木块将向右倾倒 上海居不易1年前1
上海居不易1年前1 -
 彩色oo糖 共回答了24个问题
彩色oo糖 共回答了24个问题 |采纳率91.7%解题思路:(1)摩擦力的产生条件,两物体相互接触,并且物体之间要发生或已经发生相对了运动.
(2)惯性的大小只与物体的质量有关,速度大小、受力大小,都不影响惯性.
(3)相互作用力,必须同时满足四个条件:大小相等、方向相反、作用在同一直线上、作用在不同的物体上.
(4)牛顿第一定律:物体不受外力时,总保持静止状态或匀速直线运动.A、由于木块静止在小车上,不具备摩擦力产生的条件,所以它没有受到摩擦力的作用.故A符合题意.
B、物体的运动速度不影响惯性,惯性是物体保持原来动状态不变的性质.故B不符合题意.
C、木块对小车的压力与小车对木块的支持力分别作用在小车和木块上,属于相互作用力,是一对作用力和反作用力.故C符合题意.
D、小车突然停止运动,而木块由于惯性仍然保持原来的运动状态.如果木块与小车接触面光滑,木块不会倾倒,由于木块具有惯性,会向前运动.故D不符合题意.
故选AC.点评:
本题考点: 摩擦力产生的条件;力作用的相互性;牛顿第一定律;惯性.
考点点评: 此类题考查了摩擦力产生的条件、惯性的影响因素、作用力和反作用力、牛顿第一定律等多方面的知识,是一道综合性较强的题目.1年前查看全部
- (2009•和平区)小羽的储蓄罐里共有125个硬币,其中一元硬币的个数占44%,五角硬币的个数占20%,一角硬币的个数占
(2009•和平区)小羽的储蓄罐里共有125个硬币,其中一元硬币的个数占44%,五角硬币的个数占20%,一角硬币的个数占36%.那么储蓄罐里共有( )元.
A.109.5
B.84.5
C.72
D.125 sjjc19811年前1
sjjc19811年前1 -
 沈金燕 共回答了23个问题
沈金燕 共回答了23个问题 |采纳率87%解题思路:把硬币的总数量看成单位“1”,分别求出各种硬币有多少个,再根据各种硬币的面值求出总钱数即可.125×44%=55(个);
125×20%=25(个);
125×36%=45(个);
5角=0.5元,
1角=0.1元;
55×1+25×0.5+45×0.1,
=55+12.5+4.5,
=72(元).
答:储蓄罐里共有72元.
故选:C.点评:
本题考点: 百分数的实际应用.
考点点评: 本题关键是找出单位“1”,求单位“1”的百分之几是多少,用乘法;求出硬币的数量后再根据面值求出总钱数.1年前查看全部
- (2006•和平区二模)根据“伏安法测电阻”的实验完成下列要求:
(2006•和平区二模)根据“伏安法测电阻”的实验完成下列要求:
(1)用伏安法测电阻所依据的原理是:R=[U/I]或欧姆定律R=[U/I]或欧姆定律.
(2)用伏安法测电阻需测定的数据:______;
(3)设计并画出用伏安法测电阻的电路图,在图中连好实物图,要求滑动变阻器的滑片P向左移动时,电流表的示数变小;
(4)若电压表和电流表的示数分别如图2所示,则被测电阻的阻值为______.
 大虫他哥1年前1
大虫他哥1年前1 -
 2008mimi2008 共回答了17个问题
2008mimi2008 共回答了17个问题 |采纳率94.1%解题思路:(1)伏安法测电阻的实验原理:R=[U/I]或欧姆定律;
(2)需要测量的物理量有:电压和电流;
(3)画出测电阻的电路图,电流表、滑动变阻器与电阻串联,电压表与电阻并联;
按电路图连接实物电路,注意连接的顺序和方式要一致;
(4)根据电压表、电流表的量程和分度值得出示数,根据R=[U/I]计算出电阻值.(1)伏安法测电阻的实验原理:R=[U/I]或欧姆定律;
(2)在实验中,需用电压表测出待测电阻两端的电压,用电流表测出待测电阻的电流;
(3)电路图如图: ;
;
按电路图连接电路,滑片向左滑动,电流变小,则电阻应变大,下面应接右边的B接线柱,如图所示: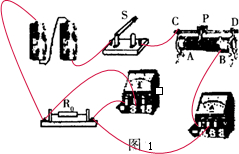 ;
;
由图2知,电压表的量程为0~15V,分度值为0.5V,示数为4V;
电流表的量程为0~0.6A,分度值为0.02A,示数为0.2A;
则R=[U/I]=[4V/0.2A]=20Ω.
故答案为:(1)R=[U/I]或欧姆定律;(2)待测电阻两端的电压、通过待测电阻的电流;(3)见上图;(4)20Ω.点评:
本题考点: 伏安法测电阻的探究实验.
考点点评: 此题是“伏安法测电阻”的实验,考查了实验原理、电路图的画法及实物电路的连接,同时考查了电流表、电压表的读数及电阻的计算.1年前查看全部
- (2010•和平区一模)某小组同学研究动滑轮的使用特点,他们先用弹簧测力计缓慢提起钩码,如图(a)所示,再分别用重力不同
(2010•和平区一模)某小组同学研究动滑轮的使用特点,他们先用弹簧测力计缓慢提起钩码,如图(a)所示,再分别用重力不同的动滑轮甲、乙、丙(G甲>G乙>G丙)缓慢提起相同钩码,如图(b)、(c)、(d)所示.请仔细观察图是的操作和弹簧测力计的示数,然后归纳得出结论.
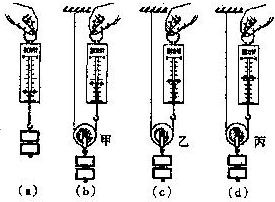
(1)比较图(a)与(b)[或(a)与(c),或(a)与(d)]两图可得:______;
(2)比较图(b)与(c)与(d)三图可得______. 冰明侠客1年前1
冰明侠客1年前1 -
 Alizee-andy 共回答了18个问题
Alizee-andy 共回答了18个问题 |采纳率88.9%解题思路:要解答本题需掌握:动滑轮可以省力,但不可以改变力的方向.根据图中弹簧测力计的示数,可以得出结论:
(1)(缓慢提起相同重物)使用动滑轮能省力,但不能改变用力方向.
(2)使用动滑轮(缓慢)提起相同重物时,动滑轮的重力越小,所用的拉力越小.点评:
本题考点: 动滑轮及其工作特点;滑轮组绳子拉力的计算.
考点点评: 本题主要考查学生对:动滑轮的特点的了解和掌握.1年前查看全部
- (2012•和平区模拟) 1时45分=1[3/4]1[3/4]时 265毫升=______立方分米 0.057公顷=__
(2012•和平区模拟)
1时45分= 1[3/4]1[3/4]时265毫升=______立方分米 0.057公顷=______平方米 60800克=______吨.  抢沙发041年前1
抢沙发041年前1 -
 草摩威威 共回答了19个问题
草摩威威 共回答了19个问题 |采纳率94.7%解题思路:(1)把1时45分换算成小时数,把45分除以进率60,然后把得数再加上1即可;
(2)把265毫升换算成立方分米数,用265除以进率1000即可;
(3)把0.057公顷换算成平方米数,用0.057乘进率10000即可;
(4)把60800克换算成吨数,用60800除以进率1000000即可.1时45分=(1[3/4])时;
265毫升=(0.265)立方分米;
0.057公顷=(570)平方米;
60800克=(0.0608)吨;
故答案为:1[3/4],0.265,570,0.0608.点评:
本题考点: 时、分、秒及其关系、单位换算与计算;质量的单位换算;面积单位间的进率及单位换算;体积、容积进率及单位换算.
考点点评: 此题考查名数的换算,把高级单位的名数换算成低级单位的名数,就乘单位间的进率,反之,则除以进率.1年前查看全部
- (2014•和平区二模)如图所示,当开关S闭合后,下列说法正确的是( )
(2014•和平区二模)如图所示,当开关S闭合后,下列说法正确的是( )

A.灯L1与灯L2是串联
B.电压表可测出灯L1两端的电压
C.电流表 测得是灯L1的电流
测得是灯L1的电流
D.电流表 测的是灯L2的电流
测的是灯L2的电流  jmr08961年前1
jmr08961年前1 -
 幸运儿舞儿 共回答了15个问题
幸运儿舞儿 共回答了15个问题 |采纳率100%由电路图可知,两灯泡并联,电压表即测量灯L2两端的电压,电流表A1测量干路电流,电流表A2测量通过L2的电流.
故选BD.1年前查看全部
- (2007•和平区二模)下列粒子结构示意图中,表示具有稳定结构原子的是( )
(2007•和平区二模)下列粒子结构示意图中,表示具有稳定结构原子的是( )
A.
B.
C.
D.
 o蓝彩o1年前1
o蓝彩o1年前1 -
 忘却的音符 共回答了16个问题
忘却的音符 共回答了16个问题 |采纳率87.5%解题思路:当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;若原子的最外层电子数为8,属于相对稳定结构;据此进行分析判断.A、该粒子最外层电子数为2,不具有稳定结构,故选项错误.
B、该粒子最外层电子数为8,但该粒子质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,故选项错误.
C、该粒子质子数=核外电子数=10,为原子;且最外层电子数为8,具有稳定结构,故选项正确.
D、该粒子最外层电子数为1,不具有稳定结构,故选项错误.
故选C.点评:
本题考点: 原子结构示意图与离子结构示意图.
考点点评: 本题考查学生对原子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.1年前查看全部
- (2012•和平区二模)小明在研究影响“电流的热效应”的因素时,做了如图所示的实验,该试验是研究产生电热的多少与____
 (2012•和平区二模)小明在研究影响“电流的热效应”的因素时,做了如图所示的实验,该试验是研究产生电热的多少与______是否有关的实验,你判断的依据是______.
(2012•和平区二模)小明在研究影响“电流的热效应”的因素时,做了如图所示的实验,该试验是研究产生电热的多少与______是否有关的实验,你判断的依据是______.  cclxd1年前1
cclxd1年前1 -
 lhj19820310 共回答了19个问题
lhj19820310 共回答了19个问题 |采纳率94.7%解题思路:电流流过导体时,都会产生热量,产生热量多少跟电流大小、通电时间长短、电阻有关.探究电热跟电阻关系时,控制通电时间和电流相同;探究电热跟电流关系时,控制电阻和通电时间相同;探究电热跟通电时间的关系,控制电阻和电流相同.如图,铜丝和镍铬合金串联在电路中,电流是相等的,通电时间是相等的,控制了电流和通电时间相同,铜丝和镍铬合金的电阻是不同的,所以实验探究电热和电阻的关系,其判断的依据是电流和通电时间相同.
故答案为:电阻;实验时控制电流和通电时间相同.点评:
本题考点: 焦耳定律;控制变量法与探究性实验方案.
考点点评: 一个物理量受多个因素影响时,探究物理量和其中一个因素的关系时,一定控制其它因素不变,这是初中最常用的控制变量法.1年前查看全部
- (2010•和平区一模)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸
(2010•和平区一模)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.
问题1 工业生产碘酸钾的流程如下:
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同.请写出反应器中发生反应的化学方程式:______;
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是______.
问题2 已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2温度/℃ 20 40 60 80 KIO3g/100g水 8.08 12.6 18.3 24.8
=2I-+S4O 2−3
.O 2−6
(1)测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是[1270/3W][1270/3W]mg/kg(以含w的代数式表示).
(2)学生乙又进行了下列实验:
①请推测实验中产生蓝色现象的可能原因,用离子方程式表示______.操作步骤 实验现象 取1g纯净的NaCl,加3mL水配成溶液. 溶液无变化 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. 溶液无变化 然后再滴入1滴1mol/L的H2SO4,振荡. 溶液变蓝色
②根据学生乙的实验结果,请对学生甲的实验结果作出简要评价:______(填“偏大”、“偏小”或“正确”).
其原因是______. wwy1987221年前1
wwy1987221年前1 -
 ff11gg 共回答了18个问题
ff11gg 共回答了18个问题 |采纳率88.9%解题思路:问题1
(1)反应中I2→KH(IO3)2,I元素化合价由0价升高为+5价,共升高10价.KClO3→KCl、Cl2,氯元素化合价降低,还原产物为KCl、Cl2,KClO3→KCl氯元素化合价由+5降低为-1价,化合价降低6价,KClO3→Cl2氯元素化合价由+5降低为0价,化合价总共降低10价,二者获得的电子数目相同,获得电子最小公倍数为30,则KCl的系数为5,Cl2的系数为3,所以化合价降低60价,故I2系数为6,根据元素守恒配平KClO3、H2O、KH(IO3)2的系数;
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得晶体需要蒸发结晶;
问题2
(1)根据硫代硫酸钠与碘酸钾的关系式计算碘酸钾的物质的量,再根据质量分数公式计算碘的含量;
(2)①酸性条件下,碘离子被氧气氧化生成碘单质;
②过量的碘离子易被空气氧化生成碘单质.(1)反应中I2→KH(IO3)2,I元素化合价由0价升高为+5价,共升高10价.KClO3→KCl、Cl2,氯元素化合价降低,还原产物为KCl、Cl2,KClO3→KCl氯元素化合价由+5降低为-1价,化合价降低6价,KClO3→Cl2氯元素化合价由+5降低为0价,化合价总共降低10价,二者获得的电子数目相同,获得电子最小公倍数为30,则KCl的系数为5,Cl2的系数为3,所以化合价降低共60价,故I2系数为6,根据氯元素守恒可知KClO3系数为11,根据碘元素守恒可知KH(IO3)2的系数为6,根据氢元素守恒可知H2O、系数为3,检查氧元素守恒,故方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,故答案为:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得KIO3晶体需要蒸发结晶,故答案为:蒸发结晶;
(1)设碘酸钾的物质的量为x.
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O①; I2+2S2O3 2-=2I-+S4 O62-②,将方程式②×3+①得
IO3-+6H++6S2O32-=I-+3S4O62-+3H2O
16
x2.0×10-3mol/L×0.01L
x=
2.0×10−3mol/L×0.01L×1
6=[1/3×10−5mol,根据碘原子守恒知,碘元素的质量=
1
3×10−5mol/L×127g/mol=4.23×10-4g,所以碘元素的质量分数=
1.27×10−3
3
w]×100%=[1270/3W]mg/kg,
故答案为:[1270/3W];
(2)①酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O,故答案为:4I-+4H++O2=2I2+2H2O;
②酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,导致测定结果偏大,故答案为:偏大,过量的I-会被空气中的O2氧化为I2.点评:
本题考点: 化学实验方案的评价;离子方程式的书写;氧化还原反应;中和滴定.
考点点评: 本题考查了氧化还原反应方程式的配平及有关计算,计算时注意是求食盐中碘的含量不是碘酸钾的含量,为易错点.1年前查看全部
- (2012•和平区二模)如图所示,A是悬挂在弹簧下的铁块,B是螺丝管的铁芯,P是滑动变阻器的滑片.闭合开关后的电磁铁的下
 (2012•和平区二模)如图所示,A是悬挂在弹簧下的铁块,B是螺丝管的铁芯,P是滑动变阻器的滑片.闭合开关后的电磁铁的下端是______极(选填“N”或“S”);若将变阻器的滑片P向右移动,弹簧的长度会______(选填“变长”或“变短”).
(2012•和平区二模)如图所示,A是悬挂在弹簧下的铁块,B是螺丝管的铁芯,P是滑动变阻器的滑片.闭合开关后的电磁铁的下端是______极(选填“N”或“S”);若将变阻器的滑片P向右移动,弹簧的长度会______(选填“变长”或“变短”).  彬四哦可1年前1
彬四哦可1年前1 -
 liuxinliuxin123 共回答了21个问题
liuxinliuxin123 共回答了21个问题 |采纳率85.7%解题思路:(1)由电源的正负极可知电流方向,则由右手螺旋定则可知螺线管的磁极;
(2)当滑动变阻器的滑片向右移动时,可知滑动变阻器的接入电阻变化,则由欧姆定律可知电流的变化,则可知螺线管磁性强弱的变化,根据螺线管的磁性变化以及磁铁的性质判断弹簧长度的变化.(1)根据安培定则可得,螺线管的上端为S极,下端为N极,
(2)若将变阻器的滑片P向右移动,滑动变阻器接入电路的电阻变大,所以电路中的电流变小,通电螺线管的磁性减弱;故对铁块的作用力减小,即弹簧长度应变短.
故答案为:N;变短.点评:
本题考点: 安培定则;影响电磁铁磁性强弱的因素.
考点点评: 本题将电路知识及磁场知识结合在一起考查了学生综合分析的能力,要求学生能灵活运用所学知识进行综合分析从而找出正确答案.1年前查看全部
- (2013•和平区一模)如图所示是一个欧姆表的外部构造示意图,其正、负插孔内分别插有红、黑表笔,则虚线内的电路图应是选项
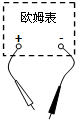 (2013•和平区一模)如图所示是一个欧姆表的外部构造示意图,其正、负插孔内分别插有红、黑表笔,则虚线内的电路图应是选项图中的( )
(2013•和平区一模)如图所示是一个欧姆表的外部构造示意图,其正、负插孔内分别插有红、黑表笔,则虚线内的电路图应是选项图中的( )
A.
B.
C.
D.
 fgs12fgsr1年前1
fgs12fgsr1年前1 -
 cleo72 共回答了24个问题
cleo72 共回答了24个问题 |采纳率75%解题思路:红表笔插在正极孔中,与内部电源的负极相连,选档后要进行调零.正极插孔接电源的负极,所以BC错误;每次换挡时都要进行短接调零,所以电阻要可调节,故A正确,D错误.
故选A点评:
本题考点: 用多用电表测电阻.
考点点评: 本题考查了欧姆表的内部结构,要记住电流从红表笔进,从黑表笔出.1年前查看全部
- (2014•和平区二模)在△ABC中,AB=AC,以AB为直径的⊙O交BC于点D,交AC于点E,DF为⊙O的切线,
(2014•和平区二模)在△ABC中,AB=AC,以AB为直径的⊙O交BC于点D,交AC于点E,DF为⊙O的切线,

(1)如图①,求∠DFC的度数;
(2)如图②,过点A作BC的平行线交BE的延长线于点G,连接CG,当△ABC时等边三角形时,求∠AGC的度数. 永远的支持者1年前0
永远的支持者1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•和平区二模)写出下列反应的化学方程式:
(2012•和平区二模)写出下列反应的化学方程式:
(1)实验室用过氧化氢制氧气2H2O2
2H2O+O2↑MnO2 .2H2O2;
2H2O+O2↑MnO2 .
(2)铜丝加入到硝酸银溶液中______;
(3)酒精燃烧C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2;
2CO2+3H2O点燃 .
(4)碳化钙(CaC2)与水反应生成氢氧化钙和乙炔(C2H2)气体______. taoyongjun08241年前1
taoyongjun08241年前1 -
 xzf007 共回答了25个问题
xzf007 共回答了25个问题 |采纳率84%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
MnO2
.
2H2O+O2↑.
(2)铜丝加入到硝酸银溶液中生成硝酸铜和银,反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag.
(3)酒精燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O.
(4)碳化钙(CaC2)与水反应生成氢氧化钙和乙炔(C2H2)气体,反应的化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑.
故答案为:(1)2H2O2
MnO2
.
2H2O+O2↑;
(2)Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)C2H5OH+3O2
点燃
.
2CO2+3H2O;
(4)CaC2+2H2O═Ca(OH)2+C2H2↑.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
大家在问
- 1愧疚什么意思
- 2蚓无爪牙之利中的爪牙的今义是什么意思
- 3英语翻译Chengdu is______ ______ ______ ______from my home __
- 4蛋白质是有机高分子材料吗?老师们还有别的说法吗
- 5急求一道聪明题甲乙两个修路队,共修3600米长的一条铁路.当甲完成所分任务的四分之三,乙完成所分任务的五分之四又40米时
- 6导数应用问题已知路程函数:s=2t3-1/2gt2,求t=2时,加速度是多少
- 7汉译英:电吉他与传统吉他有着相同的形状(the same...as)
- 8思考题圆是以一个正方形的边长为半径,正方形的面积为8平方米,正方形在圆中,求除了正方形外的圆的面积
- 9下列关于油脂的说法正确的是( )
- 10真核生物中共有几种核苷酸,几种碱基?原核生物中有几种核苷酸,几种碱基?病毒中有几种核苷酸,几种碱基?
- 11初中化学怎么学才学的好?
- 12什么是刃型位错?什么是螺型位错?写出作用在位错线上力的表达式和位错运动的晶格阻力.
- 13美国微软公司总裁比尔·盖茨曾说过:“你甚至不知道和你交流的对方,是一条坐在电脑前敲击键盘的狗。”这说明 [ &
- 14matter that is not clean 和metal bars that a train move along
- 15你能用乘法计算吗?11+12+13+14+15+16+17=( )*( )=( )
