重铬酸根+过氧化氢 的产物是什么颜色?
 zhangna09022022-10-04 11:39:543条回答
zhangna09022022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 边城游子007 共回答了20个问题
边城游子007 共回答了20个问题 |采纳率85%- 重铬酸根里铬是7价的 只能被还原 是强氧化剂 过氧化氢也是氧化剂 但是重铬酸钾强 所以过氧化氢歧化生成水和氧气 铬离子被还原为6价或者5价 为绿色或者黄色 因为过氧化氢不是强还原剂 应该不能还原到3价
- 1年前
 安格L 共回答了119个问题
安格L 共回答了119个问题 |采纳率- 紫色或紫绿色,三价铬离子的颜色
- 1年前
 darkangel2 共回答了271个问题
darkangel2 共回答了271个问题 |采纳率- 方程式如下:
Cr2O72−+8H++3H2O2=3O2↑+2Cr3++7H2O
Cr3+是绿色的 - 1年前
相关推荐
- 溶液中Cl-、重铬酸根(CrO4 2-)离子浓度均为0.001mol·L-1,若逐滴加入AgNO3溶液.
溶液中Cl-、重铬酸根(CrO4 2-)离子浓度均为0.001mol·L-1,若逐滴加入AgNO3溶液.
试计算:(1)哪一种离子先产生沉淀?(2)第二种离子开始沉淀时,溶液中残留的第一种离子的浓度是多少?
注意:这是对于Ksp有关的问题(大学的)有什么特殊的求法? 甜味的蔬菜沙拉1年前2
甜味的蔬菜沙拉1年前2 -
 悯月公主 共回答了19个问题
悯月公主 共回答了19个问题 |采纳率94.7%我也学生物的
因为容度积AgCl 1.8*10^(-10) Ag2CrO4 1.1*10(-12)
K[AgCl]=[Ag+]*[Cl-] K[Ag2CrO4]=[Ag+]^2*[CrO4]
所以溶解度AgCl比Ag2CrO4小,先沉淀
CrO4 2-沉淀时需要Ag+浓度可由K sp算出来,再用AgCl的Ksp计算Cl-的浓度就好了啊
真是累诶,买一本我们北大的《普通化学实验 B》就好了啊1年前查看全部
- 一道高二化学题,详细问题见补充工业上处理含Cr2O72-(重铬酸根离子)的酸性废水,采用以下方法:往废水中加入适量的氯化
一道高二化学题,详细问题见补充
工业上处理含Cr2O72-(重铬酸根离子)的酸性废水,采用以下方法:往废水中加入适量的氯化钠,以铁为电极进行电解,过一端时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水铬的含量已低于排放标准,回答下列问题:
(1)两极发生反应的电极反应式:
请问为什么Cr2O72-不能做阴极呢
 茉珂1年前1
茉珂1年前1 -
 allenshyan 共回答了21个问题
allenshyan 共回答了21个问题 |采纳率100%阳极:Fe-2e-==Fe2+
副反应:Cr2O7 2-+6Fe2++14H+==2Cr3++6Fe3++7H2O
阴极:2H++2e-==H2
其实重铬酸根不参加阴极反应的主要原因是亚铁离子还原性较大,在溶液中直接还原重铬酸根,而阴极铁棒上附有大量电子,从电性角度来看,重铬酸根很难靠近阴极区,因而不能直接反应.
从上面方程式可以看出,两边都在消耗氢离子,会使得溶液pH升高,将Cr3+和Fe3+沉淀出来.
希望对你有所帮助!
望采纳!1年前查看全部
- 铬酸根离子与二氧化硫反应离子方程式
 人称胖哥1年前1
人称胖哥1年前1 -
 illusion1977 共回答了13个问题
illusion1977 共回答了13个问题 |采纳率92.3%2CrO4 2- + 3SO2 + 4H+ == 3SO4 2- + 2Cr3+ + 2H2O
把SO2氧化为硫酸根,自己还原成+3价离子1年前查看全部
- 工业上处理含Cr2O72-(重铬酸根离子)的酸性废水,采用以下方法:往废水中加入适量的氯化钠,以铁为电极进行电解,过一端
工业上处理含Cr2O72-(重铬酸根离子)的酸性废水,采用以下方法:往废水中加入适量的氯化钠,以铁为电极进行电解,过一端时间,有Cr(OH)3和Fe(OH)3沉淀生成
想知道离子方程式
Cr2O7(2-) + 14H+ + 6Fe2+ == 2Cr3+ + 7H2O + 6Fe3+
之中Fe2+是哪里来的?不是铁单质嘛. yiran0081年前1
yiran0081年前1 -
 testabcs 共回答了12个问题
testabcs 共回答了12个问题 |采纳率91.7%因为用铁做了电极.
电解池中若阳极为金属
则金属放电.
所以阳极的铁放电形成Fe2+进入溶液(Fe放电和置换反应中若无强氧化剂一律生成Fe2+)1年前查看全部
- 等物质的量的重铬酸根和稀硝酸,哪个能将更多的硫化氢氧化为单质硫?
等物质的量的重铬酸根和稀硝酸,哪个能将更多的硫化氢氧化为单质硫?
Cr2O72-~Cr3+ HNO3~NO
我觉得应该是一样的,可答案说是重铬酸根, 鸟人第三1年前3
鸟人第三1年前3 -
 meshallgga 共回答了14个问题
meshallgga 共回答了14个问题 |采纳率92.9%Cr2O72- +8H+ +3H2S=3S+2Cr3+ +7H2O
所以1molCr2O72-氧化3molH2S
2NO3- +2H+ +3H2S=2NO+3S+4H2O
所以1molHNO3氧化1.5molH2S
当然是重铬酸根能将更多的硫化氢氧化为单质硫1年前查看全部
- 简单的化学基础问题S2O32-怎么读?还有Cr2O72-是重铬酸根读CHONG还是ZHONG 谢谢
 LOVE8161年前4
LOVE8161年前4 -
 wawzm9999 共回答了16个问题
wawzm9999 共回答了16个问题 |采纳率93.8%S2O32-硫代硫酸根
Cr2O72-重铬酸根(chong)1年前查看全部
- 氧化还原反应 污水处理2011年全国卷 13题题中提到用硫酸亚铁铵 处理 铬酸根离子请问铬酸根离子会不会将其中的铵根氧化
氧化还原反应 污水处理
2011年全国卷 13题
题中提到用硫酸亚铁铵 处理 铬酸根离子
请问铬酸根离子会不会将其中的铵根氧化? wendy8107091年前1
wendy8107091年前1 -
 周丹 共回答了14个问题
周丹 共回答了14个问题 |采纳率92.9%溶液中,NH4+没那么容易被氧化,
试想,NO3-都无法在溶液中氧化NH4+,NH4NO3溶液存在.
(NH4)2Cr2O7 重铬酸铵,很重要的重铬酸盐试剂.
一般认为,固态中,NH4NO3、(NH4)2Cr2O7都能发生自氧化还原反应.
即加热固体,NH4+会被NO3-氧化,NH4+会被Cr2O72-氧化,溶液中不可以1年前查看全部
- 蒸馏水中是否含有离子有一溶液,含有钙,镁,钠,氯,钾,重铬酸根离子,钡,硫酸跟离子等,用其蒸发,冷凝制备蒸馏水,所制备的
蒸馏水中是否含有离子
有一溶液,含有钙,镁,钠,氯,钾,重铬酸根离子,钡,硫酸跟离子等,
用其蒸发,冷凝制备蒸馏水,所制备的蒸馏水中含有哪些离子?100摄氏度的水蒸气中能含有金属离子吗? 雁过云烟1年前1
雁过云烟1年前1 -
 winsunwu 共回答了21个问题
winsunwu 共回答了21个问题 |采纳率90.5%镁,钠,钾
能的吧,离子很小的1年前查看全部
- 求问铬离子,重铬酸根离子和铬酸根离子的颜色,急在线等
 xia505551年前1
xia505551年前1 -
 huhuhu369 共回答了14个问题
huhuhu369 共回答了14个问题 |采纳率71.4%三价铬离子是绿色,重铬酸根是橙黄色至棕黄色(个人色觉不同会有差异),铬酸根离子是黄色.
希望对你有所帮助!1年前查看全部
- 求解亚硫酸根离子与氢离子与重铬酸根离子的离子反应方程式
 该给我打针了1年前2
该给我打针了1年前2 -
 飘雨季节selina 共回答了20个问题
飘雨季节selina 共回答了20个问题 |采纳率95%Cr2O72- + 3SO32- + 8H+ = 2Cr3+ + 3SO42- + 4H2O1年前查看全部
- 重铬酸根离子以及铬酸根离子在水溶液中是什么颜色
 又能挣钱了1年前3
又能挣钱了1年前3 -
 阳光百分百 共回答了10个问题
阳光百分百 共回答了10个问题 |采纳率90%重铬酸根离子是橙红色,铬酸根离子是亮黄色.1年前查看全部
- 一道高中化学题,请问A中的这个重铬酸根化合价降低,发生还原反应,不应该移向阴极吗?我知道那个阴离子移向阳极,但这个是发生
一道高中化学题,请问A中的这个重铬酸根化合价降低,发生还原反应,不应该移向阴极吗?我知道那个阴离子移向阳极,但这个是发生还原
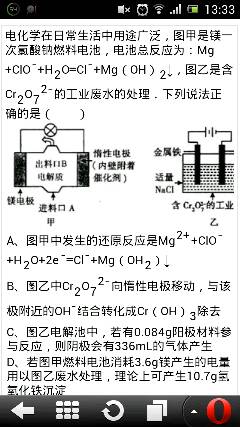
 少耶1年前3
少耶1年前3 -
 龙类倒戈 共回答了20个问题
龙类倒戈 共回答了20个问题 |采纳率95%甲是原电池,左边是负极,Mg失去电子,发生氧化反应;右边是正极,NaClO得到电子,发生还原反应.
正极:ClO-+H2O+2e-==Cl-+2OH-
负极:Mg-2e-+2OH-==Mg(OH)2
乙是电解池,因为左边连的是电源的正极,那麼左边是阳极,失去电子,发生氧化反应;右边是阴极,得到电子,发生还原反应.
阴极:Cr2O72- 十6e- 十7H2O=2Cr(OH)3↓+8OH-
阳极:Fe-2e-+2OH=Fe(OH)2
Fe(OH)2遇到空气被迅速氧化成Fe(OH)3
所以A,B错误
C没说是标况下的体积也错误
D:Mg失去的电子量为3.6/24*2=0.3mol
0.1mol Fe变成Fe(OH)3转移电子量是0.3mol
那麼Fe(OH)3物质的量是0.1mol
Fe(OH)3质量就是0.1*107=10.7克
所以D是正确的.1年前查看全部
- 铬酸根—重铬酸根的平衡常数H+ + CrO4 2- = HCrO4- K1=?2HCrO4-=Cr2O7 2- + H2
铬酸根—重铬酸根的平衡常数
H+ + CrO4 2- = HCrO4- K1=?
2HCrO4-=Cr2O7 2- + H2O K2=?
温度在24.当然可以认为是25度。 坐在星星上看你1年前1
坐在星星上看你1年前1 -
 w_咖啡ice 共回答了20个问题
w_咖啡ice 共回答了20个问题 |采纳率100%自己去查大学书吧1年前查看全部
- 亚铁离子与重铬酸根离子的反应
 duck1471年前1
duck1471年前1 -
 holleywuhan 共回答了14个问题
holleywuhan 共回答了14个问题 |采纳率92.9%6(Fe2+)+(Cr2O7)(2-)+14(H+)=2(Cr3+)+7H2O+6Fe3+1年前查看全部
- 某溶液由钠离子,钡离子,铝离子,偏铝酸根,重铬酸根,碳酸根,硫酸根中的若干种组成.取适量该溶液进行如下实验:(1),加入
某溶液由钠离子,钡离子,铝离子,偏铝酸根,重铬酸根,碳酸根,硫酸根中的若干种组成.取适量该溶液进行如下实验:(1),加入过量盐酸有气体生成并得到无色溶液;(2),在(1)所得的溶液中加入过量碳酸氢氨溶液,有气体生成并析出白色沉淀甲;(3),在(2)中间所得溶液中加入过量氢氧化钡也有气体生成并产生白色沉淀乙,则原沉淀中一定存在的离子是钠离子,偏铝酸根,碳酸根.为什么
 hz9191年前2
hz9191年前2 -
 luosi007 共回答了22个问题
luosi007 共回答了22个问题 |采纳率72.7%由第一步可以知道溶液中含有CO32-,无Cr2O72-,Ba2+和Al3+.所以阳离子只有Na+.(1)所得的溶液含有Na+,Cl-,H+,可能含有AlO2-,SO42-.第二步可知其含有AlO2-,因为第一步中AlO2-变成了Al3+,跟HCO3-双水解得到沉淀.(2)所得溶...1年前查看全部
- 酸性溶液中重铬酸根还原为铬(III)离子的半反应式为
 bedim1年前1
bedim1年前1 -
 爱娜520 共回答了18个问题
爱娜520 共回答了18个问题 |采纳率94.4%Cr2O7 2- + 14H+ + 6e → 2Cr 3+ 7H2O1年前查看全部
- 求 乙酸根离子 和 重铬酸根离子
 abl8843311年前4
abl8843311年前4 -
 瓷砖小子 共回答了15个问题
瓷砖小子 共回答了15个问题 |采纳率100%乙酸根离子 的化学式CH3COO-
重铬酸根离子 的化学式Cr2O72-1年前查看全部
- 重铬酸根铬酸根怎么铬化合价是一样的A
 清冷帝1年前1
清冷帝1年前1 -
 废墟中歌唱 共回答了29个问题
废墟中歌唱 共回答了29个问题 |采纳率89.7%是一样的,但他们在溶液中存在的形态不同.
重铬酸根在酸性条件下可以转化为铬酸根,如下:
2CrO4(2-) + 2H+ == Cr2O7(2-) + H2O
当然,如果溶液中存在还原性物质,重铬酸根会被还原成Cr3+1年前查看全部
- 重铬酸根都能氧化什么离子重铬酸根具有氧化性 也能氧化乙醇 二价铁等 但是我不知道还能氧化什么离子 请举例 请明白的人回答
重铬酸根都能氧化什么离子
重铬酸根具有氧化性 也能氧化乙醇 二价铁等 但是我不知道还能氧化什么离子 请举例 请明白的人回答 要准确 真心❤感谢❤! bopite1年前1
bopite1年前1 -
 楚楚的小猪 共回答了22个问题
楚楚的小猪 共回答了22个问题 |采纳率100%可以氧化大部分有还原性的离子.重铬酸钾的氧化性与高锰酸钾相当,可以当作高锰酸钾来用.
举几个例子:可氧化S 2- 、Fe2+、H2O2、I-、SO3 2-等等.
满意请采纳(手机版点“满意”即可)1年前查看全部
- 酸性条件下的重铬酸根,还有浓硫酸都有强氧化性,谁可以氧化醛基?
酸性条件下的重铬酸根,还有浓硫酸都有强氧化性,谁可以氧化醛基?
可以的话把原理说一下吧! vincentqy1年前2
vincentqy1年前2 -
 谁动了我的感情 共回答了6个问题
谁动了我的感情 共回答了6个问题 |采纳率83.3%浓硫酸遇到有机物应该是以脱水反应为优先,当然也会氧化,但是反应较复杂
酸性条件下重铬酸跟可以氧化醇(伯醇和仲醇),到酸,别说是醛了,肯定没问题
用CrO3和吡啶的络合物可以氧化醇到醛类,1年前查看全部
- 亚硝酸根离子与氢离子与重铬酸根离子的离子反应方程式
 mawenjing1年前1
mawenjing1年前1 -
 wufan1997 共回答了19个问题
wufan1997 共回答了19个问题 |采纳率94.7%3(NO2)- + (Cr2O7)2- + 8H+ ==3(NO3)- + 2Cr3+ + 4H2O1年前查看全部
- 铬酸根和亚铁离子反应的离子反应方程式是什么?是铬酸根不是重铬酸根
 jmlaw21年前1
jmlaw21年前1 -
 i1357 共回答了19个问题
i1357 共回答了19个问题 |采纳率94.7%CrO4^2-不同于Cr2O7^2-的特点是存在于中性,或者碱性环境,即方程式不能用H+配平
生成物就是Fe(OH)3和Cr(OH)3
CrO4^2- + 3Fe2+ + 4 OH- + 4 H2O = 3Fe(OH)3 + Cr(OH)31年前查看全部
大家在问
- 1迟,词语接龙接四个?
- 2重铬酸根与铬酸根的转化是氧化还原反应吗
- 3使用旋转阳极X线管时,无X线发生,试述该故障产生的原因!
- 4小明在姑姑家玩的很开心,他不想回去,姑姑笑着说;;你真有点【 ]了填上三国歇后语
- 5至今为止,科学家们一直在研究地球的起源以及它的构造.(as well as)
- 61.一个数的因数的个数是什么,其中最大的是什么,最小的是什么?2.一个数的倍数的个数有什么,其中最小的是什么?
- 7三年级数学上册节余多少钱教案以及课件
- 8求…能简单给解释下无意突变的抑制作用?
- 9x的平方减去a的2倍是多少?用含有字母的式子表示就行了.
- 10七年级下册第二课的笔记
- 11英语翻译BANK OF TIERRA DEL FUEGO PROVINCE—BUENOS AIRES,ARGENTNA
- 12我把一只蜗牛放在一个硬纸盒里.改变词序,不改变句意
- 13浓度百分之十的稀盐酸弄在手上回怎么样
- 14李大伯比小明今年大48岁,李大伯的年龄是小明的5倍,李大伯和小明各多少岁?怎么列式?
- 15asina+cosa=1,bsina-cosa=1,求ab的值
