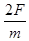电火花所产生的频率是从零到无限吗?
 kittyzhq08712022-10-04 11:39:541条回答
kittyzhq08712022-10-04 11:39:541条回答一个电火花所包含的频率相当丰富,但具体的范围是多少呢?
电火花(包括雷电)所产生的电磁波频谱范围肯定非常宽,不然收音机的各个波段为何都能听到它的喀喀噪声呢?

已提交,审核后显示!提交回复
共1条回复
 不过是晴天 共回答了16个问题
不过是晴天 共回答了16个问题 |采纳率87.5%- 你说的对,是0到无限.但是,在各个频段的强度分布,并不是平均的.有的频段强,有的频段弱.具体的话,要看你的脉冲时间,就是电火花的放电曲线.用放电曲线做傅立叶分析就是频谱分布了.
一般,这种脉冲会被当作比较窄的高斯波包.根据傅立叶变换的性质,高斯波包越窄,其变换后的波包越宽.也就是,电火花放电时间越短,它的频谱分布就越广.当然,这个广,是指一定强度以上的分布.如果只要有就算上的话,不管强度,那就是零到无限了.建议你去查一下高斯波包的傅立叶变换. - 1年前
相关推荐
- 某密闭容器中有100g氧气和足量的过氧化钠,向其中冲入5g co 和 H2 的混合气体后,电火花点燃,反映足够长时间后,
某密闭容器中有100g氧气和足量的过氧化钠,向其中冲入5g co 和 H2 的混合气体后,电火花点燃,反映足够长时间后,容器内气体的质量是?
是 “等于100g” 为啥呢没? 全额为如下1年前2
全额为如下1年前2 -
 甘木日识 共回答了12个问题
甘木日识 共回答了12个问题 |采纳率91.7%2CO+O2=2CO2 2CO2+2Na2O2=2Na2CO3+O2
合并得:CO+Na2O2=Na2CO3
2H2+O2=2H2O 2H2O+2Na2O2=4NaOH+O2
合并得:H2+Na2O2=4NaOH
由反应可以看出,CO,H2与Na2O2反应,并没有消耗O2
所以体积仍等于100g1年前查看全部
- 如图所示是加油站设有的“禁止使用手机”警示标志,该标志是为了防止拨打手机产生的电火花点燃汽油引起火灾,这是因为汽油在常温
如图所示是加油站设有的“禁止使用手机”警示标志,该标志是为了防止拨打手机产生的电火花点燃汽油引起火灾,这是因为汽油在常温下容易

A.液化 B.汽化 C.凝华 D.升华  想做墙上的画1年前1
想做墙上的画1年前1 -
 敲钟人a 共回答了12个问题
敲钟人a 共回答了12个问题 |采纳率83.3%B
了防止拨打手机产生的电火花点燃汽油引起火灾,这是因为汽油在常温下容易汽化,选B1年前查看全部
- (2011•徐汇区二模)汽车行驶时,由于电火花的作用,气缸里有一系列的化学反应发生,其中N2+O2→2NO,2NO+O2
(2011•徐汇区二模)汽车行驶时,由于电火花的作用,气缸里有一系列的化学反应发生,其中N2+O2→2NO,2NO+O2→2NO2.这两个反应都属于
( )
A.置换反应
B.分解反应
C.化合反应
D.复分解反应 k885261年前1
k885261年前1 -
 ftw100200 共回答了24个问题
ftw100200 共回答了24个问题 |采纳率91.7%解题思路:化合反应是指由两种或两种以上物质反应生成另外一种物质的反应.N2+O2→2NO和2NO+O2→2NO2这两个反应中,反应物都是两种,生成物都是一种,属于化合反应.
故选C.点评:
本题考点: 反应类型的判定.
考点点评: 本题主要考查反应类型方面的知识,解答时要分析反应物和生成物的种类,然后再根据各种反应类型的概念方面进行分析、判断,从而得出正确的结论.1年前查看全部
- (2002•徐州)汽车的尾气中含有氮的氧化物,它们是空气污染物.汽车行驶时,由于电火花的作用.汽缸里有系列化学反应发生,
(2002•徐州)汽车的尾气中含有氮的氧化物,它们是空气污染物.汽车行驶时,由于电火花的作用.汽缸里有系列化学反应发生,其中有N2+O2
2NO;2NO+O2═2NO2 这两个反应所属的反应类型是( )放电 .
A.化合反应
B.分解反应
C.置换反应
D.复分解反应 张酒1年前1
张酒1年前1 -
 小猴999 共回答了21个问题
小猴999 共回答了21个问题 |采纳率95.2%在N2+O2
放电
.
2NO和2NO+O2=2NO2这两个反应中,反应物都是两种,生成物都是一种,属于化合反应.
故选A.1年前查看全部
- 如果天气干燥,晚上脱毛衣时会听到“噼啪”响声,还会看到电火花。这种现象产生的原因是 [
如果天气干燥,晚上脱毛衣时会听到“噼啪”响声,还会看到电火花。这种现象产生的原因是 [ ]A.人身体上产生电流
B.接触带电造成的
C.摩擦起电造成的
D.感应起电造成的 童波罗1年前1
童波罗1年前1 -
 yiran019 共回答了27个问题
yiran019 共回答了27个问题 |采纳率81.5%C1年前查看全部
- 常温常压下,分别将等物质的量的氢气 氧气冲入密闭容器内,电火花引燃,恢复到原状态,最后
常温常压下,分别将等物质的量的氢气 氧气冲入密闭容器内,电火花引燃,恢复到原状态,最后
气体的体积为反应前气体的四分之一,为什么是四分之一 7f3dasgas1年前2
7f3dasgas1年前2 -
 yahui1980 共回答了11个问题
yahui1980 共回答了11个问题 |采纳率90.9%由反应:2H2+O2=2H2O可知;分别设氢气与氧气为1mol.
2 1
1 1
由上式可知,当氧气与氢气等物质的量反应时,氢气完全反应,而氧气剩余一半,则
剩余的气体:2-1-0.5=0.5=四分之一1年前查看全部
- 如图所示是一个演示实验,老师向盒中滴入数滴酒精,再将盒盖盖紧,然后揿动电火花发生器的按钮看到盒盖飞出。课堂上教师用该演示
如图所示是一个演示实验,老师向盒中滴入数滴酒精,再将盒盖盖紧,然后揿动电火花发生器的按钮看到盒盖飞出。课堂上教师用该演示实验是用来说明 能转化为 能。列举应用这一原理的机器: 。

 维生素专题1年前1
维生素专题1年前1 -
 zhenyu1111 共回答了24个问题
zhenyu1111 共回答了24个问题 |采纳率91.7%内能 机械 汽油机(柴油机)
分析:热机是燃料在气缸内燃烧,产生高温高压的燃气,燃气对活塞做功,内能转化为机械能.
透明的塑料盒相当于一个气缸,塑料盒的盖相当于活塞,酒精在塑料盒内燃烧,产生高温高压的燃气,推动塑料盒盖运动,把内能转化为机械能;此过程类似于内燃机中的做功冲程.
故答案为:内、机械,汽油机.1年前查看全部
- 把11mol氢气、5mol氧气和1mol氯气在密闭容器中用电火花点燃,恰好完全反应,生成水的物质的量为10mol,生成氯
把11mol氢气、5mol氧气和1mol氯气在密闭容器中用电火花点燃,恰好完全反应,生成水的物质的量为10mol,生成氯化氢质量73g,所得溶液溶质的质量分数为( ),溶液中H+和H2O的个数比为( ) 详解.
 qingkemaolv1年前1
qingkemaolv1年前1 -
 l5byib 共回答了25个问题
l5byib 共回答了25个问题 |采纳率96%生成水的物质的量为10mol即质量m(H2O)=n(H2O)*M(H2O)=10mol*18g/mol=180g,m(溶液)=m(HCl)+m(H2O)=73g+180g=253g,溶液溶质的质量分数=溶质质量除以溶液的质量=73g/253g=28.85%
由物质的量的公式n=N/NA知道,微粒的个数之比就等于物质的量之比,故溶液中H+和H2O的个数比N(H+)/N(H2O)=n(H+)/n(H2O),而溶液中的H+可看做是有HCl电离得到,故n(H+)=n(HCl),而氯化氢质量为73g,故n(HCl)=m(HCl)/M(HCl)=1mol,所以N(H+)/N(H2O)=n(H+)/n(H2O)=1mol:10mol=1:10.
关于高一化学物质的量的题目,这个算是很基础的了,刚接触这个概念可能会觉得比较难,多做点题会好点.以后再回过头来看,会觉得很容易的.1年前查看全部
- Na金属化合物XmolCO YmolH2O ZmolO2的混合气体充入盛有足量的过氧化钠的密闭容器中,并用电火花将其充分
Na金属化合物
XmolCO YmolH2O ZmolO2的混合气体充入盛有足量的过氧化钠的密闭容器中,并用电火花将其充分反应,有关容器内反应的下列叙述不正确的是:
A 参加反应的过氧化钠为(X+Y)mol
B反应后容器内的O2为(X+Y)/2mol
C反应前后容器中的压强之比为(温度不变)(X+Y+Z)/Z
D反应后生成Xmol碳酸钠和2Ymol氢氧化钠 信心在哪里er1年前1
信心在哪里er1年前1 -
 jinweimin 共回答了17个问题
jinweimin 共回答了17个问题 |采纳率94.1%应该选AD.
XCO+X/2 O2==XCO2
XCO2+XNa2O2==XNa2CO3+X/2 O2
YH2O+YNa2O2==2YNaOH+Y/2 O2
过氧化钠是足量的所以二氧化碳和水肯定消耗完全,所以A、D正确;由上式可以看出最后容器中的氧气为(Z+Y/2)mol,其他产物都是固体,所以前后压强比为(X+Y+Z):(Z+Y/2),所以C选项不正确.
不知道我说明白了吗?1年前查看全部
- 化学关于物质的量……把11体积的氢气,5体积的氧气和1体积的氯气在密闭容器中用电火花点燃,恰好完全反应,所得溶液溶质的质
化学关于物质的量……
把11体积的氢气,5体积的氧气和1体积的氯气在密闭容器中用电火花点燃,恰好完全反应,所得溶液溶质的质量分数为多少? 文莱特1年前1
文莱特1年前1 -
 菲常YOUYUN 共回答了26个问题
菲常YOUYUN 共回答了26个问题 |采纳率88.5%其实就是10体积H2 与 5体积O2 ,生成10体积H2O 作为溶剂
剩下的1体积H2与1体积Cl2反应生成两体积HCl 作为溶质
所以溶液质量分数为73/(73+10*18)=0.291年前查看全部
- 在“探究小车速度随时间变化的规律”实验中,同学们利用电磁(或电火花)式打点计时器在纸带上打下一系列的点迹,由此研究小车的
在“探究小车速度随时间变化的规律”实验中,同学们利用电磁(或电火花)式打点计时器在纸带上打下一系列的点迹,由此研究小车的运动情况.(以下有关计算保留两位有效数字) 
(1)打点计时器使用的电源是______(选填“交流电”或者“直流电”).
(2)如图是在实验中的一条纸带示意图,图中O、A、B、C、D、E为相邻的计数点(相邻两点之间还有四个计时点未画出),则相邻两计数点间的时间间隔T=______s.
(3)根据测量数据,计算B点瞬时速度v B =______m/s.
(4)由此你能判断小车的运动的情况是______小车的加速度a=______m/s 2 . 鲨鱼大象1年前1
鲨鱼大象1年前1 -
 胖子孙007 共回答了18个问题
胖子孙007 共回答了18个问题 |采纳率94.4%(1)根据打点计时器的工作原理可知,打点计时器使用的是交流电源.
(2)打点计时器的打点周期0.02s,相邻两点之间还有四个计时点未画出,因此相邻两计数点间的时间间隔T=0.1s.
(3)根据匀变速直线运动中某段时间内的平均速度等于中间时刻的瞬时速度求出B点的瞬时速度为:
v B =
x AC
2T =
(27.80-3.20)×1 0 -2 m
2×0.1s ≈1.2m/s
(4)由题中数据可知,连续相等时间内的位移差为常数,因此小车做匀加速直线运动,根据x=aT 2 得:
x 4 - x 2 =2a 1 T 2
x 3 - x 1 =2a 2 T 2
a=
a 1 + a 2
2 =
( x 3 + x 4 )-( x 1 + x 2 )
4 T 2 =
(49.1-12.50)×1 0 -2 m-12.5×1 0 -2 m
4×(0.1s ) 2 =6.0m/ s 2
故答案为:(1)交流电;(2)0.10;(3)1.2;(4)匀加速直线运动,6.0.1年前查看全部
- 常温常压下,分别将等物质的量的H2和O2充入密闭容器中,电火花引燃,恢复到原状态,最后容器压强为反应前
常温常压下,分别将等物质的量的H2和O2充入密闭容器中,电火花引燃,恢复到原状态,最后容器压强为反应前
过程和思路都写下
反应前的百分之多少
A1/4 B3/4 C1/2 D1/3 平头ll61年前2
平头ll61年前2 -
 ymj6ghu 共回答了14个问题
ymj6ghu 共回答了14个问题 |采纳率92.9%太监贴,呵呵 压强为多少呢?
这个假设都是2mol 那么反应后O2多了1mol,生成的水常温常压为液态,故最后还剩下1molO2为气体 反应前有4mol气体,根据阿伏伽德罗定律的推论,同温同体积下,压强比等于气体的物质的量之比,因此答案为A1年前查看全部
- 常温常压下,分别将等物质的量的H2和O2充入密闭容器中,电火花引燃,恢复到原状态,最后容器压强为反应前
 飞鲽1年前1
飞鲽1年前1 -
 青凤于飞 共回答了17个问题
青凤于飞 共回答了17个问题 |采纳率100%设物质的量为n
P初=(n+n)RT/V
P末=(n/2)RT/V
最后容器压强为反应前1/41年前查看全部
- 干燥的天气,由于摩擦身体带电,手指在距门把1个厘米时,就会打出电火花,此时人体带的电压大约有多高?
 绅士鱼1年前5
绅士鱼1年前5 -
 awqs190 共回答了21个问题
awqs190 共回答了21个问题 |采纳率95.2%10000伏,是2005年科技周媒体联动“趣味物理有奖知识竞赛”试题1年前查看全部
- 试述一次电火花的放电过程,并详细分析极间介质的击穿机理
 在镜中飞翔1年前2
在镜中飞翔1年前2 -
 dasong1901 共回答了26个问题
dasong1901 共回答了26个问题 |采纳率96.2%首先电极附近的电场强度达到空气的击穿电压,从而使空气中的微量离子加速运动,同时撞击中性的空气分子使之电离产生更多的离子 这样雪崩式的作用结果就是两个电极间产生了由离子组成的电离通道(电弧)因其中有很多的离子而有很好的导电性,其中的原子会因温度较高而放出很强的光线1年前查看全部
- 打火机给人们生活带来方便.普通打火机一般由以下几部分组成:①压电陶瓷(产生电火花)②塑料机身 ③通风口
打火机给人们生活带来方便.普通打火机一般由以下几部分组成:①压电陶瓷(产生电火花)②塑料机身 ③通风口 ④铁皮配件 ⑤燃料(丁烷).其中符合燃烧条件使打火机能打火的组合是( )
A.①②③
B.①③④
C.①③⑤
D.①②④ 明日在相见1年前1
明日在相见1年前1 -
 wanshi1986 共回答了11个问题
wanshi1986 共回答了11个问题 |采纳率100%解题思路:根据燃烧的条件(燃烧需要同时满足三个条件:①可燃物②氧气或空气③达到燃烧所需的最低温度即着火点)解答本题.根据燃烧需要同时满足三个条件:①可燃物 ②氧气或空气 ③达到燃烧所需的最低温度即着火点,可知要使打火机燃烧必须具备:电火花,氧气即通风口,可燃物.
故选C.点评:
本题考点: 燃烧与燃烧的条件.
考点点评: 本题考查学生依据燃烧需要同时满足的三个条件进行分析解题的能力.1年前查看全部
- 小杨同学用如图所示的实验装置“探究小车动能变化与合外力做功的关系”,图中A为小车,连接在小车后面的纸带穿过电火花打点计时
小杨同学用如图所示的实验装置“探究小车动能变化与合外力做功的关系”,图中A为小车,连接在小车后面的纸带穿过电火花打点计时器B的限位孔,它们均置于水平放置的一端带有定滑轮的足够长的木板上,C为弹簧测力计,假设绳与滑轮之间的摩擦以及纸带穿过计时器时受到的摩擦均不计,实验时,先接通电源再松开小车,计时器在纸带上留下一系列点。
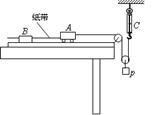
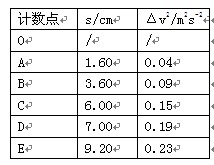
(1)该同学在一条比较理想的纸带上,依次选取O、A、B、C、D、E共6个计数点,分别测量后5个计数点与计数点O之间的距离,并计算了它们与O点之间的速度平方差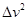 (注:
(注: ),填入下表:
),填入下表:
请以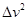 纵坐标,以s为横坐标作出
纵坐标,以s为横坐标作出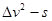 图像;若测出小车质量为0.2kg,结合图像可求得小车所受合外力的大小为 N。(结果保留两位有效数字)
图像;若测出小车质量为0.2kg,结合图像可求得小车所受合外力的大小为 N。(结果保留两位有效数字)
(2)该同学通过计算发现小车所受合外力小于测力计读数,明显超出实验误差的正常范围,你认为主要原因是 。 aini呀1年前1
aini呀1年前1 -
 ophen 共回答了11个问题
ophen 共回答了11个问题 |采纳率81.8%1年前查看全部
- 形成矿井外因火灾的原因有()A存在明火B违章放炮C电火花D机械摩擦
形成矿井外因火灾的原因有()A存在明火B违章放炮C电火花D机械摩擦
多选 乖橙子1年前2
乖橙子1年前2 -
 tiger0527 共回答了17个问题
tiger0527 共回答了17个问题 |采纳率100%a c d、全是.1年前查看全部
- (2007•黄冈)在一密闭容器中,盛放A,B,C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下: 物
(2007•黄冈)在一密闭容器中,盛放A,B,C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
关于此反应,下列认识不正确的是( )物质 A B C 新物质D 反应前物质质量/g 30 30 30 0 反应后物质质量/g 待测 33 0 22
A.C物质中所含有的元素种类是A,B,D三种物质中所有元素种类之和
B.变化后待测的A质量为5g
C.该变化的基本反应类型是分解反应
D.A物质有可能是单质 taotao_space1年前1
taotao_space1年前1 -
 fzy007 共回答了17个问题
fzy007 共回答了17个问题 |采纳率76.5%解题思路:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.计算出变化后待测的A质量;然后根据反应类型的特征确定反应类型;根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.确定A的正误;根据分解反应的概念确定D的正误.B、根据质量守恒定律可知,变化后待测的A质量=(30+30+30)-(33+22)=35g.故B不正确;
A、C、由图表数据可知,反应过程中C物质完全反应,A、B物质质量增加,还生成了新物质D.故此反应属于分解反应,化学方程式为;C=A+B+D.故AC都正确;
D、分解反应的产物可能是单质,也可能是化合物,在这个题目中同样是没有限制的.故D正确.点评:
本题考点: 质量守恒定律及其应用;反应类型的判定.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 在密闭容器中盛有氢气和氧气和氯气的混合气体,通过电火花点燃后,三种气体正好完全反应,所得溶质的质量
在密闭容器中盛有氢气和氧气和氯气的混合气体,通过电火花点燃后,三种气体正好完全反应,所得溶质的质量
分数为25.26%,则原有的氢气和氧气和氯气的分子数比? qi7sro5v1年前1
qi7sro5v1年前1 -
 酒兽 共回答了10个问题
酒兽 共回答了10个问题 |采纳率80%设所得到的混合物的总质量是100克,由于溶质的质量分数是25.26%,则氢气和氯气反应生成的氯化氢就是25.26g,氢气和氧气反应得到的水的质量就是74.74g,再根据氯化氢中氯元素的质量分数为97.26%,得氯元素的质量为24.57g,即原混合气体中氯气的质量为24.57g,可算知氯气的物质的量为24.57/71=0.346mol(0.5mol),
同理可知,氢气的物质的量是4.498mol(4.5mol),氧气的物质的量是2.076mol(2mol)
思路就是这样,不知是数据有问题还是什么,算出来有点出入,你可以再试试!
m(氢气):m(氧气):m(氯气)=4.5:2:0.5 =9:4:11年前查看全部
- 美国学者米勒在一烧瓶中模拟原始大气的成分充入CH 4 、NH 3 、H 2 、水蒸气等气体经连续7天电火花放电后获得了氨
美国学者米勒在一烧瓶中模拟原始大气的成分充入CH 4 、NH 3 、H 2 、水蒸气等气体经连续7天电火花放电后获得了氨基酸,此实验为无机小分子生成有机小分子创造了条件,证明了生命起源是通过化学过程而进行的。该实验的机制是( )
A.火花放电发出的光加速了化学反应 B.通过电场将气电离或断开化学键 C.提供能量使气体分子能级增大 D.通过电场使气体分子加速碰撞  yfhjy1年前1
yfhjy1年前1 -
 思汇泉 共回答了18个问题
思汇泉 共回答了18个问题 |采纳率100%B
此实验为无机小分子生成有机小分子创造了条件,这说明在反应中有化学键的断裂和生成,选项B正确,其余都是错误的,答案选B。1年前查看全部
- 蓄电池点火系是怎样产生电火花的
 华跃1年前1
华跃1年前1 -
 stone2438 共回答了17个问题
stone2438 共回答了17个问题 |采纳率82.4%无论是传统点火系还是电子点火系以及微机控制点火系统,其点火系产生电火花的原理都是电磁感应原理.即通过对初级线圈通断的控制使之产生磁通从而使次级线圈感应出高电压,一般可达15--20KV.高电压击穿火花塞间隙产生电火花.1年前查看全部
- 在密闭容器中盛有H2、O2、Cl2三种气体, 电火花点燃后,三种气体都正好反应完全,冷却到室温,所得溶液得质量分数为25
在密闭容器中盛有H2、O2、Cl2三种气体, 电火花点燃后,三种气体都正好反应完全,冷却到室温,所得溶液得质量分数为25.26%,则原混合气体中三者得分子个数之比为 ( )
(A)6:3:1 (B)9:6:1 (C)13:6:1 (D)15:8:1
选C
不是应该是n(H2):n(O2):n(Cl2)=3:1:1
为什么可以 根据2H2+O2==2H2O,H2+Cl2===2HCl.可得出
n(H2)=2n(O2)+n(Cl2)?
麻烦说明白点 重点是“n(H2)=2n(O2)+n(Cl2)”是怎么得出来的?
万分感谢.
 朝洗心1年前1
朝洗心1年前1 -
 gqmqt 共回答了16个问题
gqmqt 共回答了16个问题 |采纳率81.3%根据反应2H2+O2=2H2O,H2+Cl2===2HCl,
可设所需O2为Xmol Cl2为ymol,则一共消耗的H2为(2X+Y)mol
所以写做n(H2)=2n(O2)+n(Cl2)
只有C选项符合
希望可以明白1年前查看全部
- 30g氧气和氢气的混合气体经电火花引燃后冷却到室温,剩余3g气体
30g氧气和氢气的混合气体经电火花引燃后冷却到室温,剩余3g气体
问:则混合气体中氢气和氧气的质量分别是多少 弹雨1年前2
弹雨1年前2 -
 Kennedy_04 共回答了24个问题
Kennedy_04 共回答了24个问题 |采纳率91.7%①若剩余的3g气体为H2,那么有27g气体参加反应,根据质量守恒可知,生成H2O也为27g:
2H2+O2=2H2O
4 32 36
x y 27g
x=3g y=24g
故混合气体中氢气的质量为:3g+3g=6g,氧气的质量为:24g
②若剩余的3g气体为O2,那么有27g气体参加反应,根据质量守恒可知,生成H2O也为27g:
2H2+O2=2H2O
4 32 36
x y 27g
x=3g y=24g
故混合气体中氢气的质量为:3g,氧气的质量为:24g+3g=27g1年前查看全部
- “高频电火花塑料表面处理机”的英文怎样!
“高频电火花塑料表面处理机”的英文怎样!
小弟要做这机器的箱麦.请英语强的哥们帮帮忙. 11狼1年前1
11狼1年前1 -
 流浪的BOY 共回答了15个问题
流浪的BOY 共回答了15个问题 |采纳率86.7%High-frequency sparkling plastics surface processo1年前查看全部
- 把20克氢气和氧气的混合体充入一密闭容器中(无其他气体和物质),经电火花点火充分反应后,有18g水生成.
 xbean1年前3
xbean1年前3 -
 吊你看不懂 共回答了22个问题
吊你看不懂 共回答了22个问题 |采纳率90.9%2H2 + O2= 2H2O
4 32 36
2 16 18
(1)O2过量2g O2是18g H2是2g
(2)H2过量2g H2是4g O2是16g1年前查看全部
- 在一个密闭的钢桶内,有甲、乙、丙、丁四种物质,在电火花的作用,发生充分反应,反应前后各物质的质量:
在一个密闭的钢桶内,有甲、乙、丙、丁四种物质,在电火花的作用,发生充分反应,反应前后各物质的质量:
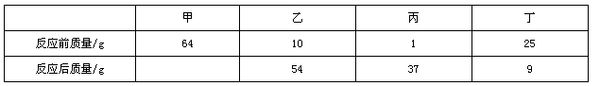 已知乙与丙相对分子质量之比为11:18.则该反应的化学方程式中乙与丙的化学计量之比为( )
已知乙与丙相对分子质量之比为11:18.则该反应的化学方程式中乙与丙的化学计量之比为( )
A.1:2 B.1:1 C.2:1 D.2:3
 wsjl867221年前3
wsjl867221年前3 -
 gdfhjj00 共回答了13个问题
gdfhjj00 共回答了13个问题 |采纳率84.6%选C
根据表格数据可知:
乙反应前的质量为10克,反应后质量为54克,说明乙为生成物,生成乙的质量=54g-10g=44g;
丙反应前的质量为1克,反应后质量为37克,说明丙为生成物,生成丙的质量=37g-1g=36g
丁反应前的质量为25克,反应后质量为9克,说明丁反应物,反应丁的质量=25g-9g=16g
乙+丙=44g+36g=80g
80g-16g=64g
说明甲也是反应物,甲完全反应,反应后甲的质量为0;
根据化学计量数之比=质量比除上各自的相对分子质量得:
该反应的化学方程式中乙与丙的化学计量之比=44g/11:36g/18=2:1
所以选C1年前查看全部
- 在密闭容器中盛有H2、O2、Cl2的混合气体,通过电火花点燃,三种气体恰好完全反应,冷却至室温,所得溶液的质量分数为25
在密闭容器中盛有H2、O2、Cl2的混合气体,通过电火花点燃,三种气体恰好完全反应,冷却至室温,所得溶液的质量分数为25.26%,则容器中H2、O2、Cl2分子个数之比为( )
A. 6:3:1
B. 9:6:1
C. 13:6:1
D. 10:6:1 我怕了行了吧1年前4
我怕了行了吧1年前4 -
 阳光每一天 共回答了19个问题
阳光每一天 共回答了19个问题 |采纳率63.2%解题思路:发生反应H2+Cl2
2HCl、2H2+O2点燃 .
2H2O,恰好完全反应,设生成HCl的物质的量为n1,生成H2O的物质的量为n2,根据质量分数列方程确定n1、n2的关系,根据方程式可知n(H2)=[1/2]n(HCl)+n(H2O),n(O2)=[1/2]n(H2O),n(Cl2)=[1/2]n(HCl),在相同状况下,气体的物质的量之比等于其体积比,据此解答.点燃 .发生反应H2+Cl2
点燃
.
2HCl、2H2+O2
点燃
.
2H2O,
恰好完全反应,设生成HCl的物质的量为n1,生成H2O的物质的量为n2,则:
36.5n1
36.5n1+18n2×100%=25.26%
整理得,n1:n2=1:6,
令n1=1mol,n2=6mol,根据方程式可知n(H2)=[1/2]n(HCl)+n(H2O)=0.5mol+6mol=6.5mol,n(O2)=[1/2]n(H2O)=3mol,n(Cl2)=[1/2]n(HCl)=0.5mol,
所以,n(H2):n(O2):n(Cl2)=6.5mol:3mol:0.5mol=13:6:1
在相同状况下,气体的物质的量之比等于其体积比,所以V(H2):V(O2):V(Cl2)=13:6:1,
故选C.点评:
本题考点: 有关混合物反应的计算;溶液中溶质的质量分数及相关计算.
考点点评: 本题考查混合物的有关计算,根据质量分数确定氯化氢与水的物质的量关系是关键,难度中等,注意利用赋值法简化计算.1年前查看全部
- 氧气和甲烷混合气充入有23.4克过氧化钠的密闭容器中,电火花引燃.反应结束后,容器内于150度压强为0
 天子曰1年前1
天子曰1年前1 -
 stephenysky 共回答了17个问题
stephenysky 共回答了17个问题 |采纳率88.2%甲烷燃烧后生成CO 和H O都可以与Na O 反应,反应完全后容器内压强为0(150°C),说明反应后没有气体物质剩余,根据元素守恒,可以推断产物应该为Na CO 和NaOH(不可能有NaHCO ,因为在150°C时不稳定,会分解),所以
2CH + O + 6Na O == 2Na CO + 8NaOH (根据元素守恒配平)
那么,原混合气体中氧气与甲烷的物质量之比为:
m(O ):m(CH )=1⨉32:2⨉16=1:11年前查看全部
- 甲烷,氧气,过氧化钠在电火花作用下生成什么
 iamadream1年前3
iamadream1年前3 -
 donkey27 共回答了12个问题
donkey27 共回答了12个问题 |采纳率83.3%水和碳酸钠1年前查看全部
- 将一定体积的N2和02的混合气体置于一密闭的容器中经电火花作用后,恢复到原来的温度和压强,若气体体积无变化,则原混合气体
将一定体积的N2和02的混合气体置于一密闭的容器中经电火花作用后,恢复到原来的温度和压强,若气体体积无变化,则原混合气体中,N2和O2的体积比是?
A.1:1 B.<1:1 C.≥1:1 D.任意比
求详解!感激不尽. 我叫大胃1年前2
我叫大胃1年前2 -
 关你叉事F 共回答了17个问题
关你叉事F 共回答了17个问题 |采纳率76.5%A1年前查看全部
- 将02 c2h6 na2o2放入密闭容器中,在150°C时,电火花引发反应后,压强为零,将残留物溶于水,无气体逸出,由此
将02 c2h6 na2o2放入密闭容器中,在150°C时,电火花引发反应后,压强为零,将残留物溶于水,无气体逸出,由此正确的是
A残留物中含有naoh,na3co3和nahco3
B残留物中只含有na2co3
C残留物中含有naoh,na3co3
D原混合物中O2和c3h6的体积比为1:2 爱情的季节1年前1
爱情的季节1年前1 -
 lolita818 共回答了14个问题
lolita818 共回答了14个问题 |采纳率100%貌似是C吧
A中naoh,nahco3 不能共存
B中只含有na2co3 ,则违背了元素守恒,少了H
C最合理,满足所有条件
D中答案需要算一下,还不确定1年前查看全部
- 在一固定的容器中放入适量碳粉和8g氧气,电火花点燃反应后恢复到原来的状态.测得其压强是反应前的1.2倍
在一固定的容器中放入适量碳粉和8g氧气,电火花点燃反应后恢复到原来的状态.测得其压强是反应前的1.2倍
则参加反应碳的质量为---
A.3.6gB.2.4gC.4.4gD.1.2g mengdayezaici1年前2
mengdayezaici1年前2 -
 可以炫耀的美丽 共回答了12个问题
可以炫耀的美丽 共回答了12个问题 |采纳率83.3%炭和氧气生成CO2是压强不变的,但生成CO是
2C + O2 ==== 2CO
由阿佛加德罗定律得,压强比等于物质的量之比.
原来氧气0.25mol 现在气体共0.3mol
设氧气最多反应了Xmol,生成CO
则 2X+(0.25-X)=0.3
X=0.05
所以有0.1molC反应成CO 2.4克
余下的0.15mol氧气和C反应生成CO2
所以一共耗炭 0.25molC 3克 !
选C!1年前查看全部
- 密封容器中,有一定量的H2 O2 Cl2的混合气体,通过电火花点燃,三种气体恰好完全反应,冷却至室温后,所得盐酸的质量分
密封容器中,有一定量的H2 O2 Cl2的混合气体,通过电火花点燃,三种气体恰好完全反应,冷却至室温后,所得盐酸的质量分数为25.26% 则容器中原有的H2 O2 Cl2的物质的量之比为 13:6:1
怎么算的啊 windboy1431年前1
windboy1431年前1 -
 cyy850917 共回答了11个问题
cyy850917 共回答了11个问题 |采纳率90.9%设混合物总重量a克:
HCl:0.2526a 克
H2O:0.7474a 克
Cl2:(35.5/36.5)*0.2526a=0.246a 克
O2:(16/18)*0.7474a=0.664a 克
H2:a-0.246a-0.664a=0.09a 克
(0.09a/2):(0.664a/32):(0.246a/71)=13:6:11年前查看全部
- 将氧气,甲烷,过氧化钠放入密闭容器中,在150度条件下电火花引发反应后,容器内压强为零.我想知道这个反应真的发生的了么?
 诺诺胖猪1年前1
诺诺胖猪1年前1 -
 海航办公室主任 共回答了22个问题
海航办公室主任 共回答了22个问题 |采纳率95.5%肯定发生了.容器内反应物有气体,肯定有压强,反应后压强为0,则气体全部反应了1年前查看全部
- 在密闭容器中盛有H2、O2、Cl2三种气体,电火花点燃后,三种气体都正好反应完全,冷
在密闭容器中盛有H2、O2、Cl2三种气体,电火花点燃后,三种气体都正好反应完全,冷
在密闭容器中盛有H2、O2、Cl2三种气体,电火花点燃后,三种气体都正好反应完全,冷却到室温,所得溶液得质量分数为33.4%,则原混合气体中三者得物质的量之比为 吖芝吖左391年前1
吖芝吖左391年前1 -
 飘浮在水中的浮萍 共回答了18个问题
飘浮在水中的浮萍 共回答了18个问题 |采纳率88.9%溶液为盐酸.
设取100克溶液,其中含HCl33.4克,含H2O66.6克,则含Cl元素33.4*35.5/36.5=32.5克;含O元素66.6*16/18=59.2克;含H元素=100-32.5-59.2=8.3克.
原混合物含H2=8.3/2=4.15摩尔、O2=59.2/32=1.85摩尔、Cl2=32.5/71=0.46摩尔,原混合气体中三者得物质的量之比为4.15:1.85:0.46=9:4:1.1年前查看全部
- CO和O2的混合aL,在密闭容器中用电火花点燃,使之充分反应,恢复到原状态,气体体积变为bL,则原混合气体中CO的体积可
CO和O2的混合aL,
在密闭容器中用电火花点燃,使之充分反应,恢复到原状态,气体体积变为bL,则原混合气体中CO的体积可能为
A.(b-a)L B.(a-b)L
C.2(a-b)L D.(2b-a)L 雪候鸟hby1年前2
雪候鸟hby1年前2 -
 zzq4714 共回答了24个问题
zzq4714 共回答了24个问题 |采纳率87.5%2CO+O2=2CO2
即是3个体积的气体燃烧变成2个体积的气体.
减少了1个体积的气体.
题中减少的体积为a-b,则燃烧了的CO的量为2(a-b),总共的CO的体积大于等于2(a-b),所以选c.
扩展思维:d也是可能的.可能答案没有这个,你跟老师讨论讨论,d是绝对也行的1年前查看全部
- 电火花成型加工的工具电极的相对损耗率与哪些因素有关
 饮血机1年前1
饮血机1年前1 -
 荏苒一叶丘 共回答了15个问题
荏苒一叶丘 共回答了15个问题 |采纳率80%电火花加工的质量和加工效率不仅与极性选择有关,还与电规准(即电加工的主要参数)、工作液、工件、电极的材料、放电间隙等因素有关.1年前查看全部
- 在一密闭容器中,盛放a、b、c三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
在一密闭容器中,盛放a、b、c三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
关于此反应,下列说法正确的是( )物质 a b c 新物质d 反应前物质的质量(g) 30 30 30 0 反应后物质的质量(g) 待测 33 0 22
A. c物质中所含有的元素种类是a、b、d三种物质中所有元素种类之和
B. 变化后待测的a质量为5g
C. 该变化的基本反应类型是分解反应
D. a物质有不可能是单质 chao99711年前2
chao99711年前2 -
 tt3202 共回答了17个问题
tt3202 共回答了17个问题 |采纳率88.2%解题思路:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.计算出变化后待测的a质量;然后根据反应类型的特征确定反应类型;根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.确定A的正误;根据分解反应的概念确定C的正误.根据质量守恒定律可知,变化后待测的a质量=(30+30+30)-(33+22)=35g.由图表数据可知,反应过程中c物质完全反应,a、b物质质量增加,还生成了新物质d.故此反应符合“一变多”,则属于分解反应,化学方程式为:c=a+b+d.
A、由分析可知:c物质中所含有的元素种类是a、b、d三种物质中所有元素种类之和,故A正确;
B、计算可知,变化后待测的a质量为35g,故B错误;
C、由分析可知:该变化的基本反应类型是分解反应,故C正确;
D、分解反应的产物可能是单质,也可能是化合物,在这个题目中同样是没有限制的.故D错误.
故选:A、C.点评:
本题考点: 质量守恒定律及其应用;单质和化合物的判别;反应类型的判定.
考点点评: 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 电弧和电火花的区别物理本质是什么?电火花的物理本质好像电弧是电火花的聚集
 王晴霏1年前1
王晴霏1年前1 -
 echoliujie 共回答了14个问题
echoliujie 共回答了14个问题 |采纳率100%火化得碰上
电弧是有一段距离的1年前查看全部
- (2011•河西区一模)在一个密闭的钢筒内有甲、乙、丙、丁四种物质,在电火花作用下,发生充分反应,测得反应前后各物质的质
(2011•河西区一模)在一个密闭的钢筒内有甲、乙、丙、丁四种物质,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
已知甲的相对分子质量为丁的2倍,则该反应的化学方程式中甲与丁的化学计量数之比为( )甲 乙 丙 丁 反应前质量/g 64 10 1 25 反应后质量/g 54 37 9
A.1:2
B.1:1
C.2:1
D.2:3 求知小生1年前1
求知小生1年前1 -
 allmoneygomyhome 共回答了15个问题
allmoneygomyhome 共回答了15个问题 |采纳率100%解题思路:根据质量守恒定律,由物质质量的增减可确定反应物和生成物;由增减量的多少可确定反应物和生成物的质量关系,再结合甲、丁的相对分子质量关系得出本题答案.根据质量守恒定律,由表中乙、丙质量增加,可确定乙、丙为生成物,共增加了(54-10)g+(37-1)g=80g,
丁减少了(25-9)g=16g,减少的质量还差(80-16)g=64g,由此可知64g甲完全反应无剩余.即甲、丁反应时的质量比为64g:16g=4:1.
设该反应的化学方程式中甲与丁的化学计量数的比为m:n,又知甲的相对分子质量为丁的2倍,则2m:n=4:1,解得m:n=2:1.
故选C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 本题主要考查质量守恒定律,通过反应中物质的质量变化确定了反应物和生成物,再结合物质的相对分子质量关系,得出反应中物质的化学计量数之比,从而加深了对质量守恒定律的理解和应用.1年前查看全部
- 火石打出来的火花和电火花是同一种东西吗?
火石打出来的火花和电火花是同一种东西吗?
我只问结果不问过程 我是gg我鸟谁1年前5
我是gg我鸟谁1年前5 -
 s不懂 共回答了18个问题
s不懂 共回答了18个问题 |采纳率100%只要是火花就是一样的,都是气体电离发出的光
他俩都是产生高温的过程1年前查看全部
- 电子打点计时器和电火花打点记时器哪个误差大
 michels1年前1
michels1年前1 -
 sztaotao 共回答了11个问题
sztaotao 共回答了11个问题 |采纳率90.9%由于电磁打点计时器是撞针撞击纸带计时,因此电磁打点计时器纸带受到的阻力比电火花打点计时器纸带受到的阻力大,误差也就大些.1年前查看全部
- 某同学设计了一个“探究加速度与物体所受合力F及质量m的关系”实验.如图(a)为实验装置简图,A为小车,B为电火花打点计时
某同学设计了一个“探究加速度与物体所受合力F及质量m的关系”实验.如图(a)为实验装置简图,A为小车,B为电火花打点计时器,C为装有砝码的小桶,D为一端带有定滑轮的长方形木板,实验中认为细绳对小车拉力F等于砝码和小桶的总重量,小车运动加速度a可用纸带上点求得.
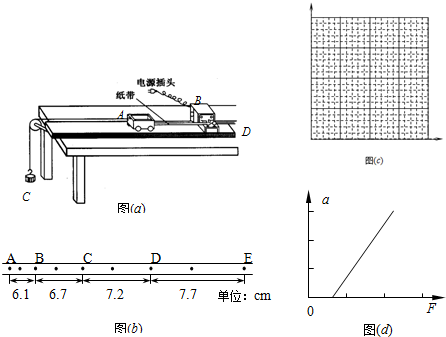
(1)图(b)为某次实验得到的纸带,根据纸带可求出小车的加速度大小为______m/s2.(保留两位有效数字)
(2)在“探究加速度与质量的关系”时,保持砝码和小桶质量不变,改变小车质量m,分别得到小车加速度a与质量m数据如表:
①请将上表中所有空格补全.次数 1 2 3 4 5 6 7 8 9 小车加速度a/m•s-2 1.98 1.72 1.48 1.25 1.00 0.75 0.48 0.50 0.30 小车质量m/kg 0.25 0.29 0.33 0.40 0.50 0.71 0.75 1.00 1.67 4.00 3.45 3.03 2.00 1.41 1.00 0.60
②根据表数据,为直观反映F不变时a与m的关系,请在图(c)方格坐标纸中选择恰当物理量建立坐标系,并作出图线.
③在“探究加速度与力的关系”时,保持小车的质量不变,改变小桶中砝码的质量,该同学根据实验数据作出了加速度a与合力F图线如图(d),试分析图线不通过坐标原点的原因.
答:______. 林伯士1年前1
林伯士1年前1 -
 不羁 共回答了12个问题
不羁 共回答了12个问题 |采纳率75%解题思路:(1)根据△x=aT2求出纸带的加速度.(2)为研究a与m的关系,作a与1m的关系图线,注意选取好标度.(3)图线不通过坐标原点,当F为某一值时,加速度为零,知平衡摩擦力不足.(1)从纸带上看出,相邻两点间位移之差为一恒量,△x=0.51cm,根据△x=aT2得,a=
△x
T2=
0.0051
0.042m/s2=3.2m/s2.
(2)第三行的数据是质量的倒数,则第四次对应的数据为2.50,第7次对应的数据为1.33,
根据表格数据,通过描点,作出图线,如下图所示.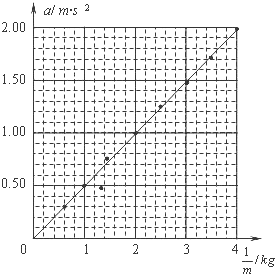
(3)图线不通过坐标原点,F不为零时,加速度仍为零,知实验前未平衡摩擦力或平衡摩擦力不充分.
故答案为:(1)3.2;(2)2.50;1.33;如图所示;没有平衡摩擦力或摩擦力平衡不足点评:
本题考点: 探究加速度与物体质量、物体受力的关系.
考点点评: 解决本题的关键会从纸带上求瞬时速度和加速度,以及在作图时注意,偏离比较远的点可以舍去.1年前查看全部
- 已知同温同压下,相同体积的任何气体都含有相同数目的分子在一个密闭容器中盛有H2 O2 CL2组成的混合气体.通过电火花引
已知同温同压下,相同体积的任何气体都含有相同数目的分子在一个密闭容器中盛有H2 O2 CL2组成的混合气体.通过电火花引爆后,三种气体恰好完全反应.经充分冷却后,所得溶液中溶质的质量分数为33.4%,则原混合气体中H2 O2 CL2分子数目简单整数比是?(氢气和氯气点燃生成氯化氢气体,氯化氢气体易容与水)
 emilyxu1年前1
emilyxu1年前1 -
 蟾树烟然 共回答了19个问题
蟾树烟然 共回答了19个问题 |采纳率84.2%假设氧气物质的量为x,氯气物质的量为y
2H2+O2=2H2O H2+Cl2=2HCl
2x x 2x y y 2y 36.5*2y/(36.5*2y+18*2x)=33.4%
解出 H2 O2 CL2之比即(2x+y):x:y=9:4:11年前查看全部
- (2011•邵阳)2010年11月15日,上海静安区高层住宅发生火灾,原因是电焊工违章操作产生的电火花,引燃了事故现场使
(2011•邵阳)2010年11月15日,上海静安区高层住宅发生火灾,原因是电焊工违章操作产生的电火花,引燃了事故现场使用的大量尼龙网、聚氨酯泡沫塑料等易燃材料.就此事件回答下列问题:
(1)聚氨酯泡沫塑料属于______(填“天然”或“合成”)有机高分子材料.
(2)溅落的电火花在这场火灾中所起的作用是______(填序号).
A、提供氧气 B、使温度达到可燃物的着火点 C、提供可燃物
(3)聚氨酯泡沫塑料燃烧产生的烟气中,含有多种对人体有害的气体,写出其中一种能与血红蛋白结合的有毒气体的化学式______.
(4)废弃的聚氨酯泡沫塑料会给环境带来______. 121青菜1年前1
121青菜1年前1 -
 xhhy12 共回答了22个问题
xhhy12 共回答了22个问题 |采纳率95.5%解题思路:(1)聚氨酯属于有机合成材料,这种材料有可燃性.
(2)电火花起到了点燃的作用,也就是提供了物质燃烧时的热量.
(3)CO是能与血红蛋白结合的有毒气体.
(4)废弃的聚氨酯泡沫塑料任意丢弃会造成白色污染.(1)聚氨酯属于有机合成材料,这种材料有可燃性;
(2)电火花起到了点燃聚氨酯的作用,也就是提供了其燃烧时的热量;
(3)不完全燃烧会生成一种能与血红蛋白结合的有毒气体CO;
(4)一聚氨酯泡沫塑料难于降解,废弃的聚氨酯泡沫塑料任意丢弃会造成白色污染.
故答案为:(1)合成;(2)B;(3)CO;(4)白色污染.点评:
本题考点: 有机高分子材料的分类及鉴别;化学式的书写及意义;燃烧与燃烧的条件;白色污染与防治.
考点点评: 此题是对生活中化学的考查,利用题干提供的信息结合相关的化学知识是解题的关键.1年前查看全部
- (2010•南昌二模)向装有足量K2O2的密闭容器中充入20g一氧化碳、氧气混合气体,并且电火花引燃使其充分反应,测得固
(2010•南昌二模)向装有足量K2O2的密闭容器中充入20g一氧化碳、氧气混合气体,并且电火花引燃使其充分反应,测得固体质量增加9g,则原混合气体中氧气的质量分数为( )
A.33.3%
B.55%
C.40%
D.36% zjwl20061年前1
zjwl20061年前1 -
 孚游 共回答了12个问题
孚游 共回答了12个问题 |采纳率83.3%解题思路:CO与氧气反应:2CO+O2
2CO2,一氧化碳与二氧化碳物质的量相等,生成的CO2再与K2O2反应:2CO2+2K2O2=2K2CO3+O2,质量增重△m=2K2CO3-2K2O2=2CO,可知反应后固体质量增加量为CO的质量,据此计算计算;点燃 .CO与氧气反应:2CO+O2
点燃
.
2CO2,一氧化碳与二氧化碳物质的量相等,生成的CO2再与K2O2反应:2CO2+2K2O2=2K2CO3+O2,质量增重△m=2K2CO3-2K2O2=2CO,可知反应后固体质量增加量为CO的质量,故混合气体中CO的质量为9g,氧气的质量为20g-9g=11g,则氧气的质量分数=[11g/20g]×100%=55%,故选B.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题考查混合物的计算,难度中等,侧重对学生思维能力的考查,关键是根据化学方程式从质量守恒的角度判断固体增重为CO的质量.1年前查看全部
- 电火花极性效应产生的根本原因?窄脉宽和宽脉冲放电时各采用哪种极性,并说明理由.
电火花极性效应产生的根本原因?窄脉宽和宽脉冲放电时各采用哪种极性,并说明理由.
书上找不到 gemini_F911年前1
gemini_F911年前1 -
 weigd525 共回答了14个问题
weigd525 共回答了14个问题 |采纳率85.7%电火花加工时,无论是正极还是负极都会受到不同程度的电腐蚀.即使两个电极材料相同也往往会出现正,负两极的蚀除速度不一样,这种现象就是极性效应.在生产中,把工件接脉冲电源正极时的加工称为正极性加工,反之则称为负极性加工.短脉宽精加工选用正极性加工,长脉宽加工时,选用负极性加工.理由就是为了减小电极损耗1年前查看全部
- 1 .在一个密闭的钢筒内有A,B,C,D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反应前后个物质的质量如下
1 .在一个密闭的钢筒内有A,B,C,D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反应前后个物质的质量如下:
物质 A B C D
反应前质量(g) 4 10 1 25
反应后质量(g)(未测) 21 10 9
若A的分子量为n,D的分子量为2n,则该反应中A与D的化学计量数之比为______.
2.现取2.3g有机物在足量的氧气中充分燃烧,生成4.4gCO2和2.7gH2O,判断正误.
A.分子中C.H的原子个数比为2:5
B.分子中C.H.O的元素质量比为12:3:8.
3.将铁粉加入含有铜离子和银离子的溶液中,充分反应后加入盐酸,发现无气泡产生,但却有白色沉淀产生,则加入盐酸前的物质中含有____.
A.铜离子、银离子、铁离子、银单质 B.铁离子、银离子、铜离子、铜单质
C.铜单质、银单质、银离子、铁离子 D.铜离子、银离子、铁单质、铁离子
4.某样品含有氢氧化钾、碳酸钾和水三种物质.室温下,向该样品中加入浓度为14.6%的稀盐酸100g,恰好完全反应得到中性溶液,蒸干该溶液得到的固体质量为_____.
A.74.5g B.29.8g C.10g D.7.45g
5.下图是某元素的原子结构示意图,下列对该元素的认识正确的是_____.
A.该元素属于金属元素
B.该元素的原子在化学反应中容易失电子
C.该元素的原子核外电子总数为18
D.该元素位于元素周期表的第四周期第VIA族
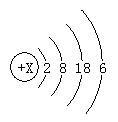
 xudiok1122111年前3
xudiok1122111年前3 -
 家居猫 共回答了22个问题
家居猫 共回答了22个问题 |采纳率86.4%1:2
错 对
A
B
D1年前查看全部
大家在问
- 1《庄子.天下篇》中写道:“一尺之棰,日取其半,万世不竭”意思是:一根一尺的木棍,如果每天截取它的一半,永远也取不完,如图
- 2英语翻译产品介绍:本品为低噪音,交直流两用可充电增氧泵,独创气量调节,间歇充氧功能.使用说明:气量调节:将旋纽由左向右旋
- 350%X-1/3+1/2=1(这是X,不是乘号),1/4X+1/8X=2除1/2(这是X,不是乘号),
- 47分之4除(5分之1加14分之5除7分之5)
- 5(2013•杭州模拟)如图是某同学用于计算S=sin1+sin2+sin3+…+sin2012值的程序框图,则在判断框中
- 6物理 半径为R的光滑圆形轨道安置在一竖直平面上,左侧连接一个光滑的弧形轨道,
- 7( 填《水浒传》 中的人名或官名) 风雪山神庙 陆虞候火烧草料场(水浒传)
- 8《冬阳 童年 骆驼队》练习摘录课文中描写老北京特点的句子._______________________________
- 9英语翻译Ever since the accelerated development of human civiliza
- 10Have you ever notice the sadness and tears of others*翻译成中文什么
- 11一堆煤重45吨,一辆卡车要十小时才能运完.三分之四小时运走多少吨?
- 12高一下期物理有哪些重点知识点啊,求详解
- 13设x∈(0.π/2),则"xsin^2x
- 14"我很好 "他说______"谢谢你的关心." 在横线上加标点
- 15如果要用电流表测一个灯泡的电流,哪个前?哪个后?