取暖片(Fe氧化)中的活性炭有什么作用?
 xmmiracle2022-10-04 11:39:541条回答
xmmiracle2022-10-04 11:39:541条回答如题

已提交,审核后显示!提交回复
共1条回复
 zb8765 共回答了19个问题
zb8765 共回答了19个问题 |采纳率84.2%- 活性炭是很好的干燥剂,性质稳定.
- 1年前
相关推荐
- 取暖片的主要成分为铁粉 氯化钠 水 活性炭,其发热原理是利用了铁生锈.问其中氯化钠的作用是什么?
 caroly1年前1
caroly1年前1 -
 lily蔡 共回答了24个问题
lily蔡 共回答了24个问题 |采纳率87.5%电解质溶液,容易发生腐蚀1年前查看全部
- 人类生活离不开金属。(1)铁是生活中常用的金属。下图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性
人类生活离不开金属。
(1)铁是生活中常用的金属。下图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。
①发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是 。
应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应。
A.Fe 和CuSO 4 溶液 B.Mg和MnSO 4 溶液 C.Al和FeSO 4 溶液
(2)写出Fe 和CuSO 4 溶液反应的化学方程式 。
(3)Al、Fe、Mg 、Cu四种金属的活动性由强到弱的顺序 。 1顆糖2穜味1年前1
1顆糖2穜味1年前1 -
 蔷薇草228 共回答了24个问题
蔷薇草228 共回答了24个问题 |采纳率83.3%(1)①水;氧气
②加速铁粉生锈,更快地放出热量
(2)Fe+ CuSO 4 === FeSO 4 + Cu
(3)Mg、Al、Fe、Cu1年前查看全部
- (2012•湛江)天冷时,可以在衣服外贴上一次性的“取暖片”.其发热原理是利用铁生锈时会放热.发热剂的主要成分有铁粉、活
(2012•湛江)天冷时,可以在衣服外贴上一次性的“取暖片”.其发热原理是利用铁生锈时会放热.发热剂的主要成分有铁粉、活性炭、食盐等.以下是分离这三种物质的实验方案:
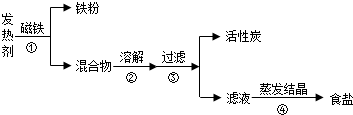
(1)第③步时,发现滤液浑浊,可能的原因是______(填字母)
A、滤纸破损 B、液面始终低于滤纸的边缘
C、烧杯不干净 D、滤纸的边缘低于漏斗的边缘
(2)第③步后,用蒸馏水洗涤活性炭2~3次.为了检验活性炭中是否还含有未洗净的食盐,可取少量最后一次洗涤溶液于试管中,往其中滴加硝酸银溶液,观察是否有白色沉淀生成.请写出食盐与硝酸银溶液反应的化学方程式______.
(3)第④步时,用玻璃棒搅拌的作用是______. 花瓣雨_谎言1年前1
花瓣雨_谎言1年前1 -
 苦海727 共回答了18个问题
苦海727 共回答了18个问题 |采纳率100%解题思路:(1)运用A、滤纸破损未起到过滤的作用,滤液会浑浊.B、液面始终低于滤纸的边缘,未过滤的液体不会不经滤纸就流下,不会浑浊.C、烧杯不干净滤液也会浑浊. D、滤纸的边缘低于漏斗的边缘,正确操作,滤液不会浑浊分析解答.
(2)运用氯化钠和硝酸银反应生成氯化银白色沉淀和硝酸钠分析.
(3)运用蒸发操作中用玻璃棒不断搅拌的作用有两个,一是加快蒸发,二是防止局部受热造成液滴飞溅分析.(1)A、滤纸破损未起到过滤的作用,滤液会浑浊.
B、液面始终低于滤纸的边缘,未过滤的液体不会不经滤纸就流下,不会浑浊.
C、烧杯不干净滤液也会浑浊.
D、滤纸的边缘低于漏斗的边缘,正确操作,滤液不会浑浊.
故选AC.
(2)氯化钠和硝酸银反应生成氯化银白色沉淀和硝酸钠,故答案:NaCl+AgNO3=AgCl↓+NaNO3.
(3)蒸发操作中用玻璃棒不断搅拌的作用有两个,一是加快蒸发,二是防止局部受热造成液滴飞溅分析,故答案:加快蒸发,防止局部受热造成液滴飞溅.点评:
本题考点: 混合物的分离方法;过滤的原理、方法及其应用;金属的物理性质及用途;盐的化学性质.
考点点评: 过滤液体时,要注意一贴二低三靠的原则.即一贴:用少量水润湿的滤纸要紧贴漏斗壁,二低:滤纸边缘低于漏斗边缘、滤液低于滤纸边缘,三靠:烧杯紧靠玻璃棒、玻璃棒靠在三层滤纸上、漏斗下端口紧靠烧杯内壁.蒸发时玻璃棒不断搅拌的作用有两个,一是加快蒸发,二是防止局部受热造成液滴飞溅.1年前查看全部
- 人类生活离不开金属。 (1)铁是生活中常用的金属。下图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分
人类生活离不开金属。
(1)铁是生活中常用的金属。下图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热 。
①发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是 。
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应。 A.Fe 和CuSO 4 溶液 B.Mg和MnSO 4 溶液 C.Mn和FeSO 4 溶液
①写出Fe 和CuSO 4 溶液反应的化学方程式 。
②Mn、Fe、Mg 、Cu四种金属的活动性由强到弱的顺序 。 刚爱西1年前1
刚爱西1年前1 -
 我爱饭炒蛋 共回答了24个问题
我爱饭炒蛋 共回答了24个问题 |采纳率91.7%(1)①水;氧气 ②加速铁粉生锈,更快地放出热量 (2)①Fe+CuSO 4 ===FeSO 4 +Cu ②Mg Mn Fe Cu ...1年前查看全部
- (一)人类生活离不开金属.(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉
 (一)人类生活离不开金属.
(一)人类生活离不开金属.
(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
①发热剂需接触到空气才会发热,原因是铁要与______、______等物质共同作用才会生锈.
②推测发热剂成分中氯化钠的作用是______.
(2)应用金属活动性顺序能帮助我们进一步学习金属性质.已知下列各组物质间均能发生置换反应.
A.Fe 和CuSO4溶液B.Mg和MnSO4溶液C.Mn和FeSO4溶液
①写出Fe 和CuSO4溶液反应的化学方程式______.
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序______.
(二)阅读材料,回答问题.
材料一:2009年1月,某市酒吧发生一起特大火灾.该事故的起因是几个年轻人在酒吧内燃放烟花,引燃聚氨酯泡沫塑料天花板,聚氨酯泡沫塑料燃烧产生大量有毒烟气,造成人员中毒伤亡.
材料二:氢氧化镁是一种新型的阻燃剂.当温度达到380℃时,氢氧化镁开始分解出水蒸气,同时生成耐高温的氧化镁固体.利用氢氧化镁这一性质,将它添加在塑料等易燃性材料中能起阻燃作用.
(1)聚氨酯泡沫塑料属于______材料(填“有机”或“无机”).
请回答聚氨酯泡沫塑料的一点化学性质______.
(2)燃着的烟花在引发这场火灾中所起的作用是______.(填标号)
A.提供氧气B.使可燃物的温度达到着火点C.提供可燃物
(3)根据灭火原理初步分析氢氧化镁能作阻燃剂的原因______.(答一点)
氢氧化镁受热分解的化学方程式为Mg(OH)2
MgO+H2O△ .Mg(OH)2.
MgO+H2O△ . zouabojun1年前1
zouabojun1年前1 -
 贾妹儿 共回答了23个问题
贾妹儿 共回答了23个问题 |采纳率95.7%解题思路:铁与氧气和水充分接触时容易生锈,盐能够加快铁的生锈速率,根据金属活动性顺序可判断物质之间能否发生化学反应,含有碳元素的化合物属于有机物,有机物一般容易燃烧,根据反应物和生成物及其质量守恒定律可以书写化学方程式.(一)人类生活离不开金属.
(1)①发热剂需接触到空气才会发热,原因是铁要与水、氧气等物质共同作用才会生锈.故填:水;氧气.
②推测发热剂成分中氯化钠的作用是加速铁粉生锈,更快地放出热量.故填:加速铁粉生锈,更快地放出热量.
(2)①Fe 和CuSO4溶液反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
②Fe能和CuSO4溶液反应说明铁比铜活泼,Mg和MnSO4溶液能反应说明镁比锰活泼,Mn和FeSO4溶液能反应说明锰比铁活泼.
所以Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序Mg、Mn、Fe、Cu.
(二)阅读材料,回答问题.
(1)聚氨酯泡沫塑料属于有机高分子材料.故填:有机.
聚氨酯泡沫塑料容易燃烧.故填:易燃烧.
(2)燃着的烟花在引发这场火灾中所起的作用是:使可燃物的温度达到着火点.故填:B.
(3)氢氧化镁能作阻燃剂的原因是:氢氧化镁高温分解出水蒸气带走热量,使温度低于着火点.
氢氧化镁受热分解的化学方程式为:Mg(OH)2
△
.
MgO+H2O点评:
本题考点: 金属锈蚀的条件及其防护;金属活动性顺序及其应用;有机物与无机物的区别;化学性质与物理性质的差别及应用;物质发生化学变化时的能量变化;书写化学方程式、文字表达式、电离方程式;燃烧与燃烧的条件;灭火的原理和方法.
考点点评: 解答本题的关键是要掌握化学方程式的书写方法、物质的分类方法、金属的活动性顺序等方面的知识,只有这样才能对问题做出正确的判断.1年前查看全部
- (1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其
 (1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
①发热剂需接触到空气才会发热,原因是铁要与______、______等物质共同作用才会生锈.防止铁制品锈蚀的方法______.
②推测发热剂成分中氯化钠的作用是______.
(2)应用金属活动性顺序能帮助我们进一步学习金属性质.
已知下列各组物质间均能发生置换反应.A.Fe 和CuSO4 溶液B.Mg和MnSO4 溶液C.Mn和FeSO4 溶液
①写出Fe 和CuSO4 溶液反应的化学方程式______,工业上用赤铁矿炼铁的原理的化学方程式Fe2O3+3CO
2Fe+3CO2高温 .Fe2O3+3CO.
2Fe+3CO2高温 .
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序______. 动感超人BBB1年前1
动感超人BBB1年前1 -
 521bs 共回答了19个问题
521bs 共回答了19个问题 |采纳率89.5%解题思路:(1)①铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈.
②盐存在时,会使铁生锈的速度加快.
(2)在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此根据各组物质间的反应,可确定四种金属活动性由强到弱的顺序.(1)①发热剂需接触到空气才会发热,原因是铁要与氧气、水等物质共同作用才会生锈.
为了防止钢铁的锈蚀,人们常采用保持铁制品表面干燥与洁净、在其表面刷油漆或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水.
②盐存在时,会使铁生锈的速度加快,故发热剂成分中氯化钠的作用是加速铁粉生锈,更快地放出热量.
(2)①铁和CuSO4溶液反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.
工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
高温
.
2Fe+3CO2.
②在金属活动性顺序中,排在前面的金属能够把排在后面的金属从它的盐溶液中置换出来,由A可知,铁的活动性比铜强;由B可知,镁的活动性比锰强;由C可知,锰的活动性比铁强,Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序为:Mg、Mn、Fe、Cu.
故答案为:(1)①氧气;水;保持铁制品表面干燥与洁净等;②加速铁粉生锈,更快地放出热量;(2)①Fe+CuSO4═Cu+FeSO4;Fe2O3+3CO
高温
.
2Fe+3CO2;②Mg、Mn、Fe、Cu.点评:
本题考点: 金属锈蚀的条件及其防护;金属活动性顺序及其应用.
考点点评: 本题难度不大,考查铁锈蚀的条件、金属活动性应用等,掌握“反应则活泼、不反应则不活泼”是正确解答确定金属活动性顺序题目的关键.1年前查看全部
大家在问
- 1we are delighted (that) you can come. 中的 that 引导的是什么句子?
- 2(2013•广西)平面镜成正立的______(选填“实”或“虚”)像,像的大小与物体的大小______(选填“相等”或“
- 3欲戴皇冠,必承其重 用英语怎么讲
- 4《无言的父爱》按什么顺序写的,通过叙述了什么,表达了作者什么的思想感情.
- 5题中两图分别为一列沿x轴方向传播的简谐横波在t=0时的波形图和这列波中质点P的振动图线,
- 6设随机变量X和Y的相关系数为0.9,若Z=X-0.4,则Y与Z的相关系数为______.
- 7英语自我介绍(最好把中文对照也写出来)10句左右就可以了.简单一点的.对了我喜欢游泳,打羽毛球,要写进去,还有要写到父母
- 8(2008•汕头二模)下列哪些变异的性状是不可以遗传给后代的?( )
- 9谁会这道题:阅读文章,选择正确的
- 10正比例和反比例的知识点怎么回事
- 11某校学生会在“社会实践”活动中组织学生进行社会调查,并组织评委会对学生写出的调查报告进行了评比.学生会随机抽取了部分评比
- 12用英语翻译她比较喜欢种花而不是植树
- 13已知函数f(x)=ax-1+4(a>0,a≠1)的反函数y=f-1(x)的图象经过一个定点,这个定点的坐标为( )
- 14“H”是读“诶去”还是“诶尺”?
- 15莲花出淤泥而不染的秘密什么叫莲花效应
