含杀菌剂的污水处理方法最近遇到一个含杀菌剂的污水 请教各位需要哪种处理方法 急
 abusww2022-10-04 11:39:541条回答
abusww2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 jusanliangyiyi 共回答了23个问题
jusanliangyiyi 共回答了23个问题 |采纳率95.7%- 先电化学或高级氧化处理后,再生化.
- 1年前
相关推荐
- 硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如图所示:
硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如图所示: 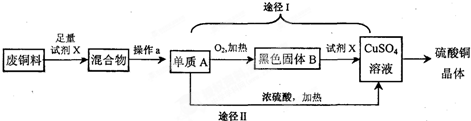
(1)操作a的名称是:______;
(2)已知:Cu+2H 2 SO 4 (浓)=CuSO 4 +SO 2 ↑+2H 2 O.则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;②______;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为:______. 凌思心1年前1
凌思心1年前1 -
 smzyy 共回答了13个问题
smzyy 共回答了13个问题 |采纳率92.3%(1)黑色固体为金属铜在加热条件下与氧气化合产生的氧化铜;操作a为过滤操作,把不与稀硫酸反应的金属铜与硫酸亚铁溶液分离开来;所以操作a的名称是过滤;
(2)已知:Cu+2H 2 SO 4 (浓)=CuSO 4 +SO 2 ↑+2H 2 O.根据图框,反应②,加热条件下金属铜与氧气化合生成氧化铜;反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水,所以方程式是:CuO+H 2 SO 4 =CuSO 4 +H 2 O;则可知途径I与途径II相比,途径II产生的二氧化硫既会污染环境,又使硫酸不能全部转化为产品硫酸铜而形成浪费;即其优点体现在:①不产生二氧化硫有毒气体,不会污染空气;②硫酸中的硫酸根完全转化到产物硫酸铜中,硫酸的利用率高;
(3)将废铜料投入硫酸铜溶液中充分搅拌,铁和硫酸铜溶液反应,则发生反应的化学方程式为:Fe+CuSO 4 =FeSO 4 +Cu.
故答案为:
(1)过滤;
(2)硫酸中的硫酸根完全转化到产物硫酸铜中,硫酸的利用率高;
(3)Fe+CuSO 4 =FeSO 4 +Cu.1年前查看全部
- (2010•汕头)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程.
(2010•汕头)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程.
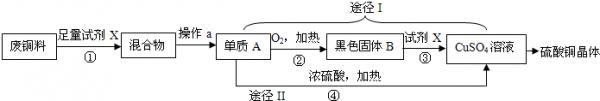
(1)B的化学式为______,操作a的名称是______.
(2)②的反应基本类型为______;反应①、③的化学方程式分别为①______;③______.
(3)已知:Cu+2H2SO4 (浓)
CuSO4+SO2↑+2H2O.从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和______.△ . 桥风儿1年前1
桥风儿1年前1 -
 古典私人 共回答了20个问题
古典私人 共回答了20个问题 |采纳率100%解题思路:(1)根据流程图可推断,黑色固体B应是铜在加热条件下与氧气反应的产物;单质A为不与试剂X稀硫酸反应的铜,因此,操作a是把不溶性固体和溶液分离开的操作;
(2)反应②为金属单质铜与氧气在加热条件下所发生的反应,生成黑色固体氧化铜,两种物质生成一种物质的反应;反应①为使用稀硫酸把铁反应而除去的置换反应;反应③则应是黑色固体氧化铜与稀硫酸得到硫酸而发生的复分解反应;
(3)途径II中产生二氧化硫气体不但会产生污染,而且会使部分硫酸因转化成二氧化硫而造成转化率不高,(1)黑色固体为金属铜在加热条件下与氧气化合产生的氧化铜;操作a为过滤操作,把不与稀硫酸反应的金属铜与硫酸亚铁溶液分离开来;
故答案为:CuO;过滤;
(2)反应②,加热条件下金属铜与氧气化合生成氧化铜;反应①则是铁与稀硫酸反应生成硫酸亚铁和氢气;反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水;
故答案为:化合反应;Fe+H2SO4=FeSO4+H2↑;CuO+H2SO4=CuSO4+H2O;
(3)途径II产生的二氧化硫既会污染环境,又使硫酸不能全部转化为产品硫酸铜而形成浪费;
故答案为:硫酸的利用率高.点评:
本题考点: 物质的相互转化和制备;化学实验方案设计与评价;过滤的原理、方法及其应用;金属的回收利用及其重要性;反应类型的判定.
考点点评: 根据生产流程图,正确理解每个过程在生产中的作用,从而达到全面掌握生产过程的目的,为解答问题做足准备.1年前查看全部
- (2012•高新区一模)胆矾常用作农业和渔业的杀虫剂、杀菌剂.某课外研究小组用废铜料(含铁),通过不同的化学反应制取胆矾
(2012•高新区一模)胆矾常用作农业和渔业的杀虫剂、杀菌剂.某课外研究小组用废铜料(含铁),通过不同的化学反应制取胆矾(CuSO4•5H2O).其设计的实验过程为:
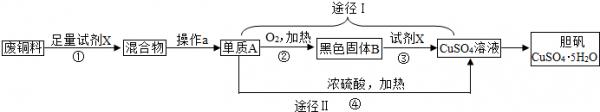
(1)波尔多液是由胆矾、生石灰(或熟石灰)生石灰(或熟石灰)和水配制成的天蓝色胶状悬浊液,有杀菌作用.
(2)反应①、③的化学方程式分别为①Fe+H2SO4═FeSO4+H2↑Fe+H2SO4═FeSO4+H2↑;③CuO+H2SO4═CuSO4+H2OCuO+H2SO4═CuSO4+H2O.
(3)由CuSO4溶液获得CuSO4•5H2O晶体,需要经过蒸发操作,该步骤所需仪器除酒精灯、三脚架以外还有蒸发皿、玻璃棒蒸发皿、玻璃棒.
(4)已知:途径II发生的化学反应是:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O.从环保和经济的角度对比分析途径I、II,途径I的优点有:不产生有害气体和硫酸的利用率高硫酸的利用率高.△ . .  panyongren1年前1
panyongren1年前1 -
 在网上流浪 共回答了22个问题
在网上流浪 共回答了22个问题 |采纳率95.5%(1)波尔多液为硫酸铜和氢氧化钙及水的混合物,所以题干中所缺少的是生石灰或是熟石灰;
(2)根据反应②在加热条件下金属铜与氧气化合生成氧化铜;可以判断反应①则是铁与稀核酸反应生成硫酸亚铁和氢气;而反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水;
(3)蒸发操作除了需要三脚架和酒精灯外,还需要蒸发的容器蒸发皿,为了防止液体迸溅还需要玻璃棒;
(4)途径II产生的二氧化碳既会污染环境,又使硫酸不能全部转化为产品硫酸铜而形成浪费,而途径Ⅰ可以不会产生二氧化硫,同时能更充分的利用硫酸,而不造成浪费.
故答案为:(1)生石灰(或熟石灰);
(2)Fe+H2SO4═FeSO4+H2↑;CuO+H2SO4═CuSO4+H2O;
(3)蒸发皿、玻璃棒;
(4)硫酸的利用率高.1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表示):______,该反应的基本反应类型是:______.
 567七1年前1
567七1年前1 -
 kofyong 共回答了28个问题
kofyong 共回答了28个问题 |采纳率92.9%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:Fe+CuSO4═FeSO4+Cu;置换反应.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;反应类型的判定.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.1年前查看全部
- 医院常用下列手段来杀菌消毒,1.紫外线照射病房2.煮沸法消毒医疗器械3.为什么能用硫酸铜来制杀菌剂怎样解释生活中的这些事
医院常用下列手段来杀菌消毒,
1.紫外线照射病房
2.煮沸法消毒医疗器械
3.为什么能用硫酸铜来制杀菌剂
怎样解释生活中的这些事例
1.沙被子
2.流行感冒时室内用醋熏
3.豆浆中加盐卤制成豆腐
羊毛衫为什么不能用普通肥皂洗涤? 2004绿茶1年前3
2004绿茶1年前3 -
 450677 共回答了14个问题
450677 共回答了14个问题 |采纳率92.9%这些全部都是有关蛋白质的性质啊.
首先,蛋白质有两大性质,在某些饱和无机盐溶液的条件下容易盐析,就是因为有盐溶液的存在而使蛋白质的溶解性减小而析出,但该反应是可逆的,再加入大量的水时,蛋白质仍然可以继续溶解,所以是物理变化.
另外,蛋白质在高温,强酸,强碱,重金属盐(金属相对原子质量大于55),某些有机物,如甲醛,乙醇,还有紫外线.X射线等物理条件下都容易失去活性.叫做失活,也叫变性.这个理解就是蛋白质“死亡”了.是不可逆的化学变化.
还有,细菌的主要成分是蛋白质,所谓杀菌,就是使细菌的蛋白质变性.
1.紫外线消毒时利用紫外线使蛋白质变性.
2.煮沸法消毒时利用高温条件使蛋白质变性.
3.硫酸铜消毒时利用重金属盐使蛋白质变性.
1.晒被子,也是利用阳光中紫外线照射,使蛋白质变性.
2.醋是有机物,使蛋白质变性.
3.盐卤是饱和无机盐,使蛋白质盐析.
羊毛衫的主要成分为羊毛,羊毛的化学成分为蛋白质.普通肥皂呈碱性,容易使蛋白质变性,会使羊毛衫硬化.1年前查看全部
- (2009•杭州)过碳酸钠(Na2CO4)是一种常见的漂白杀菌剂,其水溶液显碱性,能和盐酸发生下列反应:2Na2CO4+
(2009•杭州)过碳酸钠(Na2CO4)是一种常见的漂白杀菌剂,其水溶液显碱性,能和盐酸发生下列反应:2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O.工业用的过碳酸钠往往含有少量的碳酸钠.为了测定工业用的过碳酸钠的纯度,可以选择利用下列仪器(包括仪器中的药品)及石蕊试液进行实验,请回答下列问题:
(1)取适量过碳酸钠样品与足量的稀盐酸反应,只要测定反应过程中产生的
______(写化学式)体积,就可推算出过碳酸钠的纯度.
(2)请选取该实验需要的装置,并按正确连接顺序排列______(填字母,仪器中的试剂都是足量的).
(3)判定过碳酸钠试样是否完全反应的实验操作方法和现象是______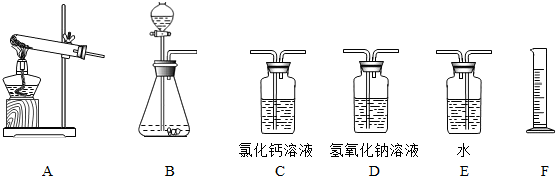
 香山一树1年前1
香山一树1年前1 -
 oppig 共回答了21个问题
oppig 共回答了21个问题 |采纳率85.7%解题思路:(1)由题给反应方程式可知,过碳酸钠和盐酸反应生成二氧化碳和氧气,碳酸钠和盐酸反应也有二氧化碳生成,所以只能通过测生成氧气的量求过碳酸钠的量;
(2)根据反应物的状态和反应条件选择反应发生装置;根据实验思路,要测生成氧气的量,可用排水法,必须先除去生成的二氧化碳,由此选择实验装置;
(3)由题意知,过碳酸钠显碱性,盐酸显酸性,可用酸碱指示剂检测是否完全反应.(1)过碳酸钠和盐酸反应生成二氧化碳和氧气,碳酸钠和盐酸反应也有二氧化碳生成,所以只能通过测生成氧气的量求过碳酸钠的量;
(2)过碳酸钠和盐酸反应为固体和液体反应且不需要加热,故选择装置B.要测定生成氧气的量,需要先除去二氧化碳,可用氢氧化钠溶液吸收二氧化碳,再通入水中,F量筒中水的体积即为E装置中氧气排开水的体积,二者体积相等.
(3)判断是否完全反应,应使用酸碱指示剂,若溶液变红,则酸过量,若溶液变蓝,则过碳酸钠过量.
故答案为:(1)O2;
(2)B→D→E→F;
(3)向反应后的B装置中滴入几滴石蕊试液,若锥形瓶内溶液变红色,则说明过碳酸钠完全反应,若溶液变蓝色,则过碳酸钠未完全反应.点评:
本题考点: 量气装置;仪器的装配或连接;证明碳酸盐.
考点点评: 本题考查化学实验的装置连接及判断反应物过量问题,解题时要注意反应发生装置的选取依据的原则是反应物状态和反应条件.(3)实验设计要注意语言描述的准确性.1年前查看全部
- (三选一)【有机化学基础】用石油裂解产物A可合成多种产物(如F是一种称为富马酸二甲酯的杀菌剂),下图用A合成一些有机产物
(三选一)【有机化学基础】
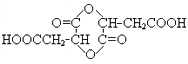
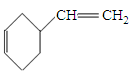
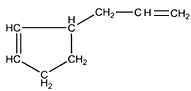
用石油裂解产物A可合成多种产物(如F是一种称为富马酸二甲酯的杀菌剂),下图用A合成一些有机产物的转化关系:
(1)上述反应中属于加成反应的是___________。
(2) 1 H核磁共振谱图表明A分子只有两种化学环境不同的氢原子,红外光谱研究表明A分子中含有两个碳碳双键,写出A、D的结构简式。A__________,D_____________
(3)写出B转化为C的化学方程式__________________________________________。
(4)H物质在浓硫酸存在下可分别生成一种含六元环、七元环、八元环的产物,写出生成六圆环产物相关反应的化学方程式______________________________________。
(5)写出跟A互为同分异构体,且分子中有4个碳原子共直线的有机物的结构简式________________________________。
(6)D被氧化成HOOCCH 2 CHClCOOH的过程中会有中间产物生成,中间产物的结构简式可能是_________________(写出一种),检验该物质存在的试剂是________________。 夜宴1231年前1
夜宴1231年前1 -
 栗亮 共回答了15个问题
栗亮 共回答了15个问题 |采纳率93.3%1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、熟石灰加水配制而成的.若用铁质容器来配置波尔多液,铁质容器表面会出现一层
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、熟石灰加水配制而成的.若用铁质容器来配置波尔多液,铁质容器表面会出现一层红色物质,使杀菌剂的药效降低,你能解释这种现象的原因吗?
 唏嘘人海1年前1
唏嘘人海1年前1 -
 鄢强 共回答了7个问题
鄢强 共回答了7个问题 |采纳率100%铁质容器表面会出现一层红色物质是因为铁与硫酸铜反应生成了铜;
药效降低时因为铜离子变成了铁离子,影响了杀菌效果.1年前查看全部
- (2011•常熟市二模)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程
(2011•常熟市二模)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程
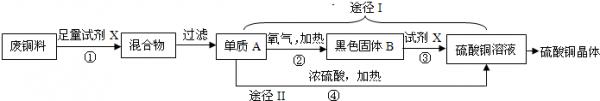
(1)反应①的化学方程式为______.
(2)途径I中,反应②、③的化学方程式分别为②2Cu+O2
2CuO△ .2Cu+O2,③______;途径Ⅱ中,反应④的化学方程式为Cu+2H2SO4(浓)
2CuO△ .
CuSO4+SO2↑+2H2O.从环保和经济的角度分析,利用途径______(选填“I”或“Ⅱ”)制取硫酸铜的方案更合理.△ .
(3)某化学兴趣小组同学用足量铜与10g质量分数为98%的浓硫酸在加热条件下充分反应,生成SO2的质量应______(选填字母).
A.等于3.2gB.小于3.2gC.大于3.2g
(4)该化学兴趣小组同学通过查阅资料,发现大多数金属与浓硫酸都能发生反应.现取足量锌与浓硫酸反应,其化学方程式为:Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O.反应一段时间后,老师指出除了SO2,还可能生成另一种气体.请你根据锌的化学性质,推断此气体可能是______,理由是______. 蓝海蒙云1年前1
蓝海蒙云1年前1 -
 jia30765 共回答了16个问题
jia30765 共回答了16个问题 |采纳率93.8%解题思路:(1)欲制得硫酸铜必须先把铁除去,故反应①为铁盒硫酸的反应;
(2)反应②为金属单质铜与氧气在加热条件下所发生的反应,生成黑色固体氧化铜,两种物质生成一种物质的反应;反应③则应是黑色固体氧化铜与稀硫酸的复分解反应,途径II要生成二氧化硫会污染空气,所以应该选择途径I;
(3)根据质量守恒定律来解答该题;
(4)根据锌的性质,结合浓硫酸随着反应的进行浓度的变化来解答该题.(1)废铜料中含有铁,所以要值得硫酸铜,应该先把铁除去,除去铁应该选用稀硫酸,故可以写出该反应的化学方程式;
(2)反应②为金属单质铜与氧气在加热条件下所发生的反应,生成黑色固体氧化铜,两种物质生成一种物质的反应;反应③则应是黑色固体氧化铜与稀硫酸的复分解反应,途径II要生成二氧化硫会污染空气,所以应该选择途径I;
(3)反应是在浓硫酸中进行的,如果完全反应根据化学方程式可以计算出应该生成3.2g气体,但是随着反应的进行浓硫酸会变稀,而使反应终止,故难以生成3.2g二氧化硫,即实际上生成的气体要小于3.2g;
(4)锌是活泼金属可以和稀硫酸反应生成氢气,所以随着反应的进行浓硫酸的浓度越来越小,故可能生成氢气;
故答案为:(1)Fe+H2SO4═FeSO4+H2↑;
(2)②2Cu+O2═2CuO;③CuO+H2SO4═CuSO4+H2O;Ⅰ;
(3)B;
(4)H2(或氢气);反应一段时间后,硫酸溶液溶质的质量分数变小,锌与稀硫酸反应生成氢气(或反应一段时间后,硫酸溶液溶质的质量分数变小,Zn+H2SO4═ZnSO4+H2↑);点评:
本题考点: 物质的相互转化和制备;金属活动性顺序及其应用;酸碱盐的应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 据生产流程图,正确理解每个过程在生产中的作用,从而达到全面掌握生产过程的目的,为解答问题做足准备.1年前查看全部
- (2004•上海)从石油裂解中得到的1,3-丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯.
(2004•上海)从石油裂解中得到的1,3-丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯.

(1)写出D的结构简式______
(2)写出B的结构简式______
(3)写出第②步反应的化学方程式______
(4)写出富马酸的一种相邻同系物的结构简式______
(5)写出第⑨步反应的化学方程式______
(6)以上反应中属于消去反应的是______(填入编号). peking111年前1
peking111年前1 -
 lulu2500 共回答了16个问题
lulu2500 共回答了16个问题 |采纳率93.8%解题思路:1,3-丁二烯和溴发生加成反应生成1,4-二溴-2-丁烯,1,4-二溴-2-丁烯发生反应生成A,A反应生成B,B发生消去反应生成2-氯-1,3-丁二烯,则B是2-氯-1,3-丁二醇,A为HOCH2CH=CHCH2OH,2-氯-1,3-丁二烯发生加聚反应生成合成橡胶D;
2-氯-1,4-丁二酸发生消去反应生成C,则C的结构简式为:NaOOCCH=CHCOONa,C然后酸化得富马酸,富马酸的结构简式为:HOOCCH=CHCOOH,在浓硫酸作催化剂、加热条件下,富马酸和甲醇发生酯化反应生成杀菌剂.1,3-丁二烯和溴发生加成反应生成1,4-二溴-2-丁烯,1,4-二溴-2-丁烯发生反应生成A,A反应生成B,B发生消去反应生成2-氯-1,3-丁二烯,则B是2-氯-1,3-丁二醇,A为HOCH2CH=CHCH2OH,2-氯-1,3-丁二烯发生加聚反应生成合成橡胶D,D的结构简式为:
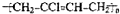 ;
;
2-氯-1,4-丁二酸发生消去反应生成C,则C的结构简式为:NaOOCCH=CHCOONa,C然后酸化得富马酸,富马酸的结构简式为:HOOCCH=CHCOOH,在浓硫酸作催化剂、加热条件下,富马酸和甲醇发生酯化反应生成杀菌剂.
(1)通过以上分析知,D为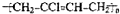 ,
,
故答案为: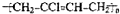 ;
;
(2)通过以上分析知,B的结构简式为:HOCH2CHClCH2CH2OH,
故答案为:HOCH2CHClCH2CH2OH;
(3)1,4-二溴-2-丁烯和氢氧化钠的水溶液发生取代反应生成A,反应方程式为: ,
,
故答案为: ;
;
(4)富马酸的相邻一种同系物的结构简式为:HOOCCH=CHCH2COOH,
故答案为:HOOCCH=CHCH2COOH;
(5)在浓硫酸作催化剂、加热条件下,富马酸和甲醇发生酯化反应,反应方程式为: ,
,
故答案为: ;
;
(6)通过以上分析知,属于消去反应的是④⑦,故答案为:④⑦.点评:
本题考点: 有机物的合成.
考点点评: 本题考查了有机物的推断,明确有机物的官能团及其性质是解本题关键,注意氯代烃发生消去反应和取代反应断键位置和反应条件,为易错点.1年前查看全部
- (2009•安徽模拟)农业生产中使用的杀菌剂波尔多液是用CuSO4和Ca(OH)2按一定比例溶于水配制而成的,它能防止植
(2009•安徽模拟)农业生产中使用的杀菌剂波尔多液是用CuSO4和Ca(OH)2按一定比例溶于水配制而成的,它能防止植物病菌的原因是( )
A.CuSO4可使菌体休眠
B.Ca(OH)2使菌体失去繁殖能力
C.细菌被波尔多液冲离植物表面
D.CuSO4和Ca(OH)2使菌体蛋白质变性 紫环舞蝶1年前1
紫环舞蝶1年前1 -
 xfzw 共回答了15个问题
xfzw 共回答了15个问题 |采纳率86.7%解题思路:CuSO4属于重金属盐,蛋白质在重金属盐或碱性条件下变性.用CuSO4和Ca(OH)2按一定比例溶于水配制而成的波尔多液中含有CuSO4和Ca(OH)2,
CuSO4属于重金属盐,蛋白质在重金属盐或碱性条件下变性,能防止植物病菌.
故选D.点评:
本题考点: 氨基酸、蛋白质的结构和性质特点.
考点点评: 本题考查蛋白质的性质,题目难度不大,注意相关基础知识的积累.1年前查看全部
- 用化学方程式解释下列问题:(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波
用化学方程式解释下列问题:
(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,其原因是______;
(2)铝通常情况下具有良好的抗腐蚀性能,其原因是______;
(3)盛放澄清石灰水的试剂内壁常附有一层白色固体,其形成原因是______. admy1年前1
admy1年前1 -
 pao3231050 共回答了16个问题
pao3231050 共回答了16个问题 |采纳率93.8%解题思路:根据各反应的反应物、生成物、反应条件,写出反应的化学方程式即可.(1)铁的活动性比铜强,铁和硫酸铜反应会生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.(2)铝具有很好的抗腐蚀性能的原因是:铝在空气中能与氧气反应,表面形成致密的氧化铝薄膜,反应的化学方程式...
点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握常见化学反应的反应原理、化学方程式的书写方法是正确解答本题的关键.1年前查看全部
- 当室内的有毒细菌开始增加时,就要使用杀菌剂.刚开始使用的时候,细菌数量还会继续增加,随着时间的增加,它增加幅度逐渐变小,
当室内的有毒细菌开始增加时,就要使用杀菌剂.刚开始使用的时候,细菌数量还会继续增加,随着时间的增加,它增加幅度逐渐变小,到一定时间,细菌数量开始减少.如果使用杀菌剂t小时后的细菌数量为b(t)=105+104t-103t2.
(1)求细菌在t=5与t=10时的瞬时速度;
(2)细菌在哪段时间增加,在哪段时间减少?为什么? 一骑烟雨1年前1
一骑烟雨1年前1 -
 ronnieweng 共回答了19个问题
ronnieweng 共回答了19个问题 |采纳率94.7%解题思路:(1)求导数,b′(t),然后分别代入t=5和t=10可求得结果;
(2)分别解不等式b′(t)>0,b′(t)<0可求得函数的单调区间,即细菌增加、减少的时间段;(1)b′(t)=104-2×103t,
b′(t)|t=5=104-2×103×5=0,b′(t)|t=10=104-2×103×10=-10000,
∴细菌在t=5与t=10时的瞬时速度分别为0和-10000.
(2)由104-2×103t>0,得t<5,由104-2×103t<0,得t>5,
∴细菌在t∈(0,5)时间段数量增加,在t∈(5,+∞)时间段数量减少.点评:
本题考点: 利用导数研究函数的单调性;变化的快慢与变化率.
考点点评: 本题以函数为载体,考查函数模型的构建及导数的应用,属于中档题.1年前查看全部
- (2012•南京)臭氧水是臭氧(O3)溶入水中制成的,能脱色去臭,还是很好地杀虫、杀菌剂,下列说法错误的是( )
(2012•南京)臭氧水是臭氧(O3)溶入水中制成的,能脱色去臭,还是很好地杀虫、杀菌剂,下列说法错误的是( )
A.臭氧是单质
B.1个臭氧分子由3个氧原子构成
C.臭氧水是氧化物
D.臭氧水是混合物 arabfreeze1年前1
arabfreeze1年前1 -
 专业HPF 共回答了22个问题
专业HPF 共回答了22个问题 |采纳率81.8%解题思路:A、由同种元素组成的纯净物是单质,据此进行分析判断.
B、根据臭氧(O3)化学式的含义进行分析判断.
C、氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据此进行分析解答.
D、由两种或两种以上的物质混合而成的物质是混合物,据此据此进行分析解答.A、臭氧(O3)是由一种元素组成的纯净物,属于单质,故选项说法正确.
B、由臭氧(O3)化学式可知,1个臭氧分子由3个氧原子构成,故选项说法正确.
C、根据题意,臭氧水是臭氧(O3)溶入水中制成的,含有臭氧、水等物质,属于混合物,不是纯净物,故不属于氧化物;故选项说法错误.
D、根据题意,臭氧水是臭氧(O3)溶入水中制成的,含有臭氧、水等物质,属于混合物,故选项说法正确.
故选C.点评:
本题考点: 氧元素组成的单质;从组成上识别氧化物;纯净物和混合物的判别;单质和化合物的判别.
考点点评: 本题难度不大,考查同学们新信息获取、处理及灵活运用所学知识进行解题的能力,掌握单质、氧化物、混合物的特征、化学式的含义等是正确解答本题的关键.1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、术士回家谁配制而成的 若用铁制容器.下面.
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、术士回家谁配制而成的 若用铁制容器.下面.
来配制波尔多液,铁制容器表面会出现一层红色物质,使杀菌剂的药效降低,你能解释产生这种现象的原因吗? mcgrady12231年前3
mcgrady12231年前3 -
 xly8387 共回答了19个问题
xly8387 共回答了19个问题 |采纳率84.2%波尔多液是用熟石灰和硫酸铜搅拌得到,主要有效成分是Cu(OH)2.杀菌主要靠重金属离子Cu2+.铁会和Cu2+反应.Fe+Cu2+==Cu+Fe2+,看到的红色物质就是铜了,Cu2+减少了,杀菌剂的药效降低.1年前查看全部
- 四羟甲基硫酸膦杀菌剂有介绍四羟甲基硫酸膦,阳离子表面活性剂,还原性很强,可用作杀菌剂,其水溶液用于浸泡消毒高等生物组织,
四羟甲基硫酸膦杀菌剂
有介绍四羟甲基硫酸膦,阳离子表面活性剂,还原性很强,可用作杀菌剂,其水溶液用于浸泡消毒高等生物组织,请推测对生物组织伤害很大吗?为什么?谢 zyc99811年前2
zyc99811年前2 -
 es7039 共回答了22个问题
es7039 共回答了22个问题 |采纳率77.3%只要是消毒剂,就会对生物组织造成一定伤害,但是四羟甲基硫酸磷的伤害相对较小.因为它的强还原性使其在空气中极易被氧化,而失去杀菌和对生物组织的伤害作用.
因此它广泛应用于水处理、油田、造纸等行业,大大减轻对环境的影响,在处理完生物组织后,因为它的迅速失活也可以保护生物组织免受进一步的伤害.1年前查看全部
- (3分)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所
(3分)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所示:
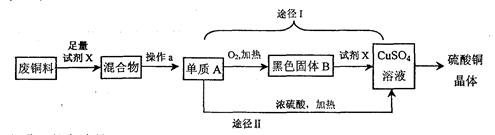
(1)操作a的名称是: ;
(2)已知:Cu+2H 2 SO 4 (浓) △ CuSO 4 +SO 2 ↑+2H 2 O。则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;② ;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为: 。 gfdgfgfccc1年前1
gfdgfgfccc1年前1 -
 godguoshen 共回答了18个问题
godguoshen 共回答了18个问题 |采纳率100%(1)过滤; (2)硫酸根全部转化为硫酸铜,硫酸的利用率高; (3) Fe + CuSO 4 ="=" Cu + FeSO 4 。
1年前查看全部
- (2007•虹口区)二氧化氯(ClO2)已被世界卫生组织确认为一种安全、高效的强力杀菌剂,制取二氧化氯的反应是:2NaC
(2007•虹口区)二氧化氯(ClO2)已被世界卫生组织确认为一种安全、高效的强力杀菌剂,制取二氧化氯的反应是:2NaClO3+4HCl(浓)
Cl2↑+2ClO2↑+2NaCl+2X则X的化学式是( )一定温度 .
A.H2O
B.H2
C.O2
D.HCl jjjoy1年前1
jjjoy1年前1 -
 爱的汤力水 共回答了19个问题
爱的汤力水 共回答了19个问题 |采纳率89.5%解题思路:根据质量守恒定律可知,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,然后除以2,就是X的化学式中含有的元素的原子个数.据此写出其化学式,然后对照选项进行选择即可.根据化学方程式(2NaClO3+4HCl(浓)
一定温度
.
Cl2↑+2ClO2↑+2NaCl+2X)和质量守恒定律可知,X的化学式中含有的
Na元素的原子个数为(2-2)÷2=0,
Cl元素的原子个数为(2+4-2-2-2)÷2=0,
O元素的原子个数为:(2×3-2×2)÷2=1,
H元素的原子个数为4÷2=2;
故X的化学式为:H2O.
故选A.点评:
本题考点: 有关化学式的计算和推断;质量守恒定律及其应用.
考点点评: 本题主要考查学生根据化学方程式,运用质量守恒定律解答问题的能力.1年前查看全部
- 多菌灵类杀菌剂(1)百度介绍多菌灵有内吸治疗和保护作用.它既是内吸性杀菌剂也是保护性杀菌剂?(2)苯菌灵、甲基托布津本身
多菌灵类杀菌剂
(1)百度介绍多菌灵有内吸治疗和保护作用.它既是内吸性杀菌剂也是保护性杀菌剂?
(2)苯菌灵、甲基托布津本身没有杀菌活性,被植物代谢成多菌灵才有杀菌性,
(3)用来杀灭植物表面菌类(浸种、泡果),用多菌灵比其他两种效果好,
多菌灵是保护性杀菌剂还是治疗性杀菌剂? 只这一次_1年前1
只这一次_1年前1 -
 chick1983 共回答了20个问题
chick1983 共回答了20个问题 |采纳率75%多菌灵既是保护性杀菌剂也是治疗性杀菌剂1年前查看全部
- (2014?南昌模拟)ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的
(2014?南昌模拟)ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的
 (2014?南昌模拟)ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的新工艺是电解法.
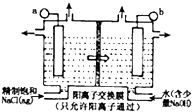
(2014?南昌模拟)ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的新工艺是电解法.
(1)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,写出阳极ClO2产生的电极方程式:______;图中b电极为______;(填“阳极”或“阴极”)
(2)电解一段时间,当阴极产生标准状况下气体112ml时,停止电解,则通过阳离子交换膜的阳离子物质的量为______mol,阴极区pH______(填“变大”、“变小”或“不变”)
(3)ClO2对污水中Fe2+,Mn2+,S2-,CN-等有明显去除效果,某工厂中污水含CN-(a mg/L),现将ClO2把CN-氧化成两种无毒气体,写出该反应的离子方程式:______.
 海蓝蓝ok1年前1
海蓝蓝ok1年前1 -
 梅花之恋 共回答了18个问题
梅花之恋 共回答了18个问题 |采纳率88.9%(1)由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子,电极反应式为:Cl--5e-+2H2O=ClO2↑+4H+,
从图上可见,阳离子移向阴极,所以b为阴极,故答案为:Cl--5e-+2H2O=ClO2↑+4H+;阴极;
(2)在阴极发生2H++2e-=H2↑,氢气的物质的量为[V
Vm=
0.112L/22.4L/mol]=0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,电解中阴极H+浓度减小,使得H2O?OH-+H+的平衡向右移动,溶液的pH增大,
故答案为:0.01;pH变大;
(3)ClO2将CN-氧化,只生成两种气体,应生成氮气与二氧化碳,同时生成氯离子,反应离子方程式为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-,
故答案为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-.1年前查看全部
- 过碳酸钠(2Na2CO3•3H2O2)是一种新型高效固体漂白杀菌剂,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中
过碳酸钠(2Na2CO3•3H2O2)是一种新型高效固体漂白杀菌剂,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中.依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如图1:
请回答下列问题:
(1)反应容器中加入稳定剂的作用是______.
(2)操作①需要的玻璃仪器有______(填写仪器名称),工业采用冰水洗涤晶体的目的有______.
(3)与Cl2相比,用过碳酸钠作为漂白杀菌剂具有的优点是______.
(4)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图2所示装置,测定工业纯碱中Na2CO3的含量.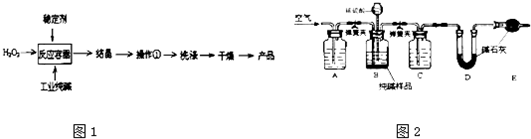
①要检验工业纯碱中杂质的存在,最好选用______试剂.
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹,往长颈漏斗中加水,______,说明装置不漏气.
③若纯碱样品的质量为m,反应前后C、D、E装置的质量分别增加ag、bg、cg,则纯碱中Na2CO3的含量为[106b/44m]×100%[106b/44m]×100%(用含m、a、b、c的代数式表示),若缺少装置E,Na2CO3的含量将______(填“偏大”“偏小”或“不变”). hyunceng1年前1
hyunceng1年前1 -
 fattyboy 共回答了17个问题
fattyboy 共回答了17个问题 |采纳率82.4%解题思路:(1)过碳酸钠溶于水后所得溶液,在水溶液中能解离成过氧化氢与碳酸钠,过氧化氢溶液是极弱的弱酸,而碳酸钠在水中由于水解会显示碱性,反应容器中加入稳定剂的作用是防止过氧化氢分解;
(2)操作①是过滤分离固体和溶液,过滤装置需要的玻璃仪器分析,工业采用冰水洗涤晶体的目的有洗涤去表面杂质,减少晶体损失;
(3)与Cl2相比,用过碳酸钠作为漂白杀菌剂具有的优点是无毒、环保、高效;
(4)①纯碱中常含有少量NaCl,用检验氯离子的方法进行检验,需要试剂为硝酸银和稀硝酸,
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,利用压强变化和液面变化分析判断,若漏斗中与试剂瓶中的液面差保持不再变化,证明装置气密性完好,
③若纯碱样品的质量为m,反应前后C、D、E装置的质量分别增加ag、bg、cg,利用D装置吸收的二氧化碳计算碳酸钠质量分数,依据碳元素守恒计算得到碳酸钠质量分数;若缺少装置E,空气中的二氧化碳和水蒸气被装置D吸收,称量质量增大,Na2CO3的含量将偏高;(1)过碳酸钠溶于水后所得溶液,在水溶液中能解离成过氧化氢与碳酸钠,过氧化氢溶液是极弱的弱酸,而碳酸钠在水中由于水解会显示碱性,反应容器中加入稳定剂的作用是防止过氧化氢分解;
故答案为:防止过氧化氢分解;
(2)操作①是过滤分离固体和溶液,过滤装置需要的玻璃仪器为漏斗、烧杯、玻璃棒,工业采用冰水洗涤晶体的目的有洗涤去表面杂质,减少晶体损失;
故答案为:普通漏斗、烧杯、玻璃棒;除去晶体表面的杂质并减少晶体的损失;
(3)与Cl2相比,用过碳酸钠作为漂白杀菌剂具有的优点是无毒、环保、高效;
故答案为:无毒、环保、高效;
(4)①纯碱中常含有少量NaCl,用检验氯离子的方法进行检验,需要试剂为硝酸银和稀硝酸,
故答案为:硝酸银和稀硝酸;
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,利用压强变化和液面变化分析判断,若漏斗中与试剂瓶中的液面差保持不再变化,证明装置气密性完好,
故答案为:至漏斗中液面高于洗气瓶液面,静置一段时间后,液面不下降;
③若纯碱样品的质量为m,反应前后C、D、E装置的质量分别增加ag、bg、cg,利用D装置吸收的二氧化碳计算碳酸钠质量分数,依据碳元素守恒计算得到碳酸钠质量分数=
bg
44g/mol×106g/mol
mg×100%=[106b/44m]×100%;若缺少装置E,空气中的二氧化碳和水蒸气被装置D吸收,称量质量增大,Na2CO3的含量将偏高;
故答案为:[106b/44m]×100%;偏大;点评:
本题考点: 探究物质的组成或测量物质的含量.
考点点评: 本题考查了物质组成的实验探究方法,实验工厂分析,物质性质和离子检验,掌握实验基础和过程分析方法是解题关键,题目难度中等.1年前查看全部
- 可用于出去面团发酵生成的酸是?农业上用作杀菌剂的是?
 lusis1年前1
lusis1年前1 -
 海兰色浪花 共回答了22个问题
海兰色浪花 共回答了22个问题 |采纳率81.8%可用于出去面团发酵生成的酸是 碳酸钠Na2CO3
农业上用作杀菌剂的是 硫酸铜 CuSO41年前查看全部
- 杀菌消毒剂的问题如果一种杀菌剂对于大肠杆菌的杀菌效果非常理想,那么对于结核杆菌是不是也会有相应的效果呢?
 我怕蚊子咬1年前1
我怕蚊子咬1年前1 -
 天啊几几 共回答了13个问题
天啊几几 共回答了13个问题 |采纳率69.2%不一定,即使同为大肠杆菌,也分为对某种抗生素的敏感型和非敏感型.1年前查看全部
- 二氧化氯(ClO 2 )已被世界卫生组织确认为一种安全、高效、广谱的强力杀菌剂,二氧化氯的制取可通过下列反应完成:2Na
二氧化氯(ClO 2 )已被世界卫生组织确认为一种安全、高效、广谱的强力杀菌剂,二氧化氯的制取可通过下列反应完成:2NaClO 3 +4HCl(浓)  Cl 2 ↑+2ClO 2 ↑+2NaCl+2X。则X的化学式为
Cl 2 ↑+2ClO 2 ↑+2NaCl+2X。则X的化学式为[ ]
A.O 2
B.H 2 O
C.H 2
D.NaClO 桑宜9991年前1
桑宜9991年前1 -
 sxzycxxcxq 共回答了12个问题
sxzycxxcxq 共回答了12个问题 |采纳率100%B1年前查看全部
- (2009•徐州模拟)高锰酸钾是日常生活常用的一种杀菌剂.它是一种紫黑色固体,取少量固体放入研钵内研磨,做如下图实验.
(2009•徐州模拟)高锰酸钾是日常生活常用的一种杀菌剂.它是一种紫黑色固体,取少量固体放入研钵内研磨,做如下图实验.

试根据上述实验过程填空.
(1)步骤②将少许高锰酸钾粉末溶于水后得到紫红紫红色溶液,其中振荡的作用是加速溶解,混合均匀加速溶解,混合均匀.
(2)上述实验中,步骤①②①②(选填实验步骤的序号)说明物质是可分的;步骤④中溶液几乎变为无色.溶液中溶质微粒不是不是(选填“是”或“不是”)变得更小了.
(3)水是重要的溶剂,可以溶解很多种盐.盐溶液的颜色通常与溶液中的离子有关.已知NaCl溶液中含有Na+和Cl-,KMnO4溶液中含有K+和MnO4-.据此推测,高锰酸钾溶液的颜色与MnO4-MnO4-(填离子符号)离子有关,理由是KNO3溶液是无色的,说明K+不能使溶液显色,因此,KMnO4溶液呈现的颜色与MnO4-有关KNO3溶液是无色的,说明K+不能使溶液显色,因此,KMnO4溶液呈现的颜色与MnO4-有关. sirpaladin1年前1
sirpaladin1年前1 -
 yidaer 共回答了26个问题
yidaer 共回答了26个问题 |采纳率92.3%(1)由于高锰酸钾能够溶于水,形成的溶液是紫红色的;振荡能加速溶解,使溶质和溶剂混合均匀.
(2)在上述实验第一步研磨的过程中,大颗粒的高锰酸钾晶体被分为了更小的颗粒.在第二步溶解中,小颗粒的高锰酸钾分为了更小的颗粒是以K+和MnO4-的形式进入了溶液,故第一步和第二步中说明高锰酸钾的可分性;步骤④实际上是将步骤3中溶液进行稀释,不是溶液中溶质的微粒变小了,而是溶液中溶质的质量分数变小了,溶液的颜色只是变淡了.
(3)KCl、KNO3溶液均是无色的,说明K+不能使溶液显色,因此,KMnO4溶液呈现的颜色与MnO4-有关.
故答案为:(1)紫红;加速溶解,混合均匀;(2)①②,不是;(3)MnO4-;KNO3溶液是无色的,说明K+不能使溶液显色,因此,KMnO4溶液呈现的颜色与MnO4-有关.1年前查看全部
- 异噻唑啉酮做为杀菌剂有哪方面的优点?
 xubiah1231年前1
xubiah1231年前1 -
 cxazyc 共回答了19个问题
cxazyc 共回答了19个问题 |采纳率89.5%这个东西比较复杂.唑啉酮是通过断开细菌和藻类蛋白质的键而起杀生作用的.异噻唑啉酮微生物接触后,能迅速地不可逆地抑制其生长,从而导致微生物细胞的死亡,故对常见细菌、真菌、藻类等具有很强的抑制和杀灭作用.杀生效率高,降解性好,具有不产生残留、操作安全、配伍性好、稳定性强、使用成本低等特点.能与氯及大多数阴、阳离子及非离子表面活性剂相混溶.高剂量时,异噻唑啉酮对生物粘泥剥离有显著效果.1年前查看全部
- (2008•海珠区一模)A、B、C、D、甲、乙、丙都是初中化学中的常见物质,其中A是配制波尔多液杀菌剂的一种试剂,B是蓝
(2008•海珠区一模)A、B、C、D、甲、乙、丙都是初中化学中的常见物质,其中A是配制波尔多液杀菌剂的一种试剂,B是蓝色沉淀,D是黑色粉末,它们之间的转化关系如下图所示(图中略去了部分反应产物).
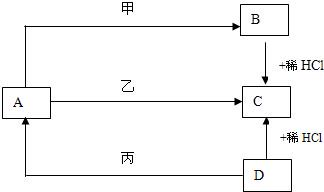
请回答:
(1)写出有关物质的化学式:A______;B______;D______.
(2)写出A+乙反应的化学方程式:______. loloyou1年前1
loloyou1年前1 -
 wswire 共回答了22个问题
wswire 共回答了22个问题 |采纳率90.9%解题思路:(1)框图题是推断题中考查元素化合物知识的重要题型.这类题目一般是把物质的变化、性质、组成、结构等之间的联系用框图的形式在新情境中出现,试题面目新,考查容量大,综合推理能力.解题的关键是找准“题眼”,即找到解题的突破口.
(2)本题的“题眼”为“A是配制波尔多液杀菌剂的一种试剂,B是蓝色沉淀,D是黑色粉末”,则可假设:B是氢氧化铜,A是硫酸铜,D为氧化铜,C为氯化铜,把此结论带入题中,进行检验验证,正好符合.(1)有分析可知:A是配制波尔多液杀菌剂的一种试剂,B是蓝色沉淀,D是黑色粉末,则可假设定为:B是氢氧化铜,A是硫酸铜,D为氧化铜,C为氯化铜;把此结论带入题中,进行验证.
(2)已知反应物中有硫酸铜,生成物中有氯化铜;如果要发生反应,则生成物中还得有沉淀硫酸钡,所以可写化学方程式.
故答为:(1)CuSO4;Cu(OH)2;CuO;(
2)CuSO4+BaCl2=BaSO4↓+CuCl2点评:
本题考点: 物质的鉴别、推断;酸碱盐的应用;化学式的书写及意义;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了物质的一般推断方法,掌握酸碱盐的应用,了解化学性质与物理性质的差别及应用.1年前查看全部
- 波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若
波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若涉及化学反应必须用化学方程式表示)?
 5219394a1年前1
5219394a1年前1 -
 这样非勒 共回答了19个问题
这样非勒 共回答了19个问题 |采纳率94.7%解题思路:根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
故答案为:Fe+CuSO4═FeSO4+Cu;腐蚀铁制容器、农药不纯影响药.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法即可正确解答本题.1年前查看全部
- 高锰酸钾是日常生活常用的一种杀菌剂,又称为“PP粉”.它是一种紫黑色固体,取少量固体放入研钵内研磨.做如下图实验.
高锰酸钾是日常生活常用的一种杀菌剂,又称为“PP粉”.它是一种紫黑色固体,取少量固体放入研钵内研磨.做如下图实验.
试根据上述实验过程填空.
(1)步骤②将少许高锰酸钾粉末溶于水后得到 ▲ 色溶液,其中振荡的作用是 ▲ .
(2)上述实验中,▲ (选填实验步骤的序号)说明物质是可分的;步骤④中溶液
几乎变为无色.溶液中溶质微粒 ▲ (选填“是”或“不是”)变得更小了.
(3)将步骤②所得溶液的一部分倒入U型管内,再加适量水,接入右图所示的电路.闭合电键,发现灯泡发光,这是由于高锰酸钾溶于水时生成了 ▲ 的缘故.过一段时间后,在与电源相连的两电极区域溶液的颜色深浅出现差异,这又说明高锰酸钾溶液的颜色是由 ▲ (填微粒的符号)决定的. tjfsupermp31年前4
tjfsupermp31年前4 -
 小疯子飘飘 共回答了19个问题
小疯子飘飘 共回答了19个问题 |采纳率100%紫红色 加速溶解
? 不是
可自由移动的高锰酸根离子和钾离子 KMnO4-
PS:题目有点不完整哦,第2小题第一空没办法做1年前查看全部
- 波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若
波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若涉及化学反应必须用化学方程式表示)?
 psrain1年前1
psrain1年前1 -
 upc的laurent 共回答了13个问题
upc的laurent 共回答了13个问题 |采纳率76.9%解题思路:根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
故答案为:Fe+CuSO4═FeSO4+Cu;腐蚀铁制容器、农药不纯影响药.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法即可正确解答本题.1年前查看全部
- 高锰酸钾是日常生活中常用的一种杀菌剂,又称为“PP粉”.它是一种紫黑色固体,取少量固体放入研钵内研磨,做如图1实验.
高锰酸钾是日常生活中常用的一种杀菌剂,又称为“PP粉”.它是一种紫黑色固体,取少量固体放入研钵内研磨,做如图1实验.

试根据上述实验过程填空.
(1)步骤②将少许高锰酸钾粉末溶于水后得到______色溶液,其中振荡的作用是______.
(2)上述实验中,步骤______(选填实验步骤的序号)说明物质是可分的;步骤④中溶液几乎变为无色,溶液中溶质微粒______(选填“是”或“不是”)变得更小了.
(3)将步骤②所得溶液的一部分倒入U型管内,再加适量水,接入如图2所示的电路闭合电键,发现灯炮发光,这是由于高锰酸钾溶于水时生成了______的缘故.过一段时间后,在与电源相连的两电极区域溶液的颜色深浅出现差异,这又说明高锰酸钾溶液的颜色是由______(填微粒的符合)决定的. cuijing7151年前4
cuijing7151年前4 -
 风云任务 共回答了18个问题
风云任务 共回答了18个问题 |采纳率100%解题思路:(1)高锰酸钾能够溶于水,形成的溶液是紫红色的;
(2)高锰酸钾能被研细,说明它能变成更小的颗粒,高锰酸钾能够被水溶解,说明在水分子的作用下,成了肉眼看不到的更小的粒子;溶液加水稀释,颜色变浅,并不是因为构成物质的粒子变小了;
(3)液能够导电是因为溶液中有自由移动的带电的微粒.(1)由于高锰酸钾能够溶于水,形成的溶液是紫红色的,振荡的作用是加速溶解,混合均匀,故答案为:紫红 加速溶解,混合均匀;
(2)高锰酸钾能被研细,说明它能变成更小的颗粒,高锰酸钾能够被水溶解,说明在水分子的作用下,成了肉眼看不到的更小的粒子;溶液加水稀释,颜色变浅,并不是因为构成物质的粒子变小了;故答案为:①②,不是
(3)有的溶液能够导电是因为溶液中有自由移动的带电的微粒.由于在电极的正负极的作用下,带电离子发生定向运动,导致高锰酸根离子分布不均,而产生了不同的颜色深度,所以高锰酸钾溶液的颜色由高锰酸根离子来决定.故答案为:自由移动的离子,MnO4-
答案:
(1)紫红,加速溶解,混合均匀
(2)①②不是
(3)自由移动的离子MnO4−点评:
本题考点: 实验探究物质的性质或变化规律;溶液的概念、组成及其特点;溶液的导电性及其原理分析.
考点点评: 弄清高锰酸钾的某些性质及组成,和溶液导电的原因:有自由移动的离子,为解决问题奠定良好的基础.以此来培养学生抓住规律、解决问题的能力.1年前查看全部
- 好几道化学计算题的问题一、将胆矾与生石灰、水按质量比为1:0.56:100混合配制成无机铜杀菌剂波尔多液:此波尔多液中C
好几道化学计算题的问题
一、将胆矾与生石灰、水按质量比为1:0.56:100混合配制成无机铜杀菌剂波尔多液:
此波尔多液中Cu2+和Ca2+的物质的量之比为( )
波尔多液有效成分的化学式可表示为CuSO4·xCu(OH)2·yCa(OH)2,此种配比当x=1时,是确定y的数值为( )
二、已知:2Fe3+ +2碘离子=2Fe2+ +碘单质. 2Fe2+溴单质=2Fe3+ +2溴离子
含有1molFeI2和2molFeBr2的溶液通入2mol Cl2,此时被氧化的离子是( ),被氧化的离子的物质的量是( )
如果向溶液中通入3mol Cl2 则最后被氧化的离子是( ),其对应氧化产生的物质的量是( ).
三、高锰酸钾和碘化钾和硫酸反应生成锰酸钾和碘单质和碘酸钾和硫酸钾和水的化学方程式配平
四、下列物质不能作为从溴水中萃取溴的溶剂是( )
A酒精 B苯 C分馏汽油
我化学不好,理由详细到我懂了为止 我们要分手了1年前1
我们要分手了1年前1 -
 竽儿LOVE 共回答了20个问题
竽儿LOVE 共回答了20个问题 |采纳率100%1,胆矾,CuSO4·5H2O分子量是250 生石灰是CaO 分子量是56物质的量之比 1/250 :0.56/56 = 2:52,好像题目有点问题,确定是1mol FeCl2不是2mol吗?3,就是高锰酸钾中的锰从+7到锰酸钾中的+6,碘化钾中的I- 变成碘单质其他的...1年前查看全部
- (2012•泉州模拟)过氧乙酸是一种高效广谱杀菌剂.水灾过后,为预防灾区发生瘟疫,常用0.2%的过氧乙酸溶液进行环境的表
(2012•泉州模拟)过氧乙酸是一种高效广谱杀菌剂.水灾过后,为预防灾区发生瘟疫,常用0.2%的过氧乙酸溶液进行环境的表面消毒.对于20%的过氧乙酸溶液8Kg,请计算:
(1)含溶质过氧乙酸多少千克?
(2)可稀释成0.2%的过氧乙酸溶液多少千克? 乐乐永远1年前1
乐乐永远1年前1 -
 kaiven909 共回答了19个问题
kaiven909 共回答了19个问题 |采纳率84.2%解题思路:(1)根据溶质的质量分数不变进行计算
(2)运用稀释前后溶液中溶质的质量不变再结合溶质质量分数的公式解答(1)溶质过氧乙酸的质量为:8kg×20%=1.6kg
(2)稀释前后溶液中溶质的质量不变,所以在此基础上列等式解答.
设可稀释成0.2%的过氧乙酸溶液的质量为x
0.2%x=1.6kg
x=800kg
答:(1)含溶质过氧乙酸1.6kg
(2)可稀释成0.2%的过氧乙酸溶液800kg点评:
本题考点: 有关溶质质量分数的简单计算;用水稀释改变浓度的方法.
考点点评: 溶液中溶质的质量分数的计算题目,是计算性的题型,计算能力要求比较高.1年前查看全部
- 已知每升A种液体约含有10^12个有害细菌,科学实验发现,1滴杀菌剂可以杀死约10^9个这种细菌,按此计算,
已知每升A种液体约含有10^12个有害细菌,科学实验发现,1滴杀菌剂可以杀死约10^9个这种细菌,按此计算,
用杀菌剂10^4滴,能否将1LA种液体中的有害细菌全部杀死?
要详细过程和列出算式. ryw5331年前1
ryw5331年前1 -
 月下清茶 共回答了12个问题
月下清茶 共回答了12个问题 |采纳率66.7%10^9*10^4=10^(9+4)=10^13
所以可以全部杀死1年前查看全部
- 杀菌剂波尔多液是用硫酸铜、熟石灰加水配置而成的.能用化学方程式解释不能用铁制容器配置该溶液的原因吗?(硫酸铜会和熟石灰先
杀菌剂波尔多液是用硫酸铜、熟石灰加水配置而成的.能用化学方程式解释不能用铁制容器配置该溶液的原因吗?(硫酸铜会和熟石灰先反应吗?)
 桃源二舍1年前4
桃源二舍1年前4 -
 嘉木茶艺 共回答了21个问题
嘉木茶艺 共回答了21个问题 |采纳率95.2%Ca(OH)2 + CuSO4 === Cu(OH)2 + CaSO4 ,生成的Cu(OH)2 是波尔多液的有效成分.
不能用铁质容器配置是因为硫酸铜会腐蚀铁桶,反应方程式为:
Fe + CuSO4 === FeSO4 + Cu1年前查看全部
- 波尔多液是果树上常用的保护型杀菌剂,由硫酸铜,生石灰和水配制而成.果农用波尔多也是要做到十个忌,以保证使用效果.其中,一
波尔多液是果树上常用的保护型杀菌剂,由硫酸铜,生石灰和水配制而成.果农用波尔多也是要做到十个忌,以保证使用效果.其中,一忌用陈旧的熟石灰,代替生石灰,二忌用铁,铝等容器盛装溶液
1.写出配制波尔多液时发生的有关化学反应方程式
2.回答两个禁忌中包含的化学原理 睁一只眼闭只眼1年前2
睁一只眼闭只眼1年前2 -
 2200255 共回答了26个问题
2200255 共回答了26个问题 |采纳率96.2%1.CuSO4+Ca(OH)2=Cu(OH)2沉淀+CaSO4
2.(1)陈旧的熟石灰会与空气中的二氧化碳和水蒸气反应生成碳酸钙而导致变质.
(2)铁,铝等容器不能装波尔多液是因为波尔多液中含有硫酸铜,因为在配比的时候不可能完全正好反应,所以会有过量的,然后硫酸铜会和那些铝,铁反应,生成新的物质.1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成.为什么不能用铁制容器来配制波尔多液?
 kane0081年前1
kane0081年前1 -
 yy易碎的心 共回答了7个问题
yy易碎的心 共回答了7个问题 |采纳率57.1%硫酸铜与铁发生置换反应1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、熟石灰加水配置而成.若用铁容器配置波尔多液.
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、熟石灰加水配置而成.若用铁容器配置波尔多液.
容器表面会出现一层红色物质,使杀菌效果降低,解释产生原因.
我的疑问是:红色物质是什么?氢氧化亚铁是沉淀么?
顺便把反应的化学方程式都写完整, qwer6841年前4
qwer6841年前4 -
 mrb8866 共回答了18个问题
mrb8866 共回答了18个问题 |采纳率94.4%红色物质是铜
氢氧化亚铁是白色沉淀
CuSO4+Fe=FeSO4+Cu
由于铁的置换,硫酸铜浓度会降低,所以使杀菌效果降低.1年前查看全部
- 波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若
波尔多液农药是一种农业上常用的杀菌剂,它是由硫酸铜,熟石灰加水配制而成.为什么不能用铁制容器来配置波尔多液农药(答题时若涉及化学反应必须用化学方程式表示)?
 bedbed27bed1年前1
bedbed27bed1年前1 -
 罗二毛01230 共回答了23个问题
罗二毛01230 共回答了23个问题 |采纳率91.3%解题思路:根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
故答案为:Fe+CuSO4═FeSO4+Cu;腐蚀铁制容器、农药不纯影响药.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法即可正确解答本题.1年前查看全部
- 杀菌剂用量范围的含义杀菌剂(包括工业用、医用等)说明书的推荐用量是个范围(如0.3%-0.8%),问是不是浓度太高(超过
杀菌剂用量范围的含义
杀菌剂(包括工业用、医用等)说明书的推荐用量是个范围(如0.3%-0.8%),问是不是浓度太高(超过0.8%)杀菌力反而降低了?
浓度过高 杀菌力就降下来吗?杀菌力呈n形? warriorzgl1年前1
warriorzgl1年前1 -
 clava 共回答了13个问题
clava 共回答了13个问题 |采纳率92.3%不是,应该说浓度越高杀菌效果越好,但是要考虑诸多因素.比如,浓度太大会影响到人体健康等,另外也没必要太高.人家是经过很多次试验计算出来的,你就按照这个标准来就没错.1年前查看全部
- 春季是传染病菌繁衍流行的季节,必须做好预防.二氧化氯(C1O2)已被世界卫生组织确认为一种安全、高效、广谱的强力杀菌剂.
春季是传染病菌繁衍流行的季节,必须做好预防.二氧化氯(C1O2)已被世界卫生组织确认为一种安全、高效、广谱的强力杀菌剂.制取二氧化氯的反应是:2NaClO3+4HCl(浓)=2NaCl+Cl2↑+2C1O2+2X
(1)X的化学式是______.
(2)Cl2和二氧化氯两种分子中所含氯原子的个数比为______.
(3)135g二氧化氯中含氧元素的质量是______g. roadrunner5211年前1
roadrunner5211年前1 -
 柴火煮饭 共回答了25个问题
柴火煮饭 共回答了25个问题 |采纳率88%解题思路:(1)根据质量守恒定律反应前后原子的种类及数目不变,由2NaClO3+4HCl(浓)=2NaCl+Cl2↑+2C1O2+2X,推断X的化学式;
(2)根据化学式的意义分析计算;
(3)根据化学式进行计算135g二氧化氯中含氧元素的质量.(1)由反应的化学方程式2NaClO3+4HCl═2ClO2↑+Cl2↑+2X+2NaCl可知:反应前有钠、氯、氧、氢原子的数目分别是:2、6、6、4.反应后有钠、氯、氧原子2、6、4.由质量守恒定律化学变化前后原子的种类、数目不变,生成物X的2个分子中含有2个O原子和4个H原子,则每个X分子由2个H原子和1个O原子构成,则物质X的化学式为H2O;
(2)由化学式的意义可知,Cl2和二氧化氯两种分子中所含氯原子的个数比为2:1;
(3)135g二氧化氯中含氧元素的质量是:135g×[32/67.5]×100%=64g
故答为:(1)H2O;(2)2:1;(3)64.点评:
本题考点: 质量守恒定律及其应用;化合物中某元素的质量计算.
考点点评: 本题主要考查了根据质量守恒定律推断物质的化学式及根据化学式的计算,难度不大.会根据化学式的意义机型有关的分析、计算等.1年前查看全部
- 用化学方程式解释下列问题:(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波
用化学方程式解释下列问题:
(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,其原因是 ;
(2)铝通常情况下具有良好的抗腐蚀性能,其原因是 ;
(3)盛放澄清石灰水的试剂内壁常附有一层白色固体,其形成原因是 . beijingcgj1年前1
beijingcgj1年前1 -
 勇敢敢 共回答了14个问题
勇敢敢 共回答了14个问题 |采纳率78.6%(1)Fe+CuSO 4 ═FeSO 4 +Cu;(2)4Al+3O 2 =2Al 2 O 3 ;(3)CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O. 1)铁的活动性比铜强,铁和硫酸铜反应会生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO 4 =FeSO...1年前查看全部
- 过碳酸钠是一种常见的漂白杀菌剂,往过碳酸钠中滴加稀盐酸,可产生两种气体,[提出问题]过碳酸钠与稀盐酸,产生两种什么气体?
过碳酸钠是一种常见的漂白杀菌剂,往过碳酸钠中滴加稀盐酸,可产生两种气体,[提出问题]过碳酸钠与稀盐酸,产生两种什么气体?
[作出猜想]生成的两种可能是:1、二氧化碳和水蒸气;2、二氧化碳和氯化氢;3、二氧化碳和氧气;4、氧气和水蒸气.
提出以上猜想的依据是什么? 找你好吗1年前3
找你好吗1年前3 -
 709436594 共回答了13个问题
709436594 共回答了13个问题 |采纳率69.2%应该是选3(CO2和O2),过碳酸钠其实就是Na2CO3和H2O2的复合物,化学式可以写成2Na2CO3·H2O2,接下来应该很清楚了.
产生CO2:Na2CO3 + 2HCl = 2NaCl + H2O + CO2(气)
产生O2(过氧化氢分解):2H2O2 = 2H2O + O2(气)
或者也可以这样考虑:由题意可知,过碳酸钠具有强氧化性(能漂白),因此很可能发生一个氧化还原反应,产物中会有元素的化合价发生了变化(氧).另一方面,实验用的是稀盐酸,它可以和碳酸根反应得到CO2.1年前查看全部
- 二氧化氯(ClO 2 )是联合国世界卫生组织确认的一种安全、高效、广谱、强力杀菌剂.二氧化氯常温下是橘红色气体,有窒息性
二氧化氯(ClO 2 )是联合国世界卫生组织确认的一种安全、高效、广谱、强力杀菌剂.二氧化氯常温下是橘红色气体,有窒息性臭味,二氧化氯气体易溶于水,形成黄绿色的溶液,一般采用向上排空气法来收集二氧化氯.它是一种有强氧化性的物质,其杀菌能力是氯气的5倍,能与很多物质能发生剧烈反应,如能与镁反应生成亚氯酸镁【Mg(C10 2 ) 2 】.根据上述信息,请回答:
(1)二氧化氯的物理性质有______;
(2)二氧化氯的化学性质有______;
(3)写出镁与二氧化氯反应的化学方程式______,生成物中氯元素的化合价为______. 竟陵王子1年前1
竟陵王子1年前1 -
 lmokch 共回答了18个问题
lmokch 共回答了18个问题 |采纳率88.9%(1)二氧化氯的物理性质有:常温下二氧化氯是橘红色气体,有窒息性臭味,易溶于水,密度比空气大.
(2)二氧化氯的化学性质有:有强氧化性,能与镁发生化学反应.
(3)镁与二氧化氯反应的化学方程式为:Mg+2ClO 2 =Mg(ClO 2 ) 2
在Mg(ClO 2 ) 2 中,镁元素的化合价是+2价,氧元素的化合价是-2价,
设氯元素的化合价为X,根据化合物中元素化合价代数和为零有:
(+2)+2X+(-2)×4=0.
解得:X=+3.
氯元素的化合价是+3价.1年前查看全部
- 用化学方程式解释下列问题:(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波
用化学方程式解释下列问题:
(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,其原因是______;
(2)铝通常情况下具有良好的抗腐蚀性能,其原因是______;
(3)盛放澄清石灰水的试剂内壁常附有一层白色固体,其形成原因是______. 湘-西1年前1
湘-西1年前1 -
 摸黑找手电 共回答了16个问题
摸黑找手电 共回答了16个问题 |采纳率93.8%(1)铁的活动性比铜强,铁和硫酸铜反应会生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO 4 =FeSO 4 +Cu.
(2)铝具有很好的抗腐蚀性能的原因是:铝在空气中能与氧气反应,表面形成致密的氧化铝薄膜,反应的化学方程式为:4Al+3O 2 =2Al 2 O 3 .
(3)石灰水中的溶质是氢氧化钙,能与空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式为CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O.
故答案为:(1)Fe+CuSO 4 ═FeSO 4 +Cu;(2)4Al+3O 2 =2Al 2 O 3 ;(3)CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O.1年前查看全部
- (17分)顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
(17分)顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
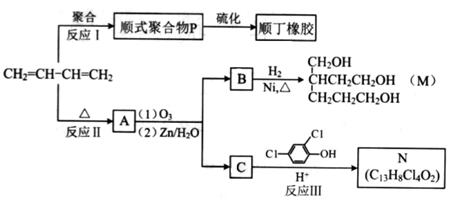

(1)CH 2 =CH-CH=CH 2 的名称是_______;
(2)反应I的反应类型是(选填字母)_______;
a.加聚反应 b.缩聚反应
(3)顺式聚合物P的结构式是(选填字母)_______;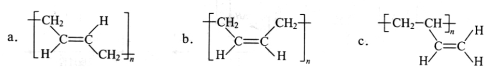
(4)A的相对分子质量为108.
①反应II的化学方程式是_____________________
②1molB完全转化为M所消耗的H 2 的质量是______g。
(5)反应III的化学方程式是______________________________。
(6)A的某些同分异构体在相同反应条件下也能生成B和C,写出其中一种同分异构体的结构简式__________。 左彬1年前1
左彬1年前1 -
 budingcc_1981 共回答了23个问题
budingcc_1981 共回答了23个问题 |采纳率87%1年前查看全部
- 氧化亚铜(Cu 2 O)是鲜红色粉末状固体,可用作杀菌剂、陶瓷和搪瓷的着色剂、红色玻璃染色剂等。现将 Cu 2 O 和
氧化亚铜(Cu 2 O)是鲜红色粉末状固体,可用作杀菌剂、陶瓷和搪瓷的着色剂、红色玻璃染色剂等。现将 Cu 2 O 和 Cu 的固体混合物 6.8g 放入烧杯中,加入足量的稀硫酸,充分反应后,过滤、洗涤、干燥,得到 4.8g 固体。(已知Cu 2 O+H 2 SO 4 =CuSO 4 +Cu+H 2 O)。则原混合物中的 Cu 2 O 和 Cu 质量比为
A.9∶8 B.17∶12 C.1∶1 D.9∶4  lemore1年前1
lemore1年前1 -
 梨花院里叩重门 共回答了24个问题
梨花院里叩重门 共回答了24个问题 |采纳率87.5%A
1年前查看全部
- 波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表
波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,但不能用铁制容器来配制波尔多液,原因是(用化学方程式表示):______,该反应的基本反应类型是:______.
 linglingpyro1年前3
linglingpyro1年前3 -
 微风浊月 共回答了14个问题
微风浊月 共回答了14个问题 |采纳率100%解题思路:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故不能用铁制容器来配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:Fe+CuSO4═FeSO4+Cu;置换反应.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;反应类型的判定.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.1年前查看全部
- 某房间内每立方米空气中含3×10的六次方个病菌,1毫升杀菌剂可以杀灭2×10的5次个这种病菌、
某房间内每立方米空气中含3×10的六次方个病菌,1毫升杀菌剂可以杀灭2×10的5次个这种病菌、
某房间内每立方米空气中含3×10的六次方个病菌,1毫升杀菌剂可以杀灭2×10的5次个这种病菌,若要将长10米、宽8米、高3米的房间内的病菌全部杀灭,则需要多少毫升杀菌剂?p31,t6) woaijin1年前1
woaijin1年前1 -
 ewsd900 共回答了15个问题
ewsd900 共回答了15个问题 |采纳率100%共需要(10*8*3*3*10^6)/(2*10^5)=3600ml=3.6L
绝对正确,要是有不懂得还可以继续问,1年前查看全部
大家在问
- 1求几篇文言文的原文与译文晏子进谏 永之氓 艾子有孙 巧诈不如拙诚 和氏璧
- 2变化的磁场产生变化的电场 这句话对吗
- 3是一种工业循环水的添加剂,非氧化性杀菌剂啊,是酸性,溅射到了衣服表面,侵蚀了小半天
- 4灯丝电阻随温度升高而变大还是变小
- 5要开学了,做都做不完,所以只能抄了.
- 6小学生五年级下学期口算、脱式计算(简算)
- 7请问醛还原能不能成醇,什么时候成醇.反应进程是怎么样的.
- 8电阻会不会像灯丝一样随温度的升高而增大?
- 9青春励志名言 短句
- 10青春励志名言短句
- 11高中焰色反应实验需要掌握什么
- 12描述.江碧鸟逾白,山青花欲燃所展现的画面
- 13月球的公转周期
- 1412.已知下面三个数据:①7.2×10-4、②2.6×10-4、③4.9×10-10分别是三种酸的电离平衡常数,若已知这
- 15鉴别苯,苯酚,乙醇选用什么试剂?只能一种