剧毒的光气可以用氨解毒.其方程式为:cocl2+4nh3=co(nh2)2+2nh4cl 某坑道容积为33m的立方中光气
 绿绾潇湘2022-10-04 11:39:541条回答
绿绾潇湘2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 娜娜小夭 共回答了15个问题
娜娜小夭 共回答了15个问题 |采纳率93.3%- 剧毒的光气可以用氨解毒.其方程式为:cocl2+4nh3=co(nh2)2+2nh4cl 某坑道容积为33m的立方中光气的浓度为0.3*10的负三次方g/l 解毒最少消耗的能量分数为25%的氨水多少克(1m的立方+1000L)
33m3=33×103 L
浓度为0.3×10-3g•L-1的33m3光气中光气的含量为:
0.3×10-3g•L-1×33 10的3次方 L=9.9g
COCl2 + 4NH3 =CO(NH2)2+2NH4Cl
12+16+35.5×2 4×(14+1×3)
=99 =68
9.9g 计算得:m=6.8g
那么最少消耗的质量分数为25%的氨水的质量为:
M=m÷25%=6.8g÷25%=27.2g - 1年前
相关推荐
- 一氧化碳是一种无色、无味但有剧毒的气体,其密度与空气很接近,难溶于水.现要收集一瓶一氧化碳气体,可采用的方法是( )
一氧化碳是一种无色、无味但有剧毒的气体,其密度与空气很接近,难溶于水.现要收集一瓶一氧化碳气体,可采用的方法是( )
A.向下排空气法
B.向上排空气法
C.排水法
D.向上排空气法或排水法 longline1年前1
longline1年前1 -
 吴先平 共回答了18个问题
吴先平 共回答了18个问题 |采纳率88.9%解题思路:能用排水法收集,说明气体不溶于水或不易溶于水,能用向上排空气法收集,说明气体的密度比空气大且与空气中的其它物质不反应.一氧化碳是一种有剧毒的气体,其密度与空气很接近,不能用排空气法收集,一氧化碳难溶于水,可用排水法收集
故选C点评:
本题考点: 常用气体的收集方法.
考点点评: 考虑收集气体的方法时,应该从气体的密度、水溶性、是否有毒等方面进行分析、判断,从而找出最好的收集方法.1年前查看全部
- 2004年4月,重庆天原化工厂一个冷凝管破裂厂导致剧毒氯气外泄,造成多人中毒.小龙同学听到这一消息后立即上网,查找氯气的
2004年4月,重庆天原化工厂一个冷凝管破裂厂导致剧毒氯气外泄,造成多人中毒.小龙同学听到这一消息后立即上网,查找氯气的资料,得知:①由氯元素组成;②常温下氯气是一种黄绿色气体;③有刺激性气味;④氯浓度过高或接触时间较久,常可致深部呼吸道病变;⑤加热时,能与铁反应生成氯化铁;⑥实验室常用加热二氧化锰和浓盐酸的方法制取氯气;⑦可用于消毒、制盐酸、制多种农药等.请根据以上信息回答:(填序号)
(1)属于氯气物理性质的是______.
(2)属于氯气化学性质的是______.
(3)属于氯气组成的是______.
(4)属于氯气用途的是______.
(5)属于氯气制取的是______. 王春1141年前1
王春1141年前1 -
 柳以寒 共回答了13个问题
柳以寒 共回答了13个问题 |采纳率76.9%解题思路:物理性质是不需要通过化学变化表现出来的性质,包括颜色、状态、气味、密度、硬度、熔点、沸点、溶解性、挥发性、导电性、导热性等,化学性质是通过化学变化表现出来的性质.组成是物质的元素组成,用途是物质的用法,制取是怎样得到该气体.(1)②常温下氯气是一种黄绿色气体是物质的颜色、状态属于物理性质;③有刺激性气味是氯气的气味不需要通过化学变化表现出来,属于物理性质;
(2)④氯浓度过高或接触时间较久,常可致深部呼吸道病变,是氯气与人体组织发生了反应,发生了病变,通过化学变化表现出来,属于化学性质;⑤加热时,能与铁反应生成氯化铁说明氯气与铁反应生成氯化铁属于化学变化,所以能与铁反应生成氯化铁属于化学性质;
(3)①由氯元素组成是说的氯气的组成;
(4)可用于消毒、制盐酸、制多种农药说的都是用氯气来做什么,所以属于氯气的用途;
(5)⑥实验室常用加热二氧化锰和浓盐酸的方法制取氯气,说的是怎样制取氯气,所以属于氯气的制法.
故答案为:(1)②③;(2)④⑤;(3)①;(4)⑦;(5)⑥.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 解答本题关键是要知道物理性质和化学性质的区别:是否通过化学变化表现出来的性质,知道物质的用途和制取方法的识别.1年前查看全部
- 常温下,CO是一种无色、无味难溶于水的气体,能燃烧,有剧毒,不与石灰水反应,在加热或高温的条件下,CO能夺取金属氧化物中
常温下,CO是一种无色、无味难溶于水的气体,能燃烧,有剧毒,不与石灰水反应,在加热或高温的条件下,CO能夺取金属氧化物中的氧元素,使金属氧化物失去氧元素,成为金属,具有还原性.现用混有3量SO2、水蒸汽的CO混合气体,还原黑色CuO,根据下列实验装置q进行实验.
请回答下列问题: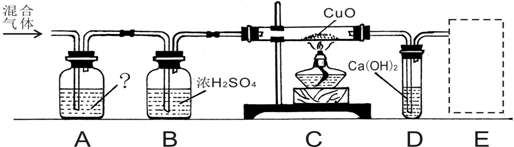
(1)了装置中应盛装______溶液,除去混合气体中的j氧化硫气体.
(2)B装置用于______.
(3)C处观察到______,反应的化学方程式CuO+CO
Cu+CO2△ .CuO+CO.
Cu+CO2△ .
(4)q处观察到澄清石灰水变浑浊,写出反应的化学方程式______.
(5)E处应______,防止剩余的CO有毒气体污染空气. 36271271年前1
36271271年前1 -
 ll方向盘 共回答了11个问题
ll方向盘 共回答了11个问题 |采纳率100%(8)0氧化硫是酸性氧化物可以与碱反应生成盐和水,所以该出可放置NaO少 或 KO少 或 Ba(O少)2 或 石灰水的溶液完成0氧化硫的除掉工作;
(2)浓硫酸具有吸水性是常用的干燥剂;
(3)从一氧化碳还原氧化铜时会生成铜与0氧化碳,所以C处观察到的现象是黑色粉末变成红色;
(它)0氧化碳能与澄清石灰水生成碳酸钙和水,其化学方程式为:CO2+Ca(O少)2=CaCO3↓+少2O;
(五)一氧化碳有毒因此为防止环境污染可在0处加入尾气处理装置;
故答案为:(8)NaO少 或 KO少 或 Ba(O少)2 或 石灰水;
(2)干燥CO气体 或吸收水分;
(3)黑色粉末变成红色,C4O+CO
△
.
C4+CO2.
(它)CO2+Ca(O少)2=CaCO3↓+少2O.
(五)将CO气体燃烧 或 用气球收集CO销毁处理;1年前查看全部
- (2012•上海)PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低.下列判断错误的是(
(2012•上海)PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低.下列判断错误的是( )
A.PH3分子呈三角锥形
B.PH3分子是极性分子
C.PH3沸点低于NH3沸点,因为P-H键键能低
D.PH3分子稳定性低于NH3分子,因为N-H键键能高 eebgvgi1年前1
eebgvgi1年前1 -
 yxt889 共回答了27个问题
yxt889 共回答了27个问题 |采纳率92.6%解题思路:A、NH3是三角锥型,PH3分子结构和NH3相似,也是三角锥型;
B、分子结构是三角锥型,正负电荷重心不重合,为极性分子;
C、NH3分子之间存在氢键,沸点高;
D、化学键越稳定,分子越稳定,键能越大化学键越稳定.A、PH3分子结构和NH3相似,NH3是三角锥型,故PH3也是三角锥型,故A正确;
B、PH3分子结构是三角锥型,正负电荷重心不重合,为极性分子,故B正确;
C、NH3分子之间存在氢键,PH3分子之间为范德华力,氢键作用比范德华力强,故NH3沸点比PH3高,故C错误;
D、P-H键键能比N-H键键能低,故N-H更稳定,化学键越稳定,分子越稳定,故D正确;
故选C.点评:
本题考点: 键能、键长、键角及其应用;判断简单分子或离子的构型;极性分子和非极性分子.
考点点评: 本题考查空间结构、氢键、键能与性质关系等,比较基础,注意C选项中常见具有氢键的物质.1年前查看全部
- 请化学好的来帮个忙甲醇是一种剧毒的、具有酒精气味的液体.现把一定量的甲醇与4.4克氧气混合于一个密封容器内,引燃发生如下
请化学好的来帮个忙
甲醇是一种剧毒的、具有酒精气味的液体.现把一定量的甲醇与4.4克氧气混合于一个密封容器内,引燃发生如下反应:8CH3OH+xO2=mCO2+nCO+16H2O.当反应物完全转化为生成物后,降至常温常压下,容器内余下液体为3.6克.求:1.系数m与n的和、系数x的值.2.该反应生成CO2的质量.(精确到0.01) 害虫路易1年前1
害虫路易1年前1 -
 wyh2006 共回答了13个问题
wyh2006 共回答了13个问题 |采纳率84.6%根据原子个数守恒 8CH3OH+xO2=mCO2+nCO+16H2O 32x 288 4.4g 3.6g x=11 由碳原子数守恒得:m+n=8 由氧原子数守恒得:8+11×2=2m+n+16 则2m+n=14 列方程组{m+n=8 {2m+n=14 m=6,n=2 设反应生成CO2的质量为W 44*6/W=288/3.6g W=3.30g 答:(1)生成CO2的质量为3.30g(2)x=111年前查看全部
- 现有氧气、一氧化碳、二氧化碳、甲烷等四种气体,其中可供给呼吸的是______;能用于灭火的是______,有剧毒的是__
现有氧气、一氧化碳、二氧化碳、甲烷等四种气体,其中可供给呼吸的是______;能用于灭火的是______,有剧毒的是______,目前城市公交系统的清洁燃料车所用的清洁燃料是______.
 欲语砖先下1年前1
欲语砖先下1年前1 -
 Kelly_Zou 共回答了20个问题
Kelly_Zou 共回答了20个问题 |采纳率90%解题思路:物质的性质决定物质的用途,根据常见气体的性质和用途进行分析解答即可.氧气具有供给呼吸的性质,可供给呼吸.
二氧化碳不能燃烧、不能支持燃烧、密度比空气大,可用于灭火.
一氧化碳有剧毒.
目前城市公交系统的清洁燃料车所用的清洁燃料是天然气,其主要成分是甲烷.
故答案为:氧气;二氧化碳;一氧化碳;甲烷.点评:
本题考点: 常见气体的用途.
考点点评: 本题难度不大,物质的性质决定物质的用途,掌握常见气体的性质和用途是正确解答此类题的关键.1年前查看全部
- (2005•无锡)常温下氯气(Cl2)是一种黄绿色的气体,密度比空气大,可溶于水,有剧毒,能与水、碱等物质发生化学反应.
(2005•无锡)常温下氯气(Cl2)是一种黄绿色的气体,密度比空气大,可溶于水,有剧毒,能与水、碱等物质发生化学反应.
下列关于氯分子的说法错误的是( )
A.氯分子在不断地运动
B.氯分子是由氯原子构成的
C.氯分子很大,肉眼可以看到
D.氯分子之间有间隔 班主任刘文倜ii1年前1
班主任刘文倜ii1年前1 -
 siren0205 共回答了21个问题
siren0205 共回答了21个问题 |采纳率90.5%A、由分子的基本性质可知,氯分子是在不断的运动的,故选项说法正确.
B、分子是由原子构成的,由氯气的化学式可知氯分子是由氯原子构成的;故选项说法正确.
C、分子的质量和体积都很小,肉眼不能直接看到氯分子;故选项说法错误.
D、由分子的基本性质可知,氯分子之间有间隔的,故选项说法正确.
故选C.1年前查看全部
- 哪种气体含有剧毒是一氧化碳,还是二氧化碳,还是氦气,还是氧气
 成dd人请入1年前1
成dd人请入1年前1 -
 fhnw5688 共回答了15个问题
fhnw5688 共回答了15个问题 |采纳率86.7%一氧化碳
二氧化碳,氦气,氧气 都是空气主要成分~
所以.1年前查看全部
- ①CuO+H2== 现象:,H2还原优点是反应生成物之一是 ,且产物较纯净.②CuO+CO== (CO有剧毒,实
①CuO+H2== 现象:,H2还原优点是反应生成物之一是 ,且产物较纯净.②CuO+CO== (CO有剧毒,实
①CuO+H2== 现象:,H2还原优点是反应生成物之一是 ,且产物较纯净.
②CuO+CO== (CO有剧毒,实验时一定 )
③2CuO+C ;现象:
(虽然C的还原能力强于H2,但固体还原剂与氧化物的充分接触程度没有固体与气体还原剂充分,自然反应温度就比H2要高,最好使用酒精喷灯或加罩的酒精灯.C要稍微过量.)
④2Fe2O3+3C ;
⑤Fe2O3+3CO ;(加热时一定要持续高温)
⑥Fe2O3+3H2 ;现象: o半生缘o1年前1
o半生缘o1年前1 -
 wfmll 共回答了19个问题
wfmll 共回答了19个问题 |采纳率89.5%①CuO+H2== CU紫红色+H2O 现象:,H2还原优点是反应生成物之一是 ,且产物较纯净.
②CuO+CO== CO2+CU (CO有剧毒,实验时一定 )
③2CuO+2C =2CO+2CU ;现象:黑色粉末变成紫红色粉末
(虽然C的还原能力强于H2,但固体还原剂与氧化物的充分接触程度没有固体与气体还原剂充分,自然反应温度就比H2要高,最好使用酒精喷灯或加罩的酒精灯.C要稍微过量.)
④2Fe2O3+3C =2FE+3CO ;
⑤Fe2O3+3CO =3CO2+2FE ;(加热时一定要持续高温)
⑥Fe2O3+3H2 =2FE+3H2O ;现象:棕红色变黑色1年前查看全部
- Ba2+为重金属离子,对人体剧毒,医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4
Ba2+为重金属离子,对人体剧毒,医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4做内服造影剂,这种检查手段称为钡餐透视.
Ⅰ.请写出BaSO4能作为钡餐透视的另外一个理由:______.
Ⅱ.请用文字叙述和离子方程式说明钡餐透视时为什么不用BaCO3?______.
Ⅲ.某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5mL水
②20mL 0.5mol•L-1的Na2SO4溶液
③40mL 0.2mol•L-1的Ba(OH)2溶液
④40mL 0.1mol•L-1的H2SO4溶液中,溶解至饱和.
(1)以上各溶液中,c(Ba2+)的大小顺序正确的是______,BaSO4的溶解度的大小顺序为______(填序号).
A.③>①>④>②B.③>①>②>④C.①>④>③>②D.①>③>④>②
(2)已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO
)为______,溶液②中c(Ba2+)为______.2−4
(3)某同学取溶液③和溶液④直接混合,则混合溶液的pH为______(假设混合后溶液的体积为混合前两溶液的体积之和). ymn5251年前2
ymn5251年前2 -
 allenljp 共回答了18个问题
allenljp 共回答了18个问题 |采纳率88.9%解题思路:Ⅰ.根据硫酸钡在酸和水中的溶解性分析;
Ⅱ.根据BaCO3的溶解平衡:BaCO3⇌Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动;
Ⅲ.(1)含有相同的离子能抑制硫酸钡的溶解,难溶物质向更难溶物质进行转化,硫酸根离子或钡离子浓度越大,硫酸钡的溶解度越小;
(2)根据硫酸钡的溶度积常数计算硫酸根离子和钡离子浓度;
(3)先计算混合溶液中氢氧根离子浓度,再根据离子积公式计算氢离子浓度,从而确定溶液的pH值.Ⅰ.BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不会引起Ba2+中毒,所以常用BaSO4做内服造影剂,故答案为:BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不会引起Ba2+中毒;
Ⅱ.硫酸钡不溶于水和酸,但胃酸可与CO32-反应生成水和二氧化碳,使CO32-浓度降低,从而使平衡BaCO3(s)⇌Ba2+(aq)+CO32-(aq) 向溶解方向移动,使Ba2+浓度增大,且Ba2+有毒,所以不能用碳酸钡代替硫酸钡,反应离子方程式为:BaCO3+2H+═Ba2++H2O+CO2↑,
故答案为:BaCO3遇到胃酸生成Ba2+会使人中毒,反应离子方程式为:BaCO3+2H+=Ba2++H2O+CO2↑;
Ⅲ.(1)根据难溶电解质的溶度积常数知,溶液中硫酸根离子浓度越大,硫酸钡的溶解度越小,钡离子浓度越低,氢氧化钡能抑制硫酸钡的电离,但氢氧化钡溶液中含有钡离子,所以钡离子浓度最大;水中的钡离子浓度次之;硫酸钠溶液和硫酸溶液中都含有硫酸根离子,抑制硫酸钡的电离,硫酸钠中的硫酸根浓度大于硫酸中的浓度,所以硫酸钠溶液中钡离子的浓度小于硫酸溶液中钡离子浓度,所以钡离子浓度大小顺序是:③>①>④>②;硫酸钡溶液中加入硫酸根离子和钡离子都会导致硫酸钡的沉淀溶解平衡逆移,硫酸钡的溶解度减小,硫酸根离子或钡离子浓度越大,硫酸钡的溶解度越小,所以BaSO4的溶解度的大小顺序:①>④>③>②,
故答案为:A;C;
(2)已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO
2−4)=[Ksp
c(Ba2+)=
1.1×10−10/0.2]=5.5×10-10mol/L,②中C(Ba2+)=mol/L=2.2×10-10mol/L,
故答案为:5.5×10-10mol/L,2.2×10-10mol/L;
(3)40ml 0.2mol•L-1的Ba(OH)2溶液和40ml 0.1mol•L-1的H2SO4溶液中混合后溶液中C(OH-)=
(0.2−0.1)mol/L×2×0.04L
0.04L×2=0.1mol/L,则C(H+)=10-13 mol/L,所以pH=13,
故答案为:13.点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质;离子浓度大小的比较.
考点点评: 本题考查了沉淀溶解平衡的移动,Ksp的计算;要准确掌握Ksp表达式及计算方法,题目难度中等.1年前查看全部
- 甲醇是一种剧毒的、具有酒精气味的液体,现把一定量的甲醇与4.4g氧气混合于一个密封容器内,引燃发生如下反应:8CH3OH
甲醇是一种剧毒的、具有酒精气味的液体,现把一定量的甲醇与4.4g氧气混合于一个密封容器内,引燃发生如下反应:8CH3OH+xO2__点燃mCO2+nCO+16H2O 当反应物完全转化为生成物后,降至常温常压下,容器内余下的液体为3.6g,求:
(1)系数m与n的和;
(2)该反应生成CO2的质量(精确到0.01g);
(3)系数x的值
没有学过mol,麻烦用化学式计算做做看~ uououououo1年前6
uououououo1年前6 -
 lyl63219 共回答了15个问题
lyl63219 共回答了15个问题 |采纳率86.7%(1)根据C的质量守恒,CO2+CO物质的量=CH3OH物质的量,所以m+n=8.
(2)根据O的质量守恒计算.
CH3OH物质的量可根据余下液体H2O(因完全反应)的数据算出,为0.1mol,其含O为0.1mol.氧气共0.1375mol,含氧原子0.275mol,水含氧原子0.2mol,所以CO2+CO共含氧原子0.1+0.275-0.2=0.175mol,而CO2+CO共0.1mol,用十字相乘法可得CO2=0.075mol,CO=0.025mol.以CO2分子量44计算,CO2质量为3.30g.
(3)根据上面数据已知,m+n=8,m/n=0.075/0.025=3/1.所以m=6,n=2.通过配平得x=11.
顺便说一句,甲醇不是剧毒!甲醇只是中等毒,乙醇是微毒.
问题补充:没有学过mol,麻烦用化学式计算做做看~
你是在自学化学吗?mol是化学里最基本的概念和单位,即便不学化学也应当知道的,如果现在不了解,劝你还是尽早的看看,没什么难度.
我们可以绕过这个概念给你算出结果,但是:第一、那样浪费彼此的时间;第二、那样做是在绕弯路,对你并没有丝毫好处,甚至会有反作用;第三、我和AIR之AIR的解答已经足够详尽了,你应该可以按照这种思路自己做做看.
花几分钟看看书就知道什么是mol了,你也可以按这种关键词去找:摩尔、物质的量.1年前查看全部
- 所有化学药品的实际用途?想知道各种化学药品在生活上的用途,不是化学方程式.例如:CO 是剧毒气体,会和人体中的血红蛋白结
所有化学药品的实际用途?
想知道各种化学药品在生活上的用途,不是化学方程式.例如:CO 是剧毒气体,会和人体中的血红蛋白结合,使人缺氧而死.越多越好! hawkkong1年前1
hawkkong1年前1 -
 星夜别离 共回答了23个问题
星夜别离 共回答了23个问题 |采纳率87%香肠、腌肉、咸菜中含有亚硝酸钠,在人体中一定条件下生成亚硝酸胺,致癌物质.维生素C有还原性,不能与海鲜类食物一起吃.瓜果催熟,可以在生果中放入一个熟透的梨.水果会释放乙烯,乙烯有催熟作用.新家具中通常有甲醛存在,可以放上浓氨水来吸收甲醛 重金属中毒时,可以先喝牛奶或鸡蛋清来紧急处理,然后送医院.切洋葱的时候含一口水或在切洋葱的菜刀上抹一些水就可以防止流眼泪.生了锈的水壶可以用白醋来恢复原样.医用酒精浓度一般在75%左右.小苏打是碳酸氢钠.用来发面的可以用碳酸钠.铁放久了会生锈 菜刀用醋涂抹可除绣 等等,很多很多的啦~1年前查看全部
- 对一氧化碳的防毒措施封闭不严的煤炉在缓缓燃烧过程中产生大量的剧毒气体一氧化碳,请制定出对这种煤炉的防毒措施.
 cenziran1年前1
cenziran1年前1 -
 甲低患者 共回答了16个问题
甲低患者 共回答了16个问题 |采纳率87.5%主要是排气要做好,给你举个例子,我在北方的农村长大,冬天一般取暖全是靠烧煤的炉子,在防止一氧化碳中毒方面主要就是靠通畅的自排烟系统,什么叫自排烟就是不需要动力装置去排,而是靠自然的气压去排,一是排烟路线尽可能短,不宜设置过长的烟囱,二是保证烟囱通畅,房屋的附墙烟囱竖直向上,一般要高出房顶一点,便于通风,当烟囱出口有气流通过时,对烟囱就产生一种吸力,另外热的烟一般都是向上对流的,所以能顺利排出去.(事实上绝对密封的炉子反而不利于排烟,因为有气压差才能形成对流)
会出现中毒的情况是往往都是排烟不畅造成的,比如阴天,气压低,有的人家的烟囱是水平排烟的而不是向上,使得气压差不大,不足以形成通畅的排烟,这样一来多余的不完全燃烧的一氧化碳就会弥漫在屋子里,尤其是夜里(北方农村夜里炉子一般都处于不完全燃烧状态)睡觉极易导致中毒身亡.1年前查看全部
- 下列说法中,错误的是( ) A.在有剧毒气体的环境中,人们要佩戴防毒面具 B.当发生沙尘暴时,要戴上口罩以减少尘埃的吸
下列说法中,错误的是( ) A.在有剧毒气体的环境中,人们要佩戴防毒面具 B.当发生沙尘暴时,要戴上口罩以减少尘埃的吸入 C.尘肺是长期在粉尘场所工作的人易患的一种职业病 D.呼吸道传染病流行季节不采取措施也不会感染疾病  yangxxx1年前1
yangxxx1年前1 -
 吃碗冷面 共回答了20个问题
吃碗冷面 共回答了20个问题 |采纳率95%呼吸系统包括呼吸道和肺两部分.呼吸道的组成由上到下依次是鼻腔、咽、喉、气管和支气管,鼻腔内有鼻毛,可以阻挡灰尘,呼吸道都有骨或软骨做支架,其内表面覆盖着黏膜,黏膜内还分布有丰富的毛细血管.这些特点既保证了气体的畅通,又对吸入的空气具有清洁、温暖和湿润的作用;肺是气体交换的场所,是呼吸系统的主要器官.呼吸道能阻挡灰尘,使空气清洁,但不能清除空气中的所有的有害物质,对空气的处理能力是有限的,流感病毒仍然可以由呼吸道进入人体使人患病.因此空气质量会影响人的健康.传染病是由病原体引起的,能在生物体之间传播的一种疾病,具有传染性和流行性等特点.传染病能够在人群中流行,必须同时具备传染源、传播途径、易感人群这三个环节,缺少其中任何一个环节,传染病就流行不起来.所以只要切断传染病的流行的任何一个环节,传染病就流行不起来.故传染病的预防措施有三个:控制传染源、切断传播途径、保护易感人群.故在有剧毒气体的环境中,人们要佩戴防毒面具.当发生沙尘暴时,要戴上口罩以减少尘埃的吸入.尘肺是长期在粉尘场所工作的人易患的一种职业病的说法是正确的.
故选:D.1年前查看全部
- 工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
 工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
A.甲醇的化学式为CH4O
B.甲醇的相对分子质量为32
C.甲醇是由1个碳原子、4个氢原子和1个氧原子构成
D.甲醇中氧元素的质量分数为50% i_am_bt1年前0
i_am_bt1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 2,4二硝基氯苯 属剧毒么
 perfect-boy1年前2
perfect-boy1年前2 -
 mopa 共回答了17个问题
mopa 共回答了17个问题 |采纳率70.6%属于剧毒1年前查看全部
- 某地天然气井发生井喷事故,喷出的天然气中H 2 S气体含量很高,H 2 S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发
某地天然气井发生井喷事故,喷出的天然气中H 2 S气体含量很高,H 2 S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,附近村民就闻到了臭鸡蛋气味,这体现了分子______的性质; 当村民得知这种气体有剧毒时,迅速撤离村庄.为减少村民的中毒机会,你认为村民在撤离时应尽量走______(填“低处”或“高处”).技术人员后来成功点燃了H 2 S气体,使气体不再扩散.已知H 2 S(硫化氢)燃烧时生成两种常见的氧化物,试写出H 2 S燃烧的化学方程式:______.  weiweikind1年前1
weiweikind1年前1 -
 gamekey 共回答了15个问题
gamekey 共回答了15个问题 |采纳率80%由于气体的分子不断运动,所以硫化氢会不断地扩散到空气中. 由于硫化氢密度比空气大所以会存于低处,H 2 S(硫化氢)燃烧时生成两种常见的氧化物,根据元素的种类在反应前后不变的规律,可判断生成物是二氧化硫和水,故反应的化学方程式为2H 2 S+3O 2
点燃
.
2SO 2 +2H 2 O.
故答案为:不断运动;高出;2H 2 S+3O 2
点燃
.
2SO 2 +2H 2 O.1年前查看全部
- 某电动自行车厂一月份的产量为1000辆,由于市场需求量不断增大,该厂计划第一剧毒共生产3310辆,求2,3月平均增长率.
某电动自行车厂一月份的产量为1000辆,由于市场需求量不断增大,该厂计划第一剧毒共生产3310辆,求2,3月平均增长率.
某电动自行车厂一月份的产量为1000辆,由于市场需求量不断增大,该厂计划第一季度共生产3310辆,求2,3月平均增长率. Althe1年前1
Althe1年前1 -
 我是F1王舒马赫 共回答了16个问题
我是F1王舒马赫 共回答了16个问题 |采纳率81.3%设平均增长率为p,则2月产量为1000(1+p),3月产量为1000(1+p)(1+p).由题意得 1000+1000(1+p)+1000(1+p)(1+p)=3310 解得p=10% 答:…1年前查看全部
- 已知HCN是一种极弱酸,其电离产生的CN - 离子能与人体血红蛋白中心离子Fe 2+ 结合,因而有剧毒。通常Fe 2+
已知HCN是一种极弱酸,其电离产生的CN - 离子能与人体血红蛋白中心离子Fe 2+ 结合,因而有剧毒。通常Fe 2+ 、Fe 3+ 均易与CN - 形成络离子:[Fe(CN) 6 ] 3- 、[Fe(CN) 6 ] 4- ,其中[Fe(CN) 6 ] 3- 在中性条件下能发生水解,生成Fe(OH) 3 。试回答下列问题:
⑴.写出HCN分子的结构式_________,电子式_____________;
⑵.[Fe(CN) 6 ] 3- 在中性条件下水解可生成Fe(OH) 3 ,同时还能生成的微粒有_____、_____。 6185658571年前0
6185658571年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 甲醇是一种具有酒精气味的剧毒液体.现把一定量的甲醇与4.4g氧气混合于一个密闭容器内,引燃发生如下反应:
甲醇是一种具有酒精气味的剧毒液体.现把一定量的甲醇与4.4g氧气混合于一个密闭容器内,引燃发生如下反应:
8CH3OH+xO2
mCO2+2CO+16H2O,完全反应后至常温常压状况下,容器内余下的液体为3.6g.求:点燃 .
(1)化学计量数x的值
(2)该反应生成CO2的质量. lixuhui_0081年前3
lixuhui_0081年前3 -
 rhhjdsgd 共回答了18个问题
rhhjdsgd 共回答了18个问题 |采纳率88.9%解题思路:(1)依据质量守恒定律的有关应用解答即可;
(2)依据已知的化学方程式利用水的质量可以求出生成的二氧化碳质量;(1)依据化学反应前后各原子的个数不会变化对x、m进行计算;
反应前碳原子的个数是8,故反应后碳原子个数也是8,则有m+2=8,故m=6;反应前氧原子的个数是8+2x,反应后为2m+2+16,则有8+2x=12+2+16,解得x=11,故方程式应为8CH3OH+11O2
点燃
.
6CO2+2CO+16H2O;
(2)完全反应后至常温常压状况下,容器内余下的液体为3.6g,则可知水的质量是3.6g,设生成的二氧化碳质量是y
8CH3OH+11O2
点燃
.
6CO2+2CO+16H2O
264288
y3.6g
[264/288=
y
3.6g]
y=3.3g
答:(1)化学计量数x的值为6;(2)该反应生成CO2的质量是3.3g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对化学反应方程式计算的考查,解题的关键是掌握质量守恒定律的基本应用,属基础计算考查题;1年前查看全部
- 某地天然气井发生井喷事故,喷出的天然气中H2S气体含量很高,H2S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,
某地天然气井发生井喷事故,喷出的天然气中H2S气体含量很高,H2S气体在臭鸡蛋气味,密度比空气大,有剧毒.井喷发生不久,附近村民就闻到了臭鸡蛋气味,这体现了分子______的性质; 当村民得知这种气体有剧毒时,迅速撤离村庄.为减少村民的中毒机会,你认为村民在撤离时应尽量走______(填“低处”或“高处”).技术人员后来成功点燃了H2S气体,使气体不再扩散.已知H2S(硫化氢)燃烧时生成两种常见的氧化物,试写出H2S燃烧的化学方程式:2H2S+3O2
2SO2+2H2O点燃 .2H2S+3O2.
2SO2+2H2O点燃 . 星星一点亮1年前1
星星一点亮1年前1 -
 夜风七 共回答了14个问题
夜风七 共回答了14个问题 |采纳率100%解题思路:根据题意,结合分子的不断运动,以及硫化氢的性质进行解答.硫化氢具有可燃性属于化学性质,根据反应物和生成物及反应条件可以判断化学方程式.由于气体的分子不断运动,所以硫化氢会不断地扩散到空气中. 由于硫化氢密度比空气大所以会存于低处,H2S(硫化氢)燃烧时生成两种常见的氧化物,根据元素的种类在反应前后不变的规律,可判断生成物是二氧化硫和水,故反应的化学方程式为2H2S+3O2
点燃
.
2SO2+2H2O.
故答案为:不断运动;高出;2H2S+3O2
点燃
.
2SO2+2H2O.点评:
本题考点: 利用分子与原子的性质分析和解决问题;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题是对硫化氢气体的考查,主要是对硫化氢的物理性质的应用,并结合质量守恒定律书写化学方程式.1年前查看全部
- 氢氧化钠与空气中接触,产生的液态有没有剧毒?
氢氧化钠与空气中接触,产生的液态有没有剧毒?
同上
对不起,我忘记说了一点,就是如果把它接触空气后防入饮料当中,人喝了会有什么事情发生,严重的话,会不会直接导***亡! 离去的芳草1年前10
离去的芳草1年前10 -
 闪电小老鼠27 共回答了16个问题
闪电小老鼠27 共回答了16个问题 |采纳率93.8%就是吸潮 或者和二氧化碳反应生成碳酸钠(大苏打)或者碳酸氢钠(小苏打)
氢氧化钠本身是强碱 有腐蚀性
放入饮料中会中和掉你的胃酸 这不要紧 重要的是腐蚀你的消化道 太危险 要是碳酸饮料的话 可能会好点1年前查看全部
- 化学药品上画一个骷髅头 是一点毒,中毒,还是剧毒?
 killer44441年前1
killer44441年前1 -
 车载cc 共回答了22个问题
车载cc 共回答了22个问题 |采纳率86.4%代表的是剧毒的意义,起警告作用.实际是利用了人类对死亡的天生恐惧以使被标志的物品更加被注意.1年前查看全部
- A、B、C、D是初中化学常见的四种无色气体,其中两种是单质,两种是化合物,且C有剧毒,E能使紫色石蕊溶液变红,它们之间的
A、B、C、D是初中化学常见的四种无色气体,其中两种是单质,两种是化合物,且C有剧毒,E能使紫色石蕊溶液变红,它们之间的转化关系如图所示:
(1)试分析推断B的化学式:______;
(2)E能使紫色石蕊溶液变红,则E的名称是______;
(3)写出A+C→B的化学方程式:______,此反应属于基本反应类型中的______反应.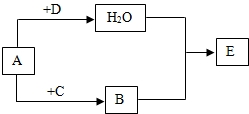
 Rockylai1年前1
Rockylai1年前1 -
 fdjhvmn 共回答了17个问题
fdjhvmn 共回答了17个问题 |采纳率88.2%由图示可知A+D→H 2 O,A+C→B,C是剧毒气体,所以C是一氧化碳,A是氧气,则B是二氧化碳,二氧化碳可与水生成碳酸E,碳酸能使紫色石蕊溶液变红.A+C→B的化学方程式为O 2 +2CO
点燃
.
2CO 2 ,该反应的特征符合“多变一”的化合反应特征,所以是化合反应;
由于上述推断均符合图示的转化关系,因此上述推断的结果是正确的.
故答案为:(1)CO 2 ;(2)碳酸;(3)O 2 +2CO
点燃
.
2CO 2 ;化合(硫及其化合物也可);1年前查看全部
- 禁止使用含磷洗衣粉;禁止使用剧毒、残留期长的农药;禁止使用氟利昂作电冰箱、空调等电器的制冷剂。 [
禁止使用含磷洗衣粉;禁止使用剧毒、残留期长的农药;禁止使用氟利昂作电冰箱、空调等电器的制冷剂。 [ ] 荡悠悠21年前1
荡悠悠21年前1 -
 taike99 共回答了15个问题
taike99 共回答了15个问题 |采纳率80%√1年前查看全部
- (2009•静安区一模)为探究燃烧的条件,实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,
(2009•静安区一模)为探究燃烧的条件,实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为
240℃.探究可燃物燃烧的条件的实验设计如下:
(1)按图-1实验,可观察到现象:铜片上白磷燃烧,红磷和水中的白磷没有燃烧.由此可得出的结论是:通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点;
(2)按图-2实验,可观察到现象:镁条可以在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成.请用化学方程式表示该反应2Mg+CO2
C+2MgO2Mg+CO2点燃 .
C+2MgO.点燃 .
(3)对照实验(1)、(2),你对燃烧和灭火有哪些新认识呢?物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火. camel841年前1
camel841年前1 -
 竹月薇 共回答了21个问题
竹月薇 共回答了21个问题 |采纳率90.5%答:(1)铜片上白磷燃烧满足燃烧的三个条件,红磷和水中的白磷没有燃烧不能满足燃烧的条件,故答案为:通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点;
(2)又知条件和质量守恒定律知,镁在二氧化碳中燃烧生成碳和氧化镁,方程式为:2Mg+CO2
点燃
.
C+2MgO,故答案为:2Mg+CO2
点燃
.
C+2MgO
(3)在(1)中,可燃物的燃烧需要满足:一是与氧气接触,二是温度要达到着火点;而在(2)中物质的燃烧不需要氧气,从而得出结论:物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火.故答案为:物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火.1年前查看全部
- A、B、C、D是初中化学常见的四种无色气体,其中两种是单质,两种是化合物,且C有剧毒,E能使紫色石蕊溶液变红,它们之间的
A、B、C、D是初中化学常见的四种无色气体,其中两种是单质,两种是化合物,且C有剧毒,E能使紫色石蕊溶液变红,它们之间的转化关系如图所示:
(1)试分析推断B的化学式:______;
(2)E能使紫色石蕊溶液变红,则E的名称是______;
(3)写出A+C→B的化学方程式:O2+2CO
2CO2点燃 .O2+2CO,此反应属于基本反应类型中的______反应.
2CO2点燃 .
 乱思1年前1
乱思1年前1 -
 xx22711 共回答了19个问题
xx22711 共回答了19个问题 |采纳率100%解题思路:根据所学知识,可以推测出C是一氧化碳,B是二氧化碳;气体A和一氧化碳反应会生成二氧化碳,可以知道A就是氧气,氧气和氢气反应生成水,水和二氧化碳可生成碳酸E,据此分析解答;.由图示可知A+D→H2O,A+C→B,C是剧毒气体,所以C是一氧化碳,A是氧气,则B是二氧化碳,二氧化碳可与水生成碳酸E,碳酸能使紫色石蕊溶液变红.A+C→B的化学方程式为O2+2CO 点燃 . 2CO2,该反应的特征...
点评:
本题考点: 物质的鉴别、推断.
考点点评: 本题主要考查常见的无色气体的性质和物质的相互转化关系,解题时要找准突破口,然后根据化学特性进行判断并完成解答.1年前查看全部
- 2003年12月23日重庆市发生高压天然气井喷,造成了重大灾害.据分析该天然气中每立方米中含剧毒硫化氢11g.已知,硫化
2003年12月23日重庆市发生高压天然气井喷,造成了重大灾害.据分析该天然气中每立方米中含剧毒硫化氢11g.已知,硫化氢密度比空气大,能溶于水形成酸性溶液,能被多孔固体颗粒吸附,具有可燃性,完全燃烧生成二氧化硫和水.下列说法错误的是( ) A.点燃硫化氢气体前要检验纯度 B.木炭、活性炭可以吸附硫化氢气体 C.点燃该天然气对大气没有不良影响 D.可以用石灰水泥浆压井的方法处理事故  dongshisan1年前1
dongshisan1年前1 -
 lkjlkadj 共回答了16个问题
lkjlkadj 共回答了16个问题 |采纳率81.3%A、点燃硫化氢气体前要检验纯度.正确;
B、木炭、活性炭可以吸附硫化氢气体.正确;
C、点燃该天然气时,硫化氢燃烧生成的二氧化硫能够污染空气.错误;
D、石灰水能够吸收硫化氢气体,可以用石灰水泥浆压井的方法处理事故.正确.
故选C.1年前查看全部
- PH3是一种无色剧毒气体,其分子结构和NH3相似.下列判断错误的是( )
PH3是一种无色剧毒气体,其分子结构和NH3相似.下列判断错误的是( )
A.PH3分子呈三角锥形
B.PH3分子是极性分子
C.PH3分子中所有原子最外层都满足8e-结构
D.PH3分子稳定性低于NH3分子,因为N-H键键长更短、键能更高 一弯冷月1年前1
一弯冷月1年前1 -
 月有泪 共回答了17个问题
月有泪 共回答了17个问题 |采纳率82.4%解题思路:A、NH3是三角锥型,PH3分子结构和NH3相似,也是三角锥型;
B、分子结构是三角锥型,正负电荷重心不重合,为极性分子;
C、H原子为2电子稳定结构;
D、共价键键长越短,键能越大,分子越稳定.A、PH3分子结构和NH3相似,NH3是三角锥型,故PH3也是三角锥型,故A正确;
B、PH3分子结构是三角锥型,正负电荷重心不重合,为极性分子,故B正确;
C、氢化物中H原子为2电子稳定结构,所以PH3分子中不是所有原子最外层都满足8e-结构,故C错误;
D、共价键键长越短,键能越大,分子越稳定,P-H键键能比N-H键键能低,是因为P的原子半径比N大,P-H键长比N-H长,则N-H键键长更短、键能更高,所以PH3分子稳定性低于NH3分子,故D正确;
故选C.点评:
本题考点: 不同晶体的结构微粒及微粒间作用力的区别;判断简单分子或离子的构型;极性分子和非极性分子.
考点点评: 本题考查空间结构、氢键、键能与性质关系等,题目比较基础,注意8电子微粒的判断方法.1年前查看全部
- 二氧化硫是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H 2 S)是一种具有臭鸡蛋气味的剧毒气体
二氧化硫是造成酸雨的主要气体,其水溶液叫亚硫酸(H 2 SO 3 )。硫化氢(H 2 S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H 2 S+H 2 SO 3 =3S↓+3H 2 O。下列溶液的pH随通入硫化氢体积的变化曲线示意图中,正确的是()
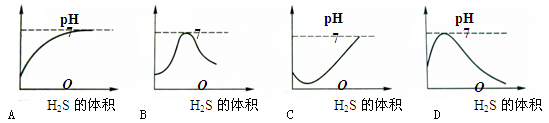
 ck888991年前1
ck888991年前1 -
 xieyishu78 共回答了17个问题
xieyishu78 共回答了17个问题 |采纳率82.4%B
1年前查看全部
- 英语翻译1人究竟什么时候会死呢?是心脏被枪打中的时候?不对.得了不治之症吗?也不对.喝了剧毒香菇汤之后吗?当然不是.而是
英语翻译
1人究竟什么时候会死呢?是心脏被枪打中的时候?不对.得了不治之症吗?也不对.喝了剧毒香菇汤之后吗?当然不是.而是被世人遗忘的时候
2就算敌人恐怖得要死也好,作为一个男人,也有不能逃避的时侯!那就是同伴的梦想被取笑的时侯
3人的梦想,永远不会结束
实在翻译不了的话,意思大概正确也行 liubao1101年前6
liubao1101年前6 -
 bdbqbdbq 共回答了21个问题
bdbqbdbq 共回答了21个问题 |采纳率95.2%1人究竟什么时候会死呢?
是心脏被枪打中的时候?不对.
得了不治之症吗?也不对.
喝了剧毒香菇汤之后吗?当然不是.
而是被世人遗忘的时候
When on earth would a man die?
Is it the time to get a gunshot,no;
a incurable disease,no;
or taking a toxic mushroom soup,of course not as well.
It turns out to be the moment when he has been put of of the mind.
2就算敌人恐怖得要死也好,作为一个男人,也有不能逃避的时侯!
那就是同伴的梦想被取笑的时侯
Even if the enemy is terribly horrible,
as a man,you still have to hold that very moment to face it,
that's when your partner's dream is despised.
3人的梦想,永远不会结束
Dreams of people will never die.1年前查看全部
- 工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
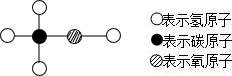 工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
A.甲醇的化学式为CH4O
B.甲醇的相对分子质量为32
C.甲醇中C、H、O三种元素的质量比为1:4:1
D.甲醇在氧气中完全燃烧,产生二氧化碳和水 xuyihua12341年前1
xuyihua12341年前1 -
 悦光倾城 共回答了16个问题
悦光倾城 共回答了16个问题 |采纳率100%解题思路:A、根据甲醇的分子结构图,1个甲醇分子是由1个碳原子、4个氢原子和1个氧原子构成的,据此进行分析判断.
B、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据质量守恒定律进行分析判断.A、根据甲醇的分子结构图,1个甲醇分子是由1个碳原子、4个氢原子和1个氧原子构成的,其化学式为:CH4O,故选项说法正确.
B、甲醇的相对分子质量为12+1×4+16=32,故选项说法正确.
C、甲醇中C、H、O三种元素的质量比为12:(1×4):16≠1:4:1,故选项说法错误.
D、由质量守恒定律,甲醇在氧气中完全燃烧,生成二氧化碳和水,故选项说法正确.
故选C.点评:
本题考点: 化学式的书写及意义;相对分子质量的概念及其计算;元素质量比的计算;完全燃烧与不完全燃烧.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.1年前查看全部
- 重庆市某天然气井发生井喷事故,喷出的天然气中H2S气体的含量很高,H2S气体有臭蛋气味,密度比空气大,有剧毒.当村民们得
重庆市某天然气井发生井喷事故,喷出的天然气中H2S气体的含量很高,H2S气体有臭蛋气味,密度比空气大,有剧毒.当村民们得知这种臭气有剧毒时,迅速撤离村庄,远离井喷地点.为了减少中毒机会,村民在撤离井喷地点时应及时往高处走的原因是______;技术人员通过原有的H2S放喷管线,成功点燃了地下喷出的H2S气体,使气体不再扩散,此时H2S能燃烧生成了一种淡黄色的固体硫和水,属于化学性质的是:______,属于物理性质的是:______,______H2S燃烧的符号表达式为:2H2S+3O2
2SO2+2H2O点燃 .2H2S+3O2.
2SO2+2H2O点燃 . 飞檐走比1年前1
飞檐走比1年前1 -
 39119611 共回答了10个问题
39119611 共回答了10个问题 |采纳率90%解题思路:硫化氢的气味、密度、状态等属于物理性质.硫化氢具有可燃性属于化学性质;根据硫化氢的物理性质是密度比空气大判断;根据反应物和生成物及其质量守恒定律可以书写化学方程式.由题意可知,硫化氢的物理性质有:是具有臭鸡蛋气味的气体,密度比空气大.故填:臭鸡蛋气味,密度比空气大.硫化氢燃烧能生成水和二氧化硫,具有可燃性.由于硫化氢的密度比空气大,所以村民在撤离井喷地点时应尽量走高处.硫化氢燃烧能生成水和二氧化硫,化学方程式为:2H2S+3O2
点燃
.
2SO2+2H2O.
故答案:硫化氢的密度比空气大;具有可燃性,具有臭鸡蛋气味,密度比空气大; 2H2S+3O2
点燃
.
2SO2+2H2O.点评:
本题考点: 化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和各种物质的性质方面的知识,只有这样才能对问题做出正确的判断.1年前查看全部
- 碘盐里加的碘酸钾不是有毒的吗?碘盐加碘都是加的碘酸钾,以前中学学化学,碘酸钾不是有剧毒的吗?为什么能食用呢?中文名称:碘
碘盐里加的碘酸钾不是有毒的吗?
碘盐加碘都是加的碘酸钾,以前中学学化学,碘酸钾不是有剧毒的吗?为什么能食用呢?
中文名称:碘酸钾
健康危害
侵入途径:吸入、食入、经皮吸收.
健康危害:对上呼吸道、眼及皮肤有刺激性.口服引起头晕、恶心、呕吐、眩晕及胃肠道刺激.可致视神经损害. 东方子磨1年前1
东方子磨1年前1 -
 18的我 共回答了16个问题
18的我 共回答了16个问题 |采纳率87.5%碘盐中碘酸钾的含量并不高,而我们所需要的不是碘酸根(KIO3-)而是碘负离子(I-),而碘酸根进入人体后可以补充碘证明在人体内碘酸根可以转变为碘负离子供人体使用,因为人体内有许多还原物质,如维生素C还有还原态H等等,也就是说微量的碘酸钾在人体内可以转换为无害的碘负离子,从而也就不会伤害人体了,而你所说的一般要大量的碘酸钾,这个时候他与我们的胃酸反应生成强氧化性的碘酸才会氧化腐蚀我们的胃肠道,不过通常食盐中那点碘酸钾要们被食物(蔬菜水果中有大量强还原性的酚类和维生素C)还原,要们被人体内的还原物质还原根本构不成伤害.1年前查看全部
- H2S是一种无色有臭鸡蛋气味的气体有剧毒H2S燃烧生成两种常见的氧化物写出该反应的化学方程式.(着急,
 roshyang1年前1
roshyang1年前1 -
 手的纹路 共回答了20个问题
手的纹路 共回答了20个问题 |采纳率85%2H2S+O2=2H2O+S
2H2S+3O2=2H2O+2SO2
如果H2S:O2>2:1 只有第一个1年前查看全部
- 秋水仙素为什么不会使动物细胞染色体加倍,是因为其有剧毒吗,
秋水仙素为什么不会使动物细胞染色体加倍,是因为其有剧毒吗,
植物和动物都有微管,有丝分裂时,一个是纺垂体,一个是中心体,不都是靠其牵引吗?可以讲深一点,不怕听不懂. csy_6uu1年前4
csy_6uu1年前4 -
 xshxsh731 共回答了17个问题
xshxsh731 共回答了17个问题 |采纳率100%植物细胞分裂是由于纺锤体的牵引,纺锤体是由微管组成,秋水仙素可抑制微管去组装而抑制染色体的分离从而使细胞形成多倍体.
动物细胞虽然有中心体也是微管组织中心,但是动物细胞分裂时不形成纺锤体,而是有中心体产生星射线将染色体拉开,星射线是微丝组成,若使动物细胞染色体加倍可用细胞松驰素B,其作用于微丝.1年前查看全部
- 氰是否是种化合物,含他的物质为何都具剧毒
 无赖20051年前1
无赖20051年前1 -
 stanely2068 共回答了24个问题
stanely2068 共回答了24个问题 |采纳率91.7%中文名称:氰 英文名称:cyanogen CAS No.:460-19-5 分子式:(CN)2 分子量:52.04 理化特性 主要成分:纯品 外观与性状:无色气体,具有类似杏仁的气味.熔点(℃):-34.4 沸点(℃):-21.2 相对密度(水=1):0.96 相对蒸气密度(空气=1):2.34 饱和蒸气压(kPa):53.32/-33℃ 爆炸上限%(V/V):42.6 爆炸下限%(V/V):6.6 溶解性:溶于水,易溶于乙醇、乙醚等.主要用途:用作熏蒸剂及有机合成原料.健康危害:氰的刺激性比氰化氢略弱,而毒性则小得多.氰的轻度中毒,病人出现乏力、头痛、头昏、胸闷及粘膜刺激症状;严重中毒者,呼吸困难,意识丧失,出现惊厥,最后可因呼吸中枢麻痹而死亡.燃爆危险:本品易燃,高毒,具刺激性.危险特性:与空气混合能形成爆炸性混合物.遇明火、高热能引起燃烧爆炸.其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃.遇水或水蒸气、酸或酸气产生剧毒的烟雾.若遇高热,容器内压增大,有开裂和爆炸的危险.氰化物特指带有氰基(CN)的化合物,其中的碳原子和氮原子通过叁键相连接.这一叁键给予氰基以相当高的稳定性,使之在通常的化学反应中都以一个整体存在.因该基团具有和卤素类似的化学性质,常被称为拟卤素.一般将其无机化合物归为氰类,有机化合物归为腈类.通常为人所了解的氰化物都是无机氰化物,俗称-{zh-cn:山奈;zh-hk:山埃}-(来自英语音译“Cyanide”),是指包含有氰根离子(CN-)的无机盐,可认为是氢氰酸(HCN)的盐,常见的有氰化钾和氰化钠.它们多有剧毒,故而为世人熟知.另有有机氰化物,是由氰基通过单键与另外的碳原子结合而成.视结合方式的不同,有机氰化物可分类为腈(C-CN)和异腈(C-NC),相应的,氰基可被称为腈基(-CN)或异腈基(-NC).最常见的氰化物是氢氰酸、氰化钠和氰化钾.氢氰酸,HCN-,别名氰化氢,(HCN)是一种无色、带有淡淡的苦杏仁味气体.有趣的是,有四成人根本就闻不到它的味道,仅仅因为缺少相应的基因.易溶于水、酒精和乙醚.易在空气中均匀弥散,在空气中可燃烧.氰化氢在空气中的含量达到5.12.8%时,具有爆炸性.氰化氢为气体,其水溶液称氢氰酸.氢氰酸属于剧毒类.其主要应用于电镀业(镀铜、镀金、镀银)、采矿业(提取金银)、船舱、仓库的烟熏灭鼠,制造各种树脂单体如丙烯酸树酯、甲基丙烯酸树酯等行业,此外也可在制备氰化物的生产过程中接触到本物质.氰化钾和氰化钠都是无色晶体,在潮湿的空气中,水解产生氢氰酸而具有苦杏仁味.氰化物拥有令人生畏的毒性,可以说,只要用舌头舐它一下就会中毒.人们在电影或电视上不止一次看到,间谍在被捕时突然咬一下衣领中预藏的氰化钾,立即就会死去.这并非戏剧夸张,一般人只要一次误服0.1克左右氰化钠或氰化钾就会中毒死亡,敏感的人甚至吃进0.06克就可以致死.这种急性中毒可以在几分钟之内猝死.因而,氰化物被称为“谋杀者毒药”.1年前查看全部
- 请问有没有一种物质,0度或10度左右是液态或固态,到30度左右会变成剧毒的气态.
 karanhu1年前1
karanhu1年前1 -
 单眼皮的小龟 共回答了18个问题
单眼皮的小龟 共回答了18个问题 |采纳率100%vcwil,
液溴应该符合条件,常温下为棕红色发烟液体,沸点58.76℃,也就是说30度是不会完全气化,但会部分挥发,其无论是液态还是气态都有剧毒,有较强腐蚀性.希望我的回答对你有所帮助.1年前查看全部
- 白磷和红磷都是由磷原子构成的,白磷着火点只有40摄氏度,颜色为黄色,剧毒.而红磷着火点却高达260摄氏度,颜色为赤红色,
白磷和红磷都是由磷原子构成的,白磷着火点只有40摄氏度,颜色为黄色,剧毒.而红磷着火点却高达260摄氏度,颜色为赤红色,毒性强.分析他们性质不同的原因
 F_L_Y01231年前1
F_L_Y01231年前1 -
 原来只是一个人 共回答了16个问题
原来只是一个人 共回答了16个问题 |采纳率100%由于有很多公式不会输入,看不懂的只能靠你猜了
白磷与红磷是同素异形体
白磷:为无色晶体,有蒜臭的蜡状固体.剧毒,不溶于水,易溶于二硫化碳,在空气中40度自燃,常温氧化必、发磷光.
红磷:长链状结构,暗红色粉末状固体.无毒,不溶于水,也不溶于二硫化碳.240度着火,不自燃.
白磷隔绝空气加热到260度转化为红磷,红磷则加热416度升华蒸气冷却转化为白磷.
共同化学性质:1 与氧气反应 生成5氧化2硫
2 与卤素反应(白磷反应剧烈)
3 与强氧化性酸反应
除此,白磷可以与碱反应
制备:将磷酸钙混以石英砂和碳粉在1500度电炉中加热,生成的P4和CO通过冷水,即得白磷固体
具体的区别如下:1年前查看全部
- (2009•静安区一模)为探究燃烧的条件,实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,
(2009•静安区一模)为探究燃烧的条件,实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为
240℃.探究可燃物燃烧的条件的实验设计如下:
(1)按图-1实验,可观察到现象:铜片上白磷燃烧,红磷和水中的白磷没有燃烧.由此可得出的结论是:通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点;
(2)按图-2实验,可观察到现象:镁条可以在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成.请用化学方程式表示该反应2Mg+CO2
C+2MgO2Mg+CO2点燃 .
C+2MgO.点燃 .
(3)对照实验(1)、(2),你对燃烧和灭火有哪些新认识呢?物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火物质燃烧不一定是跟氧气的反应,有些火灾不能用CO2灭火. 阿俊卿1年前1
阿俊卿1年前1 -
 Kiko98 共回答了17个问题
Kiko98 共回答了17个问题 |采纳率82.4%解题思路:(1)燃烧的三要素:物质具有可燃性、与氧气接触、温度达到着火点;
(2)根据质量守恒定律写成方程式;
(3)根据实验(1)、(2)对比得出结论;答:(1)铜片上白磷燃烧满足燃烧的三个条件,红磷和水中的白磷没有燃烧不能满足燃烧的条件,故答案为:通常情况下,可燃物燃烧,一是与氧气接触,二是温度要达到着火点;(2)又知条件和质量守恒定律知,镁在二氧化...
点评:
本题考点: 燃烧的条件与灭火原理探究.
考点点评: 探究燃烧条件,着眼于对可燃物周围环境进行对比分析:可燃物能否燃烧,要看是否接触到氧气、温度是否达到着火点,还有并不是所用的物质燃烧不一定是跟氧气的反应.1年前查看全部
- 温度计打碎后没有清理在地面上的水银,挥发有剧毒,怎么办?
温度计打碎后没有清理在地面上的水银,挥发有剧毒,怎么办?
不小心把温度计打碎了,当时水银呈非常细小的珠粒(针尖般大小)在地上.用手拿不起来,我就用扫帚扫在了阳台上.我知道水银会挥发,而且有剧毒,应该用硫粉覆盖,但哪里买的到呢?是那种比较小的温度计,我不知道那么多的量会不会导致中毒,甚至有生命危险,或者会致癌.我很害怕.希望有人可以告诉我多少量会威胁生命以及我该怎么处理它.请尽快回复. 我还是生愁1年前1
我还是生愁1年前1 -
 多久才算爱 共回答了17个问题
多久才算爱 共回答了17个问题 |采纳率88.2%汞通称水银,常温下是银白色液体,汞和它的大多数化合物都有毒.
在我们的日常生活中,有不少用品与水银有关.比如,各类荧光灯中都含有水银;电脑显示器等电子产品中也含有—定量的水银……
专家指出,水银是常温下惟一呈液态的金属,含有它的用品一旦被打碎,水银就会蒸发.而且,它的吸附性特别好.水银蒸气易被墙壁和衣物等吸
附,成为不断污染空气的源头.虽然少量吸人它不会对身体造成太大的危害,但长期大量吸人,则会造成汞中毒.汞中毒分急性和慢性两种:急性中毒有腹痛、腹泻、血尿等症状;慢性中毒主要表现为口腔发炎、肌肉震颤和精神失常等.
含有水银的用品一旦被打破,水银会形成球体滚落.这时,要先关掉室内所有加热装置,打开窗户通风;然后戴上手套,用小铲子把水银收集起来深埋,或在上面撒些硫磺粉末,硫和汞反应能生成不易溶于水的硫化汞,危害会大大降低.由于水银在常温下即可蒸发成气态,很容易被吸人呼吸道,引起中毒,所以,处理散落在地的水银时最好戴上口罩.如果伤口碰到水银,则应到医院中毒防治科进行检查,出现中毒现象再进行治疗.1年前查看全部
- 盐酸萘乙二胺是否是剧毒试剂
 waxgq1年前1
waxgq1年前1 -
 晨宇YES 共回答了15个问题
晨宇YES 共回答了15个问题 |采纳率93.3%不是剧毒1年前查看全部
- A与B级剧毒物的区别级剧毒物RT 剧毒物品按照化学类别和毒性大小分为四类.那么A和B级有什么区别?是不是毒性不一样?如果
A与B级剧毒物的区别级剧毒物
RT 剧毒物品按照化学类别和毒性大小分为四类.那么A和B级有什么区别?是不是毒性不一样?如果是的话哪个更毒一点呢?(不需要列举各个种类有哪些了 这个百度一下都有的) 六月橙茶1年前1
六月橙茶1年前1 -
 离心草 共回答了14个问题
离心草 共回答了14个问题 |采纳率92.9%A毒性最强5mg/kg以下
B 毒性次之50毫克以下5毫克以上1年前查看全部
- (2000•湖北)在如图所示转化关系中,A、B、C、D、E、F都是初中化学所学过的物质,其中B是单质,A是一种有剧毒的气
(2000•湖北)在如图所示转化关系中,A、B、C、D、E、F都是初中化学所学过的物质,其中B是单质,A是一种有剧毒的气体,D在自然界中广泛存在,组成A、C两种物质的元素种类相同.

(1)写出A、F的化学式:
A:______F:______
(2)写出下列转化过程中的化学方程式:
B→C:C+O2
CO2点燃 .C+O2
CO2点燃 .
D→C:CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 . prettybin1年前1
prettybin1年前1 -
 libin44022 共回答了19个问题
libin44022 共回答了19个问题 |采纳率89.5%解题思路:根据题意“A是一种有剧毒的气体”,则为A一氧化碳;根据“A、C两物质中组成元素相同”,则推测A、C为一氧化碳与二氧化碳,则C为二氧化碳;根据“D在自然界中广泛存在”,则推测为D碳酸钙;根据图框可知,因为C、B高温生成A,则B为碳,则E为氧气,F为氢氧化钙溶液.代入原题,进行验证,符合题意,可以据此解答.根据题意“A是一种有剧毒的气体”,则为A一氧化碳;根据“A、C两物质中组成元素相同”,则推测A、C为一氧化碳与二氧化碳,则C为二氧化碳;根据“D在自然界中广泛存在”,则推测为D碳酸钙;根据图框可知,因为C、B高温生成A,则B为碳,则E为氧气,F为氢氧化钙溶液.代入进行验证,符合题意.
(1)由分析可知:A、F为一氧化碳、氢氧化钙,故其化学式分别为:CO;Ca(OH)2;
(2)由分析可知:B、C、D分别为碳、二氧化碳、碳酸钙,故其化学方程式分别为:C+O2
点燃
.
CO2; CaCO3
高温
.
CaO+CO2↑.
故答案为:
(1)CO;Ca(OH)2;
(2)B→C:C+O2
点燃
.
CO2; D→C:CaCO3
高温
.
CaO+CO2↑点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为框图式推断题,解题关键是从信息中找准突破口,直接得出答案,然后再顺推或逆推或向中间推的方法推测出其它答案,做出正确解答即可.1年前查看全部
- PH 3 是一种无色剧毒气体,其分子结构和NH 3 相似,但P-H键键能比N-H键键能低。下列判断中错误的是( ) A
PH 3 是一种无色剧毒气体,其分子结构和NH 3 相似,但P-H键键能比N-H键键能低。下列判断中错误的是( )
A.PH 3 分子呈三角锥形 B.PH 3 分子是极性分子 C.PH 3 沸点低于NH 3 沸点,因为P—H键键能低 D.PH 3 分子稳定性低于NH 3 分子,因为N—H键键能高  missx1年前1
missx1年前1 -
 keqinwang 共回答了19个问题
keqinwang 共回答了19个问题 |采纳率89.5%C
氨气是三角锥形结构,所以PH 3 的结构也是三角锥形,A正确;氨气是极性分子,则PH 3 也是极性分子,B正确;由于氨气分子中存在氢键,所以氨气的沸点高于PH 3 的,沸点高低与键能无关,键能大小影响分子的稳定性,所以选项C不正确,D正确。1年前查看全部
- 氢氧化钠只要拿出来放在空气中 就会迅速吸收水分子成为液态的剧毒
 小溪里的鹅卵石1年前1
小溪里的鹅卵石1年前1 -
 wangjk79 共回答了20个问题
wangjk79 共回答了20个问题 |采纳率95%吸了水就变成了浓碱,只是有腐蚀性,之后又会跟CO2反应成Na2CO3,并不算毒1年前查看全部
- (2013•大理州模拟)日本福岛核泄漏危机发生后,福岛土壤首现剧毒放射性钚元素.原子序数为94的钚元素的一种原子中,质子
(2013•大理州模拟)日本福岛核泄漏危机发生后,福岛土壤首现剧毒放射性钚元素.原子序数为94的钚元素的一种原子中,质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A.中子数为145
B.核电荷数为239
C.质子数为94
D.核外电子数为94 深圳之无名小子1年前1
深圳之无名小子1年前1 -
 地理老师的耳朵 共回答了24个问题
地理老师的耳朵 共回答了24个问题 |采纳率91.7%解题思路:根据在原子中,原子序数=质子数=核电荷数=核外电子数,结合质子数加中子数的数值进行解答;A、在原子中质子数=核电荷数=核外电子数=原子序数,钚的原子序数为94,则其质子数为94,质子数+中子数=239,则其中子数为239-94=145,所以正确.
B、在原子中质子数=核电荷数=核外电子数=原子序数,钚的原子序数为94,则其核电荷数为94,所以错误.
C、在原子中质子数=核电荷数=核外电子数=原子序数,钚的原子序数为94,则其质子数为94,所以正确.
D、在原子中质子数=核电荷数=核外电子数=原子序数,钚的原子序数为94,则其核外电子数为94,所以正确.
故选B.点评:
本题考点: 原子的有关数量计算.
考点点评: 此题是对原子内部微粒的考查,解题的关键是利用了原子中:①原子序数等于质子数等于核电荷数等于核外电子数②相对原子质量等于质子数加中子数,进行解答问题1年前查看全部
- (2013•海淀区二模)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的
(2013•海淀区二模)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.
(1)某化学小组设计了制取H2S并验证其性质的实验,如下图所示.A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液.资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸.
②H2S可与许多金属离子反应生成沉淀.
③H2S在空气中燃烧,火焰呈淡蓝色.
回答下列问题:
①A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为______.
②B中的现象是______.
③C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为______.
④D中盛放的试剂可以是______(填标号).
a.水b.盐酸c.NaCl溶液d.NaOH溶液
(2)为进一步探究-2价硫的化合物与+4价硫的化合物反应条件,小组同学又设计了下列实验.
已知:电离平衡常数:H2SKa1=1.3×10-7;Ka2=7.1×10-15实验操作 实验现象 实验1 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 无明显现象 实验2 将H2S通入Na2SO3溶液中 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 实验3 将SO2通入Na2S溶液中 有浅黄色沉淀产生
H2SO3Ka1=1.7×10-2;Ka2=5.6×10-8
①根据上述实验,可以得出结论:在______条件下,+4价硫的化合物可以氧化-2价硫的化合物.
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是______(填序号).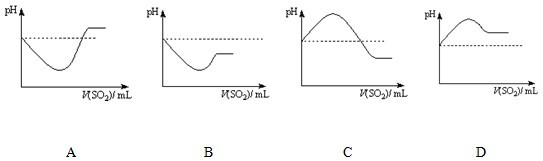
(3)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应______. cc11091年前1
cc11091年前1 -
 阿露儿 共回答了15个问题
阿露儿 共回答了15个问题 |采纳率86.7%解题思路:(1)①CuSO4与H2S反应生成CuS沉淀;
②H2S水溶液呈酸性;
③FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+;
④H2S可与碱反应.
(2)①H2S与SO2发生氧化还原反应生成S;
②根据H2SO3 酸性比H2S强判断;
(3)如与Ag发生置换反应生成H2,可用点燃的方法检验.(1)①CuSO4与H2S反应生成CuS沉淀,反应的方程式为H2S+CuSO4=CuS↓+H2SO4,故答案为:H2S+CuSO4=CuS↓+H2SO4;
②H2S水溶液呈酸性,可使湿润的蓝色石蕊试纸变红,故答案为:蓝色石蕊试纸变红;
③FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+,反应的离子方程式为H2S+2Fe3+=S↓+2H++2Fe2+,故答案为:H2S+2Fe3+=S↓+2H++2Fe2+;
④H2S有毒,不能排放到空气中,可与碱反应,故答案为:d;
(2)①由实验现象可知反应应下酸性条件下发生氧化还原反应生成S,故答案为:酸性(或酸性较强);
②H2SO3 酸性比H2S强,通入过量的SO2,溶液酸性更强,pH更小,故答案为:C;
(3)如与Ag发生置换反应生成H2,可用点燃的方法检验,但应先将H2S除去,方法是将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应,
故答案为:将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应.点评:
本题考点: 制备实验方案的设计;含硫物质的性质及综合应用.
考点点评: 本题考查实验制备方案的设计,侧重于硫化氢的性质的设计,题目难度不大,注意把握实验原理和实验的基本操作方法的学习.1年前查看全部
- 下列说法中错误的是( )。 A.当发生沙尘暴时,要戴口罩以减少尘埃的吸入 B.在剧毒的环境中,人们应戴防毒面具 C.尘
下列说法中错误的是( )。
A.当发生沙尘暴时,要戴口罩以减少尘埃的吸入 B.在剧毒的环境中,人们应戴防毒面具 C.尘肺患者会出现恶心、呕吐等症状 D.尘肺是长期在粉尘较多的场所工作的人容易患的一类职业病  沙滩树1年前1
沙滩树1年前1 -
 就说明世界不太糟 共回答了19个问题
就说明世界不太糟 共回答了19个问题 |采纳率78.9%C
发生沙尘暴时,空气中沙尘较多,应戴口罩以减少吸入尘埃对呼吸系统的伤害。在剧毒环境中,只有佩戴防毒面具才能减少有毒物质对呼吸系统的损伤。尘肺是由于在职业活动中长期吸入生产性粉尘(灰尘),并在肺内贮留而引起的疾病。当疾病发展到一定程度时,患者会出现胸闷、呼吸困难等症状,但不会出现恶心、呕吐等症状。1年前查看全部
大家在问
- 1I am fine后必须加谢谢吗?
- 2星光的波长按5500A计算,孔径为127cm的大型望远镜所能分辨的两颗星的最小角距离,怎
- 3下列防止噪声传播的措施中,属于阻断噪声传播的是?
- 4小学数学题+分100%在数+8.9,-3分之43,0.5,0,-3.5,12,-8,4又3分之2,12,+7中非质数有.
- 5知之为知之的之(后一个)的意思
- 6鲁在古文中是什么意思“圣人之道,卒于鲁也传之.”中的“鲁”是什么意思?
- 7英语翻译:他所发生的事情.
- 8--Let's go to the park by taxi .Oh,it is not far away from h
- 9把3米长的铁丝平均分成9段,每段长()()米,5段是全长的()().
- 10已知函数f(x)=4x+m•2x+1有且仅有一个零点,求m的取值范围,并求出该零点.
- 11写出12个表示十分专心的四字词
- 12一种铜和铝的合金重240千克,铜和铝的质量比是3:5,这种合金中谁的含量少,是多少?
- 13种一片太阳花6-9写的是什么
- 14各用一段精练的话对冰心,鲁迅做简单介绍(20字)
- 15甲的45%等于乙的60%,乙是甲的( )%
